Л. 6 Алкены.ppt
- Количество слайдов: 22
 Алкены (этиленовые углеводороды, олефины) - непредельные алифатические углеводороды, молекулы которых содержат двойную связь. Общая формула ряда алкенов Cn. H 2 n.
Алкены (этиленовые углеводороды, олефины) - непредельные алифатические углеводороды, молекулы которых содержат двойную связь. Общая формула ряда алкенов Cn. H 2 n.
 Простейшие представители: В отличие от предельных УВ, алкены содержат двойную связь С = С, которая осуществляется 4 -мя общими электронами:
Простейшие представители: В отличие от предельных УВ, алкены содержат двойную связь С = С, которая осуществляется 4 -мя общими электронами:
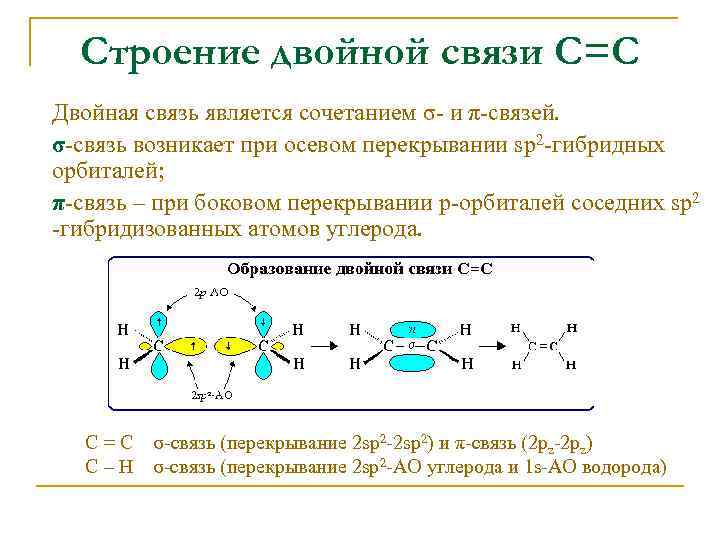 Строение двойной связи С=С Двойная связь является сочетанием σ- и π-связей. σ-связь возникает при осевом перекрывании sp 2 -гибридных орбиталей; π-связь – при боковом перекрывании р-орбиталей соседних sp 2 -гибридизованных атомов углерода. С = С σ-связь (перекрывание 2 sp 2 -2 sp 2) и π-связь (2 рz-2 рz) С – Н σ-связь (перекрывание 2 sp 2 -АО углерода и 1 s-АО водорода)
Строение двойной связи С=С Двойная связь является сочетанием σ- и π-связей. σ-связь возникает при осевом перекрывании sp 2 -гибридных орбиталей; π-связь – при боковом перекрывании р-орбиталей соседних sp 2 -гибридизованных атомов углерода. С = С σ-связь (перекрывание 2 sp 2 -2 sp 2) и π-связь (2 рz-2 рz) С – Н σ-связь (перекрывание 2 sp 2 -АО углерода и 1 s-АО водорода)
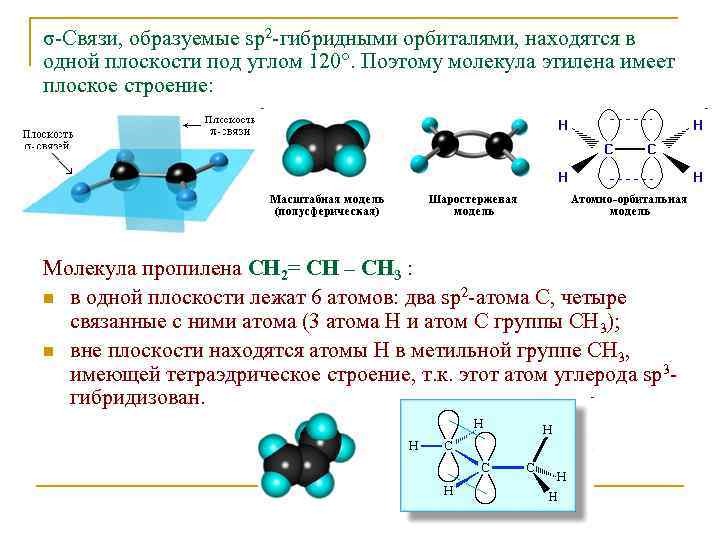 σ-Связи, образуемые sp 2 -гибридными орбиталями, находятся в одной плоскости под углом 120°. Поэтому молекула этилена имеет плоское строение: Молекула пропилена СН 2= СН – СН 3 : n в одной плоскости лежат 6 атомов: два sp 2 -атома С, четыре связанные с ними атома (3 атома Н и атом С группы СН 3); n вне плоскости находятся атомы Н в метильной группе СН 3, имеющей тетраэдрическое строение, т. к. этот атом углерода sp 3 гибридизован.
σ-Связи, образуемые sp 2 -гибридными орбиталями, находятся в одной плоскости под углом 120°. Поэтому молекула этилена имеет плоское строение: Молекула пропилена СН 2= СН – СН 3 : n в одной плоскости лежат 6 атомов: два sp 2 -атома С, четыре связанные с ними атома (3 атома Н и атом С группы СН 3); n вне плоскости находятся атомы Н в метильной группе СН 3, имеющей тетраэдрическое строение, т. к. этот атом углерода sp 3 гибридизован.
 Номенклатура алкенов По международной номенклатуре: n n n названия алкенов производят от названий соответствующих алканов заменой суффикса –ан на –ен: 2 атома С → этан → этен; 3 атома С → пропан → пропен и т. д Главная цепь выбирается так, чтобы она обязательно включала двойную связь (она может быть не самой длинной). Нумерацию углеродных атомов начинают с ближнего к двойной связи конца цепи. Цифра, обозначающая положение двойной связи, ставится обычно после суффикса –ен.
Номенклатура алкенов По международной номенклатуре: n n n названия алкенов производят от названий соответствующих алканов заменой суффикса –ан на –ен: 2 атома С → этан → этен; 3 атома С → пропан → пропен и т. д Главная цепь выбирается так, чтобы она обязательно включала двойную связь (она может быть не самой длинной). Нумерацию углеродных атомов начинают с ближнего к двойной связи конца цепи. Цифра, обозначающая положение двойной связи, ставится обычно после суффикса –ен.
 Названия одновалентных радикалов алкенов: Рациональная номенклатура: n Алкены – производные этилена, в молекуле которого один или несколько атомов водорода замещены на радикалы. Поскольку возможны варианты замещения, то атомы С при двойной связи предварительно обозначаются греческими буквами α и β.
Названия одновалентных радикалов алкенов: Рациональная номенклатура: n Алкены – производные этилена, в молекуле которого один или несколько атомов водорода замещены на радикалы. Поскольку возможны варианты замещения, то атомы С при двойной связи предварительно обозначаются греческими буквами α и β.
 Изомерия алкенов
Изомерия алкенов
 Структурная изомерия алкенов n Изомерия углеродного скелета (начиная с С 4 Н 8): n Изомерия положения двойной связи (начиная с С 4 Н 8): n Межклассовая изомерия с циклоалканами, начиная с С 3 Н 6:
Структурная изомерия алкенов n Изомерия углеродного скелета (начиная с С 4 Н 8): n Изомерия положения двойной связи (начиная с С 4 Н 8): n Межклассовая изомерия с циклоалканами, начиная с С 3 Н 6:
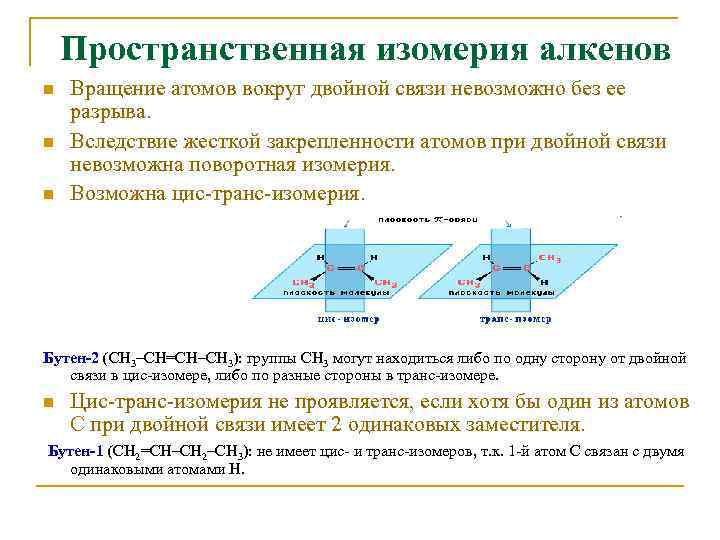 Пространственная изомерия алкенов n n n Вращение атомов вокруг двойной связи невозможно без ее разрыва. Вследствие жесткой закрепленности атомов при двойной связи невозможна поворотная изомерия. Возможна цис-транс-изомерия. Бутен-2 (СН 3–СН=СН–СН 3): группы СН 3 могут находиться либо по одну сторону от двойной связи в цис-изомере, либо по разные стороны в транс-изомере. n Цис-транс-изомерия не проявляется, если хотя бы один из атомов С при двойной связи имеет 2 одинаковых заместителя. Бутен-1 (СН 2=СН–СН 2–СН 3): не имеет цис- и транс-изомеров, т. к. 1 -й атом С связан с двумя одинаковыми атомами Н.
Пространственная изомерия алкенов n n n Вращение атомов вокруг двойной связи невозможно без ее разрыва. Вследствие жесткой закрепленности атомов при двойной связи невозможна поворотная изомерия. Возможна цис-транс-изомерия. Бутен-2 (СН 3–СН=СН–СН 3): группы СН 3 могут находиться либо по одну сторону от двойной связи в цис-изомере, либо по разные стороны в транс-изомере. n Цис-транс-изомерия не проявляется, если хотя бы один из атомов С при двойной связи имеет 2 одинаковых заместителя. Бутен-1 (СН 2=СН–СН 2–СН 3): не имеет цис- и транс-изомеров, т. к. 1 -й атом С связан с двумя одинаковыми атомами Н.
 Физические свойства алкенов закономерно изменяются в гомологическом ряду: n С 2 Н 4 до С 4 Н 8 – газы; n начиная с С 5 Н 10 – жидкости: n с С 18 Н 36 – твердые вещества. Алкены практически нерастворимы в воде, но хорошо растворяются в органических растворителях. Характеристики углерод-углеродных связей: Еπ на 76 к. Дж/моль меньше Еσ. Для алкенов наиболее характерны реакции, протекающие за счет раскрытия менее прочной π-связи. При этом π-связь (в исходном алкене) преобразуется в σ-связь в продукте реакции. Исходное ненасыщенное соединение превращается в насыщенное без образования других продуктов, т. е. происходит реакция присоединения.
Физические свойства алкенов закономерно изменяются в гомологическом ряду: n С 2 Н 4 до С 4 Н 8 – газы; n начиная с С 5 Н 10 – жидкости: n с С 18 Н 36 – твердые вещества. Алкены практически нерастворимы в воде, но хорошо растворяются в органических растворителях. Характеристики углерод-углеродных связей: Еπ на 76 к. Дж/моль меньше Еσ. Для алкенов наиболее характерны реакции, протекающие за счет раскрытия менее прочной π-связи. При этом π-связь (в исходном алкене) преобразуется в σ-связь в продукте реакции. Исходное ненасыщенное соединение превращается в насыщенное без образования других продуктов, т. е. происходит реакция присоединения.
 Химические свойства алкенов n n Реакции присоединения Реакции изомеризации Реакции полимеризации Реакции окисления
Химические свойства алкенов n n Реакции присоединения Реакции изомеризации Реакции полимеризации Реакции окисления
 Гидрирование (присоединение водорода) n Алкены взаимодействуют с водородом при нагревании и повышенном давлении в присутствии катализаторов (Pt, Pd, Ni и др. ) с образованием алканов: Эта реакция используется в промышленности для получения высокооктанового топлива. Галогенирование (присоединение галогенов) n Присоединение галогенов по двойной связи С=С происходит легко в обычных условиях (при комнатной температуре, без катализатора). Например, быстрое обесцвечивание красно-бурой окраски раствора брома в воде (бромной воды) служит качественной реакцией на наличие двойной связи
Гидрирование (присоединение водорода) n Алкены взаимодействуют с водородом при нагревании и повышенном давлении в присутствии катализаторов (Pt, Pd, Ni и др. ) с образованием алканов: Эта реакция используется в промышленности для получения высокооктанового топлива. Галогенирование (присоединение галогенов) n Присоединение галогенов по двойной связи С=С происходит легко в обычных условиях (при комнатной температуре, без катализатора). Например, быстрое обесцвечивание красно-бурой окраски раствора брома в воде (бромной воды) служит качественной реакцией на наличие двойной связи
 Гидрогалогенирование (присоединение галогеноводородов) n Направление реакции присоединения галогеноводородов к алкенам несимметричного строения (например, к пропилену CH 2=CH–СН 3) определяется правилом Марковникова: В реакциях присоединения полярных молекул типа НХ к несимметричным алкенам водород присоединяется к более гидрогенизированному атому углерода при двойной связи (т. е. атому углерода, связанному с наибольшим числом атомов водорода).
Гидрогалогенирование (присоединение галогеноводородов) n Направление реакции присоединения галогеноводородов к алкенам несимметричного строения (например, к пропилену CH 2=CH–СН 3) определяется правилом Марковникова: В реакциях присоединения полярных молекул типа НХ к несимметричным алкенам водород присоединяется к более гидрогенизированному атому углерода при двойной связи (т. е. атому углерода, связанному с наибольшим числом атомов водорода).
 Гидратация (присоединение воды) n Гидратация происходит в присутствии минеральных кислот n В реакциях несимметричных алкенов соблюдается правило Марковникова.
Гидратация (присоединение воды) n Гидратация происходит в присутствии минеральных кислот n В реакциях несимметричных алкенов соблюдается правило Марковникова.
 Полимеризация алкенов n Полимеризация – реакция образования высокомолекулярного соединения (полимера) путем последовательного присоединения молекул низкомолекулярного вещества (мономера) по схеме: n M → Mn Число n в формуле полимера (Mn) называется степенью полимеризации. Реакции полимеризации алкенов идут за счёт присоединения по кратным связям:
Полимеризация алкенов n Полимеризация – реакция образования высокомолекулярного соединения (полимера) путем последовательного присоединения молекул низкомолекулярного вещества (мономера) по схеме: n M → Mn Число n в формуле полимера (Mn) называется степенью полимеризации. Реакции полимеризации алкенов идут за счёт присоединения по кратным связям:
 Изомеризация алкенов Алкены вступают в реакцию изомеризации при нагревании в присутствии катализаторов (Al 2 O 3). Изомеризация алкенов приводит или к перемещению π–связи: или к перестройке углеродного скелета:
Изомеризация алкенов Алкены вступают в реакцию изомеризации при нагревании в присутствии катализаторов (Al 2 O 3). Изомеризация алкенов приводит или к перемещению π–связи: или к перестройке углеродного скелета:
 Реакции окисления алкенов 1. Алкены в отличие от алканов легко окисляются в присутствии окислителей: а) мягкое окисление водным раствором перманганата калия: Происходит обесцвечивание фиолетовой окраски водного раствора KMn. O 4. Это качественная реакция на алкены. б) При жестком окислении алкенов кипящим раствором KMn. O 4 в кислой среде происходит полный разрыв двойной связи: 2. Полное окисление (горение): 3. Частичное окисление алкенов с образованием циклических оксидов, которые широко используются в органическом синтезе:
Реакции окисления алкенов 1. Алкены в отличие от алканов легко окисляются в присутствии окислителей: а) мягкое окисление водным раствором перманганата калия: Происходит обесцвечивание фиолетовой окраски водного раствора KMn. O 4. Это качественная реакция на алкены. б) При жестком окислении алкенов кипящим раствором KMn. O 4 в кислой среде происходит полный разрыв двойной связи: 2. Полное окисление (горение): 3. Частичное окисление алкенов с образованием циклических оксидов, которые широко используются в органическом синтезе:
 Получение алкенов 1. 2. 3. Крекинг алканов: Дегидрогалогенирование галогеналканов при действии спиртового раствора щелочи: Дегидратация спиртов при повышенной температуре (выше 140° C) в присутствии водоотнимающих реагентов:
Получение алкенов 1. 2. 3. Крекинг алканов: Дегидрогалогенирование галогеналканов при действии спиртового раствора щелочи: Дегидратация спиртов при повышенной температуре (выше 140° C) в присутствии водоотнимающих реагентов:
 4. Дегалогенирование дигалогеналканов, имеющих атомы галогена у соседних атомов углерода, при действии активных металлов : 5. Дегидрирование алканов при 500°С:
4. Дегалогенирование дигалогеналканов, имеющих атомы галогена у соседних атомов углерода, при действии активных металлов : 5. Дегидрирование алканов при 500°С:
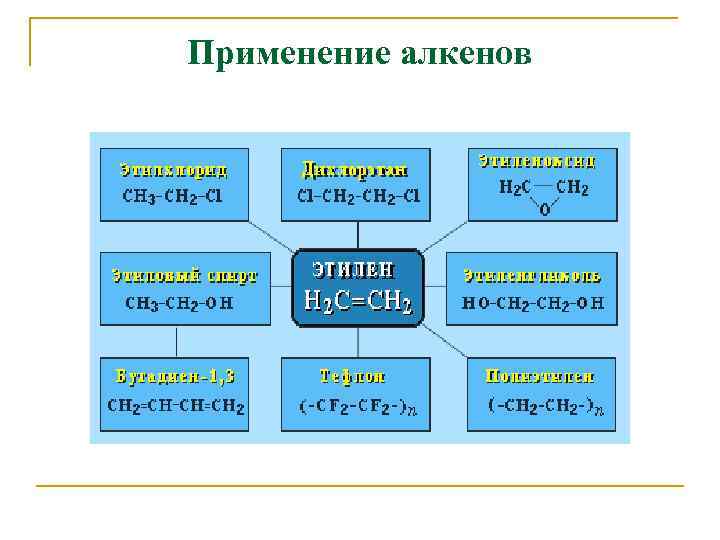 Применение алкенов
Применение алкенов
 Домашнее задание по теме « Циклоалканы. Алкены. Химические свойства и способы получения» : 1. 2. Электронный учебник: часть II: раздел – 3 и 4; Учебник Скворцов А. В. : глава 4 (стр. 43 - 44); глава 5 (стр. 47 - 54); устно – вопросы, стр. 54; письменно: 5. 10 – 5. 14; задачи – 5. 15 – 5. 16.
Домашнее задание по теме « Циклоалканы. Алкены. Химические свойства и способы получения» : 1. 2. Электронный учебник: часть II: раздел – 3 и 4; Учебник Скворцов А. В. : глава 4 (стр. 43 - 44); глава 5 (стр. 47 - 54); устно – вопросы, стр. 54; письменно: 5. 10 – 5. 14; задачи – 5. 15 – 5. 16.



