5_алкены(37).ppt
- Количество слайдов: 37
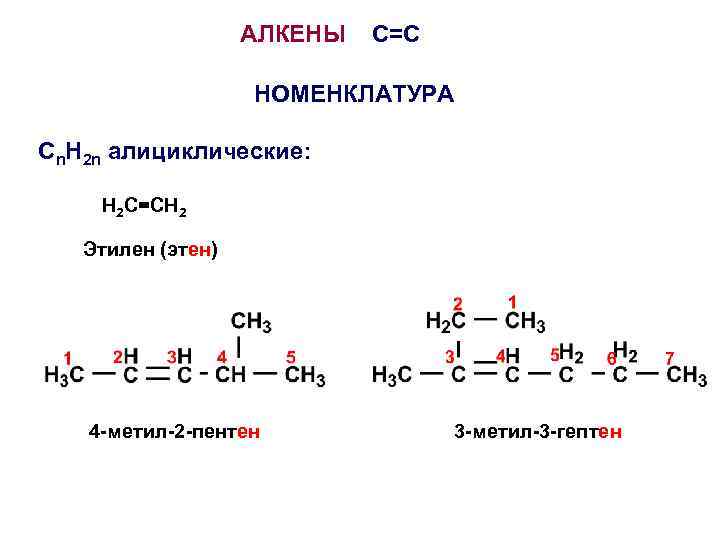 АЛКЕНЫ C=C НОМЕНКЛАТУРА Сn. H 2 n алициклические: H 2 C=СH 2 Этилен (этен) 4 -метил-2 -пентен 3 -метил-3 -гептен
АЛКЕНЫ C=C НОМЕНКЛАТУРА Сn. H 2 n алициклические: H 2 C=СH 2 Этилен (этен) 4 -метил-2 -пентен 3 -метил-3 -гептен
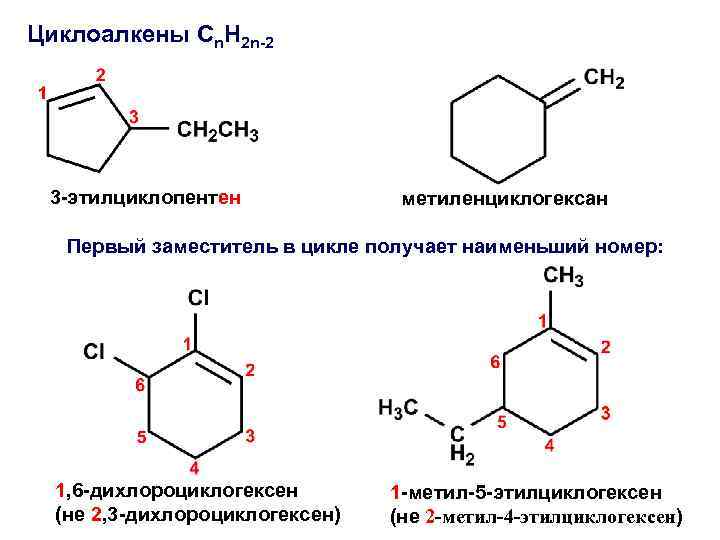 Циклоалкены Cn. H 2 n-2 3 -этилциклопентен метиленциклогексан Первый заместитель в цикле получает наименьший номер: 1, 6 -дихлороциклогексен (не 2, 3 -дихлороциклогексен) 1 -метил-5 -этилциклогексен (не 2 -метил-4 -этилциклогексен)
Циклоалкены Cn. H 2 n-2 3 -этилциклопентен метиленциклогексан Первый заместитель в цикле получает наименьший номер: 1, 6 -дихлороциклогексен (не 2, 3 -дихлороциклогексен) 1 -метил-5 -этилциклогексен (не 2 -метил-4 -этилциклогексен)
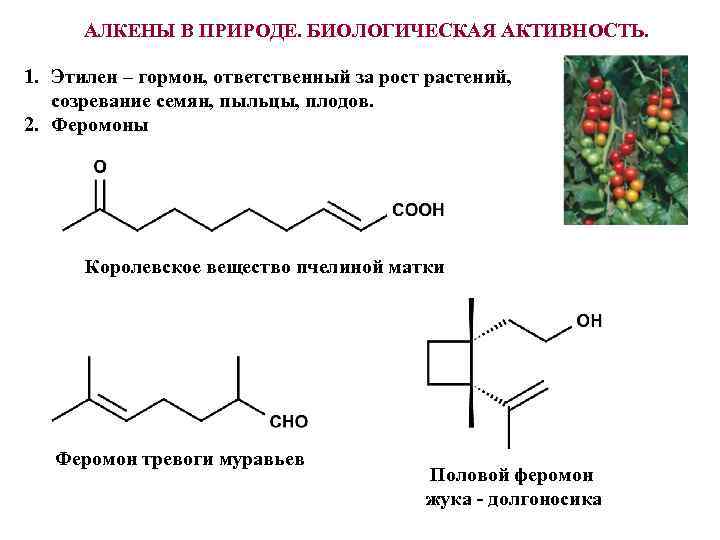 АЛКЕНЫ В ПРИРОДЕ. БИОЛОГИЧЕСКАЯ АКТИВНОСТЬ. 1. Этилен – гормон, ответственный за рост растений, созревание семян, пыльцы, плодов. 2. Феромоны Королевское вещество пчелиной матки Феромон тревоги муравьев Половой феромон жука - долгоносика
АЛКЕНЫ В ПРИРОДЕ. БИОЛОГИЧЕСКАЯ АКТИВНОСТЬ. 1. Этилен – гормон, ответственный за рост растений, созревание семян, пыльцы, плодов. 2. Феромоны Королевское вещество пчелиной матки Феромон тревоги муравьев Половой феромон жука - долгоносика
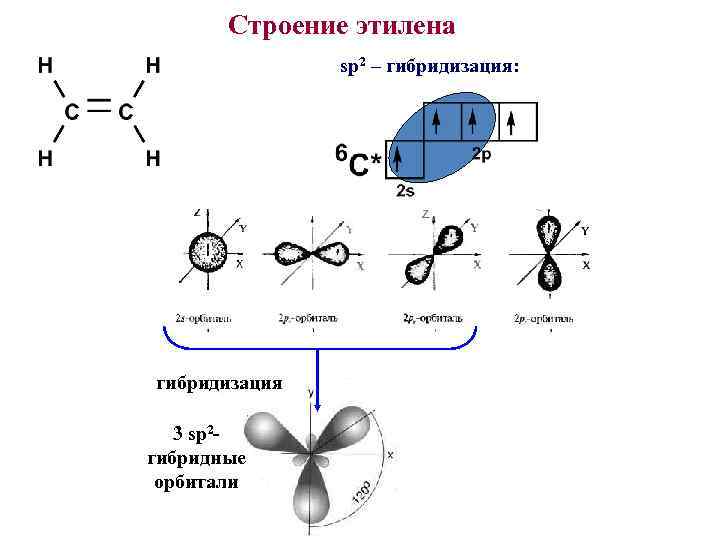 Строение этилена sp 2 – гибридизация: гибридизация 3 sp 2 гибридные орбитали
Строение этилена sp 2 – гибридизация: гибридизация 3 sp 2 гибридные орбитали
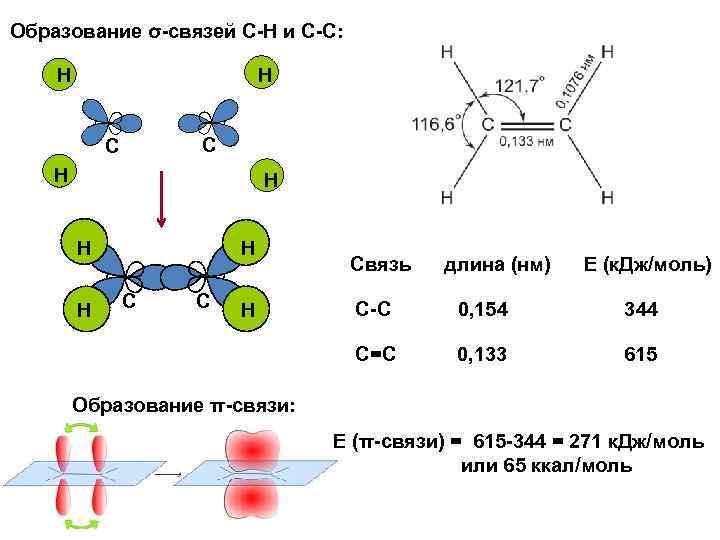 Образование σ-связей С-H и С-С: H H C C H Связь длина (нм) Е (к. Дж/моль) С-С 0, 154 344 С=С 0, 133 615 Образование π-связи: Е (π-связи) = 615 -344 = 271 к. Дж/моль или 65 ккал/моль
Образование σ-связей С-H и С-С: H H C C H Связь длина (нм) Е (к. Дж/моль) С-С 0, 154 344 С=С 0, 133 615 Образование π-связи: Е (π-связи) = 615 -344 = 271 к. Дж/моль или 65 ккал/моль
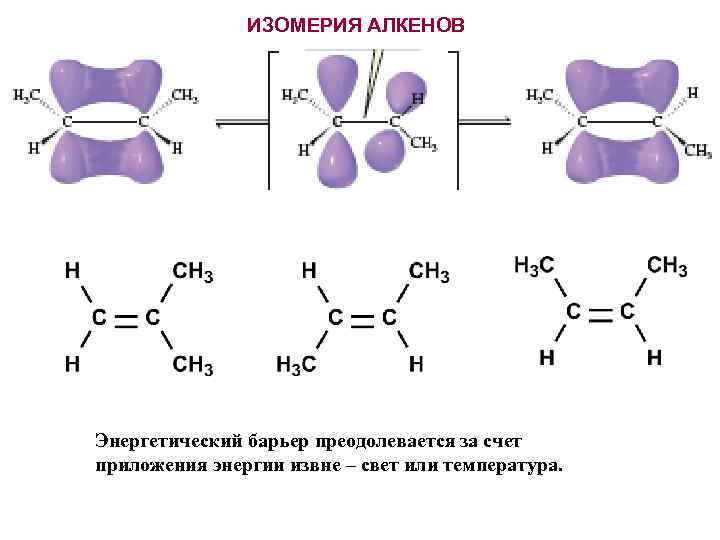 ИЗОМЕРИЯ АЛКЕНОВ Энергетический барьер преодолевается за счет приложения энергии извне – свет или температура.
ИЗОМЕРИЯ АЛКЕНОВ Энергетический барьер преодолевается за счет приложения энергии извне – свет или температура.
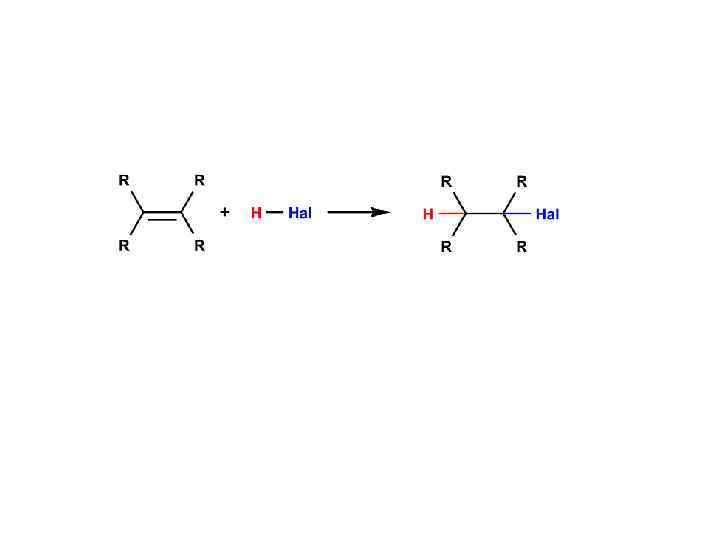
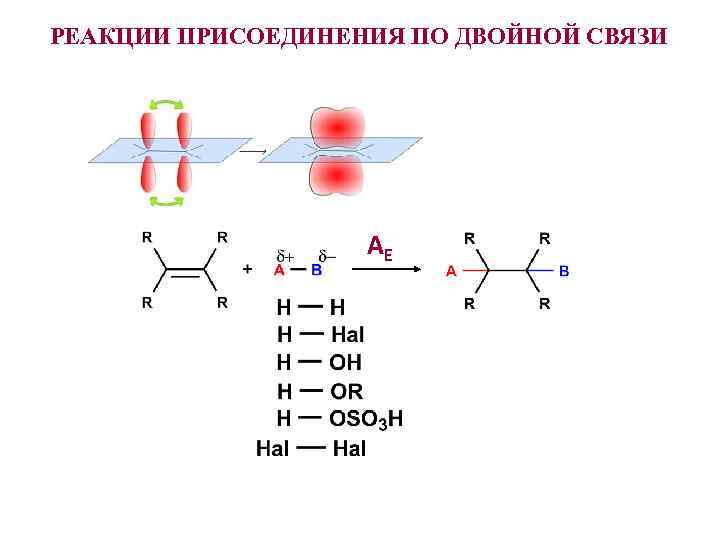 РЕАКЦИИ ПРИСОЕДИНЕНИЯ ПО ДВОЙНОЙ СВЯЗИ AE
РЕАКЦИИ ПРИСОЕДИНЕНИЯ ПО ДВОЙНОЙ СВЯЗИ AE
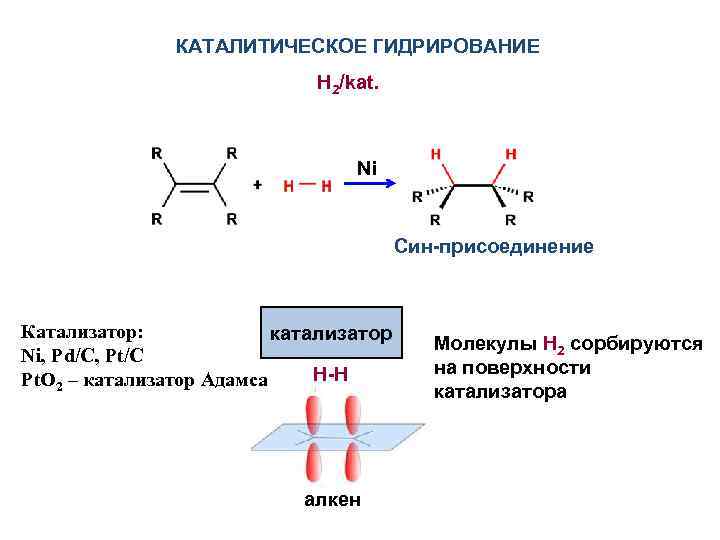 КАТАЛИТИЧЕСКОЕ ГИДРИРОВАНИЕ H 2/kat. Ni Син-присоединение Катализатор: катализатор Ni, Pd/C, Pt/C H-H Pt. O 2 – катализатор Адамса алкен Молекулы H 2 сорбируются на поверхности катализатора
КАТАЛИТИЧЕСКОЕ ГИДРИРОВАНИЕ H 2/kat. Ni Син-присоединение Катализатор: катализатор Ni, Pd/C, Pt/C H-H Pt. O 2 – катализатор Адамса алкен Молекулы H 2 сорбируются на поверхности катализатора
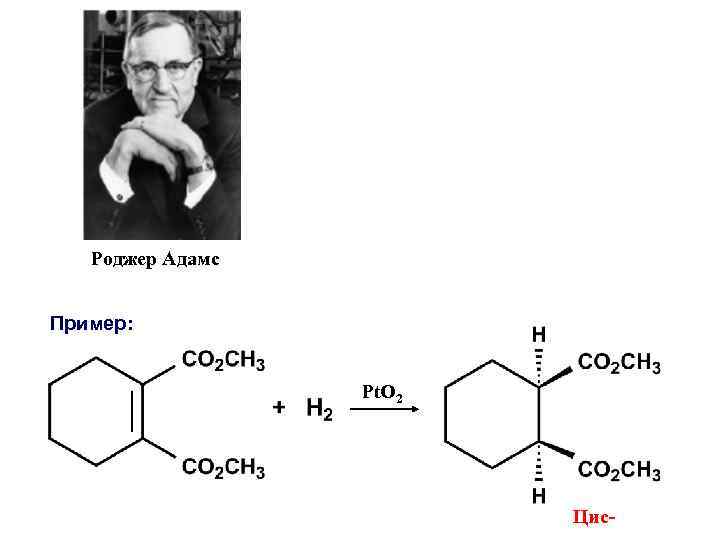 Роджер Адамс Пример: Pt. O 2 Цис-
Роджер Адамс Пример: Pt. O 2 Цис-
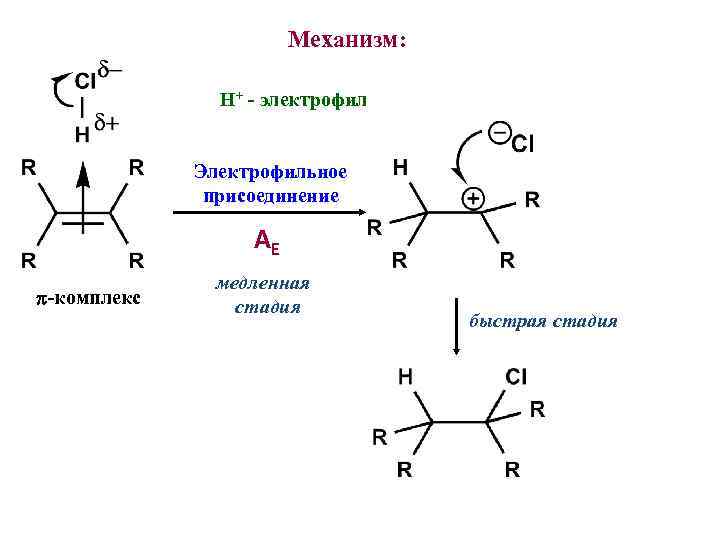 Механизм: H+ - электрофил Электрофильное присоединение AE -комплекс медленная стадия быстрая стадия
Механизм: H+ - электрофил Электрофильное присоединение AE -комплекс медленная стадия быстрая стадия
 Владимир Васильевич Марковников ПРАВИЛО МАРКОВНИКОВА: в несимметричных алкенах водород присоединяется к наиболее гидрогенизированному атому углерода. Современный вариант: Направление присоединения реагентов типа HX к несимметричным алкенам определяется относительной устойчивостью промежуточно образующихся карбокатионов.
Владимир Васильевич Марковников ПРАВИЛО МАРКОВНИКОВА: в несимметричных алкенах водород присоединяется к наиболее гидрогенизированному атому углерода. Современный вариант: Направление присоединения реагентов типа HX к несимметричным алкенам определяется относительной устойчивостью промежуточно образующихся карбокатионов.
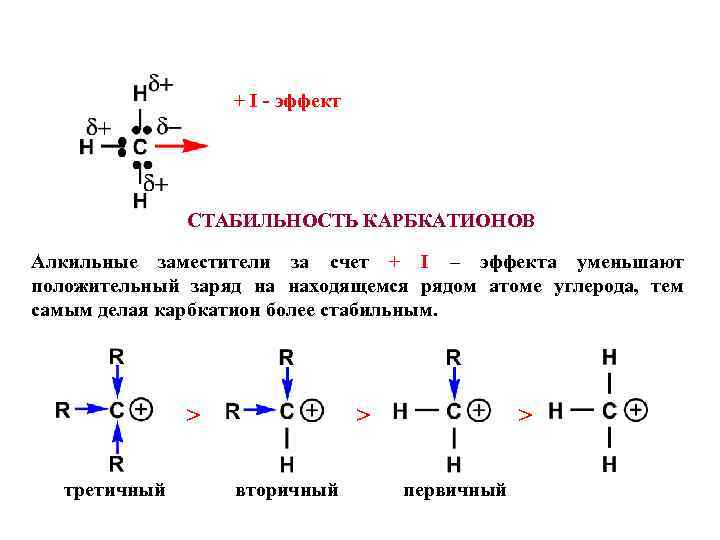 + I - эффект СТАБИЛЬНОСТЬ КАРБКАТИОНОВ Алкильные заместители за счет + I – эффекта уменьшают положительный заряд на находящемся рядом атоме углерода, тем самым делая карбкатион более стабильным. > третичный > вторичный > первичный
+ I - эффект СТАБИЛЬНОСТЬ КАРБКАТИОНОВ Алкильные заместители за счет + I – эффекта уменьшают положительный заряд на находящемся рядом атоме углерода, тем самым делая карбкатион более стабильным. > третичный > вторичный > первичный
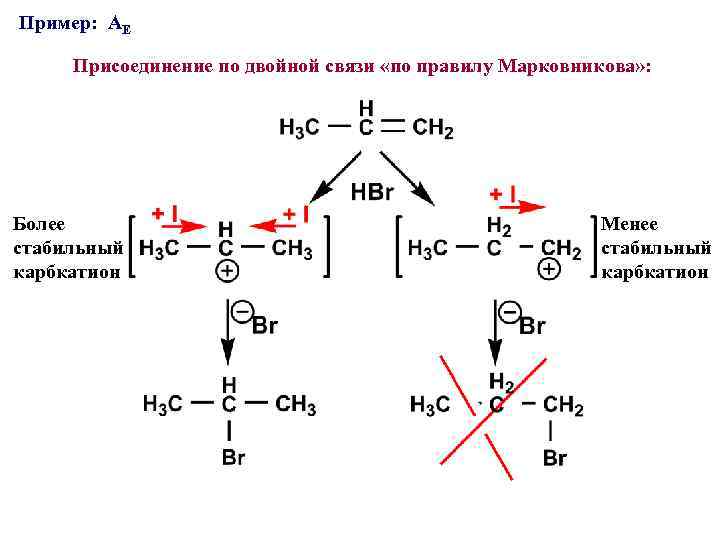 Пример: AE Присоединение по двойной связи «по правилу Марковникова» : Более стабильный карбкатион Менее стабильный карбкатион
Пример: AE Присоединение по двойной связи «по правилу Марковникова» : Более стабильный карбкатион Менее стабильный карбкатион
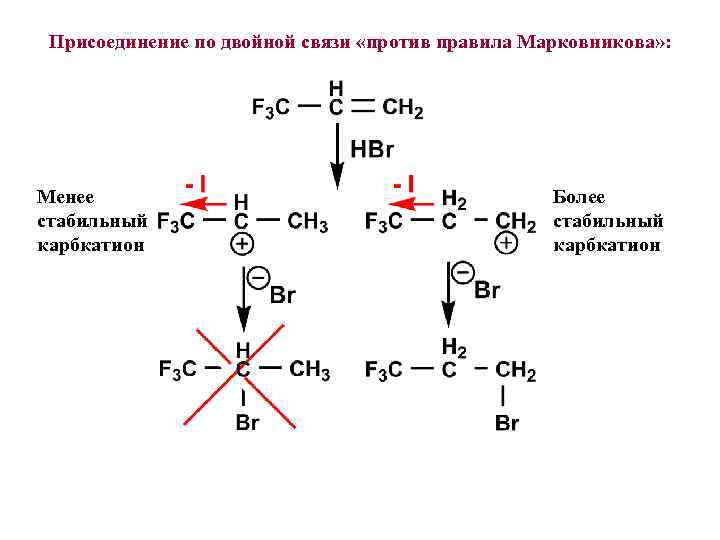 Присоединение по двойной связи «против правила Марковникова» : Менее стабильный карбкатион Более стабильный карбкатион
Присоединение по двойной связи «против правила Марковникова» : Менее стабильный карбкатион Более стабильный карбкатион
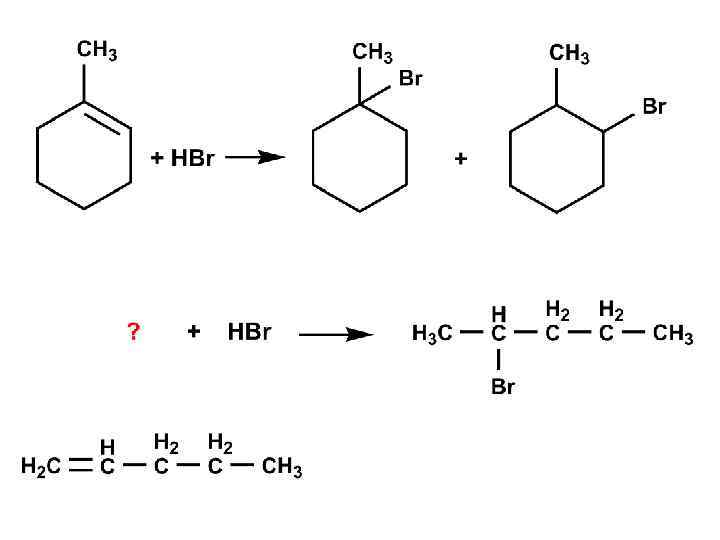
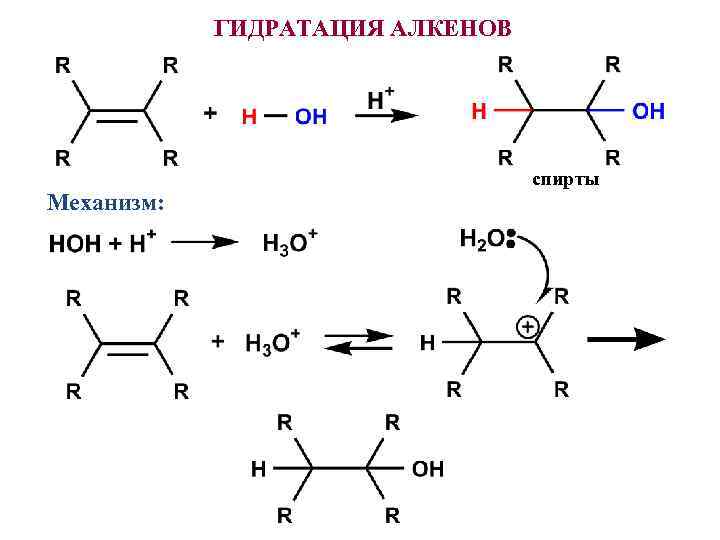 ГИДРАТАЦИЯ АЛКЕНОВ Механизм: спирты
ГИДРАТАЦИЯ АЛКЕНОВ Механизм: спирты
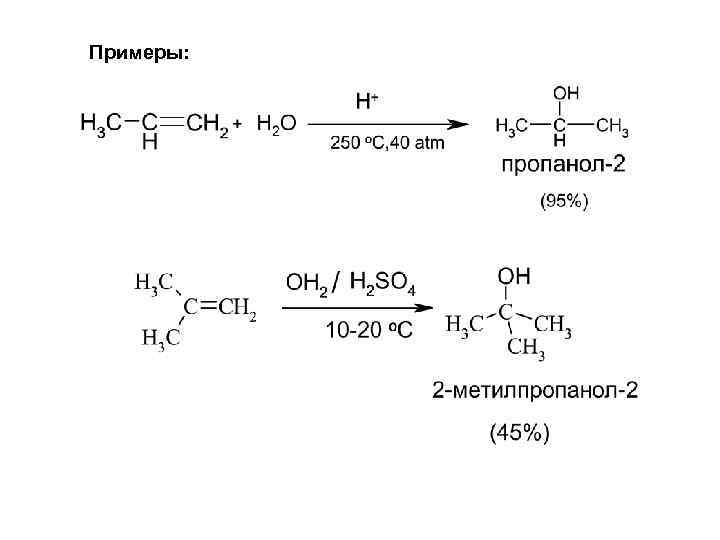 Примеры:
Примеры:
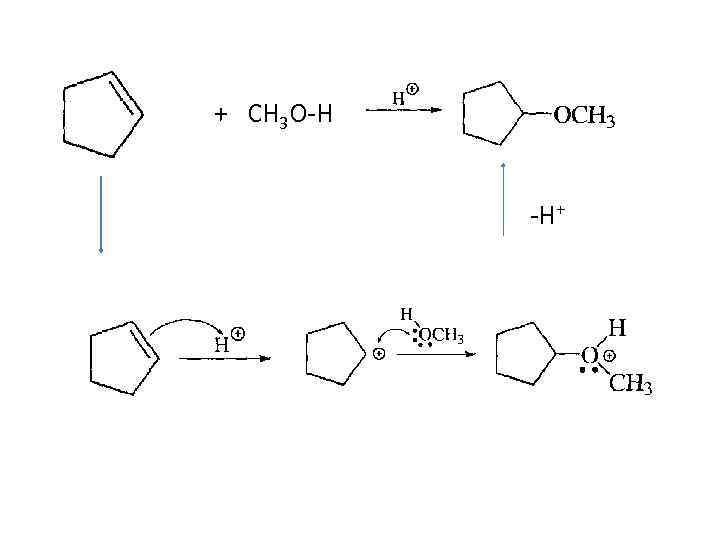 + СH 3 O-H -H+
+ СH 3 O-H -H+
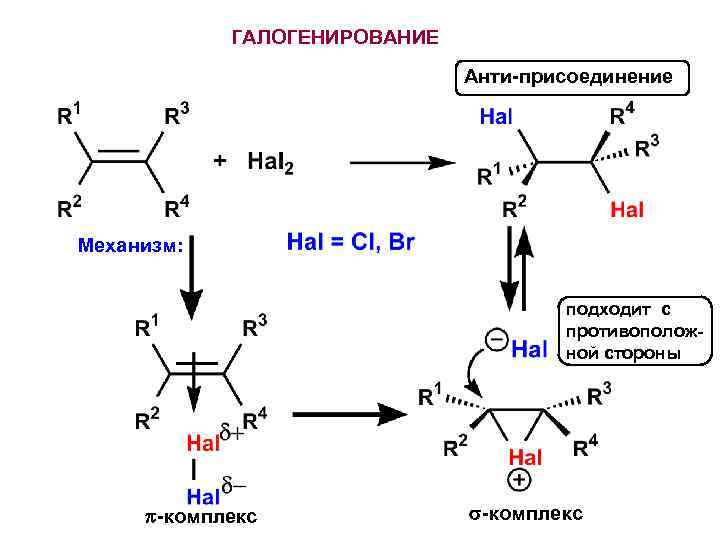 ГАЛОГЕНИРОВАНИЕ Анти-присоединение Механизм: подходит с противоположной стороны -комплекс
ГАЛОГЕНИРОВАНИЕ Анти-присоединение Механизм: подходит с противоположной стороны -комплекс
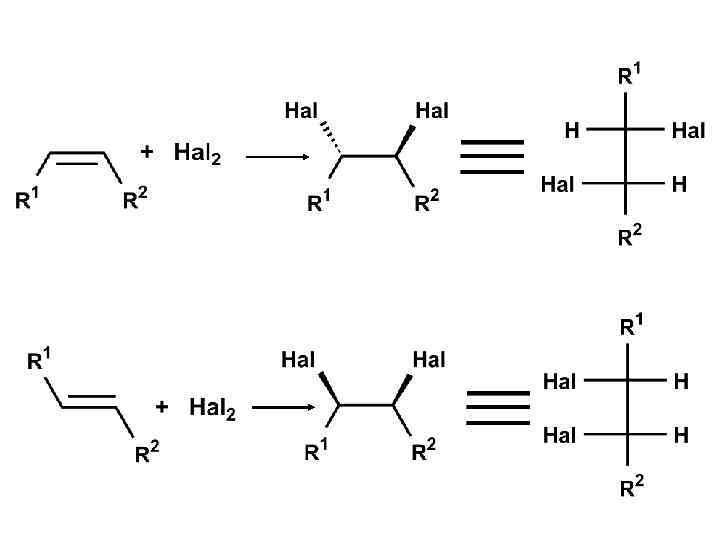
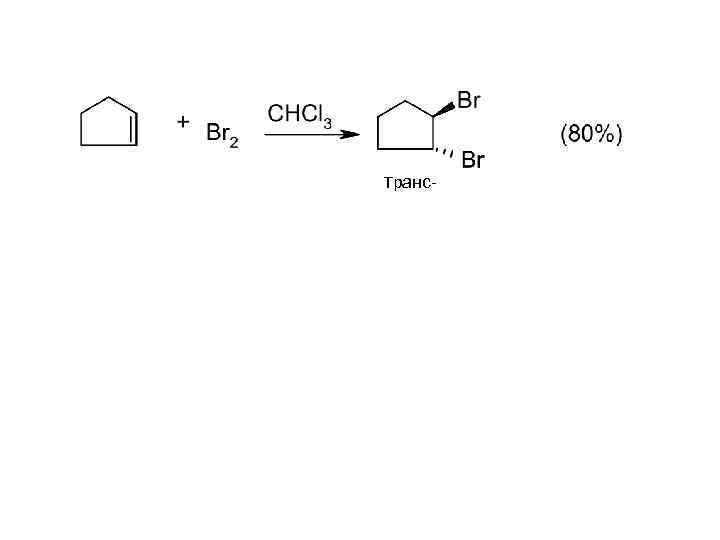 Транс-
Транс-
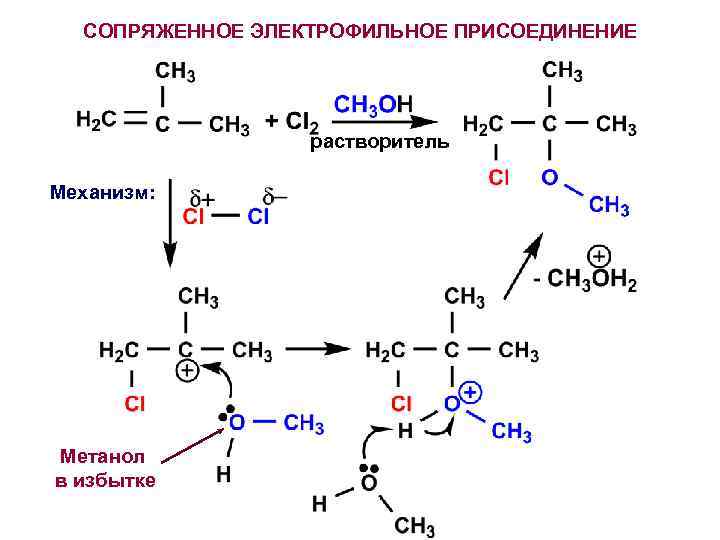 СОПРЯЖЕННОЕ ЭЛЕКТРОФИЛЬНОЕ ПРИСОЕДИНЕНИЕ растворитель Механизм: Метанол в избытке
СОПРЯЖЕННОЕ ЭЛЕКТРОФИЛЬНОЕ ПРИСОЕДИНЕНИЕ растворитель Механизм: Метанол в избытке
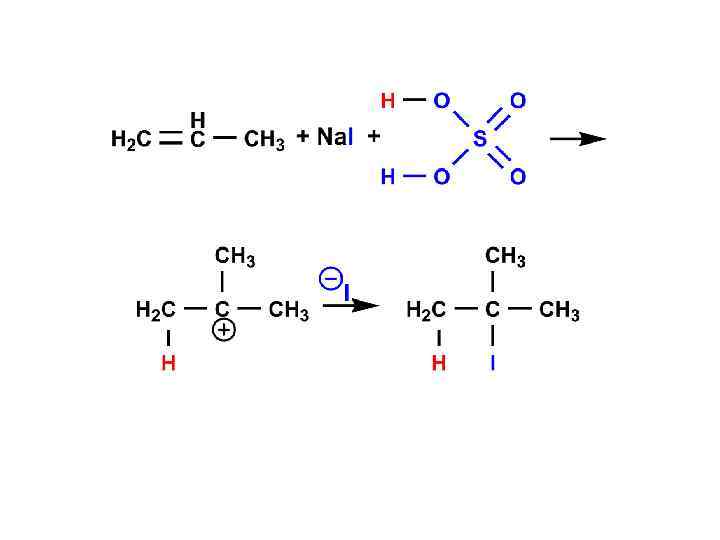
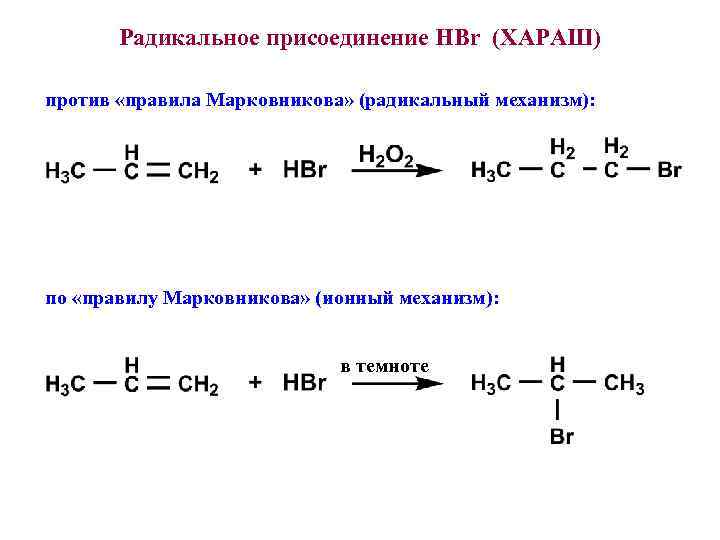 Радикальное присоединение HBr (ХАРАШ) против «правила Марковникова» (радикальный механизм): по «правилу Марковникова» (ионный механизм): в темноте
Радикальное присоединение HBr (ХАРАШ) против «правила Марковникова» (радикальный механизм): по «правилу Марковникова» (ионный механизм): в темноте
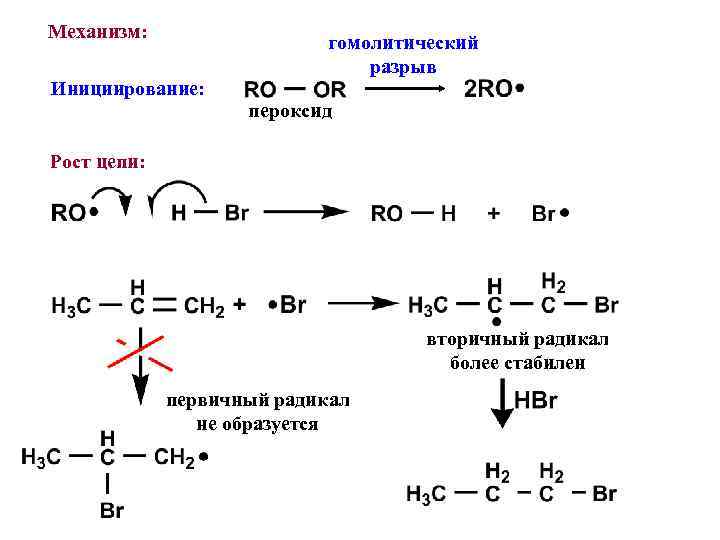 Механизм: Инициирование: гомолитический разрыв пероксид Рост цепи: вторичный радикал более стабилен первичный радикал не образуется
Механизм: Инициирование: гомолитический разрыв пероксид Рост цепи: вторичный радикал более стабилен первичный радикал не образуется
 РЕАКЦИЯ ГИДРОБОРИРОВАНИЯ - ОКИСЛЕНИЯ Против правила Марковникова Согласованный перециклический процесс
РЕАКЦИЯ ГИДРОБОРИРОВАНИЯ - ОКИСЛЕНИЯ Против правила Марковникова Согласованный перециклический процесс
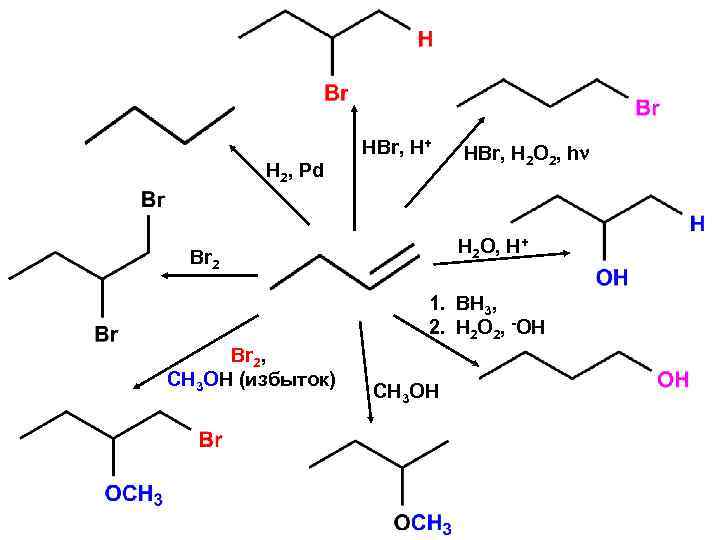 HBr, H+ H 2, Pd HBr, H 2 O 2, h H 2 O, H+ Br 2 1. BH 3, 2. H 2 O 2, -OH Br 2, CH 3 OH (избыток) CH 3 OH
HBr, H+ H 2, Pd HBr, H 2 O 2, h H 2 O, H+ Br 2 1. BH 3, 2. H 2 O 2, -OH Br 2, CH 3 OH (избыток) CH 3 OH
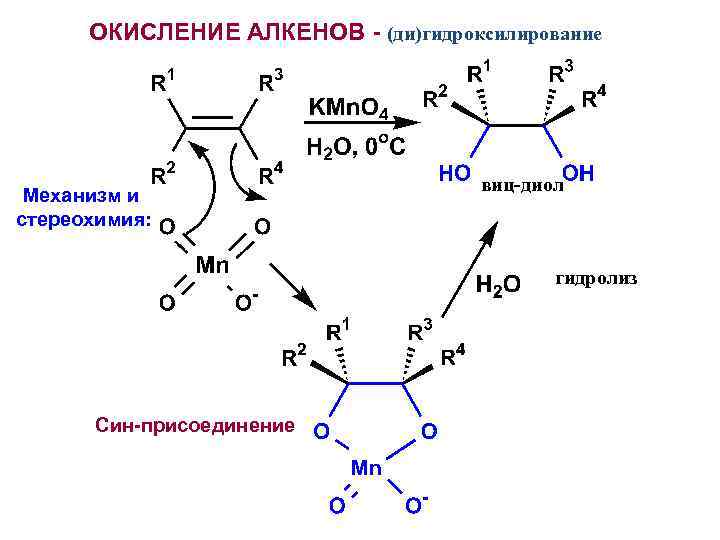 ОКИСЛЕНИЕ АЛКЕНОВ - (ди)гидроксилирование Механизм и стереохимия: виц-диол гидролиз Син-присоединение
ОКИСЛЕНИЕ АЛКЕНОВ - (ди)гидроксилирование Механизм и стереохимия: виц-диол гидролиз Син-присоединение
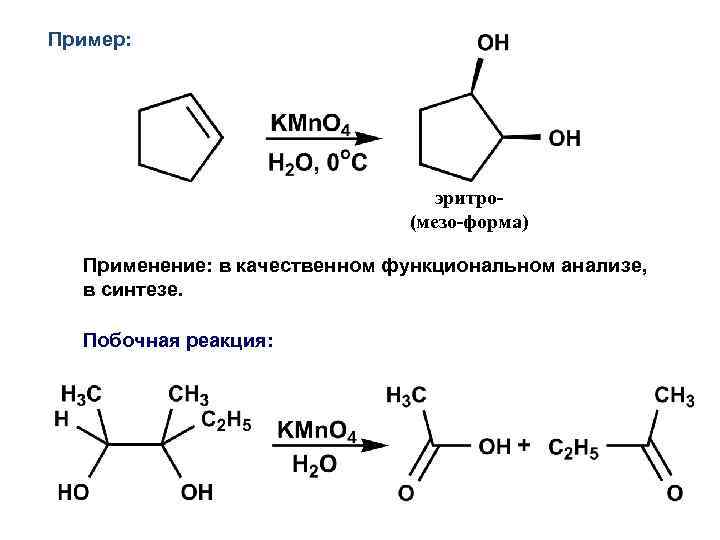 Пример: эритро(мезо-форма) Применение: в качественном функциональном анализе, в синтезе. Побочная реакция:
Пример: эритро(мезо-форма) Применение: в качественном функциональном анализе, в синтезе. Побочная реакция:
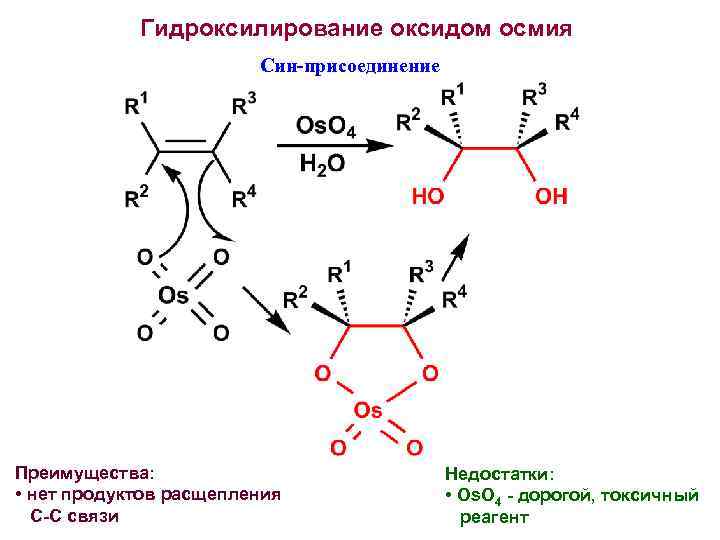 Гидроксилирование оксидом осмия Син-присоединение Преимущества: • нет продуктов расщепления С-С связи Недостатки: • Os. O 4 - дорогой, токсичный реагент
Гидроксилирование оксидом осмия Син-присоединение Преимущества: • нет продуктов расщепления С-С связи Недостатки: • Os. O 4 - дорогой, токсичный реагент
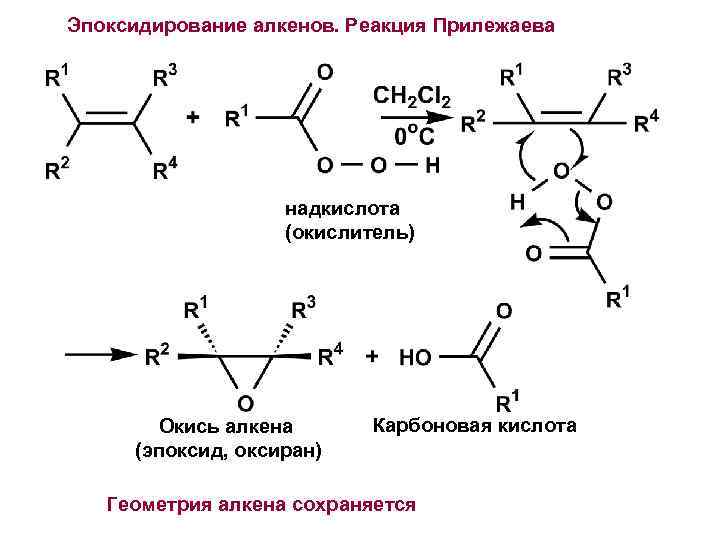 Эпоксидирование алкенов. Реакция Прилежаева надкислота (окислитель) Окись алкена (эпоксид, оксиран) Карбоновая кислота Геометрия алкена сохраняется
Эпоксидирование алкенов. Реакция Прилежаева надкислота (окислитель) Окись алкена (эпоксид, оксиран) Карбоновая кислота Геометрия алкена сохраняется
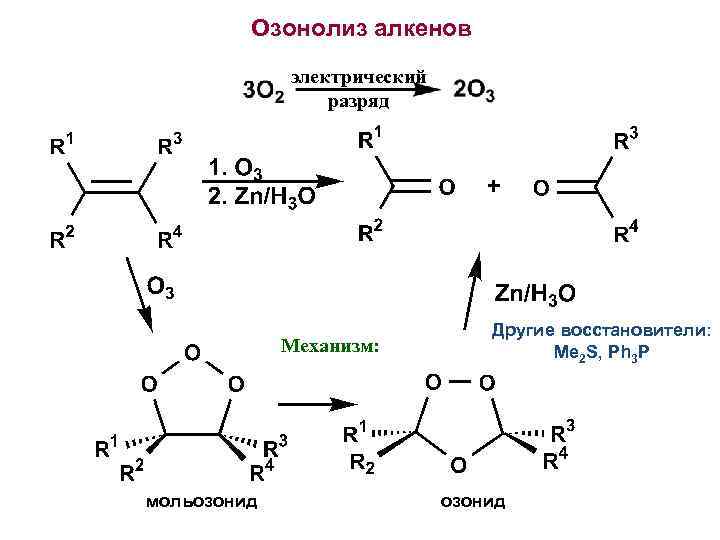 Озонолиз алкенов электрический разряд Механизм: мольозонид Другие восстановители: Me 2 S, Ph 3 P озонид
Озонолиз алкенов электрический разряд Механизм: мольозонид Другие восстановители: Me 2 S, Ph 3 P озонид
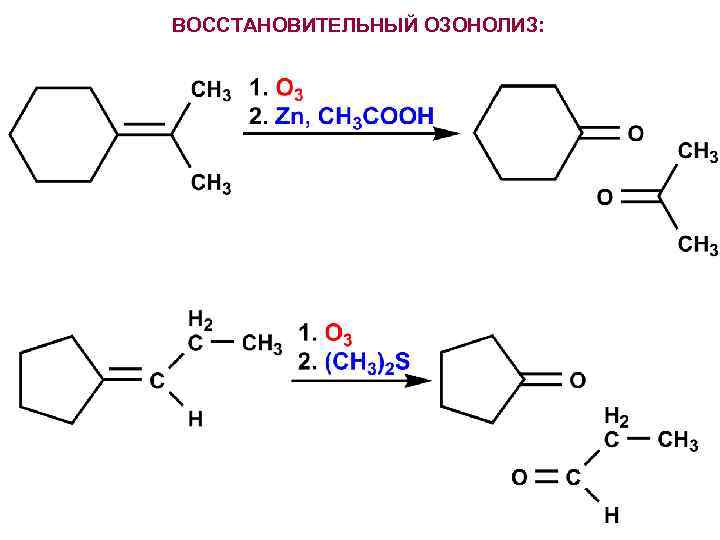 ВОССТАНОВИТЕЛЬНЫЙ ОЗОНОЛИЗ:
ВОССТАНОВИТЕЛЬНЫЙ ОЗОНОЛИЗ:
 ПОЛИМЕРИЗАЦИЯ
ПОЛИМЕРИЗАЦИЯ
 Нобелевская премия по химии 1963 года. Карл Вальдемар Циглер Джулио Натта
Нобелевская премия по химии 1963 года. Карл Вальдемар Циглер Джулио Натта
 мономер полипропилен поливинилхлорид (ПВХ) полистирол тефлон
мономер полипропилен поливинилхлорид (ПВХ) полистирол тефлон


