АЛКЕНЫ.ppt
- Количество слайдов: 49
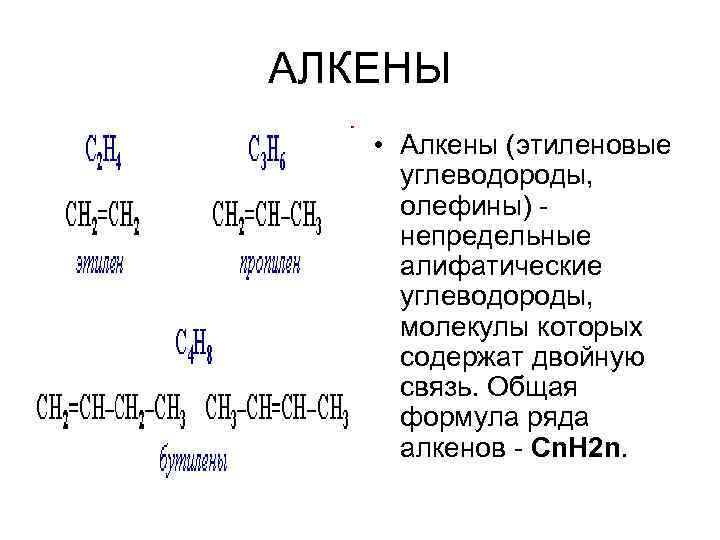 АЛКЕНЫ • Алкены (этиленовые углеводороды, олефины) - непредельные алифатические углеводороды, молекулы которых содержат двойную связь. Общая формула ряда алкенов - Cn. H 2 n.
АЛКЕНЫ • Алкены (этиленовые углеводороды, олефины) - непредельные алифатические углеводороды, молекулы которых содержат двойную связь. Общая формула ряда алкенов - Cn. H 2 n.
 • В отличие от предельных углеводородов, алкены содержат двойную связь С=С, которая осуществляется 4 -мя общими электронами: • В образовании такой связи участвуют атомы углерода в sp 2 -гибридизованном состоянии. Каждый из них имеет по три 2 sp 2 -гибридных орбитали, направленных друг к другу под углом 120°, и одну негибридизованную 2 рорбиталь, расположенную под углом 90° к плоскости гибридных АО.
• В отличие от предельных углеводородов, алкены содержат двойную связь С=С, которая осуществляется 4 -мя общими электронами: • В образовании такой связи участвуют атомы углерода в sp 2 -гибридизованном состоянии. Каждый из них имеет по три 2 sp 2 -гибридных орбитали, направленных друг к другу под углом 120°, и одну негибридизованную 2 рорбиталь, расположенную под углом 90° к плоскости гибридных АО.

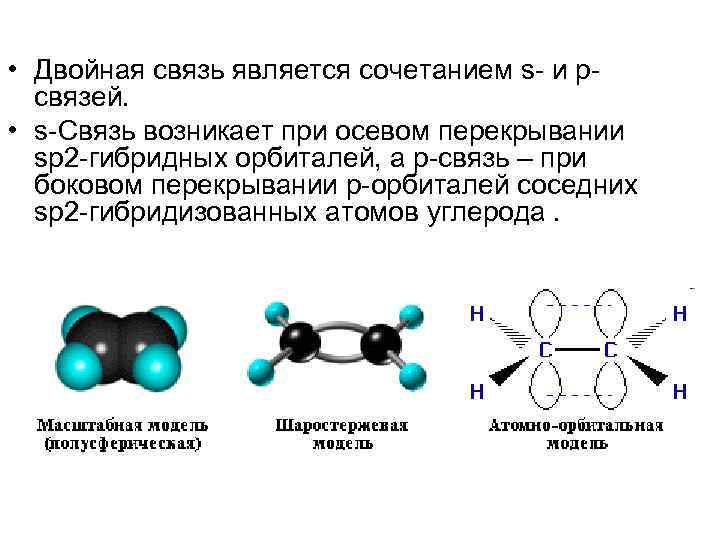 • Двойная связь является сочетанием s- и pсвязей. • s-Связь возникает при осевом перекрывании sp 2 -гибридных орбиталей, а p-связь – при боковом перекрывании р-орбиталей соседних sp 2 -гибридизованных атомов углерода.
• Двойная связь является сочетанием s- и pсвязей. • s-Связь возникает при осевом перекрывании sp 2 -гибридных орбиталей, а p-связь – при боковом перекрывании р-орбиталей соседних sp 2 -гибридизованных атомов углерода.
 • По своей природе p-связь отличается от s-связи: p-связь менее прочная вследствие меньшей эффективности перекрывания рорбиталей. • В молекуле пропилена СН 2=СН–СН 3 в одной плоскости лежат 6 атомов: два sp 2 -атома углерода и четыре связанные с ними атома. • Вне этой плоскости находятся атомы водорода в метильной группе СН 3, имеющей тетраэдрическое строение.
• По своей природе p-связь отличается от s-связи: p-связь менее прочная вследствие меньшей эффективности перекрывания рорбиталей. • В молекуле пропилена СН 2=СН–СН 3 в одной плоскости лежат 6 атомов: два sp 2 -атома углерода и четыре связанные с ними атома. • Вне этой плоскости находятся атомы водорода в метильной группе СН 3, имеющей тетраэдрическое строение.
 • Номенклатура алкенов • Названия алкенов производят от названий соответствующих алканов путем замены суффикса –ан на –ен: • 2 атома С ® этан ® этен; 3 атома С ® пропан ® пропен и т. д. • Главная цепь выбирается таким образом, чтобы она обязательно включала в себя двойную связь.
• Номенклатура алкенов • Названия алкенов производят от названий соответствующих алканов путем замены суффикса –ан на –ен: • 2 атома С ® этан ® этен; 3 атома С ® пропан ® пропен и т. д. • Главная цепь выбирается таким образом, чтобы она обязательно включала в себя двойную связь.
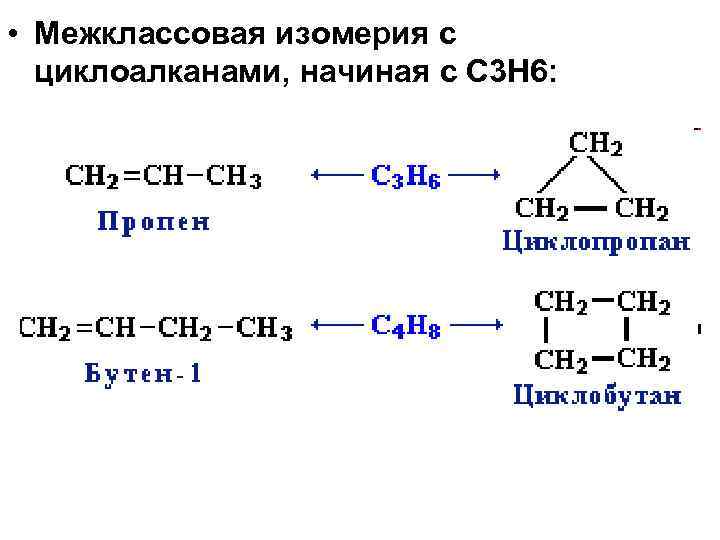 • Межклассовая изомерия с циклоалканами, начиная с С 3 Н 6:
• Межклассовая изомерия с циклоалканами, начиная с С 3 Н 6:
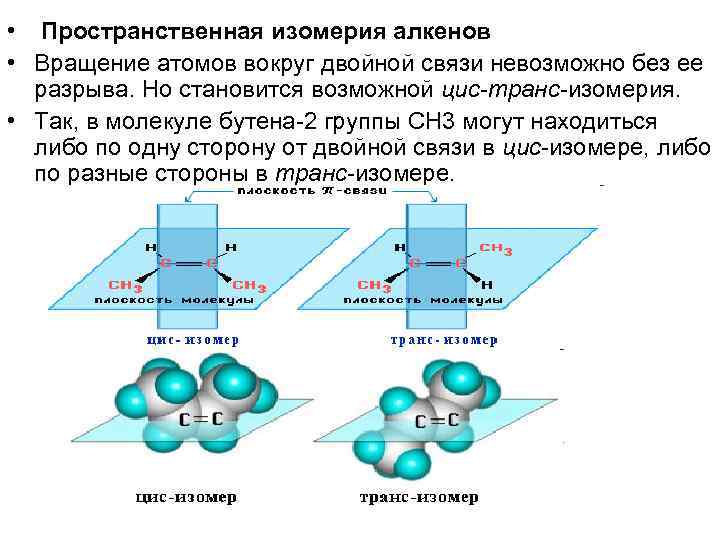 • Пространственная изомерия алкенов • Вращение атомов вокруг двойной связи невозможно без ее разрыва. Но становится возможной цис-транс-изомерия. • Так, в молекуле бутена-2 группы СН 3 могут находиться либо по одну сторону от двойной связи в цис-изомере, либо по разные стороны в транс-изомере.
• Пространственная изомерия алкенов • Вращение атомов вокруг двойной связи невозможно без ее разрыва. Но становится возможной цис-транс-изомерия. • Так, в молекуле бутена-2 группы СН 3 могут находиться либо по одну сторону от двойной связи в цис-изомере, либо по разные стороны в транс-изомере.
 • Физические свойства алкенов закономерно изменяются в гомологическом ряду: от С 2 Н 4 до С 4 Н 8 – газы, начиная с С 5 Н 10 – жидкости, с С 18 Н 36 – твердые вещества. Алкены практически нерастворимы в воде, но хорошо растворяются в органических растворителях. • Химические свойства алкенов определяются строением и свойствами двойной связи С=С, которая значительно активнее других связей в молекулах этих соединений. Алкены химически более активны, чем алканы.
• Физические свойства алкенов закономерно изменяются в гомологическом ряду: от С 2 Н 4 до С 4 Н 8 – газы, начиная с С 5 Н 10 – жидкости, с С 18 Н 36 – твердые вещества. Алкены практически нерастворимы в воде, но хорошо растворяются в органических растворителях. • Химические свойства алкенов определяются строением и свойствами двойной связи С=С, которая значительно активнее других связей в молекулах этих соединений. Алкены химически более активны, чем алканы.
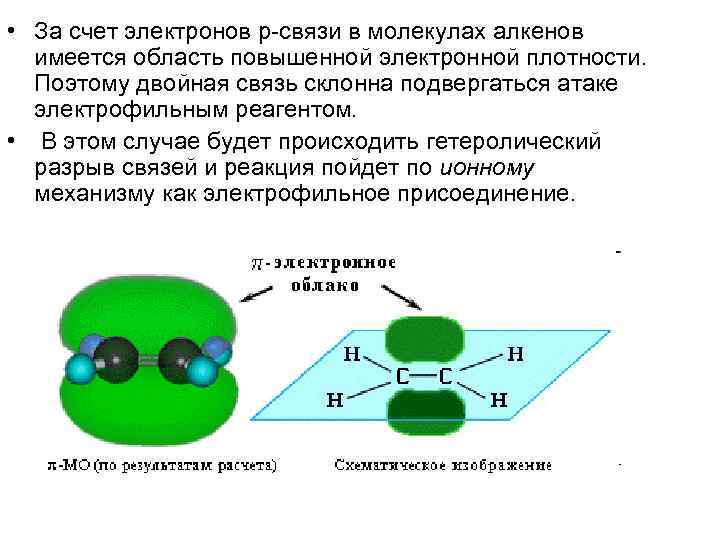 • За счет электронов p-связи в молекулах алкенов имеется область повышенной электронной плотности. Поэтому двойная связь склонна подвергаться атаке электрофильным реагентом. • В этом случае будет происходить гетеролический разрыв связей и реакция пойдет по ионному механизму как электрофильное присоединение.
• За счет электронов p-связи в молекулах алкенов имеется область повышенной электронной плотности. Поэтому двойная связь склонна подвергаться атаке электрофильным реагентом. • В этом случае будет происходить гетеролический разрыв связей и реакция пойдет по ионному механизму как электрофильное присоединение.

 • Гидрирование (присоединение водорода) • Алкены взаимодействуют с водородом при нагревании в присутствии металлов Pt, Pd или Ni: • • Присоединение водорода к атомам углерода в алкенах приводит к понижению степени их окисления: •
• Гидрирование (присоединение водорода) • Алкены взаимодействуют с водородом при нагревании в присутствии металлов Pt, Pd или Ni: • • Присоединение водорода к атомам углерода в алкенах приводит к понижению степени их окисления: •
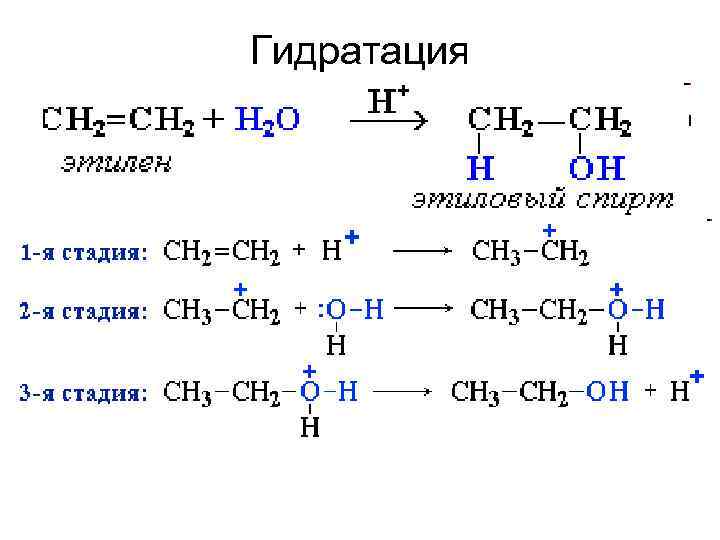 Гидратация
Гидратация
 • Реакции окисления алкенов • 1. Мягкое окисление алкенов водным раствором перманганата калия приводит к образованию двухатомных спиртов (реакция Вагнера):
• Реакции окисления алкенов • 1. Мягкое окисление алкенов водным раствором перманганата калия приводит к образованию двухатомных спиртов (реакция Вагнера):
 • 2. При жестком окислении алкенов кипящим раствором KMn. O 4 в кислой среде происходит полный разрыв двойной связи:
• 2. При жестком окислении алкенов кипящим раствором KMn. O 4 в кислой среде происходит полный разрыв двойной связи:
 Горение
Горение
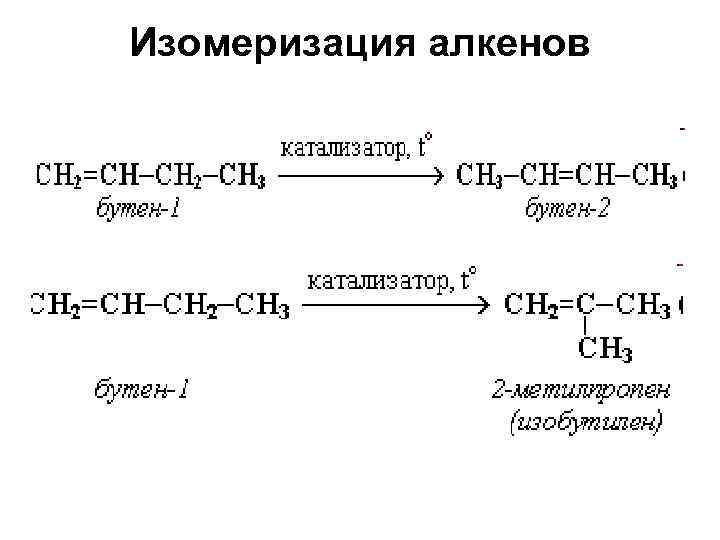 Изомеризация алкенов
Изомеризация алкенов
 • Получение алкенов • В природе алкены встречаются в меньшей степени, чем предельные углеводороды, по-видимому, вследствие своей высокой реакционной способности. • Крекинг алканов:
• Получение алкенов • В природе алкены встречаются в меньшей степени, чем предельные углеводороды, по-видимому, вследствие своей высокой реакционной способности. • Крекинг алканов:
 • Отщепление (элиминирование) двух атомов или групп атомов от соседних атомов углерода с образованием между ними p-связи.
• Отщепление (элиминирование) двух атомов или групп атомов от соседних атомов углерода с образованием между ними p-связи.
 • АЛКИНЫ • Алкины (ацетиленовые углеводороды) – непредельные алифатические углеводороды, молекулы которых содержат тройную связь C≡C. • Общая формула алкинов с одной тройной связью Сn. H 2 n-2
• АЛКИНЫ • Алкины (ацетиленовые углеводороды) – непредельные алифатические углеводороды, молекулы которых содержат тройную связь C≡C. • Общая формула алкинов с одной тройной связью Сn. H 2 n-2
 • В образовании такой связи участвуют атомы углерода в sp-гибридизованном состоянии. Каждый из них имеет по две sp-гибридных орбитали, направленных друг к другу под углом 180°, и две негибридных р-орбитали, расположенных под углом 90° по отношению друг к другу и к sp-гибридным орбиталям:
• В образовании такой связи участвуют атомы углерода в sp-гибридизованном состоянии. Каждый из них имеет по две sp-гибридных орбитали, направленных друг к другу под углом 180°, и две негибридных р-орбитали, расположенных под углом 90° по отношению друг к другу и к sp-гибридным орбиталям:
 • Номенклатура алкинов • По систематической номенклатуре названия ацетиленовых углеводородов производят от названий соответствующих алканов путем замены суффикса –ан на –ин: • 2 атома С → этан → этин; 3 атома С → пропан → пропин и т. д. • Главная цепь выбирается таким образом, чтобы она обязательно включала в себя тройную связь. • Нумерацию углеродных атомов начинают с ближнего к тройной связи конца цепи. Цифра, обозначающая положение тройной связи, ставится обычно после суффикса –ин. Например:
• Номенклатура алкинов • По систематической номенклатуре названия ацетиленовых углеводородов производят от названий соответствующих алканов путем замены суффикса –ан на –ин: • 2 атома С → этан → этин; 3 атома С → пропан → пропин и т. д. • Главная цепь выбирается таким образом, чтобы она обязательно включала в себя тройную связь. • Нумерацию углеродных атомов начинают с ближнего к тройной связи конца цепи. Цифра, обозначающая положение тройной связи, ставится обычно после суффикса –ин. Например:
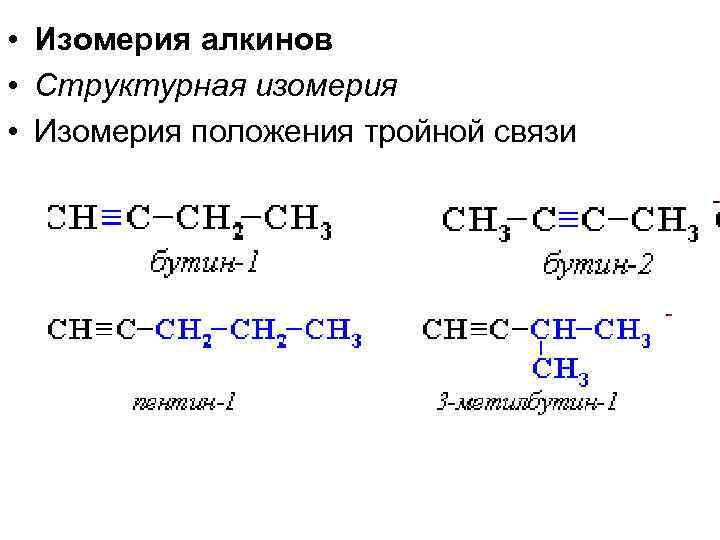 • Изомерия алкинов • Структурная изомерия • Изомерия положения тройной связи
• Изомерия алкинов • Структурная изомерия • Изомерия положения тройной связи
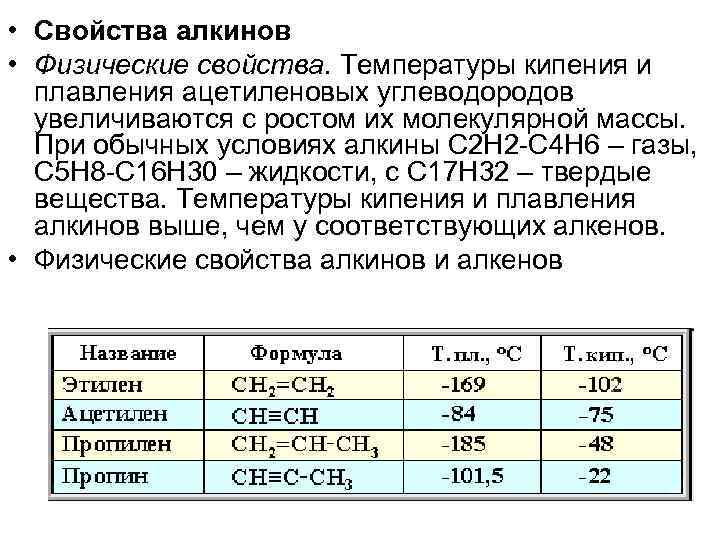 • Свойства алкинов • Физические свойства. Температуры кипения и плавления ацетиленовых углеводородов увеличиваются с ростом их молекулярной массы. При обычных условиях алкины С 2 Н 2 -С 4 Н 6 – газы, С 5 Н 8 -С 16 Н 30 – жидкости, с С 17 Н 32 – твердые вещества. Температуры кипения и плавления алкинов выше, чем у соответствующих алкенов. • Физические свойства алкинов и алкенов
• Свойства алкинов • Физические свойства. Температуры кипения и плавления ацетиленовых углеводородов увеличиваются с ростом их молекулярной массы. При обычных условиях алкины С 2 Н 2 -С 4 Н 6 – газы, С 5 Н 8 -С 16 Н 30 – жидкости, с С 17 Н 32 – твердые вещества. Температуры кипения и плавления алкинов выше, чем у соответствующих алкенов. • Физические свойства алкинов и алкенов
 • Химические свойства алкинов сходны с алкенами, что обусловлено их ненасыщенностью. • Характеристики химических связей в алкинах
• Химические свойства алкинов сходны с алкенами, что обусловлено их ненасыщенностью. • Характеристики химических связей в алкинах
 • π-Электроны более короткой тройной связи прочнее удерживаются ядрами атомов углерода. Поэтому реакции электрофильного присоединения к алкинам протекают медленнее, чем к алкенам. • π-Электронное облако тройной связи сосредоточено в основном в межъядерном пространстве. • Следствием этого является доступность ядер углерода при атаке нуклеофильными реагентами. • Алкины способны вступать в реакции нуклеофильного присоединения.
• π-Электроны более короткой тройной связи прочнее удерживаются ядрами атомов углерода. Поэтому реакции электрофильного присоединения к алкинам протекают медленнее, чем к алкенам. • π-Электронное облако тройной связи сосредоточено в основном в межъядерном пространстве. • Следствием этого является доступность ядер углерода при атаке нуклеофильными реагентами. • Алкины способны вступать в реакции нуклеофильного присоединения.
 • Связь атома водорода с углеродом в spгибридизованном состоянии значительно более полярна по сравнению с С–Н-связями в алканах и алкенах. • Это объясняется различным вкладом в гибридизованное состояние s-орбитали, которая более прочно, чем р-АО, удерживает электроны. • Доля s-АО в sp 3 -состоянии составляет 25%, в sp 2 – 33%, а в sp – 50%. • Чем больше вклад s-АО, тем выше способность атома удерживать внешние электроны, т. е. его электроотрицательность.
• Связь атома водорода с углеродом в spгибридизованном состоянии значительно более полярна по сравнению с С–Н-связями в алканах и алкенах. • Это объясняется различным вкладом в гибридизованное состояние s-орбитали, которая более прочно, чем р-АО, удерживает электроны. • Доля s-АО в sp 3 -состоянии составляет 25%, в sp 2 – 33%, а в sp – 50%. • Чем больше вклад s-АО, тем выше способность атома удерживать внешние электроны, т. е. его электроотрицательность.
 • Реакции присоединения к алкинам • 1. Гидрирование • В присутствии металлических катализаторов (Pt, Ni) алкины присоединяют водород с образованием алкенов (разрывается первая π-связь), а затем алканов (разрывается вторая π-связь): • 2. Галогенирование • Электрофильное присоединение галогенов к алкинам протекает медленнее, чем для алкенов. • 3. Гидрогалогенирование • Присоединение галогеноводородов также идет по электрофильному механизму. • 4. Гидратация (реакция Кучерова) • Присоединение воды к ацетилену происходит в присутствии катализатора соли ртути (II) и идет через образование неустойчивого непредельного спирта, который изомеризуется в уксусный альдегид.
• Реакции присоединения к алкинам • 1. Гидрирование • В присутствии металлических катализаторов (Pt, Ni) алкины присоединяют водород с образованием алкенов (разрывается первая π-связь), а затем алканов (разрывается вторая π-связь): • 2. Галогенирование • Электрофильное присоединение галогенов к алкинам протекает медленнее, чем для алкенов. • 3. Гидрогалогенирование • Присоединение галогеноводородов также идет по электрофильному механизму. • 4. Гидратация (реакция Кучерова) • Присоединение воды к ацетилену происходит в присутствии катализатора соли ртути (II) и идет через образование неустойчивого непредельного спирта, который изомеризуется в уксусный альдегид.
 • Образование солей • Ацетилен и его гомологи с концевой тройной связью R–C≡C–H (алкины-1) вследствие полярности связи С(sp)-Н проявляют слабые кислотные свойства: атомы водорода могут замещаться атомами металла. При этом образуются соли – ацетилениды: •
• Образование солей • Ацетилен и его гомологи с концевой тройной связью R–C≡C–H (алкины-1) вследствие полярности связи С(sp)-Н проявляют слабые кислотные свойства: атомы водорода могут замещаться атомами металла. При этом образуются соли – ацетилениды: •
 • Алкины обесцвечивают разбавленный раствор перманганата калия, что используется для доказательства их ненасыщенности. • В этих условиях происходит мягкое окисление без разрыва σ-связи С–С (разрушаются только π-связи).
• Алкины обесцвечивают разбавленный раствор перманганата калия, что используется для доказательства их ненасыщенности. • В этих условиях происходит мягкое окисление без разрыва σ-связи С–С (разрушаются только π-связи).
 • Получение алкинов • Ацетилен является важнейшим исходным продуктом в производстве многих органических веществ и материалов. Его получают в больших количествах, используя ряд промышленных методов. • Реакцию проводят электродуговым способом, пропуская метан между электродами с временем контакта 0, 1 -0, 01 секунды. Столь малое время нагревания обусловлено тем, что ацетилен при такой температуре может разлагаться на углерод и водород.
• Получение алкинов • Ацетилен является важнейшим исходным продуктом в производстве многих органических веществ и материалов. Его получают в больших количествах, используя ряд промышленных методов. • Реакцию проводят электродуговым способом, пропуская метан между электродами с временем контакта 0, 1 -0, 01 секунды. Столь малое время нагревания обусловлено тем, что ацетилен при такой температуре может разлагаться на углерод и водород.
 • Применение алкинов • Наибольшее практическое значение имеют ацетилен H–C≡C–H и винилацетилен CH 2=CH– C≡CH. Ацетилен используется для получения самых разнообразных веществ:
• Применение алкинов • Наибольшее практическое значение имеют ацетилен H–C≡C–H и винилацетилен CH 2=CH– C≡CH. Ацетилен используется для получения самых разнообразных веществ:
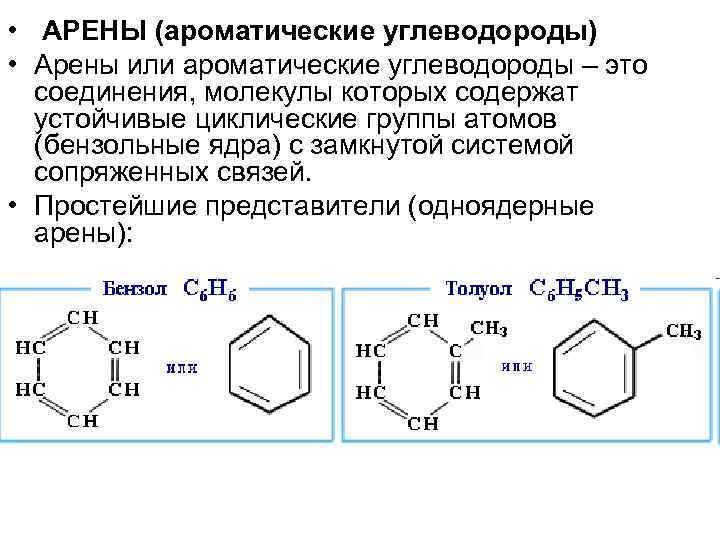 • АРЕНЫ (ароматические углеводороды) • Арены или ароматические углеводороды – это соединения, молекулы которых содержат устойчивые циклические группы атомов (бензольные ядра) с замкнутой системой сопряженных связей. • Простейшие представители (одноядерные арены):
• АРЕНЫ (ароматические углеводороды) • Арены или ароматические углеводороды – это соединения, молекулы которых содержат устойчивые циклические группы атомов (бензольные ядра) с замкнутой системой сопряженных связей. • Простейшие представители (одноядерные арены):
 • Строение бензола • Бензол С 6 Н 6 – родоначальник ароматических углеводородов. • Каждый из шести атомов углерода в его молекуле находится в состоянии sp 2 -гибридизации (и связан с двумя соседними атомами углерода и атомом водорода тремя σ-связями. • Валентные углы между каждой парой π-связей равны 120°. • Скелет σ-связей представляет собой правильный шестиугольник, в котором все атомы углерода и все σ-связи С–С и С–Н лежат в одной плоскости:
• Строение бензола • Бензол С 6 Н 6 – родоначальник ароматических углеводородов. • Каждый из шести атомов углерода в его молекуле находится в состоянии sp 2 -гибридизации (и связан с двумя соседними атомами углерода и атомом водорода тремя σ-связями. • Валентные углы между каждой парой π-связей равны 120°. • Скелет σ-связей представляет собой правильный шестиугольник, в котором все атомы углерода и все σ-связи С–С и С–Н лежат в одной плоскости:
 • р-Электроны всех атомов углерода взаимодействуют между собой путем бокового перекрывания соседних 2 р-АО, расположенных перпендикулярно плоскости σскелета бензольного кольца. • Они образуют единое циклическое π-электронное облако, сосредоточенное над и под плоскостью кольца.
• р-Электроны всех атомов углерода взаимодействуют между собой путем бокового перекрывания соседних 2 р-АО, расположенных перпендикулярно плоскости σскелета бензольного кольца. • Они образуют единое циклическое π-электронное облако, сосредоточенное над и под плоскостью кольца.
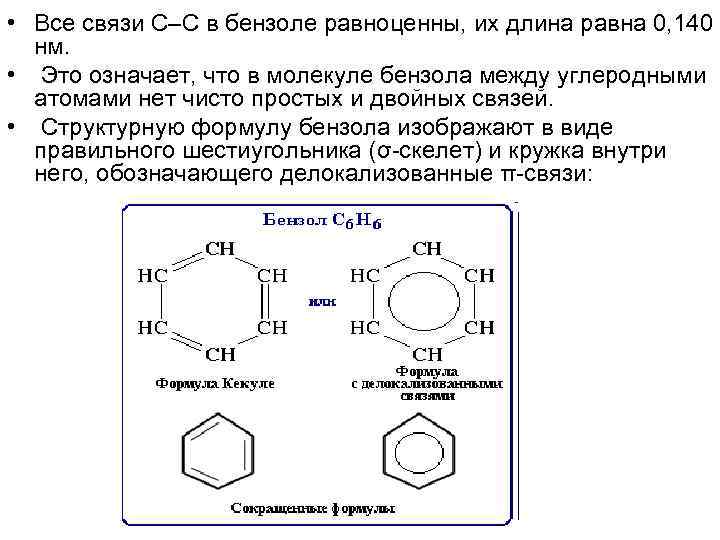 • Все связи С–С в бензоле равноценны, их длина равна 0, 140 нм. • Это означает, что в молекуле бензола между углеродными атомами нет чисто простых и двойных связей. • Структурную формулу бензола изображают в виде правильного шестиугольника (σ-скелет) и кружка внутри него, обозначающего делокализованные π-связи:
• Все связи С–С в бензоле равноценны, их длина равна 0, 140 нм. • Это означает, что в молекуле бензола между углеродными атомами нет чисто простых и двойных связей. • Структурную формулу бензола изображают в виде правильного шестиугольника (σ-скелет) и кружка внутри него, обозначающего делокализованные π-связи:
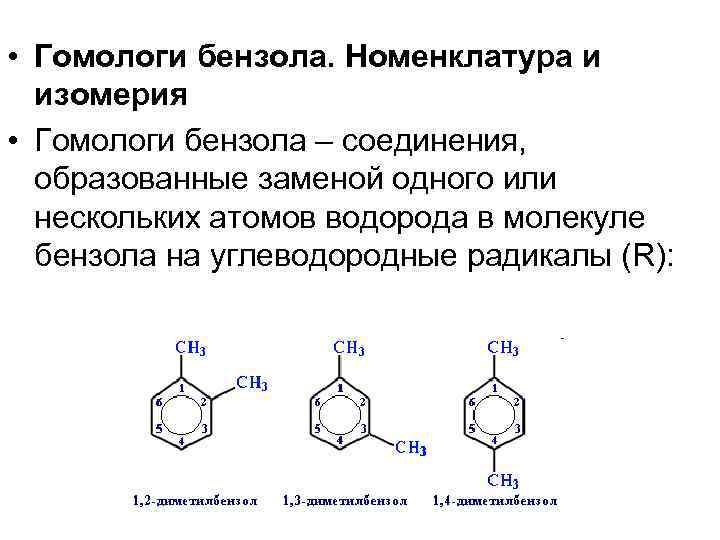 • Гомологи бензола. Номенклатура и изомерия • Гомологи бензола – соединения, образованные заменой одного или нескольких атомов водорода в молекуле бензола на углеводородные радикалы (R):
• Гомологи бензола. Номенклатура и изомерия • Гомологи бензола – соединения, образованные заменой одного или нескольких атомов водорода в молекуле бензола на углеводородные радикалы (R):
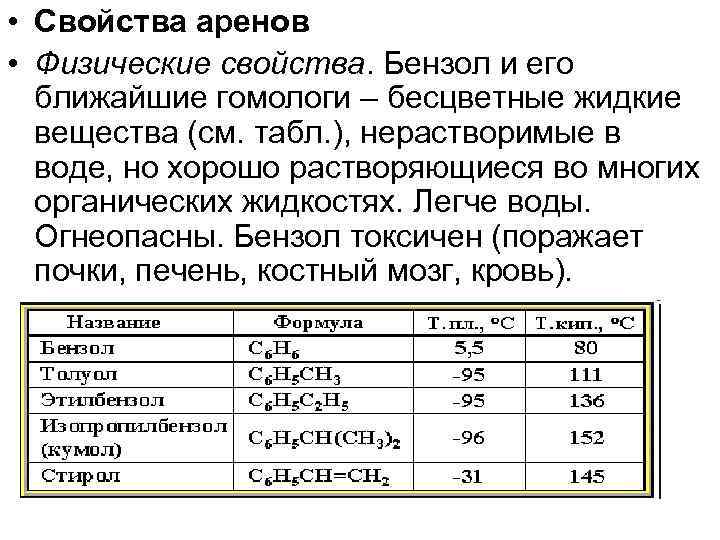 • Свойства аренов • Физические свойства. Бензол и его ближайшие гомологи – бесцветные жидкие вещества (см. табл. ), нерастворимые в воде, но хорошо растворяющиеся во многих органических жидкостях. Легче воды. Огнеопасны. Бензол токсичен (поражает почки, печень, костный мозг, кровь).
• Свойства аренов • Физические свойства. Бензол и его ближайшие гомологи – бесцветные жидкие вещества (см. табл. ), нерастворимые в воде, но хорошо растворяющиеся во многих органических жидкостях. Легче воды. Огнеопасны. Бензол токсичен (поражает почки, печень, костный мозг, кровь).
 • По химическим свойствам арены отличаются от предельных и непредельных углеводородов. Это объясняется особенностями строения бензольного кольца. Делокализация шести π-электронов в циклической системе понижает энергию молекулы, что обусловливает повышенную устойчивость (ароматичность) бензола и его гомологов. • Поэтому арены не склонны вступать в реакции присоединения или окисления, которые ведут к нарушению ароматичности.
• По химическим свойствам арены отличаются от предельных и непредельных углеводородов. Это объясняется особенностями строения бензольного кольца. Делокализация шести π-электронов в циклической системе понижает энергию молекулы, что обусловливает повышенную устойчивость (ароматичность) бензола и его гомологов. • Поэтому арены не склонны вступать в реакции присоединения или окисления, которые ведут к нарушению ароматичности.
 • Наличие областей повышенной pэлектронной плотности с двух сторон плоского ароматического цикла ведет к тому, что бензольное кольцо является нуклеофилом и в связи с этим склонно подвергаться атаке электрофильным реагентом. • Таким образом, для ароматических соединений наиболее типичны реакции электрофильного замещения.
• Наличие областей повышенной pэлектронной плотности с двух сторон плоского ароматического цикла ведет к тому, что бензольное кольцо является нуклеофилом и в связи с этим склонно подвергаться атаке электрофильным реагентом. • Таким образом, для ароматических соединений наиболее типичны реакции электрофильного замещения.
 • . Реакции замещения в бензольном кольце • Механизм реакций – электрофильное замещение. • 1. Галогенирование • Замещение атома водорода в бензольном кольце на галоген происходитв присутствии катализаторов Al. Cl 3, Al. Br 3, Fe. Cl 3 и т. п. (кислот Льюиса): •
• . Реакции замещения в бензольном кольце • Механизм реакций – электрофильное замещение. • 1. Галогенирование • Замещение атома водорода в бензольном кольце на галоген происходитв присутствии катализаторов Al. Cl 3, Al. Br 3, Fe. Cl 3 и т. п. (кислот Льюиса): •
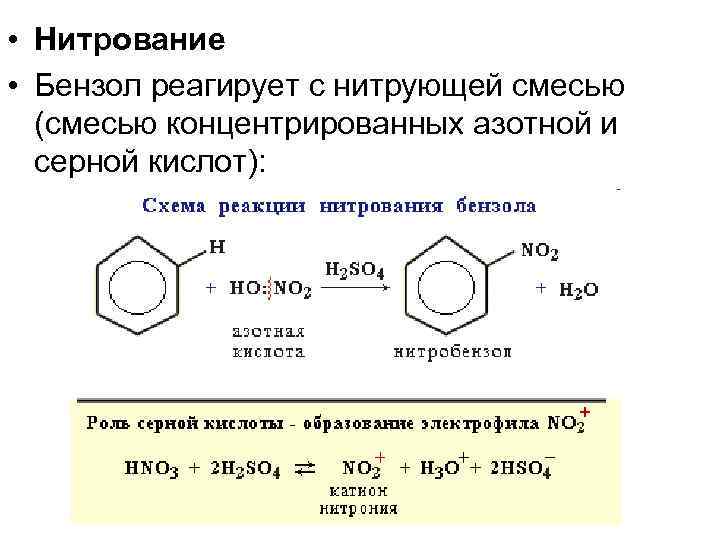 • Нитрование • Бензол реагирует с нитрующей смесью (смесью концентрированных азотной и серной кислот):
• Нитрование • Бензол реагирует с нитрующей смесью (смесью концентрированных азотной и серной кислот):
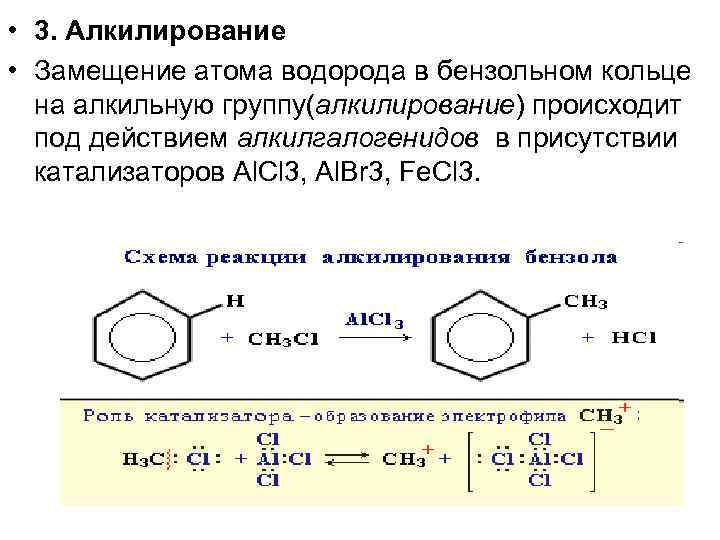 • 3. Алкилирование • Замещение атома водорода в бензольном кольце на алкильную группу(алкилирование) происходит под действием алкилгалогенидов в присутствии катализаторов Al. Cl 3, Al. Br 3, Fe. Cl 3.
• 3. Алкилирование • Замещение атома водорода в бензольном кольце на алкильную группу(алкилирование) происходит под действием алкилгалогенидов в присутствии катализаторов Al. Cl 3, Al. Br 3, Fe. Cl 3.

 • . Реакции окисления аренов • Бензол не окисляется даже под действием сильных окислителей (KMn. O 4). Поэтому он часто используется как инертный растворитель при проведении реакций окисления других органических соединений. • В отличие от бензола его гомологи окисляются довольно легко. • При действии раствора KMn. O 4 в кислой среде и нагревании в гомологах бензола окислению подвергаются только боковые цепи:
• . Реакции окисления аренов • Бензол не окисляется даже под действием сильных окислителей (KMn. O 4). Поэтому он часто используется как инертный растворитель при проведении реакций окисления других органических соединений. • В отличие от бензола его гомологи окисляются довольно легко. • При действии раствора KMn. O 4 в кислой среде и нагревании в гомологах бензола окислению подвергаются только боковые цепи:

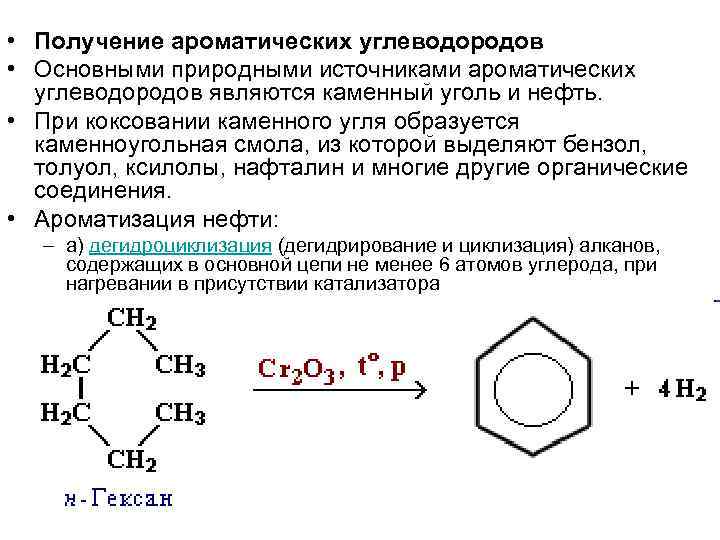 • Получение ароматических углеводородов • Основными природными источниками ароматических углеводородов являются каменный уголь и нефть. • При коксовании каменного угля образуется каменноугольная смола, из которой выделяют бензол, толуол, ксилолы, нафталин и многие другие органические соединения. • Ароматизация нефти: – а) дегидроциклизация (дегидрирование и циклизация) алканов, содержащих в основной цепи не менее 6 атомов углерода, при нагревании в присутствии катализатора
• Получение ароматических углеводородов • Основными природными источниками ароматических углеводородов являются каменный уголь и нефть. • При коксовании каменного угля образуется каменноугольная смола, из которой выделяют бензол, толуол, ксилолы, нафталин и многие другие органические соединения. • Ароматизация нефти: – а) дегидроциклизация (дегидрирование и циклизация) алканов, содержащих в основной цепи не менее 6 атомов углерода, при нагревании в присутствии катализатора
 • Применение ароматических углеводородов • Бензол С 6 Н 6 используется как исходный продукт для получения различных ароматических соединений – нитробензола, хлорбензола, анилина, фенола, стирола и т. д. , применяемых в производстве лекарств, пластмасс, красителей, ядохимикатов и многих других органических веществ.
• Применение ароматических углеводородов • Бензол С 6 Н 6 используется как исходный продукт для получения различных ароматических соединений – нитробензола, хлорбензола, анилина, фенола, стирола и т. д. , применяемых в производстве лекарств, пластмасс, красителей, ядохимикатов и многих других органических веществ.
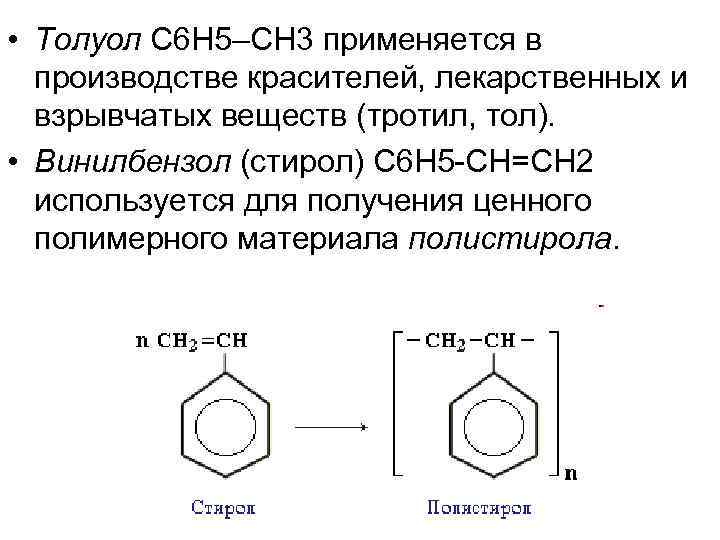 • Толуол С 6 Н 5–СН 3 применяется в производстве красителей, лекарственных и взрывчатых веществ (тротил, тол). • Винилбензол (стирол) C 6 H 5 -CН=СН 2 используется для получения ценного полимерного материала полистирола.
• Толуол С 6 Н 5–СН 3 применяется в производстве красителей, лекарственных и взрывчатых веществ (тротил, тол). • Винилбензол (стирол) C 6 H 5 -CН=СН 2 используется для получения ценного полимерного материала полистирола.


