Alkany2.pptx
- Количество слайдов: 21
 Алканы Выполнил студент группы ИВ-101: Иванов Максим 1
Алканы Выполнил студент группы ИВ-101: Иванов Максим 1
 Алканы Ациклические углеводороды линейного или разветвлённого строения, содержащие только простые связи и образующие гомологический ряд с общей формулой Cn. H 2 n+2. Начало 2
Алканы Ациклические углеводороды линейного или разветвлённого строения, содержащие только простые связи и образующие гомологический ряд с общей формулой Cn. H 2 n+2. Начало 2
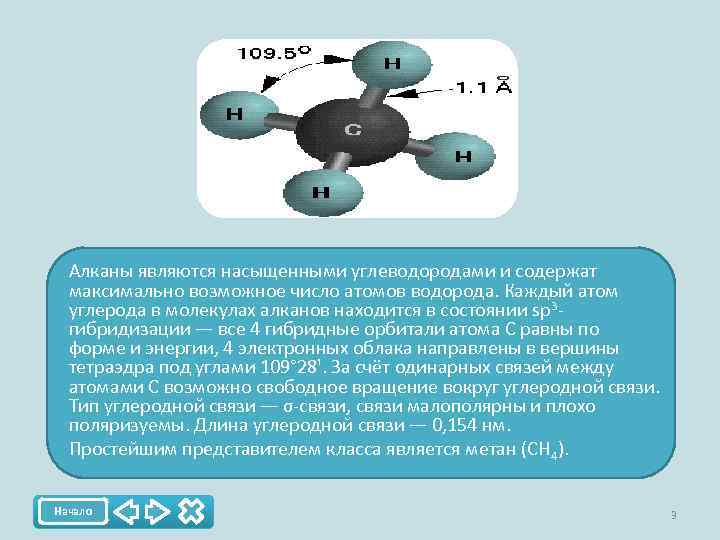 Алканы являются насыщенными углеводородами и содержат максимально возможное число атомов водорода. Каждый атом углерода в молекулах алканов находится в состоянии sp 3 гибридизации — все 4 гибридные орбитали атома С равны по форме и энергии, 4 электронных облака направлены в вершины тетраэдра под углами 109° 28'. За счёт одинарных связей между атомами С возможно свободное вращение вокруг углеродной связи. Тип углеродной связи — σ-связи, связи малополярны и плохо поляризуемы. Длина углеродной связи — 0, 154 нм. Простейшим представителем класса является метан (CH 4). Начало 3
Алканы являются насыщенными углеводородами и содержат максимально возможное число атомов водорода. Каждый атом углерода в молекулах алканов находится в состоянии sp 3 гибридизации — все 4 гибридные орбитали атома С равны по форме и энергии, 4 электронных облака направлены в вершины тетраэдра под углами 109° 28'. За счёт одинарных связей между атомами С возможно свободное вращение вокруг углеродной связи. Тип углеродной связи — σ-связи, связи малополярны и плохо поляризуемы. Длина углеродной связи — 0, 154 нм. Простейшим представителем класса является метан (CH 4). Начало 3
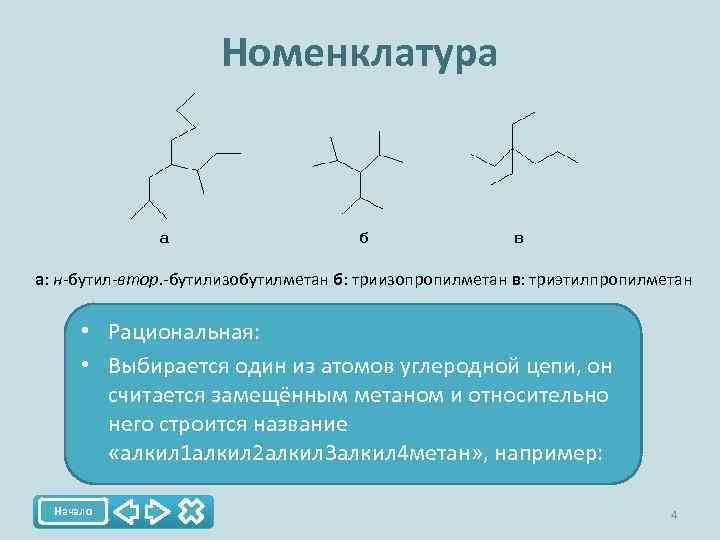 Номенклатура а: н-бутил-втор. -бутилизобутилметан б: триизопропилметан в: триэтилпропилметан • Рациональная: • Выбирается один из атомов углеродной цепи, он считается замещённым метаном и относительно него строится название «алкил 1 алкил 2 алкил 3 алкил 4 метан» , например: Начало 4
Номенклатура а: н-бутил-втор. -бутилизобутилметан б: триизопропилметан в: триэтилпропилметан • Рациональная: • Выбирается один из атомов углеродной цепи, он считается замещённым метаном и относительно него строится название «алкил 1 алкил 2 алкил 3 алкил 4 метан» , например: Начало 4
 Систематическая ИЮПАК: 2, 6, 6 -триметил-3 -этилгептан (слева направо) / 2, 2, 6 -триметил-5 -этилгептан (справа налево) • • • По номенклатуре ИЮПАК названия алканов образуются при помощи суффикса -ан путём добавления к соответствующему корню от названия углеводорода. Выбирается наиболее длинная неразветвлённая углеводородная цепь так, чтобы у наибольшего числа заместителей был минимальный номер в цепи. В названии соединения цифрой указывают номер углеродного атома, при котором находится замещающий радикал, затем название радикала и название главной цепи. Если радикалы повторяются, то перечисляют цифры, указывающие их положение, а число одинаковых радикалов указывают приставками ди-, три-, тетра-. Если радикалы неодинаковые, то их названия перечисляются в алфавитном порядке. Например: Начало 5
Систематическая ИЮПАК: 2, 6, 6 -триметил-3 -этилгептан (слева направо) / 2, 2, 6 -триметил-5 -этилгептан (справа налево) • • • По номенклатуре ИЮПАК названия алканов образуются при помощи суффикса -ан путём добавления к соответствующему корню от названия углеводорода. Выбирается наиболее длинная неразветвлённая углеводородная цепь так, чтобы у наибольшего числа заместителей был минимальный номер в цепи. В названии соединения цифрой указывают номер углеродного атома, при котором находится замещающий радикал, затем название радикала и название главной цепи. Если радикалы повторяются, то перечисляют цифры, указывающие их положение, а число одинаковых радикалов указывают приставками ди-, три-, тетра-. Если радикалы неодинаковые, то их названия перечисляются в алфавитном порядке. Например: Начало 5
 Спектральные свойства • • • ИК-спектроскопия В ИК-спектрах алканов четко проявляются частоты валентных колебаний связи С-Н в области 2850— 3000 см− 1. Частоты валентных колебаний связи С-С переменны и часто малоинтенсивны. Характеристические деформационные колебания в связи С-Н в метильной и метиленовой группах обычно лежат в интервале 1400— 1470 см− 1, однако метильная группа дает в спектрах слабую полосу при 1380 см− 1. УФ-спектроскопия Чистые алканы не поглощают в ультрафиолетовой области выше 2000 Å и по этой причине часто оказываются отличными растворителями для снятия УФ-спектров других соединений. ЯМР-спектроскопия Масс-спектрометрия Начало 6
Спектральные свойства • • • ИК-спектроскопия В ИК-спектрах алканов четко проявляются частоты валентных колебаний связи С-Н в области 2850— 3000 см− 1. Частоты валентных колебаний связи С-С переменны и часто малоинтенсивны. Характеристические деформационные колебания в связи С-Н в метильной и метиленовой группах обычно лежат в интервале 1400— 1470 см− 1, однако метильная группа дает в спектрах слабую полосу при 1380 см− 1. УФ-спектроскопия Чистые алканы не поглощают в ультрафиолетовой области выше 2000 Å и по этой причине часто оказываются отличными растворителями для снятия УФ-спектров других соединений. ЯМР-спектроскопия Масс-спектрометрия Начало 6
 Химические свойства Алканы имеют низкую химическую активность. Это объясняется тем, что единичные C-H и C-C связи относительно прочны и их сложно разрушить. Поскольку углеродные связи неполярны, а связи С — Н малополярны, оба вида связей малополяризуемы и относятся к σ виду, их разрыв наиболее вероятен по гомолитическому механизму то есть с образованием радикалов. Начало 7
Химические свойства Алканы имеют низкую химическую активность. Это объясняется тем, что единичные C-H и C-C связи относительно прочны и их сложно разрушить. Поскольку углеродные связи неполярны, а связи С — Н малополярны, оба вида связей малополяризуемы и относятся к σ виду, их разрыв наиболее вероятен по гомолитическому механизму то есть с образованием радикалов. Начало 7
 Реакции радикального замещения • • • Галогенирование алканов протекает по радикальному механизму. Галогенирование — это одна из реакций замещения. В первую очередь галогенируется наименее гидрированый атом углерода (третичный атом, затем вторичный, первичные атому галогенируются в последнюю очередь). Галогенирование алканов проходит поэтапно — за один этап замещается не более одного атома водорода: • • 1. CH 4 + Cl 2 → CH 3 Cl + HCl (хлорметан) 2. CH 3 Cl + Cl 2 → CH 2 Cl 2 + HCl (дихлорметан) 3. CH 2 Cl 2 + Cl 2 → CHCl 3 + HCl (трихлорметан) 4. CHCl 3 + Cl 2 → CCl 4 + HCl (тетрахлорметан). Начало 8
Реакции радикального замещения • • • Галогенирование алканов протекает по радикальному механизму. Галогенирование — это одна из реакций замещения. В первую очередь галогенируется наименее гидрированый атом углерода (третичный атом, затем вторичный, первичные атому галогенируются в последнюю очередь). Галогенирование алканов проходит поэтапно — за один этап замещается не более одного атома водорода: • • 1. CH 4 + Cl 2 → CH 3 Cl + HCl (хлорметан) 2. CH 3 Cl + Cl 2 → CH 2 Cl 2 + HCl (дихлорметан) 3. CH 2 Cl 2 + Cl 2 → CHCl 3 + HCl (трихлорметан) 4. CHCl 3 + Cl 2 → CCl 4 + HCl (тетрахлорметан). Начало 8
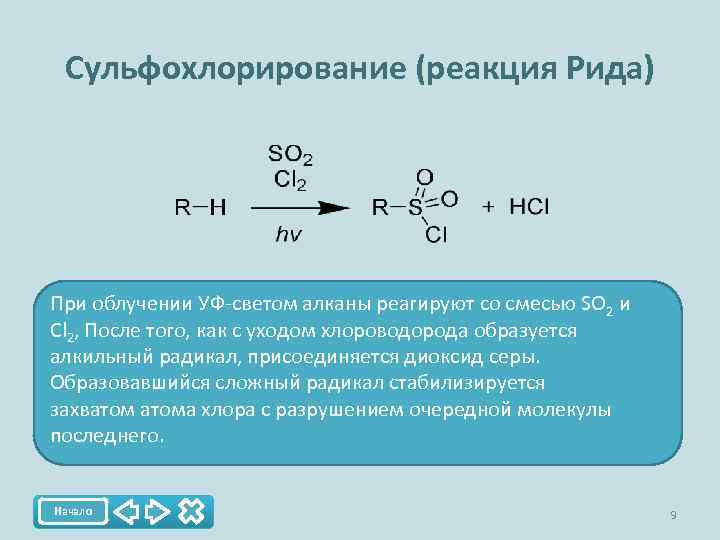 Сульфохлорирование (реакция Рида) При облучении УФ-светом алканы реагируют со смесью SO 2 и Cl 2, После того, как с уходом хлороводорода образуется алкильный радикал, присоединяется диоксид серы. Образовавшийся сложный радикал стабилизируется захватома хлора с разрушением очередной молекулы последнего. Начало 9
Сульфохлорирование (реакция Рида) При облучении УФ-светом алканы реагируют со смесью SO 2 и Cl 2, После того, как с уходом хлороводорода образуется алкильный радикал, присоединяется диоксид серы. Образовавшийся сложный радикал стабилизируется захватома хлора с разрушением очередной молекулы последнего. Начало 9
 Реакция Вюрца • • • Реакция Вюрца, или синтез Вюрца — метод синтеза симметричных насыщенных углеводородов действием металлического натрия на алкилгалогениды (обычно бромиды или хлориды): 2 RBr + 2 Na → R—R + 2 Na. Br Реакция Вюрца открыта Ш. А. Вюрцем в 1855 году[1]. P. Фиттиг распространил реакцию Вюрца на область ароматических углеводородов[2] (реакция Вюрца — Фиттига): C 6 H 5 Br + 2 Na + Вr. C 4 H 9 -> С 6 Н 5 — С 4 Н 9+ 2 Na. Вr Долгое время считалось, что реакция Вюрца проходит в две стадии. Первая — обмен галогена на металл, вторая — алкилирование образованного карбаниона. Современная физическая органическая химия утверждает гомолитический механизм, хотя окончательно этот механизм не доказан. При проведении реакции Вюрца очень распространены побочные реакции (элиминирование и перегруппировки), что сильно ограничивает ее использование в качестве препаративного метода. Кроме того, классическая реакция Вюрца практически не используется для кросс-сочетания разноименных алкилгалогенидов. Начало 10
Реакция Вюрца • • • Реакция Вюрца, или синтез Вюрца — метод синтеза симметричных насыщенных углеводородов действием металлического натрия на алкилгалогениды (обычно бромиды или хлориды): 2 RBr + 2 Na → R—R + 2 Na. Br Реакция Вюрца открыта Ш. А. Вюрцем в 1855 году[1]. P. Фиттиг распространил реакцию Вюрца на область ароматических углеводородов[2] (реакция Вюрца — Фиттига): C 6 H 5 Br + 2 Na + Вr. C 4 H 9 -> С 6 Н 5 — С 4 Н 9+ 2 Na. Вr Долгое время считалось, что реакция Вюрца проходит в две стадии. Первая — обмен галогена на металл, вторая — алкилирование образованного карбаниона. Современная физическая органическая химия утверждает гомолитический механизм, хотя окончательно этот механизм не доказан. При проведении реакции Вюрца очень распространены побочные реакции (элиминирование и перегруппировки), что сильно ограничивает ее использование в качестве препаративного метода. Кроме того, классическая реакция Вюрца практически не используется для кросс-сочетания разноименных алкилгалогенидов. Начало 10
 • Современный подход к реакции Вюрца • Для преодоления множества побочных процессов было предложено использовать более селективные и современные методы. Основные разработки ведутся по применению не -натриевых металлов. Для проведения реакции Вюрца используют серебро[3], цинк, железо[4] и пирофорный свинец[5]. Последний реагент позволяет проводить реакцию в присутствии карбоксильной группы. Начало 11
• Современный подход к реакции Вюрца • Для преодоления множества побочных процессов было предложено использовать более селективные и современные методы. Основные разработки ведутся по применению не -натриевых металлов. Для проведения реакции Вюрца используют серебро[3], цинк, железо[4] и пирофорный свинец[5]. Последний реагент позволяет проводить реакцию в присутствии карбоксильной группы. Начало 11
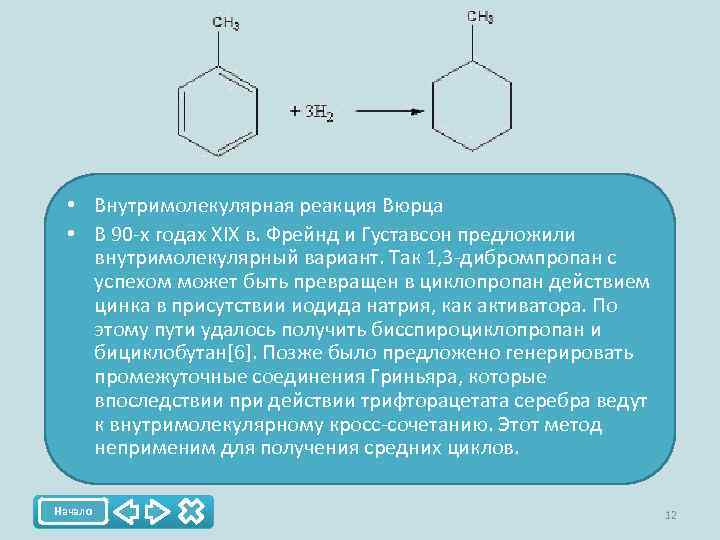 • Внутримолекулярная реакция Вюрца • В 90 -х годах XIX в. Фрейнд и Густавсон предложили внутримолекулярный вариант. Так 1, 3 -дибромпропан с успехом может быть превращен в циклопропан действием цинка в присутствии иодида натрия, как активатора. По этому пути удалось получить бисспироциклопропан и бициклобутан[6]. Позже было предложено генерировать промежуточные соединения Гриньяра, которые впоследствии при действии трифторацетата серебра ведут к внутримолекулярному кросс-сочетанию. Этот метод неприменим для получения средних циклов. Начало 12
• Внутримолекулярная реакция Вюрца • В 90 -х годах XIX в. Фрейнд и Густавсон предложили внутримолекулярный вариант. Так 1, 3 -дибромпропан с успехом может быть превращен в циклопропан действием цинка в присутствии иодида натрия, как активатора. По этому пути удалось получить бисспироциклопропан и бициклобутан[6]. Позже было предложено генерировать промежуточные соединения Гриньяра, которые впоследствии при действии трифторацетата серебра ведут к внутримолекулярному кросс-сочетанию. Этот метод неприменим для получения средних циклов. Начало 12
 Реакции горения • • Начало Реакции окисления Горение Основным химическим свойством предельных углеводородов, определяющих их использование в качестве топлива, является реакция горения. Пример: CH 4 + 2 O 2 → CO 2 + 2 H 2 O + Q Значение Q достигает 46 000 — 50 000 к. Дж/кг. В случае нехватки кислорода вместо углекислого газа получается угарный газ или уголь (в зависимости от концентрации кислорода). В общем виде реакцию горения алканов можно записать следующим образом: Сn. Н 2 n+2 +(1, 5 n+0, 5)O 2 → n. CO 2 + (n+1)H 2 O 13
Реакции горения • • Начало Реакции окисления Горение Основным химическим свойством предельных углеводородов, определяющих их использование в качестве топлива, является реакция горения. Пример: CH 4 + 2 O 2 → CO 2 + 2 H 2 O + Q Значение Q достигает 46 000 — 50 000 к. Дж/кг. В случае нехватки кислорода вместо углекислого газа получается угарный газ или уголь (в зависимости от концентрации кислорода). В общем виде реакцию горения алканов можно записать следующим образом: Сn. Н 2 n+2 +(1, 5 n+0, 5)O 2 → n. CO 2 + (n+1)H 2 O 13
 Каталитическое окисление • Могут образовываться спирты, альдегиды, карбоновые кислоты. • При мягком окислении СН 4 в присутствии катализатора кислородом при 200 °C) могут образоваться: • метиловый спирт: • СН 4 + О 2 → СН 3 ОН • формальдегид: • СН 4 + О 2 → СН 2 О + Н 2 O • муравьиная кислота: • 2 СН 4 + 3 О 2 → 2 НСООН + 2 Н 2 O Начало 14
Каталитическое окисление • Могут образовываться спирты, альдегиды, карбоновые кислоты. • При мягком окислении СН 4 в присутствии катализатора кислородом при 200 °C) могут образоваться: • метиловый спирт: • СН 4 + О 2 → СН 3 ОН • формальдегид: • СН 4 + О 2 → СН 2 О + Н 2 O • муравьиная кислота: • 2 СН 4 + 3 О 2 → 2 НСООН + 2 Н 2 O Начало 14
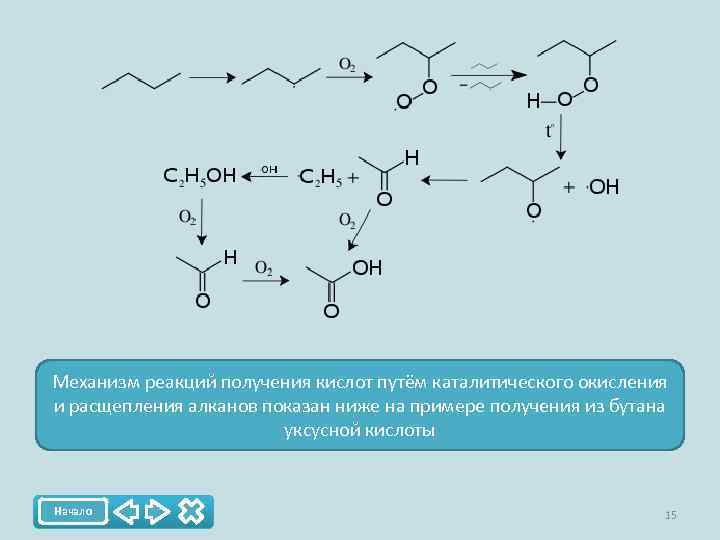 Механизм реакций получения кислот путём каталитического окисления и расщепления алканов показан ниже на примере получения из бутана уксусной кислоты Начало 15
Механизм реакций получения кислот путём каталитического окисления и расщепления алканов показан ниже на примере получения из бутана уксусной кислоты Начало 15
 Дегидрирование • Образование: 1)В углеродном скелете 2 (этан) или 3 (пропан) атома углерода — получение (терминальных) алкенов, так как других в данном случае не может получиться; выделение водорода: Условия протекания: 400— 600 °C, катализаторы — Pt, Ni, Al 2 O 3, Cr 2 O 3 • а) • б) 3 2 (пропан → пропен) • • Начало CH 3 -CH 3 → CH 2=CH 2 + H 2 (этан → этен) CH -CH 3 → CH 2=CH-CH 3 + H 2 16
Дегидрирование • Образование: 1)В углеродном скелете 2 (этан) или 3 (пропан) атома углерода — получение (терминальных) алкенов, так как других в данном случае не может получиться; выделение водорода: Условия протекания: 400— 600 °C, катализаторы — Pt, Ni, Al 2 O 3, Cr 2 O 3 • а) • б) 3 2 (пропан → пропен) • • Начало CH 3 -CH 3 → CH 2=CH 2 + H 2 (этан → этен) CH -CH 3 → CH 2=CH-CH 3 + H 2 16
 • 2)В углеродном скелете 4 (бутан, изобутан) или 5 (пентан, 2 -метилбутан, неопентан) атомов углерода — получение алкадиенов; выделение водорода: • в)CH 3 -CH 2 -CH 3 → CH 2=CH-CH=CH 2 + 2 H 2 (бутан → бутадиен-1, 3) • в')CH 3 -CH 2 -CH 3 → CH 2=C=CH-CH 3 + 2 H 2 (бутан → бутадиен-1, 2) (ЭТО — ОДНА РЕАКЦИЯ!) Начало 17
• 2)В углеродном скелете 4 (бутан, изобутан) или 5 (пентан, 2 -метилбутан, неопентан) атомов углерода — получение алкадиенов; выделение водорода: • в)CH 3 -CH 2 -CH 3 → CH 2=CH-CH=CH 2 + 2 H 2 (бутан → бутадиен-1, 3) • в')CH 3 -CH 2 -CH 3 → CH 2=C=CH-CH 3 + 2 H 2 (бутан → бутадиен-1, 2) (ЭТО — ОДНА РЕАКЦИЯ!) Начало 17
 • 3) В углеродном скелете 6 (гексан) и более атомов углерода — получение бензола и его производных: CH -CH -CH -CH • г) 3 2 2 2 3 (октан) → П. ксилол, параллельно М. -ксилол, параллельно этилбензол + 3 H 2 Начало 18
• 3) В углеродном скелете 6 (гексан) и более атомов углерода — получение бензола и его производных: CH -CH -CH -CH • г) 3 2 2 2 3 (октан) → П. ксилол, параллельно М. -ксилол, параллельно этилбензол + 3 H 2 Начало 18
 Применение алканов • • Начало Предельные углеводороды находят широкое применение в самых разнообразных сферах жизни и деятельности человека. Газообразные алканы (метан и пpопан-бутановая смесь) используются в качестве ценного топлива. Жидкие углеводоpоды составляют значительную долю в моторных и ракетных топливах и используются в качестве растворителей. Вазелиновое масло (смесь жидких углеводоpодов с числом атомов углерода до 15) - пpозpачная жидкость без запаха и вкуса, используется в медицине, паpфюмеpии и косметике. 19
Применение алканов • • Начало Предельные углеводороды находят широкое применение в самых разнообразных сферах жизни и деятельности человека. Газообразные алканы (метан и пpопан-бутановая смесь) используются в качестве ценного топлива. Жидкие углеводоpоды составляют значительную долю в моторных и ракетных топливах и используются в качестве растворителей. Вазелиновое масло (смесь жидких углеводоpодов с числом атомов углерода до 15) - пpозpачная жидкость без запаха и вкуса, используется в медицине, паpфюмеpии и косметике. 19
 • • • Вазелин (смесь жидких и твеpдых пpедельных углеводоpодов с числом углеpодных атомов до 25) пpименяется для пpиготовления мазей, используемых в медицине. Паpафин (смесь твеpдых алканов С 19 -С 35) - белая твеpдая масса без запаха и вкуса (т. пл. 50 -70 °C) - пpименяется для изготовления свечей, пpопитки спичек и упаковочной бумаги, для тепловых пpоцедуp в медицине. Служит сырьём при получении органических кислот и спиртов, моющих средств и поверхностно-активных веществ. Нормальные предельные углеводороды средней молекулярной массы используются как питательный субстрат в микробиологическом синтезе белка из нефти. Большое значение имеют галогенопроизводные алканов, которые используются как растворители, хладоагенты и сырье для дальнейших синтезов. В современной нефтехимической промышленности предельные улеводороды являются базой для получения разнообразных органических соединений, важным сырьем в процессах получения полупродуктов для производства пластмасс, каучуков, синтетических волокон, моющих средств и многих других веществ. Начало 20
• • • Вазелин (смесь жидких и твеpдых пpедельных углеводоpодов с числом углеpодных атомов до 25) пpименяется для пpиготовления мазей, используемых в медицине. Паpафин (смесь твеpдых алканов С 19 -С 35) - белая твеpдая масса без запаха и вкуса (т. пл. 50 -70 °C) - пpименяется для изготовления свечей, пpопитки спичек и упаковочной бумаги, для тепловых пpоцедуp в медицине. Служит сырьём при получении органических кислот и спиртов, моющих средств и поверхностно-активных веществ. Нормальные предельные углеводороды средней молекулярной массы используются как питательный субстрат в микробиологическом синтезе белка из нефти. Большое значение имеют галогенопроизводные алканов, которые используются как растворители, хладоагенты и сырье для дальнейших синтезов. В современной нефтехимической промышленности предельные улеводороды являются базой для получения разнообразных органических соединений, важным сырьем в процессах получения полупродуктов для производства пластмасс, каучуков, синтетических волокон, моющих средств и многих других веществ. Начало 20
 Биологическое действие При хроническом действии алканы нарушают работу нервной системы, что проявляется в виде бессонницы, брадикардии, повышенной утомляемости и функциональных неврозов. Начало 21
Биологическое действие При хроническом действии алканы нарушают работу нервной системы, что проявляется в виде бессонницы, брадикардии, повышенной утомляемости и функциональных неврозов. Начало 21


