АЛКАНЫ.ppt
- Количество слайдов: 10

Алканы Работа Кудряшовой Валерии и Пленкиной Аллы 11 А

Алканы. (Предельные углеводороды. Парафины. Насыщенные углеводороды. ) Алканы - углеводороды , в молекулах которых в атомы углерода связаны одинарными связям и имеют общую формулу : Cn. H 2 n+2
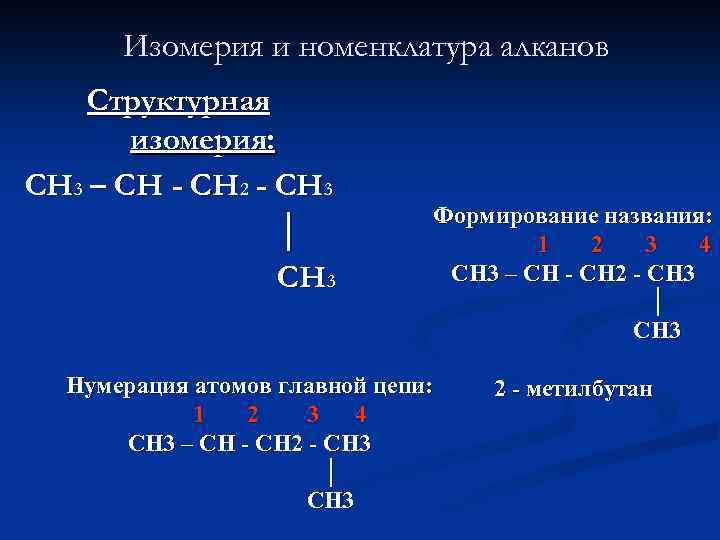
Изомерия и номенклатура алканов Структурная изомерия: CH 3 – CH - CH 2 - CH 3 │ CH 3 Формирование названия: 1 2 3 4 CH 3 – CH - CH 2 - CH 3 │ CH 3 Нумерация атомов главной цепи: 1 2 3 4 CH 3 – CH - CH 2 - CH 3 │ CH 3 2 - метилбутан

Простейшим представителем класса является Метан. Гомологический ряд метана: n СН 4 метан n С 2 H 6 n C 6 H 14 гексан этан n C 3 H 8 n C 7 H 16 гептан пропан n C 4 H 10 n C 8 H 18 октан бутан n C 5 H 12 n C 9 H 20 нонан пентан n C 10 H 22 декан
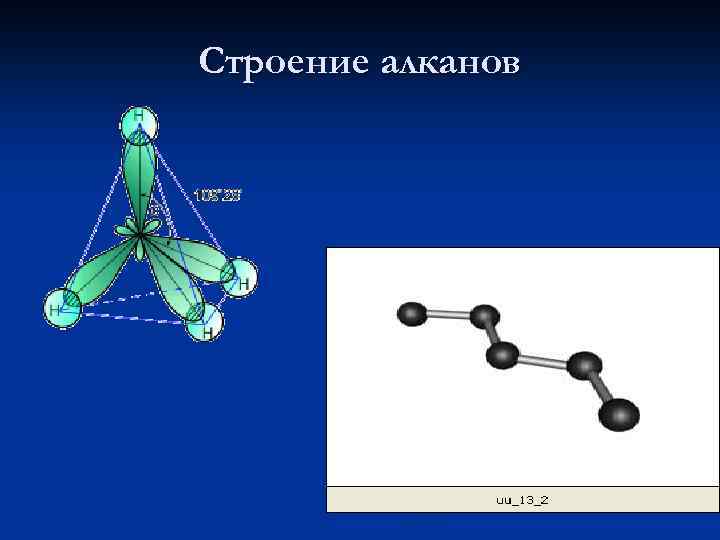
Строение алканов

Физические свойства алканов СН 4…C 4 Н 10 – газы T кипения: -161, 6…-0, 5 °C T плавления: -182, 5…-138, 3 °C С 5 Н 12…C 15 Н 32 С 16 Н 34…и далее– – жидкости твёрдые вещества T кипения: 36, 1… 270, 5 °C 287, 5 °C T плавления: -129, 8… 10 °C 20 °C С увеличением относительных молекулярных масс предельных углеводородов закономерно повышаю температуры кипения и плавления.
Химические свойства алканов
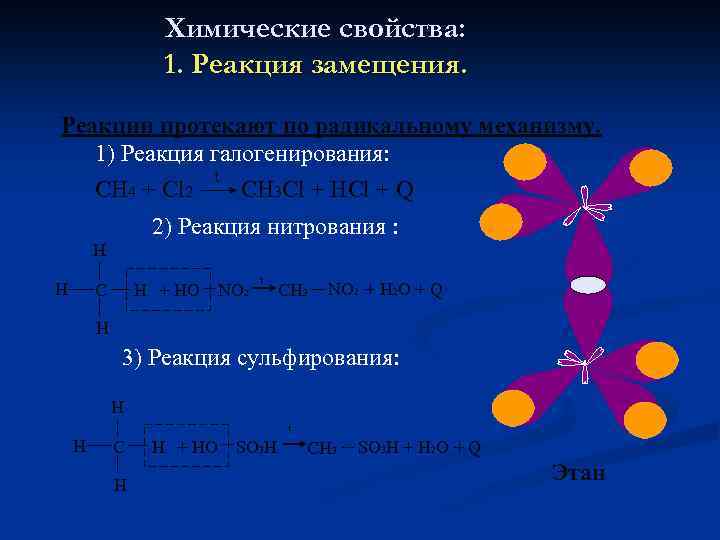
Химические свойства: 1. Реакция замещения. Реакции протекают по радикальному механизму. 1) Реакция галогенирования: t СН 4 + Сl 2 CH 3 Cl + HCl + Q 2) Реакция нитрования : Н Н С Н + НО NO 2 t СН 3 NO 2 + H 2 O + Q Н 3) Реакция сульфирования: Н t Н С Н Н + НО SO 3 H СН 3 SO 3 H + H 2 O + Q Этан

t, катализатор СН 3 СН 2 СН 3 СН СН 2 СН 3 800°С СН 4 + Н 2 О СО + 3 Н 2 синтез-газ 2 СН 4 СН 3 1500°С Н С≡С СН 3 Н + 3 Н 2 + Q Н 2 С=СН 2 + Q Предельные углеводороды горят (пламя не коптящее) С 3 Н 8 + 5 О 2 3 СО 2 + 4 Н 2 О + Q В присутствии катализаторов окисляются: СН 4 + О 2 500°С, катализатор Н С О + Н 2 О + Q Н 2 СН 3(СН 2)34 СН 3 + 5 О 2 4 СН 3 (СН 2)16 СООН +2 Н 2 О + Q

Применение: -Нефтехимическая промышленность -Медицина -Парфюмерия -Для сажи -Для топлива
АЛКАНЫ.ppt