3.Алканы.ppt
- Количество слайдов: 19
 Алканы Презентацию выполнила: Пелипенко Ирина Владимировна Учитель химии «Красноярской средней общеобразовательной школы с углубленным изучением предметов художественно-эстетического цикла» Кривошеинского района Томской области 2009
Алканы Презентацию выполнила: Пелипенко Ирина Владимировна Учитель химии «Красноярской средней общеобразовательной школы с углубленным изучением предметов художественно-эстетического цикла» Кривошеинского района Томской области 2009
 Содержание • Строение алканов • Изомерия и номенклатура алканов • Физические свойства • Нахождение в природе • Получение • Химические свойства • Применение алканов • Контрольные вопросы
Содержание • Строение алканов • Изомерия и номенклатура алканов • Физические свойства • Нахождение в природе • Получение • Химические свойства • Применение алканов • Контрольные вопросы
 Строение алканов Алканы – углеводороды, молекулы которых состоят из атомов углерода и водорода, связанных друг с другом одинарными связями. Основой молекулы является незамкнутая углеродная цепь. Общая формула – Cn H 2 n+2.
Строение алканов Алканы – углеводороды, молекулы которых состоят из атомов углерода и водорода, связанных друг с другом одинарными связями. Основой молекулы является незамкнутая углеродная цепь. Общая формула – Cn H 2 n+2.
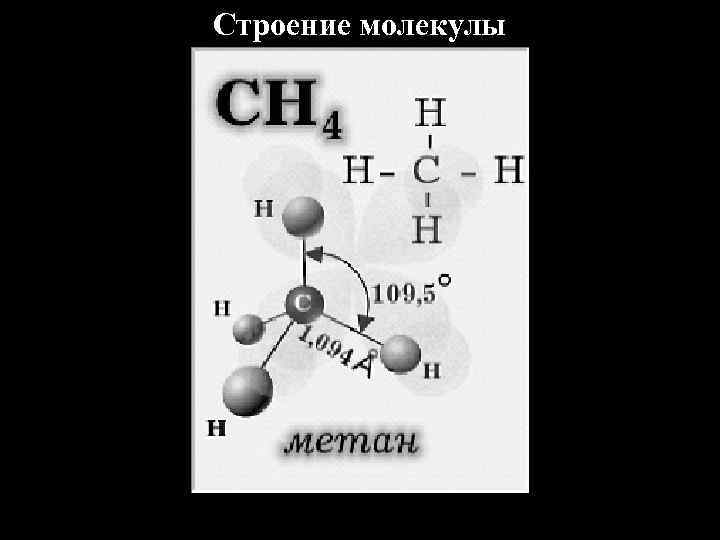 Строение молекулы
Строение молекулы
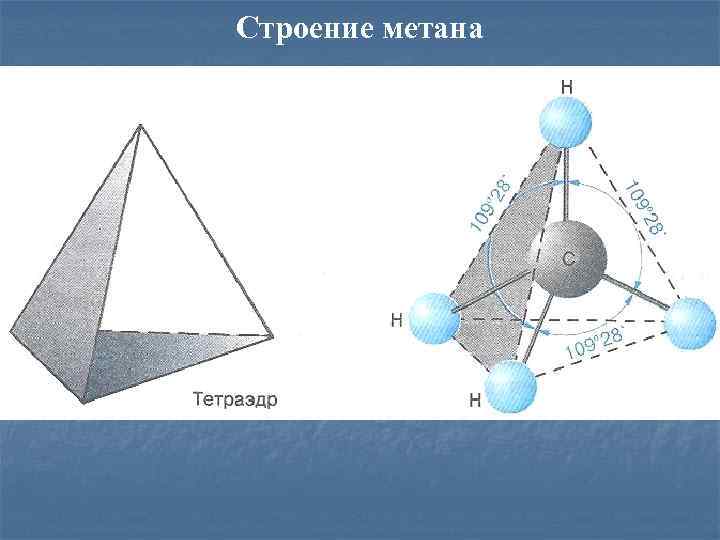 Строение метана
Строение метана
 Изомерия и номенклатура алканов Изомерия структурная (по углеродному скелету) H 3 C – CH 2 – CH 3 первичный вторичный H 3 C – CH 2 – CH 3 2 -метилбутан CH 3 третичный CH 3 H 3 C – CH 3 четвертичный CH 3 2, 2 -диметилпропан Номенклатура: 1. главная цепь 2. нумерация цепи 3. формирование названия
Изомерия и номенклатура алканов Изомерия структурная (по углеродному скелету) H 3 C – CH 2 – CH 3 первичный вторичный H 3 C – CH 2 – CH 3 2 -метилбутан CH 3 третичный CH 3 H 3 C – CH 3 четвертичный CH 3 2, 2 -диметилпропан Номенклатура: 1. главная цепь 2. нумерация цепи 3. формирование названия
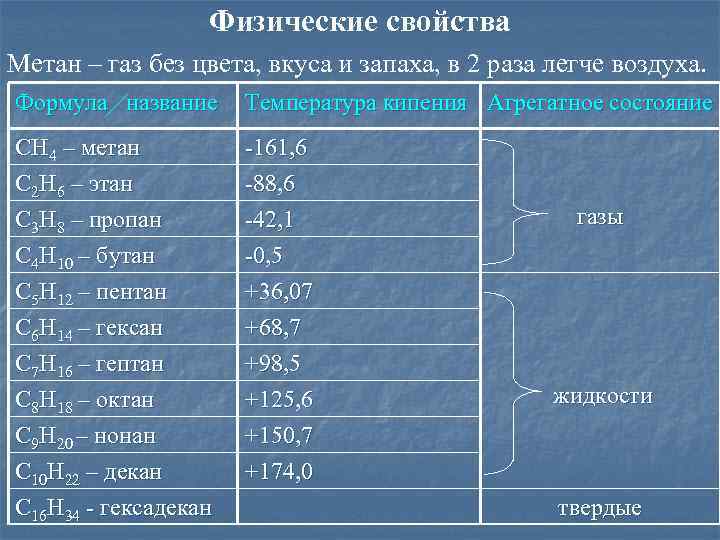 Физические свойства Метан – газ без цвета, вкуса и запаха, в 2 раза легче воздуха. Формула название Температура кипения Агрегатное состояние CH 4 – метан C 2 H 6 – этан C 3 H 8 – пропан -161, 6 -88, 6 -42, 1 C 4 H 10 – бутан C 5 H 12 – пентан C 6 H 14 – гексан C 7 H 16 – гептан C 8 H 18 – октан C 9 H 20 – нонан C 10 H 22 – декан C 16 H 34 - гексадекан -0, 5 +36, 07 +68, 7 +98, 5 +125, 6 +150, 7 +174, 0 газы жидкости твердые
Физические свойства Метан – газ без цвета, вкуса и запаха, в 2 раза легче воздуха. Формула название Температура кипения Агрегатное состояние CH 4 – метан C 2 H 6 – этан C 3 H 8 – пропан -161, 6 -88, 6 -42, 1 C 4 H 10 – бутан C 5 H 12 – пентан C 6 H 14 – гексан C 7 H 16 – гептан C 8 H 18 – октан C 9 H 20 – нонан C 10 H 22 – декан C 16 H 34 - гексадекан -0, 5 +36, 07 +68, 7 +98, 5 +125, 6 +150, 7 +174, 0 газы жидкости твердые

 Получение 1. Из природного сырья (нефть, газ) – перегонка 2. Крекинг нефтепродуктов C 16 H 34 C 8 H 18 + C 8 H 16 C 8 H 18 C 4 H 10 + C 4 H 8 C 4 H 10 C 2 H 6 + C 2 H 4 3. Гидрирование алкенов H 2 C = CH 2 + H 2 Pt CH 3 – CH 3 4. Гидролиз карбидов Al 4 C 3 + 12 H 2 O 3 CH 4 + 4 Al(OH)3 5. Синтез Вюрца 2 CH 3 – CH 2 Br + 2 Na C 4 H 10 + 2 Na. Br 6. Декарбоксилирование натриевых солей карбоновых кислот CH 3 COONa + Na. OH CH 4 + Na 2 CO 3
Получение 1. Из природного сырья (нефть, газ) – перегонка 2. Крекинг нефтепродуктов C 16 H 34 C 8 H 18 + C 8 H 16 C 8 H 18 C 4 H 10 + C 4 H 8 C 4 H 10 C 2 H 6 + C 2 H 4 3. Гидрирование алкенов H 2 C = CH 2 + H 2 Pt CH 3 – CH 3 4. Гидролиз карбидов Al 4 C 3 + 12 H 2 O 3 CH 4 + 4 Al(OH)3 5. Синтез Вюрца 2 CH 3 – CH 2 Br + 2 Na C 4 H 10 + 2 Na. Br 6. Декарбоксилирование натриевых солей карбоновых кислот CH 3 COONa + Na. OH CH 4 + Na 2 CO 3
 Химические свойства I. Радикальное замещение II. Разрушение цепи 1. Галогенирование 1. Изомеризация 2. Нитрование 1. 1. CH 4 + Cl 2 свет CH 3 Cl + HCl CH 3 Cl + Cl 2 свет CH 2 Cl 2 + HCl CH 2 Cl 2 + Cl 2 свет CHCl 3 + HCl CHCl 3 + Cl 2 свет CCl 4 + HCl 1. 2. CH 4 + HONO 2 t CH 3 NO 2 + H 2 O (р-я Коновалова) 0 2. 1. CH 3 – CH 2 –CH 3 Al. Cl 3, 400 CH 3 – CH 2 – CH 3
Химические свойства I. Радикальное замещение II. Разрушение цепи 1. Галогенирование 1. Изомеризация 2. Нитрование 1. 1. CH 4 + Cl 2 свет CH 3 Cl + HCl CH 3 Cl + Cl 2 свет CH 2 Cl 2 + HCl CH 2 Cl 2 + Cl 2 свет CHCl 3 + HCl CHCl 3 + Cl 2 свет CCl 4 + HCl 1. 2. CH 4 + HONO 2 t CH 3 NO 2 + H 2 O (р-я Коновалова) 0 2. 1. CH 3 – CH 2 –CH 3 Al. Cl 3, 400 CH 3 – CH 2 – CH 3
 Химические свойства III. Отщепление 1. Дегидрирование 2. Ароматизация 3. 1. CH 3 – CH 3 Pt, t 0 IV. Окисление 1. Крекинг 2. Пиролиз 3. Горение CH 2 = CH 2 + H 2 3. 2. CH 3 – CH 2 – CH 3 (ароматизация) 4. 1. C 4 H 10 4. 2. CH 4 C 2 H 6 + C 2 H 4 (крекинг) to, 1000 o C + 2 H 2 (пиролиз) CH 4 to, 1500 o CH 2 = CH 2+ 3 H 2 4. 3. CH 4 + 2 O 2 CO 2 + 2 H 2 O + 880 к. Дж кат + 4 H 2
Химические свойства III. Отщепление 1. Дегидрирование 2. Ароматизация 3. 1. CH 3 – CH 3 Pt, t 0 IV. Окисление 1. Крекинг 2. Пиролиз 3. Горение CH 2 = CH 2 + H 2 3. 2. CH 3 – CH 2 – CH 3 (ароматизация) 4. 1. C 4 H 10 4. 2. CH 4 C 2 H 6 + C 2 H 4 (крекинг) to, 1000 o C + 2 H 2 (пиролиз) CH 4 to, 1500 o CH 2 = CH 2+ 3 H 2 4. 3. CH 4 + 2 O 2 CO 2 + 2 H 2 O + 880 к. Дж кат + 4 H 2
 Нахождение в природе Метан – образуется в природе в результате разложения остатков растений и животных без воздуха. Метан содержится в природном газе, в газах, выделяющихся при добыче нефти. В состав природного и нефтяных газов входят этан, пропан, бутан и другие. Газообразные, жидкие и твердые придельные углеводороды содержатся в нефти.
Нахождение в природе Метан – образуется в природе в результате разложения остатков растений и животных без воздуха. Метан содержится в природном газе, в газах, выделяющихся при добыче нефти. В состав природного и нефтяных газов входят этан, пропан, бутан и другие. Газообразные, жидкие и твердые придельные углеводороды содержатся в нефти.
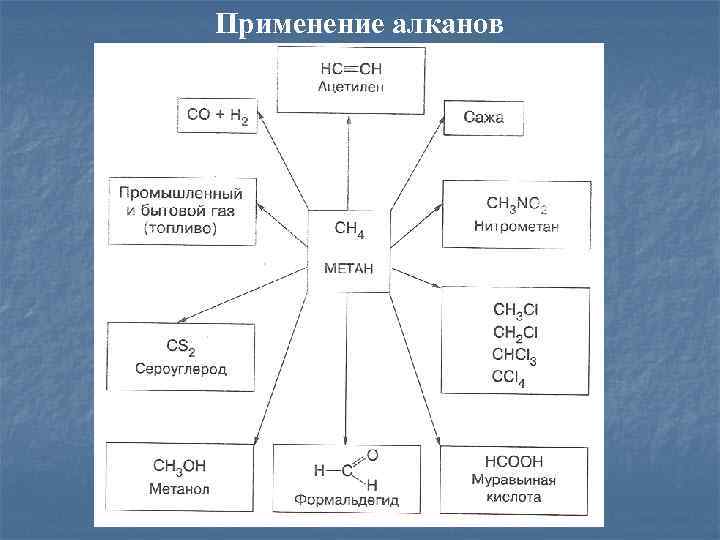 Применение алканов
Применение алканов
 Контрольные вопросы 1. Сколько углеводородов изображено формулами? CH 3 – CH 2 – CH 3 – CH 2 CH 3 CH 2 – CH 3 а) Один б) Два в) Три г) Четыре 2. Найдите формулу гомолога н-бутана: а) CH 3 – CH 3 б) CH 3 – CH 2 CH 3 в) CH 2 – CH 2 CH 3 г) СH 3 – CH 2 – CH 3
Контрольные вопросы 1. Сколько углеводородов изображено формулами? CH 3 – CH 2 – CH 3 – CH 2 CH 3 CH 2 – CH 3 а) Один б) Два в) Три г) Четыре 2. Найдите формулу гомолога н-бутана: а) CH 3 – CH 3 б) CH 3 – CH 2 CH 3 в) CH 2 – CH 2 CH 3 г) СH 3 – CH 2 – CH 3
 3. Вставьте в текст пропущенные термины и символы. Алканами называются углеводороды, в молекулах которых все атомы связаны…связями. Их общая формула…. Все атомы углерода в алканах находятся в состоянии… – гибридизации. Оси гибридных орбиталей направлены по вершинам правильного…, угол между ними составляет…. Относительно одинарных С – С связей…свободное вращение. 4. Исключите лишнее вещество: а) C 3 H 8, б) C 6 H 12, в) C 4 H 10, г) CH 4. Для алканов характерна изомерия: а) углеводородного скелета, б) положение кратной связи, в) положение функциональной группы, г) геометрическая.
3. Вставьте в текст пропущенные термины и символы. Алканами называются углеводороды, в молекулах которых все атомы связаны…связями. Их общая формула…. Все атомы углерода в алканах находятся в состоянии… – гибридизации. Оси гибридных орбиталей направлены по вершинам правильного…, угол между ними составляет…. Относительно одинарных С – С связей…свободное вращение. 4. Исключите лишнее вещество: а) C 3 H 8, б) C 6 H 12, в) C 4 H 10, г) CH 4. Для алканов характерна изомерия: а) углеводородного скелета, б) положение кратной связи, в) положение функциональной группы, г) геометрическая.
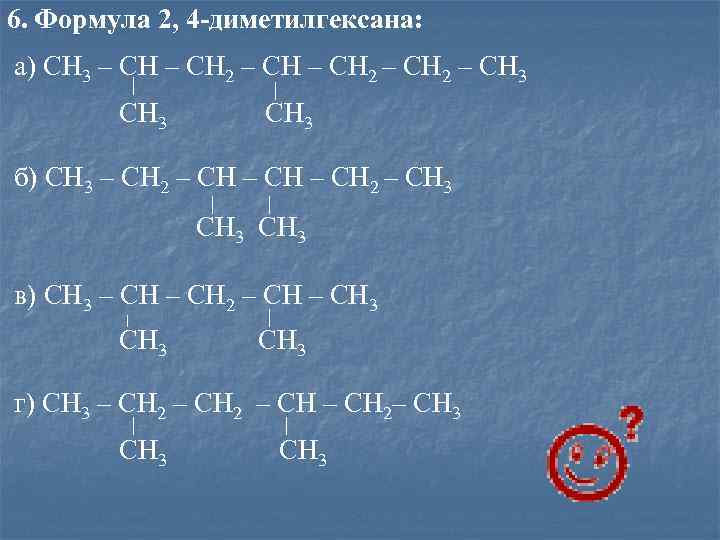 6. Формула 2, 4 -диметилгексана: а) CH 3 – CH 2 – CH 3 CH 3 б) CH 3 – CH 2 – CH 3 CH 3 в) CH 3 – CH 2 – CH 3 г) CH 3 – CH 2– CH 3
6. Формула 2, 4 -диметилгексана: а) CH 3 – CH 2 – CH 3 CH 3 б) CH 3 – CH 2 – CH 3 CH 3 в) CH 3 – CH 2 – CH 3 г) CH 3 – CH 2– CH 3
 7. Название углеводорода с формулой CH 3 – CH 2 – CH 3: CH 3 а) 4 -метилпентан, б) 2 -метилпропан, в) 3 -метилпентан, г) 2 -метилпентан. 8. Углеводороды с формулами C 6 H 12 и C 6 H 14 являются: а) изомерами, б) гомологами, в) верного ответа в перечисленных нет.
7. Название углеводорода с формулой CH 3 – CH 2 – CH 3: CH 3 а) 4 -метилпентан, б) 2 -метилпропан, в) 3 -метилпентан, г) 2 -метилпентан. 8. Углеводороды с формулами C 6 H 12 и C 6 H 14 являются: а) изомерами, б) гомологами, в) верного ответа в перечисленных нет.
 9. Метан в промышленности получают главным образом: а) из реакции Вюрца, б) из природного газа, в) коксованием каменного угля, г) гидролизом карбида алюминия. 10. Для алканов характерны реакции: а) присоединение, б) замещение, в) полимеризации 11. Какая из реакций алканов протекает при облучении смеси исходных веществ светом? а) крекинг, б) дегидрирование, в) хлорирование, г) горение. 12. Составьте уравнение реакции, при помощи которых можно осуществить следующие CH 4 CH 3 Cl C 2 H 6 C 2 H 5 Cl превращения: C
9. Метан в промышленности получают главным образом: а) из реакции Вюрца, б) из природного газа, в) коксованием каменного угля, г) гидролизом карбида алюминия. 10. Для алканов характерны реакции: а) присоединение, б) замещение, в) полимеризации 11. Какая из реакций алканов протекает при облучении смеси исходных веществ светом? а) крекинг, б) дегидрирование, в) хлорирование, г) горение. 12. Составьте уравнение реакции, при помощи которых можно осуществить следующие CH 4 CH 3 Cl C 2 H 6 C 2 H 5 Cl превращения: C
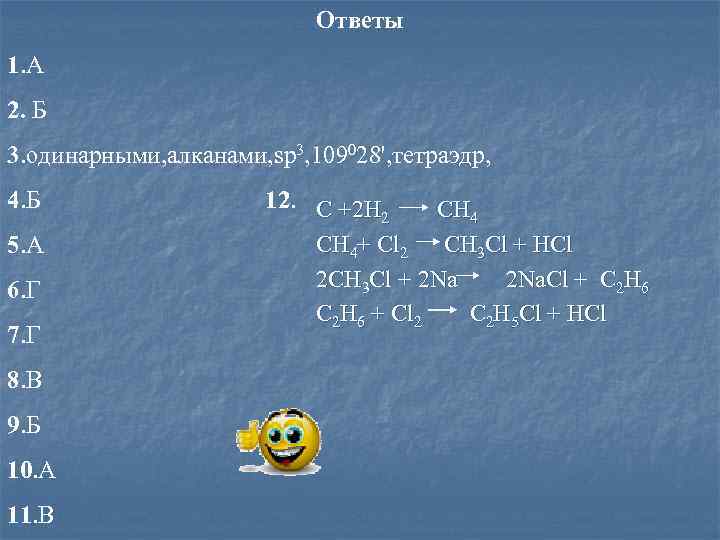 Ответы 1. А 2. Б 3. одинарными, алканами, sp 3, 109028', тетраэдр, 4. Б 5. А 6. Г 7. Г 8. В 9. Б 10. А 11. В 12. C +2 H CH 4 2 CH 4+ Cl 2 CH 3 Cl + HCl 2 CH 3 Cl + 2 Na. Cl + C 2 H 6 + Cl 2 C 2 H 5 Cl + HCl
Ответы 1. А 2. Б 3. одинарными, алканами, sp 3, 109028', тетраэдр, 4. Б 5. А 6. Г 7. Г 8. В 9. Б 10. А 11. В 12. C +2 H CH 4 2 CH 4+ Cl 2 CH 3 Cl + HCl 2 CH 3 Cl + 2 Na. Cl + C 2 H 6 + Cl 2 C 2 H 5 Cl + HCl


