алканы.ppt
- Количество слайдов: 37
 АЛКАНЫ (предельные углеводороды ряда метана, парафины) Презентация к уроку химии в 10 классе. Учитель химии МБОУ СОШ № 3 г. Светлого Калининградской обл. Ракович Лариса Викторовна
АЛКАНЫ (предельные углеводороды ряда метана, парафины) Презентация к уроку химии в 10 классе. Учитель химии МБОУ СОШ № 3 г. Светлого Калининградской обл. Ракович Лариса Викторовна
 НАХОЖДЕНИЕ АЛКАНОВ В ПРИРОДЕ
НАХОЖДЕНИЕ АЛКАНОВ В ПРИРОДЕ
 НАХОЖДЕНИЕ В КОСМОСЕ В небольших количествах алканы содержатся в атмосфере планет Солнечной системы: • на Юпитере — 0, 1% метана, 0, 0002% этана, • на Сатурне метана 0, 2%, а этана — 0, 0005%, метана и этана, • на Уране — соответственно 1, 99% и 0, 00025%, • на Нептуне же — 1, 5% и 1, 5· 10 -10 %. На спутнике Сатурна Титане метан (1, 6%) содержится в жидком виде, причем, подобно воде, находящейся на Земле. Кроме того, метан найден в хвосте кометы Хиякутаке и в метеоритах. Предполагается также, что метановые и этановые кометные льды образовались в межзвёздном пространстве. Комета Хиякутаке Сатурн Юпитер Уран 3
НАХОЖДЕНИЕ В КОСМОСЕ В небольших количествах алканы содержатся в атмосфере планет Солнечной системы: • на Юпитере — 0, 1% метана, 0, 0002% этана, • на Сатурне метана 0, 2%, а этана — 0, 0005%, метана и этана, • на Уране — соответственно 1, 99% и 0, 00025%, • на Нептуне же — 1, 5% и 1, 5· 10 -10 %. На спутнике Сатурна Титане метан (1, 6%) содержится в жидком виде, причем, подобно воде, находящейся на Земле. Кроме того, метан найден в хвосте кометы Хиякутаке и в метеоритах. Предполагается также, что метановые и этановые кометные льды образовались в межзвёздном пространстве. Комета Хиякутаке Сатурн Юпитер Уран 3
 НАХОЖДЕНИЕ НА ЗЕМЛЕ В земной атмосфере метан присутствует в очень небольших количествах (около 0, 0001%), он производится некоторыми архебактериями, в частности, находящимися в кишечном тракте крупного рогатого скота. Промышленное значение имеют месторождения низших алканов в форме природного газа, нефти и, вероятно, в будущем — газовых гидратов (найдены в областях вечной мерзлоты и под океанами). Также метан содержится в биогазе. Добыча газа Добыча нефти 4
НАХОЖДЕНИЕ НА ЗЕМЛЕ В земной атмосфере метан присутствует в очень небольших количествах (около 0, 0001%), он производится некоторыми архебактериями, в частности, находящимися в кишечном тракте крупного рогатого скота. Промышленное значение имеют месторождения низших алканов в форме природного газа, нефти и, вероятно, в будущем — газовых гидратов (найдены в областях вечной мерзлоты и под океанами). Также метан содержится в биогазе. Добыча газа Добыча нефти 4
 НАХОЖДЕНИЕ НА ЗЕМЛЕ Высшие алканы содержатся в кутикуле растений, предохраняя их от высыхания, паразитных грибков и мелких растительноядных тварей. Это обыкновенно цепи с нечётным числом атомов углерода. Среди животных алканы встречаются в качестве феромонов у насекомых, в частности у мухи цеце. Некоторые орхидеи при помощи алканов-феромонов привлекают опылителей. 5
НАХОЖДЕНИЕ НА ЗЕМЛЕ Высшие алканы содержатся в кутикуле растений, предохраняя их от высыхания, паразитных грибков и мелких растительноядных тварей. Это обыкновенно цепи с нечётным числом атомов углерода. Среди животных алканы встречаются в качестве феромонов у насекомых, в частности у мухи цеце. Некоторые орхидеи при помощи алканов-феромонов привлекают опылителей. 5
 СТРОЕНИЕ МОЛЕКУЛ АЛКАНОВ
СТРОЕНИЕ МОЛЕКУЛ АЛКАНОВ
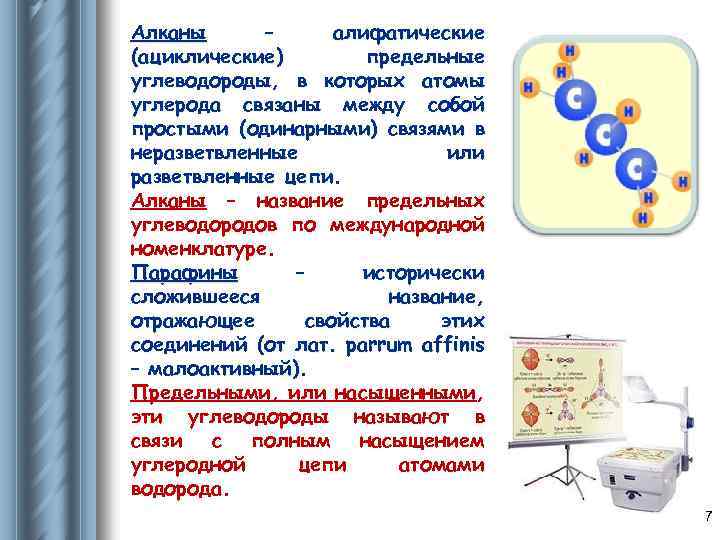 Алканы – алифатические (ациклические) предельные углеводороды, в которых атомы углерода связаны между собой простыми (одинарными) связями в неразветвленные или разветвленные цепи. Алканы – название предельных углеводородов по международной номенклатуре. Парафины – исторически сложившееся название, отражающее свойства этих соединений (от лат. parrum affinis – малоактивный). Предельными, или насыщенными, эти углеводороды называют в связи с полным насыщением углеродной цепи атомами водорода. 7
Алканы – алифатические (ациклические) предельные углеводороды, в которых атомы углерода связаны между собой простыми (одинарными) связями в неразветвленные или разветвленные цепи. Алканы – название предельных углеводородов по международной номенклатуре. Парафины – исторически сложившееся название, отражающее свойства этих соединений (от лат. parrum affinis – малоактивный). Предельными, или насыщенными, эти углеводороды называют в связи с полным насыщением углеродной цепи атомами водорода. 7
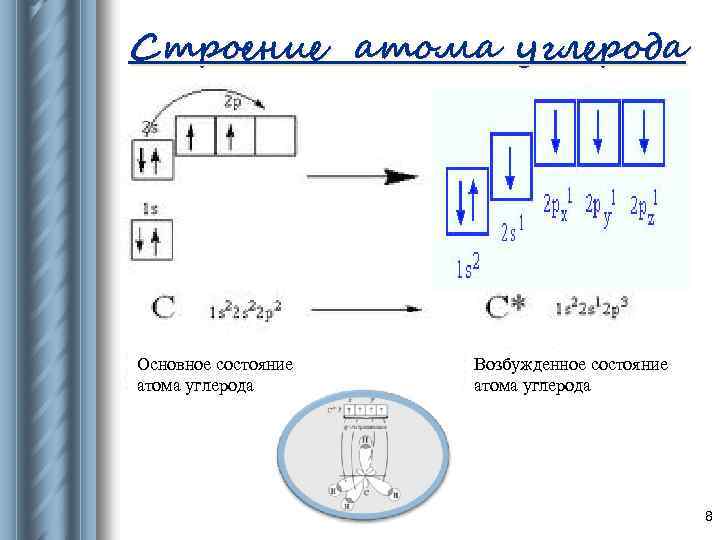 Строение атома углерода Основное состояние атома углерода Возбужденное состояние атома углерода 8
Строение атома углерода Основное состояние атома углерода Возбужденное состояние атома углерода 8
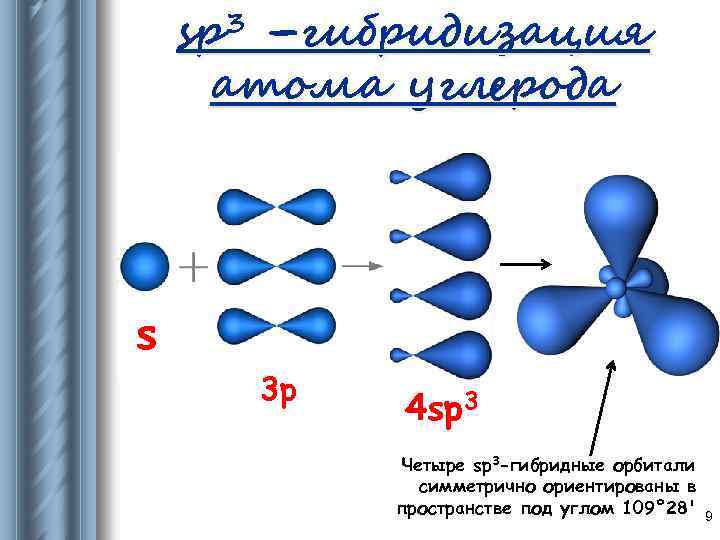 sp 3 –гибридизация атома углерода s 3 p 4 sp 3 Четыре sp 3 -гибридные орбитали симметрично ориентированы в пространстве под углом 109° 28' 9
sp 3 –гибридизация атома углерода s 3 p 4 sp 3 Четыре sp 3 -гибридные орбитали симметрично ориентированы в пространстве под углом 109° 28' 9
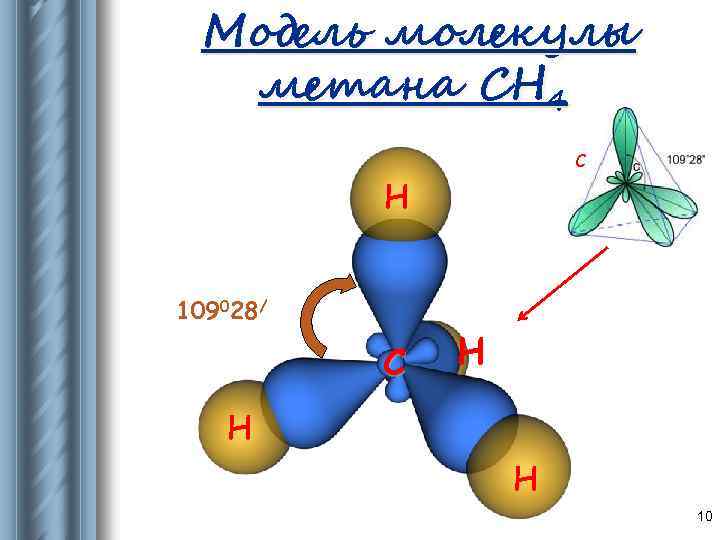 Модель молекулы метана CH 4 C Н 109028/ С Н Н Н 10
Модель молекулы метана CH 4 C Н 109028/ С Н Н Н 10
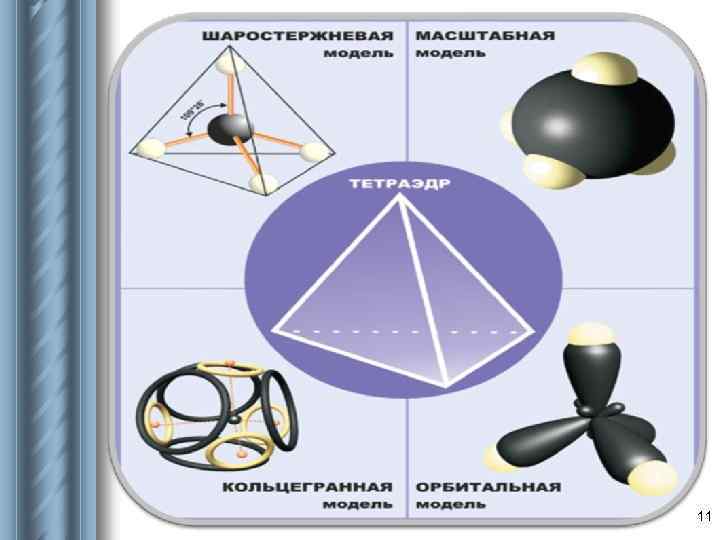 11
11
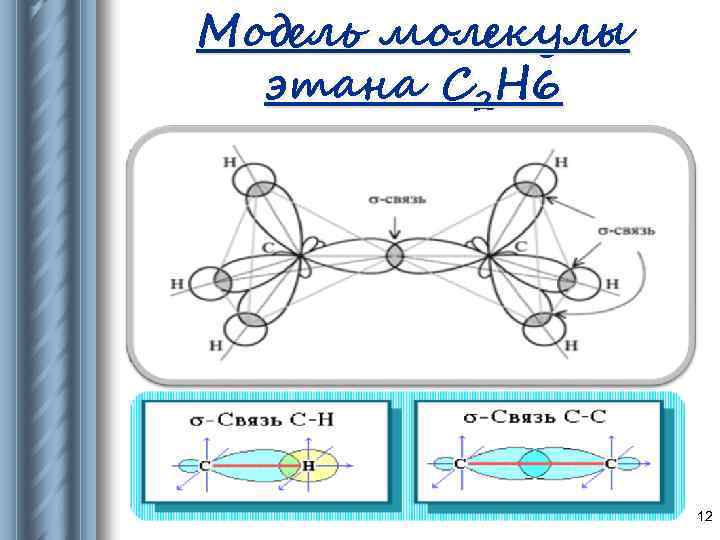 Модель молекулы этана C 2 H 6 12
Модель молекулы этана C 2 H 6 12
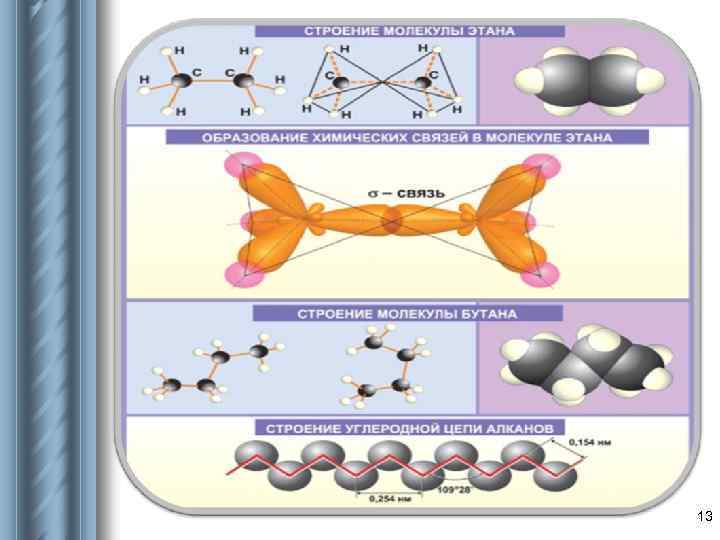 13
13
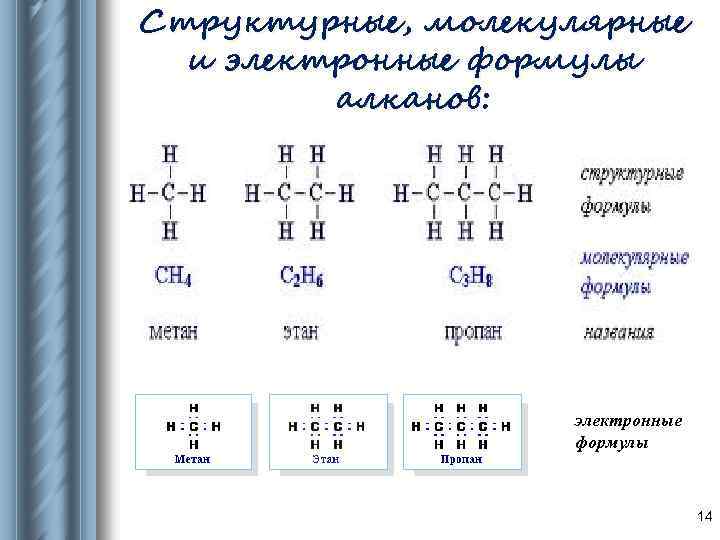 Структурные, молекулярные и электронные формулы алканов: электронные формулы 14
Структурные, молекулярные и электронные формулы алканов: электронные формулы 14
 Характеристика строения алканов 1. Тетраэдрическое строение молекул 2. Валентный угол : α = 109028ʹ 3. Длина связи: λ с-с = 0, 154 нм 4. Связи и их особенности: σсвязи прочные, трудно поляризуемые; возможно свободное вращение вокруг σсвязи. 5. Пространственное строение: могут образовывать пространственные формы. 15
Характеристика строения алканов 1. Тетраэдрическое строение молекул 2. Валентный угол : α = 109028ʹ 3. Длина связи: λ с-с = 0, 154 нм 4. Связи и их особенности: σсвязи прочные, трудно поляризуемые; возможно свободное вращение вокруг σсвязи. 5. Пространственное строение: могут образовывать пространственные формы. 15
 ГОМОЛОГИЯ АЛКАНОВ (гомологический ряд алканов)
ГОМОЛОГИЯ АЛКАНОВ (гомологический ряд алканов)
 Существуют углеродистые соединения выполняющие те же химические отправления, следующие тем же законам метаморфоз и содержащие тоже количество элементов: водорода, кислорода, хлора, азота и т. д. увеличенных или уменьшенных на СН 2. Я называю их гомологическими телами. Шарль Жерар 17
Существуют углеродистые соединения выполняющие те же химические отправления, следующие тем же законам метаморфоз и содержащие тоже количество элементов: водорода, кислорода, хлора, азота и т. д. увеличенных или уменьшенных на СН 2. Я называю их гомологическими телами. Шарль Жерар 17
 Основные определения Ряд соединений, в котором каждый последующий член отличается от предыдущего на одну и ту же величину, группу СН 2, называется гомологическим рядом. Каждый член гомологического ряда по отношению к предыдущим или последующим членам будет являться гомологом. Сама группа СН 2 называется разницей. гомологической 18
Основные определения Ряд соединений, в котором каждый последующий член отличается от предыдущего на одну и ту же величину, группу СН 2, называется гомологическим рядом. Каждый член гомологического ряда по отношению к предыдущим или последующим членам будет являться гомологом. Сама группа СН 2 называется разницей. гомологической 18
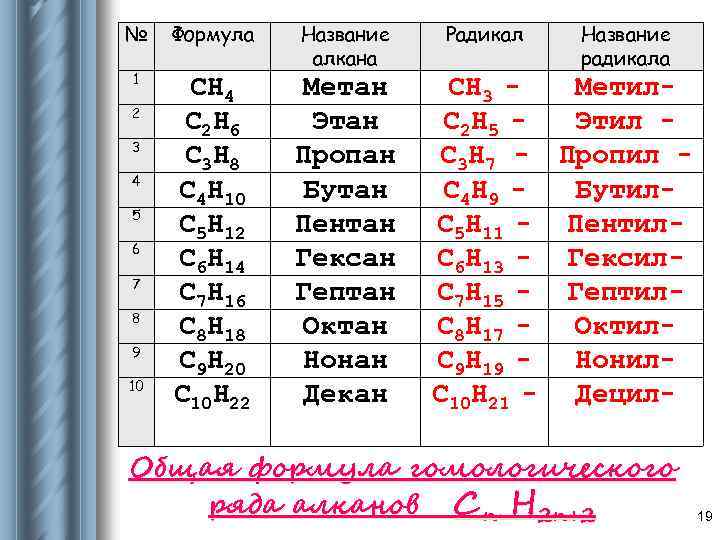 № Формула 1 Название алкана CH 4 C 2 H 6 C 3 H 8 C 4 H 10 C 5 H 12 C 6 H 14 C 7 H 16 C 8 H 18 C 9 H 20 C 10 H 22 Метан Этан Пропан Бутан Пентан Гексан Гептан Октан Нонан Декан 2 3 4 5 6 7 8 9 10 Радикал Название радикала CH 3 Метил. C 2 H 5 Этил C 3 H 7 - Пропил C 4 H 9 Бутил. C 5 H 11 - Пентил. C 6 H 13 - Гексил. C 7 H 15 - Гептил. C 8 H 17 Октил. C 9 H 19 Нонил. C 10 H 21 - Децил- Общая формула гомологического ряда алканов Сn H 2 n+2 19
№ Формула 1 Название алкана CH 4 C 2 H 6 C 3 H 8 C 4 H 10 C 5 H 12 C 6 H 14 C 7 H 16 C 8 H 18 C 9 H 20 C 10 H 22 Метан Этан Пропан Бутан Пентан Гексан Гептан Октан Нонан Декан 2 3 4 5 6 7 8 9 10 Радикал Название радикала CH 3 Метил. C 2 H 5 Этил C 3 H 7 - Пропил C 4 H 9 Бутил. C 5 H 11 - Пентил. C 6 H 13 - Гексил. C 7 H 15 - Гептил. C 8 H 17 Октил. C 9 H 19 Нонил. C 10 H 21 - Децил- Общая формула гомологического ряда алканов Сn H 2 n+2 19
 ИЗОМЕРИЯ АЛКАНОВ
ИЗОМЕРИЯ АЛКАНОВ
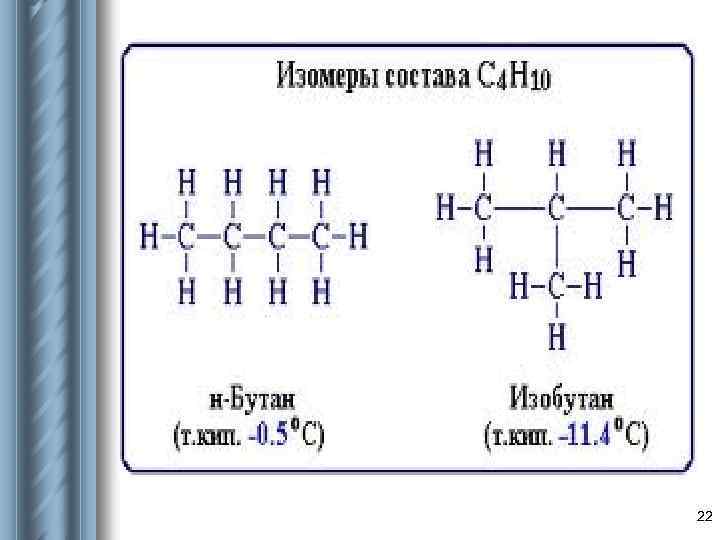
 ПОВТОРИМ! Изомерия – явление существования соединений, которые имеют одинаковый состав (одинаковую молекулярную формулу), но разное строение и свойства. Такие соединения называются изомерами. 21
ПОВТОРИМ! Изомерия – явление существования соединений, которые имеют одинаковый состав (одинаковую молекулярную формулу), но разное строение и свойства. Такие соединения называются изомерами. 21
 22
22
 Признаки гомологов и изомеров понятия состав качественный гомологи одинаковый химиче- свойства ское количественный строение отличны сходные на разницу СН 2 изомеры одинако- одинаковый различные сходные различные 23
Признаки гомологов и изомеров понятия состав качественный гомологи одинаковый химиче- свойства ское количественный строение отличны сходные на разницу СН 2 изомеры одинако- одинаковый различные сходные различные 23
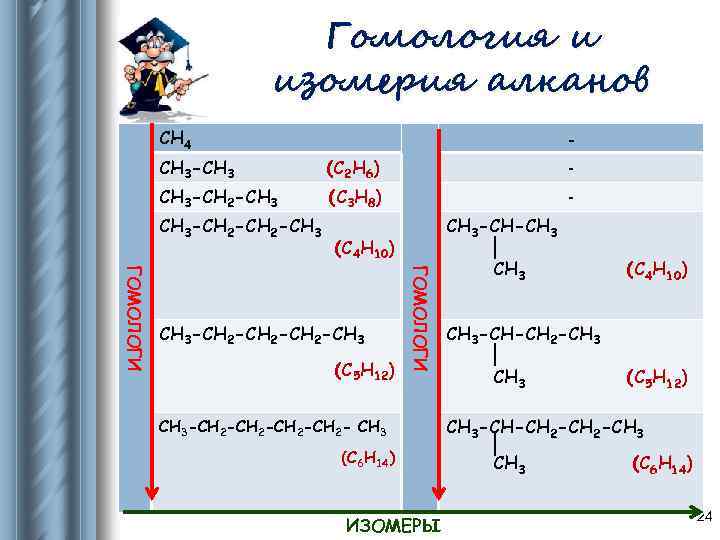 Гомология и изомерия алканов СН 4 - СН 3 -СН 3 (С 2 Н 6) - СН 3 -СН 2 -СН 3 (С 3 Н 8) - СН 3 -СН 2 -СН 3 -СН-СН 3 (С 4 Н 10) (С 5 Н 12) ГОМОЛОГИ СН 3 -СН 2 -СН 3 СН 3 -СН 2 -СН 2 - СН 3 (С 6 Н 14) ИЗОМЕРЫ СН 3 (С 4 Н 10) СН 3 -СН-СН 2 -СН 3 (С 5 Н 12) СН 3 -СН-СН 2 -СН 3 (С 6 Н 14) 24
Гомология и изомерия алканов СН 4 - СН 3 -СН 3 (С 2 Н 6) - СН 3 -СН 2 -СН 3 (С 3 Н 8) - СН 3 -СН 2 -СН 3 -СН-СН 3 (С 4 Н 10) (С 5 Н 12) ГОМОЛОГИ СН 3 -СН 2 -СН 3 СН 3 -СН 2 -СН 2 - СН 3 (С 6 Н 14) ИЗОМЕРЫ СН 3 (С 4 Н 10) СН 3 -СН-СН 2 -СН 3 (С 5 Н 12) СН 3 -СН-СН 2 -СН 3 (С 6 Н 14) 24
 ФИЗИЧЕСКИЕ СВОЙСТВА АЛКАНОВ
ФИЗИЧЕСКИЕ СВОЙСТВА АЛКАНОВ
 • В обычных условиях (при 25 °С и атмосферном давлении) первые четыре члена гомологического ряда алканов (С 1 -С 4)-газы. Нормальные алканы от пентана до гептадекана (С 5 -С 17) - жидкости, начиная с С 18 и выше - твердые вещества. • По мере увеличения числа атомов углерода в цепи, т. е. с ростом относительной молекулярной массы, возрастают температуры кипения и плавления алканов. • При одинаковом числе атомов углерода в молекуле алканы с разветвленным строением имеют более низкие температуры кипения, чем нормальные алканы. • Алканы практически не растворимы в воде, так как их молекулы малополярны и не взаимодействуют с молекулами воды. Жидкие алканы легко смешиваются друг с другом. Они хорошо растворяются в неполярных органических растворителях, таких как бензол, тетрахлорметан (четыреххлористый углерод), диэтиловый эфир и др. 26
• В обычных условиях (при 25 °С и атмосферном давлении) первые четыре члена гомологического ряда алканов (С 1 -С 4)-газы. Нормальные алканы от пентана до гептадекана (С 5 -С 17) - жидкости, начиная с С 18 и выше - твердые вещества. • По мере увеличения числа атомов углерода в цепи, т. е. с ростом относительной молекулярной массы, возрастают температуры кипения и плавления алканов. • При одинаковом числе атомов углерода в молекуле алканы с разветвленным строением имеют более низкие температуры кипения, чем нормальные алканы. • Алканы практически не растворимы в воде, так как их молекулы малополярны и не взаимодействуют с молекулами воды. Жидкие алканы легко смешиваются друг с другом. Они хорошо растворяются в неполярных органических растворителях, таких как бензол, тетрахлорметан (четыреххлористый углерод), диэтиловый эфир и др. 26
 ХИМИЧЕСКИЕ СВОЙСТВА АЛКАНОВ
ХИМИЧЕСКИЕ СВОЙСТВА АЛКАНОВ
 Предельные углеводороды характеризуются малой реактивной способностью. Их называют инерционными, химически стойкими, парафинами (от латинского parum affinis – “мало сродства”). 28
Предельные углеводороды характеризуются малой реактивной способностью. Их называют инерционными, химически стойкими, парафинами (от латинского parum affinis – “мало сродства”). 28
 1. Реакции окисления При поджигании (t = 600 o. С) алканы вступают в реакцию с кислородом, при этом происходит их окисление до углекислого газа и воды. Сn. Н 2 n+2 + O 2 → CO 2 + H 2 O + Q например: СН 4 + 2 O 2 → CO 2 + 2 H 2 O + Q Смесь метана с кислородом или воздухом при поджигании может взрываться. Наиболее сильный взрыв получается при объёмных отношениях 1 : 2 (с кислородом) или 1 : 10 (с воздухом), т. к. метан и кислород вступают в реакцию полностью. Подобные смеси опасны в каменноугольных шахтах. Чтобы обеспечить безопасность работы в шахтах, там устанавливают анализаторы, сигнализирующие о появлении газа, и мощные вентиляционные устройства. С 3 Н 8 + 5 O 2 → 3 CO 2 + 4 H 2 O + Q 29
1. Реакции окисления При поджигании (t = 600 o. С) алканы вступают в реакцию с кислородом, при этом происходит их окисление до углекислого газа и воды. Сn. Н 2 n+2 + O 2 → CO 2 + H 2 O + Q например: СН 4 + 2 O 2 → CO 2 + 2 H 2 O + Q Смесь метана с кислородом или воздухом при поджигании может взрываться. Наиболее сильный взрыв получается при объёмных отношениях 1 : 2 (с кислородом) или 1 : 10 (с воздухом), т. к. метан и кислород вступают в реакцию полностью. Подобные смеси опасны в каменноугольных шахтах. Чтобы обеспечить безопасность работы в шахтах, там устанавливают анализаторы, сигнализирующие о появлении газа, и мощные вентиляционные устройства. С 3 Н 8 + 5 O 2 → 3 CO 2 + 4 H 2 O + Q 29
 Сравните пламя при горении различных алканов парафин Метан пентан 30
Сравните пламя при горении различных алканов парафин Метан пентан 30
 2. Реакции разложения Сn. Н 2 n+2 → C + H 2↑ СН 4 → C + 2 H 2↑ С 4 Н 10 → 4 C + 5 H 2↑ Метан в термическом отношении более устойчив, чем другие алканы. Причина этого в достаточной прочности С – Н связей. 31
2. Реакции разложения Сn. Н 2 n+2 → C + H 2↑ СН 4 → C + 2 H 2↑ С 4 Н 10 → 4 C + 5 H 2↑ Метан в термическом отношении более устойчив, чем другие алканы. Причина этого в достаточной прочности С – Н связей. 31
 3. Реакции замещения Протекают с галогенами и другими окислителями при определённых условиях: свет, температура: СН 4 + Cl 2 → CH 3 Cl + HCl СН 3 Cl + Cl 2 → CH 2 Cl 2 + HCl СН 2 Cl 2 + Cl 2 → CHCl 3 + HCl СНCl 3 + Cl 2 → CCl 4 + HCl Механизм цепных реакций достаточно сложен, объяснение ему было дано русским учёным Н. Н. Семёновым, за что он в 1956 г. был удостоен Нобелевской премии. Н. Н. Семёнов (1896 -25. 09. 1986 г. г. ) 32
3. Реакции замещения Протекают с галогенами и другими окислителями при определённых условиях: свет, температура: СН 4 + Cl 2 → CH 3 Cl + HCl СН 3 Cl + Cl 2 → CH 2 Cl 2 + HCl СН 2 Cl 2 + Cl 2 → CHCl 3 + HCl СНCl 3 + Cl 2 → CCl 4 + HCl Механизм цепных реакций достаточно сложен, объяснение ему было дано русским учёным Н. Н. Семёновым, за что он в 1956 г. был удостоен Нобелевской премии. Н. Н. Семёнов (1896 -25. 09. 1986 г. г. ) 32
 4. Реакции изомеризации Характерны не для всех алканов. Возможны превращения одних изомеров в другие при наличии катализаторов. С 4 Н 10 → C 4 H 10 Уравнение вызывает недоумение, т. к. вы не встречались с реакциями, при которых состав молекул не изменялся. Значит, химические реакции могут сопровождаться не только изменением состава веществ, но и изменением их строения, что часто встречается в органической химии. Чтобы выразить такое превращение, надо пользоваться структурными формулами. Структурно это выглядит следующим образом: СН 3 – СН 2 – СН 3 н-бутан Al. Clз СН 3 – СН 3 изобутан (2 -метилпропан) 33
4. Реакции изомеризации Характерны не для всех алканов. Возможны превращения одних изомеров в другие при наличии катализаторов. С 4 Н 10 → C 4 H 10 Уравнение вызывает недоумение, т. к. вы не встречались с реакциями, при которых состав молекул не изменялся. Значит, химические реакции могут сопровождаться не только изменением состава веществ, но и изменением их строения, что часто встречается в органической химии. Чтобы выразить такое превращение, надо пользоваться структурными формулами. Структурно это выглядит следующим образом: СН 3 – СН 2 – СН 3 н-бутан Al. Clз СН 3 – СН 3 изобутан (2 -метилпропан) 33
 ПРИМЕНЕНИЕ АЛКАНОВ
ПРИМЕНЕНИЕ АЛКАНОВ
 35
35
 ИСТОЧНИКИ ИНФОРМАЦИИ • http: //ru. wikipedia. org/wiki/Алканы • http: //hybridation. ru/sp 3. htm • http: //www. chem. asu. ru/org/ochem_bio/ALKANY/fisic. htm
ИСТОЧНИКИ ИНФОРМАЦИИ • http: //ru. wikipedia. org/wiki/Алканы • http: //hybridation. ru/sp 3. htm • http: //www. chem. asu. ru/org/ochem_bio/ALKANY/fisic. htm



