Алканы.ppt
- Количество слайдов: 51
Алканы.

Образование ковалентных связей в алканах
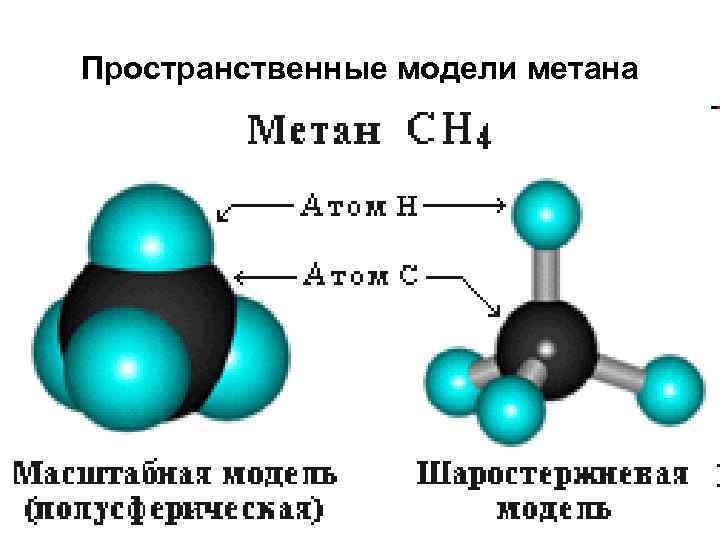
Пространственные модели метана

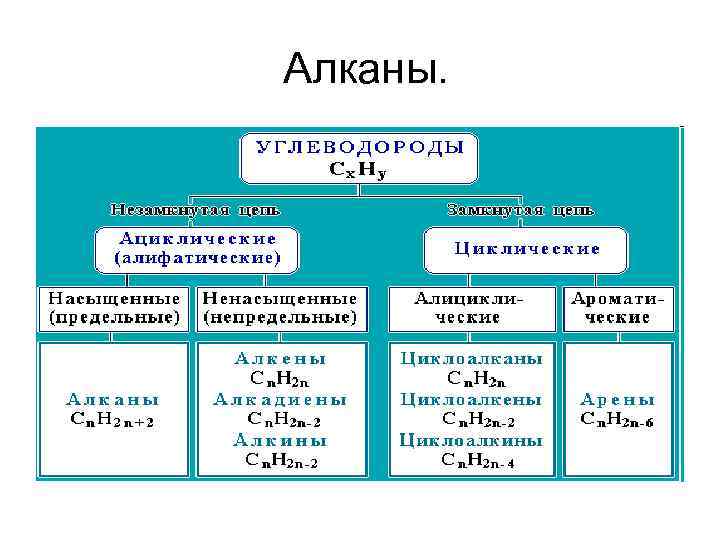
• Классификация углеводородов • Классификацию углеводородов проводят по следующим структурным признакам: • строение углеродной цепи; • наличие в цепи кратных связей С=С и С C. • 1. В зависимости от строения углеродной цепи углеводороды подразделяют на две группы: • алифатические, т. е. "жирные"; • циклические.

• Среди циклических углеводородов выделяют: • алициклические (т. е. алифатические циклические); • ароматические (арены).

• По степени насыщенности различают: • насыщенные (предельные) углеводороды (алканы и циклоалканы), в которых имеются только простые связи С-С и отсутствуют кратные связи; • ненасыщенные (непредельные), содержащие наряду с одинарными связями С-С двойные и/или тройные связи (алкены, алкадиены, алкины, циклоалкены, циклоалкины).

• Алканы – алифатические предельные углеводороды, в которых атомы углерода связаны между собой простыми (одинарными) связями. • Предельными, или насыщенными, эти углеводороды называют в связи с полным насыщением углеродной цепи атомами водорода.
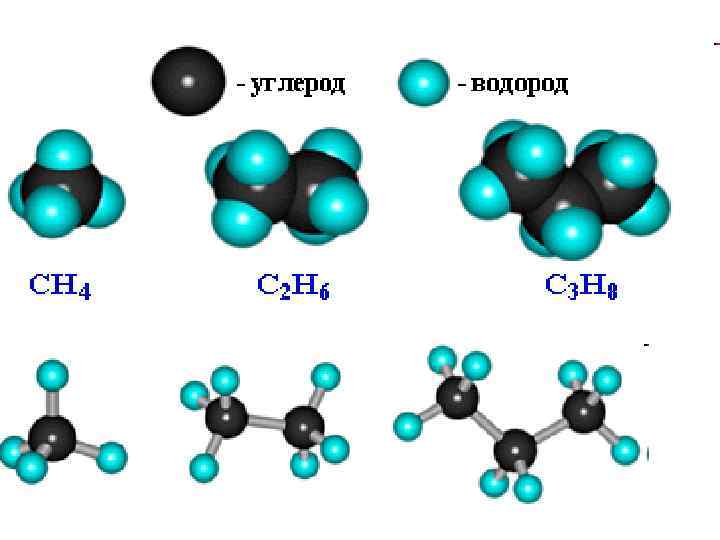

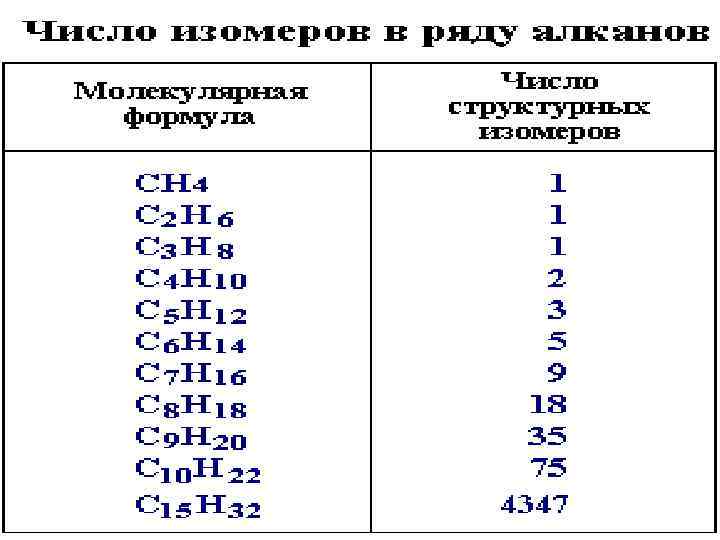
• При сравнении этих соединений видно, что они отличаются друг от друга на группу СН 2 - (метилен). Добавляя к пропану еще одну группу -СН 2 -, получим бутан С 4 Н 10 и т. д. • Общая формула алканов. Число атомов углерода в ряду алканов примем за n, тогда число атомов водорода составит величину 2 n+2.

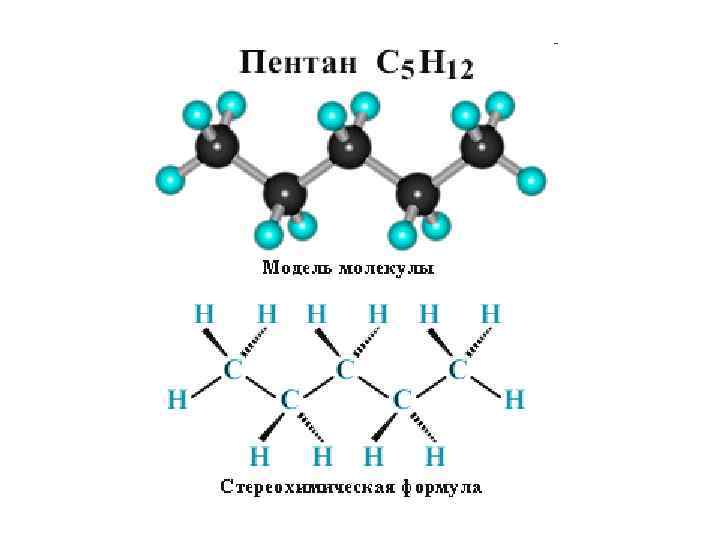
• Суффикс -ан является характерным для названия всех алканов. Начиная с пятого гомолога, название алкана образуется из греческого числительного, указывающего число атомов углерода в молекуле, и суффикса -ан: пентан С 5 Н 12, гексан С 6 Н 14, гептан С 7 Н 16, октан С 8 Н 18, нонан С 9 Н 20, декан С 10 Н 22 и т. д.

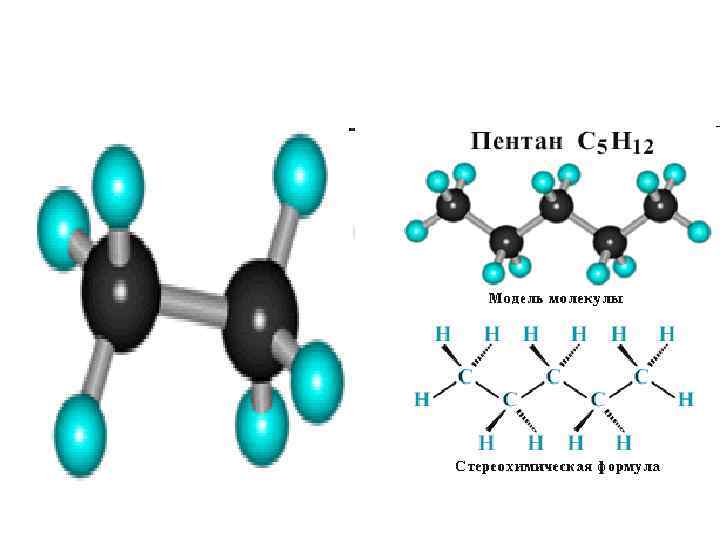
• Гомологи отличаются молекулярной массой, и следовательно, физическими характеристиками. • С увеличением числа углеродных атомов в молекуле алкана в гомологическом ряду наблюдается закономерное изменение физических свойств гомологов: • повышаются температуры кипения и плавления, увеличивается плотность. • Алканы от СН 4 до С 4 Н 10– газы, от С 5 Н 12 до С 17 Н 36 – жидкости, далее – твердые вещества.

• Строение алканов • В алканах имеются два типа химических связей: С–С и С–Н. • Связь С–С является ковалентной неполярной. Связь С–Н - ковалентная слабополярная. • Образование ковалентных связей в алканах за счет общих электронных пар атомов углерода и водорода можно показать с помощью электронных формул:
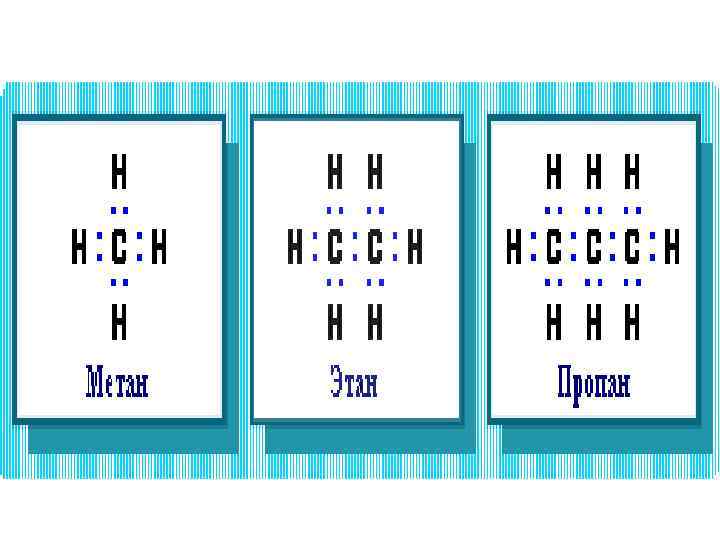

• Пространственное строение, т. е. взаимное расположение атомов молекулы в пространстве, зависит от направленности атомных орбиталей (АО) этих атомов. • В углеводородах главную роль играет пространственная ориентация атомных орбиталей углерода.
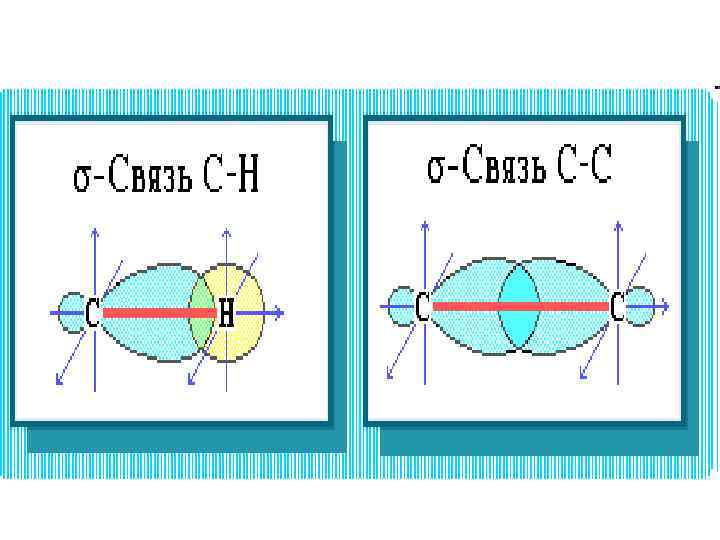

• Насыщенный атом углерода в алканах связан с четырьмя другими атомами. • Его состояние соответствует sp 3 -гибридизации. • Каждая из четырех sp 3 -гибридных АО углерода участвует в осевом (s-) перекрывании с s-АО водорода или с sp 3 -АО другого атома углерода, образуя s-связи С-Н или С-С.
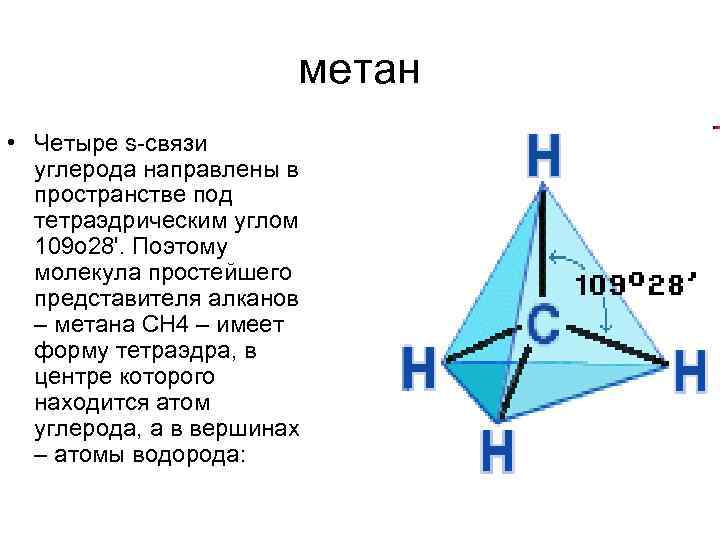
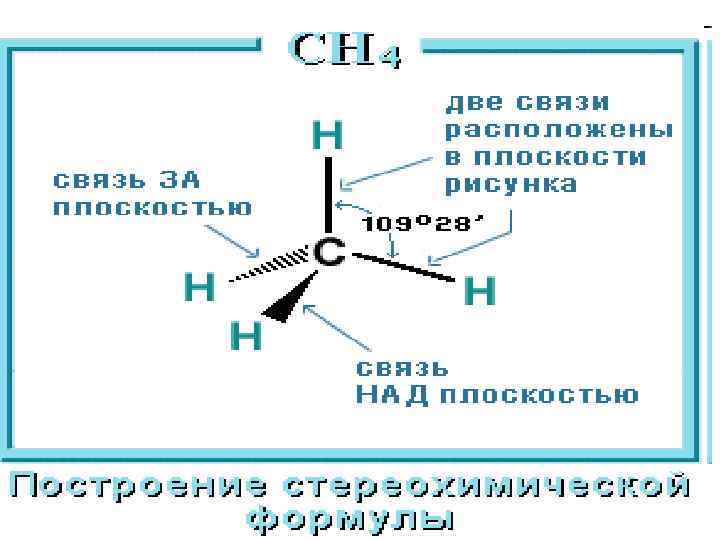
метан • Четыре s-связи углерода направлены в пространстве под тетраэдрическим углом 109 о 28'. Поэтому молекула простейшего представителя алканов – метана СН 4 – имеет форму тетраэдра, в центре которого находится атом углерода, а в вершинах – атомы водорода:
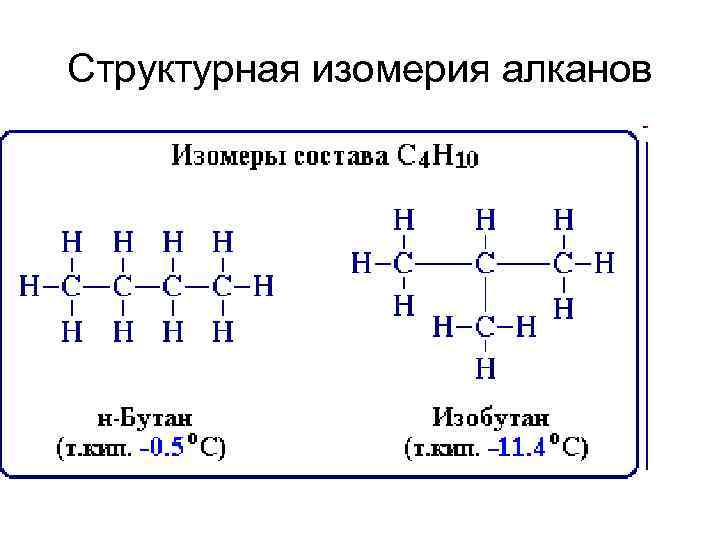
Структурная изомерия алканов

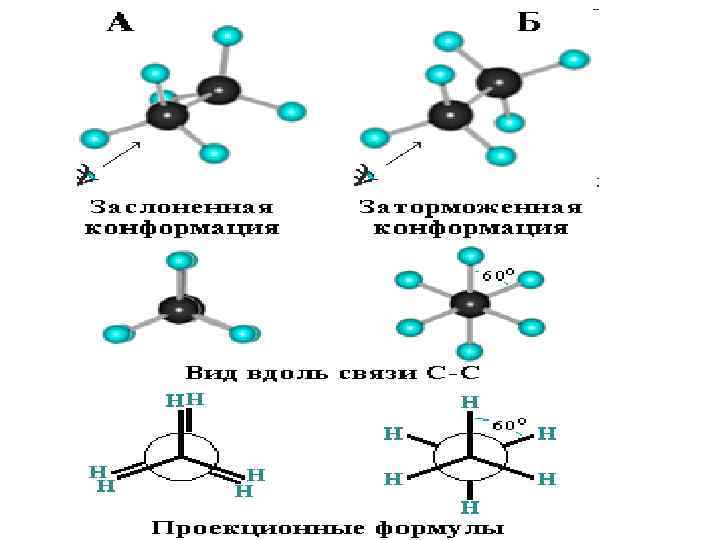
• Поворотная изомерия алканов • Характерной особенностью s-связей является то, что электронная плотность в них распределена симметрично относительно оси, соединяющей ядра связываемых атомов (цилиндрическая или вращательная симметрия). Поэтому вращение атомов вокруг s-связи не будет приводить к ее разрыву. В результате внутримолекулярного вращения по s-связям С–С молекулы алканов, начиная с этана С 2 Н 6, могут принимать разные геометрические формы. • Различные пространственные формы молекулы, переходящие друг в друга путем вращения вокруг s -связей С–С, называют конформациями или поворотными изомерами (конформерами).
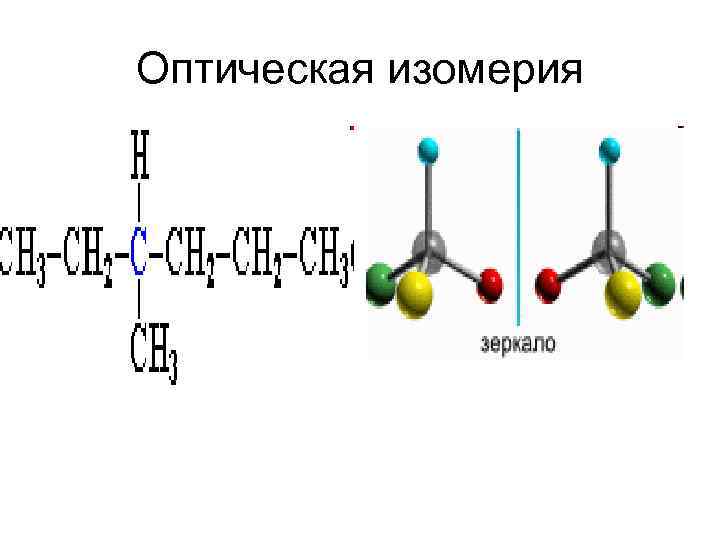
Оптическая изомерия

• Номенклатура органических соединений – система правил, позволяющих дать однозначное название каждому индивидуальному веществу. • Это язык химии, который используется для передачи в названиях соединений их строения. Соединению определенного строения соответствует одно систематическое название, и по этому названию можно представить строение соединения (его структурную формулу). • В настоящее время общепринятой является систематическая номенклатура ИЮПАК (IUPAC – International Union of the Pure and Applied Chemistry – Международный союз теоретической и прикладной химии).

• Радикалы в ряду алканов • Если от молекулы алкана "отнять" один атом водоpода, то обpазуется одновалентный "остаток" – углеводоpодный pадикал (R–). Общее название одновалентных радикалов алканов – алкилы – обpазовано заменой суффикса -ан на -ил: метан – метил, этан – этил. • Одновалентные pадикалы выpажаются общей фоpмулой Сn. Н 2 n+1.
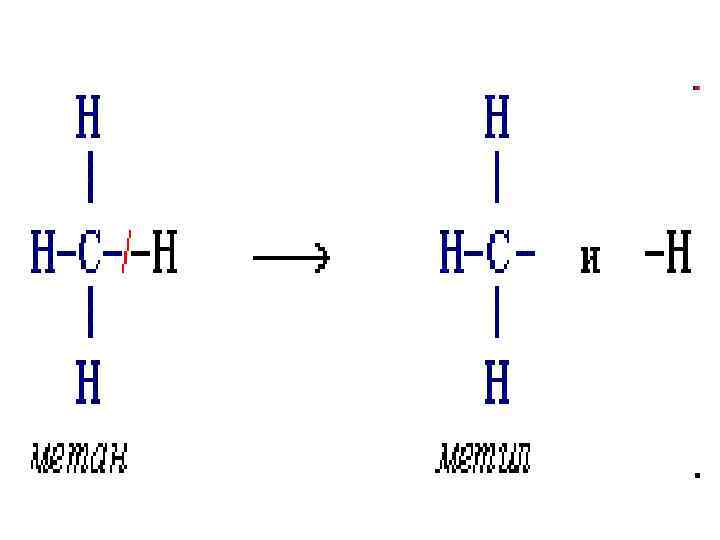
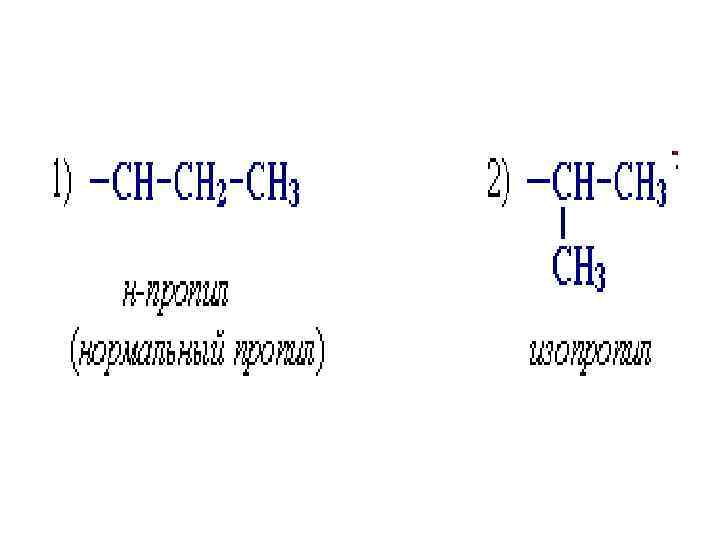
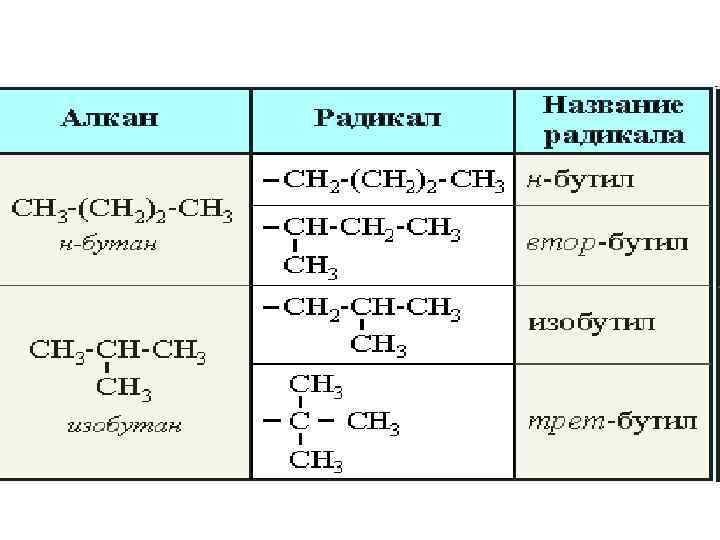

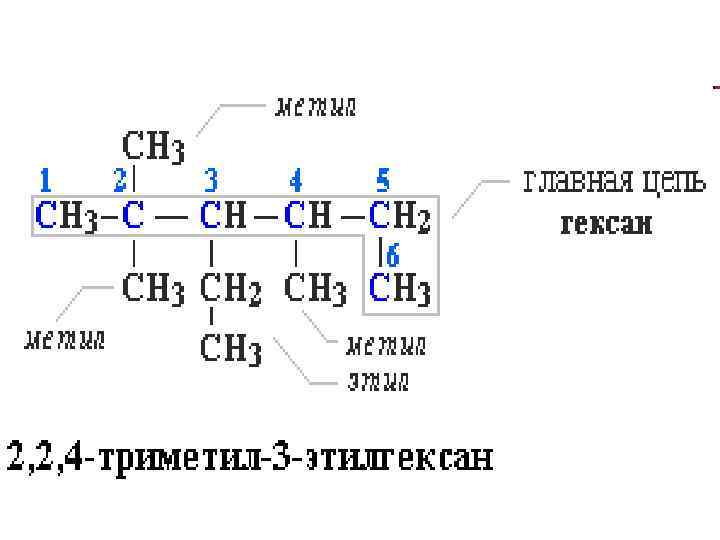
• • • Для простейших алканов (С 1 -С 4) приняты тpивиальные названия: метан, этан, пpопан, бутан, изобутан. Начиная с пятого гомолога, названия нормальных алканов стpоят в соответствии с числом атомов углеpода, используя гpеческие числительные и суффикс -ан: пентан, гексан, гептан, октан, нонан, декан и т. д. В основе названия разветвленного алкана лежит название входящего в его конструкцию нормального алкана с наиболее длинной углеродной цепью. При этом углеводоpод с pазветвленной цепью pассматpивают как пpодукт замещения атомов водоpода в ноpмальном алкане углеводоpодными pадикалами.

• Химические свойства алканов • Химические свойства любого соединения определяются его строением. • Предельная насыщенность алканов не допускает реакций присоединения, но не препятствует реакциям разложения, изомеризации и замещения. • Симметричность неполярных С–С и слабополярных С–Н ковалентных связей предполагает их гомолитический (симметричный) разрыв на свободные радикалы. • Следовательно, для реакций алканов характерен радикальный механизм.

• С разрывом связей С–С происходят реакции разложения (крекинг алканов) и изомеризации углеродного скелета. • По связям С–Н возможны реакции замещения атома водорода или его отщепления (дегидрирование алканов). • В присутствии окислителей в определенных условиях будут происходить реакции окисления алканов с участием связей С–С и С–Н.

• Крекинг - реакции расщепления углеродного скелета крупных молекул при нагревании и в присутствии катализаторов. • При температуре 450 – 700°С алканы распадаются за счет разрыва связей С–С (более прочные связи С–Н при такой температуре сохраняются) и образуются алканы и алкены с меньшим числом углеродных атомов. • Например: • C 6 H 14 ® C 2 H 6 + C 4 H 8
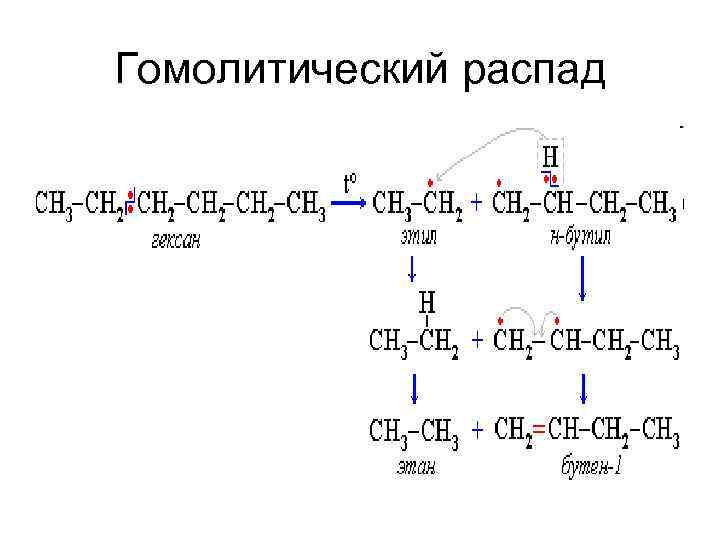
Гомолитический распад
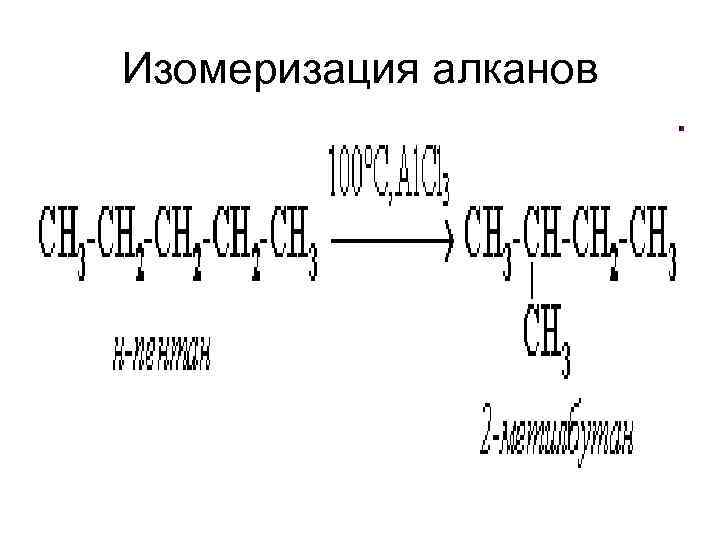
Изомеризация алканов
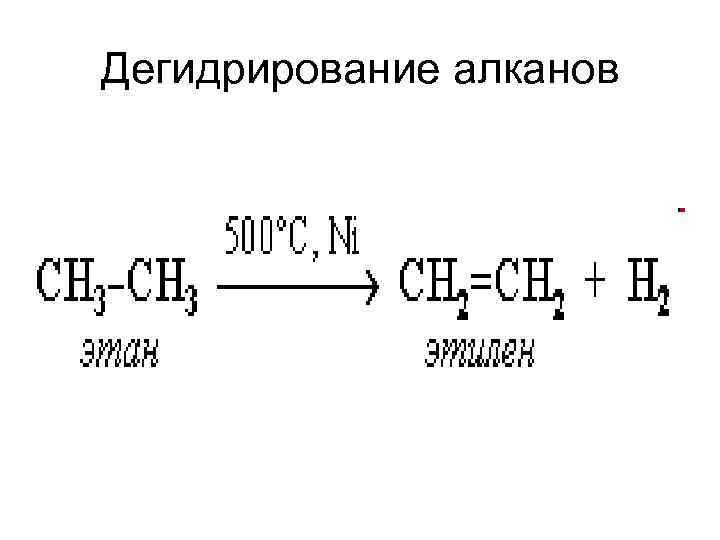
Дегидрирование алканов
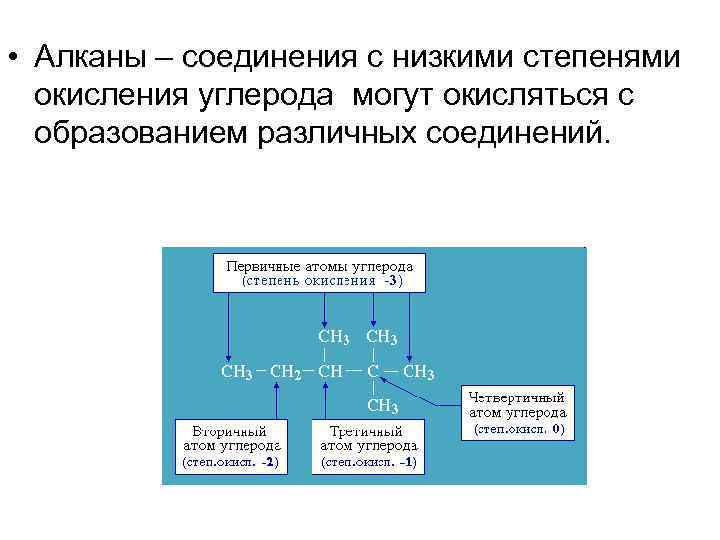
• Алканы – соединения с низкими степенями окисления углерода могут окисляться с образованием различных соединений.

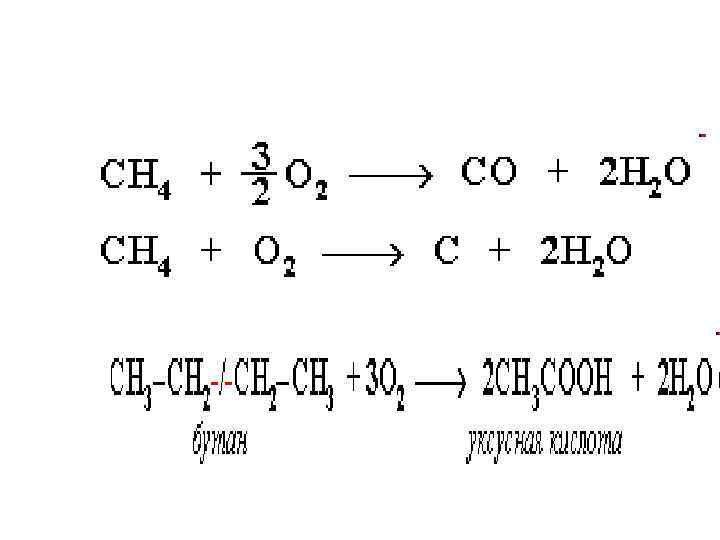
• При внесении в открытое пламя происходит полное окисление алканов до СО 2, где углерод имеет высшую степень окисления +4, и воды. • Горение углеводородов приводит к разрыву всех связей С–С и С–Н.

• Реакции замещения • В молекулах алканов связи C-Н пространственно более доступны для атаки другими частицами, чем менее прочные связи C-C. • Галогенирование алканов – реакция замещения одного или более атомов водорода в молекуле алкана на галоген. Продукты реакции называют галогеналканами или галогенопроизводными алканов. • Хлорирование метана:

• Реакция галогенирования алканов протекает по радикальному цепному механизму.

• При хлорировании или бромировании алкана с вторичными или третичными атомами углерода легче всего идет замещение водорода у третичного атома, труднее у вторичного и еще труднее у первичного. • Это объясняется большей устойчивостью третичных и вторичных углеводородных радикалов по сравнению с первичными вследствие делокализации неспаренного электрона.

• . Нитрование алканов (реакция Коновалова) • На алканы действует pазбавленная азотная кислота пpи нагpевании и давлении. В pезультате пpоисходит замещение атома водоpода на остаток азотной кислоты – нитpогpуппу NO 2. Эту pеакцию называют pеакцией нитpования, а пpодукты pеакции – нитpосоединениями.

• При нитровании алканов также соблюдается порядок реакционной способности С-Н-связей, характерный для реакций радикального замещения: Стрет. – Н > Свтор. – Н > Cперв. – Н

• Замена атомов водорода на галоген делает соединение химически активным, т. к. связь углерода с более электроотрицательным атомом галогена является полярной. • Полярность ковалентной связи, например С–Cl, приводит к смещению электронной плотности соседних связей в молекуле (индуктивный эффект). • Галогенопроизводные алканов применяются для синтеза алканов с заданным строением молекул.

• Для галогенпроизводных характерно замещение галогена на другие группы атомов при действии воды, оснований и солей. Эти реакции протекают по механизму нуклеофильного замещения (SN), т. к. положительно заряженный углеродный атом, связанный с галогеном, является центром атаки нуклеофильными частицами (OH-, OR-, NH 2 - и др. ).
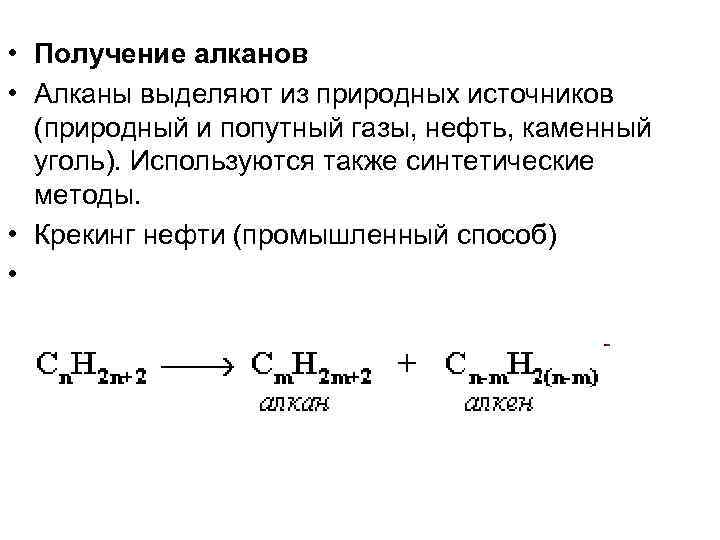
• Получение алканов • Алканы выделяют из природных источников (природный и попутный газы, нефть, каменный уголь). Используются также синтетические методы. • Крекинг нефти (промышленный способ) •

• При крекинге алканы получаются вместе с непредельными соединениями (алкенами). Этот способ важен тем, что при разрыве молекул высших алканов получается очень ценное сырье для органического синтеза: пропан, бутан, изопентан и др. Гидpиpование непpедельных углеводоpодов:

• Применение алканов • Газообразные алканы (метан и пpопанбутановая смесь) используются в качестве топлива. • Жидкие углеводоpоды составляют значительную долю в моторных и ракетных топливах и используются в качестве растворителей. • Вазелиновое масло (смесь жидких углеводоpодов с числом атомов углерода до 15) - пpозpачная жидкость без запаха и вкуса, используется в медицине, паpфюмеpии и косметике.
Алканы.ppt