 Алканы. Алкены.
Алканы. Алкены.
 Изомерия – явление существования соединений, которые имеют одинаковый состав (одинаковую молекулярную формулу), но разное строение. Такие соединения называются изомерами. Гомологи – вещества, сходные по строению и свойствам и отличающиеся на одну или более группу СН 2 ; СН 2 – называется гомологической разностью.
Изомерия – явление существования соединений, которые имеют одинаковый состав (одинаковую молекулярную формулу), но разное строение. Такие соединения называются изомерами. Гомологи – вещества, сходные по строению и свойствам и отличающиеся на одну или более группу СН 2 ; СН 2 – называется гомологической разностью.
 Заполняем таблицу: Критерий Определение Общая формула Гомологический ряд Физические свойства Химические свойства Алканы Алкены
Заполняем таблицу: Критерий Определение Общая формула Гомологический ряд Физические свойства Химические свойства Алканы Алкены
 Определение: Алка ны (также насыщенные УВ, парафины, алифатические соединения) — ациклические углеводороды линейного или разветвлённого строения, содержащие только одинарные связи. Алкены (также ненасыщенные УВ, олефины, этилены) – непредельные углеводороды, в молекулах которых содержится одна двойная связь.
Определение: Алка ны (также насыщенные УВ, парафины, алифатические соединения) — ациклические углеводороды линейного или разветвлённого строения, содержащие только одинарные связи. Алкены (также ненасыщенные УВ, олефины, этилены) – непредельные углеводороды, в молекулах которых содержится одна двойная связь.
 Общая формула: Алканы - Сn. H 2 n+2 Алкены - Сn. H 2 n
Общая формула: Алканы - Сn. H 2 n+2 Алкены - Сn. H 2 n
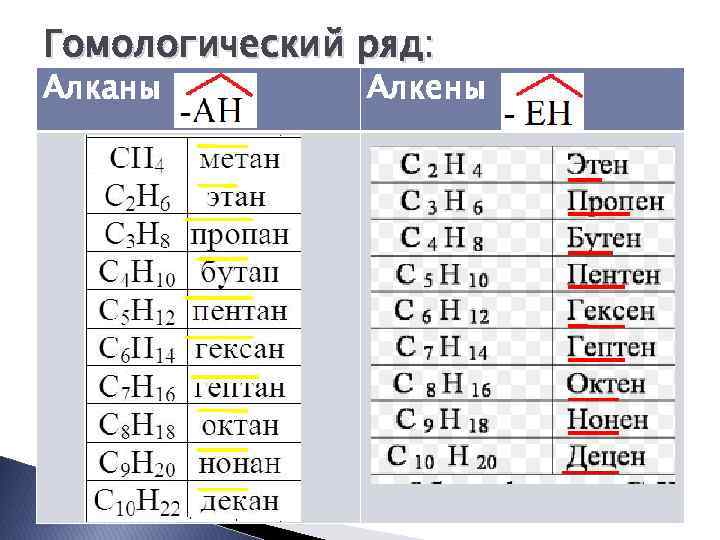 Гомологический ряд: Алканы Алкены
Гомологический ряд: Алканы Алкены
 Физические свойства: Алканы: с CH 4 до C 4 H 10 — газы; с C 5 H 12 до C 13 H 28 — жидкости; с C 14 H 30 и далее — твёрдые вещества. Алкены: с C 2 H 4 до C 4 H 8 — газы; с C 5 H 10 до C 17 H 34 — жидкости; с C 18 H 36 — твёрдые вещества. (с повышением молекулярной массы возрастают температуры плавления и кипения)
Физические свойства: Алканы: с CH 4 до C 4 H 10 — газы; с C 5 H 12 до C 13 H 28 — жидкости; с C 14 H 30 и далее — твёрдые вещества. Алкены: с C 2 H 4 до C 4 H 8 — газы; с C 5 H 10 до C 17 H 34 — жидкости; с C 18 H 36 — твёрдые вещества. (с повышением молекулярной массы возрастают температуры плавления и кипения)
 Химические свойства Алканов: 1) Реакция горения: СН 4 + 2 O 2 → CO 2 + 2 H 2 O +Q 2) Реакции разложения: СН 4 → C + 2 H 2 ↑ С 2 Н 6 → С 2 Н 4 + Н 2↑ Реакции, в которых от молекул органического вещества отщепляются молекулы водорода, называют реакциями дегидрирования.
Химические свойства Алканов: 1) Реакция горения: СН 4 + 2 O 2 → CO 2 + 2 H 2 O +Q 2) Реакции разложения: СН 4 → C + 2 H 2 ↑ С 2 Н 6 → С 2 Н 4 + Н 2↑ Реакции, в которых от молекул органического вещества отщепляются молекулы водорода, называют реакциями дегидрирования.
 Химические свойства алкенов: 1) Реакции горения: Н 2 С=СН 2 + 3 O 2 → 2 СO 2 + 2 Н 2 O 2) Реакция гидратации (присоединения воды): Kat H 2 С=СН 2 + Н 2 О → Н 3 С—CH 2 ОН 3) Реакции галогенирования (присоединение галогенов): Н 2 С=СН 2 + Cl 2 → Cl. H 2 C—CH 2 Cl 4) Окисление перманганатом калия: 3 H 2 C=CH 2 + 2 KMn. O 4 + 4 H 2 O → → 3 CH 2—CH 2 + 2 Mn. O 2 + KOH | OH
Химические свойства алкенов: 1) Реакции горения: Н 2 С=СН 2 + 3 O 2 → 2 СO 2 + 2 Н 2 O 2) Реакция гидратации (присоединения воды): Kat H 2 С=СН 2 + Н 2 О → Н 3 С—CH 2 ОН 3) Реакции галогенирования (присоединение галогенов): Н 2 С=СН 2 + Cl 2 → Cl. H 2 C—CH 2 Cl 4) Окисление перманганатом калия: 3 H 2 C=CH 2 + 2 KMn. O 4 + 4 H 2 O → → 3 CH 2—CH 2 + 2 Mn. O 2 + KOH | OH
 5) Реакция полимеризации:
5) Реакция полимеризации:
 Получение алкенов: 1) Дегидратация спиртов (отщепление молекулы воды): H 2 SO 4 H−CH 2−OH → CH 2=CH 2 + H 2 O
Получение алкенов: 1) Дегидратация спиртов (отщепление молекулы воды): H 2 SO 4 H−CH 2−OH → CH 2=CH 2 + H 2 O