Алканы.ppt
- Количество слайдов: 19

Алканы 10 ен
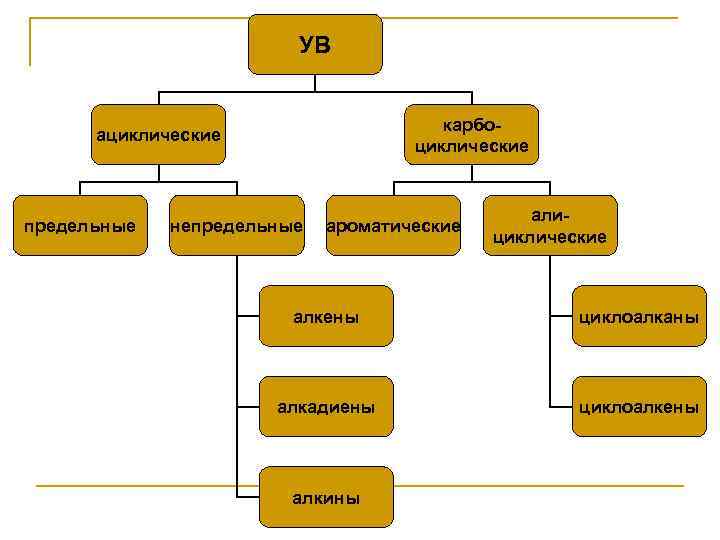
УВ карбоциклические ациклические предельные непредельные ароматические алициклические алкены циклоалканы алкадиены циклоалкены алкины

Строение n n n n sp 3 – гибридизация 4 гибридные орбитали угол между гибридными орбиталями - 109 º, 28' Расположение гибридных орбиталей – тетраэдрическое Длина С-С (σ – связи) – 0, 154 нм Нелинейная форма молекул (зигзагообразная цепь) Свободное вращение вокруг σ – связи
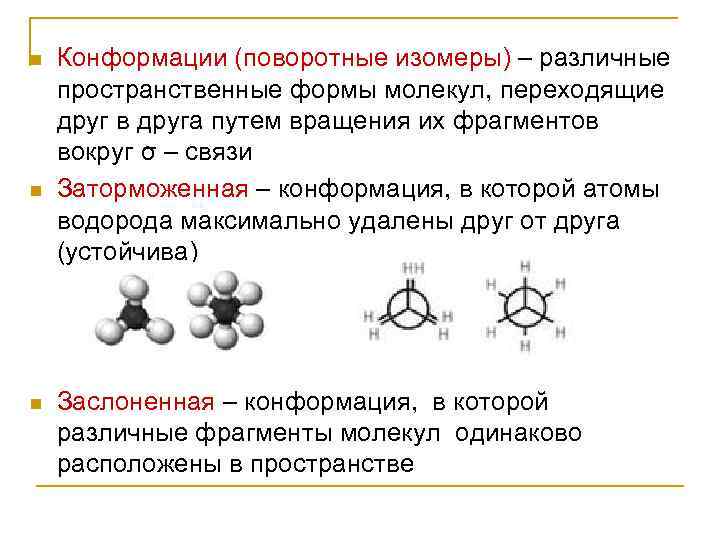
n n n Конформации (поворотные изомеры) – различные пространственные формы молекул, переходящие друг в друга путем вращения их фрагментов вокруг σ – связи Заторможенная – конформация, в которой атомы водорода максимально удалены друг от друга (устойчива) Заслоненная – конформация, в которой различные фрагменты молекул одинаково расположены в пространстве

Гомологический ряд алканов n n n n Сn. H 2 n+2 СН 4 – метан С 2 Н 6 – этан С 3 Н 8 – пропан С 4 Н 10 – бутан С 5 Н 12 – пентан С 6 Н 14 – гексан С 7 Н 16 – гептан С 8 Н 18 – октан С 9 Н 20 – нонан С 10 Н 22 – декан С 17 Н 36 - гептадекан С 20 Н 42 - эйкозан Гомологи – вещества, имеющие сходное строение и свойства, отличающиеся на одну или несколько групп СН 2 Группа СН 2 – гомологическая разность

Изомерия n n Изомеры – вещества, имеющие одинаковый состав, но разное строение и свойства Структурная изомерия (изомерия углеродного скелета) Чем больше углеродный скелет, тем больше изомеров С 5 Н 12 – 3 изомера (н-пентан, изопентан, неопентан)

Номенклатура n n n n Выбрать самую длинную углеродную цепь, как бы она ни была изогнута Пронумеровать эту выбранную цепь, начиная с того конца, к которому ближе радикал (заместитель) Сумма номеров атомов, около которых находятся радикалы (заместители) должна быть минимальной Назвать положения радикалов (заместителей) Назвать радикалы (заместители) (по алфавиту) Если радикалы одинаковы, то надо перечислить цифры, показывающие их положение; число одинаковых радикалов показывают приставкой ди-, три-, тетра- и т. д. Назвать главную (выбранную и пронумерованную) цепь

Изомерия и номенклатура предельных радикалов n n СН 3 - метил С 2 Н 5 - этил С 3 Н 7 - пропил и изопропил С 4 Н 9 - бутил, изобутил, втор-бутил, третбутил

Физические свойства n n n n n Низкие температуры кипения и плавления (из-за слабых ван-дер-вальсовых сил между молекулами) Практически не растворимы в воде и хорошо растворимы в органических растворителях (неполярность молекул) С ростом молекулярной массы температуры плавления и кипения увеличиваются (возрастание сил межмолекулярного взаимодействия) С 1 – С 4 – газы, С 5 – С 15 – жидкости, с С 16 – твердые вещества Температура кипения у разветвленных алканов меньше, чем у алканов нормального строения Температура плавления симметричных разветвленных алканов выше, чем у соотвествующих нормальных изомеров Метан, этан, твердые ув – без запапаха, жидкие ув – имеют характерный запах Легче воды Не смачиваются водой (неполярны)

Реакции замещения (SR) n n n Галогенирование (Cl 2, Br 2) Нагревание, освещение, органические пероксиды СН 4 + Сl 2 → CH 3 Cl + HCl CH 3 Cl + Cl 2 → CH 2 Cl 2 + HCl CH 2 Cl 2 + Cl 2 → CHCl 3 + HCl CHCl 3 + Cl 2 → CCl 4 + HCl

Механизм SR n n n Зарождение цепи – термо- или фотодиссоциация молекулы хлора на радикалы Cl 2 → 2 Cl· Развитие (рост) цепи – СН 4 + Cl· → CH 3· + HCl CH 3· + Cl 2 → CH 3 Cl + Cl· Цепные реакции – при которых образуются продукты, вызывающие их продолжение (Семенов, Нобелевская премия) Обрыв цепи – рекомбинация радикалов (израсходование реагентов, столкновение радикалов со стенками сосуда) СН 3· + СН 3· → С 2 Н 6; Сl · + Cl · → Cl 2

Особенности галогенирования гомологов метана n n n Легче всего идет замещение у третичных, затем у вторичных, затем у первичных атомов углерода (Е связи С-Н минимальна у третичного атома и максимальна у первичного) Бромирование идет селективно (избирательно) Пропан + Br 2 → 2 -бромпропан (97%) Хлорирование – менее селективно (большая реакционная способность хлора) Пропан + Cl 2 → 1 -хлорпропан (45%) + 2 хлорпропан (55%)
Нитрование (реакция Коновалова) n n n n Нитрование – замещение атома Н на нитрогруппу NO 2 (SR) Нагревание смеси алкана с разбавленной HNO 3 до t=140ºC CH 4 + HNO 3 → CH 3 NO 2 + H 2 O Термическая диссоциация HNO 3 → NO 2· + OH· Взаимодействие R c молекулами алканов СH 4 + OH· → CH 3· + H 2 O CH 3· + HONO 2 → CH 3 NO 2 + OH· Обрыв цепи – СH 3· + NO 2· → CH 3 NO 2; CH 3· + CH 3· → C 2 H 6

Сульфирование n n n Смесь концентрированной кислоты с серным ангидридом (олеум), нагревание Бутан + Н 2 SO 4 → 2 -сульфобутан 2 -метилбутан + Н 2 SO 4 → 2 -метил, 2 сульфобутан

Отщепление и разложение n n Дегидрирование (при нагревании до 400 -600ºС, kat – Ni, Pt, Pd, Cr 2 O 3) CH 3 – CH 2 – CH 3 → CH 2 = CH - CH 3 + Н 2 Циклизация и ароматизация (С 6 и >, t=500ºC, kat) C 6 H 14 → C 6 H 6 + 4 H 2 Пиролиз – разложение на простые вещества (при нагревании без доступа воздуха до 1000ºС) СН 4 → С + 2 Н 2 2 СН 4 → С 2 Н 2 + 3 Н 2 (t = 1200 - 1500ºC) Крекинг – термическое расщепление УВ с разрывом С-С связи (t=500 - 700ºC) СН 3 – СН 2 – СН 3 → СН 3 – СН 3 + СН 2 = СН 2

Окисление n n n Устойчивость к действию окислителей и кислорода воздуха при обычных условиях Горение С 4 Н 10 + 6, 5 О 2 → 4 СО 2 + 5 Н 2 О + Q 2 С 4 Н 10 + 13 О 2 → 8 СО 2 + 10 Н 2 О + Q Каталитическое окисление 2 С 4 Н 10 + 5 О 2 → 4 СН 3 СООН + 2 Н 2 О (200ºС, kat) CH 4 + O 2 → CH 3 OH, CH 2 O, HCOOH

Изомеризация n n n Изомеризация – превращение нормальных алканов в разветвленные (более стабильные) Катализатор – Al. Cl 3, t=100ºC C 5 H 12 → 2 -метилбутан, 2, 2 -диметилпропан

Получение n n Гидролиз карбида алюминия: Al 4 C 3 + 12 H 2 O → 4 Al(OH)3 + 3 CH 4 Гидрирование алкенов и алкинов (Pt, Pd, Ni): СН 2=СН 2 + Н 2 → СН 3 – СН 3 C 2 H 2 + 2 H 2 → C 2 H 6 Синтез Фишера – Тропша (t=200 -400ºC, kat – Fe, Co, Ni) – образование алканов неразветвленного строения n. CO + (2 n+1)H 2 → Cn. H 2 n+2 + n. H 2 O Гидролиз реактива Гриньяра RMg. Г + НОН → RH + Mg. OHГ СН 3 Mg. Cl + HOH → CH 4 + Mg. OHCl

Получение n n Реакция Вюрца 2 RCl + 2 Na → R – R + 2 Na. Cl 2 CH 3 Cl + 2 Na → CH 3 – CH 3 + 2 Na. Cl Cинтез Кольбе (электролиз водных растворов солей карбоновых кислот) 2 RCOONa + 2 H 2 O → R – R + 2 CO 2 + 2 Na. OH + H 2 2 CH 3 COONa + 2 H 2 O → CH 3 -CH 3 + 2 CO 2 + 2 Na. OH + H 2 Сплавление солей карбоновых кислот с твердыми щелочами CH 3 COONa + Na. OH → CH 4 + Na 2 CO 3 Прямой синтез из простых веществ (в вольтовой дуге между угольными электродами в атмосфере водорода) С + 2 Н 2 → СН 4
Алканы.ppt