Тема 2.4. Алкадиены.ppt
- Количество слайдов: 26
 Алкадиены: строение, номенклатура, гомологи, изомерия
Алкадиены: строение, номенклатура, гомологи, изомерия
 Алкадиены - ациклические углеводороды, содержащие в молекуле, две двойные связи между атомами углерода ¡ общая формула: Cn. H 2 n-2 ¡
Алкадиены - ациклические углеводороды, содержащие в молекуле, две двойные связи между атомами углерода ¡ общая формула: Cn. H 2 n-2 ¡
 Алкадиены с кумулированным расположением двойных связей (аллены) ¡ Углеводороды содержащие двойные связи , находящиеся возле соседних атомов углерода. 1 2 3 4 СН 2 =С=СН-СН 3 бутадиен -1, 2
Алкадиены с кумулированным расположением двойных связей (аллены) ¡ Углеводороды содержащие двойные связи , находящиеся возле соседних атомов углерода. 1 2 3 4 СН 2 =С=СН-СН 3 бутадиен -1, 2
 Сопряженные алкадиены ¡ Углеводороды содержащие двойные связи , между которыми находится одна одинарная связь. 1 2 3 4 5 6 СН 3 -СН=СН-СН 3 1 гексадиен-2, 4 2 3 4 СН 2 =СН-СН=СН 2 бутадиен -1, 3 (дивинил)
Сопряженные алкадиены ¡ Углеводороды содержащие двойные связи , между которыми находится одна одинарная связь. 1 2 3 4 5 6 СН 3 -СН=СН-СН 3 1 гексадиен-2, 4 2 3 4 СН 2 =СН-СН=СН 2 бутадиен -1, 3 (дивинил)
 Алкадиены с изолированными двойными связями ¡ Углеводороды содержащие двойные связи , между которыми находится несколько одинарных связей. 8 7 6 5 4 3 2 1 СН 3–СН 2 -СН=СН-СН 2 -СН=СН 2 октадиен-1, 5
Алкадиены с изолированными двойными связями ¡ Углеводороды содержащие двойные связи , между которыми находится несколько одинарных связей. 8 7 6 5 4 3 2 1 СН 3–СН 2 -СН=СН-СН 2 -СН=СН 2 октадиен-1, 5
 Номенклатура алкадиенов Правила: 1. Главная цепь должна содержать обе двойные связи. 2. Нумерацию ведут с того конца где ближе кратная связь. 3. Называют заместители и указывают атомы углерода от которого они отходят. 4. Указывают название алкадиена и атомы углерода от которых образована двойная связь.
Номенклатура алкадиенов Правила: 1. Главная цепь должна содержать обе двойные связи. 2. Нумерацию ведут с того конца где ближе кратная связь. 3. Называют заместители и указывают атомы углерода от которого они отходят. 4. Указывают название алкадиена и атомы углерода от которых образована двойная связь.
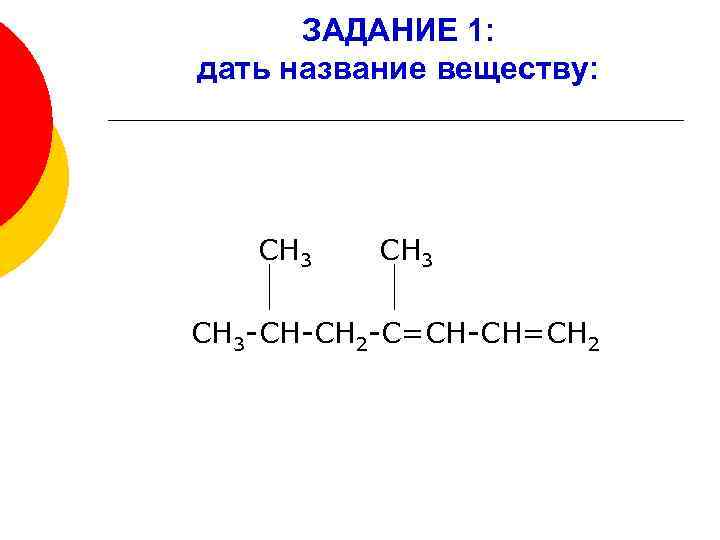 ЗАДАНИЕ 1: дать название веществу: СН 3 -СН-СН 2 -С=СН-СН=СН 2
ЗАДАНИЕ 1: дать название веществу: СН 3 -СН-СН 2 -С=СН-СН=СН 2
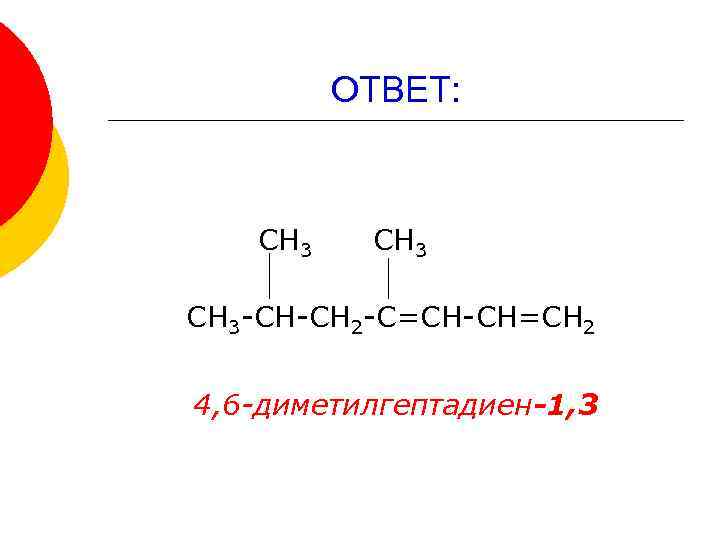 ОТВЕТ: СН 3 -СН-СН 2 -С=СН-СН=СН 2 4, 6 -диметилгептадиен-1, 3
ОТВЕТ: СН 3 -СН-СН 2 -С=СН-СН=СН 2 4, 6 -диметилгептадиен-1, 3
 ИЗОМЕРИЯ АЛКАДИЕНОВ 1. Структурная: а) изомерия углеродного скелета б) изомерия положения двойных связей. 2. Пространственная: а)цис-транс изомерия 3. Межклассовая изомерия (алкины)
ИЗОМЕРИЯ АЛКАДИЕНОВ 1. Структурная: а) изомерия углеродного скелета б) изомерия положения двойных связей. 2. Пространственная: а)цис-транс изомерия 3. Межклассовая изомерия (алкины)
 ИЗОМЕРИЯ АЛКАДИЕНОВ
ИЗОМЕРИЯ АЛКАДИЕНОВ
 ПОЛУЧЕНИЕ АЛКАДИЕНОВ Двухстадийное дегидрирование алканов СН 3 -СН 2 -СН 3 бутан СН 2=СН-СН=СН 2+2 Н 2 бутадиен -1, 3
ПОЛУЧЕНИЕ АЛКАДИЕНОВ Двухстадийное дегидрирование алканов СН 3 -СН 2 -СН 3 бутан СН 2=СН-СН=СН 2+2 Н 2 бутадиен -1, 3
 ХИМИЧЕСКИЕ СВОЙСТВА Галогенирование 1 (неполное) СН 2=СН-СН=СН 2 + Br 2 1, 2 - присоединение СН 2 -СН-СН=СН 2 Br Br 3, 4 – дибромбутен-1
ХИМИЧЕСКИЕ СВОЙСТВА Галогенирование 1 (неполное) СН 2=СН-СН=СН 2 + Br 2 1, 2 - присоединение СН 2 -СН-СН=СН 2 Br Br 3, 4 – дибромбутен-1
 ХИМИЧЕСКИЕ СВОЙСТВА Галогенирование 2 (неполное) СН 2=СН-СН=СН 2 + Br 2 1, 4 -присоединение СН 2 -СН=СН-СН 2 Br Br 1, 4 – дибромбутен-2
ХИМИЧЕСКИЕ СВОЙСТВА Галогенирование 2 (неполное) СН 2=СН-СН=СН 2 + Br 2 1, 4 -присоединение СН 2 -СН=СН-СН 2 Br Br 1, 4 – дибромбутен-2
 ХИМИЧЕСКИЕ СВОЙСТВА Галогенирование 3 (полное) СН 2=СН-СН=СН 2 + 2 Br 2 1, 2, 3, 4 -присоединение СН 2 -СН-СН-СН 2 Br Br 1, 2, 3, 4 – тетрабромбутан
ХИМИЧЕСКИЕ СВОЙСТВА Галогенирование 3 (полное) СН 2=СН-СН=СН 2 + 2 Br 2 1, 2, 3, 4 -присоединение СН 2 -СН-СН-СН 2 Br Br 1, 2, 3, 4 – тетрабромбутан
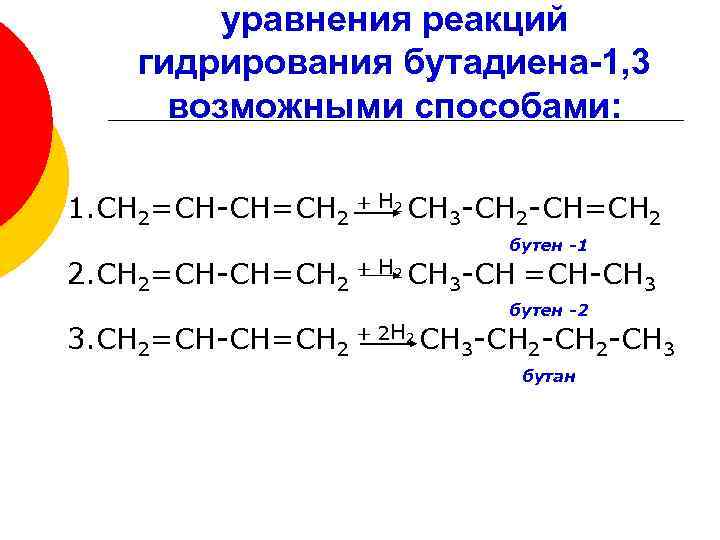 уравнения реакций гидрирования бутадиена-1, 3 возможными способами: 1. СН 2=СН-СН=СН 2 + Н 2 СН 3 -СН 2 -СН=СН 2 бутен -1 2. СН 2=СН-СН=СН 2 + Н 2 СН 3 -СН =СН-СН 3 бутен -2 3. СН 2=СН-СН=СН 2 + 2 Н 2 СН 3 -СН 2 -СН 3 бутан
уравнения реакций гидрирования бутадиена-1, 3 возможными способами: 1. СН 2=СН-СН=СН 2 + Н 2 СН 3 -СН 2 -СН=СН 2 бутен -1 2. СН 2=СН-СН=СН 2 + Н 2 СН 3 -СН =СН-СН 3 бутен -2 3. СН 2=СН-СН=СН 2 + 2 Н 2 СН 3 -СН 2 -СН 3 бутан
 ХИМИЧЕСКИЕ СВОЙСТВА Гидрогалогенирование (по правилу Марковникова) 1 стадия СН 2=СН-СН=СН 2 + НСI СН 3 -СН-СН=СН 2 СI 3 -хлорбутен -1
ХИМИЧЕСКИЕ СВОЙСТВА Гидрогалогенирование (по правилу Марковникова) 1 стадия СН 2=СН-СН=СН 2 + НСI СН 3 -СН-СН=СН 2 СI 3 -хлорбутен -1
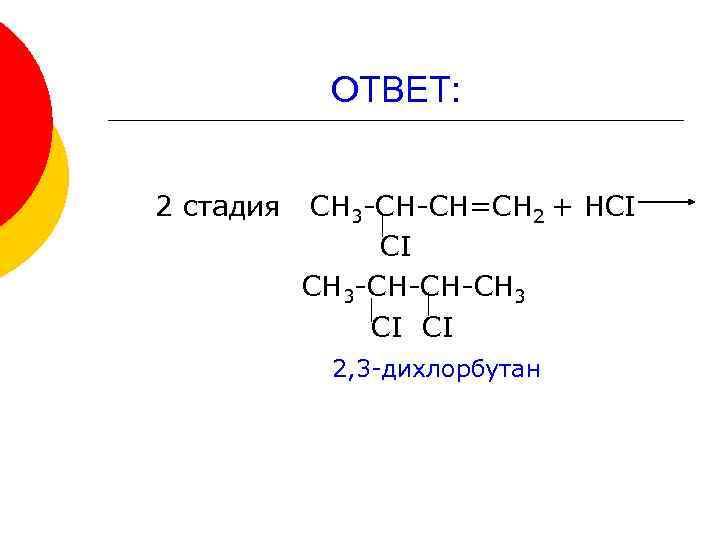 ОТВЕТ: 2 стадия СН 3 -СН-СН=СН 2 + НСI СI СН 3 -СН-СН-СН 3 СI СI 2, 3 -дихлорбутан
ОТВЕТ: 2 стадия СН 3 -СН-СН=СН 2 + НСI СI СН 3 -СН-СН-СН 3 СI СI 2, 3 -дихлорбутан
 ХИМИЧЕСКИЕ СВОЙСТВА Полимеризация диеновых УВ приводит к образованию каучуков – полимеров, обладающих высокой эластичностью. бутадиен -1, 3 бутадиеновый каучук
ХИМИЧЕСКИЕ СВОЙСТВА Полимеризация диеновых УВ приводит к образованию каучуков – полимеров, обладающих высокой эластичностью. бутадиен -1, 3 бутадиеновый каучук
 История открытия каучука ¡ Родина каучука – Центральная и Южная Америка. Во влажных жарких тропиках, по берегам реки Амазонки, растёт необычное дерево, которое называется бразильская гевея
История открытия каучука ¡ Родина каучука – Центральная и Южная Америка. Во влажных жарких тропиках, по берегам реки Амазонки, растёт необычное дерево, которое называется бразильская гевея
 История открытия каучука ¡ Если на коре дерева сделать надрез, то из ранки вытекает сок молочно-белого цвета, называемый латексом. На воздухе сок постепенно темнеет и затвердевает, превращаясь в резиноподобную смолу.
История открытия каучука ¡ Если на коре дерева сделать надрез, то из ранки вытекает сок молочно-белого цвета, называемый латексом. На воздухе сок постепенно темнеет и затвердевает, превращаясь в резиноподобную смолу.
 Синтетические каучуки ¡ Основателем первого в мире крупномасштабного производства синтетического каучука по праву считается русский ученый С. В. Лебедев.
Синтетические каучуки ¡ Основателем первого в мире крупномасштабного производства синтетического каучука по праву считается русский ученый С. В. Лебедев.
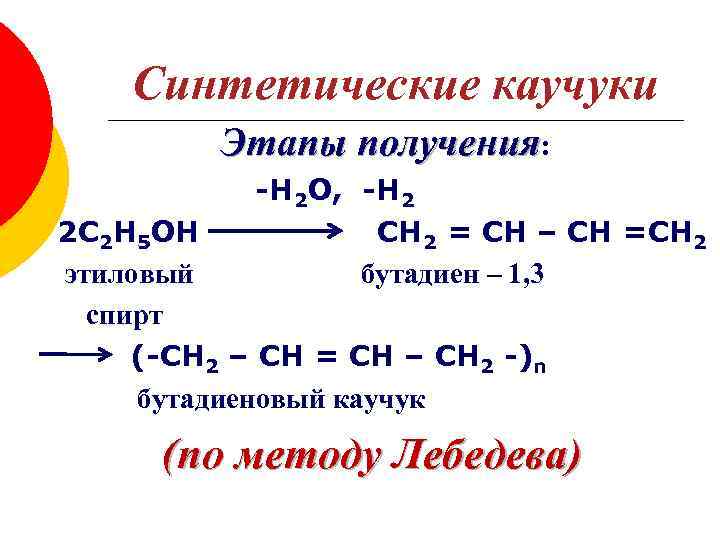 Синтетические каучуки Этапы получения: -Н 2 О, -Н 2 СН 2 = СН – СН =СН 2 бутадиен – 1, 3 2 С 2 Н 5 ОН этиловый спирт (-СН 2 – СН = СН – СН 2 -)n бутадиеновый каучук (по методу Лебедева)
Синтетические каучуки Этапы получения: -Н 2 О, -Н 2 СН 2 = СН – СН =СН 2 бутадиен – 1, 3 2 С 2 Н 5 ОН этиловый спирт (-СН 2 – СН = СН – СН 2 -)n бутадиеновый каучук (по методу Лебедева)
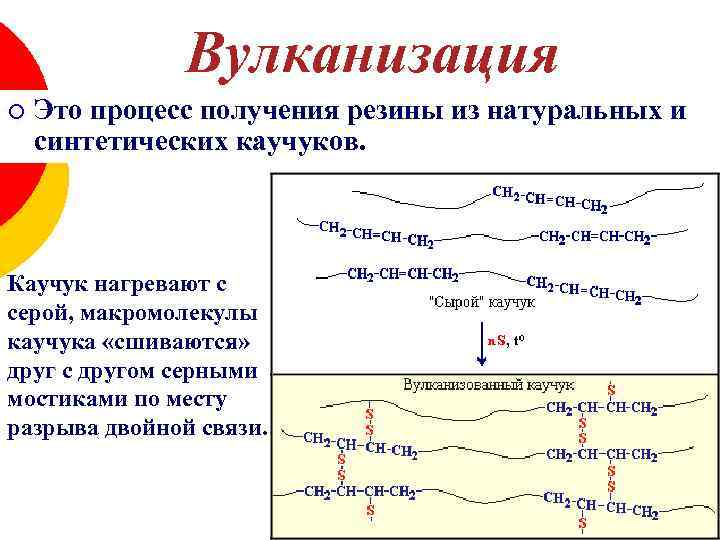 Вулканизация ¡ Это процесс получения резины из натуральных и синтетических каучуков. Каучук нагревают с серой, макромолекулы каучука «сшиваются» друг с другом серными мостиками по месту разрыва двойной связи.
Вулканизация ¡ Это процесс получения резины из натуральных и синтетических каучуков. Каучук нагревают с серой, макромолекулы каучука «сшиваются» друг с другом серными мостиками по месту разрыва двойной связи.
 Применение
Применение
 СПАСИБО ЗА Внимание!!!
СПАСИБО ЗА Внимание!!!
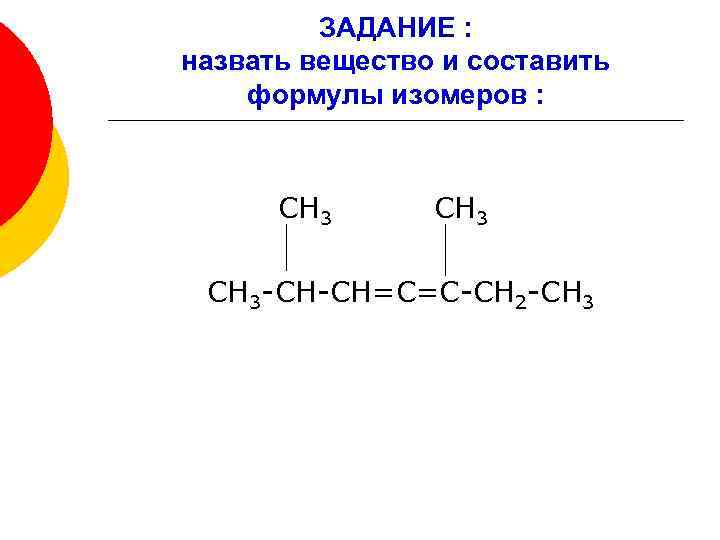 ЗАДАНИЕ : назвать вещество и составить формулы изомеров : СН 3 -СН-СН=С=С-СН 2 -СН 3
ЗАДАНИЕ : назвать вещество и составить формулы изомеров : СН 3 -СН-СН=С=С-СН 2 -СН 3


