6. Алкадиены. Каучуки.ppt
- Количество слайдов: 23
 Алкадиены. Каучуки
Алкадиены. Каучуки
 План изучения класса веществ 1. Состав и строение 2. Номенклатура и изомерия 3. Физические свойства 4. Химические свойства 5. Способы получения 6. Направления применения
План изучения класса веществ 1. Состав и строение 2. Номенклатура и изомерия 3. Физические свойства 4. Химические свойства 5. Способы получения 6. Направления применения
 1. Состав и строение Алкадиены – ациклические непредельные углеводороды, содержащие в молекуле двойные связи между атомами углерода. Общая формула Сn. H 2 n-2
1. Состав и строение Алкадиены – ациклические непредельные углеводороды, содержащие в молекуле двойные связи между атомами углерода. Общая формула Сn. H 2 n-2
 Три вида алкадиенов: 1) с кумулированным расположением двойных связей СН 2=С=СН–СН 3 2) с сопряженным расположением двойных связей СН 2=СН–СН 3 3) с изолированным расположением двойных связей СН 2=СН– СН 2–СН=СН 2
Три вида алкадиенов: 1) с кумулированным расположением двойных связей СН 2=С=СН–СН 3 2) с сопряженным расположением двойных связей СН 2=СН–СН 3 3) с изолированным расположением двойных связей СН 2=СН– СН 2–СН=СН 2
 2. Изомерия углеродного скелета: СН 2=СН–СН 2–СН=СН–СН 3 гексадиен-1, 4 СН 2=СН–СН–СН=СН 2 3 -метилпентадиен-1, 4 СН 3 Изомерия положения кратных связей СН 2=СН–СН 3 пентадиен – 1, 3 СН 2= СН– СН 2–СН= СН 2 пентадиен – 1, 4
2. Изомерия углеродного скелета: СН 2=СН–СН 2–СН=СН–СН 3 гексадиен-1, 4 СН 2=СН–СН–СН=СН 2 3 -метилпентадиен-1, 4 СН 3 Изомерия положения кратных связей СН 2=СН–СН 3 пентадиен – 1, 3 СН 2= СН– СН 2–СН= СН 2 пентадиен – 1, 4
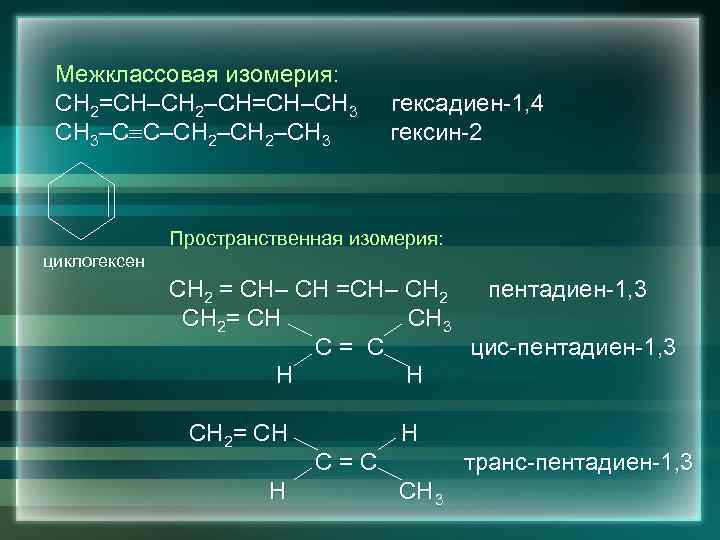 Межклассовая изомерия: СН 2=СН–СН 2–СН=СН–СН 3–С С–СН 2–СН 3 гексадиен-1, 4 гексин-2 Пространственная изомерия: циклогексен СН 2 = СН– СН =СН– СН 2 пентадиен-1, 3 СН 2= СН СН 3 С= С цис-пентадиен-1, 3 Н Н СН 2= СН Н Н С=С транс-пентадиен-1, 3 СН 3
Межклассовая изомерия: СН 2=СН–СН 2–СН=СН–СН 3–С С–СН 2–СН 3 гексадиен-1, 4 гексин-2 Пространственная изомерия: циклогексен СН 2 = СН– СН =СН– СН 2 пентадиен-1, 3 СН 2= СН СН 3 С= С цис-пентадиен-1, 3 Н Н СН 2= СН Н Н С=С транс-пентадиен-1, 3 СН 3
 3. Физические свойства Бутадиен-1, 3 является бесцветным газом (t кип. = -4, 5 С°) с характерным запахом. Изопрен – летучая жидкость (t кип. = 34, 1 С°), обладает приятным запахом.
3. Физические свойства Бутадиен-1, 3 является бесцветным газом (t кип. = -4, 5 С°) с характерным запахом. Изопрен – летучая жидкость (t кип. = 34, 1 С°), обладает приятным запахом.
 4. Химические свойства Реакции присоединения 1, 2 присоединение: СН 2=СН –СН =СН 2 + Сl 2 СН 2 Cl – СН = СН 2 1, 4 присоединение: СН 2 = СН – СН = СН 2 + Сl 2 СН 2 Cl – СН = СН – СН 2 Cl
4. Химические свойства Реакции присоединения 1, 2 присоединение: СН 2=СН –СН =СН 2 + Сl 2 СН 2 Cl – СН = СН 2 1, 4 присоединение: СН 2 = СН – СН = СН 2 + Сl 2 СН 2 Cl – СН = СН – СН 2 Cl
 Реакции гидрирования 1, 2 присоединение: СН 2=СН–СН =СН 2+ Н 2 СН 3–СН 2–СН=СН 2 СН 3–СН 2–СН 3 бутан 1, 4 присоединение: СН 2=СН–СН=СН 2 2[Н] СН 3–СН=СН–СН 3 бутен-2
Реакции гидрирования 1, 2 присоединение: СН 2=СН–СН =СН 2+ Н 2 СН 3–СН 2–СН=СН 2 СН 3–СН 2–СН 3 бутан 1, 4 присоединение: СН 2=СН–СН=СН 2 2[Н] СН 3–СН=СН–СН 3 бутен-2
 Проверим себя СН 2=СН–СН=СН 2 + HBr СН 3–СНBr–СН=СН 2 3 -бромбутен-1 (1, 2 присоединение) СН 2=СН–СН=СН 2 + HBr СН 2 Br–СН=СН–СН 3 1 -бромбутен-2 (1, 4 присоединение)
Проверим себя СН 2=СН–СН=СН 2 + HBr СН 3–СНBr–СН=СН 2 3 -бромбутен-1 (1, 2 присоединение) СН 2=СН–СН=СН 2 + HBr СН 2 Br–СН=СН–СН 3 1 -бромбутен-2 (1, 4 присоединение)
 Реакции полимеризации n. СН 2=СН–СН=СН 2 (–СН 2–СН=СН–СН 2–)n бутадиен-1, 3 бутадиеновый каучук n. СН 2=С–СН=СН 2 (–СН 2– С = СН –СН 2–) n СН 3 изопреновый каучук
Реакции полимеризации n. СН 2=СН–СН=СН 2 (–СН 2–СН=СН–СН 2–)n бутадиен-1, 3 бутадиеновый каучук n. СН 2=С–СН=СН 2 (–СН 2– С = СН –СН 2–) n СН 3 изопреновый каучук
 Проверим себя n. СН 2=С–СН=СН 2 (–СН 2–С=СН–СН 2–) Сl Сl хлоропреновый каучук
Проверим себя n. СН 2=С–СН=СН 2 (–СН 2–С=СН–СН 2–) Сl Сl хлоропреновый каучук
 Свойства синтетических каучуков Разновидности синтетических каучуков Бутадиеновый Хлоропреновый Изопреновый Бутадиен - стирольный Свойства каучуков Высокая износостойкость, устойчивость к многократным деформациям Высокая устойчивость к органическим растворителям, кислотам, щелочам, нефтепродуктам Синтетический аналог натурального каучука Высокая прочность
Свойства синтетических каучуков Разновидности синтетических каучуков Бутадиеновый Хлоропреновый Изопреновый Бутадиен - стирольный Свойства каучуков Высокая износостойкость, устойчивость к многократным деформациям Высокая устойчивость к органическим растворителям, кислотам, щелочам, нефтепродуктам Синтетический аналог натурального каучука Высокая прочность
 Знакомство европейцев с каучуком
Знакомство европейцев с каучуком
 Вулканизация —процесс взаимодействия каучуков с вулканизующим агентом (сера, пероксиды, оксиды металлов), при котором происходит сшивание молекул каучука в единую пространственную сетку. Этот процесс назван в честь Вулкана, древнеримского бога огня.
Вулканизация —процесс взаимодействия каучуков с вулканизующим агентом (сера, пероксиды, оксиды металлов), при котором происходит сшивание молекул каучука в единую пространственную сетку. Этот процесс назван в честь Вулкана, древнеримского бога огня.
 История изобретения резины
История изобретения резины
 5. Способы получения Дегидрирование: С 4 Н 10 600˚С, Al 2 O 3, Cr 2 O 3 СН 3–СH–СН 2–СН 3 t, Al 2 O 3, Cr 2 O 3 Al 2 Cr 2 СН 2=СН–СН=СН 2 + 2 Н 2 бутадиен-1, 3 СН 2= С–СН=СН 2 + 2 Н 2 СН 3 изопрен (2 -метилбутадиен-1, 3)
5. Способы получения Дегидрирование: С 4 Н 10 600˚С, Al 2 O 3, Cr 2 O 3 СН 3–СH–СН 2–СН 3 t, Al 2 O 3, Cr 2 O 3 Al 2 Cr 2 СН 2=СН–СН=СН 2 + 2 Н 2 бутадиен-1, 3 СН 2= С–СН=СН 2 + 2 Н 2 СН 3 изопрен (2 -метилбутадиен-1, 3)
 Способы получения Дегидратация и дегидрирование спиртов (метод Лебедева): С 2 Н 5 ОН 400 -500 °С, Al 2 O 3, Zn. O СН 2=СН–СН=СН 2+ +2 Н 2 O + Н 2 Дегидрогалогенирование: Cl–СН 2–СH–СН 2–Cl + 2 KOH 600˚С, Zn. O, Mg. O СН 2 = СН–СН = СН 2 + 2 KCl + 2 Н 2 O
Способы получения Дегидратация и дегидрирование спиртов (метод Лебедева): С 2 Н 5 ОН 400 -500 °С, Al 2 O 3, Zn. O СН 2=СН–СН=СН 2+ +2 Н 2 O + Н 2 Дегидрогалогенирование: Cl–СН 2–СH–СН 2–Cl + 2 KOH 600˚С, Zn. O, Mg. O СН 2 = СН–СН = СН 2 + 2 KCl + 2 Н 2 O
 Свойства и применение резины Резина для обуви (в том числе и для подошв обуви) Баскетбольный мяч Резиновые перчатки Низкая газои водопроницаемость Устойчивость к действию агрессивных сред Эластичность Хорошие электроизоляционные свойства Шланги и трубы для двигателей Обмотка электрических кабелей Изготовление шин
Свойства и применение резины Резина для обуви (в том числе и для подошв обуви) Баскетбольный мяч Резиновые перчатки Низкая газои водопроницаемость Устойчивость к действию агрессивных сред Эластичность Хорошие электроизоляционные свойства Шланги и трубы для двигателей Обмотка электрических кабелей Изготовление шин
 Упражнения для закрепления Осуществите цепочки превращений: • 1 уровень С 2 Н 6 С 2 Н 5 Cl С 4 Н 10 С 4 Н 6 Каt, t бутадиеновый каучук • 2 уровень Са. С 2 Н 2 С 2 Н 6 С 2 Н 5 Cl С 5 Н 12 Al. Cl 3, t X Каt, t Y Каt, t изопрен
Упражнения для закрепления Осуществите цепочки превращений: • 1 уровень С 2 Н 6 С 2 Н 5 Cl С 4 Н 10 С 4 Н 6 Каt, t бутадиеновый каучук • 2 уровень Са. С 2 Н 2 С 2 Н 6 С 2 Н 5 Cl С 5 Н 12 Al. Cl 3, t X Каt, t Y Каt, t изопрен
 Проверим себя 1 уровень: 1. СН 3–СН 3 +Сl 2 СН 3–СН 2 Cl + HCl 2. 2 СН 3–СН 2 Cl +2 Na СН 3–СН 2 –СН 3 +2 Na. Cl 3. СН 3–СН 2 –СН 3 Pt, t СН 2=СН –СН =СН 2 + 2 Н 2 4. СН 2=СН –СН =СН 2 Pt, t (– СН 2 – СН =СН – СН 2 –)n
Проверим себя 1 уровень: 1. СН 3–СН 3 +Сl 2 СН 3–СН 2 Cl + HCl 2. 2 СН 3–СН 2 Cl +2 Na СН 3–СН 2 –СН 3 +2 Na. Cl 3. СН 3–СН 2 –СН 3 Pt, t СН 2=СН –СН =СН 2 + 2 Н 2 4. СН 2=СН –СН =СН 2 Pt, t (– СН 2 – СН =СН – СН 2 –)n
 Проверим себя 2 уровень: 1. Са. С 2 + H 2 O СН СН + Ca(OH)2 2. СН СН + 2 H 2 Ni, t СН 3–СН 3 3. СН 3–СН 3 +Сl 2 СН 3–СН 2 Cl + HCl 4. СН 3–СН 2 Cl +2 Na СН 3–СН 2 –СН 3 +2 Na. Cl 5. СН 3–СН 2 –СН 3 Al. Cl 3, t СН 3–СН 2–СН 3 6. СН 3–СН 2–СН 3 Pt, t СН 2=С –СН=СН 2 + 2 Н 2 СН 3 7. СН 2=С –СН=СН 2 Pt, t (– СН 2 – С = СН – СН 2 – ) n СН 3
Проверим себя 2 уровень: 1. Са. С 2 + H 2 O СН СН + Ca(OH)2 2. СН СН + 2 H 2 Ni, t СН 3–СН 3 3. СН 3–СН 3 +Сl 2 СН 3–СН 2 Cl + HCl 4. СН 3–СН 2 Cl +2 Na СН 3–СН 2 –СН 3 +2 Na. Cl 5. СН 3–СН 2 –СН 3 Al. Cl 3, t СН 3–СН 2–СН 3 6. СН 3–СН 2–СН 3 Pt, t СН 2=С –СН=СН 2 + 2 Н 2 СН 3 7. СН 2=С –СН=СН 2 Pt, t (– СН 2 – С = СН – СН 2 – ) n СН 3
 Домашнее задание § 5, рабочая тетрадь, стр. 33, № 2, 3, 5 , 6.
Домашнее задание § 5, рабочая тетрадь, стр. 33, № 2, 3, 5 , 6.


