 Алена Солдаткина Кремний (Silicium)
Алена Солдаткина Кремний (Silicium)
 Кремний Кремнос (греч. ) – утёс, скала Силекс (лат. ) - кремень Кре мний — элемент главной подгруппы четвёртой группы третьего периода периодической системы химических элементов Д. И. Менделеева, с атомным номером 14. Обозначается символом Si (лат. Silicium), неметалл.
Кремний Кремнос (греч. ) – утёс, скала Силекс (лат. ) - кремень Кре мний — элемент главной подгруппы четвёртой группы третьего периода периодической системы химических элементов Д. И. Менделеева, с атомным номером 14. Обозначается символом Si (лат. Silicium), неметалл.
 Строение атома кремния
Строение атома кремния
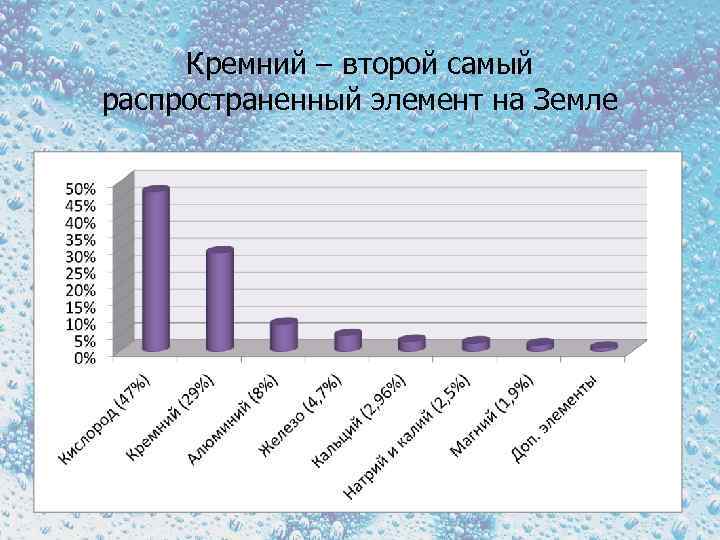 Кремний – второй самый распространенный элемент на Земле
Кремний – второй самый распространенный элемент на Земле
 История получения 1) В 1811 году французскими учёными Жозефом Луи Гей-Люссаком и Луи Жаком Тенаром. 2) В 1825 году шведский химик Йёнс Якоб Берцелиус Новому элементу было дано название «силиций» (от лат. silex — кремень)
История получения 1) В 1811 году французскими учёными Жозефом Луи Гей-Люссаком и Луи Жаком Тенаром. 2) В 1825 году шведский химик Йёнс Якоб Берцелиус Новому элементу было дано название «силиций» (от лат. silex — кремень)
 Нахождение в природе 1) Si. O 2 – кремнезём, самое распространённое соединение 2) Si. O 2 – кварцевый песок 3) яшма, опал, аметист, агат, сердолик, халцедон 4) силикаты: гранит, некоторые глины, слюда, асбест 5) Si. O 2 – входит в состав клеток растений и животных
Нахождение в природе 1) Si. O 2 – кремнезём, самое распространённое соединение 2) Si. O 2 – кварцевый песок 3) яшма, опал, аметист, агат, сердолик, халцедон 4) силикаты: гранит, некоторые глины, слюда, асбест 5) Si. O 2 – входит в состав клеток растений и животных
 Физические свойства 1) твёрдое кристаллическое вещество тёмно-серого цвета с металлическим блеском 2) имеет атомную кристаллическую решётку, как у алмаза 3) полупроводник
Физические свойства 1) твёрдое кристаллическое вещество тёмно-серого цвета с металлическим блеском 2) имеет атомную кристаллическую решётку, как у алмаза 3) полупроводник
 Химические свойства 1. Реагирует с кислородом (при t) Si + O 2 = Si. O 2 2. Реагирует с металлами (при t) Si + 2 Mg = Mg 2 Si силицид магния Mg 2 Si + 4 HCl = 2 Mg. Cl 2 + Si. H 4 ↑ силан Si. H 4 + 2 O 2 = Si. O 2 + 2 H 2 O 3. Реагирует с растворами щелочей Si + 2 Na. OH + H 2 O = Na 2 Si. O 3 + 2 H 2
Химические свойства 1. Реагирует с кислородом (при t) Si + O 2 = Si. O 2 2. Реагирует с металлами (при t) Si + 2 Mg = Mg 2 Si силицид магния Mg 2 Si + 4 HCl = 2 Mg. Cl 2 + Si. H 4 ↑ силан Si. H 4 + 2 O 2 = Si. O 2 + 2 H 2 O 3. Реагирует с растворами щелочей Si + 2 Na. OH + H 2 O = Na 2 Si. O 3 + 2 H 2
 Получение кремния Si. O 2 + 2 Mg = 2 Mg. O + Si Si. O 2 + 2 C = 2 CO + Si
Получение кремния Si. O 2 + 2 Mg = 2 Mg. O + Si Si. O 2 + 2 C = 2 CO + Si
 Соединения кремния Si. O 2 – диоксид кремния, кислотный оксид твёрдое кристаллическое вещество с атомной решёткой не взаимодействует с водой
Соединения кремния Si. O 2 – диоксид кремния, кислотный оксид твёрдое кристаллическое вещество с атомной решёткой не взаимодействует с водой
 Свойства Si. O 2 1. При спекании реагирует оксидами Ме или с карбонатами, с образованием силикатов Si. O 2 + Ca. O = Ca. Si. O 3 Si. O 2 + Ca. CO 3 = Ca. Si. O 3 + CO 2 2. Реагирует с щелочами Si. O 2 + 2 Na. OH = Na 2 Si. O 3 + H 2 O
Свойства Si. O 2 1. При спекании реагирует оксидами Ме или с карбонатами, с образованием силикатов Si. O 2 + Ca. O = Ca. Si. O 3 Si. O 2 + Ca. CO 3 = Ca. Si. O 3 + CO 2 2. Реагирует с щелочами Si. O 2 + 2 Na. OH = Na 2 Si. O 3 + H 2 O
 Соединения кремния H 2 Si. O 3 – кремниевая кислота, двухосновная, кислородсодержащая, слабая H 2 Si. O 3 = H 2 O + Si. O 2 нерастворима в воде (силикагель) образуется действием кислот на силикаты Na 2 Si. O 3 + 2 HCl = 2 Na. Cl + H 2 Si. O 3 / Si. O 2 H 2 O
Соединения кремния H 2 Si. O 3 – кремниевая кислота, двухосновная, кислородсодержащая, слабая H 2 Si. O 3 = H 2 O + Si. O 2 нерастворима в воде (силикагель) образуется действием кислот на силикаты Na 2 Si. O 3 + 2 HCl = 2 Na. Cl + H 2 Si. O 3 / Si. O 2 H 2 O
 Качественная реакция на растворимые силикаты: 1. действие щелочей 2. действие раствора аммиака 3. действие сильных кислот 4. термическое разложение
Качественная реакция на растворимые силикаты: 1. действие щелочей 2. действие раствора аммиака 3. действие сильных кислот 4. термическое разложение