Введение в клеточные технологии 2013.ppt
- Количество слайдов: 31

Алексей Юрьевич Лупатов, к. б. н. ,

Клеточные технологии входят в перечень критических технологий в рамках Приоритетных направлений развития науки, технологий и техники Российской Федерации (утв. Президентом Российской Федерации 21 мая 2006 г. Пр-842). Клеточные технологии предполагают манипуляции с эукариотическими клетками многоклеточных организмов в культуре Клеточные технологии Производство вакцин, моноклональных антител и других биопрепаратов с помощью клетокпродуцентов, тестирование фармакологических препаратов Клеточная и тканевая инженерия Клонирование Клеточная терапия Лупатов А. Ю

Как выращивают клетки ? (материалы) раньше сейчас Лупатов А. Ю
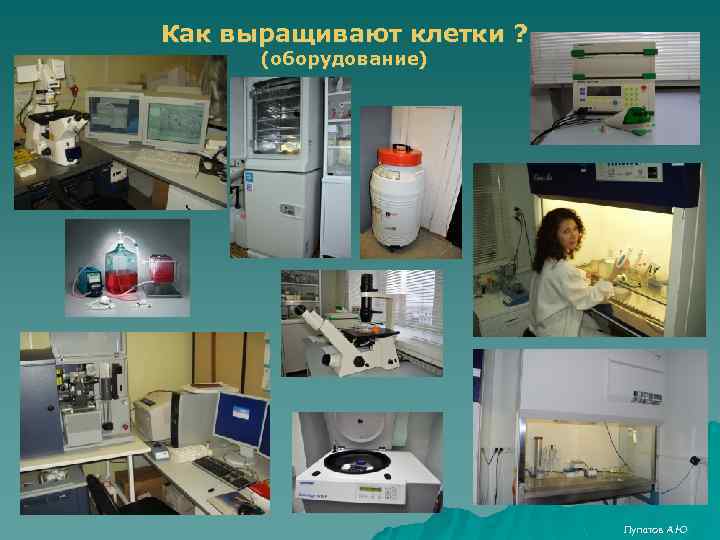
Как выращивают клетки ? (оборудование) Лупатов А. Ю

Клонирование – технология, позволяющая воспроизводить генетически однородные организмы. Естественным путем процесс происходит при делении одноклеточных организмов, партеногенезе, вегетативном размножении, появлении однозиготных близнецов (от греческого «klon» - веточка или черенок, с помощью которых осуществляется вегетативное размножение растений). Виды клонирования • Молекулярное клонирование • Клонирование микроорганизмов • Клонирование клеток в культуре • Эмбриональное клонирование • Репродуктивное клонирование • Терапевтическое клонирование Лупатов А. Ю
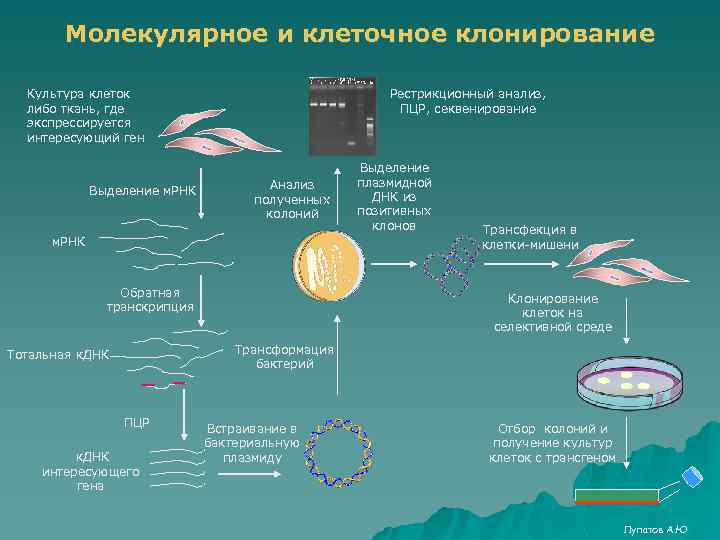
Молекулярное и клеточное клонирование Культура клеток либо ткань, где экспрессируется интересующий ген Выделение м. РНК Рестрикционный анализ, ПЦР, секвенирование Анализ полученных колоний м. РНК Обратная транскрипция Выделение плазмидной ДНК из позитивных клонов Трансфекция в клетки-мишени Клонирование клеток на селективной среде Трансформация бактерий Тотальная к. ДНК ПЦР к. ДНК интересующего гена Встраивание в бактериальную плазмиду Отбор колоний и получение культур клеток с трансгеном Лупатов А. Ю

Стволовые клетки Стволовая клетка – это клетка, способная претерпевать асимметричное деление, в результате которого образуется одна клетка, идентичная материнской, и вторая клетка, вступившая на путь дифференцировки. Тотипотентные стволовые клетки способны образовывать любые ткани организма (зигота, дробление до 8 бластомеров). Плюрипотентные стоволовые клетки способны дифференцироваться в клетки всех трех зародышевых листков и образовывать любые ткани организма кроме плаценты и зародышевой оболочки. К ним относятся клетки внутренней клеточной массы бластоцисты (эмбриональные стволовые клетки), примордиальные герминальные клетки, искусственно репрограммированные клетки. Мультипотентные и олигопотентные стволовые клетки способны дифференцироваться в клетки нескольких или одного зародышевого листка (мезенхимальные стволовые клетки из костного мозга, жировой ткани или пуповины; гемопоэтические стволовые клетки). Присутствуют как в эмбрионе, так и во взрослом организме (региональные стволовые клетки). Унипотентные стволовые клетки способны дифференцироваться в клетки определенного цитофенотипа (стволовые клетки кожи и др. ) Лупатов А. Ю
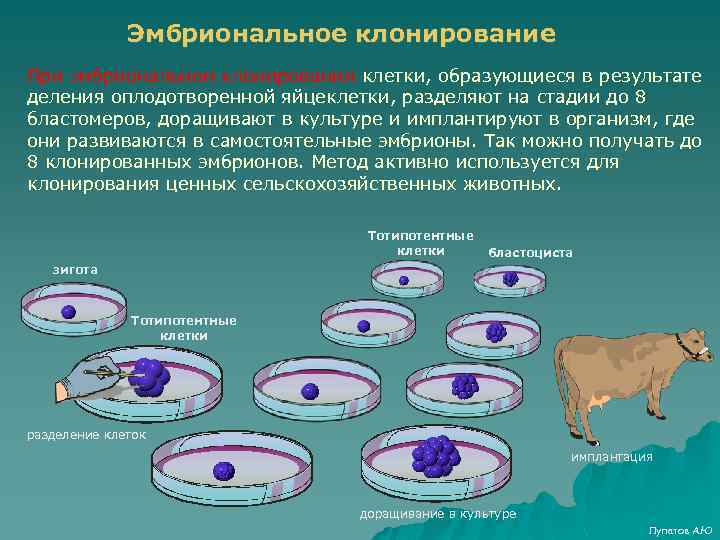
Эмбриональное клонирование При эмбриональном клонировании клетки, образующиеся в результате деления оплодотворенной яйцеклетки, разделяют на стадии до 8 бластомеров, доращивают в культуре и имплантируют в организм, где они развиваются в самостоятельные эмбрионы. Так можно получать до 8 клонированных эмбрионов. Метод активно используется для клонирования ценных сельскохозяйственных животных. Тотипотентные клетки бластоциста зигота Тотипотентные клетки разделение клеток имплантация доращивание в культуре Лупатов А. Ю

Репродуктивное клонирование – это клонирование организмов, находящихся на постнатальной стадии развития. При сохранности биологического материала возможно клонирование уже умерших организмов. First dog clone (Afghan Hound) Лупатов А. Ю
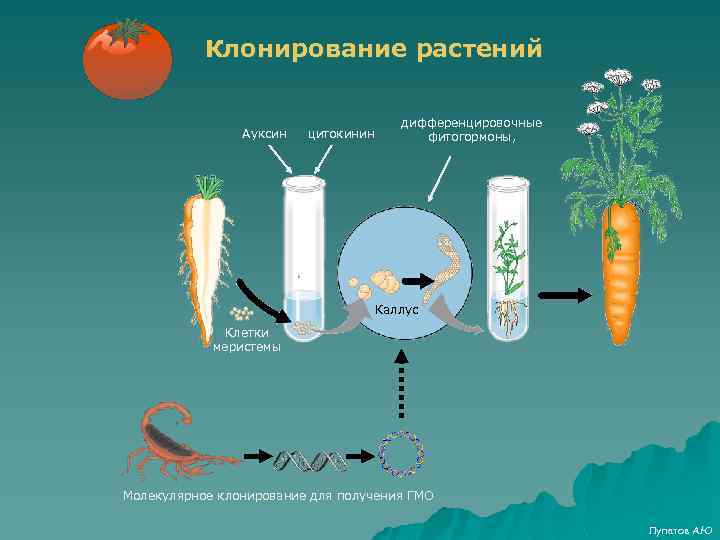
Клонирование растений Ауксин цитокинин дифференцировочные фитогормоны, Каллус Клетки меристемы Молекулярное клонирование для получения ГМО Лупатов А. Ю
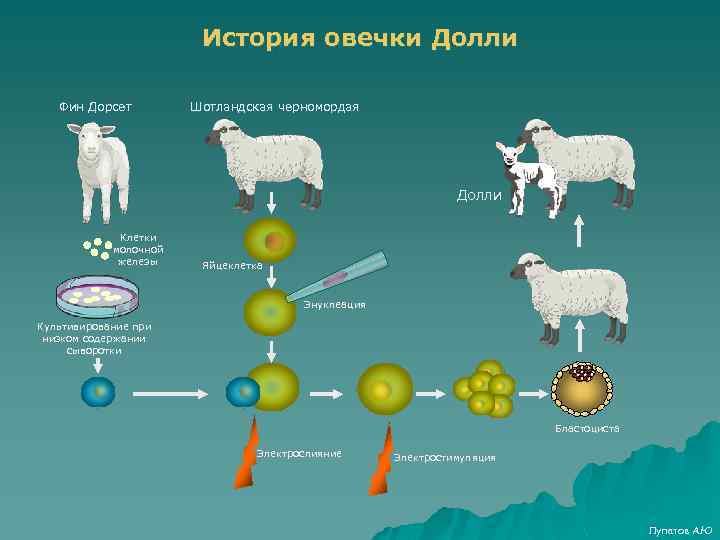
История овечки Долли Фин Дорсет Шотландская черномордая Долли Клетки молочной железы Яйцеклетка Энуклеация Культивирование при низком содержании сыворотки Бластоциста Электрослияние Электростимуляция Лупатов А. Ю
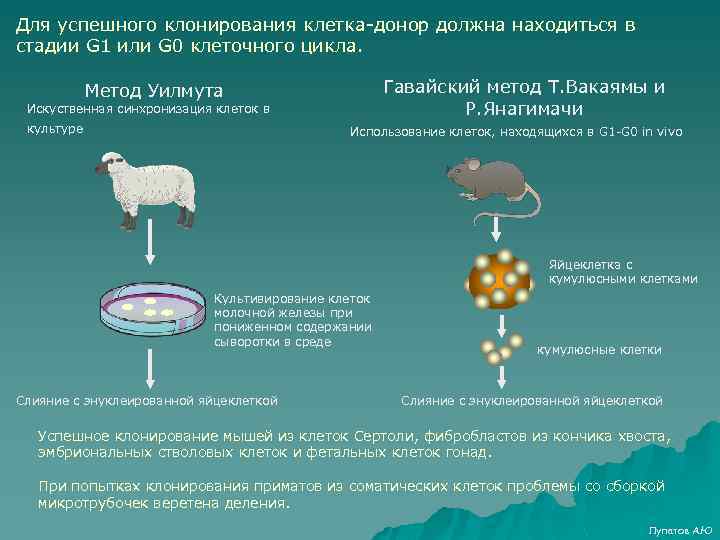
Для успешного клонирования клетка-донор должна находиться в стадии G 1 или G 0 клеточного цикла. Гавайский метод Т. Вакаямы и Р. Янагимачи Метод Уилмута Искуственная синхронизация клеток в культуре Использование клеток, находящихся в G 1 -G 0 in vivo Яйцеклетка с кумулюсными клетками Культивирование клеток молочной железы при пониженном содержании сыворотки в среде Слияние с энуклеированной яйцеклеткой кумулюсные клетки Слияние с энуклеированной яйцеклеткой Успешное клонирование мышей из клеток Сертоли, фибробластов из кончика хвоста, эмбриональных стволовых клеток и фетальных клеток гонад. При попытках клонирования приматов из соматических клеток проблемы со сборкой микротрубочек веретена деления. Лупатов А. Ю
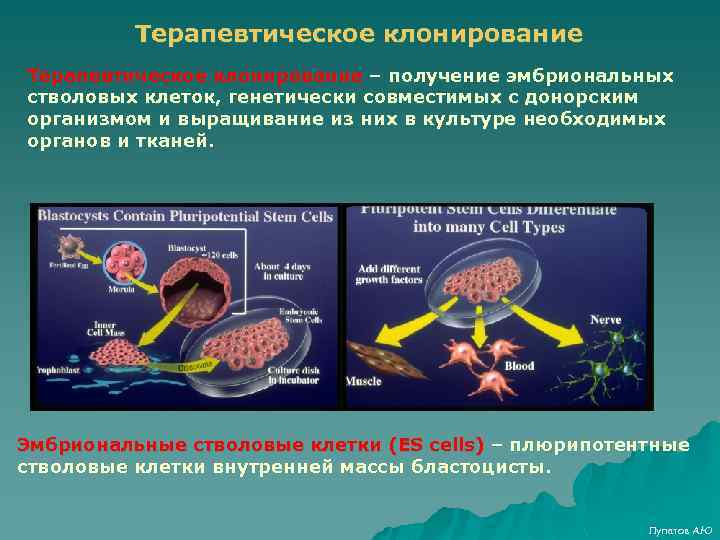
Терапевтическое клонирование – получение эмбриональных стволовых клеток, генетически совместимых с донорским организмом и выращивание из них в культуре необходимых органов и тканей. Эмбриональные стволовые клетки (ES cells) – плюрипотентные стволовые клетки внутренней массы бластоцисты. Лупатов А. Ю
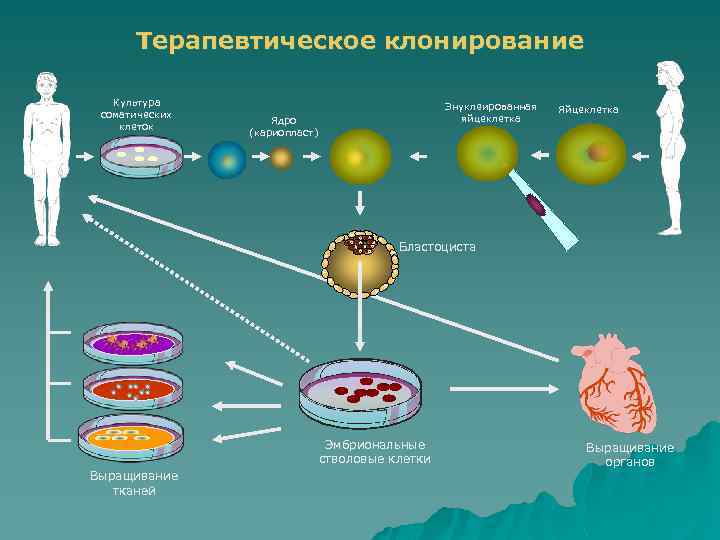
Терапевтическое клонирование Культура соматических клеток Энуклеированная яйцеклетка Ядро (кариопласт) Яйцеклетка Бластоциста Эмбриональные стволовые клетки Выращивание тканей Выращивание органов
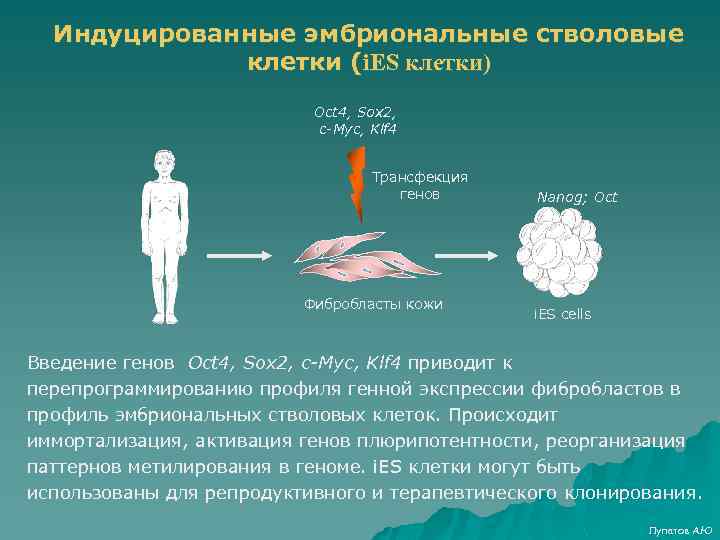
Индуцированные эмбриональные стволовые клетки (i. ES клетки) Oct 4, Sox 2, c-Myc, Klf 4 Трансфекция генов Фибробласты кожи Nanog; Oct i. ES cells Введение генов Oct 4, Sox 2, c-Myc, Klf 4 приводит к перепрограммированию профиля генной экспрессии фибробластов в профиль эмбриональных стволовых клеток. Происходит иммортализация, активация генов плюрипотентности, реорганизация паттернов метилирования в геноме. i. ES клетки могут быть использованы для репродуктивного и терапевтического клонирования. Лупатов А. Ю
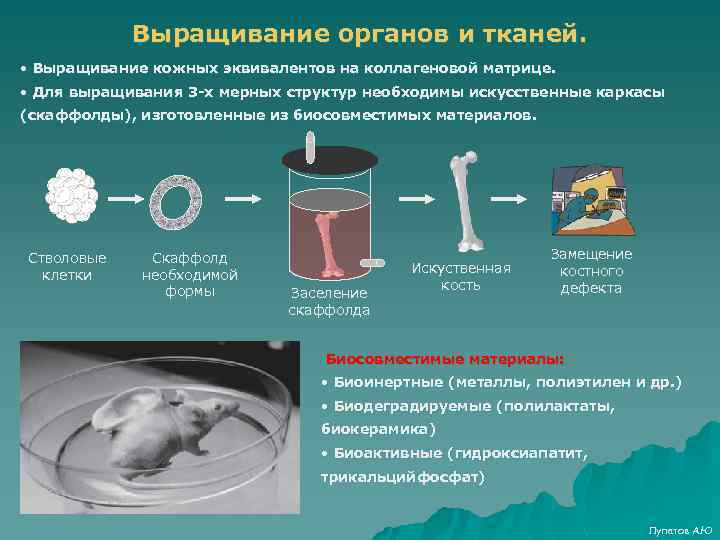
Выращивание органов и тканей. • Выращивание кожных эквивалентов на коллагеновой матрице. • Для выращивания 3 -х мерных структур необходимы искусственные каркасы (скаффолды), изготовленные из биосовместимых материалов. Стволовые клетки Скаффолд необходимой формы Заселение скаффолда Искуственная кость Замещение костного дефекта Биосовместимые материалы: • Биоинертные (металлы, полиэтилен и др. ) • Биодеградируемые (полилактаты, биокерамика) • Биоактивные (гидроксиапатит, трикальцийфосфат) Лупатов А. Ю
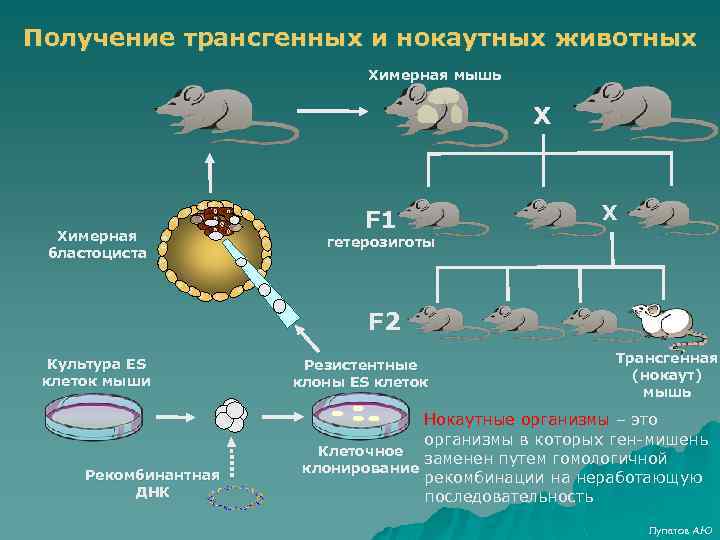
Получение трансгенных и нокаутных животных Химерная мышь Х Химерная бластоциста F 1 Х гетерозиготы F 2 Культура ES клеток мыши Рекомбинантная ДНК Резистентные клоны ES клеток Трансгенная (нокаут) мышь Нокаутные организмы – это организмы в которых ген-мишень Клеточное заменен путем гомологичной клонирование рекомбинации на неработающую последовательность Лупатов А. Ю
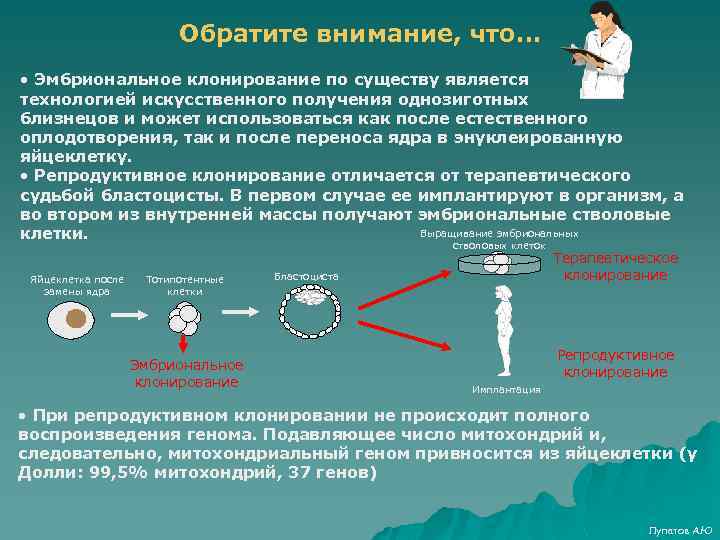
Обратите внимание, что… • Эмбриональное клонирование по существу является технологией искусственного получения однозиготных близнецов и может использоваться как после естественного оплодотворения, так и после переноса ядра в энуклеированную яйцеклетку. • Репродуктивное клонирование отличается от терапевтического судьбой бластоцисты. В первом случае ее имплантируют в организм, а во втором из внутренней массы получают эмбриональные стволовые Выращивание эмбриональных клетки. стволовых клеток Яйцеклетка после замены ядра Тотипотентные клетки Эмбриональное клонирование Бластоциста Терапевтическое клонирование Репродуктивное клонирование Имплантация • При репродуктивном клонировании не происходит полного воспроизведения генома. Подавляющее число митохондрий и, следовательно, митохондриальный геном привносится из яйцеклетки (у Долли: 99, 5% митохондрий, 37 генов) Лупатов А. Ю

Клеточная терапия. Заместительная или стимуляционная клеточная терапия- в основном используются постнатальные гемопоэтические либо мезенхимальные стволовые клетки как аутологичные, так и алогенные. Раньше применяли фетальные клетки. Эмбриональные стволовые клетки не используются изза их высокой тератогенности. Иногда вводят дифференцированные клетки после их наращивания и/или дифференцировки в культуре. Мезенхимальные стволовые клетки (МСК) обладают эффективностью при лечении травм позвоночника, инсульта, нейродегенеративных заболеваний, миодистрофии, косметических дефектов и др. МСК слабо иммуногенны из-за чего могут использоваться в схемах аллогенной трансплантации. Используются для лечения аутоиммунных заболеваний и предотвращения отторжения аллотрансплантата. Гемопоэтические стволовые клетки (ГСК) - трансплантация ГСК применяется в онкологии, особенно в онкогематологии, для восстановления кроветворения, после курсов химио- и радиотерапии, при лучевой болезни, в случае генетических дефектов гемопоэтической системы. Высокоиммуногенны, поэтому в случае аллотрансплантации требуется подбор донора. Клетки обычно получают из костного мозга и пуповинной крови. Лупатов А. Ю
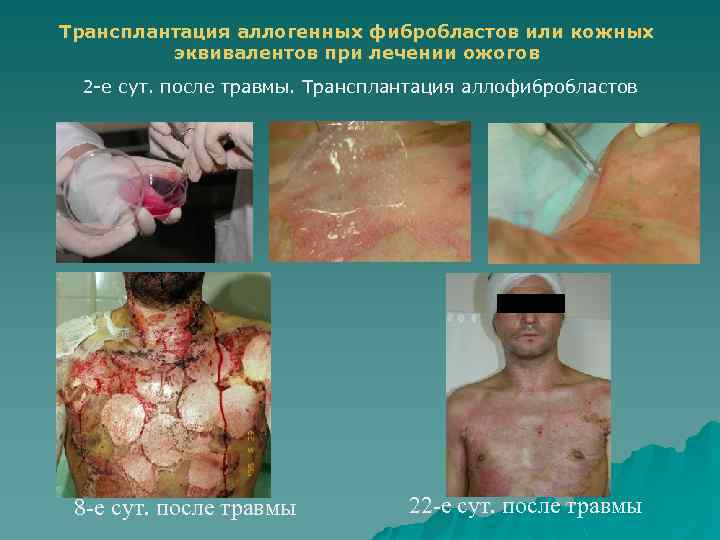
Трансплантация аллогенных фибробластов или кожных эквивалентов при лечении ожогов 2 -е сут. после травмы. Трансплантация аллофибробластов 8 -е сут. после травмы 22 -е сут. после травмы
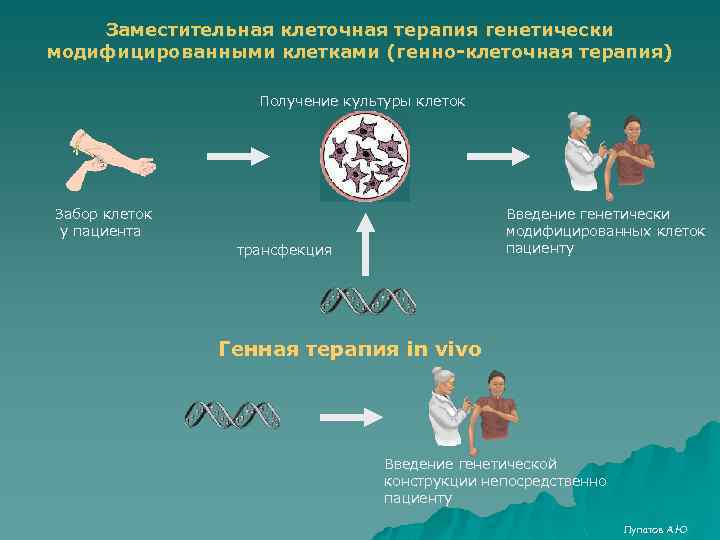
Заместительная клеточная терапия генетически модифицированными клетками (генно-клеточная терапия) Получение культуры клеток Забор клеток у пациента Введение генетически модифицированных клеток пациенту трансфекция Генная терапия in vivo Введение генетической конструкции непосредственно пациенту Лупатов А. Ю
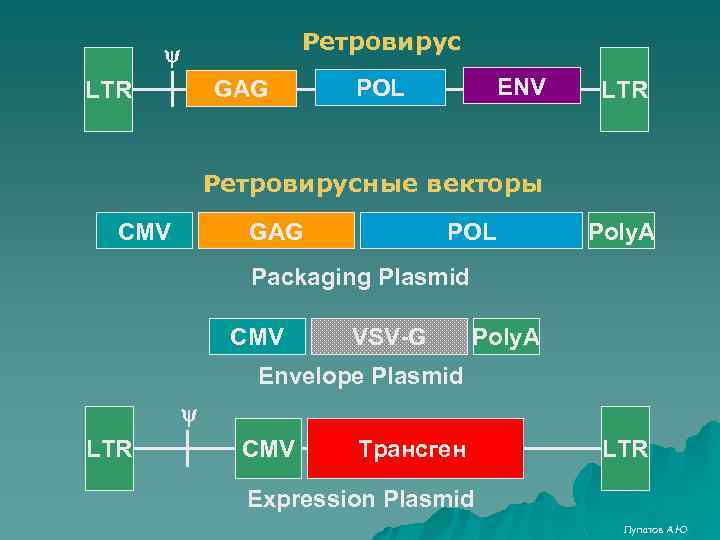
Ретровирус GAG LTR ENV POL LTR Ретровирусные векторы CMV GAG POL Poly. A Packaging Plasmid CMV VSV-G Poly. A Envelope Plasmid LTR CMV Трансген LTR Expression Plasmid Лупатов А. Ю
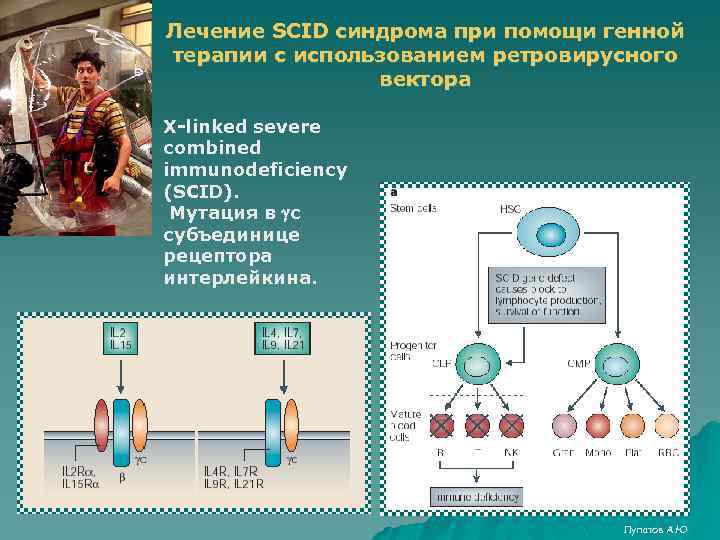
Лечение SCID синдрома при помощи генной терапии с использованием ретровирусного вектора X-linked severe combined immunodeficiency (SCID). Мутация в gc субъединице рецептора интерлейкина. Лупатов А. Ю
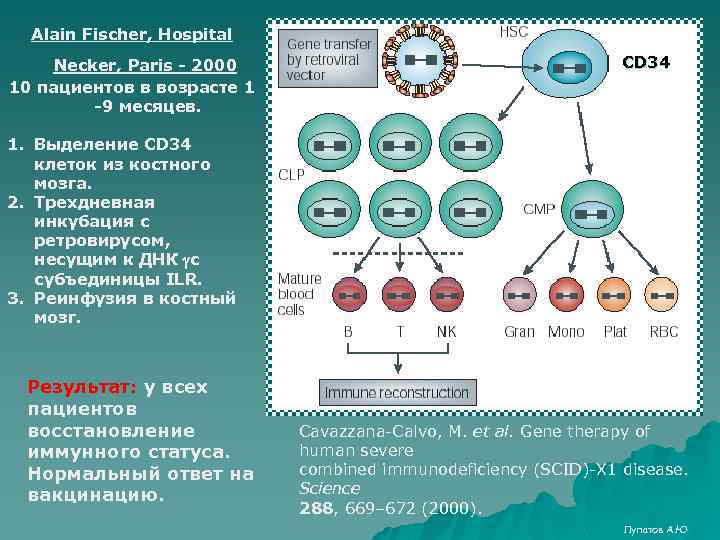
Alain Fischer, Hospital Necker, Paris - 2000 10 пациентов в возрасте 1 -9 месяцев. CD 34 1. Выделение CD 34 клеток из костного мозга. 2. Трехдневная инкубация с ретровирусом, несущим к ДНК gc субъединицы ILR. 3. Реинфузия в костный мозг. Результат: у всех пациентов восстановление иммунного статуса. Нормальный ответ на вакцинацию. Cavazzana-Calvo, M. et al. Gene therapy of human severe combined immunodeficiency (SCID)-X 1 disease. Science 288, 669– 672 (2000). Лупатов А. Ю
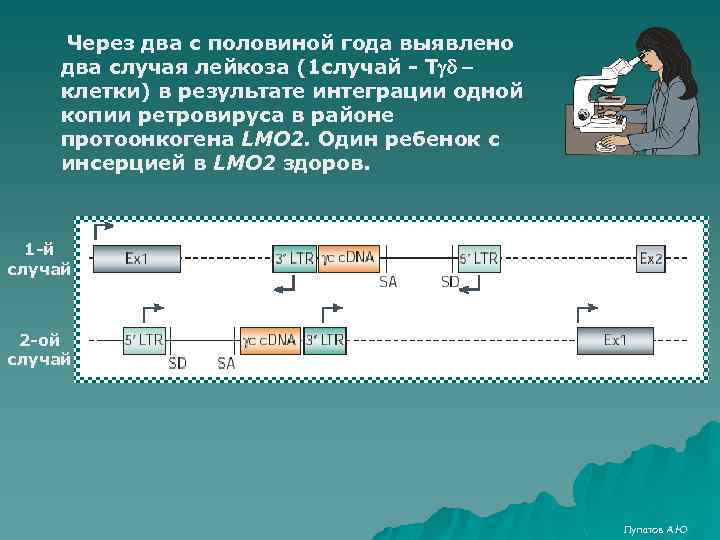
Через два с половиной года выявлено два случая лейкоза (1 случай - Tgd клетки) в результате интеграции одной копии ретровируса в районе протоонкогена LMO 2. Один ребенок с инсерцией в LMO 2 здоров. 1 -й случай 2 -ой случай Лупатов А. Ю
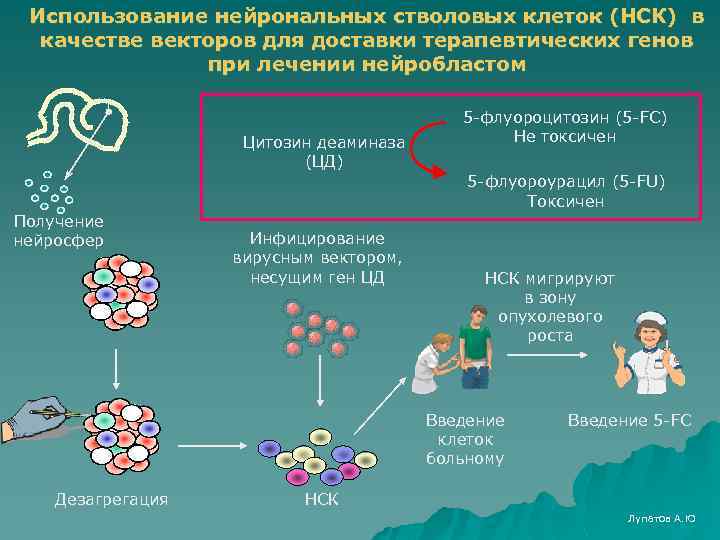
Использование нейрональных стволовых клеток (НСК) в качестве векторов для доставки терапевтических генов при лечении нейробластом Цитозин деаминаза (ЦД) 5 -флуороцитозин (5 -FC) Не токсичен 5 -флуороурацил (5 -FU) Токсичен Получение нейросфер Инфицирование вирусным вектором, несущим ген ЦД НСК мигрируют в зону опухолевого роста Введение клеток больному Дезагрегация Введение 5 -FC НСК Лупатов А. Ю
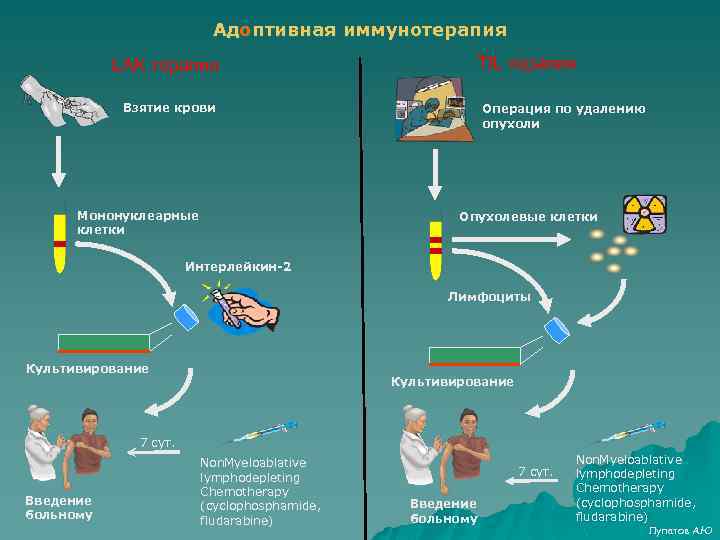
Адоптивная иммунотерапия LAK терапия TIL терапия Взятие крови Мононуклеарные клетки Операция по удалению опухоли Опухолевые клетки Интерлейкин-2 Лимфоциты Культивирование 7 сут. Введение больному Non. Myeloablative lymphodepleting Chemotherapy (cyclophosphamide, fludarabine) 7 сут. Введение больному Non. Myeloablative lymphodepleting Chemotherapy (cyclophosphamide, fludarabine) Лупатов А. Ю
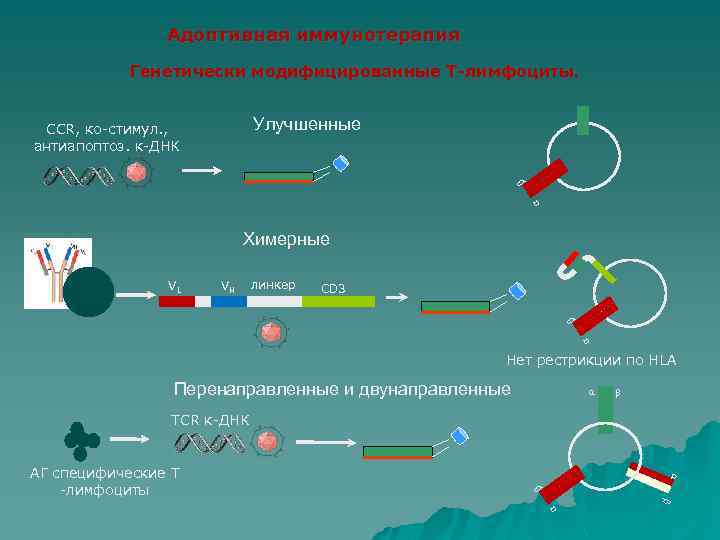
Адоптивная иммунотерапия Генетически модифицированные Т-лимфоциты. Улучшенные a b CCR, ко-стимул. , антиапоптоз. к-ДНК Химерные VH линкер CD 3 a b VL Нет рестрикции по HLA Перенаправленные и двунаправленные a b TCR к-ДНК b a АГ специфические Т -лимфоциты
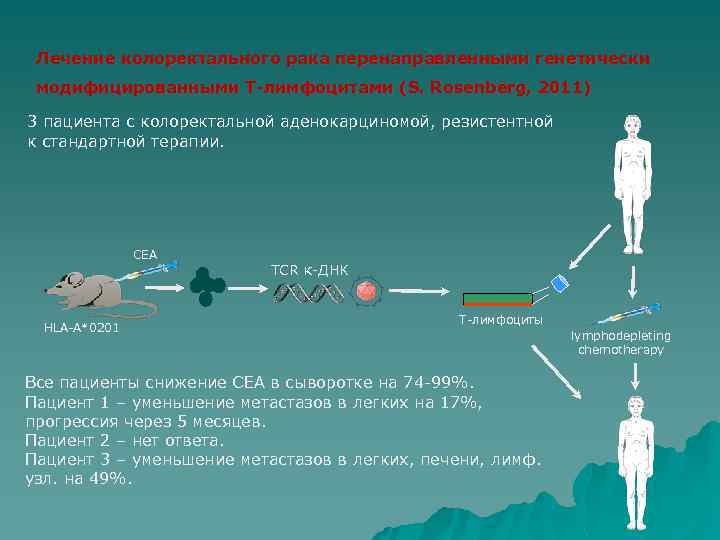
Лечение колоректального рака перенаправленными генетически модифицированными Т-лимфоцитами (S. Rosenberg, 2011) 3 пациента с колоректальной аденокарциномой, резистентной к стандартной терапии. CEA HLA-A*0201 TCR к-ДНК Т-лимфоциты Все пациенты снижение CEA в сыворотке на 74 -99%. Пациент 1 – уменьшение метастазов в легких на 17%, прогрессия через 5 месяцев. Пациент 2 – нет ответа. Пациент 3 – уменьшение метастазов в легких, печени, лимф. узл. на 49%. lymphodepleting сhemotherapy
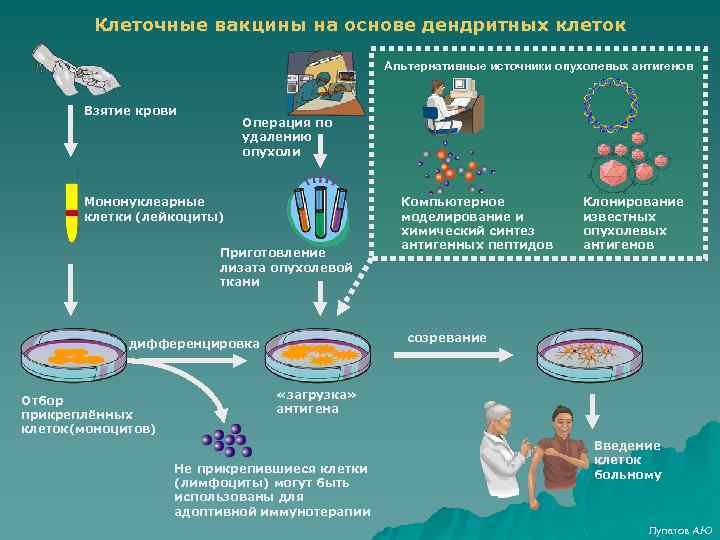
Клеточные вакцины на основе дендритных клеток Альтернативные источники опухолевых антигенов Взятие крови Операция по удалению опухоли Мононуклеарные клетки (лейкоциты) Приготовление лизата опухолевой ткани Клонирование известных опухолевых антигенов созревание дифференцировка Отбор прикреплённых клеток(моноцитов) Компьютерное моделирование и химический синтез антигенных пептидов «загрузка» антигена Не прикрепившиеся клетки (лимфоциты) могут быть использованы для адоптивной иммунотерапии Введение клеток больному Лупатов А. Ю

Подведем итоги • Клеточные технологии – это приоритетное направление развития науки и технологий в интересах медицины, фармакологии, сельского хозяйства. В основе клеточных технологий лежит выращивание в культуре клеток многоклеточных организмов. • Репродуктивное клонирование позволяет воспроизводить генетические копии взрослых, а иногда и погибших организмов. В большинстве стран существует мораторий на репродуктивное клонирование человека (имплантацию эмбриона). • При помощи терапевтического клонирования можно выращивать органы и ткани идеально пригодные для трансплантации. • Для заместительной и стимуляторной клеточной терапии обычно используют инъекции собственных либо аллогенных региональных стволовых клеток. Эмбриональные стволовые клетки не применяются из-за опасности образования тератом. • Клеточные технологии, основанные на культивировании клеток иммунной системы, могут применяться для лечения онкологических, хронических инфекционных и аутоиммунных заболеваний Лупатов А. Ю
Введение в клеточные технологии 2013.ppt