 Альдегиды
Альдегиды
 • В XIXв химики выделили из природных источников множество органических соединений; для некоторых из них были составлены структурные формулы
• В XIXв химики выделили из природных источников множество органических соединений; для некоторых из них были составлены структурные формулы
 Альдегиды несущие запах • В 1803 г из горького миндаля выделено новое вещество со специфическим запахом – бензойный альдегид. Впоследствии это вещество было найдено в косточках вишни, абрикоса, персика
Альдегиды несущие запах • В 1803 г из горького миндаля выделено новое вещество со специфическим запахом – бензойный альдегид. Впоследствии это вещество было найдено в косточках вишни, абрикоса, персика
 • 1841 г. куминовый альдегид из масла цветков антемиса • 1869 г гелиотропин из сирени
• 1841 г. куминовый альдегид из масла цветков антемиса • 1869 г гелиотропин из сирени
 • 1880 г Лауриновый альдегид из масла руты, лимона, шишек пихты 1883 г Каприновый альдегид (деканаль C 10) из масла кориандра , мандарина и лимона
• 1880 г Лауриновый альдегид из масла руты, лимона, шишек пихты 1883 г Каприновый альдегид (деканаль C 10) из масла кориандра , мандарина и лимона
 • 1888 г- цитраль из масла цитрусовых
• 1888 г- цитраль из масла цитрусовых
 1900 г -пеларгоновый альдегид или нональ ( C 9 ) из розового масла
1900 г -пеларгоновый альдегид или нональ ( C 9 ) из розового масла
 • 1816 г из стручков ванили выделено новое вещество с пряным запахом, которое назвали ванилин. Ванилин производное бензальдегида. • Первое же синтетическое душистое вещество было получено Уильямом Генри Перкином- старшим в 1867 г.
• 1816 г из стручков ванили выделено новое вещество с пряным запахом, которое назвали ванилин. Ванилин производное бензальдегида. • Первое же синтетическое душистое вещество было получено Уильямом Генри Перкином- старшим в 1867 г.
 • В концентрированном виде альдегиды имеют резкий, довольно раздражающий запах, но при сильном разбавлении у них неожиданно появляются нежные цветочные ароматы. Поэтому в малых количествах они непременная часть самых ценных душистых эссенций, потому без них не обходятся ни одни высококачественные духи.
• В концентрированном виде альдегиды имеют резкий, довольно раздражающий запах, но при сильном разбавлении у них неожиданно появляются нежные цветочные ароматы. Поэтому в малых количествах они непременная часть самых ценных душистых эссенций, потому без них не обходятся ни одни высококачественные духи.
 Альдегиды – органические вещества, содержащие функциональную группу – O СH 3 – C (альдегидную группу) H Общая формула: O R–C H, или для предельных альдегидов – O Cn. H 2 n -1 C H. Органические вещества, в молекулах которых карбонильная функциональная группа связана с двумя углеводородными радикалами, называют кетонами. Общая формула: O R 1– C – R 2
Альдегиды – органические вещества, содержащие функциональную группу – O СH 3 – C (альдегидную группу) H Общая формула: O R–C H, или для предельных альдегидов – O Cn. H 2 n -1 C H. Органические вещества, в молекулах которых карбонильная функциональная группа связана с двумя углеводородными радикалами, называют кетонами. Общая формула: O R 1– C – R 2
 Классификация. 1. По характеру углеводородного радикала: предельные, непредельные, ароматические. 2. По числу альдегидных групп: моно-, диальдегиды и т. д. Например: Предельные Непредельные Ароматические Cn. H 2 n+1 -CН=О CH 2=CH-CН=О акролеин С 6 H 5 -CН=О бензальдегид
Классификация. 1. По характеру углеводородного радикала: предельные, непредельные, ароматические. 2. По числу альдегидных групп: моно-, диальдегиды и т. д. Например: Предельные Непредельные Ароматические Cn. H 2 n+1 -CН=О CH 2=CH-CН=О акролеин С 6 H 5 -CН=О бензальдегид
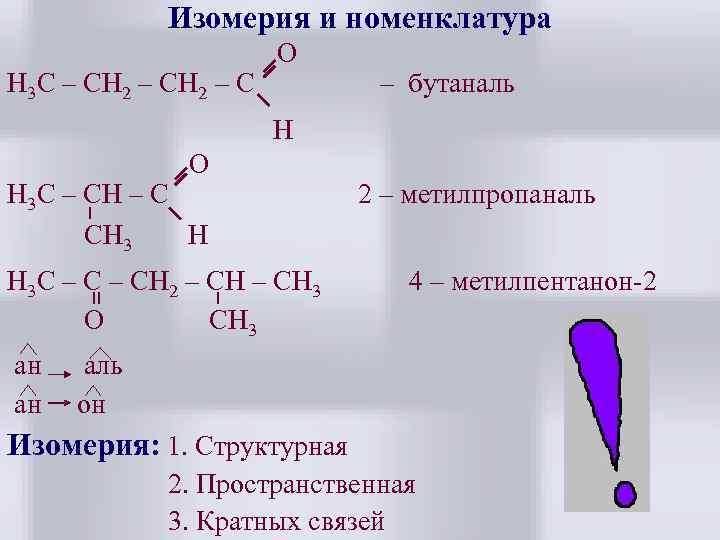 Изомерия и номенклатура Н 3 С – СН 2 – С O – бутаналь H O Н 3 С – СН – С CH 3 H Н 3 С – СН 2 – СН – CH 3 O CH 3 ан ан 2 – метилпропаналь 4 – метилпентанон-2 аль он Изомерия: 1. Структурная 2. Пространственная 3. Кратных связей
Изомерия и номенклатура Н 3 С – СН 2 – С O – бутаналь H O Н 3 С – СН – С CH 3 H Н 3 С – СН 2 – СН – CH 3 O CH 3 ан ан 2 – метилпропаналь 4 – метилпентанон-2 аль он Изомерия: 1. Структурная 2. Пространственная 3. Кратных связей
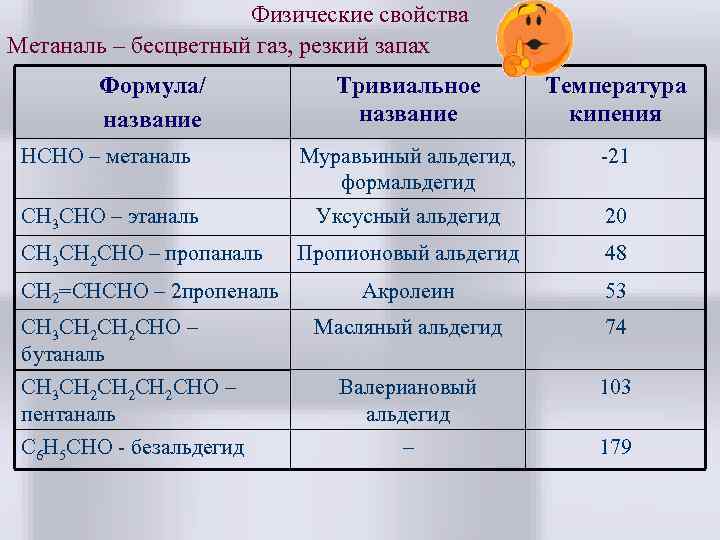 Физические свойства Метаналь – бесцветный газ, резкий запах Формула/ название Тривиальное название Температура кипения HCHO – метаналь Муравьиный альдегид, формальдегид -21 CH 3 CHO – этаналь Уксусный альдегид 20 Пропионовый альдегид 48 Акролеин 53 Масляный альдегид 74 CH 3 CH 2 CH 2 CHO – пентаналь Валериановый альдегид 103 C 6 H 5 CHO - безальдегид – 179 CH 3 CH 2 CHO – пропаналь CH 2=CHCHO – 2 пропеналь CH 3 CH 2 CHO – бутаналь
Физические свойства Метаналь – бесцветный газ, резкий запах Формула/ название Тривиальное название Температура кипения HCHO – метаналь Муравьиный альдегид, формальдегид -21 CH 3 CHO – этаналь Уксусный альдегид 20 Пропионовый альдегид 48 Акролеин 53 Масляный альдегид 74 CH 3 CH 2 CH 2 CHO – пентаналь Валериановый альдегид 103 C 6 H 5 CHO - безальдегид – 179 CH 3 CH 2 CHO – пропаналь CH 2=CHCHO – 2 пропеналь CH 3 CH 2 CHO – бутаналь

 Физические свойства. • Метаналь (формальдегид) – газ, альдегиды С 2 -C 5 – жидкости, высшие – твердые вещества. Низшие гомологи растворимы в воде, благодаря образованию водородных связей между атомами водорода молекул воды и карбонильными атомами кислорода. С увеличением углеводородного радикала растворимость в воде падает. • Альдегиды обладают удушливым запахом, который при многократном разведении становится приятным, напоминая запах плодов. Альдегиды кипят при более низкой температуре, чем спирты с тем же числом углеродных атомов. Это cвязано с отсутствием в альдегидах водородных связей. • В то же время температура кипения альдегидов выше, чем у соответствующих по молекулярной массе углеводородов, что связано с высокой полярностью альдегидов.
Физические свойства. • Метаналь (формальдегид) – газ, альдегиды С 2 -C 5 – жидкости, высшие – твердые вещества. Низшие гомологи растворимы в воде, благодаря образованию водородных связей между атомами водорода молекул воды и карбонильными атомами кислорода. С увеличением углеводородного радикала растворимость в воде падает. • Альдегиды обладают удушливым запахом, который при многократном разведении становится приятным, напоминая запах плодов. Альдегиды кипят при более низкой температуре, чем спирты с тем же числом углеродных атомов. Это cвязано с отсутствием в альдегидах водородных связей. • В то же время температура кипения альдегидов выше, чем у соответствующих по молекулярной массе углеводородов, что связано с высокой полярностью альдегидов.
 Физически свойства некоторых альдегидов. Формальдегид – газ, с резким запахом, раздражает слизистые ткани и оказывает действие на центральную нервную систему. ОПАСЕН ДЛЯ ЗДОРОВЬЯ! Водный раствор формальдегида – формалин. Ацетальдегид – жидкость , с запахом зелёной листвы. ОЧЕНЬ ТОКСИЧЕН! Подавляет дыхательные процессы в клетках. Акролеин СН 2 = CHCH=O акриловый альдегид, пропеналь (в производстве полимеров) – образуется пригорании жиров, жидкость с неприятным запахом, раздражает слизистые ткани. Бензальдегид C 6 H 5 CH=O (производство красителей) – жидкость с запахом горького миндаля, содержится в миндале, листьях черёмухи, косточках персиков, абрикосов.
Физически свойства некоторых альдегидов. Формальдегид – газ, с резким запахом, раздражает слизистые ткани и оказывает действие на центральную нервную систему. ОПАСЕН ДЛЯ ЗДОРОВЬЯ! Водный раствор формальдегида – формалин. Ацетальдегид – жидкость , с запахом зелёной листвы. ОЧЕНЬ ТОКСИЧЕН! Подавляет дыхательные процессы в клетках. Акролеин СН 2 = CHCH=O акриловый альдегид, пропеналь (в производстве полимеров) – образуется пригорании жиров, жидкость с неприятным запахом, раздражает слизистые ткани. Бензальдегид C 6 H 5 CH=O (производство красителей) – жидкость с запахом горького миндаля, содержится в миндале, листьях черёмухи, косточках персиков, абрикосов.
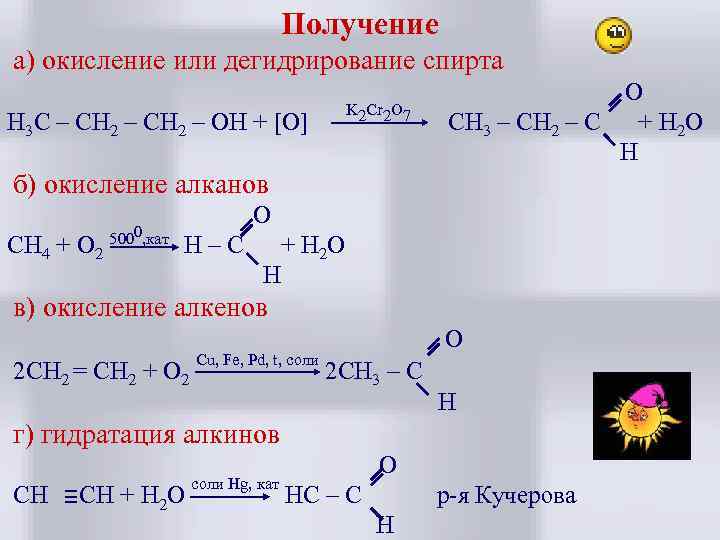 Получение а) окисление или дегидрирование спирта K 2 Cr 2 O 7 H 3 C – CH 2 – OH + [O] O CH 3 – CH 2 – C + H 2 O H б) окисление алканов CH 4 + O 2 5000, кат O H–С + H 2 O H в) окисление алкенов 2 CH 2 = CH 2 + O 2 Сu, Fe, Pd, t, соли O 2 CH 3 – C H г) гидратация алкинов CH CH + H 2 O соли Hg, кат O HC – C р-я Кучерова H
Получение а) окисление или дегидрирование спирта K 2 Cr 2 O 7 H 3 C – CH 2 – OH + [O] O CH 3 – CH 2 – C + H 2 O H б) окисление алканов CH 4 + O 2 5000, кат O H–С + H 2 O H в) окисление алкенов 2 CH 2 = CH 2 + O 2 Сu, Fe, Pd, t, соли O 2 CH 3 – C H г) гидратация алкинов CH CH + H 2 O соли Hg, кат O HC – C р-я Кучерова H
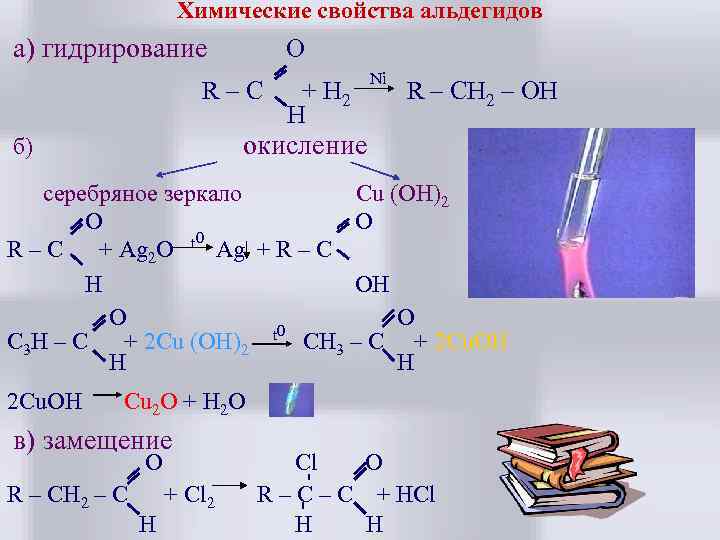 Химические свойства альдегидов а) гидрирование O R–C + H 2 H Ni R – CH 2 – OH окисление б) серебряное зеркало Cu (OH)2 O O 0 R–C + Ag 2 O t Ag + R – C H ОH O O 0 C 3 H – C + 2 Cu (OH)2 t CH 3 – C + 2 Cu. OH H H 2 Cu. OH Cu 2 O + H 2 O в) замещение O R – CH 2 – C H + Cl 2 Cl O R – C + HCl H H
Химические свойства альдегидов а) гидрирование O R–C + H 2 H Ni R – CH 2 – OH окисление б) серебряное зеркало Cu (OH)2 O O 0 R–C + Ag 2 O t Ag + R – C H ОH O O 0 C 3 H – C + 2 Cu (OH)2 t CH 3 – C + 2 Cu. OH H H 2 Cu. OH Cu 2 O + H 2 O в) замещение O R – CH 2 – C H + Cl 2 Cl O R – C + HCl H H
 гидроксидом меди (II), в результате обр. осадок кирпично-красного цвета (качественная реакция). t° СН 3 – СОН + 2 Сu(ОН)2 → СН 3 – СООН + Сu 2 О↓ + 2 Н 2 О синий кирпичнокрасный Муравьиный альдегид восстанавливает гидроксид меди (II) до меди: Н – СОН + Сu(ОН)2 → СО 2 ↑ + 2 Сu↓ + 3 Н 2 О
гидроксидом меди (II), в результате обр. осадок кирпично-красного цвета (качественная реакция). t° СН 3 – СОН + 2 Сu(ОН)2 → СН 3 – СООН + Сu 2 О↓ + 2 Н 2 О синий кирпичнокрасный Муравьиный альдегид восстанавливает гидроксид меди (II) до меди: Н – СОН + Сu(ОН)2 → СО 2 ↑ + 2 Сu↓ + 3 Н 2 О
 Химические реакции г) нуклеофильное присоединение O H 3 C – C + HC N H O H 3 C – C + Na. HSO 3 H д) поликонденсация CH 3 – CH – C OH N OH O CH 3 – CH – S – ONa O
Химические реакции г) нуклеофильное присоединение O H 3 C – C + HC N H O H 3 C – C + Na. HSO 3 H д) поликонденсация CH 3 – CH – C OH N OH O CH 3 – CH – S – ONa O
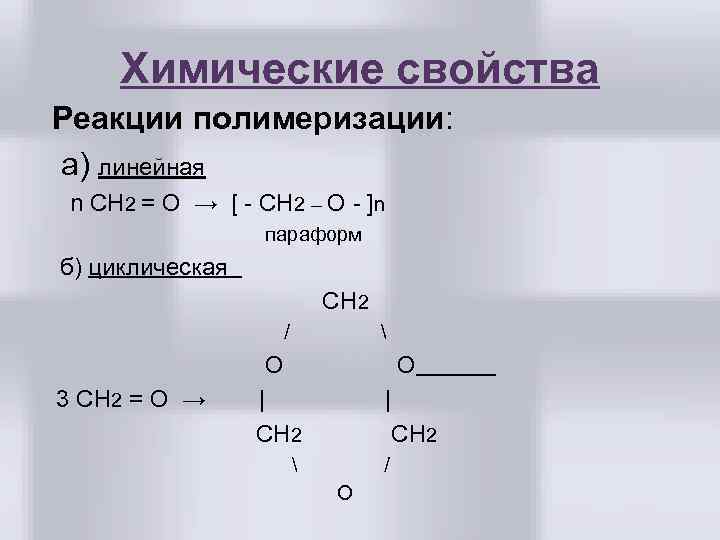 Химические свойства Реакции полимеризации: а) линейная n СН 2 = О → [ - СН 2 – О - ]n параформ б) циклическая СН 2 О 3 СН 2 = О → | СН 2 О
Химические свойства Реакции полимеризации: а) линейная n СН 2 = О → [ - СН 2 – О - ]n параформ б) циклическая СН 2 О 3 СН 2 = О → | СН 2 О
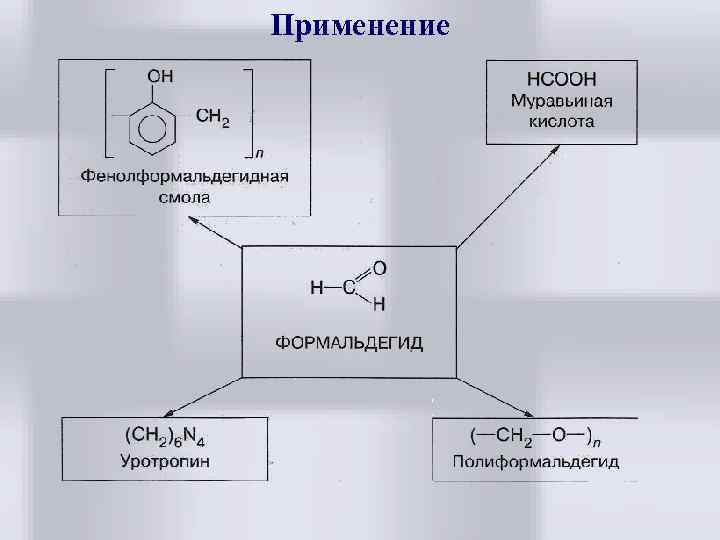 Применение
Применение
 Применение альдегидов O H C H
Применение альдегидов O H C H
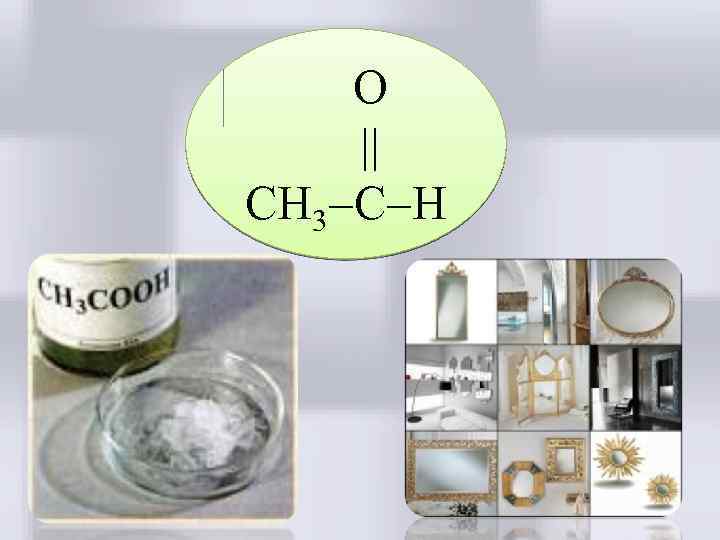 O CH 3 C H
O CH 3 C H
 • Наибольшее применение имеют метаналь и этаналь. Большое количество метаналя используется для получения фенолформальдегидной смолы. Эта смола необходима для производства различных пластмасс. Пластмассы, изготовленные из фенолформальдегидной смолы в сочетании с различными наполнителями, называются фенопластами. При растворении фенолформальдегидной смолы в ацетоне или спирте получают различные лаки. • При взаимодействии метаналя с карбамидом СО(МНг)2 получают карбамидную смолу, а из нее — аминопласты. Из этих пластмасс изготовляют микропористые материалы для нужд электротехники. • Метаналь широко применяется в производстве: в медицинской, химической и лесной промышленности, и без него многие предприятия просто бы остановились, со всеми вытекающими последствиями. То есть формальдегид кормит сотни тысяч людей!
• Наибольшее применение имеют метаналь и этаналь. Большое количество метаналя используется для получения фенолформальдегидной смолы. Эта смола необходима для производства различных пластмасс. Пластмассы, изготовленные из фенолформальдегидной смолы в сочетании с различными наполнителями, называются фенопластами. При растворении фенолформальдегидной смолы в ацетоне или спирте получают различные лаки. • При взаимодействии метаналя с карбамидом СО(МНг)2 получают карбамидную смолу, а из нее — аминопласты. Из этих пластмасс изготовляют микропористые материалы для нужд электротехники. • Метаналь широко применяется в производстве: в медицинской, химической и лесной промышленности, и без него многие предприятия просто бы остановились, со всеми вытекающими последствиями. То есть формальдегид кормит сотни тысяч людей!
 Метаналь идет также на производство красителей. Широко применяется водный раствор - формалин. Его использование основано на свойстве свертывать белок. Так, например, в кожевенном производстве дубящее действие формалина объясняется свертыванием белка, в результате чего кожа твердеет и не подвергается гниению. На этом же свойстве основано применение формалина для сохранения биологических препаратов. Иногда формалин используется для дезинфекции и протравливания семян.
Метаналь идет также на производство красителей. Широко применяется водный раствор - формалин. Его использование основано на свойстве свертывать белок. Так, например, в кожевенном производстве дубящее действие формалина объясняется свертыванием белка, в результате чего кожа твердеет и не подвергается гниению. На этом же свойстве основано применение формалина для сохранения биологических препаратов. Иногда формалин используется для дезинфекции и протравливания семян.
 Альдегиды в природе Булочки ванильные, корицы аромат, Амаретто, шоколад Альдегидов вкус таят В землянике и кокосе И в жасмине и в малине И в духах и в еде Альдегидов след везде. Что за запах, что за прелесть, И откуда эта свежесть? Это высший альдегид Аромат вам свой дарит.
Альдегиды в природе Булочки ванильные, корицы аромат, Амаретто, шоколад Альдегидов вкус таят В землянике и кокосе И в жасмине и в малине И в духах и в еде Альдегидов след везде. Что за запах, что за прелесть, И откуда эта свежесть? Это высший альдегид Аромат вам свой дарит.
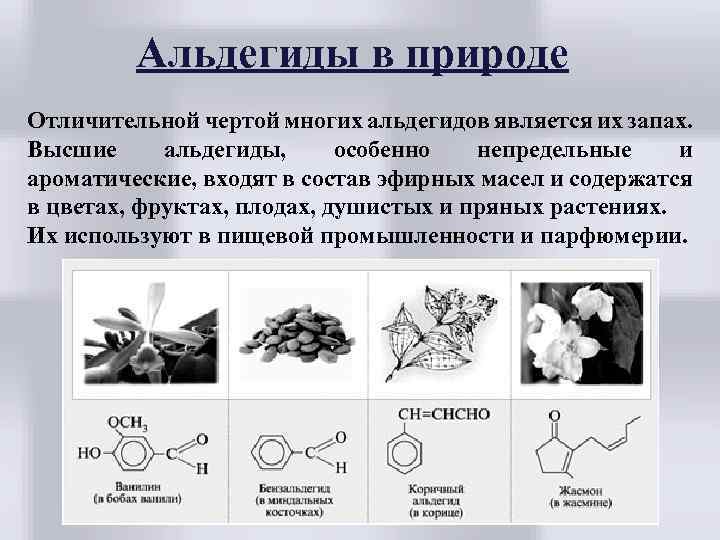 Альдегиды в природе Отличительной чертой многих альдегидов является их запах. Высшие альдегиды, особенно непредельные и ароматические, входят в состав эфирных масел и содержатся в цветах, фруктах, плодах, душистых и пряных растениях. Их используют в пищевой промышленности и парфюмерии.
Альдегиды в природе Отличительной чертой многих альдегидов является их запах. Высшие альдегиды, особенно непредельные и ароматические, входят в состав эфирных масел и содержатся в цветах, фруктах, плодах, душистых и пряных растениях. Их используют в пищевой промышленности и парфюмерии.
 Альдегиды в природе Ванилин В плодах ванили содержится ароматический альдегид, который придает им характерный запах. Ванилин применяется в парфюмерии, кондитерской промышленности, для маскировки запахов некоторых продуктов.
Альдегиды в природе Ванилин В плодах ванили содержится ароматический альдегид, который придает им характерный запах. Ванилин применяется в парфюмерии, кондитерской промышленности, для маскировки запахов некоторых продуктов.
 Альдегиды в природе Фенилэтаналь по сравнению с бензальдегидом лучше соответствует рецептору цветочного запаха. Фенилэтаналь пахнет гиацинтом.
Альдегиды в природе Фенилэтаналь по сравнению с бензальдегидом лучше соответствует рецептору цветочного запаха. Фенилэтаналь пахнет гиацинтом.
 Альдегиды в природе Бензальдегид – жидкость с запахом горького миндаля. Встречается в косточках и семечках, особенно в абрикосах и персиках.
Альдегиды в природе Бензальдегид – жидкость с запахом горького миндаля. Встречается в косточках и семечках, особенно в абрикосах и персиках.
 Альдегиды в природе Коричный альдегид содержится в масле корицы, его получают перегонкой коры дерева корицы. Применяется в кулинарии в виде палочек или порошка.
Альдегиды в природе Коричный альдегид содержится в масле корицы, его получают перегонкой коры дерева корицы. Применяется в кулинарии в виде палочек или порошка.
 • • • Альдегиды опасны для здоровья человека. Они вызывают отравление. Симптомы хронического отравления альдегидом (то есть когда в помещении постоянно присутствует довольно высокая концентрация формальдегида) – бледность, упадок сил, бессознательное состояние, депрессия, затрудненное дыхание, головная боль, не редко судороги по ночам. При длительном воздействии на человека альдегиды вызывают раздражение слизистых оболочек глаз и дыхательных путей, а при повышении концентрации отмечается головная боль, слабость, потеря аппетита, бессонница. Оказывает сильное действие на центральную нервную систему. При вдыхании больших концентраций альдегида может наступить внезапная смерть в результате отека и спазма голосовой щели. На сколько альдегиды в небольших количествах опасны для человека в жилых помещениях, таких данных нет. Опасность альдегида для конкретного человека зависит от состояния защитных сил организма человека. Но, чем ниже концентрация альдегида, тем меньше риск негативных последствий для здоровья.
• • • Альдегиды опасны для здоровья человека. Они вызывают отравление. Симптомы хронического отравления альдегидом (то есть когда в помещении постоянно присутствует довольно высокая концентрация формальдегида) – бледность, упадок сил, бессознательное состояние, депрессия, затрудненное дыхание, головная боль, не редко судороги по ночам. При длительном воздействии на человека альдегиды вызывают раздражение слизистых оболочек глаз и дыхательных путей, а при повышении концентрации отмечается головная боль, слабость, потеря аппетита, бессонница. Оказывает сильное действие на центральную нервную систему. При вдыхании больших концентраций альдегида может наступить внезапная смерть в результате отека и спазма голосовой щели. На сколько альдегиды в небольших количествах опасны для человека в жилых помещениях, таких данных нет. Опасность альдегида для конкретного человека зависит от состояния защитных сил организма человека. Но, чем ниже концентрация альдегида, тем меньше риск негативных последствий для здоровья.

 Контрольные вопросы 1. Найдите формулу альдегида: 2. Исключите лишнее вещество в ряду: 3. Какая функциональная группа называется карбонильной? 4. Атом углерода в альдегидной группе находится в состоянии гибридизации: а) sp б) sp 2 в) sp 3 г) не гибридизован 5. Назовите вещества с формулой а) 2 -метилбутанон-3, в) 3 -метилбутаналь, б) 3 -метилбутанон-2, г) 1, 2 -диметилпентаналя
Контрольные вопросы 1. Найдите формулу альдегида: 2. Исключите лишнее вещество в ряду: 3. Какая функциональная группа называется карбонильной? 4. Атом углерода в альдегидной группе находится в состоянии гибридизации: а) sp б) sp 2 в) sp 3 г) не гибридизован 5. Назовите вещества с формулой а) 2 -метилбутанон-3, в) 3 -метилбутаналь, б) 3 -метилбутанон-2, г) 1, 2 -диметилпентаналя
 6. Укажите формулу 2, 3 -диметилпентаналя: 7. Общая формула гомологического ряда предельных альдегидов: а) Cn. H 2 n. O б) Cn. H 2 n+2 O в) Cn. H 2 n-2 O г) Cn. H 2 n. O 2 8. Укажите формулу 4, 4 -диметилпентанона-2:
6. Укажите формулу 2, 3 -диметилпентаналя: 7. Общая формула гомологического ряда предельных альдегидов: а) Cn. H 2 n. O б) Cn. H 2 n+2 O в) Cn. H 2 n-2 O г) Cn. H 2 n. O 2 8. Укажите формулу 4, 4 -диметилпентанона-2:
 9. Гидратацией какого алкина можно получить альдегид? Напишите уравнение реакции, укажите условия её проведения. а) бутанол-2 в) 2 -метилбутанол-2 б) 3 -метилбутанол-2 г) 2 -метилбутанол-1 10. Нагреваем соли ацетата кальция можно получить: а) метаналь б) этаналь в) пропаналь г) пропанон 11. Какие признаки верно отражают физические свойства метаналя: 1) без цветная жидкость, 2) газообразное вещество, 3) имеется характерный запах, 4) плохо растворим в воде, 5) молекула полярная. а) 1, 3, 4 б) 2, 3, 5 в) 3, 4, 5 г) 2, 4, 5 12. Какая из реакций носит имя М. Г. Кучерова. а) гидратация ацетилена б) тримеризация ацетилена в) гидрирование ацетилена г) бромирование ацетилена
9. Гидратацией какого алкина можно получить альдегид? Напишите уравнение реакции, укажите условия её проведения. а) бутанол-2 в) 2 -метилбутанол-2 б) 3 -метилбутанол-2 г) 2 -метилбутанол-1 10. Нагреваем соли ацетата кальция можно получить: а) метаналь б) этаналь в) пропаналь г) пропанон 11. Какие признаки верно отражают физические свойства метаналя: 1) без цветная жидкость, 2) газообразное вещество, 3) имеется характерный запах, 4) плохо растворим в воде, 5) молекула полярная. а) 1, 3, 4 б) 2, 3, 5 в) 3, 4, 5 г) 2, 4, 5 12. Какая из реакций носит имя М. Г. Кучерова. а) гидратация ацетилена б) тримеризация ацетилена в) гидрирование ацетилена г) бромирование ацетилена
 Ответы 1)б 2)а 3)б 4)б 5)б 6)в 7)а 8)а 9)а 10)г 11)б 12)а
Ответы 1)б 2)а 3)б 4)б 5)б 6)в 7)а 8)а 9)а 10)г 11)б 12)а


