 Альдегиды и кетоны.
Альдегиды и кетоны.
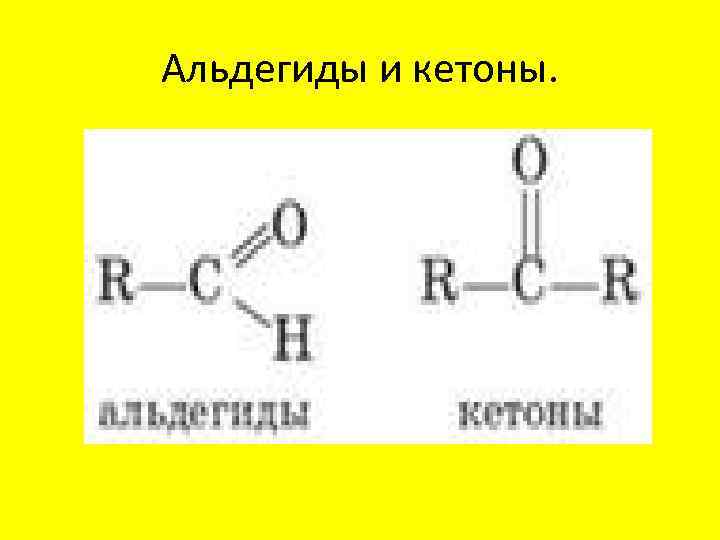
 Определение альдегидов и кетонов. • Альдегиды- это класс органических соединений, содержащих карбонильную группу С=О, соединенную с атомом водорода и углеводородным радикалом. • Кетоны – класс органических соединений, содержащих функциональную группу С=О, соединенную с двумя углеводородными радикалами.
Определение альдегидов и кетонов. • Альдегиды- это класс органических соединений, содержащих карбонильную группу С=О, соединенную с атомом водорода и углеводородным радикалом. • Кетоны – класс органических соединений, содержащих функциональную группу С=О, соединенную с двумя углеводородными радикалами.
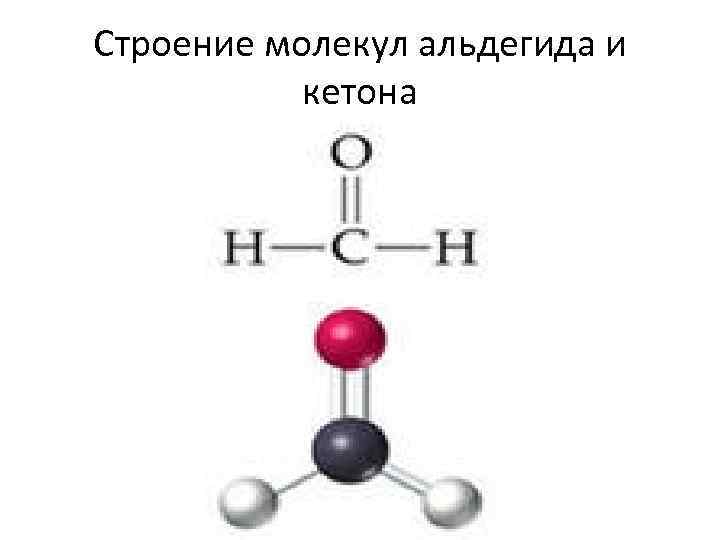 Строение молекул альдегида и кетона
Строение молекул альдегида и кетона
 Гомологический ряд альдегидов. • Метаналь – формальдегид – Н-С=ОН • Этаналь – уксусный альдегид, ацетальдегид - СН 3 -С=ОН • Пропаналь – СН 3 -СН 2 -С=ОН • Бутаналь – СН 3 -СН 2 -С=ОН • Пентаналь – СН 3 -СН 2 -СН 2 -С=ОН • Общая формула: Сn. H 2 n+1 C=OH
Гомологический ряд альдегидов. • Метаналь – формальдегид – Н-С=ОН • Этаналь – уксусный альдегид, ацетальдегид - СН 3 -С=ОН • Пропаналь – СН 3 -СН 2 -С=ОН • Бутаналь – СН 3 -СН 2 -С=ОН • Пентаналь – СН 3 -СН 2 -СН 2 -С=ОН • Общая формула: Сn. H 2 n+1 C=OH
 Физические свойства. • Формальдегид – газ с резким удушливым запахом, t кипения -19, 3, ядовит. 40% раствор формальдегида называется формалином. • Пропонон ( диметилкетон) или ацетон: СН 3 -С=О-СН 3 – бесцветная жидкость с резким запахом, tкип. 56, 24 С, хорошо растворим в воде.
Физические свойства. • Формальдегид – газ с резким удушливым запахом, t кипения -19, 3, ядовит. 40% раствор формальдегида называется формалином. • Пропонон ( диметилкетон) или ацетон: СН 3 -С=О-СН 3 – бесцветная жидкость с резким запахом, tкип. 56, 24 С, хорошо растворим в воде.
 Химические свойства. • Качественные реакции на альдегиды – это • Реакция « серебряного зеркала» взаимодействие альдегидов с аммиачным раствором серебра при нагревании. При этом альдегид окисляется до соответствующей карбоновой кислоты, а оксид серебра превращается в свободное серебро, которое покрывает пробирку. • Взаимодействие с гидроксидом меди(2) с образованием красного осадка оксида меди.
Химические свойства. • Качественные реакции на альдегиды – это • Реакция « серебряного зеркала» взаимодействие альдегидов с аммиачным раствором серебра при нагревании. При этом альдегид окисляется до соответствующей карбоновой кислоты, а оксид серебра превращается в свободное серебро, которое покрывает пробирку. • Взаимодействие с гидроксидом меди(2) с образованием красного осадка оксида меди.
 Получение альдегидов. • Метаналь получают окислением метанола : 2 СН 3 ОН + О 2 = 2 НСНО + 2 Н 2 О или окислением метана: СН 4 + О 2 = НСНО +Н 2 О Этаналь получают окислением этилена: 2 С 2 Н 4 + О 2 = 2 СН 3 -СНО Или гидратацией ацетилена: С 2 Н 2 + Н 2 О = СН 3 СНО
Получение альдегидов. • Метаналь получают окислением метанола : 2 СН 3 ОН + О 2 = 2 НСНО + 2 Н 2 О или окислением метана: СН 4 + О 2 = НСНО +Н 2 О Этаналь получают окислением этилена: 2 С 2 Н 4 + О 2 = 2 СН 3 -СНО Или гидратацией ацетилена: С 2 Н 2 + Н 2 О = СН 3 СНО
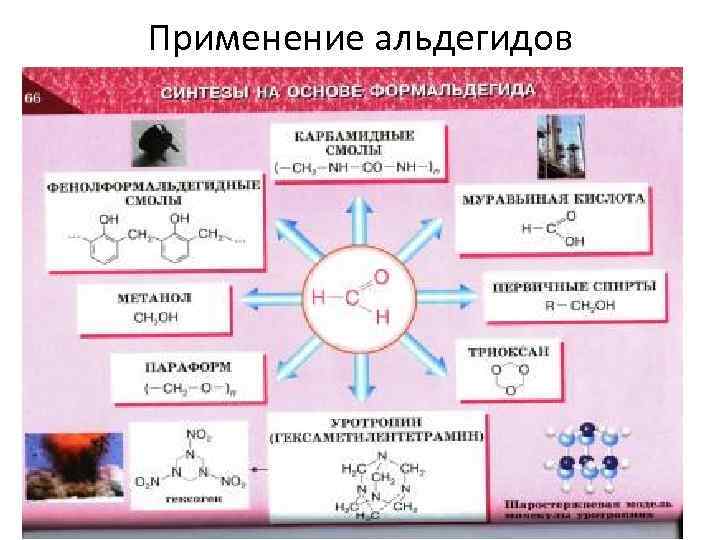 Применение альдегидов
Применение альдегидов
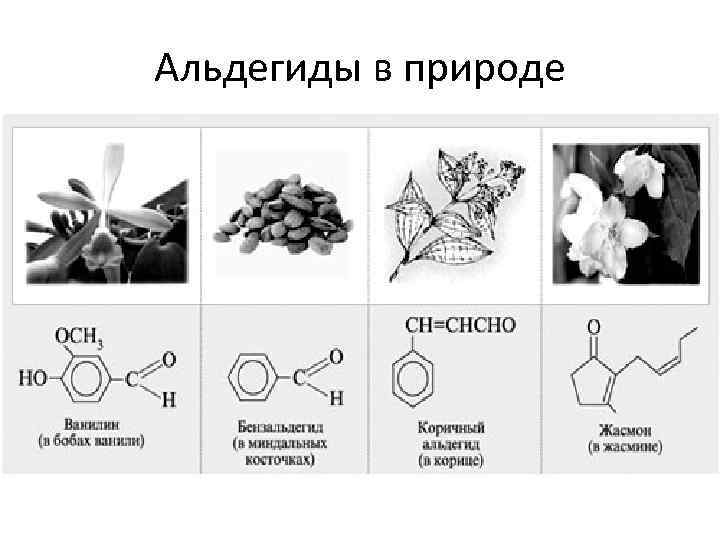 Альдегиды в природе
Альдегиды в природе