Альдегиды и кетоны.ppt
- Количество слайдов: 27
 АЛЬДЕГИДЫ И КЕТОНЫ Электронный дидактический материал информационного типа Составитель: Сабирзянова А. З. , преподаватель биохимии © ГАОУ СПР «Казанский медицинский колледж» Выход
АЛЬДЕГИДЫ И КЕТОНЫ Электронный дидактический материал информационного типа Составитель: Сабирзянова А. З. , преподаватель биохимии © ГАОУ СПР «Казанский медицинский колледж» Выход
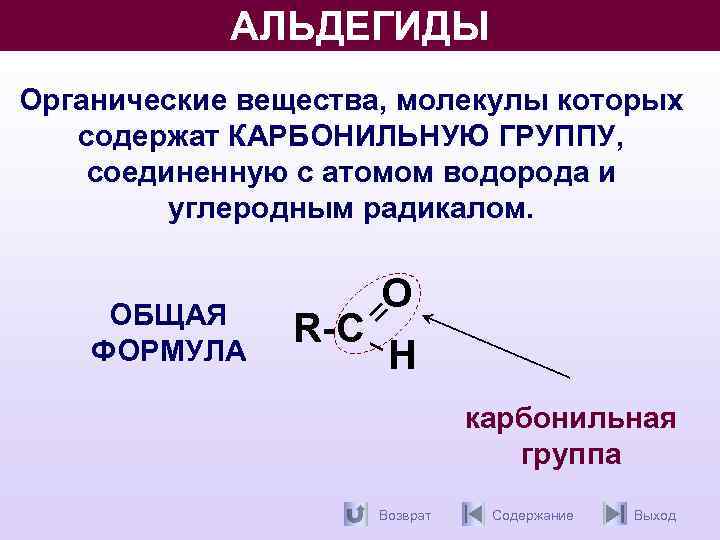 АЛЬДЕГИДЫ Органические вещества, молекулы которых содержат КАРБОНИЛЬНУЮ ГРУППУ, соединенную с атомом водорода и углеродным радикалом. ОБЩАЯ ФОРМУЛА R-С О Н карбонильная группа Возврат Содержание Выход
АЛЬДЕГИДЫ Органические вещества, молекулы которых содержат КАРБОНИЛЬНУЮ ГРУППУ, соединенную с атомом водорода и углеродным радикалом. ОБЩАЯ ФОРМУЛА R-С О Н карбонильная группа Возврат Содержание Выход
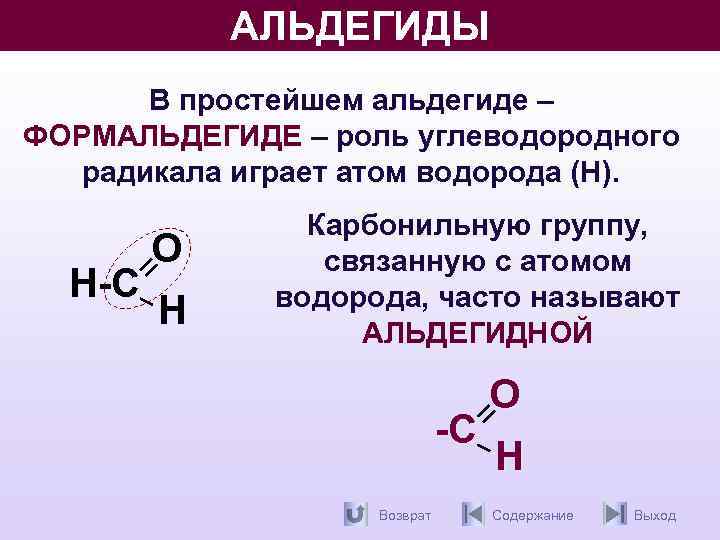 АЛЬДЕГИДЫ В простейшем альдегиде – ФОРМАЛЬДЕГИДЕ – роль углеводородного радикала играет атом водорода (Н). Н-С О Н Карбонильную группу, связанную с атомом водорода, часто называют АЛЬДЕГИДНОЙ -С Возврат О Н Содержание Выход
АЛЬДЕГИДЫ В простейшем альдегиде – ФОРМАЛЬДЕГИДЕ – роль углеводородного радикала играет атом водорода (Н). Н-С О Н Карбонильную группу, связанную с атомом водорода, часто называют АЛЬДЕГИДНОЙ -С Возврат О Н Содержание Выход
 КЕТОНЫ Органические вещества, молекулы которых содержат КАРБОНИЛЬНУЮ ГРУППУ, соединенную с двумя углеродными радикалами. ОБЩАЯ ФОРМУЛА R 1 -С О R 2 карбонильная группа Возврат Содержание Выход
КЕТОНЫ Органические вещества, молекулы которых содержат КАРБОНИЛЬНУЮ ГРУППУ, соединенную с двумя углеродными радикалами. ОБЩАЯ ФОРМУЛА R 1 -С О R 2 карбонильная группа Возврат Содержание Выход
 КЕТОНЫ Карбонильную группу кетонов называют КЕТОГРУППОЙ В простейшем кетоне – АЦЕТОНЕ – карбонильная группа связана с двумя метильными радикалами СН 3 -С О СН 3 Возврат Содержание Выход
КЕТОНЫ Карбонильную группу кетонов называют КЕТОГРУППОЙ В простейшем кетоне – АЦЕТОНЕ – карбонильная группа связана с двумя метильными радикалами СН 3 -С О СН 3 Возврат Содержание Выход
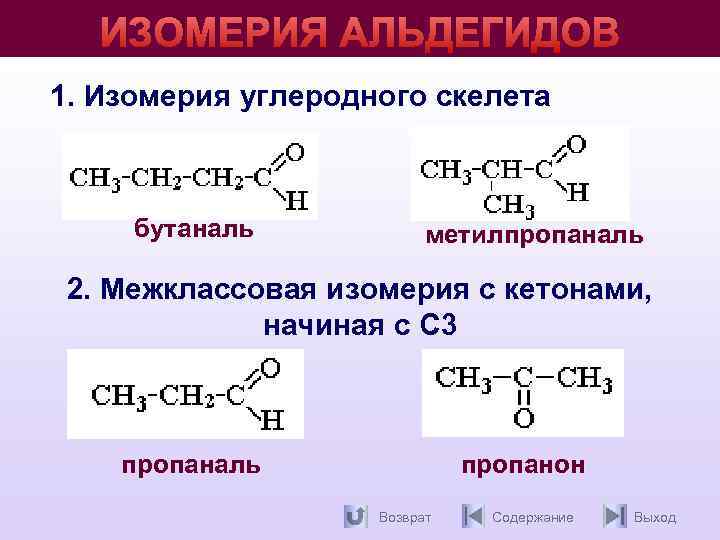 ИЗОМЕРИЯ АЛЬДЕГИДОВ 1. Изомерия углеродного скелета бутаналь метилпропаналь 2. Межклассовая изомерия с кетонами, начиная с С 3 пропаналь пропанон Возврат Содержание Выход
ИЗОМЕРИЯ АЛЬДЕГИДОВ 1. Изомерия углеродного скелета бутаналь метилпропаналь 2. Межклассовая изомерия с кетонами, начиная с С 3 пропаналь пропанон Возврат Содержание Выход
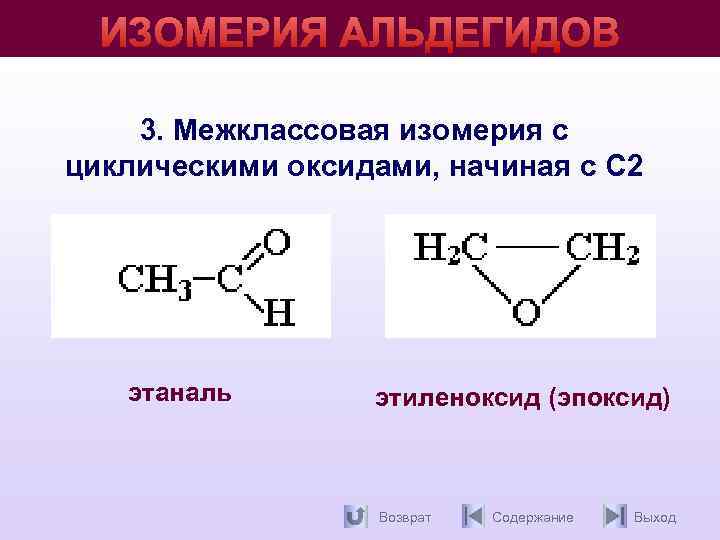 ИЗОМЕРИЯ АЛЬДЕГИДОВ 3. Межклассовая изомерия с циклическими оксидами, начиная с С 2 этаналь этиленоксид (эпоксид) Возврат Содержание Выход
ИЗОМЕРИЯ АЛЬДЕГИДОВ 3. Межклассовая изомерия с циклическими оксидами, начиная с С 2 этаналь этиленоксид (эпоксид) Возврат Содержание Выход
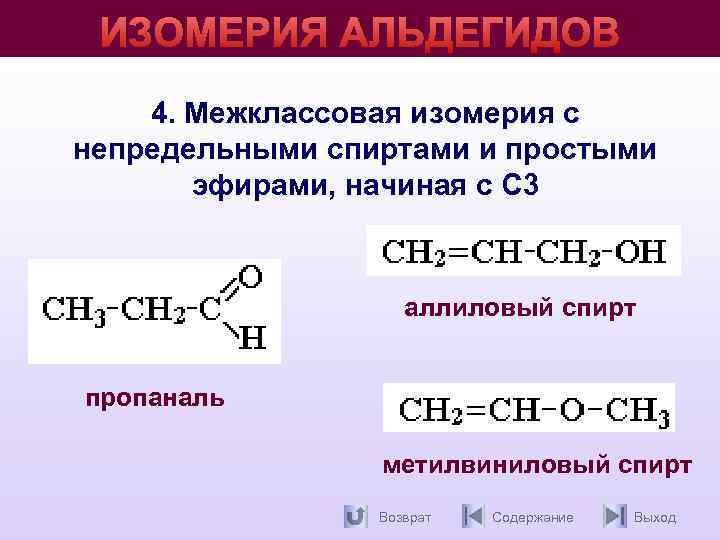 ИЗОМЕРИЯ АЛЬДЕГИДОВ 4. Межклассовая изомерия с непредельными спиртами и простыми эфирами, начиная с С 3 аллиловый спирт пропаналь метилвиниловый спирт Возврат Содержание Выход
ИЗОМЕРИЯ АЛЬДЕГИДОВ 4. Межклассовая изомерия с непредельными спиртами и простыми эфирами, начиная с С 3 аллиловый спирт пропаналь метилвиниловый спирт Возврат Содержание Выход
 ИЗОМЕРИЯ КЕТОНОВ 1. Изомерия углеродного скелета (с С 5) пентанон-2 3 -метилбутанон-2 2. Изомерия положения кетогруппы (с С 5) пентанон-2 пентанон-3 Возврат Содержание Выход
ИЗОМЕРИЯ КЕТОНОВ 1. Изомерия углеродного скелета (с С 5) пентанон-2 3 -метилбутанон-2 2. Изомерия положения кетогруппы (с С 5) пентанон-2 пентанон-3 Возврат Содержание Выход
 ФИЗИЧЕСКИЕ СВОЙСТВА АЛЬДЕГИДОВ И КЕТОНОВ • Метаналь – газ с характерным неприятным запахом, пропанон (ацетон) – жидкость. • Последующие гомологи метаналя и ацетона – жидкости. • Высшие альдегиды и кетоны – твердые вещества, обладают приятным запахом. • Альдегиды и кетоны растворимы в воде, растворимость ухудшается по мере увеличения молекулярной массы. Возврат Содержание Выход
ФИЗИЧЕСКИЕ СВОЙСТВА АЛЬДЕГИДОВ И КЕТОНОВ • Метаналь – газ с характерным неприятным запахом, пропанон (ацетон) – жидкость. • Последующие гомологи метаналя и ацетона – жидкости. • Высшие альдегиды и кетоны – твердые вещества, обладают приятным запахом. • Альдегиды и кетоны растворимы в воде, растворимость ухудшается по мере увеличения молекулярной массы. Возврат Содержание Выход
 ПОЛУЧЕНИЕ АЛЬДЕГИДОВ И КЕТОНОВ 1. ОКИСЛИТЕЛЬНОЕ ДЕГИДРИРОВАНИЕ СПИРТОВ: При окислении первичных спиртов образуются альдегиды СН 3 -СН 2 -СН 2 -ОН Cu, t СН 3 -СН 2 -С бутаналь бутанол О Н + H 2 При окислении вторичных спиртов образуются кетоны СН 3 -СН 2 -СН-СН 3 ОН бутанол-2 Cu, t СН 3 -С-СН 2 -СН 3 + H 2 О О бутанон Возврат Содержание Выход
ПОЛУЧЕНИЕ АЛЬДЕГИДОВ И КЕТОНОВ 1. ОКИСЛИТЕЛЬНОЕ ДЕГИДРИРОВАНИЕ СПИРТОВ: При окислении первичных спиртов образуются альдегиды СН 3 -СН 2 -СН 2 -ОН Cu, t СН 3 -СН 2 -С бутаналь бутанол О Н + H 2 При окислении вторичных спиртов образуются кетоны СН 3 -СН 2 -СН-СН 3 ОН бутанол-2 Cu, t СН 3 -С-СН 2 -СН 3 + H 2 О О бутанон Возврат Содержание Выход
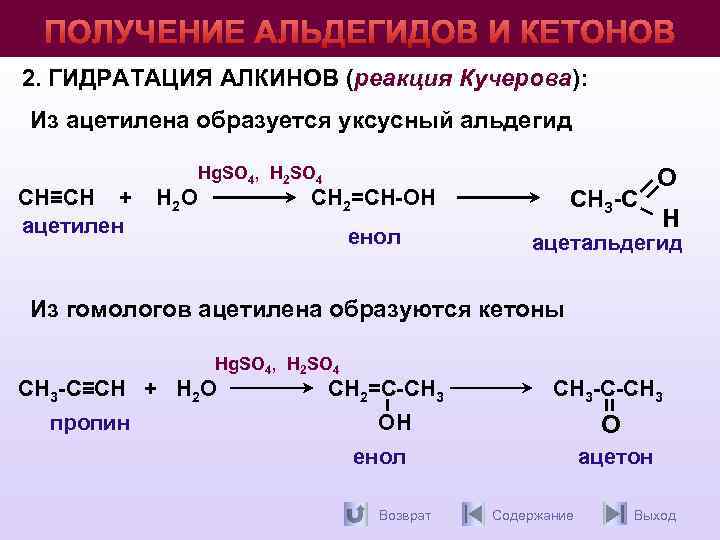 ПОЛУЧЕНИЕ АЛЬДЕГИДОВ И КЕТОНОВ 2. ГИДРАТАЦИЯ АЛКИНОВ (реакция Кучерова): Кучерова Из ацетилена образуется уксусный альдегид CН≡CH + ацетилен Н 2 О Hg. SO 4, H 2 SO 4 О СН 2=CH-ОН СН 3 -С енол ацетальдегид Н Из гомологов ацетилена образуются кетоны Hg. SO 4, H 2 SO 4 СН 3 -C≡CH + Н 2 О пропин СН 2=C-СН 3 -С-СН 3 ОН О енол Возврат ацетон Содержание Выход
ПОЛУЧЕНИЕ АЛЬДЕГИДОВ И КЕТОНОВ 2. ГИДРАТАЦИЯ АЛКИНОВ (реакция Кучерова): Кучерова Из ацетилена образуется уксусный альдегид CН≡CH + ацетилен Н 2 О Hg. SO 4, H 2 SO 4 О СН 2=CH-ОН СН 3 -С енол ацетальдегид Н Из гомологов ацетилена образуются кетоны Hg. SO 4, H 2 SO 4 СН 3 -C≡CH + Н 2 О пропин СН 2=C-СН 3 -С-СН 3 ОН О енол Возврат ацетон Содержание Выход
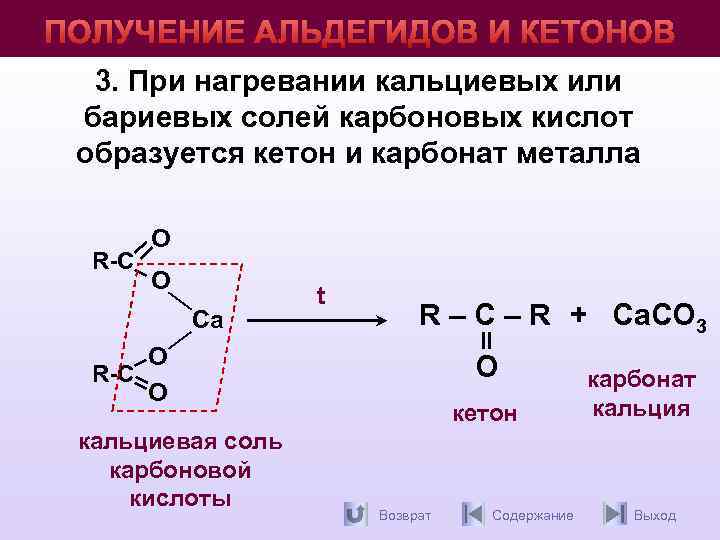 ПОЛУЧЕНИЕ АЛЬДЕГИДОВ И КЕТОНОВ 3. При нагревании кальциевых или бариевых солей карбоновых кислот образуется кетон и карбонат металла R-С О О Ca t R – С – R + Ca. CO 3 О R-С О кальциевая соль карбоновой кислоты О кетон Возврат Содержание карбонат кальция Выход
ПОЛУЧЕНИЕ АЛЬДЕГИДОВ И КЕТОНОВ 3. При нагревании кальциевых или бариевых солей карбоновых кислот образуется кетон и карбонат металла R-С О О Ca t R – С – R + Ca. CO 3 О R-С О кальциевая соль карбоновой кислоты О кетон Возврат Содержание карбонат кальция Выход
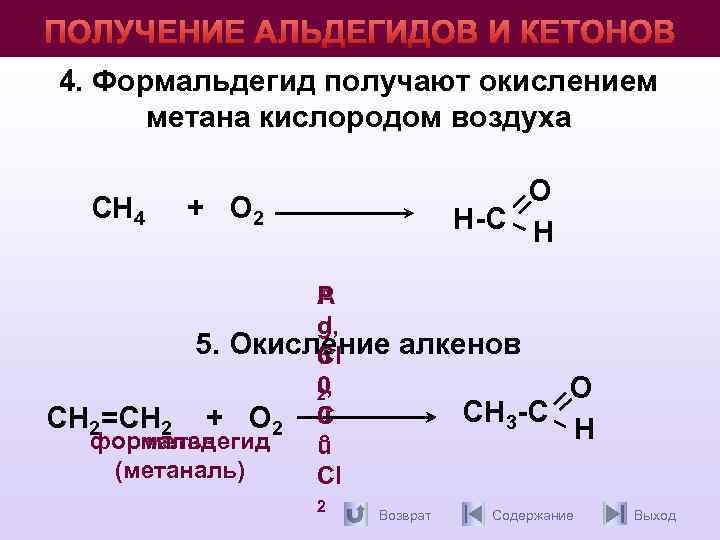 ПОЛУЧЕНИЕ АЛЬДЕГИДОВ И КЕТОНОВ 4. Формальдегид получают окислением метана кислородом воздуха СН 4 О H-С Н + О 2 P A d g, 5. Окисление Cl 5 0, 2 C СН 2=СН 2 + О 2 0 формальдегид метан º u (метаналь) Cl C 2 алкенов Возврат О СH 3 -С Н Содержание Выход
ПОЛУЧЕНИЕ АЛЬДЕГИДОВ И КЕТОНОВ 4. Формальдегид получают окислением метана кислородом воздуха СН 4 О H-С Н + О 2 P A d g, 5. Окисление Cl 5 0, 2 C СН 2=СН 2 + О 2 0 формальдегид метан º u (метаналь) Cl C 2 алкенов Возврат О СH 3 -С Н Содержание Выход
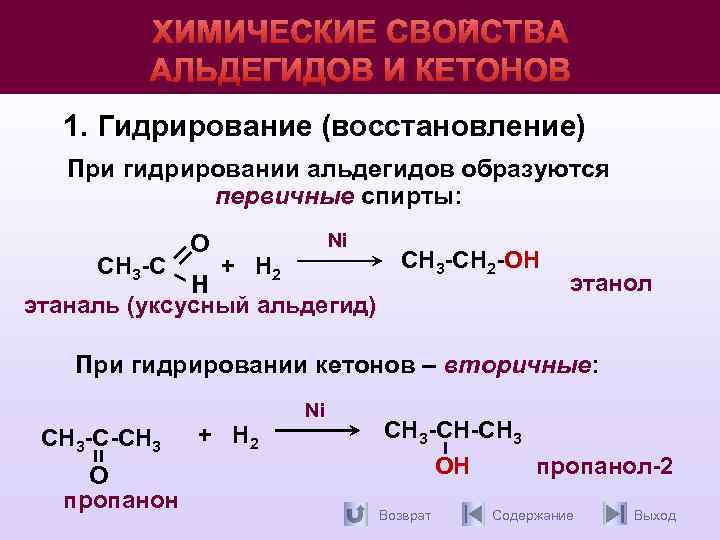 ХИМИЧЕСКИЕ СВОЙСТВА АЛЬДЕГИДОВ И КЕТОНОВ 1. Гидрирование (восстановление) При гидрировании альдегидов образуются первичные спирты: СН 3 -С О Ni + H 2 Н этаналь (уксусный альдегид) СН 3 -СН 2 -OH этанол При гидрировании кетонов – вторичные: вторичные СН 3 -С-СН 3 О пропанон + H 2 Ni СН 3 -СН-СН 3 ОН Возврат пропанол-2 Содержание Выход
ХИМИЧЕСКИЕ СВОЙСТВА АЛЬДЕГИДОВ И КЕТОНОВ 1. Гидрирование (восстановление) При гидрировании альдегидов образуются первичные спирты: СН 3 -С О Ni + H 2 Н этаналь (уксусный альдегид) СН 3 -СН 2 -OH этанол При гидрировании кетонов – вторичные: вторичные СН 3 -С-СН 3 О пропанон + H 2 Ni СН 3 -СН-СН 3 ОН Возврат пропанол-2 Содержание Выход
![ОКИСЛЕНИЕ АЛЬДЕГИДОВ 2. Окисление кислородом воздуха: R–С [O] О Н альдегид R–С О OН ОКИСЛЕНИЕ АЛЬДЕГИДОВ 2. Окисление кислородом воздуха: R–С [O] О Н альдегид R–С О OН](https://present5.com/presentation/139871603_143784957/image-16.jpg) ОКИСЛЕНИЕ АЛЬДЕГИДОВ 2. Окисление кислородом воздуха: R–С [O] О Н альдегид R–С О OН карбоновая кислота ПРИМЕР: СН 3 -СН 2 -С О Н [O] СН 3 -СН 2 -С бутаналь О OН бутановая кислота Возврат Содержание Выход
ОКИСЛЕНИЕ АЛЬДЕГИДОВ 2. Окисление кислородом воздуха: R–С [O] О Н альдегид R–С О OН карбоновая кислота ПРИМЕР: СН 3 -СН 2 -С О Н [O] СН 3 -СН 2 -С бутаналь О OН бутановая кислота Возврат Содержание Выход
 ОКИСЛЕНИЕ АЛЬДЕГИДОВ 3. РЕАКЦИЯ СЕРЕБРЯНОГО ЗЕРКАЛА – качественная реакция на наличие альдегидной группы № 1 R–С О Н альдегид + Ag 2 O t R–С О OН + 2 Ag карбоновая кислота Образующееся в реакции серебро покрывает поверхность сосуда тонкой ровной пленкой. Эту реакцию используют для изготовления зеркал, серебрения украшений, изготовления игрушек. Возврат Содержание Выход
ОКИСЛЕНИЕ АЛЬДЕГИДОВ 3. РЕАКЦИЯ СЕРЕБРЯНОГО ЗЕРКАЛА – качественная реакция на наличие альдегидной группы № 1 R–С О Н альдегид + Ag 2 O t R–С О OН + 2 Ag карбоновая кислота Образующееся в реакции серебро покрывает поверхность сосуда тонкой ровной пленкой. Эту реакцию используют для изготовления зеркал, серебрения украшений, изготовления игрушек. Возврат Содержание Выход
 ОКИСЛЕНИЕ АЛЬДЕГИДОВ 4. Окислителем альдегидов может выступать свежеосажденный гидроксид меди (II). Образовавшийся в ходе реакции гидроксид меди (I) Cu. OH сразу разлагается на оксид меди (I) красного цвета и воду. Качественная реакция на альдегидную группу № 2 R–С О + 2 Cu(OH)2 Н альдегид t R–С О OН карбоновая кислота + Cu. O + 2 H 2 O красно-бурый мелкокристаллический осадок Возврат Содержание Выход
ОКИСЛЕНИЕ АЛЬДЕГИДОВ 4. Окислителем альдегидов может выступать свежеосажденный гидроксид меди (II). Образовавшийся в ходе реакции гидроксид меди (I) Cu. OH сразу разлагается на оксид меди (I) красного цвета и воду. Качественная реакция на альдегидную группу № 2 R–С О + 2 Cu(OH)2 Н альдегид t R–С О OН карбоновая кислота + Cu. O + 2 H 2 O красно-бурый мелкокристаллический осадок Возврат Содержание Выход
 ХИМИЧЕСКИЕ СВОЙСТВА АЛЬДЕГИДОВ И КЕТОНОВ 5. Альдегиды и кетоны реагируют с галогенами, вступая в реакции замещения (α-галогенирования) даже в отсутствие освещения: Br Н О О t α α R–С–С + Br 2 + HBr R–С–С Н Н альдегид Н α R–С–С Н кетон О R + Br 2 t Br α R–С–С Н Возврат О R Содержание + HBr Выход
ХИМИЧЕСКИЕ СВОЙСТВА АЛЬДЕГИДОВ И КЕТОНОВ 5. Альдегиды и кетоны реагируют с галогенами, вступая в реакции замещения (α-галогенирования) даже в отсутствие освещения: Br Н О О t α α R–С–С + Br 2 + HBr R–С–С Н Н альдегид Н α R–С–С Н кетон О R + Br 2 t Br α R–С–С Н Возврат О R Содержание + HBr Выход
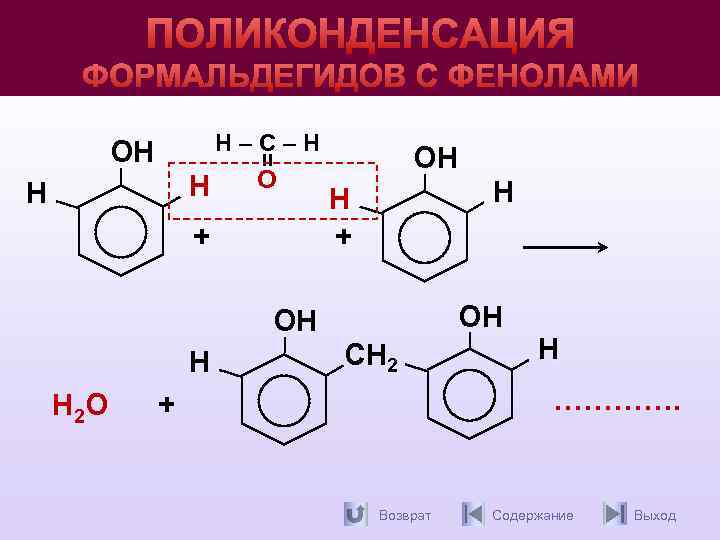 ПОЛИКОНДЕНСАЦИЯ ФОРМАЛЬДЕГИДОВ С ФЕНОЛАМИ Н–С–Н ОН Н Н О + ОН Н Н 2 О ОН Н + Н ОН СН 2 Н …………. + Возврат Содержание Выход
ПОЛИКОНДЕНСАЦИЯ ФОРМАЛЬДЕГИДОВ С ФЕНОЛАМИ Н–С–Н ОН Н Н О + ОН Н Н 2 О ОН Н + Н ОН СН 2 Н …………. + Возврат Содержание Выход
 ПОЛИКОНДЕНСАЦИЯ АЛЬДЕГИДОВ С ФЕНОЛАМИ Полимеры на основе фенолформальдегидных смол применяются для изготовления лаков и красок. Пластмассовые изделия, изготовленные на основе этих смол, устойчивы к нагреванию, охлаждению, действию воды, щелочей и кислот, они также обладают высокими диэлектрическими свойствами. Возврат Содержание Выход
ПОЛИКОНДЕНСАЦИЯ АЛЬДЕГИДОВ С ФЕНОЛАМИ Полимеры на основе фенолформальдегидных смол применяются для изготовления лаков и красок. Пластмассовые изделия, изготовленные на основе этих смол, устойчивы к нагреванию, охлаждению, действию воды, щелочей и кислот, они также обладают высокими диэлектрическими свойствами. Возврат Содержание Выход
 ПОЛИКОНДЕНСАЦИЯ АЛЬДЕГИДОВ С ФЕНОЛАМИ Из полимеров на основе фенолформальдегидных смол изготавливают наиболее важные детали электроприборов, корпуса силовых агрегатов и детали машин, полимерную основу печатных плат для радиоприборов. Возврат Содержание Выход
ПОЛИКОНДЕНСАЦИЯ АЛЬДЕГИДОВ С ФЕНОЛАМИ Из полимеров на основе фенолформальдегидных смол изготавливают наиболее важные детали электроприборов, корпуса силовых агрегатов и детали машин, полимерную основу печатных плат для радиоприборов. Возврат Содержание Выход
 ПОЛИКОНДЕНСАЦИЯ АЛЬДЕГИДОВ С ФЕНОЛАМИ Клеи на основе фенолформальдегидных смол способны надежно соединять детали самой различной природы, сохраняя высокую прочность соединения в очень широком диапазоне температур. Возврат Содержание Выход
ПОЛИКОНДЕНСАЦИЯ АЛЬДЕГИДОВ С ФЕНОЛАМИ Клеи на основе фенолформальдегидных смол способны надежно соединять детали самой различной природы, сохраняя высокую прочность соединения в очень широком диапазоне температур. Возврат Содержание Выход
 Применение альдегидов и кетонов Метаналь (муравьиный альдегид, формальдегид) • получение фенолформальдегидных смол; • получение мочевино-формальдегидных (карбамидных) смол; • полиоксиметиленовые полимеры; • синтез лекарственных средств (уротропин); • дезинфицирующее средство; • консервант биологических препаратов Возврат Содержание Выход (благодаря способности свертывать белок).
Применение альдегидов и кетонов Метаналь (муравьиный альдегид, формальдегид) • получение фенолформальдегидных смол; • получение мочевино-формальдегидных (карбамидных) смол; • полиоксиметиленовые полимеры; • синтез лекарственных средств (уротропин); • дезинфицирующее средство; • консервант биологических препаратов Возврат Содержание Выход (благодаря способности свертывать белок).
 Применение альдегидов и кетонов Этаналь (уксусный альдегид, ацетальдегид) • производство уксусной кислоты; • органический синтез – пластмассы, ацетатное волокно. ЯДОВИТ! Ацетон • растворитель лаков, красок, ацетатов Возврат Содержание Выход
Применение альдегидов и кетонов Этаналь (уксусный альдегид, ацетальдегид) • производство уксусной кислоты; • органический синтез – пластмассы, ацетатное волокно. ЯДОВИТ! Ацетон • растворитель лаков, красок, ацетатов Возврат Содержание Выход
 ЛИЕТРАТУРА 1. «Химия» / ред. О. С. Габриеляна – М. : Изд. центр «Академия» – Учебник для профессий и специальностей естественнонаучного профиля – 2011. – 384 с. 2. «Химия 10 класс» / О. С. Габриелян, Ф. Н. Маскаев, С. Ю. Пономарев, В. И. Теренин – М. : Дрофа – Учебник – профильный уровень – 2011. – 318 с. 3. «Химия в тестах, задачах и упражнениях» / О. С. Габриелян, Г. Г. Лысова – М. : Изд. центр «Академия» – учебное пособие для студентов сред. проф. образования – 2012. – 224 с. Возврат Содержание Выход
ЛИЕТРАТУРА 1. «Химия» / ред. О. С. Габриеляна – М. : Изд. центр «Академия» – Учебник для профессий и специальностей естественнонаучного профиля – 2011. – 384 с. 2. «Химия 10 класс» / О. С. Габриелян, Ф. Н. Маскаев, С. Ю. Пономарев, В. И. Теренин – М. : Дрофа – Учебник – профильный уровень – 2011. – 318 с. 3. «Химия в тестах, задачах и упражнениях» / О. С. Габриелян, Г. Г. Лысова – М. : Изд. центр «Академия» – учебное пособие для студентов сред. проф. образования – 2012. – 224 с. Возврат Содержание Выход
 Конец работы. Вы действительно хотите закончить работу с информационным материалом темы «Альдегиды. Кетоны» ? Да Нет
Конец работы. Вы действительно хотите закончить работу с информационным материалом темы «Альдегиды. Кетоны» ? Да Нет


