АКТУАЛЬНЫЕ ВОПРОСЫ ТРАНСПЛАНТОЛОГИИ.ppt
- Количество слайдов: 80
 АКТУАЛЬНЫЕ ВОПРОСЫ ТРАНСПЛАНТОЛОГИИ к. м. н. Минаева Н. К.
АКТУАЛЬНЫЕ ВОПРОСЫ ТРАНСПЛАНТОЛОГИИ к. м. н. Минаева Н. К.
 Трансплантология /лат. transplantare - пересаживать, греч. logos – учение/ отрасль биологии и медицины, изучающая проблемы трансплантации, разрабатывающая методы консервирования органов и тканей, создания и применения искусственных органов
Трансплантология /лат. transplantare - пересаживать, греч. logos – учение/ отрасль биологии и медицины, изучающая проблемы трансплантации, разрабатывающая методы консервирования органов и тканей, создания и применения искусственных органов
 История трансплантологии Библейская «золотая легенда» Сыновья сицилийского лекаря христиане-чудотворцы Косма и Дамиан в 3 -4 в. н. э. пересадили ногу мавра белому аббату и были за это казнены
История трансплантологии Библейская «золотая легенда» Сыновья сицилийского лекаря христиане-чудотворцы Косма и Дамиан в 3 -4 в. н. э. пересадили ногу мавра белому аббату и были за это казнены
 - Китайский хирург Хуа-То - 2 в. н. э. пересадка внутренних органов - 1597 г. Тальякоцци - пересадка лоскута ткани верхней конечности для восстановления формы носа (итальянский метод кожной пластики)
- Китайский хирург Хуа-То - 2 в. н. э. пересадка внутренних органов - 1597 г. Тальякоцци - пересадка лоскута ткани верхней конечности для восстановления формы носа (итальянский метод кожной пластики)
 Основы научной трансплантологии были заложены в начале 19 века -1804 г. Бароньо - аутотрансплантация кожи у овец - отечественные хирурги Н. И. Пирогов, Ю. К. Шимановский, К. М. Сапежко (пластика) -1869 г. Реверден – пересадка кожи - 1874 г. Тирш – трансплантация кожных лоскутов
Основы научной трансплантологии были заложены в начале 19 века -1804 г. Бароньо - аутотрансплантация кожи у овец - отечественные хирурги Н. И. Пирогов, Ю. К. Шимановский, К. М. Сапежко (пластика) -1869 г. Реверден – пересадка кожи - 1874 г. Тирш – трансплантация кожных лоскутов
 Трансплантология в 20 веке 1902 г. Улльманом - пересадка почечного аллотрансплантата с анастомозированием почечных сосудов с магистральными кровеносными сосудами шеи в эксперименте на собаке, вскоре после него Каррелем
Трансплантология в 20 веке 1902 г. Улльманом - пересадка почечного аллотрансплантата с анастомозированием почечных сосудов с магистральными кровеносными сосудами шеи в эксперименте на собаке, вскоре после него Каррелем
 Ø 1902 -1905 г. г. француз Алексис Каррель - техника сосудистых анастомозов, впервые в эксперименте – трансплантация сердца Ø 1900 г. австрийский иммунолог Ландштейнер - группы крови АВО, Ø 1940 г. Ландштейнер и Винер - резус -фактор
Ø 1902 -1905 г. г. француз Алексис Каррель - техника сосудистых анастомозов, впервые в эксперименте – трансплантация сердца Ø 1900 г. австрийский иммунолог Ландштейнер - группы крови АВО, Ø 1940 г. Ландштейнер и Винер - резус -фактор
 П. И. Бахметьев (1899 -1912), Ф. А. Андреев (1913), Н. П. Кравков (1924) - открытие трансплантационного иммунитета Ø А. А. Кулябко (1902) - восстановление деятельности изолированного сердца, взятого от трупа человека Ø В. Н. Шамов (1928), С. С. Юдин (1930) переливание фибринолизной трупной крови Ø З. П. Филатов (1931) - пересадка роговицы трупа Ø Н. М. Михельсон (1935) – пересадка трупного хряща Ø
П. И. Бахметьев (1899 -1912), Ф. А. Андреев (1913), Н. П. Кравков (1924) - открытие трансплантационного иммунитета Ø А. А. Кулябко (1902) - восстановление деятельности изолированного сердца, взятого от трупа человека Ø В. Н. Шамов (1928), С. С. Юдин (1930) переливание фибринолизной трупной крови Ø З. П. Филатов (1931) - пересадка роговицы трупа Ø Н. М. Михельсон (1935) – пересадка трупного хряща Ø
 Ø 1926 -1928 гг. С. Брюхоненко создание и применение в эксперименте аппарата искусственного кровообращения Ø 1933 г. Ю. Ю. Вороной - впервые в мире пересадка трупной почки человеку с целью искусственного гемодиализа при ртутном отравлении и острой почечной недостаточности
Ø 1926 -1928 гг. С. Брюхоненко создание и применение в эксперименте аппарата искусственного кровообращения Ø 1933 г. Ю. Ю. Вороной - впервые в мире пересадка трупной почки человеку с целью искусственного гемодиализа при ртутном отравлении и острой почечной недостаточности
 Ø 1942 -1945 гг. английский иммунолог Медавар - иммунологическая природа отторжения трансплантата Ø 1939 г. Н. П. Синицын - впервые в мире полная замена сердца у лягушек ( жили после операции больше года) Ø 1948 г. - монография "Пересадка сердца как новый метод в биологии и медицине"
Ø 1942 -1945 гг. английский иммунолог Медавар - иммунологическая природа отторжения трансплантата Ø 1939 г. Н. П. Синицын - впервые в мире полная замена сердца у лягушек ( жили после операции больше года) Ø 1948 г. - монография "Пересадка сердца как новый метод в биологии и медицине"
 1946 -1960 гг. В. П. Демихов - впервые в мире на собаке пересадка сердечно-легочного комплекса, второго сердца в грудную полость и второй головы Ø 1959 – 1962 гг. – подавление реакции отторжения тотальным облучением тела реципиента Ø 1961 г. – использование цитостатика азатиоприна (имурана) Ø 1963 г. – имуран + преднизолон – стандартный режим иммуносупрессии Ø 1963 г. Харди - пересадка легкого (больной прожил 18 дней) Ø 1963 г. Старлз (США) – ортотопическая пересадка печени человеку Ø
1946 -1960 гг. В. П. Демихов - впервые в мире на собаке пересадка сердечно-легочного комплекса, второго сердца в грудную полость и второй головы Ø 1959 – 1962 гг. – подавление реакции отторжения тотальным облучением тела реципиента Ø 1961 г. – использование цитостатика азатиоприна (имурана) Ø 1963 г. – имуран + преднизолон – стандартный режим иммуносупрессии Ø 1963 г. Харди - пересадка легкого (больной прожил 18 дней) Ø 1963 г. Старлз (США) – ортотопическая пересадка печени человеку Ø
 Ø 1963 г. Фишер (Бостон) - первая аллотрансплантация тонкой кишки Ø 1966 г. Келли и Лиллихей в (Миннесотская университетская клиника) - первая аллотрансплантация поджелудочной железы
Ø 1963 г. Фишер (Бостон) - первая аллотрансплантация тонкой кишки Ø 1966 г. Келли и Лиллихей в (Миннесотская университетская клиника) - первая аллотрансплантация поджелудочной железы
 Ø 1967 г. Кристиан Барнард - ортотопическая пересадка сердца человеку (пациент Вашканский вошел в историю, прожил 18 дней) Ø 1982 г. Рейтц – первая успешная трансплантация «сердце-легкие» человеку
Ø 1967 г. Кристиан Барнард - ортотопическая пересадка сердца человеку (пациент Вашканский вошел в историю, прожил 18 дней) Ø 1982 г. Рейтц – первая успешная трансплантация «сердце-легкие» человеку
 Ø 1976 г. - иммунодепрессант циклоспорин А (сандиммун) – резкое снижение кризов отторжения Ø 1965 г. Б. В. Петровский - пересадка почки Ø 1987 г. В. И. Щумаков - пересадка сердца Ø 1989 г. С. В. Готье и А. К. Ерамишанцев – пересадка печени
Ø 1976 г. - иммунодепрессант циклоспорин А (сандиммун) – резкое снижение кризов отторжения Ø 1965 г. Б. В. Петровский - пересадка почки Ø 1987 г. В. И. Щумаков - пересадка сердца Ø 1989 г. С. В. Готье и А. К. Ерамишанцев – пересадка печени
 Ø 1992 г. - Закон РФ о трансплантации органов и /или/ тканей человека Ø Трансплантация органов и/или/ тканей от живого донора или трупа может быть применена только в случае, если другие медицинские средства не могут гарантировать сохранение жизни больного /реципиента/ либо восстановления его здоровья
Ø 1992 г. - Закон РФ о трансплантации органов и /или/ тканей человека Ø Трансплантация органов и/или/ тканей от живого донора или трупа может быть применена только в случае, если другие медицинские средства не могут гарантировать сохранение жизни больного /реципиента/ либо восстановления его здоровья
 Термины в трансплантологии l l аутотрансплантация - пересадка реципиенту собственного органа или ткани аллотрансплантация - пересадка органа от донора того же биологического вида /например от человека к человеку аллопластическая трансплантация - замена органа или ткани синтетическими материалами изогенная трансплантация - трансплантация, при которой донор к реципиент являются однояйцовыми близнецами
Термины в трансплантологии l l аутотрансплантация - пересадка реципиенту собственного органа или ткани аллотрансплантация - пересадка органа от донора того же биологического вида /например от человека к человеку аллопластическая трансплантация - замена органа или ткани синтетическими материалами изогенная трансплантация - трансплантация, при которой донор к реципиент являются однояйцовыми близнецами
 • сингенная трансплантация - трансплантация, при которой донор и реципиент являются родственниками первой степени • ксенотрансплантация - пересадка органа от донора другого биологического вида (например, от обезьяны к человеку) • имплантация - вживление в организм реципиента искусственного органа • ортотопическая трансплантация - пересадка органа в типичную анатомическую позицию • гетеротопическая трансплантация пересадка органа в атипичную анатомическую позицию
• сингенная трансплантация - трансплантация, при которой донор и реципиент являются родственниками первой степени • ксенотрансплантация - пересадка органа от донора другого биологического вида (например, от обезьяны к человеку) • имплантация - вживление в организм реципиента искусственного органа • ортотопическая трансплантация - пересадка органа в типичную анатомическую позицию • гетеротопическая трансплантация пересадка органа в атипичную анатомическую позицию
 • кондиционирование донора - совокупность медицинских мероприятий, направленных на поддержание жизнеспособности и сохранение органов, планируемых к забору и трансплантации у доноров-трупов (ИВЛ, наружное согревание, активная медикаментозная терапия и т. д. ) • донор труп - пациент с констатированной и документированной смертью мозга, при этом могут сохраняться функции других жизненно важных органов и спинальный автоматизм • перивитальный орган – орган -трансплантат, изъятый у донора
• кондиционирование донора - совокупность медицинских мероприятий, направленных на поддержание жизнеспособности и сохранение органов, планируемых к забору и трансплантации у доноров-трупов (ИВЛ, наружное согревание, активная медикаментозная терапия и т. д. ) • донор труп - пациент с констатированной и документированной смертью мозга, при этом могут сохраняться функции других жизненно важных органов и спинальный автоматизм • перивитальный орган – орган -трансплантат, изъятый у донора
 Органы и ткани могут быть изъяты у трупа для трансплантации, если имеются бесспорные доказательства факта смерти, зафиксированного консилиумом врачейспециалистов Ø Ответственность за диагноз смерти человека полностью лежит на устанавливающих смерть мозга врачах того лечебного учреждения, где умер больной Ø Заключение о смерти дается на основании констатации необратимой гибели всего головного мозга (смерть мозга) Ø
Органы и ткани могут быть изъяты у трупа для трансплантации, если имеются бесспорные доказательства факта смерти, зафиксированного консилиумом врачейспециалистов Ø Ответственность за диагноз смерти человека полностью лежит на устанавливающих смерть мозга врачах того лечебного учреждения, где умер больной Ø Заключение о смерти дается на основании констатации необратимой гибели всего головного мозга (смерть мозга) Ø
 Признаки смерти мозга полное и необратимое прекращение всех его функций, включая ствол, в условиях сохранившейся сердечно сосудистой деятельности и искусственного поддержания газообмена
Признаки смерти мозга полное и необратимое прекращение всех его функций, включая ствол, в условиях сохранившейся сердечно сосудистой деятельности и искусственного поддержания газообмена
 Клинические признаки смерти мозга Ø глубокая кома Ø апноэ двусторонний мидриаз с отсутствием фотореакции зрачков Ø отсутствие корнеальных, окулоцефалического, вестибулярного, кашлевого, глоточного и других рефлексов стволового уровня Ø
Клинические признаки смерти мозга Ø глубокая кома Ø апноэ двусторонний мидриаз с отсутствием фотореакции зрачков Ø отсутствие корнеальных, окулоцефалического, вестибулярного, кашлевого, глоточного и других рефлексов стволового уровня Ø
 Забор и заготовка органов и тканей человека разрешается только в государственных учреждениях здравоохранения, а их трансплантация только в специализированных учреждениях
Забор и заготовка органов и тканей человека разрешается только в государственных учреждениях здравоохранения, а их трансплантация только в специализированных учреждениях
 • Требуется разрешение на изъятие органов и тканей у трупа судебно медицинского эксперта с уведомлением об этом прокурора • Изъятие органов и тканей у трупа не допускается, если учреждение здравоохранения на момент изъятия поставлено в известность о том, что при жизни данное лицо либо его близкие родственники или законный представитель заявили о своем несогласии на изъятие его органов и тканей после смерти для трансплантации реципиенту
• Требуется разрешение на изъятие органов и тканей у трупа судебно медицинского эксперта с уведомлением об этом прокурора • Изъятие органов и тканей у трупа не допускается, если учреждение здравоохранения на момент изъятия поставлено в известность о том, что при жизни данное лицо либо его близкие родственники или законный представитель заявили о своем несогласии на изъятие его органов и тканей после смерти для трансплантации реципиенту
 Ø Изъятие органов и тканей у живого донора допустимо только в случае, если его здоровью по заключению консилиума врачей специалистов не будет причинен значительный вред Ø Изъятие органов и тканей для трансплантации не допускается у живого донора, не достигшего 18 лет (за исключением случаев пересадки костного мозга) либо признанного в установленном порядке недееспособным
Ø Изъятие органов и тканей у живого донора допустимо только в случае, если его здоровью по заключению консилиума врачей специалистов не будет причинен значительный вред Ø Изъятие органов и тканей для трансплантации не допускается у живого донора, не достигшего 18 лет (за исключением случаев пересадки костного мозга) либо признанного в установленном порядке недееспособным
 Изъятие органов и тканей у живого донора для трансплантации реципиенту допускается при соблюдении следующих условий если донор предупрежден о возможных осложнениях для его здоровья в связи с предстоящим оперативным вмешательством по изъятию органов и тканей Ø если донор свободно и сознательно в письменной форме выразил согласие на изъятие своих органов и тканей Ø если донор прошел всестороннее медицинское обследование и имеется заключение консилиума врачей -специалистов о возможности изъятия у него органов и тканей для трансплантации Ø
Изъятие органов и тканей у живого донора для трансплантации реципиенту допускается при соблюдении следующих условий если донор предупрежден о возможных осложнениях для его здоровья в связи с предстоящим оперативным вмешательством по изъятию органов и тканей Ø если донор свободно и сознательно в письменной форме выразил согласие на изъятие своих органов и тканей Ø если донор прошел всестороннее медицинское обследование и имеется заключение консилиума врачей -специалистов о возможности изъятия у него органов и тканей для трансплантации Ø
 Донор, изъявивший согласие на пересадку своих органов и тканей, имеет право требовать от учреждения здравоохранения полной информации о возможных осложнениях для его здоровья в связи с предстоящим оперативным вмешательством по изъятию органов и тканей Ø получать бесплатное лечение, в том числе медикаментозное, в связи с проведенной операцией Ø
Донор, изъявивший согласие на пересадку своих органов и тканей, имеет право требовать от учреждения здравоохранения полной информации о возможных осложнениях для его здоровья в связи с предстоящим оперативным вмешательством по изъятию органов и тканей Ø получать бесплатное лечение, в том числе медикаментозное, в связи с проведенной операцией Ø
 Ø У живого донора может быть изъят для трансплантации парный орган, часть органа или ткань, отсутствие которых не влечет за собой необратимого расстройства здоровья Ø Изъятие органов и тканей не допускается, если установлено, что они принадлежат лицу, страдающему болезнью, представляющей опасность для жизни и здоровья реципиента, а также у лиц, находящихся в служебной или личной зависимости от реципиента Ø Принуждение любым лицом живого донора к согласию на изъятие у него органов или тканей для трансплантации влечет уголовную ответственность в соответствии с законодательством РФ
Ø У живого донора может быть изъят для трансплантации парный орган, часть органа или ткань, отсутствие которых не влечет за собой необратимого расстройства здоровья Ø Изъятие органов и тканей не допускается, если установлено, что они принадлежат лицу, страдающему болезнью, представляющей опасность для жизни и здоровья реципиента, а также у лиц, находящихся в служебной или личной зависимости от реципиента Ø Принуждение любым лицом живого донора к согласию на изъятие у него органов или тканей для трансплантации влечет уголовную ответственность в соответствии с законодательством РФ
 Ø Врачам и иным сотрудникам учреждения здравоохранения запрещается разглашать сведения о доноре и реципиенте Ø Учреждению здравоохранения, которому разрешено проводить операции по забору и заготовке органов и тканей у трупа, запрещается осуществлять их продажу Ø Действие Закона не распространяется на препараты и пересадочные материалы, для подготовления которых использованы тканевые компоненты
Ø Врачам и иным сотрудникам учреждения здравоохранения запрещается разглашать сведения о доноре и реципиенте Ø Учреждению здравоохранения, которому разрешено проводить операции по забору и заготовке органов и тканей у трупа, запрещается осуществлять их продажу Ø Действие Закона не распространяется на препараты и пересадочные материалы, для подготовления которых использованы тканевые компоненты
 Забор и консервация донорских органов При учреждениях здравоохранения, которым разрешены трансплантация органов и забор органных трансплантатов, организуются выездные бригады специалистов по забору и заготовке органов Ø Срочная доставка реципиентов, доноров, органных и тканевых трансплантатов, бригад специалистов к месту назначения организуется силами и средствами скорой медицинской помощи и санитарной авиации Ø
Забор и консервация донорских органов При учреждениях здравоохранения, которым разрешены трансплантация органов и забор органных трансплантатов, организуются выездные бригады специалистов по забору и заготовке органов Ø Срочная доставка реципиентов, доноров, органных и тканевых трансплантатов, бригад специалистов к месту назначения организуется силами и средствами скорой медицинской помощи и санитарной авиации Ø
 В настоящее время техника операций изъятия и трансплантации паренхиматозных органов хорошо разработана и стандартизована Оптимальным считается мультиорганный забор, когда у одного донора трупа в течение одной операции изымаются несколько органов (сердце, печень, почки, легкие и т. д. )
В настоящее время техника операций изъятия и трансплантации паренхиматозных органов хорошо разработана и стандартизована Оптимальным считается мультиорганный забор, когда у одного донора трупа в течение одной операции изымаются несколько органов (сердце, печень, почки, легкие и т. д. )
 С момента прекращения кровообращения органа начинается период ишемии, который различные органы переносят неодинаково в соответствии со своими уникальными особенностями метаболизма
С момента прекращения кровообращения органа начинается период ишемии, который различные органы переносят неодинаково в соответствии со своими уникальными особенностями метаболизма
 Тепловая и холодовая ишемия Ø Тепловая ишемия продолжается с момента выделения, забора органа до начала гипотермии Ø Время тепловой ишемии очень короткое: для сердца и печени 20 минут, для поджелудочной железы 30 минут, для почки 45 минут, после этого начинаются необратимые изменения органов.
Тепловая и холодовая ишемия Ø Тепловая ишемия продолжается с момента выделения, забора органа до начала гипотермии Ø Время тепловой ишемии очень короткое: для сердца и печени 20 минут, для поджелудочной железы 30 минут, для почки 45 минут, после этого начинаются необратимые изменения органов.
 Для борьбы с ишемическими повреждениями изолированных органов используют 3 группы методов 1. 2. 3. биологической перфузии (поддержание исходного (оптимального) уровня метаболической активности в органах путем перфузии их кровью в нормотермическом или близком к нему режиме (34 З 8°С) гипотермической консервации (обеспечение сниженной, но адекватной метаболической активности трансплантата путем хранения его при температуре 8 -12°С (гипотермическая перфузия) или при температуре 2 -4°С (фармакохолодовая бесперфузионная консервация) глубокое охлаждение (криоконсервация) (обеспечение условий максимально полного обратимого прекращения метаболической активности в трансплантатах /срезы тканей, взвеси клеток/ путем хранения их при температурах ниже 0°С в замороженном состоянии)
Для борьбы с ишемическими повреждениями изолированных органов используют 3 группы методов 1. 2. 3. биологической перфузии (поддержание исходного (оптимального) уровня метаболической активности в органах путем перфузии их кровью в нормотермическом или близком к нему режиме (34 З 8°С) гипотермической консервации (обеспечение сниженной, но адекватной метаболической активности трансплантата путем хранения его при температуре 8 -12°С (гипотермическая перфузия) или при температуре 2 -4°С (фармакохолодовая бесперфузионная консервация) глубокое охлаждение (криоконсервация) (обеспечение условий максимально полного обратимого прекращения метаболической активности в трансплантатах /срезы тканей, взвеси клеток/ путем хранения их при температурах ниже 0°С в замороженном состоянии)
 Время холодовой ишемии для сердца 4 6 часов Ø поджелудочной железы 5 часов Ø для печени 8 часов Ø для почки 24 часа Ø На практике оптимальные сроки консервации определяются сроком доставки донорского органа в соответствующий центр и возможностью его трансплантации реципиенту
Время холодовой ишемии для сердца 4 6 часов Ø поджелудочной железы 5 часов Ø для печени 8 часов Ø для почки 24 часа Ø На практике оптимальные сроки консервации определяются сроком доставки донорского органа в соответствующий центр и возможностью его трансплантации реципиенту
 Смерть мозга может развиваться в результате его первичного и вторичного повреждения Ø Первичное тяжелая закрытая и открытая черепно-мозговая травма, спонтанные и иные внутричерепные кровоизлияния, инфаркт мозга, внутричерепные оперативные вмешательства Ø Вторичное в результате гипоксий различного генеза: при остановке сердца и прекращении или резком ухудшении системного кровообращения, вследствие длительно продолжающегося шока и др.
Смерть мозга может развиваться в результате его первичного и вторичного повреждения Ø Первичное тяжелая закрытая и открытая черепно-мозговая травма, спонтанные и иные внутричерепные кровоизлияния, инфаркт мозга, внутричерепные оперативные вмешательства Ø Вторичное в результате гипоксий различного генеза: при остановке сердца и прекращении или резком ухудшении системного кровообращения, вследствие длительно продолжающегося шока и др.
 Изъятие донорских органов оформляется специальным актом об изъятии донорских органов и медицинской экспертизе трупа, который прилагается к истории болезни
Изъятие донорских органов оформляется специальным актом об изъятии донорских органов и медицинской экспертизе трупа, который прилагается к истории болезни
 Подбор пар "донор реципиент" Ø Ø Решающими для приживления трансплантата являются антигены гистосовместимости групп крови АВ 0, резус-фактора и антигены гистосовместимости лейкоцитов НLА (эйч-эль-эй) Главный комплекс гистосовместимости (ГКГС) находится в 6 -ой хромосоме человека, он включает множество генов, число которых точно не установлено НLА-антигены, расположенные на поверхности клеток, могут быть определены с помощью серологических методов исследования, при которых используют сыворотки, содержащие антитела против специфических антигенов гистосовместимости Практическое значение имеет определение НLАА, В, С, Д, в том числе DR-антигенов
Подбор пар "донор реципиент" Ø Ø Решающими для приживления трансплантата являются антигены гистосовместимости групп крови АВ 0, резус-фактора и антигены гистосовместимости лейкоцитов НLА (эйч-эль-эй) Главный комплекс гистосовместимости (ГКГС) находится в 6 -ой хромосоме человека, он включает множество генов, число которых точно не установлено НLА-антигены, расположенные на поверхности клеток, могут быть определены с помощью серологических методов исследования, при которых используют сыворотки, содержащие антитела против специфических антигенов гистосовместимости Практическое значение имеет определение НLАА, В, С, Д, в том числе DR-антигенов
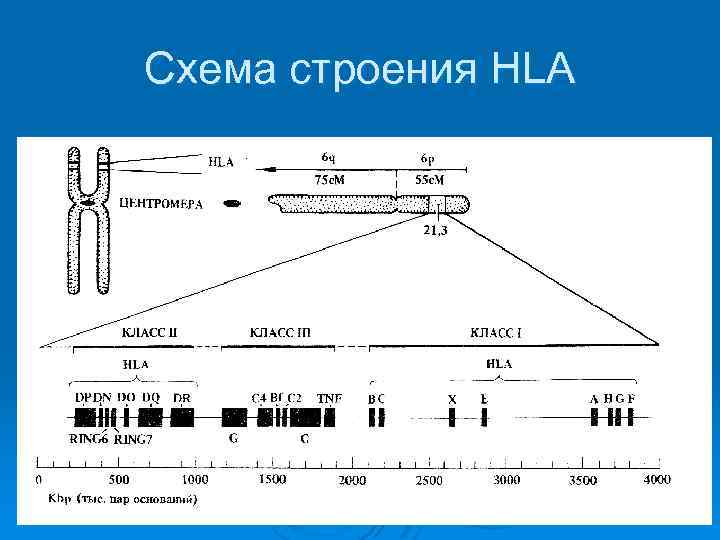 Схема строения HLA
Схема строения HLA
 С иммуногенетических позиций можно выделить несколько групп, в которых вероятность идентичности по НLА антигенам будет резко различаться 1. 2. 3. При пересадке между сиблингами, т. е. между индивидуумами, состоящими в степени родства "брат-брат" и т. п. , вероятность идентичности очень высока, так как у детей одних родителей вероятность наличия одинаковых гомологичных хромосом очень значительная При пересадке в комбинации "родитель-ребенок" эта вероятность значительно ниже, так как ребенок получает от родителей разный набор антигенов При пересадке между индивидуумами, не связанными кровным родством, вероятность идентичности по НLА-антигенам очень мала
С иммуногенетических позиций можно выделить несколько групп, в которых вероятность идентичности по НLА антигенам будет резко различаться 1. 2. 3. При пересадке между сиблингами, т. е. между индивидуумами, состоящими в степени родства "брат-брат" и т. п. , вероятность идентичности очень высока, так как у детей одних родителей вероятность наличия одинаковых гомологичных хромосом очень значительная При пересадке в комбинации "родитель-ребенок" эта вероятность значительно ниже, так как ребенок получает от родителей разный набор антигенов При пересадке между индивидуумами, не связанными кровным родством, вероятность идентичности по НLА-антигенам очень мала
 Виды отторжений Сверхострое отторжение развивается нередко уже в операционной, как только донорский орган включается в общий кровоток реципиента. Это обусловлено наличием антител у реципиента, направленных против антигенов донора, и чаще всего требует немедленного удаления пересаженного органа. Ведущая роль в этиопатогенезе сверхострого отторжения отводится гуморальным механизмам иммунного ответа
Виды отторжений Сверхострое отторжение развивается нередко уже в операционной, как только донорский орган включается в общий кровоток реципиента. Это обусловлено наличием антител у реципиента, направленных против антигенов донора, и чаще всего требует немедленного удаления пересаженного органа. Ведущая роль в этиопатогенезе сверхострого отторжения отводится гуморальным механизмам иммунного ответа
 Острое отторжение криз (или эпизод отторжения) развивается в первые дни, недели и месяцы послеоперационного периода и является результатом формирования реакции иммунологического распознавания и клеточно-опосредованного ответа реципиента на тканевые антигены донора
Острое отторжение криз (или эпизод отторжения) развивается в первые дни, недели и месяцы послеоперационного периода и является результатом формирования реакции иммунологического распознавания и клеточно-опосредованного ответа реципиента на тканевые антигены донора
 Хроническое отторжение характерно для более позднего периода, течет медленно и отличается специфическими изменениями, связанными с видом пересаженного органа. Отторжение почек характеризуется артериитом или гломерулонефритом, отторжение сердца у больных с ишемической болезнью нередко сопровождается поражением коронарных артерий
Хроническое отторжение характерно для более позднего периода, течет медленно и отличается специфическими изменениями, связанными с видом пересаженного органа. Отторжение почек характеризуется артериитом или гломерулонефритом, отторжение сердца у больных с ишемической болезнью нередко сопровождается поражением коронарных артерий
 Субклиническая форма криза отторжения напряженность трансплантационного иммунитета без явных клинических проявлений нарушения функции пересаженного органа, нередко лежит в основе хронических структурных нарушений
Субклиническая форма криза отторжения напряженность трансплантационного иммунитета без явных клинических проявлений нарушения функции пересаженного органа, нередко лежит в основе хронических структурных нарушений
 История подавления реакции отторжения пересаженного органа - - Тотальное облучение тела реципиента после трансплантации (1959 и 1962 гг. ) 1961 г. цитостатик азатиоприн (имуран) - при трансплантации почки 1963 г. имуран в комбинации с преднизолоном - после трансплантации почек и печени Комбинированная иммуносупрессия в сочетании с тщательным подбором пар "донор-реципиент" по лейкоцитарным антигенам системы HLА значительное улучшение результатов органных трансплантаций 1978 г. циклоспорин А - резко снизил кризы отторжения, показатели годичной выживаемости трансплантатов увеличились на 20 -30%
История подавления реакции отторжения пересаженного органа - - Тотальное облучение тела реципиента после трансплантации (1959 и 1962 гг. ) 1961 г. цитостатик азатиоприн (имуран) - при трансплантации почки 1963 г. имуран в комбинации с преднизолоном - после трансплантации почек и печени Комбинированная иммуносупрессия в сочетании с тщательным подбором пар "донор-реципиент" по лейкоцитарным антигенам системы HLА значительное улучшение результатов органных трансплантаций 1978 г. циклоспорин А - резко снизил кризы отторжения, показатели годичной выживаемости трансплантатов увеличились на 20 -30%
 Современная иммуносупрессивная терапия – "триплет схема” применяют пожизненно Ø циклоспорин А Ø сниженные дозы азатиоприна Ø глюкокортикоиды Для лечения кризов отторжения используют пульс терапию мегадозами глюкокортикоидов (преднизолон до 1500 мг/сут. в течение 2 -3 дней) Ø антилимфоцитарную сыворотку Ø препараты моноклональных антител к пан. Т- и Т 3 лимфоцитам (ортоклон ОКТЗ, мурамонаб и др. ) Ø
Современная иммуносупрессивная терапия – "триплет схема” применяют пожизненно Ø циклоспорин А Ø сниженные дозы азатиоприна Ø глюкокортикоиды Для лечения кризов отторжения используют пульс терапию мегадозами глюкокортикоидов (преднизолон до 1500 мг/сут. в течение 2 -3 дней) Ø антилимфоцитарную сыворотку Ø препараты моноклональных антител к пан. Т- и Т 3 лимфоцитам (ортоклон ОКТЗ, мурамонаб и др. ) Ø
 Трансплантация сердца Показания к трансплантации определяются коллегиально. Консилиум врачей (хирургтрансплантолог, кардиолог, гепатолог, нефролог, иммунологклиницист, психиатр и др. ) решает вопросы Ø Ø Ø действительно ли у пациента конечная стадия заболевания и какова продолжительность его жизни, существует ли для больного альтернатива трансплантации, переносима ли пациентом операция пересадки органа, позволяет ли состояние других органов пациента после пересадки пожизненно принимать иммуносупрессанты, может ли реципиенту быть гарантировано приемлемое качество жизни подготовлен ли больной психологически к трансплантации и сохранит ли он после нее эмоциональную устойчивость, контактность и интегральность личности
Трансплантация сердца Показания к трансплантации определяются коллегиально. Консилиум врачей (хирургтрансплантолог, кардиолог, гепатолог, нефролог, иммунологклиницист, психиатр и др. ) решает вопросы Ø Ø Ø действительно ли у пациента конечная стадия заболевания и какова продолжительность его жизни, существует ли для больного альтернатива трансплантации, переносима ли пациентом операция пересадки органа, позволяет ли состояние других органов пациента после пересадки пожизненно принимать иммуносупрессанты, может ли реципиенту быть гарантировано приемлемое качество жизни подготовлен ли больной психологически к трансплантации и сохранит ли он после нее эмоциональную устойчивость, контактность и интегральность личности
 Показания к операции трансплантации сердца Ø Ø Ø ишемическая болезнь сердца в терминальной стадии развития болезни кардиомиопатия клапанные и врожденные пороки сердца с сердечной недостаточностью 4 степени по классификации Нью. Йоркской ассоциации кардиологов с выживанием пациента менее 6 месяцев нормальная функция или обратимая дисфункция печени и почек легочное сосудистое сопротивление до 3 вудовских единиц возраст больного не старше 50 лет
Показания к операции трансплантации сердца Ø Ø Ø ишемическая болезнь сердца в терминальной стадии развития болезни кардиомиопатия клапанные и врожденные пороки сердца с сердечной недостаточностью 4 степени по классификации Нью. Йоркской ассоциации кардиологов с выживанием пациента менее 6 месяцев нормальная функция или обратимая дисфункция печени и почек легочное сосудистое сопротивление до 3 вудовских единиц возраст больного не старше 50 лет
 Противопоказания к трансплантации сердца активная инфекция злокачественный опухолевый процесс диабет с ретино-, нефро-, ангиопатией легочно-обструктивная болезнь, легочная гипертензия выраженной степени Ø кахексия с асцитом Ø психические заболевания Ø алкоголизм Ø наркомания Ø психологическая неуравновешенность, нестабильность Ø Ø
Противопоказания к трансплантации сердца активная инфекция злокачественный опухолевый процесс диабет с ретино-, нефро-, ангиопатией легочно-обструктивная болезнь, легочная гипертензия выраженной степени Ø кахексия с асцитом Ø психические заболевания Ø алкоголизм Ø наркомания Ø психологическая неуравновешенность, нестабильность Ø Ø
 üДонор не старше 35 лет со здоровым сердцем, с клинически установленной смертью мозга üПересадку сердца выполняют только в отделениях сердечной хирургии, имеющих опыт проведения искусственного кровообращения üОдновременно в смежных операционных начинают операцию изъятия сердца у донора и подготовку реципиента удаление больного сердца üВыполняются ортотопическая и гетеротопическая пересадка сердца
üДонор не старше 35 лет со здоровым сердцем, с клинически установленной смертью мозга üПересадку сердца выполняют только в отделениях сердечной хирургии, имеющих опыт проведения искусственного кровообращения üОдновременно в смежных операционных начинают операцию изъятия сердца у донора и подготовку реципиента удаление больного сердца üВыполняются ортотопическая и гетеротопическая пересадка сердца
 ü В течение первого года после операции выживают 80% больных, после 5 лет — 50% ü Фармакологическую иммунодепрессию после трансплантации сердца производят теми же препаратами, дозировка подбирается индивидуально ü Реакция отторжения проявляется низкими зубцами QR на ЭКГ ü Для выявления ранних признаков отторжения используют чрезвенозную эндокардиальную биопсию миокарда с последующим изучением его гистологической структуры
ü В течение первого года после операции выживают 80% больных, после 5 лет — 50% ü Фармакологическую иммунодепрессию после трансплантации сердца производят теми же препаратами, дозировка подбирается индивидуально ü Реакция отторжения проявляется низкими зубцами QR на ЭКГ ü Для выявления ранних признаков отторжения используют чрезвенозную эндокардиальную биопсию миокарда с последующим изучением его гистологической структуры
 Трансплантация легкого и критерии отбора Ø Ø Ø Ø прогрессирующая недостаточность внешнего дыхания (терминальная стадия заболеваний легких) с ожидаемой продолжительностью жизни 12 -18 месяцев кислородная зависимость больного (ингаляция или вентиляция) нормальная функция сердца отсутствие системных заболеваний отсутствие активной (внелегочной) инфекции отсутствие противопоказаний для иммунодепрессивной терапии возможность в течение месяца (или больше) до операции обходиться без кортикостероидов
Трансплантация легкого и критерии отбора Ø Ø Ø Ø прогрессирующая недостаточность внешнего дыхания (терминальная стадия заболеваний легких) с ожидаемой продолжительностью жизни 12 -18 месяцев кислородная зависимость больного (ингаляция или вентиляция) нормальная функция сердца отсутствие системных заболеваний отсутствие активной (внелегочной) инфекции отсутствие противопоказаний для иммунодепрессивной терапии возможность в течение месяца (или больше) до операции обходиться без кортикостероидов
 üТрансплантация обоих легких - при эмфиземе, муковисцидозе, цистофиброзе, бронхоэктатической болезни üОдносторонняя пересадка - при фиброзирующем альвеолите, первичной легочной гипертензии при отсутствии правожелудочковой недостаточности üПреимущественно - ортотопическая техника пересадки Выживаемость к концу 1 -го года жизни составляет 65 -73%
üТрансплантация обоих легких - при эмфиземе, муковисцидозе, цистофиброзе, бронхоэктатической болезни üОдносторонняя пересадка - при фиброзирующем альвеолите, первичной легочной гипертензии при отсутствии правожелудочковой недостаточности üПреимущественно - ортотопическая техника пересадки Выживаемость к концу 1 -го года жизни составляет 65 -73%
 Критерии трансплантация сердце легкие Легочная гипертензия первичного и вторичного происхождения и при "легочном сердце” заболевания сердца (синдром Эйзенменгера, клапанные пороки с фиксированной легочной гипертензией и недостаточностью правого сердца) Ø легочно-васкулярная болезнь (первичная легочная гипертензия, тромбоэмболическая болезнъ легких, идиопатический легочный гемосидероз) Ø заболевания паренхимы легких с развитием "легочного сердца" (эмфизема, муковисцидоз, фиброзирующий альвеолит, лимфоангиолейомиоматоз легких, альфа-1 -антитрипсиновый дефицит) Ø заболевания воздухоносных путей с развитием "легочного сердца" (облитерирующий бронхиолит, хронический обструктивный бронхит, цистофиброз легких, бронхоэктатическая болезнь) Ø
Критерии трансплантация сердце легкие Легочная гипертензия первичного и вторичного происхождения и при "легочном сердце” заболевания сердца (синдром Эйзенменгера, клапанные пороки с фиксированной легочной гипертензией и недостаточностью правого сердца) Ø легочно-васкулярная болезнь (первичная легочная гипертензия, тромбоэмболическая болезнъ легких, идиопатический легочный гемосидероз) Ø заболевания паренхимы легких с развитием "легочного сердца" (эмфизема, муковисцидоз, фиброзирующий альвеолит, лимфоангиолейомиоматоз легких, альфа-1 -антитрипсиновый дефицит) Ø заболевания воздухоносных путей с развитием "легочного сердца" (облитерирующий бронхиолит, хронический обструктивный бронхит, цистофиброз легких, бронхоэктатическая болезнь) Ø
 Показания к трансплантации сердца и легких Ø конечная стадия сердечно легочного заболевания (4 класс NУHА) Ø максимальная "естественная" выживаемость менее 12 24 месяцев Ø сохранение функции печени и почек Ø возраст не старше 45 лет
Показания к трансплантации сердца и легких Ø конечная стадия сердечно легочного заболевания (4 класс NУHА) Ø максимальная "естественная" выживаемость менее 12 24 месяцев Ø сохранение функции печени и почек Ø возраст не старше 45 лет
 Противопоказания к трансплантации сердца и легких Ø Ø Ø Ø Ø активная (внелегочная) инфекция сепсис системные заболевания (диабет, опухоль, коллагеноз и т. д. ) язвенная болезнь в стадии обострения кахексия с потерей мышечной массы некоррегируемый геморрагический диатез множественная лекарственная аллергия постоянная гормональная зависимость предшествующая операция со вскрытием плевры спаечный процесс в плевре
Противопоказания к трансплантации сердца и легких Ø Ø Ø Ø Ø активная (внелегочная) инфекция сепсис системные заболевания (диабет, опухоль, коллагеноз и т. д. ) язвенная болезнь в стадии обострения кахексия с потерей мышечной массы некоррегируемый геморрагический диатез множественная лекарственная аллергия постоянная гормональная зависимость предшествующая операция со вскрытием плевры спаечный процесс в плевре
 - в послеоперационном периоде - нарушение выделения мокроты в связи с потерей бронхиальной иннервации и легочных рефлексов - высок риск развития отека легких - число инфекционных осложнений более чем в 3 раза превышает таковое при трансплантации сердца, - высокий уровень смертности - осложнения: пневмония, полученная от донора, цитомегаловирусная инфекция
- в послеоперационном периоде - нарушение выделения мокроты в связи с потерей бронхиальной иннервации и легочных рефлексов - высок риск развития отека легких - число инфекционных осложнений более чем в 3 раза превышает таковое при трансплантации сердца, - высокий уровень смертности - осложнения: пневмония, полученная от донора, цитомегаловирусная инфекция
 Типы отторжения классический (уменьшается перфузия и вентиляция трансплантата) Ø атипичный (уменьшается альвеолярная вентиляция без изменения перфузии) Ø сосудистый (снижается перфузия без изменения вентиляции) Ø Большинство реципиентов переносят 2 или 3 значительных криза отторжения в первые 3 недели после трансплантации - - Все эпизоды острого отторжения проходят в первые 6 недель - Терапия криза отторжения трансплантата включает 3 -х дневную пульс-терапию метилпреднизолоном 1000 мг в сутки внутривенно, увеличение дозы циклоспорина, ОКТ-3
Типы отторжения классический (уменьшается перфузия и вентиляция трансплантата) Ø атипичный (уменьшается альвеолярная вентиляция без изменения перфузии) Ø сосудистый (снижается перфузия без изменения вентиляции) Ø Большинство реципиентов переносят 2 или 3 значительных криза отторжения в первые 3 недели после трансплантации - - Все эпизоды острого отторжения проходят в первые 6 недель - Терапия криза отторжения трансплантата включает 3 -х дневную пульс-терапию метилпреднизолоном 1000 мг в сутки внутривенно, увеличение дозы циклоспорина, ОКТ-3
 Трансплантация почки Основным показанием к трансплантации почки является терминальная стадия хронической почечной недостаточности (ХПН)
Трансплантация почки Основным показанием к трансплантации почки является терминальная стадия хронической почечной недостаточности (ХПН)
 Наиболее часто к ХПН приводят хронический гломерулонефрит Ø хронический пиелонефрит Ø сахарный диабет, поликистоз Ø системные заболевания (склеродермия, системная красная волчанка) Ø лекарственные и токсические нефропатии Ø травмы и опухоли (гипернефрома, опухоль Вильмса) по поводу которых необходима нефрэктомия Ø
Наиболее часто к ХПН приводят хронический гломерулонефрит Ø хронический пиелонефрит Ø сахарный диабет, поликистоз Ø системные заболевания (склеродермия, системная красная волчанка) Ø лекарственные и токсические нефропатии Ø травмы и опухоли (гипернефрома, опухоль Вильмса) по поводу которых необходима нефрэктомия Ø
 Показания к трансплантации Øвозраст до 65— 70 лет Øотсутствие патологии нижних мочевыводящих путей Øактивной инфекции Øвыраженной кахексии Øзлокачественных опухолей Øсистемных заболеваний в активной фазе Трансплантация почки также является методом выбора лечения детей, страдающих ХПН
Показания к трансплантации Øвозраст до 65— 70 лет Øотсутствие патологии нижних мочевыводящих путей Øактивной инфекции Øвыраженной кахексии Øзлокачественных опухолей Øсистемных заболеваний в активной фазе Трансплантация почки также является методом выбора лечения детей, страдающих ХПН
 Гетеротопическая пересадка почки 1) трансплантат помещается в подвздошную область контрлатеральную по отношению к донорской почке 2) почечная артерия анастомозируется с внутренней подвздошной артерией реципиента 3) венозный анастомоз накладывается "конец в бок" с наружной подвздошной веной 4) восстановление непрерывности мочевыводящих путей после включения трансплантата в кровоток осуществляется имплантацией мочеточника в дно мочевого пузыря
Гетеротопическая пересадка почки 1) трансплантат помещается в подвздошную область контрлатеральную по отношению к донорской почке 2) почечная артерия анастомозируется с внутренней подвздошной артерией реципиента 3) венозный анастомоз накладывается "конец в бок" с наружной подвздошной веной 4) восстановление непрерывности мочевыводящих путей после включения трансплантата в кровоток осуществляется имплантацией мочеточника в дно мочевого пузыря
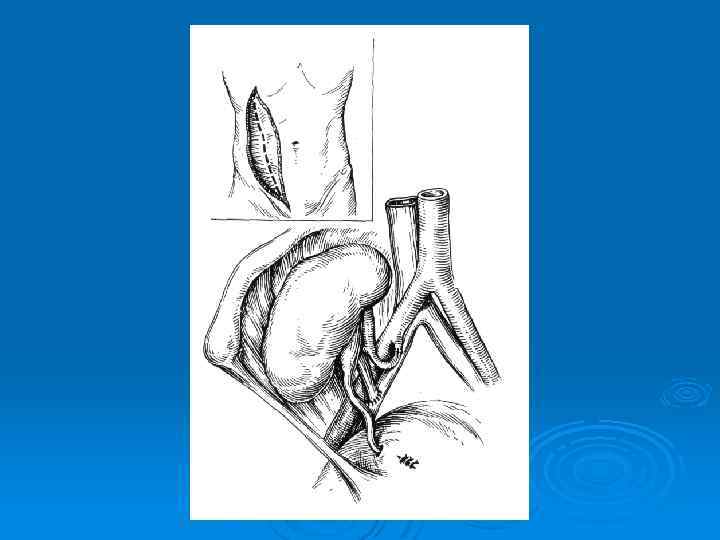
 Осложнения в раннем послеоперационном периоде • кровотечение • несостоятельность анастомоза мочеточника с мочевым пузырем • образование мочевых свищей • инфицирование раны и ложа почки • острая недостаточность трансплантата • реакция отторжения трансплантата • инфекционные осложнения мочевых путей • цитомегаловирусная и герпетическая инфекция
Осложнения в раннем послеоперационном периоде • кровотечение • несостоятельность анастомоза мочеточника с мочевым пузырем • образование мочевых свищей • инфицирование раны и ложа почки • острая недостаточность трансплантата • реакция отторжения трансплантата • инфекционные осложнения мочевых путей • цитомегаловирусная и герпетическая инфекция
 Осложнения в отдаленном периоде • артериальная гипертензия • при неэффективности консервативной терапии приходится выполнять двустороннюю нефрэктомию
Осложнения в отдаленном периоде • артериальная гипертензия • при неэффективности консервативной терапии приходится выполнять двустороннюю нефрэктомию
 Трансплантация печени Перечень клинических показаний включает более 50 нозологических форм Ø У детей наиболее частыми показаниями к ОТП является билиарная атрезия, у взрослых - постнекротический цирроз печени, первичный билиарный цирроз, склерозирующий холангит, метаболические заболевания печени Ø Показания к ОТП при злокачественных новообразованиях сужены, так как в 80% случаев возникает рецидив Ø
Трансплантация печени Перечень клинических показаний включает более 50 нозологических форм Ø У детей наиболее частыми показаниями к ОТП является билиарная атрезия, у взрослых - постнекротический цирроз печени, первичный билиарный цирроз, склерозирующий холангит, метаболические заболевания печени Ø Показания к ОТП при злокачественных новообразованиях сужены, так как в 80% случаев возникает рецидив Ø
 Абсолютные противопоказания Ø септические состояния внепеченочные метастазы рака печени Ø хронические заболевания сердца и легких в терминальной стадии Ø СПИД Ø
Абсолютные противопоказания Ø септические состояния внепеченочные метастазы рака печени Ø хронические заболевания сердца и легких в терминальной стадии Ø СПИД Ø
 ü Подбор донорского органа производится с учетом антропометрического соответствия донора и реципиента, совместимости по системе АВО, выполнения прямой перекрестной пробы ü Типирование по критериям HLА не имеет решающего значения при пересадке печени
ü Подбор донорского органа производится с учетом антропометрического соответствия донора и реципиента, совместимости по системе АВО, выполнения прямой перекрестной пробы ü Типирование по критериям HLА не имеет решающего значения при пересадке печени
 ОТП включает 4 основных этапа 1. 2. 3. 4. извлечение, консервация и подготовка донорского органа удаление собственной пораженной печени реципиента имплантация донорской печени гемостаз
ОТП включает 4 основных этапа 1. 2. 3. 4. извлечение, консервация и подготовка донорского органа удаление собственной пораженной печени реципиента имплантация донорской печени гемостаз
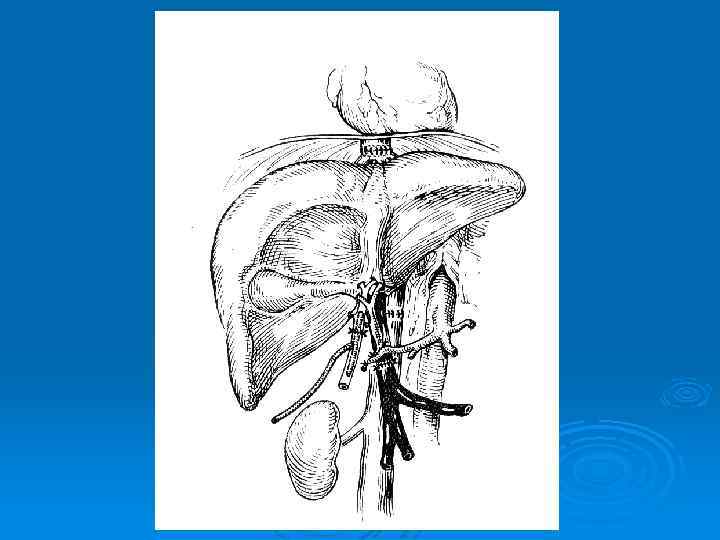
 Интраоперационные и ранние послеоперационные осложнения 1. 2. 3. 4. 5. внутрибрюшное кровотечение тромбоз печеночной артерии трансплантированной печени несостоятельность швов желчного анастомоза тромбоз воротной вены тромбоз нижней полой вены
Интраоперационные и ранние послеоперационные осложнения 1. 2. 3. 4. 5. внутрибрюшное кровотечение тромбоз печеночной артерии трансплантированной печени несостоятельность швов желчного анастомоза тромбоз воротной вены тромбоз нижней полой вены
 Послеоперационный период Ø Ø Ø Иммуносупрессия – в начале операции (метилпреднизолон 0, 75 -1, 5 мг/кг) После операции - циклоспорин и азатиоприн Доза азатиоприна со второй недели уменьшается и к концу 4 -ой отменяется Преднизолон больные получают в течение 3 -6 месяцев Больных выписывают через 4 -6 недель после трансплантации После выписки на 2 -ой, 4 -ой и 8 -ой неделе производят общий анализ крови, определяют протромбиновое время, функциональные печеночные пробы и концентрацию циклоспорина
Послеоперационный период Ø Ø Ø Иммуносупрессия – в начале операции (метилпреднизолон 0, 75 -1, 5 мг/кг) После операции - циклоспорин и азатиоприн Доза азатиоприна со второй недели уменьшается и к концу 4 -ой отменяется Преднизолон больные получают в течение 3 -6 месяцев Больных выписывают через 4 -6 недель после трансплантации После выписки на 2 -ой, 4 -ой и 8 -ой неделе производят общий анализ крови, определяют протромбиновое время, функциональные печеночные пробы и концентрацию циклоспорина
 Отторжение Реакция отторжения бывает 3 -х типов: первично-ускоренная, острая (у 70% пациентов первые 3 месяца) и отдаленная Ø Диагноз криза отторжения ставится на основании динамики желчеотделения, данных биохимического анализа крови, УЗИ и биопсии печени Ø Для лечения применяют большие дозы метилпреднизолона. Ø Ретрансплантация печени выполняется при отсутствии эффекта от лечения Ø
Отторжение Реакция отторжения бывает 3 -х типов: первично-ускоренная, острая (у 70% пациентов первые 3 месяца) и отдаленная Ø Диагноз криза отторжения ставится на основании динамики желчеотделения, данных биохимического анализа крови, УЗИ и биопсии печени Ø Для лечения применяют большие дозы метилпреднизолона. Ø Ретрансплантация печени выполняется при отсутствии эффекта от лечения Ø
 Трансплантация поджелудочной железы Ø Ø Ø Ø Пересадка ПЖ при инсулинозависимом сахарном диабете При необходимости выполняют одновременную пересадку ПЖ и почки Возможна сегментарная пересадка от живого родственного донора 2 группы способов хирургической внешнесекреторной функции трансплантата ПЖ: угнетение секреции и ее сохранение Интрадуктальное введение быстротвердеющего вещества вызывает блокирование оттока секрета трансплантата ПЖ с последующей атрофией и фиброзным перерождением ацинарных клеток без ухудшения функции островков Лангерганса, Модифкацией способа является наружное дренирование ПЖ с последующим через 30 -40 дней закрытием протоковой системы Сохранение внешней секреции ПЖ возможно при инвагинационной панкреатикоеюностомии Более перспективным является дренирование панкреатического сока в мочевой пузырь путем наложения дуоденоцистоанастомоза ПЖ пересаживают в подвздошную ямку, селезеночные артерию и вену соединяют анастомозами с подвздошными сосудами по типу конец в бок
Трансплантация поджелудочной железы Ø Ø Ø Ø Пересадка ПЖ при инсулинозависимом сахарном диабете При необходимости выполняют одновременную пересадку ПЖ и почки Возможна сегментарная пересадка от живого родственного донора 2 группы способов хирургической внешнесекреторной функции трансплантата ПЖ: угнетение секреции и ее сохранение Интрадуктальное введение быстротвердеющего вещества вызывает блокирование оттока секрета трансплантата ПЖ с последующей атрофией и фиброзным перерождением ацинарных клеток без ухудшения функции островков Лангерганса, Модифкацией способа является наружное дренирование ПЖ с последующим через 30 -40 дней закрытием протоковой системы Сохранение внешней секреции ПЖ возможно при инвагинационной панкреатикоеюностомии Более перспективным является дренирование панкреатического сока в мочевой пузырь путем наложения дуоденоцистоанастомоза ПЖ пересаживают в подвздошную ямку, селезеночные артерию и вену соединяют анастомозами с подвздошными сосудами по типу конец в бок
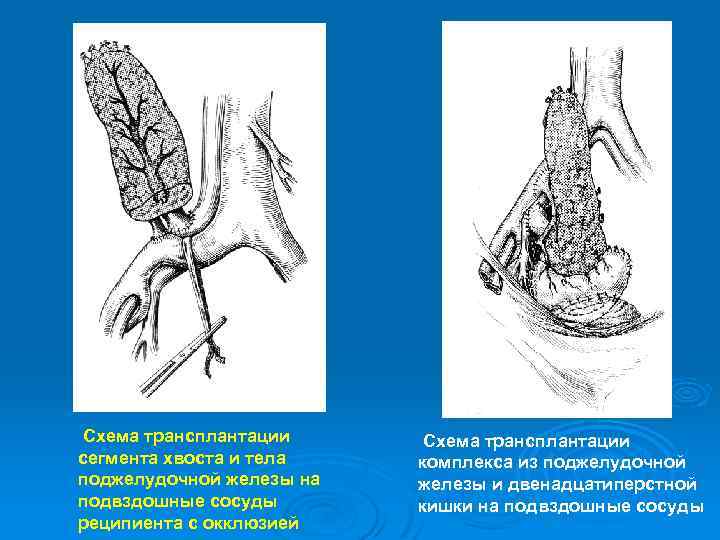 Схема трансплантации сегмента хвоста и тела поджелудочной железы на подвздошные сосуды реципиента с окклюзией Схема трансплантации комплекса из поджелудочной железы и двенадцатиперстной кишки на подвздошные сосуды
Схема трансплантации сегмента хвоста и тела поджелудочной железы на подвздошные сосуды реципиента с окклюзией Схема трансплантации комплекса из поджелудочной железы и двенадцатиперстной кишки на подвздошные сосуды
 Трансплантация кишечника Ø 1963 г. Фишер в Бостоне первая аллотрансплантация тонкой кишки новорожденному ребенку с заворотом и гангреной кишечника (сегмент тонкой кишки у матери ребенка Ø Особенность мощный лимфоидный аппарат интрамуральное скопление лимфоцитов (пейеровых бляшек/ и мезентериальных лимфоузлов) Ø Сложности: пересаженный кишечник вырабатывает антитела против нового хозяина (реакция «трансплантат против хозяина» ) Ø при пересадке кишки коллекторные пути пересекаются, наступает блок оттока лимфы Ø нарушение всасывания жиров из кишечника усугубляется моторно эвакуационными расстройствами в связи с пересечением нервных волокон и временной децентрализацией кишечного трансплантата Ø функциональная недостаточность пересаженной кишки ликвидируется медленно
Трансплантация кишечника Ø 1963 г. Фишер в Бостоне первая аллотрансплантация тонкой кишки новорожденному ребенку с заворотом и гангреной кишечника (сегмент тонкой кишки у матери ребенка Ø Особенность мощный лимфоидный аппарат интрамуральное скопление лимфоцитов (пейеровых бляшек/ и мезентериальных лимфоузлов) Ø Сложности: пересаженный кишечник вырабатывает антитела против нового хозяина (реакция «трансплантат против хозяина» ) Ø при пересадке кишки коллекторные пути пересекаются, наступает блок оттока лимфы Ø нарушение всасывания жиров из кишечника усугубляется моторно эвакуационными расстройствами в связи с пересечением нервных волокон и временной децентрализацией кишечного трансплантата Ø функциональная недостаточность пересаженной кишки ликвидируется медленно
 Трансплантация селезенки Ø Ø Ø Первую пересадку выполнил Хасавей в 1969 г. , а в нашей стране Шумаков В. И. в 1976 г. пациенту с тяжелой гемофилией Показания: тяжелая форма гемофилии А (в селезенке синтезируется 8 фактор свертывания) Гетеротопическая трансплантация с анастомозированием сосудов селезенки и подвздошных сосудов В клинике применяется метод экстракорпоральной перфузии крови больного через изолированную донорскую ксеноселезенку /ЭКПДС/ при полиорганной недостаточности, вторичных иммунодефицитах, аутоиммунных и гнойно-септических заболеваниях, разлитом гнойном перитоните, гнойном медиастините, септическое эндокардите Целесообразность метода ЭКПДС основана на выраженной способности органа фильтровать кровь, задерживать и элиминировать бактерии, токсины и другие ксенобиотики, обеспечивать фагоцитоз и выработку иммуноглобулинов, лимфокинов, лейкотриенов и других регуляторов иммунного гомеостаза Применение метода снижает летальность при гнойно-септических осложнениях в 3 -6 раз
Трансплантация селезенки Ø Ø Ø Первую пересадку выполнил Хасавей в 1969 г. , а в нашей стране Шумаков В. И. в 1976 г. пациенту с тяжелой гемофилией Показания: тяжелая форма гемофилии А (в селезенке синтезируется 8 фактор свертывания) Гетеротопическая трансплантация с анастомозированием сосудов селезенки и подвздошных сосудов В клинике применяется метод экстракорпоральной перфузии крови больного через изолированную донорскую ксеноселезенку /ЭКПДС/ при полиорганной недостаточности, вторичных иммунодефицитах, аутоиммунных и гнойно-септических заболеваниях, разлитом гнойном перитоните, гнойном медиастините, септическое эндокардите Целесообразность метода ЭКПДС основана на выраженной способности органа фильтровать кровь, задерживать и элиминировать бактерии, токсины и другие ксенобиотики, обеспечивать фагоцитоз и выработку иммуноглобулинов, лимфокинов, лейкотриенов и других регуляторов иммунного гомеостаза Применение метода снижает летальность при гнойно-септических осложнениях в 3 -6 раз
 Перспективы развития трансплантологии Трансплантология одна из самых динамично развивающихся областей клинической и экспериментальной медицины Ø Развитие трансплантологии в РФ зависит от общего состояния развития трансплантологической науки и организации службы Ø Экономическая ситуация обуславливает дальнейшее развитие отрасли и увеличение числа пересадок органов и тканей Ø Определенные надежды - на развитие генетики в области клонирования живых организмов и селекции трансгенных животных с определенными, закрепленными в генотипе нужными человеку свойствами тканей Ø
Перспективы развития трансплантологии Трансплантология одна из самых динамично развивающихся областей клинической и экспериментальной медицины Ø Развитие трансплантологии в РФ зависит от общего состояния развития трансплантологической науки и организации службы Ø Экономическая ситуация обуславливает дальнейшее развитие отрасли и увеличение числа пересадок органов и тканей Ø Определенные надежды - на развитие генетики в области клонирования живых организмов и селекции трансгенных животных с определенными, закрепленными в генотипе нужными человеку свойствами тканей Ø
 Ø Необходимо улучшить консервацию трансплантатов, кондиционирование доноров-трупов для обеспечения длительной жизнеспособности перивитального органа Ø Обсуждаются проблемы перевода трансплантации органов из вузовской медицины в муниципальную с внедрением трансплантологических операций в работу центров сердечнососудистой хирургии - как это сделано во всех развитых странах
Ø Необходимо улучшить консервацию трансплантатов, кондиционирование доноров-трупов для обеспечения длительной жизнеспособности перивитального органа Ø Обсуждаются проблемы перевода трансплантации органов из вузовской медицины в муниципальную с внедрением трансплантологических операций в работу центров сердечнососудистой хирургии - как это сделано во всех развитых странах
 ВЫВОДЫ Трансплантология одна из самых динамично развивающихся отраслей медицины. Ø В безнадежных случаях она может продлить жизнь больного Ø Задача врачей общей практики, отделений соответствующих стационаров определение показаний и противопоказаний к трансплантации органов, своевременное направление больных на трансплантацию Ø
ВЫВОДЫ Трансплантология одна из самых динамично развивающихся отраслей медицины. Ø В безнадежных случаях она может продлить жизнь больного Ø Задача врачей общей практики, отделений соответствующих стационаров определение показаний и противопоказаний к трансплантации органов, своевременное направление больных на трансплантацию Ø



