ингибиторы.ppt
- Количество слайдов: 63

Активный центр ферментов Фермент, соединяясь с субстратом: 1. очищает субстрат от водяной «шубы» 2. располагает реагирующие молекулы субстратов в пространстве нужным для протекания реакции образом 3. подготавливает к реакции (например, поляризует) молекулы субстратов. 4. присоединение фермента к субстрату происходит за счет ионных или водородных связей, редко — за счет ковалентных. В конце реакции её продукт (или продукты) отделяются от фермента. Для активных центров некоторых ферментов характерно явление коопреативности.

Активный центр ферментов • В результате фермент снижает энергию активации реакции. Это происходит потому, что в присутствии фермента реакция идет по другому пути (фактически происходит другая реакция), например: • В отсутствие фермента: • А+В = АВ • В присутствии фермента: • А+Ф = АФ • АФ+В = АВФ • АВФ = АВ+Ф • где А, В — субстраты, АВ — продукт реакции, Ф — фермент. • Ферменты не могут самостоятельно обеспечивать энергией эндергонические реакции (для протекания которых требуется энергия). • Ферменты, осуществляющие такие реакции, сопрягают их с экзергоническими реакциями, идущими с выделением большего количества энергии. • реакции синтеза биополимеров часто сопрягаются с реакцией гидролиза АТФ.

Активный центр ферментов • • Кооперативное связывание Когда субстрат связывается с активным центром одной субъединицы фермента, остальные субъединицы активируются. Лиганды могут иметь некооперативный, положительный или отрицательный кооперативный эффект. Примером положительной кооперативности может служить связывание кислорода гемоглобином. Отрицательная кооперативность означает противоположное — в момент связывания лиганда белком, аффинность белка к лиганду снижается. Примером может служить взаимодействие между глицеральдегид-3 фосфатом и ферментом глицеральдегид-3 -фосфат дегидрогеназой.

Кинетика ферментативных реакций Ингибиторы ферментивных реакций

• НАЧАЛЬНАЯ СКОРОСТЬ ПРОЦЕССА - скорость ферментативной реакции, в достаточно короткий промежуток времени, когда концентрация субстрата меняется, не настолько значительно, чтобы это отразилось на скорости процесса. • . В общем случае скорость химической реакции пропорциональна произведению концентрации реагирующих веществ. В случае ферментативной кинетики - одно из реагирующих веществ - фермент, концентрация которого на много порядков МЕНЬШЕ, чем концентрация субстрата. Это определяет некоторые особенности кинетики ферментативного катализа. • V = k+2. [E]. [S] • 1. ЗАВИСИМОСТЬ СКОРОСТИ ФЕРМЕНТАТИВНОЙ РЕАКЦИИ ОТ КОНЦЕНТРАЦИИ ФЕРМЕНТА ([E]) при постоянной и довольно большой концентрации субстрата ([S]>>[E], [S]=const) имеет такой вид:
![ЗАВИСИМОСТЬ СКОРОСТИ ФЕРМЕНТАТИВНОЙ РЕАКЦИИ ОТ КОНЦЕНТРАЦИИ ФЕРМЕНТА ([E]) при постоянной и довольно большой концентрации ЗАВИСИМОСТЬ СКОРОСТИ ФЕРМЕНТАТИВНОЙ РЕАКЦИИ ОТ КОНЦЕНТРАЦИИ ФЕРМЕНТА ([E]) при постоянной и довольно большой концентрации](https://present5.com/presentation/-11588939_131888462/image-6.jpg)
ЗАВИСИМОСТЬ СКОРОСТИ ФЕРМЕНТАТИВНОЙ РЕАКЦИИ ОТ КОНЦЕНТРАЦИИ ФЕРМЕНТА ([E]) при постоянной и довольно большой концентрации субстрата ([S]>>[E], [S]=const) • V = k+2. [E]. [S]

• Отклонение от линейности графика при очень высокой концентрации фермента возникает из-за нехватки субстрата, поэтому снижается скорость поступления субстрата на активный центр фермента. • Определять скорость ферментативной реакции надо только в том диапазоне концентраций фермента, в котором график линеен. • Линейность этого графика позволяет выразить его одной цифрой - тангенс угла наклона к оси абсцисс. • Этот тангенс представляет собой величину активности фермента. • работа (эффективность) каждого фермента количественно характеризуется величиной его активности, то есть величиной скорости ферментативной реакции в расчете на единицу количества фермента. • .

• по скорости реакции можно судить о количестве фермента • КАТАЛ - это количество фермента, которое обеспечивает превращение 1 моля субстрата за 1 секунду. • ЮНИТ - это количество фермента, которое превращает 1 мкмоль субстрата за 1 минуту. 1 Юнит = 16, 67 нкатал

• Чем выше концентрация субстрата, тем выше скорость реакции. Эта зависимость гиперболическая.
![ЗАВИСИМОСТЬ СКОРОСТИ ФЕРМЕНТАТИВНОЙ РЕАКЦИИ ОТ КОНЦЕНТРАЦИИ СУБСТРАТА ПРИ [E] = const и [S] >> ЗАВИСИМОСТЬ СКОРОСТИ ФЕРМЕНТАТИВНОЙ РЕАКЦИИ ОТ КОНЦЕНТРАЦИИ СУБСТРАТА ПРИ [E] = const и [S] >>](https://present5.com/presentation/-11588939_131888462/image-10.jpg)
ЗАВИСИМОСТЬ СКОРОСТИ ФЕРМЕНТАТИВНОЙ РЕАКЦИИ ОТ КОНЦЕНТРАЦИИ СУБСТРАТА ПРИ [E] = const и [S] >> [E]

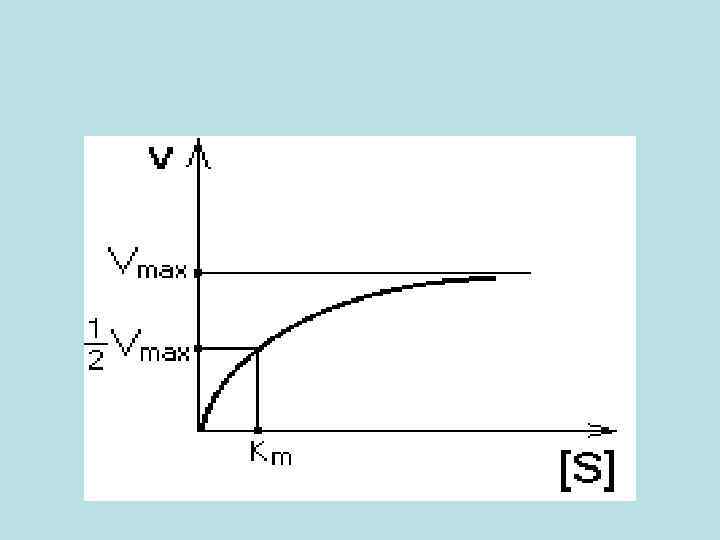
• Предельное значение, к которому стремится гипербола - Vmax данной реакции - характеризует максимальную работоспособность фермента: • Vmax=k+2. [E] • Таким образом, Vmax - это предел, к которому стремится скорость реакции при бесконечном повышении концентрации субстрата. • Км - это КОНСТАНТА МИХАЭЛИСА. • Км численно равна той концентрации субстрата, при которой скорость реакции составляет половину от максимального значения.

Уравнение кривой (Михаэлиса. Ментен)

ФИЗИЧЕСКИЙ СМЫСЛ Км - представляет собой константу равновесия между двумя реакциями, приводящими к распаду фермент-субстратного комплекса и той реакцией, которая ведет к образованию этого комплекса.

• Ks - субстратная константа. Характеризует константу равновесия 1 го этапа ферментативной реакции. Следовательно, Км обычно тоже довольно близка к Кs. Следовательно, Км, как и Кs, характеризует сродство субстрата к данному ферменту. Но экспериментально определить k-1 и k+2 очень трудно, поэтому трудно определить и Кs. А вот Км можно просто определить, используя координаты Лайнуивера-Бэрка

• С помощью Км можно характеризовать сродство данного фермента к данному субстрату. • Чем меньше Км, тем больше сродство фермента к данному субстрату, а значит тем больше равновесие первого этапа ферментативной реакции сдвинуто вправо - в сторону образования фермент-субстратного комплекса. Значит, будут созданы наилучшие условия для протекания и второго этапа ферментативного процесса. • При таких условиях для достижения эффективного превращения субстрата требуется малая концентрация субстрата. Значит, и Vmax теоретически может быть достигнута при малых количествах субстрата. • Если Км высока, то это означает, что сродство фермента к такому субстрату низкое и реакция при небольших концентрациях субстрата протекает неэффективно. • Км и Vmax - это две кинетические константы, с помощью которых можно характеризовать эффективность работы фермента, в том числе и in vivo.

ИНГИБИТОРЫ ФЕРМЕНТОВ • Ингибиторы ферментов - это вещества, замедляющие ферментативные реакции.

• диизопропилфторфосфат ингибирует ферменты, имеющие серин в активном центре. • Таким ферментом является ацетилхолинэстераза,

ацетилхолинэстераза, катализирует следующую реакцию:

Диизопропилфторфосфат - одно из отравляющих веществ нервно-паралитического действия, так как приводит к утрате способности нейронов проводить нервные импульсы.
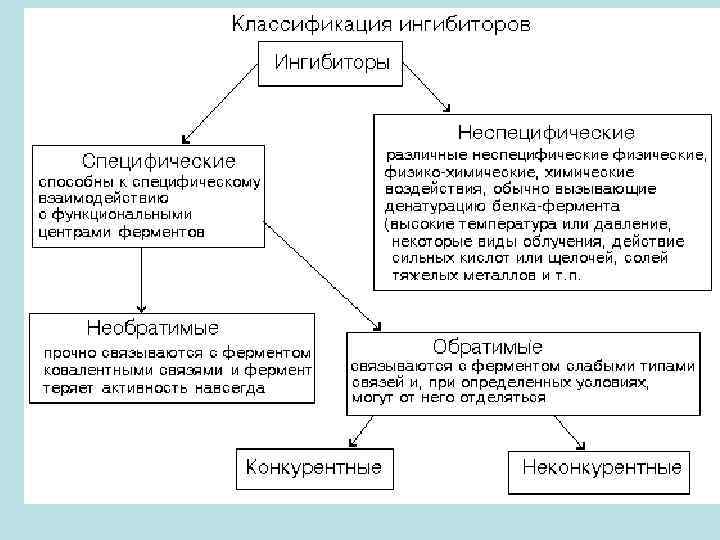

ХАРАКТЕРИСТИКА КОНКУРЕНТНЫХ ИНГИБИТОРОВ • Конкурируют с субстратом за обладание активным центром фермента. По структуре они похожи на субстрат. Присоединяются к адсорбционному центру фермента: действуют на стадии I-го этапа ферментативного катализа. Поэтому конкурентные ингибиторы увеличивают Km и уменьшают сродство фермента к субстрату. Они не изменяют Vmax ферментативной реакции: при повышении концентрации субстрата действие конкурентных ингибиторов можно преодолеть - молекулы конкурентного ингибитора постепенно вытесняются субстратом с активного центра фермента.

• Конкурентное ингибирование: Sсубстрат, I- ингибитор (своей трехмерной структурой похож на субстрат).

• В отличие от субстрата связанный с ферментом конкурентный ингибитор не подвергается ферментативному превращению. Более того, образование EI уменьшает число молекул свободного фермента, и скорость реакции снижается. Связывание S и I происходит взаимоисключающим образом. Образуется либо ES, либо EI, но не EIS. Так конкурентный ингибитор обратимо связывается с ферментом, то можно сдвинуть равновесие реакции E + I ↔ EI влево простым увеличением концентрации субстрата. Конкурентными ингибиторами являются многие химиотерапевтические средства.

ХАРАКТЕРИСТИКА НЕКОНКУРЕНТНЫХ (АЛЛОСТЕРИЧЕСКИХ) ИНГИБИТОРОВ • Связываются с аллостерическим центром фермента. • Происходят изменения конформации аллостерического центра, а затем, через всю молекулу, они передаются на каталитический центр. Изменение конформации каталитического центра вызывает снижение активности фермента. Поэтому неконкурентные ингибиторы уменьшают Vmax - снижают скорость протекания II-го этапа ферментативного катализа. Не влияют на Km и не изменяют сродство фермента к субстрату.
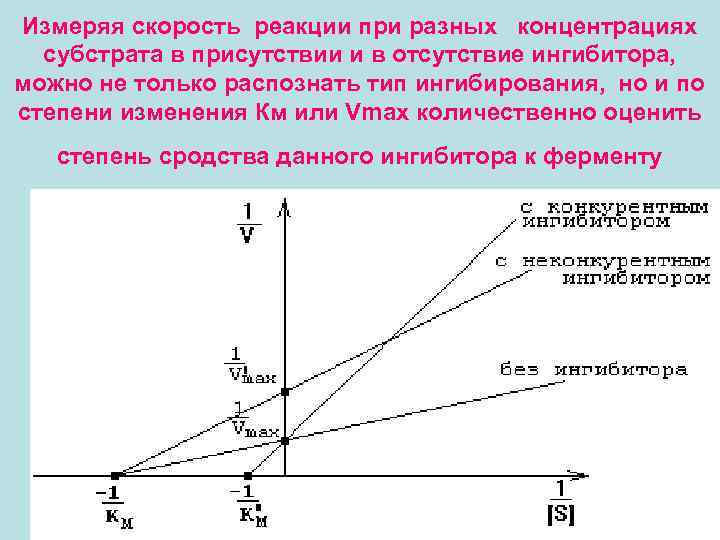
Измеряя скорость реакции при разных концентрациях субстрата в присутствии и в отсутствие ингибитора, можно не только распознать тип ингибирования, но и по степени изменения Км или Vmax количественно оценить степень сродства данного ингибитора к ферменту

АВТОНОМНАЯ САМОРЕГУЛЯЦИЯ ФЕРМЕНТАТИВНЫХ ПРОЦЕССОВ 3 уровня регуляции: • 1) Самый молодой уровень филогенетический - НЕЙРОГУМОРАЛЬНАЯ регуляция (с участием центральной нервной системы, классических гормонов и гормонов местного действия) • 2) РЕГУЛЯЦИЯ НА ГЕНЕТИЧЕСКОМ УРОВНЕ - изменение скорости биосинтеза белка. • 3) Филогенетически наиболее старый уровень - АВТОНОМНАЯ САМОРЕГУЛЯЦИЯ ФЕРМЕНТОВ.

АВТОНОМНАЯ САМОРЕГУЛЯЦИЯ • - это регуляция, которая происходит благодаря только самим участникам реакции, то есть за счет фермента, его субстрата (или субстратов) и/или продуктов деятельности данного фермента. Фермент не только работает, но еще и сам себя регулирует.

Принципы автономной саморегуляции 1) Механизмы, основанные на кинетических свойствах фермента, количественно характеризуемых Км и Vmax - это механизмы КИНЕТИЧЕСКОГО ТИПА. • 2) Второй принцип связан с аллостерическими свойствами фермента, то есть со способностью фермента угнетаться или активироваться под действием субстрата и/или продуктов. Это механизмы АЛЛОСТЕРИЧЕСКОГО ТИПА. • •

• Такие аллостерические механизмы есть не у каждого фермента. • Они обычно накладываются на механизмы кинетического типа и определяют особенности регуляции данного фермента. • E • А ----> B

• Кинетика данной ферментативной реакции описывается уравнением Михаэлиса-Ментен • Если в клетку поступает мало субстрата, то он медленно и расщепляется. При изменении скорости поступления субстрата в клетку фермент работает так, чтобы поддержать концентрацию субстрата в клетке около Км.

механизмы аллостерического типа • 1. СУБСТРАТ или ПРОДУКТ - аллостерический ИНГИБИТОР своего фермента. При чрезмерном поступлении субстрата в клетку скорость утилизации субстрата все больше будет замедляться. Так происходит, когда избыток продукта реакции опасен для клетки (опаснее, чем избыток субстрата).
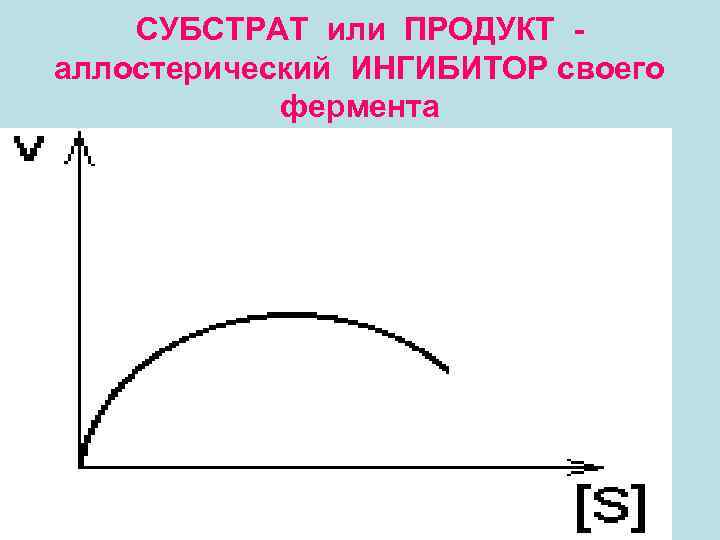
СУБСТРАТ или ПРОДУКТ аллостерический ИНГИБИТОР своего фермента

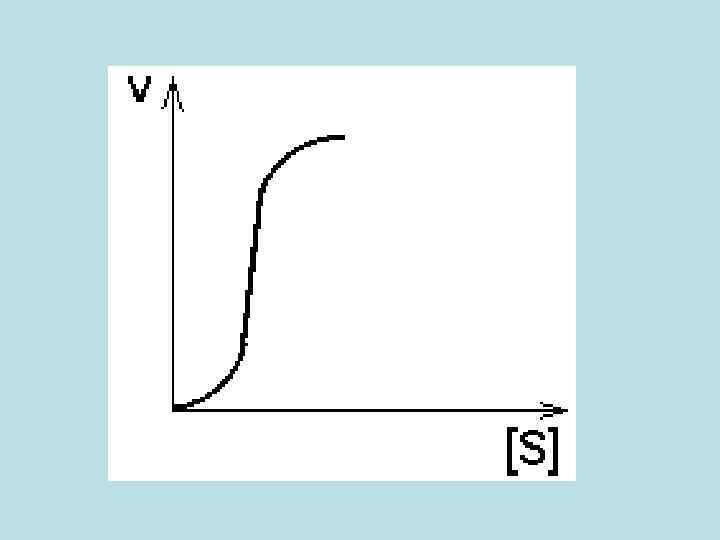
2. СУБСТРАТ - аллостерический АКТИВАТОР своего фермента. • Кинетическая кривая имеет Sобразный характер, то есть имеет 2 перегиба, как кривая диссоциации оксигемоглобина. В этом случае концентрация субстрата удерживается более эффективно на постоянном уровне и в более узком диапазоне, чем в предыдущем случае.

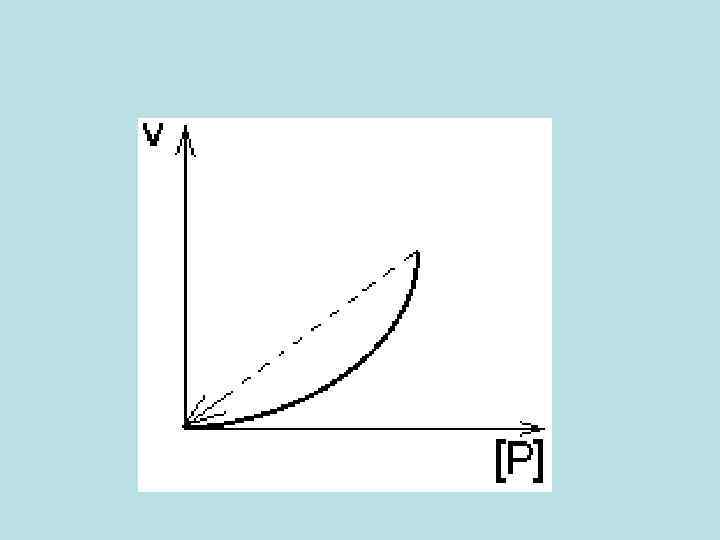
3. ПРОДУКТ реакции - аллостерический АКТИВАТОР своего фермента. • Кинетическая кривая имеет лавинообразный (взрывообразный) характер. С увеличением концентрации субстрата скорость реакции, как обычно, возрастает. Это приводит к накоплению продукта, который активирует свой фермент. Это приводит к накоплению продукта, который активирует фермент, в результате продукт накапливается еще быстрее, а фермент активируется еще сильнее. Скорость реакции становится очень большой, и реакция протекает мгновенно до полного расщепления субстрата.
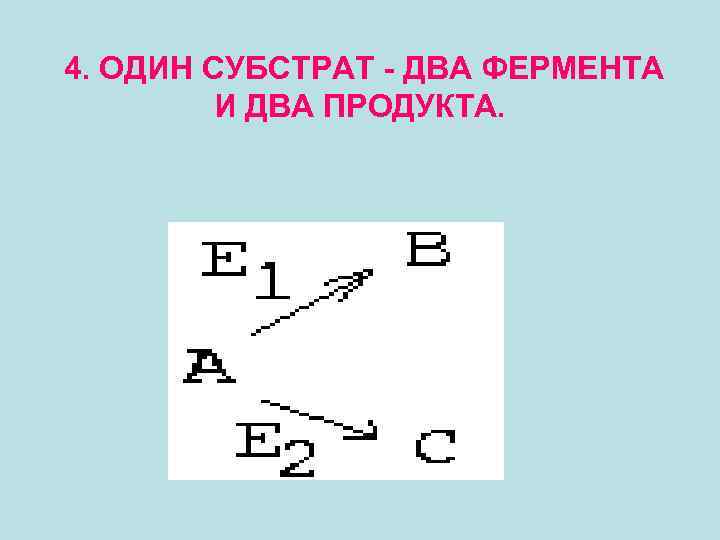
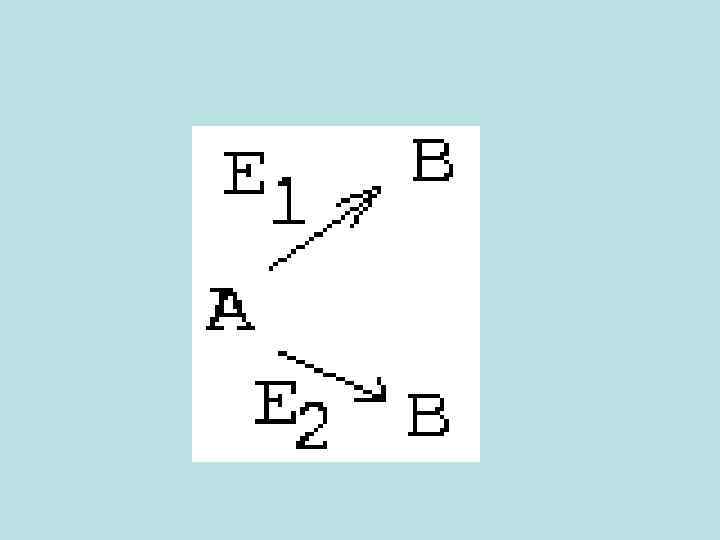
4. ОДИН СУБСТРАТ - ДВА ФЕРМЕНТА И ДВА ПРОДУКТА.

• При малых концентрациях субстрата "А" будет преимущественно протекать 1 -я реакция, то есть наибольшая часть вещества "А" будет превращаться в "В", а меньшая часть превращаться в "С". • При увеличении концентрации "А" все больше субстрата станет превращаться в "С" по второму пути. • При некоторой концентрации "А" (в точке пересечения кривых) скорости обеих реакций сравняются. В этой точке половина вещества "А" будет превращаться в "В", а вторая половина - в "С". • Если концентрацию "А" повышать дальше, то начнет преобладать второй путь превращений - в вещество "С".
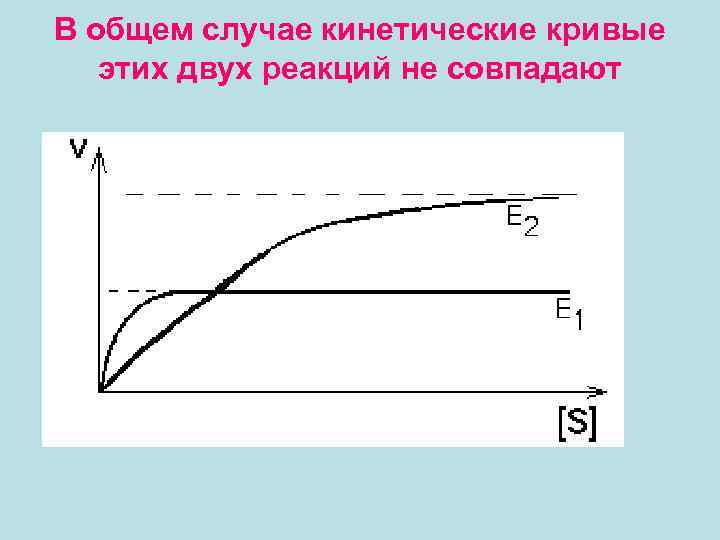
В общем случае кинетические кривые этих двух реакций не совпадают

• 5. ОДИН СУБСТРАТ, ДВА ФЕРМЕНТА И ОДИН ПРОДУКТ • Одна и та же химическая реакция в организме может катализироваться разными белками-ферментами. В таком случае они называются изоферментами - это разные молекулярные формы одного и того же фермента. Они могут отличаться обычно очень незначительно.

• если изоферменты находятся в одной клетке, то их кинетические кривые будут сливаться в одну общую кривую, которая имеет двухступенчатую форму. • Такая система регуляции работает при разных концентрациях субстрата, которые изменяются в очень широких пределах. • Наличие двух изоферментов позволяет успешно превращать субстрат и при малых, и при больших концентрациях субстрата.
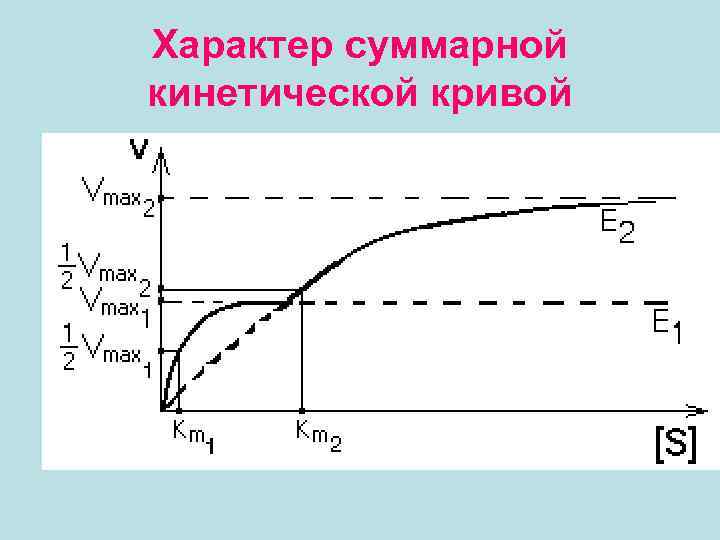
Характер суммарной кинетической кривой

• Неконкурентное обратимое ингибирование не может быть ослаблено или устранено повышением концентрации субстрата, так как эти ингибиторы присоединяются к ферменту не в активном центре, а в другом месте.
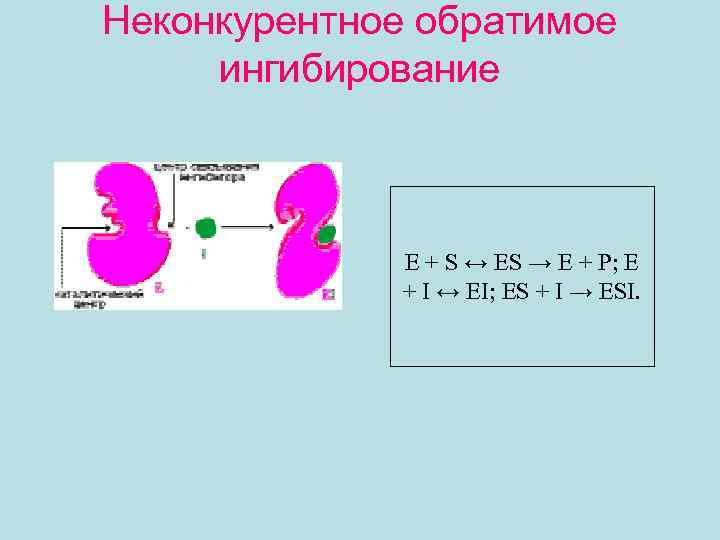
Неконкурентное обратимое ингибирование E + S ↔ ES → E + P; E + I ↔ EI; ES + I → ESI.

НЕРАЗВЕТВЛЕННЫЕ МУЛЬТИФЕРМЕНТНЫЕ СИСТЕМЫ • В большинстве случаев тот или иной биохимический процесс катализируется не одним ферментом, а целой совокупностью ферментов, каждый из которых катализирует свой этап в длинной последовательности отдельных реакций этого процесса. • Совокупность ферментов, катализирующих последовательные реакции единого процесса, называется мультиферментной системой. • E 1 E 2 E 3 E 4 En • А---->В----->C----->D------>. . L----->M

РАЗВЕТВЛЕННЫЕ МУЛЬТИФЕРМЕНТНЫЕ СИСТЕМЫ. • ключевые ферменты обычно предшествуют участкам ветвления, а сразу за разветвлением находятся ПУНКТЫ ВТОРИЧНОГО КОНТРОЛЯ, то есть такие ключевые ферменты, которые регулируют скорость реакций в своей ветви: • Е 1 - ключевой фермент, Е 4 и Е 7 - пункты вторичного контроля.

Регуляция действия ферментов В живой клетке скорость ферментативных реакций находится под строгим контролем, что позволяет каждой метаболической цепочке реакций постоянно изменяться, приспосабливаясь к меняющимся потребностям клетки в продукте.
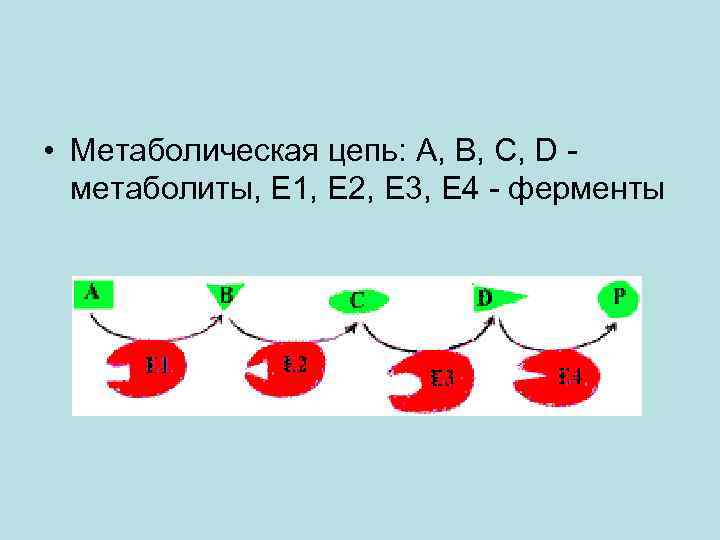
• Метаболическая цепь: А, В, С, D - метаболиты, Е 1, Е 2, Е 3, Е 4 - ферменты

• В каждой метаболической цепи есть фермент, который задает скорость всей цепочке реакций. Он называется регуляторным ферментом. Существует несколько способов регуляции действия ферментов: • изменение активности фермента при его постоянной концентрации; • изменение концентрации фермента, обычно в результате ускорения (индукции) или торможения (репрессии) синтеза фермента;

Основные способы регуляции активности ферментов • Аллостерическая регуляция. Фермент изменяет активность с помощью нековалентно связанного с ним эффектора. Связывание происходит в участке, пространственно удаленном от активного (каталитического) центра. Это связывание вызывает конформационные изменения в молекуле белка, приводящие к изменению определенной геометрии каталитического центра. Активность может увеличиться - это активация фермента, или уменьшиться - это ингибирование.
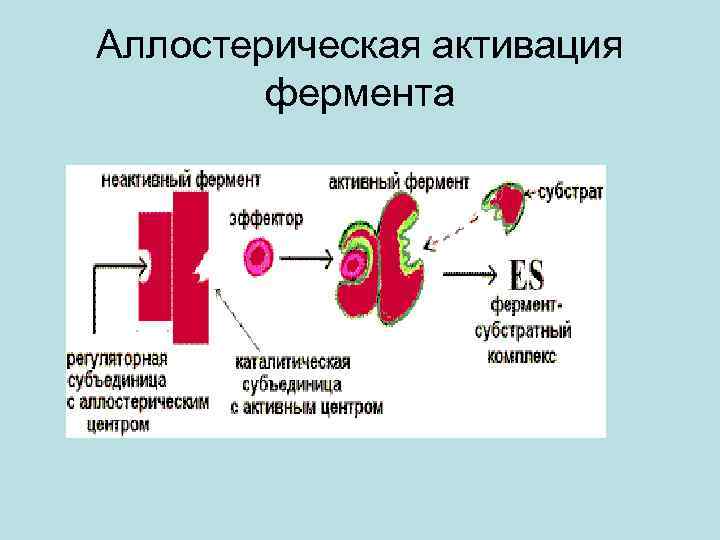
Аллостерическая активация фермента

• Сообщение» о присоединении аллостерического активатора передается посредством конформационных изменений каталитической субъединице, которая становится комплементарной субстрату, и фермент «включается» . При удалении активатора фермент вновь переходит в неактивную форму и «выключается» . Аллостерическая регуляция является основным способом регуляции метаболических путей.

• Регуляция активности ферментов путем фосфорилированиядефосфорилирования. • Фермент изменяет активность в результате ковалентной модификации
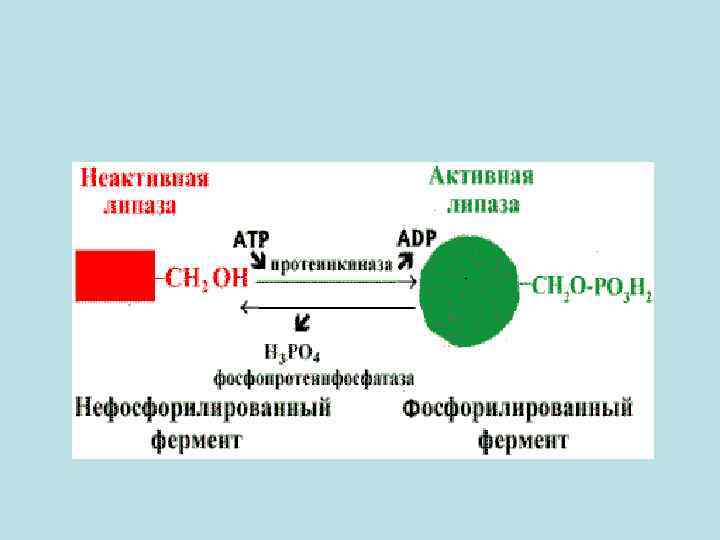

• В этом случае фосфатная группа - ОРО 32 - присоединяется к гидроксильным группам в остатках серина, треонина или тирозина. В зависимости от природы фермента фосфорилирование может его активировать или, наоборот, инактивировать. Реакция присоединения фосфатной группы и ее отщепление катализируют специальные ферменты - протеинкиназы и протеинфосфатазы.

Регуляция путем ассоциациидиссоциации субъединиц в олигомерном ферменте • . Этот процесс иногда начинается с ковалентной или нековалентной модификации одной из субъединиц. Например, фермент протеинкиназа в неактивной форме построена как тетрамер R 2 C 2 (R и С - разные субъединицы). • Активная протеинкиназа представляет собой субъединицу С, для освобождения которой необходима диссоциация комплекса. Активация фермента происходит при участии c. AMP (циклоаденозинмонофосфорная кислота), которая способна присоединиться к субъединице R, после чего изменяется конформация, комплементарность субъединиц R и С и происходит диссоциация комплекса: R 2 C 2 + 2 c. АМР 2 С + 2(R с. АМР) Циклический АМР является продуктом АТР, превращение которой катализирует фермент аденилатциклаза: АТРс АМР + Н 4 Р 2 О 7

• Аденилатциклазная система. Аденилатциклаза и протеинкиназа катализируют взаимосвязанные реакции, которые составляют единую регуляторную систему
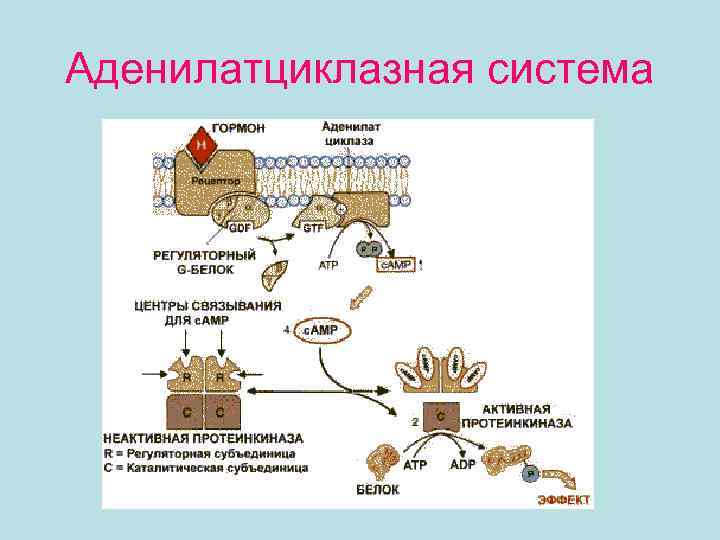
Аденилатциклазная система

• С помощью этой системы в клетку передаются сигналы из внеклеточной среды, и в нужном направлении изменяется метаболизм клетки. Внеклеточным вестником сигнала могут быть разные молекулы, в том числе и гормоны. Эти молекулы не проникают внутрь клетки, но «узнаются» мембранными рецепторами

• изменение конформации рецептора после присоединения к нему сигнальной молекулы и увеличение его сродства к регуляторному G-белку. В результате образуется комплекс рецептора и протомеров G-белка; • образование этого комплекса приводит к изменению конформации a -протомера G-белка, который теряет сродство к GDP и происходит замена GDP на GTP. В результате комплекс протомеров G-белка распадается; • a -протомер взаимодействует с аденилатциклазой, что ведет к изменению ее конформации и как следствие этого - активации; • после этого аденилатциклаза катализирует синтез c. AMP, который в свою очередь активирует c. AMP-зависимую протеинкиназу. Активация последней связана с диссоциацией комплекса входящих в нее протомеров после присоединения c. AMP. Протеинкиназа фосфорилирует соответствующие ферменты, изменяет их активность и, следовательно, скорость метаболизма в клетке.
ингибиторы.ppt