07_АФК_ПОЛ_АОС.pptx
- Количество слайдов: 32
 Активные формы кислорода. Перекисное окисление липидов. Антиоксидантная система
Активные формы кислорода. Перекисное окисление липидов. Антиоксидантная система
 95– 98 % вдыхаемого О 2 расходуется на выработку энергии и окислительный метаболизм субстратов, 2– 5 % О 2 переходит в активные формы
95– 98 % вдыхаемого О 2 расходуется на выработку энергии и окислительный метаболизм субстратов, 2– 5 % О 2 переходит в активные формы
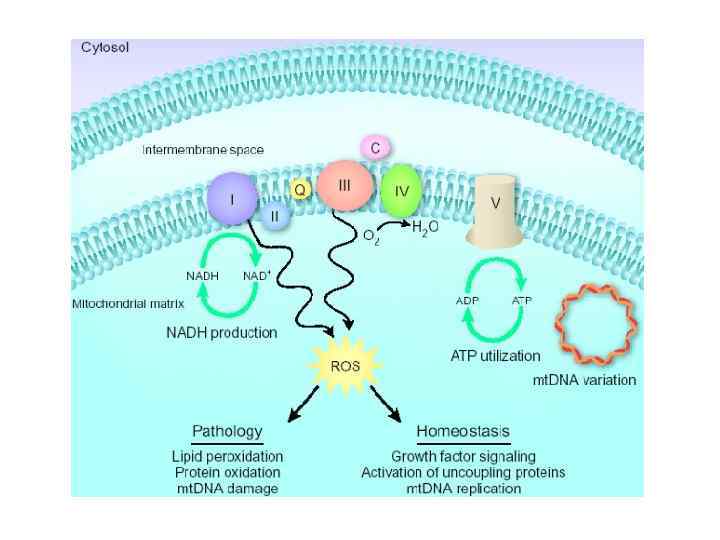
 Окислительный стресс – интенсификация процесса накопления в клетках растений, животных активных форм кислорода, к числу которых относят: синглетный кислород (1 о 2), супероксидный анион-радикал (о 2 • ‾), перекись водорода (н 2 о 2) и гидроксилрадикал (он • ).
Окислительный стресс – интенсификация процесса накопления в клетках растений, животных активных форм кислорода, к числу которых относят: синглетный кислород (1 о 2), супероксидный анион-радикал (о 2 • ‾), перекись водорода (н 2 о 2) и гидроксилрадикал (он • ).

 1) Супероксид анион-радикал о 2 • ‾ Супероксидный анион-радикал является одной из наиболее опасных форм активного кислорода, так как имеет продолжительное время жизни и становиться источником других АФК.
1) Супероксид анион-радикал о 2 • ‾ Супероксидный анион-радикал является одной из наиболее опасных форм активного кислорода, так как имеет продолжительное время жизни и становиться источником других АФК.
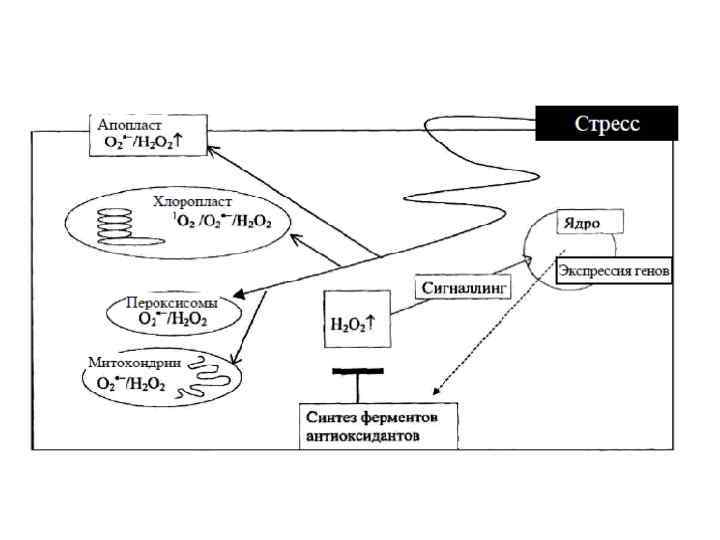
 2) Пероксид водорода H 2 O 2 Пероксид водорода относится к окислителям средней силы и в стрессовых условиях проявляет двойственные функции: с одной стороны, он является токсичным продуктом, с другой – выполняет защитную сигнальную роль. Пероксид водорода относительно стабилен и может легко диффундировать через мембраны. Однако его роль определяется не столько собственной химической реактивностью, сколько участие в образовании более токсичных АФК.
2) Пероксид водорода H 2 O 2 Пероксид водорода относится к окислителям средней силы и в стрессовых условиях проявляет двойственные функции: с одной стороны, он является токсичным продуктом, с другой – выполняет защитную сигнальную роль. Пероксид водорода относительно стабилен и может легко диффундировать через мембраны. Однако его роль определяется не столько собственной химической реактивностью, сколько участие в образовании более токсичных АФК.
 3) Гидроксильный радикал ОН • наиболее сильный окислитель. не способен к внутриклеточной миграции, так как моментально реагирует с биомолекулами. Основным источником ОН • служат реакции Фентона (1 -2) и Хабера-Вейса (3), при участии пероксида водорода и восстановленных ионов металлов переменной валентности, в частности меди и железа: О 2 • ‾ + Fe 3+ → Fe 2+ + О 2 (1) Fe 2+ + Н 2 О 2 → Fe 3+ + OH‾ + ОН • (2) О 2 • ‾ + Н 2 О 2 → OH‾ + ОН • + О 2 (3)
3) Гидроксильный радикал ОН • наиболее сильный окислитель. не способен к внутриклеточной миграции, так как моментально реагирует с биомолекулами. Основным источником ОН • служат реакции Фентона (1 -2) и Хабера-Вейса (3), при участии пероксида водорода и восстановленных ионов металлов переменной валентности, в частности меди и железа: О 2 • ‾ + Fe 3+ → Fe 2+ + О 2 (1) Fe 2+ + Н 2 О 2 → Fe 3+ + OH‾ + ОН • (2) О 2 • ‾ + Н 2 О 2 → OH‾ + ОН • + О 2 (3)
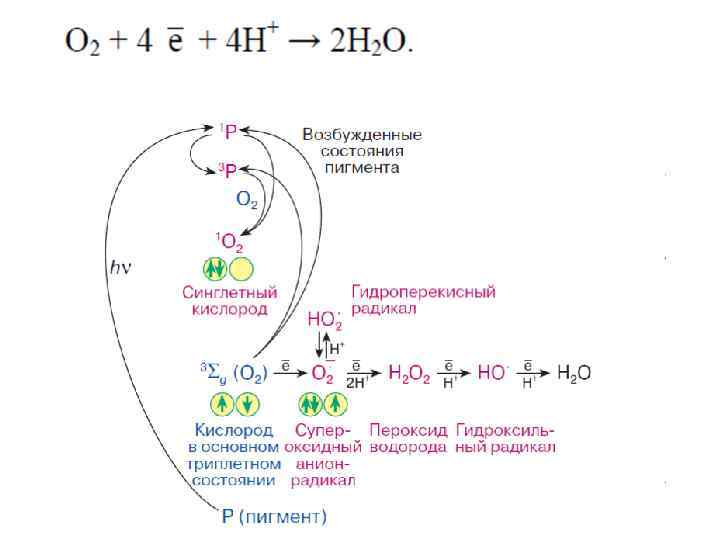
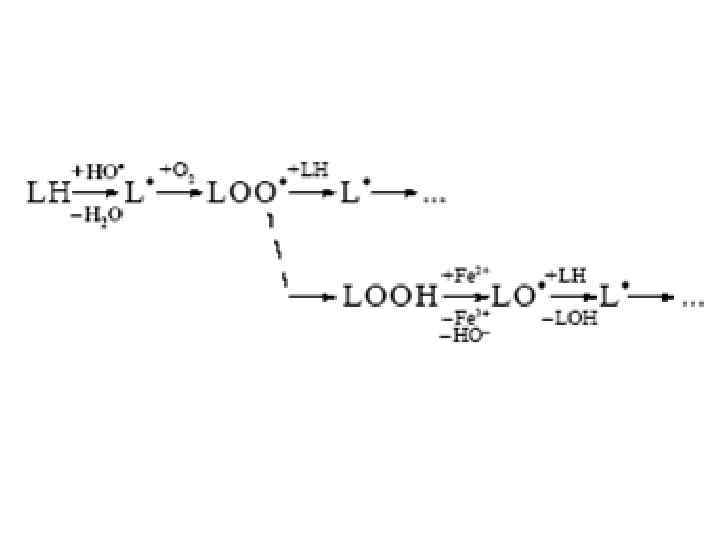
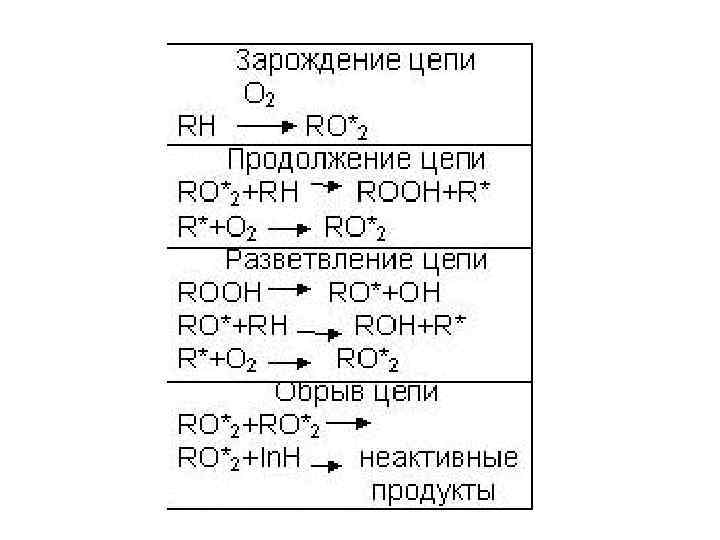
 4) Синглетный кислород 1 О 2 Возникновение преимущественно связано с фотохимическими реакциями: поглощением пигментом (Р) кванта света (hν) и переносом энергии с его возбужденных синглетных (1 Р) и триплетных (3 Р) состояний на молекулярный кислород. Синглетный кислород может быстро реагировать с большинством органических молекул (RH), продуцируя гидропероксиды (4): RH + 21 О 2 → ROOH (4)
4) Синглетный кислород 1 О 2 Возникновение преимущественно связано с фотохимическими реакциями: поглощением пигментом (Р) кванта света (hν) и переносом энергии с его возбужденных синглетных (1 Р) и триплетных (3 Р) состояний на молекулярный кислород. Синглетный кислород может быстро реагировать с большинством органических молекул (RH), продуцируя гидропероксиды (4): RH + 21 О 2 → ROOH (4)
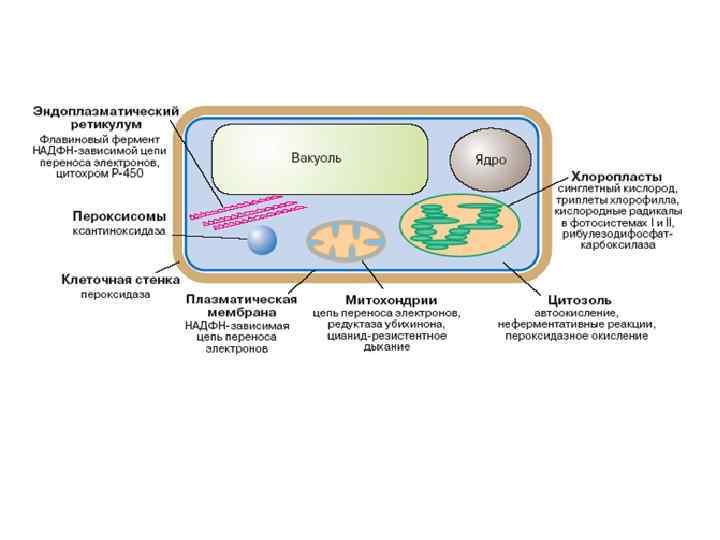
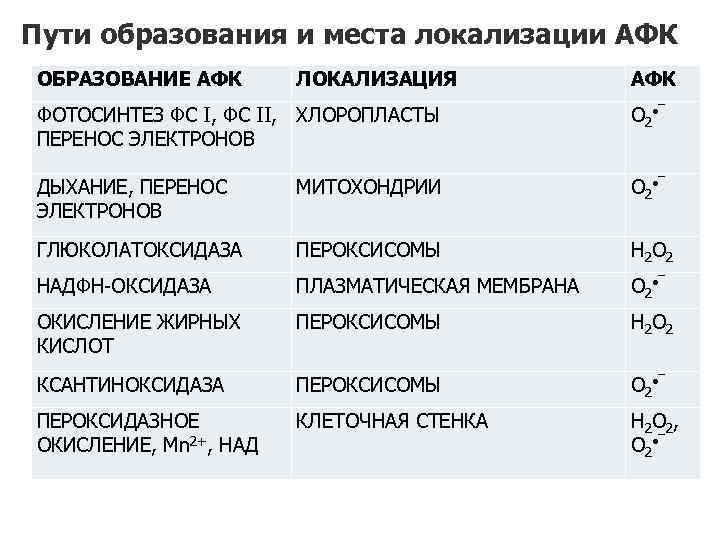 Пути образования и места локализации АФК ОБРАЗОВАНИЕ АФК ЛОКАЛИЗАЦИЯ АФК ФОТОСИНТЕЗ ФС I, ФС II, ХЛОРОПЛАСТЫ ПЕРЕНОС ЭЛЕКТРОНОВ О 2 • ‾ ДЫХАНИЕ, ПЕРЕНОС ЭЛЕКТРОНОВ МИТОХОНДРИИ О 2 • ‾ ГЛЮКОЛАТОКСИДАЗА ПЕРОКСИСОМЫ Н 2 О 2 НАДФН-ОКСИДАЗА ПЛАЗМАТИЧЕСКАЯ МЕМБРАНА О 2 • ‾ ОКИСЛЕНИЕ ЖИРНЫХ КИСЛОТ ПЕРОКСИСОМЫ Н 2 О 2 КСАНТИНОКСИДАЗА ПЕРОКСИСОМЫ О 2 • ‾ ПЕРОКСИДАЗНОЕ ОКИСЛЕНИЕ, Mn 2+, НАД КЛЕТОЧНАЯ СТЕНКА Н 2 О 2, О 2 • ‾
Пути образования и места локализации АФК ОБРАЗОВАНИЕ АФК ЛОКАЛИЗАЦИЯ АФК ФОТОСИНТЕЗ ФС I, ФС II, ХЛОРОПЛАСТЫ ПЕРЕНОС ЭЛЕКТРОНОВ О 2 • ‾ ДЫХАНИЕ, ПЕРЕНОС ЭЛЕКТРОНОВ МИТОХОНДРИИ О 2 • ‾ ГЛЮКОЛАТОКСИДАЗА ПЕРОКСИСОМЫ Н 2 О 2 НАДФН-ОКСИДАЗА ПЛАЗМАТИЧЕСКАЯ МЕМБРАНА О 2 • ‾ ОКИСЛЕНИЕ ЖИРНЫХ КИСЛОТ ПЕРОКСИСОМЫ Н 2 О 2 КСАНТИНОКСИДАЗА ПЕРОКСИСОМЫ О 2 • ‾ ПЕРОКСИДАЗНОЕ ОКИСЛЕНИЕ, Mn 2+, НАД КЛЕТОЧНАЯ СТЕНКА Н 2 О 2, О 2 • ‾
 Свободные радикалы являются ключевыми элементами регуляции многих физиологических процессов на всех уровнях: от регуляции активности внутриклеточных ферментов до нервной регуляции сократительной функции желудка и внешнего дыхания. 1987 году две независимые группы исследователей показали, что эндотелиальный фактор релаксации сосудов есть не что иное, как NО-радикал. В 1992 году журналом «Science» молекула NO • названа молекулой года, в 1998 году за открытие роли оксида азота как сигнальной молекулы в сердечно-сосудистой системе американским исследователям Роберту Ф. Фёрчготту, Луису Дж. Игнарро и Фериду М. Мьюрэду присуждена Нобелевская премия в области физиологии и медицины.
Свободные радикалы являются ключевыми элементами регуляции многих физиологических процессов на всех уровнях: от регуляции активности внутриклеточных ферментов до нервной регуляции сократительной функции желудка и внешнего дыхания. 1987 году две независимые группы исследователей показали, что эндотелиальный фактор релаксации сосудов есть не что иное, как NО-радикал. В 1992 году журналом «Science» молекула NO • названа молекулой года, в 1998 году за открытие роли оксида азота как сигнальной молекулы в сердечно-сосудистой системе американским исследователям Роберту Ф. Фёрчготту, Луису Дж. Игнарро и Фериду М. Мьюрэду присуждена Нобелевская премия в области физиологии и медицины.
 РЕГУЛЯЦИЯ СВОБОДНО-РАДИКАЛЬНОГО ОКИСЛЕНИЯ НЕСПЕЦИФИЧЕСКИЕ ФАКТОРЫ СПЕЦИФИЧЕСКИЕ МЕХАНИЗМЫ, РЕГУЛИРУЮЩИЕ ФЕРМЕНТЫ, ОТВЕТСТВЕННЫЕ ЗА КОЛИЧЕСТВО И КАЧЕСТВО СУБСТРАТА ОБРАЗОВАНИЕ И МЕТАБОЛИЗМ ОКИСЛЕНИЯ И ЕГО ДОСТУПНОСТЬ; АКТИВНЫХ ФОРМ КИСЛОРОДА ФАКТОРЫ, ВЛИЯЮЩИЕ НА (СУПЕРОКСИДДИСМУТАЗА, ИНИЦИАТОРЫ ОКИСЛЕНИЯ, В КАТАЛАЗА И ДР. ); ЧАСТНОСТИ, НА СОСТОЯНИЕ СИСТЕМЫ, УТИЛИЗИРУЮЩИЕ МЕТАЛЛОВ ПЕРЕМЕННОЙ ПЕРЕКИСНЫЕ ПРОДУКТЫ ВАЛЕНТНОСТИ; (ГЛУТАТИОН-ПЕРОКСИДАЗА, ФИЗИКО-ХИМИЧЕСКИЕ СВОЙСТВА ГЛУТАТИОН-РЕДУКТАЗА И ДР. ); БИОЛОГИЧЕСКИХ МЕМБРАН; ПЕРЕХВАТЧИКИ АКТИВНЫХ ФОРМ МЕХАНИЗМЫ, ПОДДЕРЖИВАЮЩИЕ КИСЛОРОДА (МЕТИОНИН, НИЗКОЕ СОДЕРЖАНИЕ О 2 В ТКАНЯХ; ГИСТАМИН И Т. Д. ) БИОАНТИОКСИДАНТЫ (ТОКОФЕРОЛ, УБИХИНОН, ЦЕРУЛОПЛАЗМИН И ДР. ); СКОРОСТЬ ОКИСЛЕНИЯ ПОДДЕРЖИВАЕТСЯ НА ПОСТОЯННОМ УРОВНЕ СЛОЖНОЙ, МНОГОСТУПЕНЧАТОЙ СИСТЕМОЙ РЕГУЛЯЦИИ
РЕГУЛЯЦИЯ СВОБОДНО-РАДИКАЛЬНОГО ОКИСЛЕНИЯ НЕСПЕЦИФИЧЕСКИЕ ФАКТОРЫ СПЕЦИФИЧЕСКИЕ МЕХАНИЗМЫ, РЕГУЛИРУЮЩИЕ ФЕРМЕНТЫ, ОТВЕТСТВЕННЫЕ ЗА КОЛИЧЕСТВО И КАЧЕСТВО СУБСТРАТА ОБРАЗОВАНИЕ И МЕТАБОЛИЗМ ОКИСЛЕНИЯ И ЕГО ДОСТУПНОСТЬ; АКТИВНЫХ ФОРМ КИСЛОРОДА ФАКТОРЫ, ВЛИЯЮЩИЕ НА (СУПЕРОКСИДДИСМУТАЗА, ИНИЦИАТОРЫ ОКИСЛЕНИЯ, В КАТАЛАЗА И ДР. ); ЧАСТНОСТИ, НА СОСТОЯНИЕ СИСТЕМЫ, УТИЛИЗИРУЮЩИЕ МЕТАЛЛОВ ПЕРЕМЕННОЙ ПЕРЕКИСНЫЕ ПРОДУКТЫ ВАЛЕНТНОСТИ; (ГЛУТАТИОН-ПЕРОКСИДАЗА, ФИЗИКО-ХИМИЧЕСКИЕ СВОЙСТВА ГЛУТАТИОН-РЕДУКТАЗА И ДР. ); БИОЛОГИЧЕСКИХ МЕМБРАН; ПЕРЕХВАТЧИКИ АКТИВНЫХ ФОРМ МЕХАНИЗМЫ, ПОДДЕРЖИВАЮЩИЕ КИСЛОРОДА (МЕТИОНИН, НИЗКОЕ СОДЕРЖАНИЕ О 2 В ТКАНЯХ; ГИСТАМИН И Т. Д. ) БИОАНТИОКСИДАНТЫ (ТОКОФЕРОЛ, УБИХИНОН, ЦЕРУЛОПЛАЗМИН И ДР. ); СКОРОСТЬ ОКИСЛЕНИЯ ПОДДЕРЖИВАЕТСЯ НА ПОСТОЯННОМ УРОВНЕ СЛОЖНОЙ, МНОГОСТУПЕНЧАТОЙ СИСТЕМОЙ РЕГУЛЯЦИИ
 Бэрри Холливелл и Джон М. С. Гаттеридж: "Антиоксидант - это любое вещество, которое, присутствуя в низких по сравнению с окисляемым субстратом концентрациях, существенно задерживает или ингибирует его окисление"
Бэрри Холливелл и Джон М. С. Гаттеридж: "Антиоксидант - это любое вещество, которое, присутствуя в низких по сравнению с окисляемым субстратом концентрациях, существенно задерживает или ингибирует его окисление"
 По химической природе биоантиокислители представляют собой широкий класс соединений: ферменты (СОД, каталаза ГПО), фенолы и полифенолы (токоферолы, пирокатехин, производные галловой кислоты), флавоноиды (рутин, кверцетин), стероидные гормоны (лецитин, кефалин) и многие другие соединения. В зависимости от растворимости различают жирорастворимые (витамины Е, А, К, стерины, убихинон) и водорастворимые (витамины С, В 6, РР, серотонин, SH-содержащие соединения) биоантиокислители, По молекулярной массе выделяют группу низкомолекулярных антиоксидантов (глутатион, аскорбат, каротин, токоферол) и высокомолекулярных, не способных проникать через биологические барьеры (это, прежде, ферменты). По механизму действия: антиокислители, соединения антирадикального действия, антиоксиданты-ловушки, антиоксиданты-тушители.
По химической природе биоантиокислители представляют собой широкий класс соединений: ферменты (СОД, каталаза ГПО), фенолы и полифенолы (токоферолы, пирокатехин, производные галловой кислоты), флавоноиды (рутин, кверцетин), стероидные гормоны (лецитин, кефалин) и многие другие соединения. В зависимости от растворимости различают жирорастворимые (витамины Е, А, К, стерины, убихинон) и водорастворимые (витамины С, В 6, РР, серотонин, SH-содержащие соединения) биоантиокислители, По молекулярной массе выделяют группу низкомолекулярных антиоксидантов (глутатион, аскорбат, каротин, токоферол) и высокомолекулярных, не способных проникать через биологические барьеры (это, прежде, ферменты). По механизму действия: антиокислители, соединения антирадикального действия, антиоксиданты-ловушки, антиоксиданты-тушители.
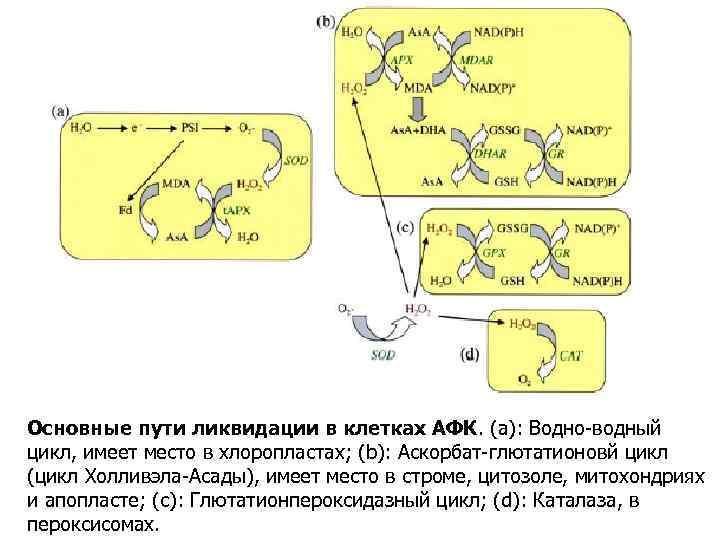 Основные пути ликвидации в клетках АФК. (a): Водно-водный цикл, имеет место в хлоропластах; (b): Аскорбат-глютатионовй цикл (цикл Холливэла-Асады), имеет место в строме, цитозоле, митохондриях и апопласте; (с): Глютатионпероксидазный цикл; (d): Каталаза, в пероксисомах.
Основные пути ликвидации в клетках АФК. (a): Водно-водный цикл, имеет место в хлоропластах; (b): Аскорбат-глютатионовй цикл (цикл Холливэла-Асады), имеет место в строме, цитозоле, митохондриях и апопласте; (с): Глютатионпероксидазный цикл; (d): Каталаза, в пероксисомах.
 Супероксиддисмутаза (СОД, ЕС 1. 15. 1. 1) • Первый антиоксидантный фермент, выделили Манн и Кейлис в 1938 году • Широко распространен в природе, присутствует у всех аэробных организмов, а также найден у некоторых анаэробных бактерий • Катализирует реакцию восстановления супероксид радикала до пероксида водорода: ·О 2 - + 2 Н = H 2 O 2 +
Супероксиддисмутаза (СОД, ЕС 1. 15. 1. 1) • Первый антиоксидантный фермент, выделили Манн и Кейлис в 1938 году • Широко распространен в природе, присутствует у всех аэробных организмов, а также найден у некоторых анаэробных бактерий • Катализирует реакцию восстановления супероксид радикала до пероксида водорода: ·О 2 - + 2 Н = H 2 O 2 +
 Каталаза (ЕС 1. 16) • Широко распространена в растительных тканях, обнаружена почти у всех аэробов и у некоторых факультативных анаэробов • Это двухкомпонентный Fe-порфириновый фермент, состоящий из белка и простетической группы гемоглобина крови. Имеет 5 изоферментов • Сущность каталитического действия каталазы 2 Н 2 О 2 → 2 Н 2 О, Fe. OH + HOOH → Fe. OOH + H 2 O, Fe. OOH + HOOH → Fe. OH + H 2 O + O 2
Каталаза (ЕС 1. 16) • Широко распространена в растительных тканях, обнаружена почти у всех аэробов и у некоторых факультативных анаэробов • Это двухкомпонентный Fe-порфириновый фермент, состоящий из белка и простетической группы гемоглобина крови. Имеет 5 изоферментов • Сущность каталитического действия каталазы 2 Н 2 О 2 → 2 Н 2 О, Fe. OH + HOOH → Fe. OOH + H 2 O, Fe. OOH + HOOH → Fe. OH + H 2 O + O 2
 Пероксидазы (ЕС 1. 17) Включают группу ферментов, использующих в качестве окислителя пероксид водорода. Они катализируют следующую реакцию: АН 2 + Н 2 О 2 → А + 2 Н 2 О В основе механизма действия лежит способность вступать во взаимодействие с перекисью водорода с образованием промежуточных комплексов, которые обладают различными спектральными характеристиками. Этот фермент в разных изоформах присутствует практически во всех клеточных компартментах, включая и клеточную стенку.
Пероксидазы (ЕС 1. 17) Включают группу ферментов, использующих в качестве окислителя пероксид водорода. Они катализируют следующую реакцию: АН 2 + Н 2 О 2 → А + 2 Н 2 О В основе механизма действия лежит способность вступать во взаимодействие с перекисью водорода с образованием промежуточных комплексов, которые обладают различными спектральными характеристиками. Этот фермент в разных изоформах присутствует практически во всех клеточных компартментах, включая и клеточную стенку.
 Виды пероксидаз • • • НАДН-пероксидаза, НАДФН-пероксидаза, глутатион-пероксидаза, гваякол-пероксидаза, аскорбат-пероксидаза и др.
Виды пероксидаз • • • НАДН-пероксидаза, НАДФН-пероксидаза, глутатион-пероксидаза, гваякол-пероксидаза, аскорбат-пероксидаза и др.
 Глутатионредуктаза (ГР, ЕС 1. 6. 4. 2) • Катализирует восстановление окисленного глутатиона при участии НAДФH + H+ в глутатион-аскорбатном цикле • Имеет у растений 4 изоформы, которые ассоциированы с разными клеточными компартментами • Локализована в хлоропластах, также в цитозоле и митохондриях
Глутатионредуктаза (ГР, ЕС 1. 6. 4. 2) • Катализирует восстановление окисленного глутатиона при участии НAДФH + H+ в глутатион-аскорбатном цикле • Имеет у растений 4 изоформы, которые ассоциированы с разными клеточными компартментами • Локализована в хлоропластах, также в цитозоле и митохондриях
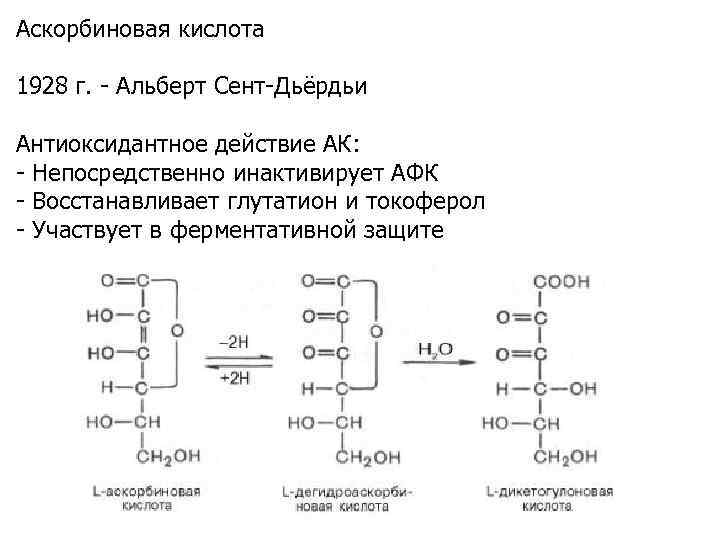 Аскорбиновая кислота 1928 г. - Альберт Сент-Дьёрдьи Антиоксидантное действие АК: - Непосредственно инактивирует АФК - Восстанавливает глутатион и токоферол - Участвует в ферментативной защите
Аскорбиновая кислота 1928 г. - Альберт Сент-Дьёрдьи Антиоксидантное действие АК: - Непосредственно инактивирует АФК - Восстанавливает глутатион и токоферол - Участвует в ферментативной защите
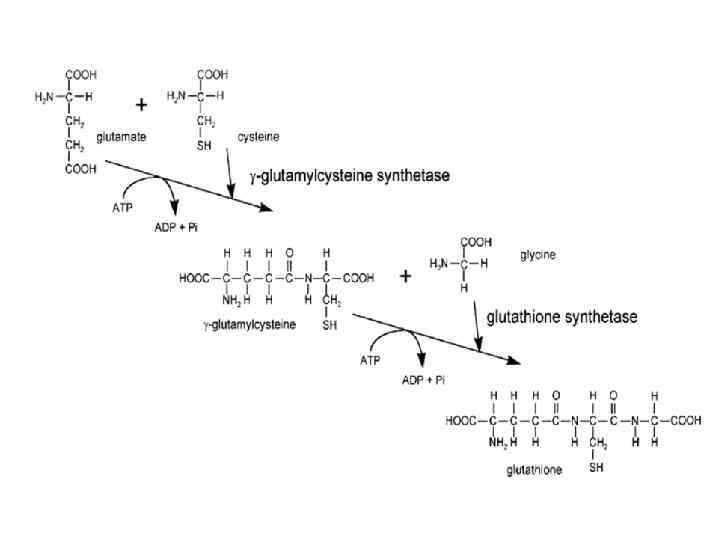
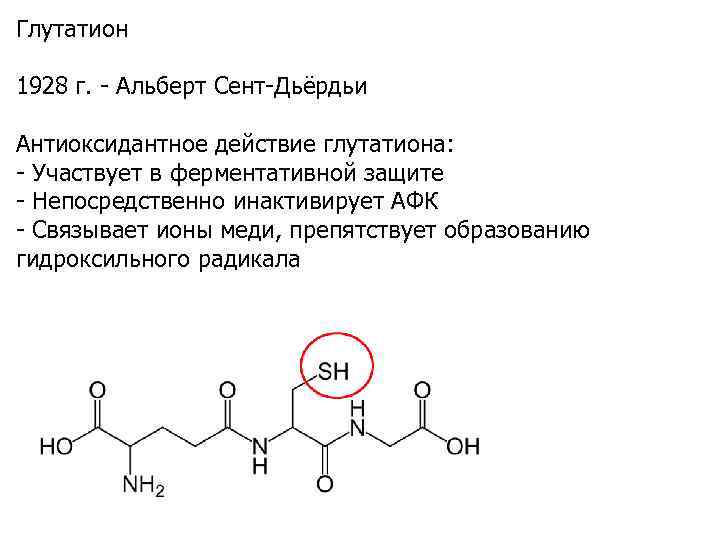 Глутатион 1928 г. - Альберт Сент-Дьёрдьи Антиоксидантное действие глутатиона: - Участвует в ферментативной защите - Непосредственно инактивирует АФК - Связывает ионы меди, препятствует образованию гидроксильного радикала
Глутатион 1928 г. - Альберт Сент-Дьёрдьи Антиоксидантное действие глутатиона: - Участвует в ферментативной защите - Непосредственно инактивирует АФК - Связывает ионы меди, препятствует образованию гидроксильного радикала
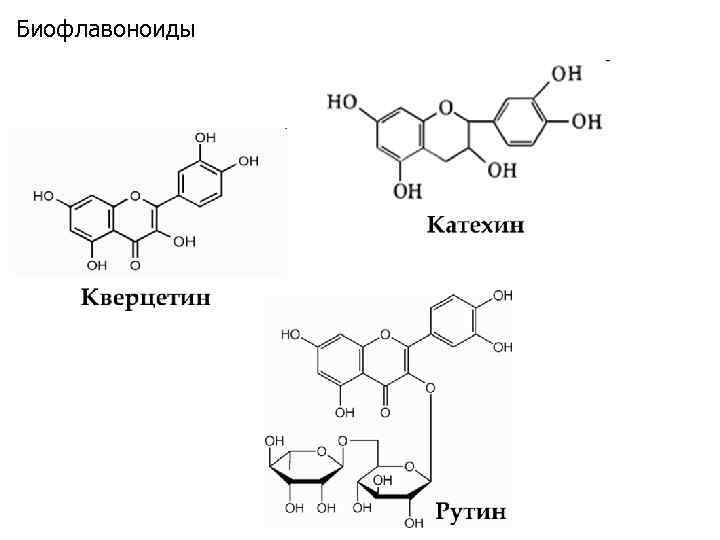 Биофлавоноиды
Биофлавоноиды
 Флавоноиды активны в отношении радикалов, возникающих как в липидной, так и водной фазах, и ингибируют процессы ПОЛ на стадии инициации, взаимодействуя с активными формами кислорода О 2 • ‾, Н 2 О 2. , RO 2 • , ОН • , синглетным кислородом и на стадии продолжения цепи, выступая донорами атомов водорода для липидных радикалов. Многие флавоноиды действую как хелаторы ионов металлов переменной валентности и способны тем самым ингибировать ПОЛ. Также восстанавливают окисленный глутатион и окисленную аскорбиновую кислоту.
Флавоноиды активны в отношении радикалов, возникающих как в липидной, так и водной фазах, и ингибируют процессы ПОЛ на стадии инициации, взаимодействуя с активными формами кислорода О 2 • ‾, Н 2 О 2. , RO 2 • , ОН • , синглетным кислородом и на стадии продолжения цепи, выступая донорами атомов водорода для липидных радикалов. Многие флавоноиды действую как хелаторы ионов металлов переменной валентности и способны тем самым ингибировать ПОЛ. Также восстанавливают окисленный глутатион и окисленную аскорбиновую кислоту.
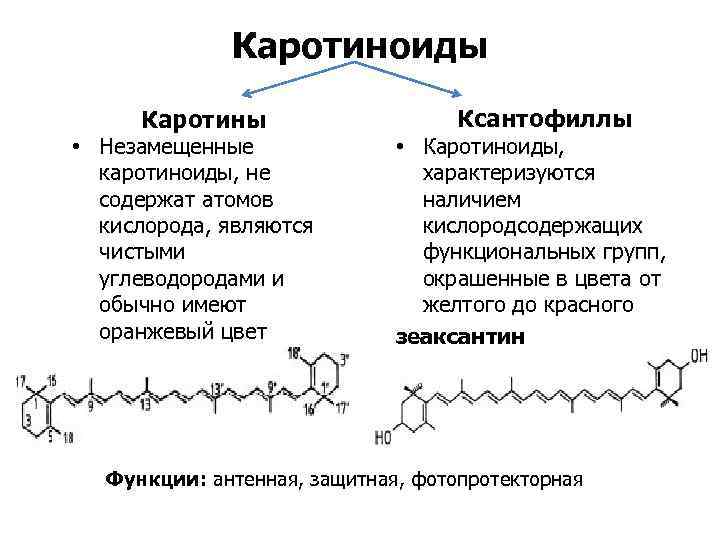 Каротиноиды Каротины • Незамещенные каротиноиды, не содержат атомов кислорода, являются чистыми углеводородами и обычно имеют оранжевый цвет в-каротин Ксантофиллы • Каротиноиды, характеризуются наличием кислородсодержащих функциональных групп, окрашенные в цвета от желтого до красного зеаксантин Функции: антенная, защитная, фотопротекторная
Каротиноиды Каротины • Незамещенные каротиноиды, не содержат атомов кислорода, являются чистыми углеводородами и обычно имеют оранжевый цвет в-каротин Ксантофиллы • Каротиноиды, характеризуются наличием кислородсодержащих функциональных групп, окрашенные в цвета от желтого до красного зеаксантин Функции: антенная, защитная, фотопротекторная
 Токоферол (витамин Е) • играет важную роль в защите основных структурных компонентов биомембран • обезвреживает свободные радикалы в жировом слое клеточных мембран • эффективно прерывает цепные свободнорадикальные реакции в процессе окисления ненасыщенных жирных кислот в мембранах • играет важную роль в обмене селена - составной части глутатионпероксидазы, которая защищает мембраны от пероксидных радикалов (альфатокоферол) • предотвращает аутоокисление липидов мембран, снижает потребность в глутатионпероксидазе
Токоферол (витамин Е) • играет важную роль в защите основных структурных компонентов биомембран • обезвреживает свободные радикалы в жировом слое клеточных мембран • эффективно прерывает цепные свободнорадикальные реакции в процессе окисления ненасыщенных жирных кислот в мембранах • играет важную роль в обмене селена - составной части глутатионпероксидазы, которая защищает мембраны от пероксидных радикалов (альфатокоферол) • предотвращает аутоокисление липидов мембран, снижает потребность в глутатионпероксидазе


