АФК,_редокс-механизмы_Лекция.pptx
- Количество слайдов: 49
 Активные формы кислорода и антиоксидантная система. Регуляция клеточного редокс-статуса в норме и при патологии. Роль глутатиона и глутатион-зависимых ферментов в редокс-зависимых механизмах формирования лекарственной устойчивости опухолевых клеток. Редокс-зависимая регуляция механизмов гибели опухолевых клеток
Активные формы кислорода и антиоксидантная система. Регуляция клеточного редокс-статуса в норме и при патологии. Роль глутатиона и глутатион-зависимых ферментов в редокс-зависимых механизмах формирования лекарственной устойчивости опухолевых клеток. Редокс-зависимая регуляция механизмов гибели опухолевых клеток
 Проблема свободных радикалов в последнее десятилетие произвела настоящую революцию в понимании многих процессов, происходящем в организме человека. Сегодня свободные радикалы рассматриваются в качестве источника многочисленных нарушений, приводящих к возникновению целого ряда болезней. В основе образования этих агрессивных радикалов, которые окрестили «молекулярными акулами» , обладающими неутолимым аппетитом в результате потери одного электрона, как ни удивительно, лежит один из самых значительных элементов для жизни человека – кислород.
Проблема свободных радикалов в последнее десятилетие произвела настоящую революцию в понимании многих процессов, происходящем в организме человека. Сегодня свободные радикалы рассматриваются в качестве источника многочисленных нарушений, приводящих к возникновению целого ряда болезней. В основе образования этих агрессивных радикалов, которые окрестили «молекулярными акулами» , обладающими неутолимым аппетитом в результате потери одного электрона, как ни удивительно, лежит один из самых значительных элементов для жизни человека – кислород.
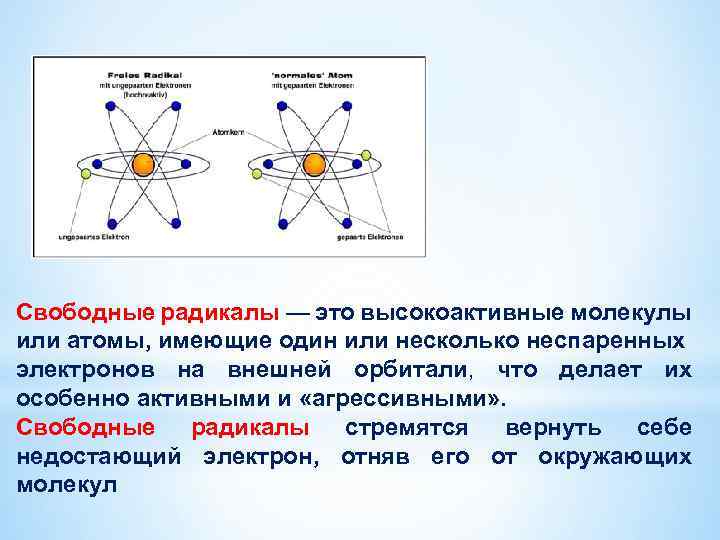 Свободные радикалы — это высокоактивные молекулы или атомы, имеющие один или несколько неспаренных электронов на внешней орбитали, что делает их особенно активными и «агрессивными» . Свободные радикалы стремятся вернуть себе недостающий электрон, отняв его от окружающих молекул
Свободные радикалы — это высокоактивные молекулы или атомы, имеющие один или несколько неспаренных электронов на внешней орбитали, что делает их особенно активными и «агрессивными» . Свободные радикалы стремятся вернуть себе недостающий электрон, отняв его от окружающих молекул
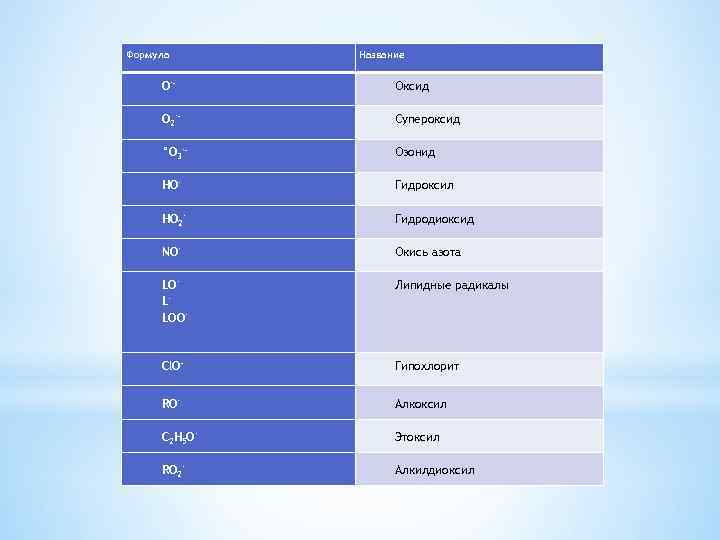 Формула Название O·– Оксид O 2·– Супероксид °O 3·– Озонид HO· Гидроксил HO 2· Гидродиоксид NO· Окись азота LO· L· LOO· Липидные радикалы Cl. O– Гипохлорит RO· Алкоксил C 2 H 5 O· Этоксил RО 2· Алкилдиоксил
Формула Название O·– Оксид O 2·– Супероксид °O 3·– Озонид HO· Гидроксил HO 2· Гидродиоксид NO· Окись азота LO· L· LOO· Липидные радикалы Cl. O– Гипохлорит RO· Алкоксил C 2 H 5 O· Этоксил RО 2· Алкилдиоксил
 Для биологических систем наиболее важны кислородные свободные радикалы, которые включены в группу активных форм кислорода – АФК. Поэтапное одноэлектронное восстановление кислорода протекает с образованием промежуточных свободнорадикальных состояний кислорода, в частности, супероксид-аниона и гидроксильного радикала: O 2 + ē O 2·– + ē Н 2 О 2 + ē супероксид-анион радикал • ОН + ē Н 2 O гидроксильный радикал время полужизни ≈ 10 -9 с
Для биологических систем наиболее важны кислородные свободные радикалы, которые включены в группу активных форм кислорода – АФК. Поэтапное одноэлектронное восстановление кислорода протекает с образованием промежуточных свободнорадикальных состояний кислорода, в частности, супероксид-аниона и гидроксильного радикала: O 2 + ē O 2·– + ē Н 2 О 2 + ē супероксид-анион радикал • ОН + ē Н 2 O гидроксильный радикал время полужизни ≈ 10 -9 с
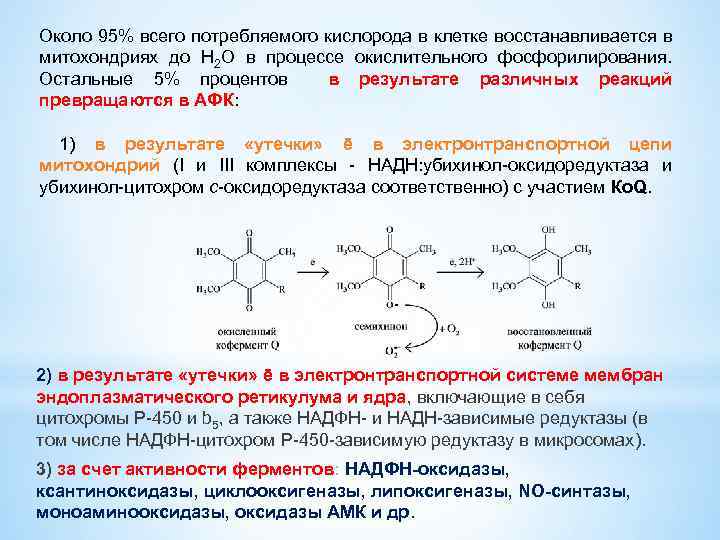 Около 95% всего потребляемого кислорода в клетке восстанавливается в митохондриях до Н 2 O в процессе окислительного фосфорилирования. Остальные 5% процентов в результате различных реакций превращаются в АФК: 1) в результате «утечки» ē в электронтранспортной цепи митохондрий (I и III комплексы - НАДН: убихинол-оксидоредуктаза и убихинол-цитохром с-оксидоредуктаза соответственно) с участием Ко. Q. 2) в результате «утечки» ē в электронтранспортной системе мембран эндоплазматического ретикулума и ядра, включающие в себя цитохромы Р-450 и b 5, а также НАДФН- и НАДН-зависимые редуктазы (в том числе НАДФН-цитохром Р-450 -зависимую редуктазу в микросомах). 3) за счет активности ферментов: НАДФН-оксидазы, ксантиноксидазы, циклооксигеназы, липоксигеназы, NO-синтазы, моноаминооксидазы, оксидазы АМК и др.
Около 95% всего потребляемого кислорода в клетке восстанавливается в митохондриях до Н 2 O в процессе окислительного фосфорилирования. Остальные 5% процентов в результате различных реакций превращаются в АФК: 1) в результате «утечки» ē в электронтранспортной цепи митохондрий (I и III комплексы - НАДН: убихинол-оксидоредуктаза и убихинол-цитохром с-оксидоредуктаза соответственно) с участием Ко. Q. 2) в результате «утечки» ē в электронтранспортной системе мембран эндоплазматического ретикулума и ядра, включающие в себя цитохромы Р-450 и b 5, а также НАДФН- и НАДН-зависимые редуктазы (в том числе НАДФН-цитохром Р-450 -зависимую редуктазу в микросомах). 3) за счет активности ферментов: НАДФН-оксидазы, ксантиноксидазы, циклооксигеназы, липоксигеназы, NO-синтазы, моноаминооксидазы, оксидазы АМК и др.
 4) фагоциты (гранулоциты и моноциты крови) и тканевые макрофаги для борьбы с бактериями образуют O 2·– при активации НАДФН-оксидазного комплекса на цитоплазматической мембране НАДФН (Н+) миелопероксидаза Н 2 О 2 Cl–, H+ Fe 2+ HOCl гипохлорид • ОН 5) ионы Fe 2+ (а также ионы других металлов переменной валентности Cu 2+, Co 2+) способствуют образованию • ОН радикалов посредством реакции Фентона 6) автоокисление гемоглобина Hb(Fe 2+) 7) УФ, радиация Hb(Fe 3+) + ē
4) фагоциты (гранулоциты и моноциты крови) и тканевые макрофаги для борьбы с бактериями образуют O 2·– при активации НАДФН-оксидазного комплекса на цитоплазматической мембране НАДФН (Н+) миелопероксидаза Н 2 О 2 Cl–, H+ Fe 2+ HOCl гипохлорид • ОН 5) ионы Fe 2+ (а также ионы других металлов переменной валентности Cu 2+, Co 2+) способствуют образованию • ОН радикалов посредством реакции Фентона 6) автоокисление гемоглобина Hb(Fe 2+) 7) УФ, радиация Hb(Fe 3+) + ē

 Таким образом, ряд биохимических процессов, протекающих в аэробных организмах, сопряжен с образованием АФК, таких как супероксидный анион -радикал (O 2·–), гидроксильный радикал ( • ОН ), перекись водорода (H 2 O 2), синглетный кислород (1 O 2), гипохлорная кислота (HOCl). Ряд авторов к АФК относят также такие активные формы азота как окись азота (NO. ) и пероксинитрит ( ), обладающий высокой реакционной способностью.
Таким образом, ряд биохимических процессов, протекающих в аэробных организмах, сопряжен с образованием АФК, таких как супероксидный анион -радикал (O 2·–), гидроксильный радикал ( • ОН ), перекись водорода (H 2 O 2), синглетный кислород (1 O 2), гипохлорная кислота (HOCl). Ряд авторов к АФК относят также такие активные формы азота как окись азота (NO. ) и пероксинитрит ( ), обладающий высокой реакционной способностью.
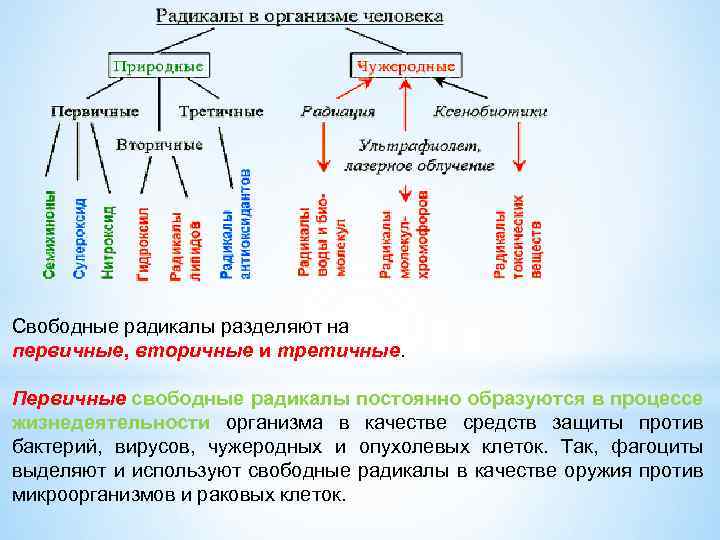 Свободные радикалы разделяют на первичные, вторичные и третичные. Первичные свободные радикалы постоянно образуются в процессе жизнедеятельности организма в качестве средств защиты против бактерий, вирусов, чужеродных и опухолевых клеток. Так, фагоциты выделяют и используют свободные радикалы в качестве оружия против микроорганизмов и раковых клеток.
Свободные радикалы разделяют на первичные, вторичные и третичные. Первичные свободные радикалы постоянно образуются в процессе жизнедеятельности организма в качестве средств защиты против бактерий, вирусов, чужеродных и опухолевых клеток. Так, фагоциты выделяют и используют свободные радикалы в качестве оружия против микроорганизмов и раковых клеток.
 Вторичные радикалы, в отличие от первичных, не выполняют физиологически полезных функций. Напротив, они оказывают разрушительное действие на клеточные структуры, стремясь отнять электроны у «полноценных» молекул, вследствие чего «пострадавшая» молекула сама становится свободным радикалом (третичным), но чаще всего слабым, не способным к разрушающему действию.
Вторичные радикалы, в отличие от первичных, не выполняют физиологически полезных функций. Напротив, они оказывают разрушительное действие на клеточные структуры, стремясь отнять электроны у «полноценных» молекул, вследствие чего «пострадавшая» молекула сама становится свободным радикалом (третичным), но чаще всего слабым, не способным к разрушающему действию.
 Образующиеся АФК могут выполнять полезные для клетки функции: * участвуют (через АФК-зависимый сигналинг) в регуляции клеточных процессов (клеточное деление, дыхание и др. ), * бактерицидное действие, * активируют иммунные реакции лейкоцитов. Однако это возможно при низком уровне АФК в клетке. При высоком уровне АФК развивается окислительный (оксидативный) стресс, который приводит к нарушению функций клетки, развитию ряда заболеваний (атеросклероз, ИБС, диабет, ХОБЛ, болезнь Альцгеймера, болезнь Паркинсона, злокачественные образования и др. ), гибели клеток путем апоптоза или некроза.
Образующиеся АФК могут выполнять полезные для клетки функции: * участвуют (через АФК-зависимый сигналинг) в регуляции клеточных процессов (клеточное деление, дыхание и др. ), * бактерицидное действие, * активируют иммунные реакции лейкоцитов. Однако это возможно при низком уровне АФК в клетке. При высоком уровне АФК развивается окислительный (оксидативный) стресс, который приводит к нарушению функций клетки, развитию ряда заболеваний (атеросклероз, ИБС, диабет, ХОБЛ, болезнь Альцгеймера, болезнь Паркинсона, злокачественные образования и др. ), гибели клеток путем апоптоза или некроза.
 Таким образом, свободные радикалы совершенно необходимы, так как они участвуют во многих физиологических процессах организма. Однако свободные радикалы в организме могут причинять вред, когда их количество возрастает и значительно превосходит, необходимое для осуществления окислительных процессов. Где та норма, при которой свободные радикалы полезны? Как контролировать свободнорадикальные процессы в организме?
Таким образом, свободные радикалы совершенно необходимы, так как они участвуют во многих физиологических процессах организма. Однако свободные радикалы в организме могут причинять вред, когда их количество возрастает и значительно превосходит, необходимое для осуществления окислительных процессов. Где та норма, при которой свободные радикалы полезны? Как контролировать свободнорадикальные процессы в организме?
 Живые клетки имеют систему защиты от повышенной продукции свободных радикалов - антиоксидантную систему, механизм действия которой направлен на блокирование действия свободных радикалов. Антиоксидантная система образована низкомолекулярными антиоксидантами и антиоксидантными ферментами. Антиоксиданты «ловят» радикалы, отдавая им свои электроны, таким образом, обезвреживая их. При этом структура антиоксидантов остается стабильной.
Живые клетки имеют систему защиты от повышенной продукции свободных радикалов - антиоксидантную систему, механизм действия которой направлен на блокирование действия свободных радикалов. Антиоксидантная система образована низкомолекулярными антиоксидантами и антиоксидантными ферментами. Антиоксиданты «ловят» радикалы, отдавая им свои электроны, таким образом, обезвреживая их. При этом структура антиоксидантов остается стабильной.
 Низкомолекулярные антиоксиданты: Токоферол (вит. Е) Ретинол (вит. А) Аскорбиновая кислота (вит. С) Глутатион восстановленный N-ацетилцистеин Мочевина, мочевая кислота, билирубин Карнозин и другие гистидинсодержащие дипептиды
Низкомолекулярные антиоксиданты: Токоферол (вит. Е) Ретинол (вит. А) Аскорбиновая кислота (вит. С) Глутатион восстановленный N-ацетилцистеин Мочевина, мочевая кислота, билирубин Карнозин и другие гистидинсодержащие дипептиды
 Ключевыми антиоксидантными ферментами являются супероксиддисмутаза (СОД), каталаза, глутатионпероксидаза. Они катализируют реакции, в результате которых свободные радикалы и перекиси превращаются в неактивные соединения Супероксиддисмутаза (разные формы содержат Cu/Zn и Mn): О 2 - + 2 Н+ Н 2 О 2 + О 2 Каталаза (гемсодержащий фермент): 2 Н 2 О 2 2 Н 2 О + О 2 Глутатионпероксидаза (содержит остаток селеноцистеина): 2 GSH + Н 2 О 2 GSSG + 2 Н 2 O
Ключевыми антиоксидантными ферментами являются супероксиддисмутаза (СОД), каталаза, глутатионпероксидаза. Они катализируют реакции, в результате которых свободные радикалы и перекиси превращаются в неактивные соединения Супероксиддисмутаза (разные формы содержат Cu/Zn и Mn): О 2 - + 2 Н+ Н 2 О 2 + О 2 Каталаза (гемсодержащий фермент): 2 Н 2 О 2 2 Н 2 О + О 2 Глутатионпероксидаза (содержит остаток селеноцистеина): 2 GSH + Н 2 О 2 GSSG + 2 Н 2 O
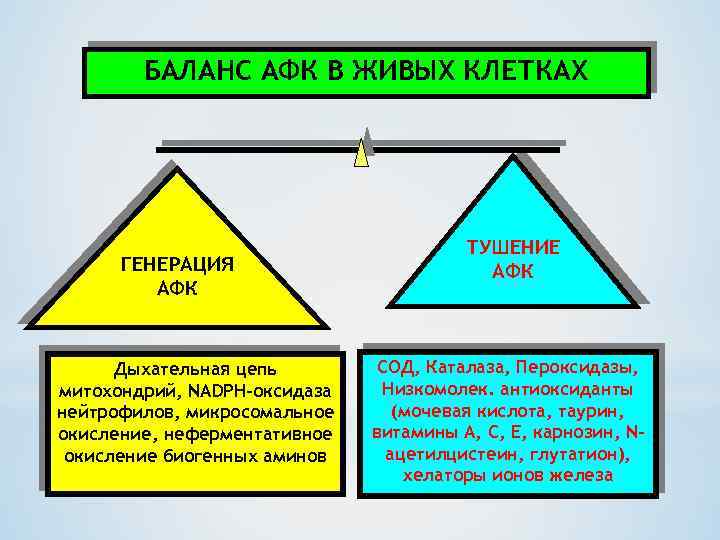 БАЛАНС АФК В ЖИВЫХ КЛЕТКАХ ГЕНЕРАЦИЯ АФК Дыхательная цепь митохондрий, NADPH-оксидаза нейтрофилов, микросомальное окисление, неферментативное окисление биогенных аминов ТУШЕНИЕ АФК СОД, Каталаза, Пероксидазы, Низкомолек. антиоксиданты (мочевая кислота, таурин, витамины A, C, E, карнозин, Nацетилцистеин, глутатион), xелаторы ионов железа
БАЛАНС АФК В ЖИВЫХ КЛЕТКАХ ГЕНЕРАЦИЯ АФК Дыхательная цепь митохондрий, NADPH-оксидаза нейтрофилов, микросомальное окисление, неферментативное окисление биогенных аминов ТУШЕНИЕ АФК СОД, Каталаза, Пероксидазы, Низкомолек. антиоксиданты (мочевая кислота, таурин, витамины A, C, E, карнозин, Nацетилцистеин, глутатион), xелаторы ионов железа
 В норме существует баланс между продукцией АФК и уровнем антиоксидантной системы, (активность антиоксидантных ферментов + содержание низкомолекулярных антиоксидантов), который обеспечивает физиологически необходимый уровень АФК. Баланс окислительно-восстановительных процессов в клетке определяет клеточный редоксстатус (от англ. redox — reduction-oxidation reaction). Баланс между продукцией АФК и уровнем антиоксидантной системы вносит значительный вклад в состояние клеточного редокс-статуса
В норме существует баланс между продукцией АФК и уровнем антиоксидантной системы, (активность антиоксидантных ферментов + содержание низкомолекулярных антиоксидантов), который обеспечивает физиологически необходимый уровень АФК. Баланс окислительно-восстановительных процессов в клетке определяет клеточный редоксстатус (от англ. redox — reduction-oxidation reaction). Баланс между продукцией АФК и уровнем антиоксидантной системы вносит значительный вклад в состояние клеточного редокс-статуса
 Поддержание нормального редокс-статуса внутри клеток играет существенную роль в таких процессах как синтез ДНК, экспрессия генов, ферментативная активность. Изменения редокс-состояния молекул, являющиеся следствием стрессовых воздействий или результатом активности самих клеток, вовлечены в редокс-регуляцию клеточных процессов. Небольшие изменения внутриклеточного уровня АФК участвуют в клеточном АФК-зависимом сигналинге.
Поддержание нормального редокс-статуса внутри клеток играет существенную роль в таких процессах как синтез ДНК, экспрессия генов, ферментативная активность. Изменения редокс-состояния молекул, являющиеся следствием стрессовых воздействий или результатом активности самих клеток, вовлечены в редокс-регуляцию клеточных процессов. Небольшие изменения внутриклеточного уровня АФК участвуют в клеточном АФК-зависимом сигналинге.
 Важную роль в поддержании клеточного редоксстатуса и в редокс-регуляции играют тиолсодержащие молекулы: трипептид глутатион (GSH: γ-глутамил-L-цистеинилглицин) и редокс-зависимые белки - тиоредоксины, глутаредоксины и пероксиредоксины
Важную роль в поддержании клеточного редоксстатуса и в редокс-регуляции играют тиолсодержащие молекулы: трипептид глутатион (GSH: γ-глутамил-L-цистеинилглицин) и редокс-зависимые белки - тиоредоксины, глутаредоксины и пероксиредоксины
 Роль в поддержании клеточного редокс-статуса за счет участия в SH –S–S– обмене, что обеспечивает регуляцию целого ряда функций клетки, в том числе регуляцию генной экспрессии, делает GSH весьма важным для жизнеспособности клеток.
Роль в поддержании клеточного редокс-статуса за счет участия в SH –S–S– обмене, что обеспечивает регуляцию целого ряда функций клетки, в том числе регуляцию генной экспрессии, делает GSH весьма важным для жизнеспособности клеток.
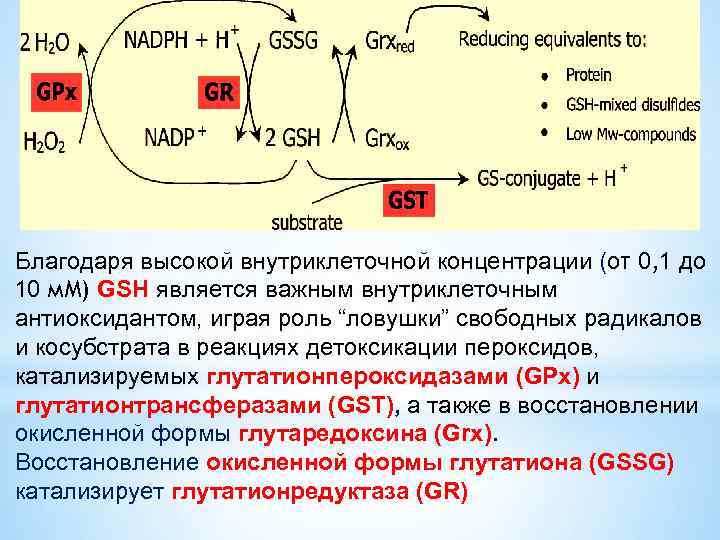 Благодаря высокой внутриклеточной концентрации (от 0, 1 до 10 м. М) GSH является важным внутриклеточным антиоксидантом, играя роль “ловушки” свободных радикалов и косубстрата в реакциях детоксикации пероксидов, катализируемых глутатионпероксидазами (GPx) и глутатионтрансферазами (GST), а также в восстановлении окисленной формы глутаредоксина (Grx). Восстановление окисленной формы глутатиона (GSSG) катализирует глутатионредуктаза (GR)
Благодаря высокой внутриклеточной концентрации (от 0, 1 до 10 м. М) GSH является важным внутриклеточным антиоксидантом, играя роль “ловушки” свободных радикалов и косубстрата в реакциях детоксикации пероксидов, катализируемых глутатионпероксидазами (GPx) и глутатионтрансферазами (GST), а также в восстановлении окисленной формы глутаредоксина (Grx). Восстановление окисленной формы глутатиона (GSSG) катализирует глутатионредуктаза (GR)
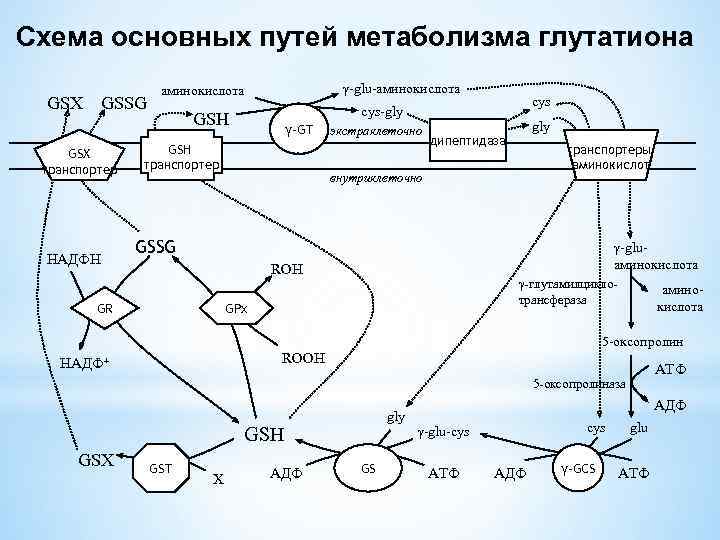 Схема основных путей метаболизма глутатиона GSX GSSG GSX транспортер НАДФН γ-glu-аминокислота cys cys-gly GSH γ-GT GSH транспортер экстраклеточно gly дипептидаза транспортеры аминокислот внутриклеточно GSSG γ-gluаминокислота ROH GR γ-глутамилциклотрансфераза GPx аминокислота 5 -оксопролин ROOH НAДФ+ ATФ 5 -оксопролиназа gly GSH GSX GST X AДФ GS AДФ cys γ-glu-cys ATФ AДФ γ-GCS glu ATФ
Схема основных путей метаболизма глутатиона GSX GSSG GSX транспортер НАДФН γ-glu-аминокислота cys cys-gly GSH γ-GT GSH транспортер экстраклеточно gly дипептидаза транспортеры аминокислот внутриклеточно GSSG γ-gluаминокислота ROH GR γ-глутамилциклотрансфераза GPx аминокислота 5 -оксопролин ROOH НAДФ+ ATФ 5 -оксопролиназа gly GSH GSX GST X AДФ GS AДФ cys γ-glu-cys ATФ AДФ γ-GCS glu ATФ
 Поддерживание оптимального для клетки соотношения GSH/GSSG является важным для ее жизнеспособности. Повышение уровня GSH способствует росту клеточной резистентности к действию радиации, подавляет гибель клеток путем апоптоза или некроза. Снижение уровня восстановленного GSH ниже обычных (для показателей нормы) значений служит индикатором дефицита антиоксидантной защиты. Нарушение внутриклеточного баланса GSH (снижение GSH/GSSG) наблюдается при ряде патологий, включая злокачественные новообразования, ВИЧ, ИБС, ХОБЛ, нейродегенеративные заболевания, болезнь Паркинсона, этиопатогенетическим фактором которых является окислительный стресс.
Поддерживание оптимального для клетки соотношения GSH/GSSG является важным для ее жизнеспособности. Повышение уровня GSH способствует росту клеточной резистентности к действию радиации, подавляет гибель клеток путем апоптоза или некроза. Снижение уровня восстановленного GSH ниже обычных (для показателей нормы) значений служит индикатором дефицита антиоксидантной защиты. Нарушение внутриклеточного баланса GSH (снижение GSH/GSSG) наблюдается при ряде патологий, включая злокачественные новообразования, ВИЧ, ИБС, ХОБЛ, нейродегенеративные заболевания, болезнь Паркинсона, этиопатогенетическим фактором которых является окислительный стресс.
 Глутатион S-трансферазы, использующие нуклеофильный GSH для конъюгации с неполярными соединениями, содержащими электрофильные атомы C, N и S. Суперсемейство GST подразделяется на три субсемейства: цитозольные, митохондриальные GST и микросомальные GST. Основными функциями GST являются: а) детоксикация ксенобиотиков; б) редокс-регуляция чувствительности клеток к апоптозу, б) детоксикация продуктов окислительного стресса:
Глутатион S-трансферазы, использующие нуклеофильный GSH для конъюгации с неполярными соединениями, содержащими электрофильные атомы C, N и S. Суперсемейство GST подразделяется на три субсемейства: цитозольные, митохондриальные GST и микросомальные GST. Основными функциями GST являются: а) детоксикация ксенобиотиков; б) редокс-регуляция чувствительности клеток к апоптозу, б) детоксикация продуктов окислительного стресса:
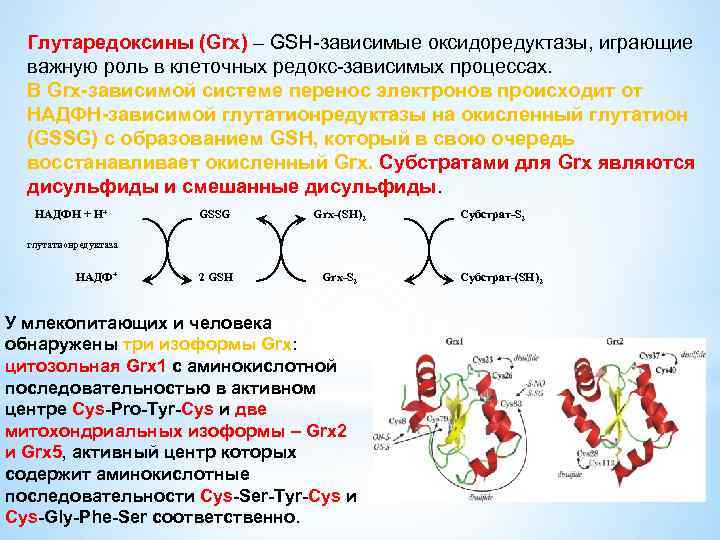 Глутаредоксины (Grx) – GSH-зависимые оксидоредуктазы, играющие важную роль в клеточных редокс-зависимых процессах. В Grx-зависимой системе перенос электронов происходит от НАДФН-зависимой глутатионредуктазы на окисленный глутатион (GSSG) с образованием GSH, который в свою очередь восстанавливает окисленный Grx. Субстратами для Grx являются дисульфиды и смешанные дисульфиды. НAДФH + H+ GSSG Grx-(SH)2 2 GSH Grx-S 2 Субстрат-S 2 глутатионредуктаза НAДФ+ У млекопитающих и человека обнаружены три изоформы Grx: цитозольная Grx 1 с аминокислотной последовательностью в активном центре Cys-Pro-Tyr-Cys и две митохондриальных изоформы – Grx 2 и Grx 5, активный центр которых содержит аминокислотные последовательности Cys-Ser-Tyr-Cys и Cys-Gly-Phe-Ser соответственно. Субстрат-(SH)2
Глутаредоксины (Grx) – GSH-зависимые оксидоредуктазы, играющие важную роль в клеточных редокс-зависимых процессах. В Grx-зависимой системе перенос электронов происходит от НАДФН-зависимой глутатионредуктазы на окисленный глутатион (GSSG) с образованием GSH, который в свою очередь восстанавливает окисленный Grx. Субстратами для Grx являются дисульфиды и смешанные дисульфиды. НAДФH + H+ GSSG Grx-(SH)2 2 GSH Grx-S 2 Субстрат-S 2 глутатионредуктаза НAДФ+ У млекопитающих и человека обнаружены три изоформы Grx: цитозольная Grx 1 с аминокислотной последовательностью в активном центре Cys-Pro-Tyr-Cys и две митохондриальных изоформы – Grx 2 и Grx 5, активный центр которых содержит аминокислотные последовательности Cys-Ser-Tyr-Cys и Cys-Gly-Phe-Ser соответственно. Субстрат-(SH)2
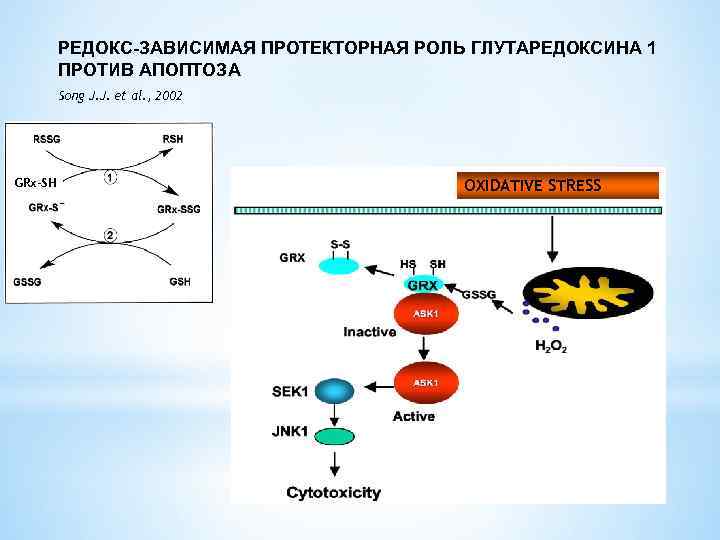 РЕДОКС-ЗАВИСИМАЯ ПРОТЕКТОРНАЯ РОЛЬ ГЛУТАРЕДОКСИНА 1 ПРОТИВ АПОПТОЗА Song J. J. et al. , 2002 GRx-SH OXIDATIVE STRESS
РЕДОКС-ЗАВИСИМАЯ ПРОТЕКТОРНАЯ РОЛЬ ГЛУТАРЕДОКСИНА 1 ПРОТИВ АПОПТОЗА Song J. J. et al. , 2002 GRx-SH OXIDATIVE STRESS
 Сочетание антиоксидантных свойств и способности активировать транскрипцию генов, в том числе некоторых антиоксидантных ферментов, а также ингибировать редокс-зависимые пути активации апоптоза свидетельствуют о важном вкладе тиоредоксина (Trx) в антиоксидантную защитную систему. Trx как и Grx является дисульфидредуктазой и входит в состав суперсемейства тиоредоксинов. Trx-зависимая система содержит помимо Trx НАДФ-зависимую тиоредоксинредуктазу (Trx. R), которая восстанавливает окисленную форму Trx. Основными изоформами Trx являются цитозольный Trx 1 и митохондриальный Trx 2.
Сочетание антиоксидантных свойств и способности активировать транскрипцию генов, в том числе некоторых антиоксидантных ферментов, а также ингибировать редокс-зависимые пути активации апоптоза свидетельствуют о важном вкладе тиоредоксина (Trx) в антиоксидантную защитную систему. Trx как и Grx является дисульфидредуктазой и входит в состав суперсемейства тиоредоксинов. Trx-зависимая система содержит помимо Trx НАДФ-зависимую тиоредоксинредуктазу (Trx. R), которая восстанавливает окисленную форму Trx. Основными изоформами Trx являются цитозольный Trx 1 и митохондриальный Trx 2.
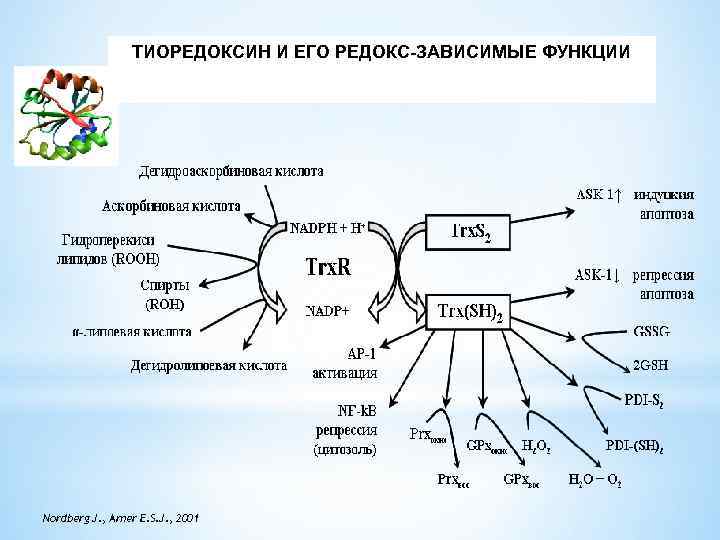 ТИОРЕДОКСИН И ЕГО РЕДОКС-ЗАВИСИМЫЕ ФУНКЦИИ Nordberg J. , Arner E. S. J. , 2001
ТИОРЕДОКСИН И ЕГО РЕДОКС-ЗАВИСИМЫЕ ФУНКЦИИ Nordberg J. , Arner E. S. J. , 2001
 Пероксиредоксины (Prx), образующие суперсемейство Se-независимых пероксидаз, открыты около 10 лет назад. Prx осуществляют ферментативную деградацию H 2 O 2, органических гидропероксидов, пероксинитрита. Известно 6 изоформ Prx (Prx 1 -6). Типичные двухцистеиновые Prx 1 – Prx 4 являются гомодимерами, и их взаимодействие с Н 2 О 2 приводит к образованию сульфеновой кислоты, которая может участвовать в формировании межпептидной дисульфидной связи, восстанавливаемой действием Trx. Окисленный Prx 6 использует в качестве источника электронов не Тrx, как другие Prx, а низкомолекулярные тиолы, в том числе GSH Механизм действия пероксиредоксинов
Пероксиредоксины (Prx), образующие суперсемейство Se-независимых пероксидаз, открыты около 10 лет назад. Prx осуществляют ферментативную деградацию H 2 O 2, органических гидропероксидов, пероксинитрита. Известно 6 изоформ Prx (Prx 1 -6). Типичные двухцистеиновые Prx 1 – Prx 4 являются гомодимерами, и их взаимодействие с Н 2 О 2 приводит к образованию сульфеновой кислоты, которая может участвовать в формировании межпептидной дисульфидной связи, восстанавливаемой действием Trx. Окисленный Prx 6 использует в качестве источника электронов не Тrx, как другие Prx, а низкомолекулярные тиолы, в том числе GSH Механизм действия пероксиредоксинов
 ТАКИМ ОБРАЗОМ, в антиоксидантной системе клеток наряду с ключевыми антиоксидантными ферментами важную роль играют редокс-белки тиоредоксин (Trx), глутаредоксин (Grx), пероксиредоксин (Prx), участвующие в процессах клеточной редокс-зависимой регуляции посредством контроля тиол-дисульфидного обмена. Эти редокс-зависимые белки высоко значимы в поддержании клеточного редокс-гомеостаза и редокс -зависимой регуляции целого ряда внутриклеточных процессов, в том числе пролиферации, дифференцировки и апоптоза.
ТАКИМ ОБРАЗОМ, в антиоксидантной системе клеток наряду с ключевыми антиоксидантными ферментами важную роль играют редокс-белки тиоредоксин (Trx), глутаредоксин (Grx), пероксиредоксин (Prx), участвующие в процессах клеточной редокс-зависимой регуляции посредством контроля тиол-дисульфидного обмена. Эти редокс-зависимые белки высоко значимы в поддержании клеточного редокс-гомеостаза и редокс -зависимой регуляции целого ряда внутриклеточных процессов, в том числе пролиферации, дифференцировки и апоптоза.
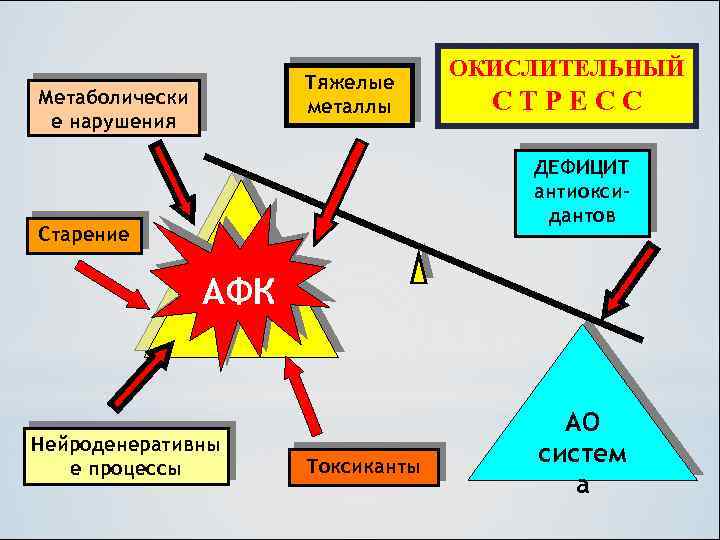 Тяжелые металлы Метаболически е нарушения ОКИСЛИТЕЛЬНЫЙ СТРЕСС ДЕФИЦИТ антиоксидантов Старение АФК Нейроденеративны е процессы Токсиканты AO систем а
Тяжелые металлы Метаболически е нарушения ОКИСЛИТЕЛЬНЫЙ СТРЕСС ДЕФИЦИТ антиоксидантов Старение АФК Нейроденеративны е процессы Токсиканты AO систем а
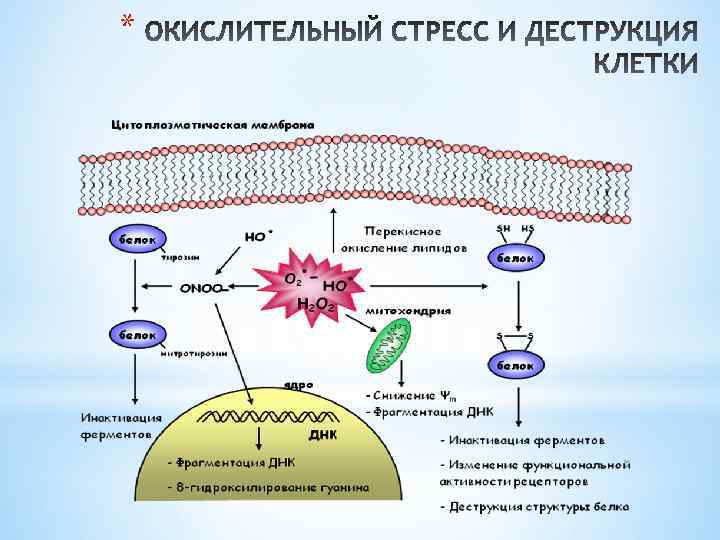
 Нарушение баланса АФК/антиоксиданты приводит к развитию окислительного стресса, который сопровождается активацией перекисного (пероксидного) окисления липидов (ПОЛ). Наиболее чувствительные к ПОЛ полиненасыщенные ВЖК липидного бислоя клеточных мембран
Нарушение баланса АФК/антиоксиданты приводит к развитию окислительного стресса, который сопровождается активацией перекисного (пероксидного) окисления липидов (ПОЛ). Наиболее чувствительные к ПОЛ полиненасыщенные ВЖК липидного бислоя клеточных мембран
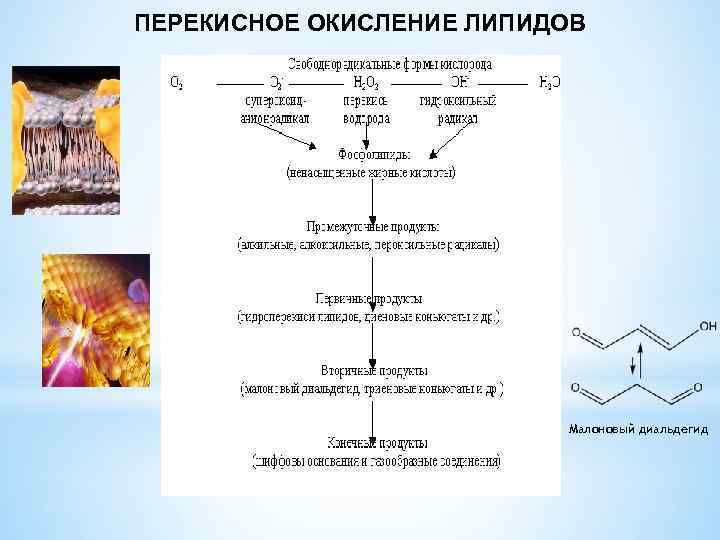 ПЕРЕКИСНОЕ ОКИСЛЕНИЕ ЛИПИДОВ Малоновый диальдегид
ПЕРЕКИСНОЕ ОКИСЛЕНИЕ ЛИПИДОВ Малоновый диальдегид
 Перекисное окисление липидов (ПОЛ) является важной причиной накопления клеточных дефектов. Основным субстратом ПОЛ являются полиненасыщенные жирные кислоты, входящих в состав клеточных мембран, а также липопротеинов. Атака кислородными радикалами приводит к образованию гидрофобных радикалов. Образующиеся липидные радикалы, а также 4 -гидроксиноненаль и малоновый диальдегид могут атаковать молекулы белков и нуклеиновых кислот. Альдегидные группы этих соединений образуют межмолекулярные сшивки, что сопровождается нарушением структуры макромолекул и их функций. ПОЛ изменяет свойства мембран: *нарушается микровязкость (↑) *образуются “мега” поры *растет проницаемость мембран → набухание *изменяется ионная проницаемость (разрушение ионных каналов и ионных насосов, например, Nа, КАТФазы)
Перекисное окисление липидов (ПОЛ) является важной причиной накопления клеточных дефектов. Основным субстратом ПОЛ являются полиненасыщенные жирные кислоты, входящих в состав клеточных мембран, а также липопротеинов. Атака кислородными радикалами приводит к образованию гидрофобных радикалов. Образующиеся липидные радикалы, а также 4 -гидроксиноненаль и малоновый диальдегид могут атаковать молекулы белков и нуклеиновых кислот. Альдегидные группы этих соединений образуют межмолекулярные сшивки, что сопровождается нарушением структуры макромолекул и их функций. ПОЛ изменяет свойства мембран: *нарушается микровязкость (↑) *образуются “мега” поры *растет проницаемость мембран → набухание *изменяется ионная проницаемость (разрушение ионных каналов и ионных насосов, например, Nа, КАТФазы)
 *
*
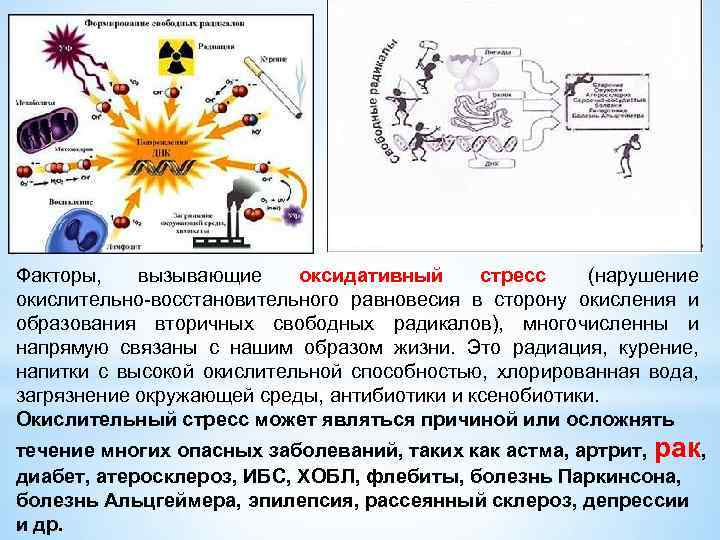 Факторы, вызывающие оксидативный стресс (нарушение окислительно-восстановительного равновесия в сторону окисления и образования вторичных свободных радикалов), многочисленны и напрямую связаны с нашим образом жизни. Это радиация, курение, напитки с высокой окислительной способностью, хлорированная вода, загрязнение окружающей среды, антибиотики и ксенобиотики. Окислительный стресс может являться причиной или осложнять течение многих опасных заболеваний, таких как астма, артрит, рак, диабет, атеросклероз, ИБС, ХОБЛ, флебиты, болезнь Паркинсона, болезнь Альцгеймера, эпилепсия, рассеянный склероз, депрессии и др.
Факторы, вызывающие оксидативный стресс (нарушение окислительно-восстановительного равновесия в сторону окисления и образования вторичных свободных радикалов), многочисленны и напрямую связаны с нашим образом жизни. Это радиация, курение, напитки с высокой окислительной способностью, хлорированная вода, загрязнение окружающей среды, антибиотики и ксенобиотики. Окислительный стресс может являться причиной или осложнять течение многих опасных заболеваний, таких как астма, артрит, рак, диабет, атеросклероз, ИБС, ХОБЛ, флебиты, болезнь Паркинсона, болезнь Альцгеймера, эпилепсия, рассеянный склероз, депрессии и др.
 В настоящее время установлено, что АФК могут играть существенную роль на всех этапах канцерогенеза: инициации, промоции и прогрессии, а также что хронический окислительный стресс может приводить к злокачественной трансформации [Эмануэль Н. М. , Саприн А. Н. ]. Число данных в пользу свободнорадикальной теории рака увеличивается, поэтому она получила широкое признание и актуальна на сегодняшний день.
В настоящее время установлено, что АФК могут играть существенную роль на всех этапах канцерогенеза: инициации, промоции и прогрессии, а также что хронический окислительный стресс может приводить к злокачественной трансформации [Эмануэль Н. М. , Саприн А. Н. ]. Число данных в пользу свободнорадикальной теории рака увеличивается, поэтому она получила широкое признание и актуальна на сегодняшний день.
 Одним из наиболее значительных ограничений эффективности химиотерапии рака является развитие множественной лекарственной устойчивости. Среди хорошо известных факторов, вызывающих развитие множественной лекарственной устойчивости, включая повышенную экспрессию трансмембранных транспортеров (Р-гп, MRP, LRP, BCRP), повышение уровня системы детоксикации, в значительной степени связанной с ростом экспрессии глутатион-Sтрансфераз, снижение экспрессии и активности топоизомеразы II, изменение экспрессии генов, блокирующее развитие апоптоза, остаются малоизученными свободнорадикальные механизмы.
Одним из наиболее значительных ограничений эффективности химиотерапии рака является развитие множественной лекарственной устойчивости. Среди хорошо известных факторов, вызывающих развитие множественной лекарственной устойчивости, включая повышенную экспрессию трансмембранных транспортеров (Р-гп, MRP, LRP, BCRP), повышение уровня системы детоксикации, в значительной степени связанной с ростом экспрессии глутатион-Sтрансфераз, снижение экспрессии и активности топоизомеразы II, изменение экспрессии генов, блокирующее развитие апоптоза, остаются малоизученными свободнорадикальные механизмы.
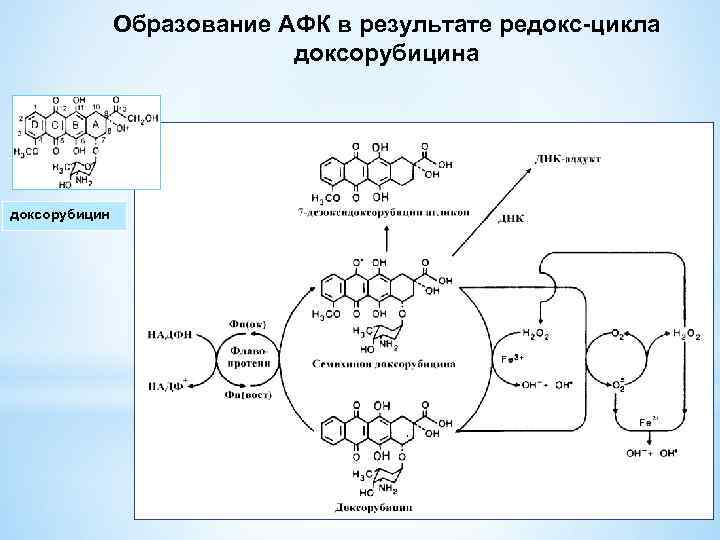 Образование АФК в результате редокс-цикла доксорубицина доксорубицин
Образование АФК в результате редокс-цикла доксорубицина доксорубицин
 Цитотоксический эффект противоопухолевого препарата доксорубицина (DOX) в значительной степени связан с прооксидантным действием, обусловленным наличием хинона в его структуре. При действии ряда флавопротеинов, в том числе NADPH-цитохром Р-450 -редуктазы, NADHдегидрогеназы, ксантиноксидазы, катализирующих одноэлектронное восстановление, происходит образование свободнорадикальной семихинонной формы DOX, легко способной к рециклу в присутствии молекулярного кислорода с образованием супероксид-аниона и последующего каскада генерации АФК, включая Н 2 О 2 и высокореакционноспособные. ОН радикалы, образование которых резко ускоряется в присутствии ионов Fe 2+
Цитотоксический эффект противоопухолевого препарата доксорубицина (DOX) в значительной степени связан с прооксидантным действием, обусловленным наличием хинона в его структуре. При действии ряда флавопротеинов, в том числе NADPH-цитохром Р-450 -редуктазы, NADHдегидрогеназы, ксантиноксидазы, катализирующих одноэлектронное восстановление, происходит образование свободнорадикальной семихинонной формы DOX, легко способной к рециклу в присутствии молекулярного кислорода с образованием супероксид-аниона и последующего каскада генерации АФК, включая Н 2 О 2 и высокореакционноспособные. ОН радикалы, образование которых резко ускоряется в присутствии ионов Fe 2+
 Установлено, что 1) формирование лекарственной устойчивости опухолевых клеток к DOX связано с редоксзависимым скоордининированным повышением экспрессии генов ключевых ферментов, контролирующих синтез GSH de novo.
Установлено, что 1) формирование лекарственной устойчивости опухолевых клеток к DOX связано с редоксзависимым скоордининированным повышением экспрессии генов ключевых ферментов, контролирующих синтез GSH de novo.
 2) формирование лекарственной устойчивости опухолевых клеток к DOX сопровождается ростом отношения содержания восстановленного GSH к уровню его окисленной формы GSSG (GSH/GSSG), что демонстрирует повышение клеточного редокс-статуса.
2) формирование лекарственной устойчивости опухолевых клеток к DOX сопровождается ростом отношения содержания восстановленного GSH к уровню его окисленной формы GSSG (GSH/GSSG), что демонстрирует повышение клеточного редокс-статуса.
 3) формирование лекарственной устойчивости опухолевых клеток к DOX сопровождается ростом экспрессии генов GSH-зависимых ферментов: глутатионтрансферазы, глутатионпероксидазы, глутаредоксина, что свидетельствует в пользу важной роли GSHзависимых процессов в редокс-механизме развития лекарственной резистентности.
3) формирование лекарственной устойчивости опухолевых клеток к DOX сопровождается ростом экспрессии генов GSH-зависимых ферментов: глутатионтрансферазы, глутатионпероксидазы, глутаредоксина, что свидетельствует в пользу важной роли GSHзависимых процессов в редокс-механизме развития лекарственной резистентности.
 4) формирование лекарственной устойчивости опухолевых клеток к DOX сопровождается повышением экспрессии генов тиоредоксина и пероксиредоксина, что способствует росту редокс-зависимых процессов восстановления дисульфидов и перекисей
4) формирование лекарственной устойчивости опухолевых клеток к DOX сопровождается повышением экспрессии генов тиоредоксина и пероксиредоксина, что способствует росту редокс-зависимых процессов восстановления дисульфидов и перекисей
 Рост внутриклеточного уровня глутатионтрансферазы Р 1 -1, Trx, Grx играет важную роль в регуляции клеточного сигналинга путем белок-белковых взаимодействий с ключевыми киназами, контролирующими развитие апоптоза – ASK 1 и JNK 1. Связываясь с ASK 1 и JNK 1 эти белки блокируют пути активации апоптоза. Поэтому рост экспрессии генов глутатионтрансферазы Р 1 -1, Trx, Grx в резистентных к DOX опухолевых клетках подавляют механизмы активации апоптотической гибели клеток.
Рост внутриклеточного уровня глутатионтрансферазы Р 1 -1, Trx, Grx играет важную роль в регуляции клеточного сигналинга путем белок-белковых взаимодействий с ключевыми киназами, контролирующими развитие апоптоза – ASK 1 и JNK 1. Связываясь с ASK 1 и JNK 1 эти белки блокируют пути активации апоптоза. Поэтому рост экспрессии генов глутатионтрансферазы Р 1 -1, Trx, Grx в резистентных к DOX опухолевых клетках подавляют механизмы активации апоптотической гибели клеток.
 5) формирование лекарственной устойчивости опухолевых клеток к DOX сопровождается редокс-зависимой активацией транскрипционного фактора Nrf 2, что приводит к скоординированному росту экспрессии генов ферментов, контролирующих синтез GSH de novo, GSH-зависимых ферментов (глутатионтрансферазы, глутатионпероксидазы, глутаредоксина), редокс-зависимых белков тиоредоксина, пероксиредоксина
5) формирование лекарственной устойчивости опухолевых клеток к DOX сопровождается редокс-зависимой активацией транскрипционного фактора Nrf 2, что приводит к скоординированному росту экспрессии генов ферментов, контролирующих синтез GSH de novo, GSH-зависимых ферментов (глутатионтрансферазы, глутатионпероксидазы, глутаредоксина), редокс-зависимых белков тиоредоксина, пероксиредоксина
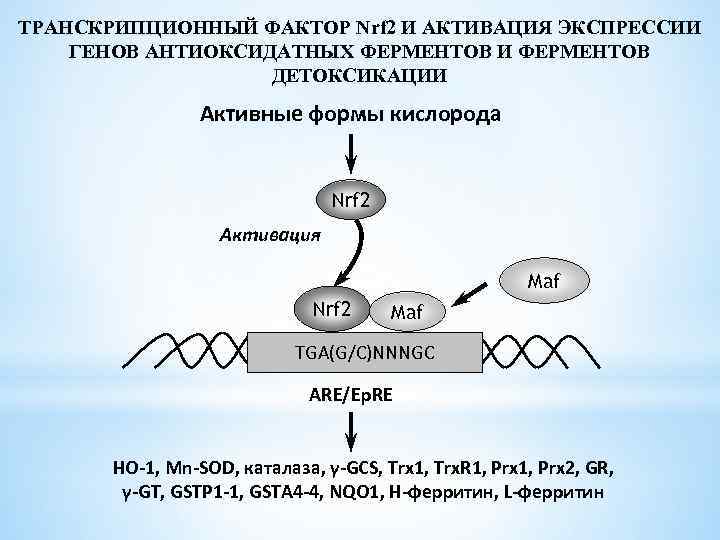 ТРАНСКРИПЦИОННЫЙ ФАКТОР Nrf 2 И АКТИВАЦИЯ ЭКСПРЕССИИ ГЕНОВ АНТИОКСИДАТНЫХ ФЕРМЕНТОВ И ФЕРМЕНТОВ ДЕТОКСИКАЦИИ Активные формы кислорода Nrf 2 Активация Maf Nrf 2 Maf TGA(G/C)NNNGC ARE/Ep. RE HO-1, Mn-SOD, каталаза, γ-GCS, Trx 1, Trx. R 1, Prx 2, GR, γ-GT, GSTP 1 -1, GSTA 4 -4, NQO 1, H-ферритин, L-ферритин
ТРАНСКРИПЦИОННЫЙ ФАКТОР Nrf 2 И АКТИВАЦИЯ ЭКСПРЕССИИ ГЕНОВ АНТИОКСИДАТНЫХ ФЕРМЕНТОВ И ФЕРМЕНТОВ ДЕТОКСИКАЦИИ Активные формы кислорода Nrf 2 Активация Maf Nrf 2 Maf TGA(G/C)NNNGC ARE/Ep. RE HO-1, Mn-SOD, каталаза, γ-GCS, Trx 1, Trx. R 1, Prx 2, GR, γ-GT, GSTP 1 -1, GSTA 4 -4, NQO 1, H-ферритин, L-ферритин
 Таким образом, развитие адаптивного антиоксидантного ответа на окислительный стресс, вызываемый доксорубицином является важным фактором формирования редокс-зависимой резистентности опухолевых клеток к противоопухолевому действию этого препарата. Развитие адаптивного антиоксидантного ответа доказывается скоординированным изменением экспрессии генов антиоксидантных ферментов, контролирующих синтез GSH de novo, GSH-зависимых ферментов (глутатионтрансферазы, глутатионпероксидазы, глутаредоксина), редоксзависимых белков тиоредоксина и пероксиредоксина
Таким образом, развитие адаптивного антиоксидантного ответа на окислительный стресс, вызываемый доксорубицином является важным фактором формирования редокс-зависимой резистентности опухолевых клеток к противоопухолевому действию этого препарата. Развитие адаптивного антиоксидантного ответа доказывается скоординированным изменением экспрессии генов антиоксидантных ферментов, контролирующих синтез GSH de novo, GSH-зависимых ферментов (глутатионтрансферазы, глутатионпероксидазы, глутаредоксина), редоксзависимых белков тиоредоксина и пероксиредоксина


