Актиноиды +нептуний-13.ppt
- Количество слайдов: 46
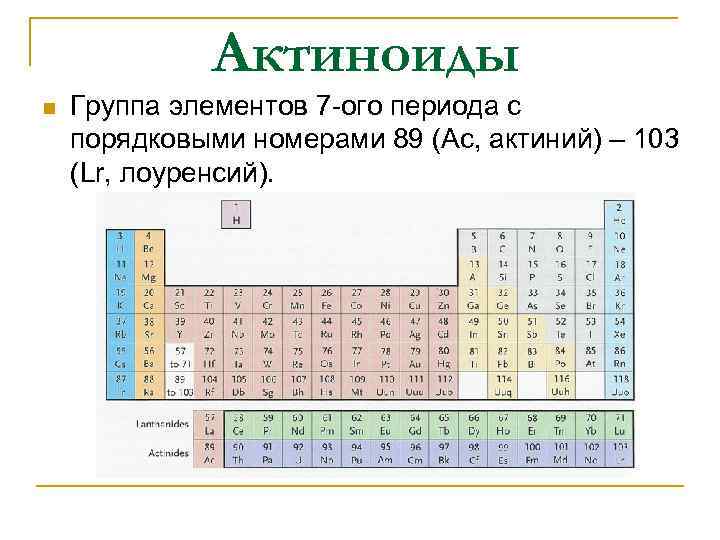 Актиноиды n Группа элементов 7 -ого периода с порядковыми номерами 89 (Ас, актиний) – 103 (Lr, лоуренсий).
Актиноиды n Группа элементов 7 -ого периода с порядковыми номерами 89 (Ас, актиний) – 103 (Lr, лоуренсий).
 Актиноиды n n n n Ac, Th, Pa – цисурановые элементы Np, Pu…. – трансурановые элементы После Pu – трансплутониевые (ТПЭ) После Cm – транскюриевые После Fm – трансфермиевые Np, Pu, Am – ураниды Сm – Lr – кюриды
Актиноиды n n n n Ac, Th, Pa – цисурановые элементы Np, Pu…. – трансурановые элементы После Pu – трансплутониевые (ТПЭ) После Cm – транскюриевые После Fm – трансфермиевые Np, Pu, Am – ураниды Сm – Lr – кюриды
 Актиноиды n n n U, Th – природные радиоактивные элементы Ac, Pa – продукты распада урана и тория Трансурановые элементы: 1. Облучение урана или другого актиноида нейтронами в ядерном реакторе. 2. Облучение урана или другого актиноида импульсным потоком нейтронов при термоядерном взрыве. (Открытие эйнштейния и фермия - результат исследований продуктов взрыва термоядерного устройства, произведенного США в Тихом океане в ноябре 1952 г. , операция "Майк"). 3. Облучение элементов 7 периода p, d, , 13 C, 18 O и т. д.
Актиноиды n n n U, Th – природные радиоактивные элементы Ac, Pa – продукты распада урана и тория Трансурановые элементы: 1. Облучение урана или другого актиноида нейтронами в ядерном реакторе. 2. Облучение урана или другого актиноида импульсным потоком нейтронов при термоядерном взрыве. (Открытие эйнштейния и фермия - результат исследований продуктов взрыва термоядерного устройства, произведенного США в Тихом океане в ноябре 1952 г. , операция "Майк"). 3. Облучение элементов 7 периода p, d, , 13 C, 18 O и т. д.
 Актиноиды n Первая попытка размещения 5 f-элементов – гипотеза М. Гайсинского (принцип аналогии химических свойств - неоднозначен) n Концепция А. А. Чайхорского (проявление степени окисления +4 у 9 из 13 актиноидов, родоначальник – торий) n Концепции В. Г. Григоровича (1963 г. ), И. А. Лебедева (1972 г. ): размещение f-элементов по группам
Актиноиды n Первая попытка размещения 5 f-элементов – гипотеза М. Гайсинского (принцип аналогии химических свойств - неоднозначен) n Концепция А. А. Чайхорского (проявление степени окисления +4 у 9 из 13 актиноидов, родоначальник – торий) n Концепции В. Г. Григоровича (1963 г. ), И. А. Лебедева (1972 г. ): размещение f-элементов по группам
 Актиноиды n Двойственность химического поведения легких актиноидов (торий-америций): аналоги соответствующих лантаноидов (4 f-элементов) и свойства d-элементов (3 d-серии). n Уменьшение разнообразия валентных форм у тяжелых актиноидов (энергия 5 f электронов меньше энергии 6 dподуровня): свойства лантаноидов. n Отсутствие полной химической аналогии между элементами 4 f и 5 f-семейств. n Актиноиды в высших степенях окисления (более 3) не имеют прямых химических аналогов.
Актиноиды n Двойственность химического поведения легких актиноидов (торий-америций): аналоги соответствующих лантаноидов (4 f-элементов) и свойства d-элементов (3 d-серии). n Уменьшение разнообразия валентных форм у тяжелых актиноидов (энергия 5 f электронов меньше энергии 6 dподуровня): свойства лантаноидов. n Отсутствие полной химической аналогии между элементами 4 f и 5 f-семейств. n Актиноиды в высших степенях окисления (более 3) не имеют прямых химических аналогов.
 Актиноиды n n Актиноидная гипотеза Г. Сиборга (1944 г. ) Элементы с порядковыми номерами 90 -103 образуют 5 fсемейство и по аналогии с лантаноидами размещаются в виде отдельной группы. Актиноиды – промежуточное положение между элементами f и dсерий. Энергии связи 5 f и 6 d-электронов очень близки.
Актиноиды n n Актиноидная гипотеза Г. Сиборга (1944 г. ) Элементы с порядковыми номерами 90 -103 образуют 5 fсемейство и по аналогии с лантаноидами размещаются в виде отдельной группы. Актиноиды – промежуточное положение между элементами f и dсерий. Энергии связи 5 f и 6 d-электронов очень близки.
 Степени окисления n n n n Ac – 3 Th – (3), 4 Pa – 4, 5 U – 3, 4, 5, 6 Np – 3, 4, 5, 6, 7 Pu – 3, 4, 5, 6, 7 Am – 2, 3, (4), 5, 6, 7 n n n n Cm – 3, 4 Bk – 3, 4 Cf – 2, 3, 4 Es – 2, 3 Fm – 2, 3 Md – 1, 2, 3 No – 2, 3 Lr - 3
Степени окисления n n n n Ac – 3 Th – (3), 4 Pa – 4, 5 U – 3, 4, 5, 6 Np – 3, 4, 5, 6, 7 Pu – 3, 4, 5, 6, 7 Am – 2, 3, (4), 5, 6, 7 n n n n Cm – 3, 4 Bk – 3, 4 Cf – 2, 3, 4 Es – 2, 3 Fm – 2, 3 Md – 1, 2, 3 No – 2, 3 Lr - 3
 Общие свойства n n Активные металлы, легко вступающие в реакции практически со всеми химическими элементами. Растворимы в разбавленных минеральных кислотах, в концентрированных HNO 3 и H 2 SO 4 – пассивируются. Оксиды обладают полиморфизмом, более высоких, чем +4 степеней окисления – малоустойчивы (исключение оксиды урана и Pa 2 O 5). Гидриды при повышении температуры выше 300 С разлагаются с выделением металлов в виде пирофорных порошков.
Общие свойства n n Активные металлы, легко вступающие в реакции практически со всеми химическими элементами. Растворимы в разбавленных минеральных кислотах, в концентрированных HNO 3 и H 2 SO 4 – пассивируются. Оксиды обладают полиморфизмом, более высоких, чем +4 степеней окисления – малоустойчивы (исключение оксиды урана и Pa 2 O 5). Гидриды при повышении температуры выше 300 С разлагаются с выделением металлов в виде пирофорных порошков.
 Общие свойства n n n Стабильность галогенидов падает с ростом атомного номера галогена и числа атомов галогена в соединении. Трифториды и тетрафориды не растворимы в воде, хлориды, бромиды и иодиды – растворимы. Карбиды Me. C легко гидролизуются водой с образованием углеводородов, мелкоизмельченные пирофорны. Me 2 C 3 и Me. C 2 более устойчивы. Мононитриды: нагревание металлов или карбидов в токе азота или аммиака. Силициды: взаимодействие металлов с кремнием при высоких температурах. Соляная кислота разлагает до Si. H 4.
Общие свойства n n n Стабильность галогенидов падает с ростом атомного номера галогена и числа атомов галогена в соединении. Трифториды и тетрафориды не растворимы в воде, хлориды, бромиды и иодиды – растворимы. Карбиды Me. C легко гидролизуются водой с образованием углеводородов, мелкоизмельченные пирофорны. Me 2 C 3 и Me. C 2 более устойчивы. Мононитриды: нагревание металлов или карбидов в токе азота или аммиака. Силициды: взаимодействие металлов с кремнием при высоких температурах. Соляная кислота разлагает до Si. H 4.
 Актиноиды в растворах n Гидратированные ионы Me 2+, Me 3+, Me 4+ Me. O 22+( «ил» ), Me. O 2+( «оил» ), Me. O 53 - Диспропорционирование 2 Me. O 2+ +4 Н+ Me. O 22+ + Me 4+ n Гидролиз, Комплексообразование: Me 4+ > Me 3+>Me. O 22+>Me. O 2+ Для оксалат и ацетат-ионов: Me 4+ > Me. O 22+ > Me 3+ >Me. O 2+ n n n Полимеризация с образованием полиядерных продуктов гидролиза Координационное число 6 -12.
Актиноиды в растворах n Гидратированные ионы Me 2+, Me 3+, Me 4+ Me. O 22+( «ил» ), Me. O 2+( «оил» ), Me. O 53 - Диспропорционирование 2 Me. O 2+ +4 Н+ Me. O 22+ + Me 4+ n Гидролиз, Комплексообразование: Me 4+ > Me 3+>Me. O 22+>Me. O 2+ Для оксалат и ацетат-ионов: Me 4+ > Me. O 22+ > Me 3+ >Me. O 2+ n n n Полимеризация с образованием полиядерных продуктов гидролиза Координационное число 6 -12.
 Химия нептуния Ядерные свойства и получение q Химические свойства q Нептуний в растворах q Аналитическая химия: методы очистки, выделения и идентификации q
Химия нептуния Ядерные свойства и получение q Химические свойства q Нептуний в растворах q Аналитическая химия: методы очистки, выделения и идентификации q
 Почему нептуний?
Почему нептуний?
 Ядерные свойства Открыт в 1940 г. Мак-Милланом и Эйблсоном. 22 изотопа 237 Np – наиболее долгоживущий Производство 238 Pu : облучение нейтронами Производство 236 Pu: 23 Me. V и 30 Me. V электроны 238, 239 Np - малые периоды полураспада Важные радиотрассеры
Ядерные свойства Открыт в 1940 г. Мак-Милланом и Эйблсоном. 22 изотопа 237 Np – наиболее долгоживущий Производство 238 Pu : облучение нейтронами Производство 236 Pu: 23 Me. V и 30 Me. V электроны 238, 239 Np - малые периоды полураспада Важные радиотрассеры
 Получение В земной коре содержится в следовых количествах, поэтому природные источники не имеют практического значения. 237 Np 238 U(n, 2 n)237 U 237 Np + - Альфа-распад 241 Am 238, 239 Np Облучение нейтронами 237 Np и 238 U(n, )239 U 239 Np + 235, 236 Np Облучение 235 U на циклотроне 235 U(d, n)236 Np q 235 U(p, n)235 Np q
Получение В земной коре содержится в следовых количествах, поэтому природные источники не имеют практического значения. 237 Np 238 U(n, 2 n)237 U 237 Np + - Альфа-распад 241 Am 238, 239 Np Облучение нейтронами 237 Np и 238 U(n, )239 U 239 Np + 235, 236 Np Облучение 235 U на циклотроне 235 U(d, n)236 Np q 235 U(p, n)235 Np q
 Химические свойства Металл n n n Строение электронной оболочки 5 s 25 p 65 d 105 f 46 p 66 d 17 s 2 Первый синтез из Np. F 3 восстановлением Ba при 1473 K Современные методы q q Np. F 4 с избытком Ca Np. O 2 (расплав солей) n n q q Может использоваться Cs 2 Np. O 2 Cl 4 и Cs 3 Np. O 2 Cl 4 Li. Cl/KCl как электролит при 723 K Np. C восстановление Ta Электроосаждение из водных растворов n n Aмальгамирование с Hg из 1 M CH 3 COOH и 0. 3 M CH 3 COONa при p. H 3. 5 Удаление Hg
Химические свойства Металл n n n Строение электронной оболочки 5 s 25 p 65 d 105 f 46 p 66 d 17 s 2 Первый синтез из Np. F 3 восстановлением Ba при 1473 K Современные методы q q Np. F 4 с избытком Ca Np. O 2 (расплав солей) n n q q Может использоваться Cs 2 Np. O 2 Cl 4 и Cs 3 Np. O 2 Cl 4 Li. Cl/KCl как электролит при 723 K Np. C восстановление Ta Электроосаждение из водных растворов n n Aмальгамирование с Hg из 1 M CH 3 COOH и 0. 3 M CH 3 COONa при p. H 3. 5 Удаление Hg
 Металл n n Температура плавления 912 K Три аллотропные модификации § Активный металл § Быстро окисляется, на воздухе устойчив благодаря оксидной пленке § Мелкораздробленный нептуний пирофорен
Металл n n Температура плавления 912 K Три аллотропные модификации § Активный металл § Быстро окисляется, на воздухе устойчив благодаря оксидной пленке § Мелкораздробленный нептуний пирофорен
 Интерметаллические соединения n Соединения q RM 2 X 2 n q RM 2 Al 3 n q R=Np или Pu; M= Ni или Pd Np. X 3 n n R=Th, Np или Pu, M – переходный металл, X = Si, Ge X=Al, Ga, Ge, In, или Sn Сплавы q Zr с Np и др. актинидами
Интерметаллические соединения n Соединения q RM 2 X 2 n q RM 2 Al 3 n q R=Np или Pu; M= Ni или Pd Np. X 3 n n R=Th, Np или Pu, M – переходный металл, X = Si, Ge X=Al, Ga, Ge, In, или Sn Сплавы q Zr с Np и др. актинидами
 Гидриды n Np с H 2 q Np. H 2+x и Np. H 3 n Изоморфны соединениям Pu n Промежуточное положение между солеподобными гидридами типа твердых растворов H в металле. n Np : H q Увеличение H с увеличением температуры Теплота образования при 298 K составляет 47. 279 Дж K-1 моль-1
Гидриды n Np с H 2 q Np. H 2+x и Np. H 3 n Изоморфны соединениям Pu n Промежуточное положение между солеподобными гидридами типа твердых растворов H в металле. n Np : H q Увеличение H с увеличением температуры Теплота образования при 298 K составляет 47. 279 Дж K-1 моль-1
 Оксиды n n n Два известных оксида q Np 2 O 5 и Np. O 2 q Термическое разложение различных соединений q Изоморфен соединениям других актинидов q Кристаллическая решетка типа флюорита q Стабилен в широком интервале температур q Фазовый переход n Стабилен до 2. 84 MПа и 673 K Np 2 O 5 q Термическое разложение Np. O 2(ОH)2 или Np. O 2(OH) q Разлагается до Np. O 2 в интервале 693 - 970 K
Оксиды n n n Два известных оксида q Np 2 O 5 и Np. O 2 q Термическое разложение различных соединений q Изоморфен соединениям других актинидов q Кристаллическая решетка типа флюорита q Стабилен в широком интервале температур q Фазовый переход n Стабилен до 2. 84 MПа и 673 K Np 2 O 5 q Термическое разложение Np. O 2(ОH)2 или Np. O 2(OH) q Разлагается до Np. O 2 в интервале 693 - 970 K
 n Np(IV) q q n Амфотерный, Np. O 2(OH) Np(VI) q q n Основный При действии щелочей на соединения Np(IV) в растворе Np(V) q n Гидроксиды Амфотерный, Np. O 2(OH)2 Окисление Np(V) в расплаве Li. NO 3/KNO 3 с O 3 Np(VII) q q Np. O 2(OH)3 или Np. O 3(OH)? Озонирование суспензии гидроксида Np(V)
n Np(IV) q q n Амфотерный, Np. O 2(OH) Np(VI) q q n Основный При действии щелочей на соединения Np(IV) в растворе Np(V) q n Гидроксиды Амфотерный, Np. O 2(OH)2 Окисление Np(V) в расплаве Li. NO 3/KNO 3 с O 3 Np(VII) q q Np. O 2(OH)3 или Np. O 3(OH)? Озонирование суспензии гидроксида Np(V)
 Двойные и тройные оксиды n n Реакции Np. O 2 с оксидами металлов или осаждение из щелочных растворов Np(V) q Li и Na соединения q Нагрев Np(VI) Li и Na оксидов в Ar с Np. O 2 Np(VI) q Из Np. O 2 и оксидов металлов в O 2 q Изоморфны соединениям урана Np(VII) q Широкий спектр n XNp. O 6 q n XNp. O 5 q n X=Rb 3, K 3, Cs 3 XNp. O 4 q q X=Li 5, Ba 2 Li X=Cs, Rb, K Некоторые соединения содержат Np(VI) и Np(VII)
Двойные и тройные оксиды n n Реакции Np. O 2 с оксидами металлов или осаждение из щелочных растворов Np(V) q Li и Na соединения q Нагрев Np(VI) Li и Na оксидов в Ar с Np. O 2 Np(VI) q Из Np. O 2 и оксидов металлов в O 2 q Изоморфны соединениям урана Np(VII) q Широкий спектр n XNp. O 6 q n XNp. O 5 q n X=Rb 3, K 3, Cs 3 XNp. O 4 q q X=Li 5, Ba 2 Li X=Cs, Rb, K Некоторые соединения содержат Np(VI) и Np(VII)
 n Фториды q q Np. F 3, Np. F 4, Np. F 5, и Np. F 6 Реакции с HF при 773 K n n q Галогениды Np. O 2+1/2 H 2+3 HF Np. F 3 + 2 H 2 O Np. F 3+1/4 O 2+HF Np. F 4 + 1/2 H 2 O Np. O 2+4 HF Np. F 4 + 2 H 2 O 10 Np. F 6+I 2 10 Np. F 5+2 IF 5 q Другие способы Np. F 6 летуч n n Сходен с UF 6 и Pu. F 6 Способен образовывать соединения Np(V) при взаимодействии с Na. F q Np. F 6+3 Na. F Na 3 Np. F 8 + 1/2 F 2 § U будет оставаться в 6 -валентном состоянии Синтез аналогичен синтезу гексафторида урана Kr. F 2 как фторирующий агент в некоторых схемах синтеза
n Фториды q q Np. F 3, Np. F 4, Np. F 5, и Np. F 6 Реакции с HF при 773 K n n q Галогениды Np. O 2+1/2 H 2+3 HF Np. F 3 + 2 H 2 O Np. F 3+1/4 O 2+HF Np. F 4 + 1/2 H 2 O Np. O 2+4 HF Np. F 4 + 2 H 2 O 10 Np. F 6+I 2 10 Np. F 5+2 IF 5 q Другие способы Np. F 6 летуч n n Сходен с UF 6 и Pu. F 6 Способен образовывать соединения Np(V) при взаимодействии с Na. F q Np. F 6+3 Na. F Na 3 Np. F 8 + 1/2 F 2 § U будет оставаться в 6 -валентном состоянии Синтез аналогичен синтезу гексафторида урана Kr. F 2 как фторирующий агент в некоторых схемах синтеза
 Галогениды n Oксифториды q Оксиды с HF при повышенных температурах или фториды Np с H 2 O q Соединения мало изучены n Np. O 2 F, Np. OF 3, Np. O 2 F 2, Np. OF 4 § Хлориды Np. Cl 4 Получение: Np. O 2 с CCl 4 q Добавление H 2 - Np. Cl 3 q Оба растворимы в воде q Np. Cl 4 подвергается гидролизу с образованием Np. OCl 2 q
Галогениды n Oксифториды q Оксиды с HF при повышенных температурах или фториды Np с H 2 O q Соединения мало изучены n Np. O 2 F, Np. OF 3, Np. O 2 F 2, Np. OF 4 § Хлориды Np. Cl 4 Получение: Np. O 2 с CCl 4 q Добавление H 2 - Np. Cl 3 q Оба растворимы в воде q Np. Cl 4 подвергается гидролизу с образованием Np. OCl 2 q
 Галогениды n Бромиды, иодиды Np. Br 4 q Np. O 2 с Al. Br 3 Np. Br 3 q Np. O 2 с Al. Br 3 и Al Np. I 3 q Аналогично Np. Br 3
Галогениды n Бромиды, иодиды Np. Br 4 q Np. O 2 с Al. Br 3 Np. Br 3 q Np. O 2 с Al. Br 3 и Al Np. I 3 q Аналогично Np. Br 3
 Другие соединения n Сульфиды и оксисульфиды q q n Нитриды q n Np. S, Np. S 3, Np 2 S 5, Np 3 S 5, Np 2 S 3, Np 3 S 4 q Np. S § Np и S § Изоморфен U и Pu Np. OS, Np 4 O 4 S Np. N n NH 3 и Np. H 3 n Np со смесью N 2 и H 2 n Восстановление Np. O 2 в N 2 n Аналогичен UN and Pu. N q Растворим в кислотах, относительно инертен в воде Карбиды q Np. C, Np 2 C 3 и Np. C 2
Другие соединения n Сульфиды и оксисульфиды q q n Нитриды q n Np. S, Np. S 3, Np 2 S 5, Np 3 S 5, Np 2 S 3, Np 3 S 4 q Np. S § Np и S § Изоморфен U и Pu Np. OS, Np 4 O 4 S Np. N n NH 3 и Np. H 3 n Np со смесью N 2 и H 2 n Восстановление Np. O 2 в N 2 n Аналогичен UN and Pu. N q Растворим в кислотах, относительно инертен в воде Карбиды q Np. C, Np 2 C 3 и Np. C 2
 Металлорганические соединения n Наиболее изучены циклопентадиенильные производные Np 4+ CP q Np. Cl 4+4 KC 5 H 5 Np(C 5 H 5)4+4 KCl n Растворяется в бензоле и тетрагидрофуране Циклооктатетраены q Np. Cl 4 + 2 K 2(C 8 H 8) Np(C 8 H 8)2+4 KCl § Осаждается при добавлении воды
Металлорганические соединения n Наиболее изучены циклопентадиенильные производные Np 4+ CP q Np. Cl 4+4 KC 5 H 5 Np(C 5 H 5)4+4 KCl n Растворяется в бензоле и тетрагидрофуране Циклооктатетраены q Np. Cl 4 + 2 K 2(C 8 H 8) Np(C 8 H 8)2+4 KCl § Осаждается при добавлении воды
 Нептуний в растворах
Нептуний в растворах
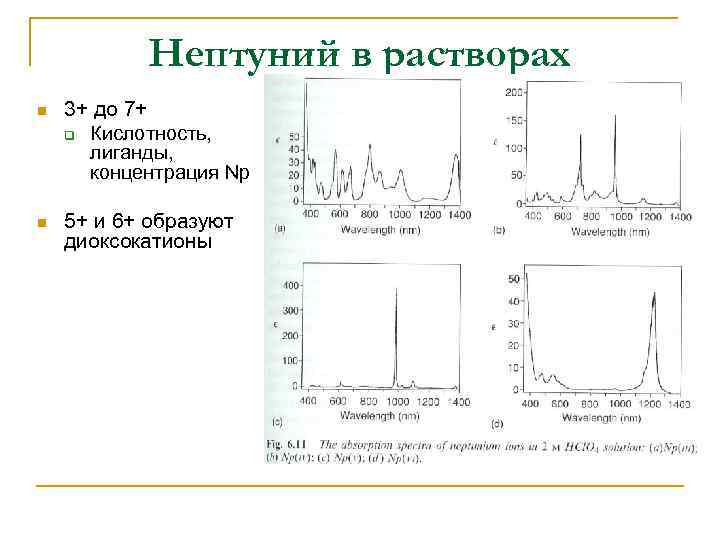 Нептуний в растворах n 3+ до 7+ q Кислотность, лиганды, концентрация Np n 5+ и 6+ образуют диоксокатионы
Нептуний в растворах n 3+ до 7+ q Кислотность, лиганды, концентрация Np n 5+ и 6+ образуют диоксокатионы
 Нептуний в растворах
Нептуний в растворах
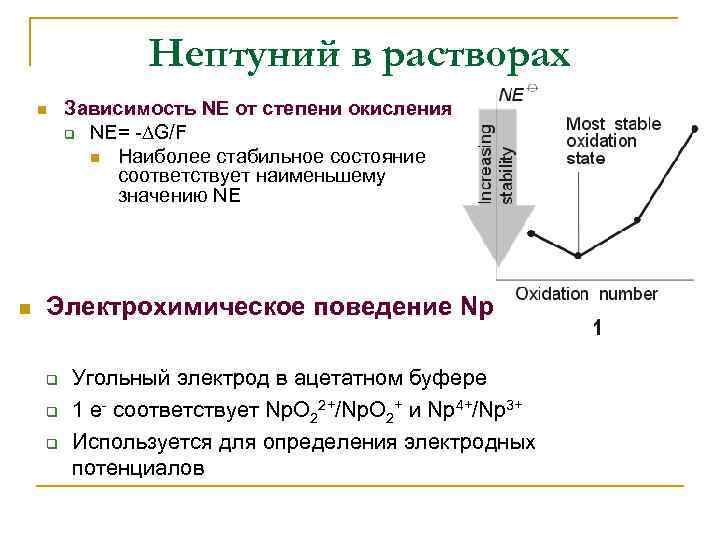 Нептуний в растворах n n Зависимость NE от степени окисления q NE= -∆G/F n Наиболее стабильное состояние соответствует наименьшему значению NE Электрохимическое поведение Np q q q Угольный электрод в ацетатном буфере 1 e- соответствует Np. O 22+/Np. O 2+ и Np 4+/Np 3+ Используется для определения электродных потенциалов
Нептуний в растворах n n Зависимость NE от степени окисления q NE= -∆G/F n Наиболее стабильное состояние соответствует наименьшему значению NE Электрохимическое поведение Np q q q Угольный электрод в ацетатном буфере 1 e- соответствует Np. O 22+/Np. O 2+ и Np 4+/Np 3+ Используется для определения электродных потенциалов
 Нептуний в растворах n Диспропорционирование q q q Np. O 2+ - Np 4+ и Np. O 22+ n Высокая кислотность и концентрация Np 2 Np. O 2+ +4 H+ Np 4+ + Np. O 22+ + 2 H 2 O Kонстанта реакции увеличивается при добавлении комплексообразователей
Нептуний в растворах n Диспропорционирование q q q Np. O 2+ - Np 4+ и Np. O 22+ n Высокая кислотность и концентрация Np 2 Np. O 2+ +4 H+ Np 4+ + Np. O 22+ + 2 H 2 O Kонстанта реакции увеличивается при добавлении комплексообразователей
 Нептуний в растворах n Гидролиз q n n n Np(IV) > Np(VI) > Np(III) > Np(V) Np(III) q Стабильный в кислых растворах (ниже p. H 4), окисляется на воздухе Np(IV) q Гидролизуется выше p. H 1 Np(V) q Не гидролизуется ниже p. H 7 Np(VI) q Ниже p. H 3 -4 Np(VII) q Мало изучен
Нептуний в растворах n Гидролиз q n n n Np(IV) > Np(VI) > Np(III) > Np(V) Np(III) q Стабильный в кислых растворах (ниже p. H 4), окисляется на воздухе Np(IV) q Гидролизуется выше p. H 1 Np(V) q Не гидролизуется ниже p. H 7 Np(VI) q Ниже p. H 3 -4 Np(VII) q Мало изучен
![[m. M] p. H [m. M] p. H](https://present5.com/presentation/3/87069140_171491063.pdf-img/87069140_171491063.pdf-33.jpg) [m. M] p. H
[m. M] p. H
 Нептуний в растворах n Комплексообразование q Np(IV) > Np(VI) > Np(III) > Np(V) q q n F-> H 2 PO 4 - > SCN- > NO 3 - > Cl. O 4 CO 32 - > HPO 42 - > SO 42 - Np. O 2+ образует комплексы «катион» Fe > In > Sc > Ga > Al
Нептуний в растворах n Комплексообразование q Np(IV) > Np(VI) > Np(III) > Np(V) q q n F-> H 2 PO 4 - > SCN- > NO 3 - > Cl. O 4 CO 32 - > HPO 42 - > SO 42 - Np. O 2+ образует комплексы «катион» Fe > In > Sc > Ga > Al
 Органические комплексы n n В основном для Np(V) Спектроскопия q Монокарбоксильные кислоты n n q 1: 3 Np: L Константы комплексобразования увеличиваются с увеличением p. Ka лиганда Ароматические поликарбоксилаты n Устойчивость зависит от числа карбоксильных групп
Органические комплексы n n В основном для Np(V) Спектроскопия q Монокарбоксильные кислоты n n q 1: 3 Np: L Константы комплексобразования увеличиваются с увеличением p. Ka лиганда Ароматические поликарбоксилаты n Устойчивость зависит от числа карбоксильных групп
 Методы определения n Содержание в окружающей среде q Отношение содержания нептуния к содержанию урана в урановых рудах – 1, 8*10 -12 q Общие уровни - 1 E-15 г/л n Радиометрические методы q Aльфа-спектрометрия n Определение в морской воде q q q Соосаждение, ионный обмен, La. F 3, экстракция Сцинтилляционный метод Активационный анализ n Образование 238 Np q q 170 барн, 2. 117 дня - период полураспада 238 Np В 500 раз более чувствительный, чем альфа-спектрометрия
Методы определения n Содержание в окружающей среде q Отношение содержания нептуния к содержанию урана в урановых рудах – 1, 8*10 -12 q Общие уровни - 1 E-15 г/л n Радиометрические методы q Aльфа-спектрометрия n Определение в морской воде q q q Соосаждение, ионный обмен, La. F 3, экстракция Сцинтилляционный метод Активационный анализ n Образование 238 Np q q 170 барн, 2. 117 дня - период полураспада 238 Np В 500 раз более чувствительный, чем альфа-спектрометрия
 Методы определения Спектрофотометрия n Пределы обнаружения q Np(III) 5 E-4, Np(IV) 1 E-4, Np(V) 5 E-5, Np(VI) 5 E-4 n Лазерно-индуцированная фотоакустическая спектроскопия (Laser induced photoacoustic spectroscopy, LIPAS) Флюоресценция n Тетрахлориды n 651 нм и 663 нм от Np Ренгенофлюоресцентный метод Масс-спектрометрия
Методы определения Спектрофотометрия n Пределы обнаружения q Np(III) 5 E-4, Np(IV) 1 E-4, Np(V) 5 E-5, Np(VI) 5 E-4 n Лазерно-индуцированная фотоакустическая спектроскопия (Laser induced photoacoustic spectroscopy, LIPAS) Флюоресценция n Тетрахлориды n 651 нм и 663 нм от Np Ренгенофлюоресцентный метод Масс-спектрометрия
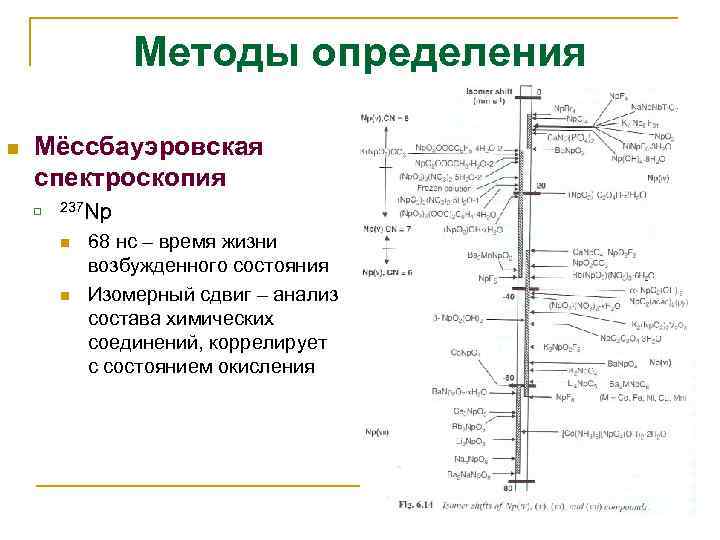 Методы определения n Мëссбауэровская спектроскопия q 237 Np n n 68 нс – время жизни возбужденного состояния Изомерный сдвиг – анализ состава химических соединений, коррелирует с состоянием окисления
Методы определения n Мëссбауэровская спектроскопия q 237 Np n n 68 нс – время жизни возбужденного состояния Изомерный сдвиг – анализ состава химических соединений, коррелирует с состоянием окисления
 n n Методы разделения Большинство методов основано на восстановительной химии Np Экстракция q 2 -теноилтрифторацетон (ТТА) n Восстановление до Np(IV) q q q Производные пиразолона n n n q Экстракция из 0. 5 M HNO 3 Реэкстракция в 8 M HNO 3 Np(IV) экстрагируется из 1 - 4 M HNO 3 Предотвращение гидролиза Np(IV) Не экстрагируются Np(V) и Np(VI) Экстракция смесью производных пиразолона и три-(ноктил) фосфин oксида (ТОФО) n Отделение Np(V) от Am, Cm, U(VI), Pu(IV) и лантанидов
n n Методы разделения Большинство методов основано на восстановительной химии Np Экстракция q 2 -теноилтрифторацетон (ТТА) n Восстановление до Np(IV) q q q Производные пиразолона n n n q Экстракция из 0. 5 M HNO 3 Реэкстракция в 8 M HNO 3 Np(IV) экстрагируется из 1 - 4 M HNO 3 Предотвращение гидролиза Np(IV) Не экстрагируются Np(V) и Np(VI) Экстракция смесью производных пиразолона и три-(ноктил) фосфин oксида (ТОФО) n Отделение Np(V) от Am, Cm, U(VI), Pu(IV) и лантанидов
 Методы разделения n Трибутилфосфат q Экстрагируемые соединения - Np. O 2(NO 3)2(TBP)2 и Np(NO 3)4(TBP)2 q Экстракция увеличивается при увеличении концентрации ТБФ и азотной кислоты q 1 -10 M HNO 3 n Степень очистки от других актинидов – контроль степени окисления нептуния
Методы разделения n Трибутилфосфат q Экстрагируемые соединения - Np. O 2(NO 3)2(TBP)2 и Np(NO 3)4(TBP)2 q Экстракция увеличивается при увеличении концентрации ТБФ и азотной кислоты q 1 -10 M HNO 3 n Степень очистки от других актинидов – контроль степени окисления нептуния
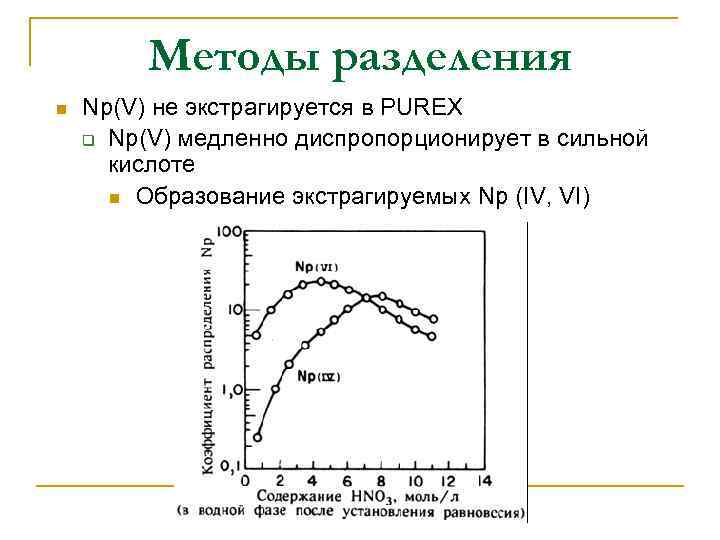 Методы разделения n Np(V) не экстрагируется в PUREX q Np(V) медленно диспропорционирует в сильной кислоте n Образование экстрагируемых Np (IV, VI)
Методы разделения n Np(V) не экстрагируется в PUREX q Np(V) медленно диспропорционирует в сильной кислоте n Образование экстрагируемых Np (IV, VI)
 Методы разделения n Реэкстракция Np(V) используется для отделения от Pu и U q Контролируемое восстановление Np(VI) в присутствии Pu(III) § Производные гидразина § N-бутиральдегид § Гидроксамовые кислоты (N-ацилгидроксиламины)
Методы разделения n Реэкстракция Np(V) используется для отделения от Pu и U q Контролируемое восстановление Np(VI) в присутствии Pu(III) § Производные гидразина § N-бутиральдегид § Гидроксамовые кислоты (N-ацилгидроксиламины)
 Методы разделения n Дифенил-N, N-дибутил карбамоил фосфин оксид (CMPO) q Обычно используется вместе с TБФ q Растворы азотной кислоты q Восстановление Pu и Np – сульфамат Fe(II) n n Np(IV) экстрагируется в органическую фазу Карбонаты, оксалаты или ЭДТА CMPO
Методы разделения n Дифенил-N, N-дибутил карбамоил фосфин оксид (CMPO) q Обычно используется вместе с TБФ q Растворы азотной кислоты q Восстановление Pu и Np – сульфамат Fe(II) n n Np(IV) экстрагируется в органическую фазу Карбонаты, оксалаты или ЭДТА CMPO
 Методы разделения n Ди(2 -этилгексил)фосфорная кислота (Д 2 ЭГФК) q В 1 M HNO 3 с добавлением Na. NO 2 n n n U, Pu, Np, Am Np(V) не экстрагируется Окисление до Np(VI) с последующей экстракцией Восстановление до Np(V), реэкстракция в 0. 1 M HNO 3 Три-n-октиламин (ТОА) q Выделение Np из объектов окружающей среды n n Экстракция из 10 M HCl Реэкстракция 1 M HCl+0. 1 M HF
Методы разделения n Ди(2 -этилгексил)фосфорная кислота (Д 2 ЭГФК) q В 1 M HNO 3 с добавлением Na. NO 2 n n n U, Pu, Np, Am Np(V) не экстрагируется Окисление до Np(VI) с последующей экстракцией Восстановление до Np(V), реэкстракция в 0. 1 M HNO 3 Три-n-октиламин (ТОА) q Выделение Np из объектов окружающей среды n n Экстракция из 10 M HCl Реэкстракция 1 M HCl+0. 1 M HF
 Методы разделения n Хроматография q Обычно используется для состояний окисления 4 -6 n q q q 4>6>5 Np 4+ и 6+ образуют анионные комплексы при высоких концентрациях хлорид- и нитрат-анионов Сорбция на анионите в 7 -8 M HNO 3 Элюент - 0. 3 M HNO 3
Методы разделения n Хроматография q Обычно используется для состояний окисления 4 -6 n q q q 4>6>5 Np 4+ и 6+ образуют анионные комплексы при высоких концентрациях хлорид- и нитрат-анионов Сорбция на анионите в 7 -8 M HNO 3 Элюент - 0. 3 M HNO 3
 Методы разделения n Соосаждение q Np соосаждается n q n La. F 3, Bi. PO 4, Ba. SO 4, Fe(OH)3, Mn. O 2 Np(V, VI) не соосаждается с La. F 3 Электроосаждение q На катоде в Li. Cl, KCl
Методы разделения n Соосаждение q Np соосаждается n q n La. F 3, Bi. PO 4, Ba. SO 4, Fe(OH)3, Mn. O 2 Np(V, VI) не соосаждается с La. F 3 Электроосаждение q На катоде в Li. Cl, KCl


