актиниды 1122.ppt
- Количество слайдов: 35

Актиниды Общая характеристика.

ПОЛУЧЕНИЕ АНТИНИДОВ Для получения актинидов в металлическом состоянии используют металлотермический способ, либо проводят электролиз расплава безводных галогенидов.

Получение актинидов Th. O₂+2 Ca= Th+2 Ca. O Ac. F₃+3 Lu=Ac+3 Lu. F 2 Am. F₃+2 Ba=2 Am+3 Ba. F₂ 3 Am. O₂+4 La=2 La. O₂+3 Am

ХИМИЧЕСКИЕ СОЕДИНЕНИЯ АКТИНИДОВ

Рассмотрим некоторые соединения актинидов на примере соединений Актиния

Актиний • На воздухе Актиний покрывается пленкой Ac₂O₃, которая предохраняет его от дальнейшего окисления, делая его похожим на лантан.

Оксид актиния Ac 2 O 3. Бесцветные гексагональные кристаллы c плотностью 9, 19 г/см 3. Основный характер выражен более ярко, чем у La 2 О 3. Получают прокаливанием в кислороде при 1100°С оксалата актиния. 2 Ac 2(C 2 O 4)3+3 O 2=2 Ac 2 O 3+ 12 CO₂ Оксалат актиния

Гидроксид актиния Ac(OH)3. Проявляет основные свойства. Не растворяется в воде. Получают в виде студнеобразного белого осадка при обработке растворов солянокислых или азотнокислых солей актиния аммиаком или щелочами. Как нерастворимое основание, разлагается:

Фторид актиния Ac. F 3. Бесцветные гексагональные кристаллы. tпл=1327°С , tкип=2277°С , плотность 7, 88 г/см 3. При нагревании до 800 о. С на воздухе переходит в оксифторид Ас. ОF. Получают действием плавиковой кислоты на гидроксид или растворы солей актиния. Ac(OH)₃+HF=Ac. F₃+H₂O

Хлорид актиния Ac. Cl 3. Бесцветные гексагональные кристаллы. tпл=927°С , tкип=1757° С, плотность 4, 81 г/см 3. При нагревании до 1000 о. С в токе аммиака переходит в оксихлорид Ac. OCl. Известен кристаллогидрат Ac. Cl 3. 7 Н 2 O.

Хлорид актиния Ac. Cl 3. Получают нагреванием при высокой температуре гидроксида или безводного оксалата актиния с CCl 4. 4 Ac(OH)₃+3 CCl₄=4 Ac. Cl₃+3 CO₂+6 H₂O

Бромид актиния Ac. Br 3. Бесцветные гексагональные кристаллы. tпл=827°С , tкип=1597°С, плотность 5, 85 г/см 3. Получают нагреванием оксида или оксалата актиния с бромидом алюминия при 750 о. C. Ac₂O₃+Al. Br₃=Ac. Br₃+Al₂O₃

Иодид актиния Ac. I 3. Белое вещество. tкип=1407°С. В парах аммиака гидролизуется с образованием оксииодида Ac. OI. Получают нагреванием оксида актиния с иодидом алюминия при 700 о. С или действием иодида аммония на оксалат актиния при 500 о. C. 2 Al. I₃+Ac₂O₃=2 Ac. I₃+Al₂O₃

Сульфид актиния Ac 2 S 3. Черные кубические кристаллы с плотностью 6, 75 г/см 3. Получают взаимодействием оксида или оксалата актиния при 1400 о. C в атмосфере смеси сероводорода и сероуглерода. Ac₂O₃+H₂S+CS₂=Ac₂S₃+H₂O+CO₂

Оксихлорид актиния Ac. OCl. Белые тетрагональные кристаллы с плотностью 7, 23 г/см 3. Получают при нагревании хлорида актиния до 1000 о. С в токе аммиака. Оксибромид актиния Ac. OBr. Белые тетрагональные кристаллы с плотностью 7, 89 г/см 3. Получают аналогично.

Ортофосфат актиния Ac. PO 4 ( 2 Ac. PO 4. H 2 O) Белые гексагональные кристаллы с плотностью 5, 48 г/см 3. Только при нагревании до 700 о. C превращается в безводную соль Ac. РО 4. Получают взаимодействием хлорида актиния с дигидроортофосфатом натрия. 2 Ac. Cl₃+2 Na. H₂PO₄+H₂O= 2 Ac. PO₄. H₂O+2 Na. Cl+4 HCl

Теперь рассмотрим подробнее важнейшие актиниды

Торий По распространенности в земной коре торий приближается к свинцу (0, 001 -0, 002%). Наиболее устойчивая С. О. +4. Из-за отсутствия электронов на 4 fорбиталях соединения тория не имеют окраски.

Торий обладает высокой химической активностью. Он хорошо реагирует с кислородом и водяным паром: Th+ ¹∕₂O₂+H₂O=Th. O₂+H₂ (нагрев) С хлором образует тетрахлорид: Th+2 Cl₂=Th. Cl₄

Th. O₂ Оксид тория это белый тугоплавкий порошок, хороший огнеупор, до сих пор используется в газовых лампах. Th. O₂ - очень инертный оксид, устойчив в щелочах и кислотах, в т. ч. расплавленных, переходит в раствор только под действием Царской водки или при сплавлении пероксидами активных металлов: Th. O₂+Na₂O₂=Na₂Th. O₃+ ¹⁄₂O₂↑(t)

И только недавно обнаружилось, что торий восстанавливается в слабокислой среде с помощью азидоводорода: 2 Th⁺⁴+2 HN₃=2 Th⁺³+N₂↑+2 H⁺

УРАН По виду уран сильно напоминает сталь, ковкий, поддается прокатке. Полиморфен. U – полный электронный аналог элементов 6 -й группы (W) но значительная разница в радиусах делает это сходство лишь формальным.

УРАН При повышенной температуре легко реагирует с водяным паром. U+2 H₂O=UO₂+2 H₂ Но считается, что первоначальный продукт такого взаимодействия – гидрид UH₃ затем реагирует с водой: 2 UH₃+4 H₂O=2 UO₂+7 H₂

Уран с галогенами Продукт р-ции галогенирования определяется природой галогена, соотношением реагентов и температуры: U+3 F₂→UF₆ (20°C) U+2 Br₂=UBr₄(700°C) 2 U+5 Br₂=2 UBr₅(50°C)

Уран легко растворим в азотной кислоте U+4 HNO₃=UO₂(NO₃)₂+2 NO↑+2 H₂O

Оксиды урана UO₂ получают восстановлением высшего оксида UO₃+CO=UO₂+CO₂ (350 °C)

Диоксид урана – типичный основный оксид: UO₂+2 H₂SO₄=U(SO₄)₂+2 H₂O

Оксид урана (6) UO₃ - желто-оранжевый порошок, при нагревании до 500 °C темнеет: 6 UO₃→ 2 U₃O₈+O₂ С водой дает гидроксид уранила: UO₃+H₂O=UO₂(OH)₂ Pазложение которого является способом получения UO₃

Растворением U₃O₈ в царской водке получают хлорид уранила: U₃O₈+18 HCl+2 HNO₃=9 UO₂Cl₂+10 H₂O
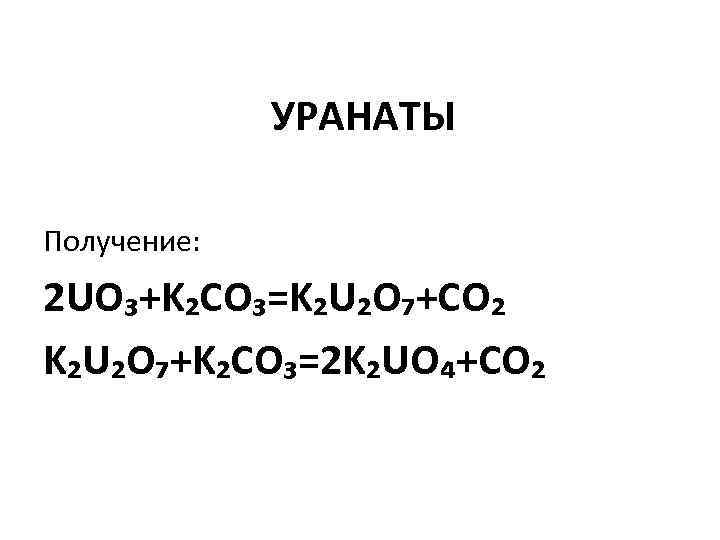
УРАНАТЫ Получение: 2 UO₃+K₂CO₃=K₂U₂O₇+CO₂ K₂U₂O₇+K₂CO₃=2 K₂UO₄+CO₂

Уранаты. После изучения соединений типа Li₄UO₅ , K₂U₇O₂₂ выяснилось, что все уранаты имеют строение [UO₆] c cильно укороченными связями U – O (уранильная группировка).

При действии кислот, а также р-ра карбоната калия уранаты переходят в раствор: K₂U₂O₇+6 HCl=2 UO₂Cl₂+3 H₂O K₂U₂O₇+6 K₂CO₃+3 H₂O= 2 K₄[UO₂(CO₃)₃]+6 KOH

Cоединения урана Соединения урана (+4) проявляют восстановительные свойства. К примеру, окисляются на воздухе: 2 UCl 4+O 2+2 H 2 O=2 UO 2 Cl 2+4 HCl

Соединения урана (+3) – очень сильные восстановители 4 UO₂SO₄+2 H₂SO₄= =2 U₂(SO₄)₃+3 O₂+2 H₂O

Свойства тяжелых 5 f-элементов (Bk, Cf, Es, Md, No, Fm, Lr) изучены мало, поскольку они получены в виде короткоживущих радиоактивных изотопов в очень малых количествах. Однако есть основания полагать, что они подобны лантанидам. Актиниды и их соединения используются в атомной энергетике. Торий используется как легирующая добавка в жаропрочных сталях, катализаторах при синтезе многих соединений, вакуумной электронике. Соли урана применяются как красители для стекла и глазурей, аналитические и фотографические препараты.
актиниды 1122.ppt