5722ee1c2489b35283261afaadf41067.ppt
- Количество слайдов: 11
 AFQ 056/Mavoglurant für Fragiles X Aktuelle klinische Studien Thomas Jaecklin & Marc Brinkman Interessegemeinschaft Fragiles X, 16 November 2012
AFQ 056/Mavoglurant für Fragiles X Aktuelle klinische Studien Thomas Jaecklin & Marc Brinkman Interessegemeinschaft Fragiles X, 16 November 2012
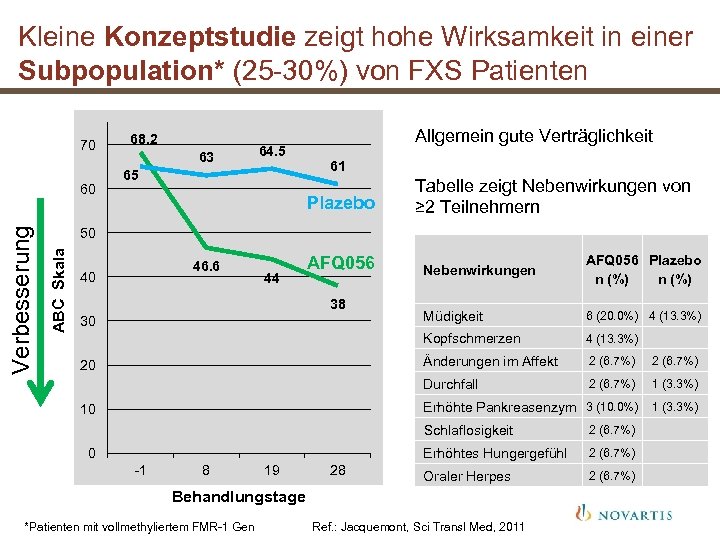 Kleine Konzeptstudie zeigt hohe Wirksamkeit in einer Subpopulation* (25 -30%) von FXS Patienten 70 63 64. 5 65 Allgemein gute Verträglichkeit 61 Plazebo Tabelle zeigt Nebenwirkungen von ≥ 2 Teilnehmern 50 ABC Skala Verbesserung 60 68. 2 30 20 10 6 (20. 0%) 4 (13. 3%) 2 (6. 7%) 1 (3. 3%) Erhöhte Pankreasenzym 3 (10. 0%) 38 Müdigkeit Durchfall 44 AFQ 056 Plazebo n (%) Änderungen im Affekt 40 AFQ 056 Nebenwirkungen Kopfschmerzen 46. 6 1 (3. 3%) Schlaflosigkeit -1 8 19 28 Erhöhtes Hungergefühl 0 2 (6. 7%) Oraler Herpes 2 (6. 7%) Behandlungstage *Patienten mit vollmethyliertem FMR-1 Gen Ref. : Jacquemont, Sci Transl Med, 2011
Kleine Konzeptstudie zeigt hohe Wirksamkeit in einer Subpopulation* (25 -30%) von FXS Patienten 70 63 64. 5 65 Allgemein gute Verträglichkeit 61 Plazebo Tabelle zeigt Nebenwirkungen von ≥ 2 Teilnehmern 50 ABC Skala Verbesserung 60 68. 2 30 20 10 6 (20. 0%) 4 (13. 3%) 2 (6. 7%) 1 (3. 3%) Erhöhte Pankreasenzym 3 (10. 0%) 38 Müdigkeit Durchfall 44 AFQ 056 Plazebo n (%) Änderungen im Affekt 40 AFQ 056 Nebenwirkungen Kopfschmerzen 46. 6 1 (3. 3%) Schlaflosigkeit -1 8 19 28 Erhöhtes Hungergefühl 0 2 (6. 7%) Oraler Herpes 2 (6. 7%) Behandlungstage *Patienten mit vollmethyliertem FMR-1 Gen Ref. : Jacquemont, Sci Transl Med, 2011
 Aktuelle AFQ 056/Mavoglurant Studien § Ziel: Wirksamkeit & Verträglichkeit von AFQ 056 zu bestätigen § 2 Hauptstudien (je 160 Teilnehmer) • Randomisiert, Plazebo-kontrolliert, doppelblind • Erwachsene 18 -45 Jahre & Jugendliche 12 -17 Jahre § 2 Erweiterungsstudien: • Teilnehmer der Hauptstudien können in die Erweiterungsstudien übertreten • Alle Teilnehmer erhalten AFQ 056/Mavoglurant, Dosis vom Studienarzt bestimmt • Dauer: mind. 2 Jahre oder bis zum Verkauf in der Apotheke 3
Aktuelle AFQ 056/Mavoglurant Studien § Ziel: Wirksamkeit & Verträglichkeit von AFQ 056 zu bestätigen § 2 Hauptstudien (je 160 Teilnehmer) • Randomisiert, Plazebo-kontrolliert, doppelblind • Erwachsene 18 -45 Jahre & Jugendliche 12 -17 Jahre § 2 Erweiterungsstudien: • Teilnehmer der Hauptstudien können in die Erweiterungsstudien übertreten • Alle Teilnehmer erhalten AFQ 056/Mavoglurant, Dosis vom Studienarzt bestimmt • Dauer: mind. 2 Jahre oder bis zum Verkauf in der Apotheke 3
 Abklärungen während der Studien • Primäre Messmethode: ABC Skala • Validierte Skala um Verhaltensauffälligkeiten zu messen • 58 einfache Fragen von der Betreuungsperson ausgefüllt • Evaluiert 6 Aspekte von auffälligem Verhalten • 4 weitere Verhaltensskalen, IQ-Test und Lebensqualitätsskala • Verträglichkeitsdaten: • Leber- und Nierenwerte, Hormone, Medikamentenpegel etc. 4
Abklärungen während der Studien • Primäre Messmethode: ABC Skala • Validierte Skala um Verhaltensauffälligkeiten zu messen • 58 einfache Fragen von der Betreuungsperson ausgefüllt • Evaluiert 6 Aspekte von auffälligem Verhalten • 4 weitere Verhaltensskalen, IQ-Test und Lebensqualitätsskala • Verträglichkeitsdaten: • Leber- und Nierenwerte, Hormone, Medikamentenpegel etc. 4
 Phase 2 b/3 2212 Erwachsene Phase 2 b/3 2214 Jugendliche 5 Studienaufbau
Phase 2 b/3 2212 Erwachsene Phase 2 b/3 2214 Jugendliche 5 Studienaufbau
 Phase 2 b/3 2212 Erwachsene Phase 2 b/3 2214 Jugendliche Europa: - 6 Dänmark Frankreich Italien Deutschland Spanien Schweden Schweiz GB Portugal? Globale Studien Australien/Asien: - Israel - Indonesien - Australien Amerikas: - USA - Kanada - Brasilien
Phase 2 b/3 2212 Erwachsene Phase 2 b/3 2214 Jugendliche Europa: - 6 Dänmark Frankreich Italien Deutschland Spanien Schweden Schweiz GB Portugal? Globale Studien Australien/Asien: - Israel - Indonesien - Australien Amerikas: - USA - Kanada - Brasilien
 Deutsche Studienzentren und Kontakt • Deutsche Studienzentren: • Prof. Barth - Universitätsklinikum, Tübingen (Erwachsene und Jugendliche) • Dr. Colla - Charité, Campus Benjamin Franklin, Berlin (nur Erwachsene) • Prof. Huss - Johannes Gutenberg-Universität, Mainz (Erwachsene und Jugendliche) • Dr. Oehler - Medizinisches Studienzentrum, Würzburg, Germany (Erwachsene und Jugendliche) • Dr. Alfred - Praxis für Kinder- und Jugendpsychiatrie, München (nur Jugendliche) • Prof. Bender - Universitätsklinikum Carl Gustav Carus der TU, Dresden (Erwachsene und Jugendliche) § Kontakt: • marc. brinkman@novartis. com – Medical Advisor Novartis Deutschland • ingrid. andresen@novartis. com – Lead-CRA, Studienmonitor • george. apostol@novartis. com – Leiter FXS Program bei Novartis 7
Deutsche Studienzentren und Kontakt • Deutsche Studienzentren: • Prof. Barth - Universitätsklinikum, Tübingen (Erwachsene und Jugendliche) • Dr. Colla - Charité, Campus Benjamin Franklin, Berlin (nur Erwachsene) • Prof. Huss - Johannes Gutenberg-Universität, Mainz (Erwachsene und Jugendliche) • Dr. Oehler - Medizinisches Studienzentrum, Würzburg, Germany (Erwachsene und Jugendliche) • Dr. Alfred - Praxis für Kinder- und Jugendpsychiatrie, München (nur Jugendliche) • Prof. Bender - Universitätsklinikum Carl Gustav Carus der TU, Dresden (Erwachsene und Jugendliche) § Kontakt: • marc. brinkman@novartis. com – Medical Advisor Novartis Deutschland • ingrid. andresen@novartis. com – Lead-CRA, Studienmonitor • george. apostol@novartis. com – Leiter FXS Program bei Novartis 7
 Deutsche FXS Beobachtungsstudie 8
Deutsche FXS Beobachtungsstudie 8
 Studienziel § Erfassung vom FXS Krankheitsbild in Deutschland • • • Symptomatik Soziale Situation Ausbildung und Arbeit Behandlung von FXS (medikamentös & nicht medikamentös) Lebensqualität der betroffenen Familien (wenn möglich Patienten) Gesundheitsökonomische Parameter § 300 Studienteilnehmer in ≥ 50 Studienzentren (unlimitiert) § Dauer: 3 Jahre, Studienbesuche alle 6 Monate § Teilnahmebedingungen: Zustimmung & FXS Diagnose § Dies ist eine Beobachungsstudie – OHNE Medikamente 9
Studienziel § Erfassung vom FXS Krankheitsbild in Deutschland • • • Symptomatik Soziale Situation Ausbildung und Arbeit Behandlung von FXS (medikamentös & nicht medikamentös) Lebensqualität der betroffenen Familien (wenn möglich Patienten) Gesundheitsökonomische Parameter § 300 Studienteilnehmer in ≥ 50 Studienzentren (unlimitiert) § Dauer: 3 Jahre, Studienbesuche alle 6 Monate § Teilnahmebedingungen: Zustimmung & FXS Diagnose § Dies ist eine Beobachungsstudie – OHNE Medikamente 9
 Leitung § Leiter: Prof. Hässler (Universität Rostock) § Leitungsausschuss: Prof. Hässler (Direktor Rostock, Präsident DGKJP) Prof. Pittrow (GWT-Dresden/München) Dr. Elsner (KEH Berlin) Dr. Gaese (TU-München; Sprecherin der Arbeitsgruppe geistige Behinderung der Bundesdirektorenkonferenz) Prof. Huss (Klinikdirektor Mainz, Studienarzt) Prof. Peters (Mainz, SPZ*) Dr. Colla (Charite, Studienarzt) Dr. Kretschmar (Dresden, Expertenkomitee und Sprecher der SPZ* in D) *SPZ: Sozialpädiatrische Zentren 10
Leitung § Leiter: Prof. Hässler (Universität Rostock) § Leitungsausschuss: Prof. Hässler (Direktor Rostock, Präsident DGKJP) Prof. Pittrow (GWT-Dresden/München) Dr. Elsner (KEH Berlin) Dr. Gaese (TU-München; Sprecherin der Arbeitsgruppe geistige Behinderung der Bundesdirektorenkonferenz) Prof. Huss (Klinikdirektor Mainz, Studienarzt) Prof. Peters (Mainz, SPZ*) Dr. Colla (Charite, Studienarzt) Dr. Kretschmar (Dresden, Expertenkomitee und Sprecher der SPZ* in D) *SPZ: Sozialpädiatrische Zentren 10
 Studienkontakte § Marc Brinkman – Projektleiter Novartis Deutschland marc. brinkman@novartis. com +49 911 273 12 102 § Mark Tomlinson – Europäische Erweiterung mark. tomlinson@novartis. com +44 79 66 515 578 § George Apostol – Leiter FXS Program bei Novartis george. apostol@novartis. com +41 61 324 1402 11
Studienkontakte § Marc Brinkman – Projektleiter Novartis Deutschland marc. brinkman@novartis. com +49 911 273 12 102 § Mark Tomlinson – Europäische Erweiterung mark. tomlinson@novartis. com +44 79 66 515 578 § George Apostol – Leiter FXS Program bei Novartis george. apostol@novartis. com +41 61 324 1402 11


