Лекция 1 2013 вводная.ppt
- Количество слайдов: 65

Адсорбция и пористая структура ~20 лекций + семинары + практика + экзамен Лекторы: д. х. н. , профессор Фенелонов Владимир Борисович, г. н. с. Борисович к. х. н. Мельгунов Максим Сергеевич, зав. лаб. Сергеевич Комната 136, тел 797, гор. тел. 3309255 (Лаборатория исследования текстуры катализаторов) 1

Основные пособия В. Б. Фенелонов Введение в физическую химию формирования супрамолекулярной структуры адсорбентов и катализаторов Курс лекций Сборник задач Взять в библиотеке НГУ 2

В лекциях принципиально важные слайды отмечены знаком не важен. . Цвет Слайды со знаком -только для сведения, соответствующие формулы запоминать не нужно, знать надо только физ. смысл и тенденции. 3

Общая цель курса: введение в физическую химию формирования и адсорбционные методы контроля текстуры гетерогенных катализаторов. Текстура –структура твердых гетерогенных катализаторов на супрамолекулярном уровне: 1 -2 нм и выше. Ее основные характеристики Поверхность Пористость Морфология и другие геометрические характеристики супрамолекулярного уровня, включая распределение частиц и пор по размерам, компонентов катализатора по радиусу зерна и т. д. 4

Роль текстуры удельная каталитическая активность гетерогенного катализатора определяется его химическим и фазовым составом –т. е. структурой атомномолекулярного уровня, но эффективность катализатора определяется его удельной поверхностью и диффузионной доступностью этой поверхности, т. е. структурой супрамолекулярного уровня (текстурой) Управление этими структурными уровнями определяется разными законами. 5

• Без химической активности нет катализа, • но без оптимизации текстуры нет хорошего промышленного катализатора. • Химический состав катализатора задается законами общей молекулярной химии, а формирование текстуры определяется специфическими законами поверхностных явлений, супрамолекулярной, коллоидной и физической химии, геометрии и т. д. , поэтому приготовление катализаторов нельзя рассматривать как чисто химическую задачу. 6

Текстура исследуется комплексом методов, включая Э-микроскопию, рентгеновские и другие спектральные методы. Но особая роль принадлежит адсорбционным методам и механизмам: 1. обеспечивают наиболее прямые измерения доступной поверхности, объема и распределения пор; 2. Адсорбция тесно связана с гетерогенным катализом 3. Многие механизмы формирования текстуры и механизмы адсорбционно-капиллярных процессов обусловлены общими закономерностями поверхностных явлений, т. е. имеют 7 общий теоретический фундамент
Содержание курса “адсорбция и пористость” Закономерности поверхностных явлений Адсорбционные методы измерения текстурных характеристик гетерогенных катализаторов Закономерности формирования текстурных характеристик гетерогенных катализаторов, обусловленные поверхностными явлениями 8

Избыточная поверхностная энергия А Разница энергий атома А на поверхности и атома В в объеме B атомы (молекулы), расположенные на поверхности конденсированной фазы, находятся под воздействием “внутреннего” силового поля, обусловленного взаимодействием с собственной фазой и создают внешнее силовое поле, приводящее к адсорбции. Оба силовых поля взаимосвязаны и в ходе адсорбции могут изменяться, приводя к согласованным структурным изменениям по обе стороны от поверхности раздела сопредельных фаз. Адсорбция снижает избыточную поверхностную энергию G и поэтому происходит самопроизвольно ( G<0); Энтальпия адсорбции Н = G + Т S; 9 обычно S < 0 и Н < 0, т. е. выделение тепла

Дисперсность и избыточная свободная поверхностная энергия В первом приближении избыточная свободная энергия пропорциональна доле поверхностных атомов NA от общего числа N атомов в частице Безразмерное отношение N = NA/N часто называют дисперсностью, это одна из важнейших характеристик пористых и дисперсных материалов 10

Дисперсность Термин дисперсность – производный от лат. dispersus (рассеянный, рассыпанный), характеризует величину, обратную размеру частиц (чем меньше размер частиц, тем дисперснее). Численно дисперсность выражают также в виде размерных параметров – как величину, обратную среднему размеру частиц D, или как отношение поверхности А к объему V частиц А/V Рассмотрим связь таких определений. 11

Простейший пример: дисперсность NA/N частицы в виде куба из N атомов; размер атома а, ребра Х=a. N 1/3 Координационная ненасыщенность в вершинах, ребрах и гранях различна X =a. N 1/3 a В 8 вершинах куба NA, верш = 8 на 12 ребрах 12(N 1/3 -2) на 6 гранях 6(N 1/3 -2)2 NA/N= 8/N + 12(N 1/3 -2)/N +6(N 1/3 -2)2/N 8/N+12/N 2/3+6/N 1/3 при больших N вклад вершин и ребер становится малым N = NA/N 6/N 1/3, т. е. N 6(а/Х) Поверхность куба с ребром а. N 1/3 равна А = 6 Х 2 = 6 (а. N 1/3)2, объем V = Х 3 = (а. N 1/3)3 отношение A/V = 6/a. N 1/3 = N/a = 6/X В результате при больших N связь N, характерного размера Х и A/V N NA/N = 6(а/Х) = a(А/V) = 6/N 1/3 12
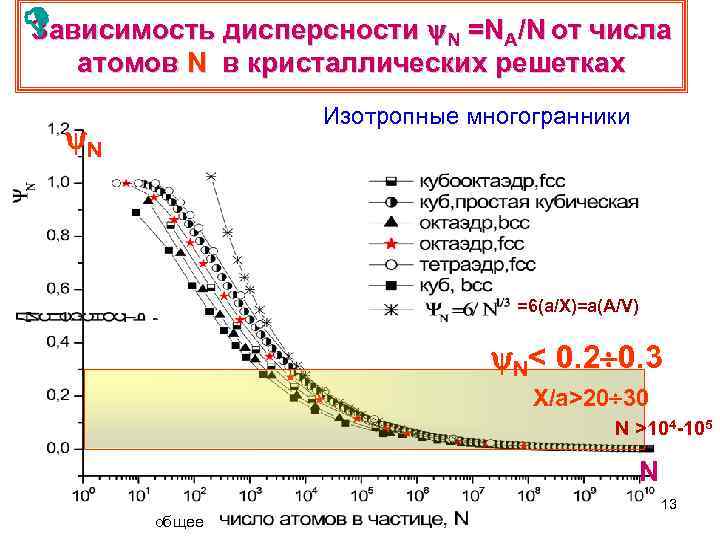
Зависимость дисперсности N =NA/N от числа атомов N в кристаллических решетках Изотропные многогранники N =6(а/Х)=a(A/V) N< 0. 2 0. 3 Х/а>20 30 N >104 -105 N 13 общее

Дисперсность выпуклых тел анизотропной формы удобно выражать через N а(A/V) и Х максимальный диаметр Х вписанной сферы Х = Каниз(V/A) Х Сфера касается всех граней, Каниз=6 A/V=6/Х; N~6(a/X) Анизотропия формы снижает численный коэффициент. В пределепри сильной анизотропии в одном направлении Х A/V=4/Х; N~4(a/X) (цилиндры, многогранные стержни, волокна ) Х При анизотропии в двух направлениях A/V=2/Х; N~2(a/Х) (гладкие пластины) 14
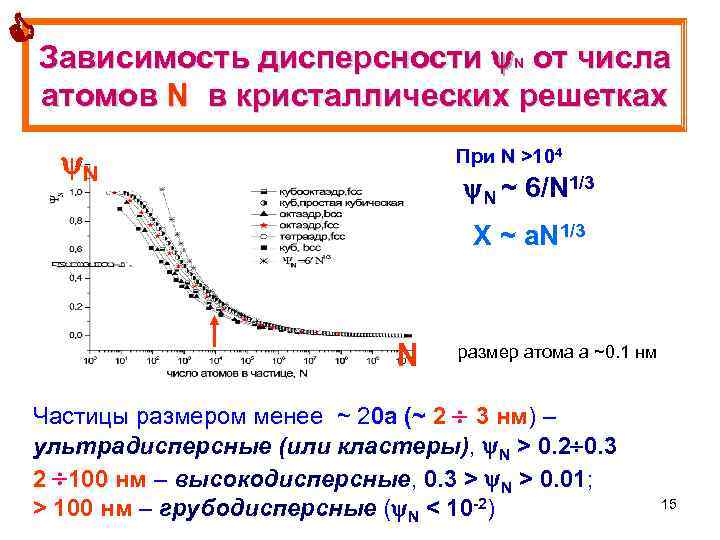
Зависимость дисперсности N от числа атомов N в кристаллических решетках N При N >104 N ~ 6/N 1/3 X ~ a. N 1/3 N размер атома а ~0. 1 нм Частицы размером менее ~ 20 a (~ 2 3 нм) – ультрадисперсные (или кластеры), N > 0. 2 0. 3 2 100 нм – высокодисперсные, 0. 3 > N > 0. 01; > 100 нм – грубодисперсные ( N < 10 -2) 15

Дисперсность Ультрадисперсные частицы (кластеры) < 1 -2 нм, N > 0. 3 по свойствам находятся на границе между молекулярными системами и обычными объемными фазами и требуют индивидуального подхода. Высокодисперсные или наночастицы (1 -2) 100 нм, 0. 3 > N >0. 01 – одновременно обладают особыми поверхностно-избыточными свойствами объемных фаз. 16

Дисперсность Грубодисперсные частицы (> 100 нм): избыточные свойства сохраняются лишь непосредственно у поверхности, но могут еще проявляться особые механические свойства (сыпучесть, агломерируемость, cпецифика механики течения и др. ) 17

• В нашем курсе основное внимание – на высокодисперсные системы (наносистемы) с наносистемы характерным размером частиц Х 2 нм и N < 0. 2 0. 3, для которых дисперсность NA/N пропорциональна А/V. Такие системы сохраняют фазовые свойства в объеме и обладают дополнительными свойствами из-за избыточной поверхностной энергии. Именно к таким системам наиболее применимы подходы, используемые в теории физадсорбции и других поверхностных явлений. 18

Высокодисперсные системы Х 2 нм, N < 0. 2 0. 3 Для таких систем переход от A/V = 6/X к А/m = A/V = 6/X , где - плотность соответствующей фазы, а m= V - масса единицы объема, позволяет определить удельную поверхность единицы массы пористого материала Am = A/V = 6/X т. е. A/V = Am = 6/Х Обычно Аm м 2/г, г/см 3, размер Х нм, при этом Am =6 103/Х силикагель = 2. 2 г/см 3, Х = 2 нм Аm = 1360 м 2/г Al 203 = 3. 3 г/см 3, Х = 2 нм Аm = 909 м 2/г Pt = 21. 45 г/см 3, Х = 2 нм Аm = 139. 8 м 2/г 19

Адсорбционная терминология Адсорбция – самопроизвольное концентрирование компонентов из объема сопредельных фаз на межфазовой поверхности раздела (от лат. sorbco поглощение и приставки ad – над); • Абсорбция – растворение в объеме конденсированной фазы (тв или ж); • Адсорбент - вещество, на котором происходит адсорбция (хозяин Н – от host); • Адсорбат – адсорбированное вещество (G – от guest); • Адсорбтив – еще не адсорбированный G; • Десорбция – удаление G c поверхности или из объема H 20
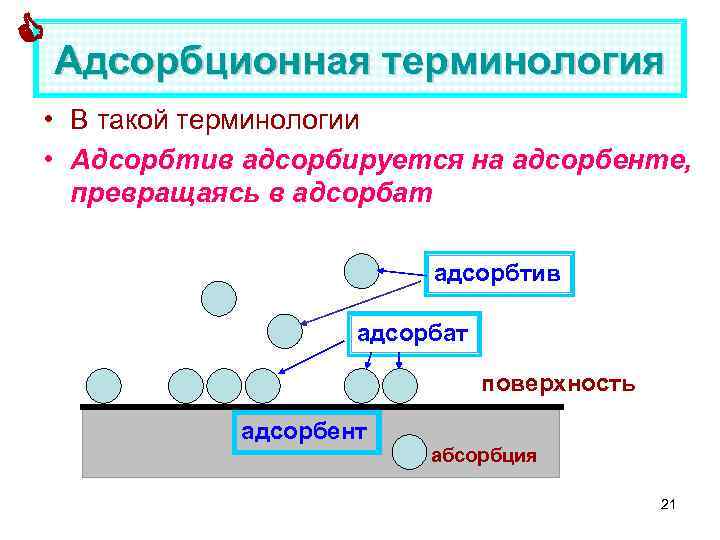
Адсорбционная терминология • В такой терминологии • Адсорбтив адсорбируется на адсорбенте, превращаясь в адсорбат адсорбтив адсорбат поверхность адсорбент абсорбция 21
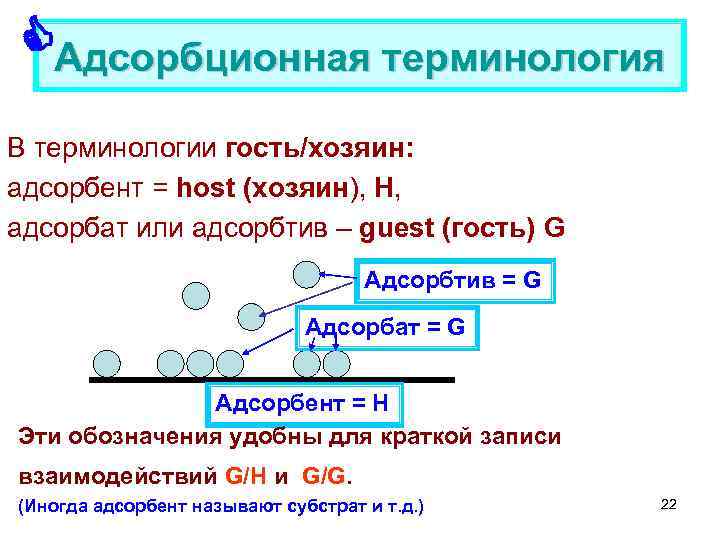
Адсорбционная терминология В терминологии гость/хозяин: адсорбент = host (хозяин), Н, адсорбат или адсорбтив – guest (гость) G Адсорбтив = G Адсорбат = G Адсорбент = H Эти обозначения удобны для краткой записи взаимодействий G/H и G/G. (Иногда адсорбент называют субстрат и т. д. ) 22
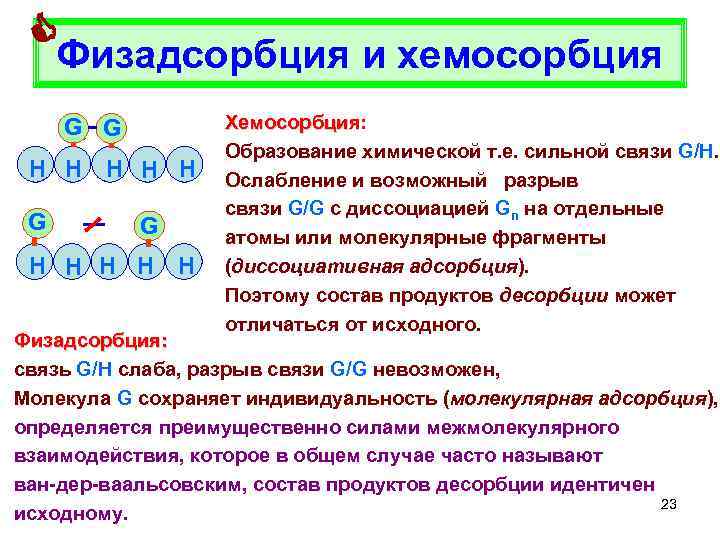
Физадсорбция и хемосорбция G G H H H Хемосорбция: Хемосорбция Образование химической т. е. сильной связи G/H. Ослабление и возможный разрыв связи G/G с диссоциацией Gn на отдельные атомы или молекулярные фрагменты (диссоциативная адсорбция). Поэтому состав продуктов десорбции может отличаться от исходного. Физадсорбция: связь G/H слаба, разрыв связи G/G невозможен, Молекула G сохраняет индивидуальность (молекулярная адсорбция), определяется преимущественно силами межмолекулярного взаимодействия, которое в общем случае часто называют ван-дер-ваальсовским, состав продуктов десорбции идентичен 23 исходному.

Ван-дер-ваальсовские (физические) взаимодействия -По Р. Фейнману силы межмолекулярного взаимодействия – результат “ «сложного взаимодействия всех электронов и ядер одной молекулы со всеми электронами и ядрами другой“. Их нельзя полностью свести к фундаментальным элементарным взаимодействиям типа кулоновских или гравитационных. Они имеют общую квантово-механическую основу, их природа определяется электронной структурой H и G. -В общем случае существует непрерывный спектр форм такого взаимодействия с разной интенсивностью, характером сил и связей. 24

Дисперсионное межмолекулярное взаимодействие А B Если молекулы не взаимодействуют, то их мгновенные дипольные моменты µ ориентированы произвольно. При сближении – дисперсионное взаимодействие. Взаимодействующие молекулы Мгновенный электрический дипольный момент µА в А создает электрическое поле с напряженностью Е = 2µА/r 2 AB , которое индуцирует дип. момент µА =αВЕ в В (и наоборот), в результате образуется пара взаимоиндуцированных и взаимоориентированных взаимодействующих диполя А B 25

Дисперсионное взаимодействие Потенциал дисперсионного взаимодействия пары сферических молекул А и В с поляризуемостью αi и потенциалом ионизации Ji по Лондону определяется = -Сдисп/r 6, где Сдисп =(3/2)αАαВ[JAJB]/[JA+JB] Более полное выражение включает вклад индуцированных диполь-квадрупольного, квадрупольного и др. взаимодействий, которые пропорциональны расстоянию r-8 и r-10 и т. д. ; их вклад мал и обычно не учитывают. Квадруполь: два противоположно направленных диполя, нулевой суммарный момент, например, N 2 : - N + + N е-оболочка ядро 26
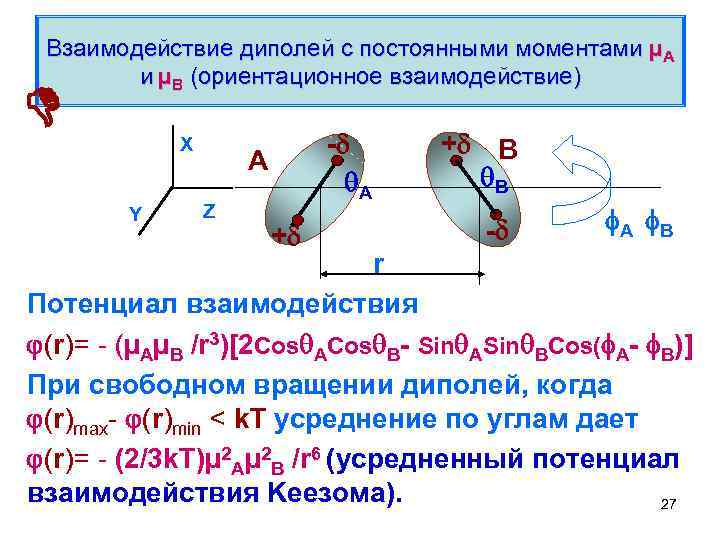
Взаимодействие диполей с постоянными моментами µА и µB (ориентационное взаимодействие) X Y - A А Z + + В B - А В r Потенциал взаимодействия (r)= - (µАµB /r 3)[2 Cos ACos B- Sin ASin BCos( A- B)] При свободном вращении диполей, когда (r)max- (r)min < k. T усреднение по углам дает (r)= - (2/3 k. Т)µ 2 Аµ 2 B /r 6 (усредненный потенциал взаимодействия Keeзома). 27

Индукционное взаимодействие диполь/поляризуемая неполярная молекула) В - + А - + r Электрическое поле диполя А поляризует неполярную молекулу В, индуцируя в ней наведенный дипольный момент. Этот же эффект индукции усиливает дипольный момент молекул с постоянными диполями. Усредненный потенциал взаимодействия с учетом вращения пропорционален µА 2 B/r 6 (усредненный потенциал взаимодействия Дебая). Индуцированное диполь/квадруполь взаимодействие ~r-8, индуцированное квадруполь/квадруполь взаимодействие ~r-10 и т. д. 28
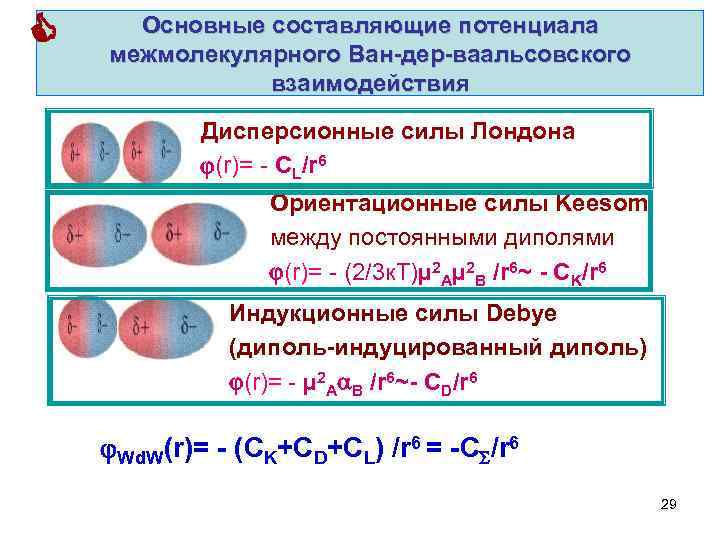
Основные составляющие потенциала межмолекулярного Ван-дер-ваальсовского взаимодействия Дисперсионные силы Лондона (r)= - СL/r 6 Ориентационные силы Keesom между постоянными диполями (r)= - (2/3 к. Т)µ 2 Аµ 2 B /r 6~ - CK/r 6 Индукционные силы Debye (диполь-индуцированный диполь) (r)= - µ 2 А B /r 6~- СD/r 6 Wd. W(r)= - (СK+СD+СL) /r 6 = -С /r 6 29
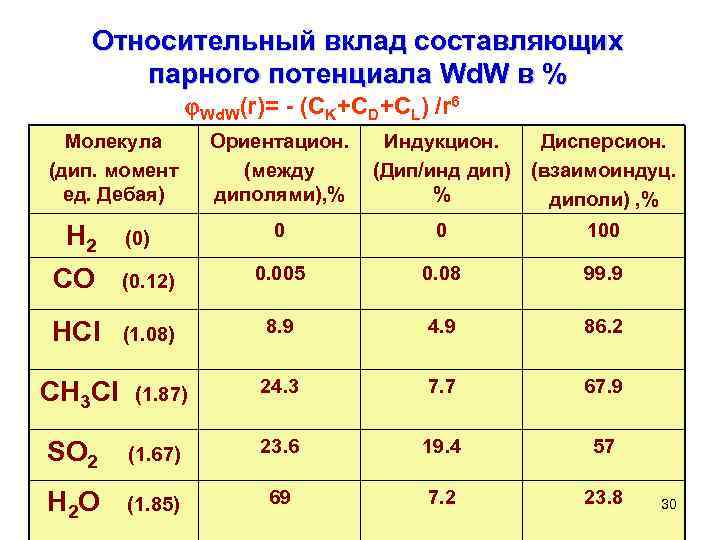
Относительный вклад составляющих парного потенциала Wd. W в % Wd. W(r)= - (СK+СD+СL) /r 6 Молекула (дип. момент ед. Дебая) Н 2 (0) Ориентацион. (между диполями), % Индукцион. (Дип/инд дип) % Дисперсион. (взаимоиндуц. диполи) , % 0 0 100 СО (0. 12) 0. 005 0. 08 99. 9 HCl (1. 08) 8. 9 4. 9 86. 2 24. 3 7. 7 67. 9 СH 3 Cl (1. 87) SO 2 (1. 67) 23. 6 19. 4 57 H 2 O (1. 85) 69 7. 2 23. 8 30
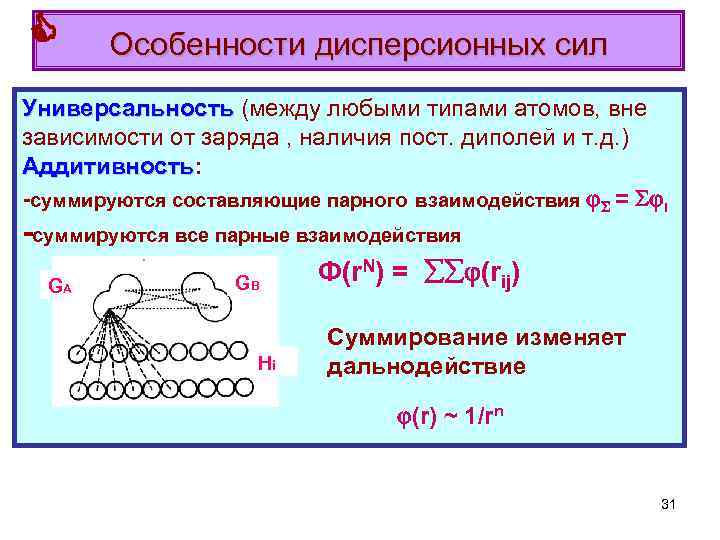
Особенности дисперсионных сил Универсальность (между любыми типами атомов, вне зависимости от заряда , наличия пост. диполей и т. д. ) Аддитивность: Аддитивность -суммируются составляющие парного взаимодействия = i -суммируются все парные взаимодействия GA В GB Hi Ф(r. N) = (rij) Cуммирование изменяет дальнодействие (r) ~ 1/rn 31
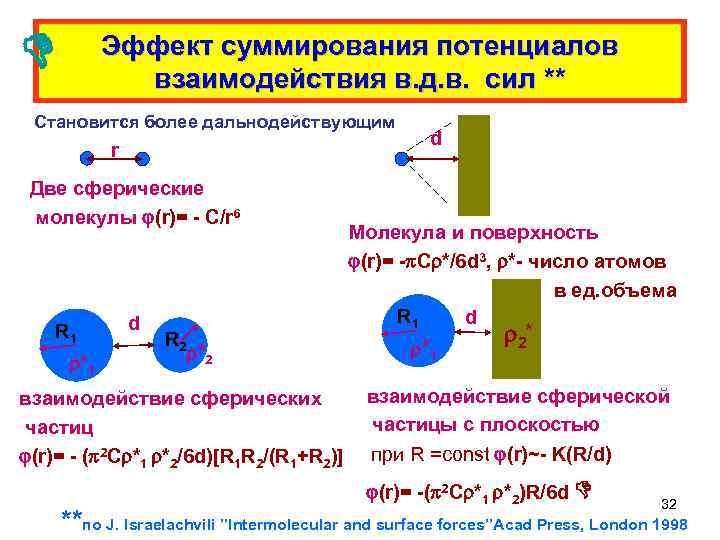
Эффект суммирования потенциалов взаимодействия в. д. в. сил ** Становится более дальнодействующим r Две сферические молекулы (r)= - С/r 6 R 1 *1 d R 2 *2 взаимодействие сферических частиц (r)= - ( 2 С *1 *2/6 d)[R 1 R 2/(R 1+R 2)] d Молекула и поверхность (r)= - С */6 d 3, *- число атомов в ед. объема R 1 d *1 2* взаимодействие сферической частицы с плоскостью при R =const (r)~- K(R/d) (r)= -( 2 С *1 *2)R/6 d 32 **по J. Israelachvili ”Intermolecular and surface forces”Acad Press, London 1998

межмолекулярные взаимодействия с участием ионов Кулоновское взаимодействие: Ион А–диполь B: A (r)= -q. Aq. B/r (r)= -q. AµB Cos /r 2 µB- дипольный момент B r B A r При возможности вращения диполя (r)= -q. A 2µB 2 /r 4 Ион А – квадруполь В: (r)= -q. AQB (3 Cos 2 -1)/4 r 3 При возможности вращения (r)= -q. A 2 QB 2/r 6 Дополнительные взаимодействия : с образованием Н-связей ~r-2 И другие специфические взаимодействия 33
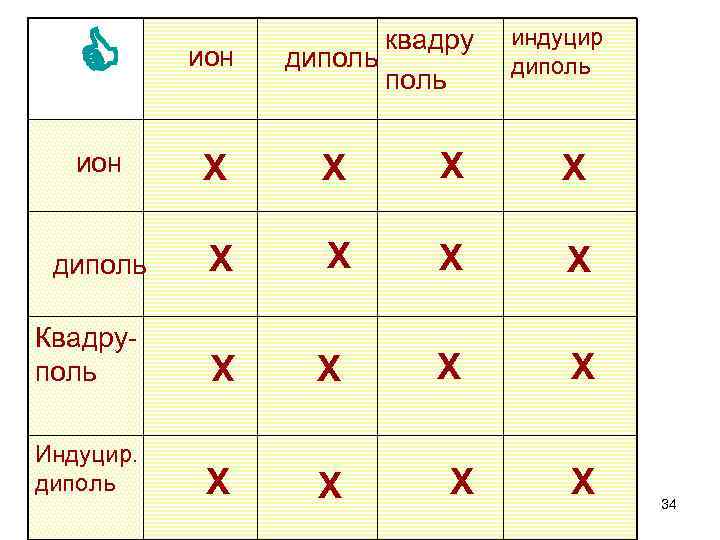
ион Х Х диполь Х Х Квадруполь Х Х Индуцир. диполь Х Х квадру диполь Х индуцир диполь Х 34

О потенциале химического взаимодействия Зависимость потенциала химического взаимодействия хим от расстояния еще более сложна, определяется спецификой взаимодействия, область действия ограничена расстояниями порядка длины химической связи. Простейшая форма приближенного выражения хим~ be –r/a, где a и b- постоянные для каждого типа взаимодействий. В общем случае это короткодействующий потенциал, который проявляется на расстояниях, где отталкивание электронных оболочек превышает межмолекулярные силы притяжения и потенциалы физического взаимодействия изза малости вклада «не работают» . 35
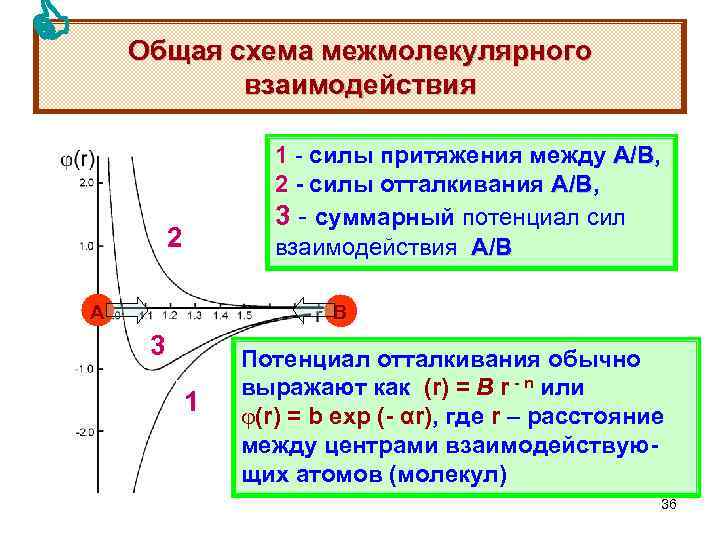
Общая схема межмолекулярного взаимодействия 1 - силы притяжения между А/В, А/В 2 - силы отталкивания А/В, 3 - cуммарный потенциал сил взаимодействия А/В 2 B A 3 1 Потенциал отталкивания обычно выражают как (r) = B r - n или (r) = b exp (- αr), где r – расстояние между центрами взаимодействующих атомов (молекул) 36
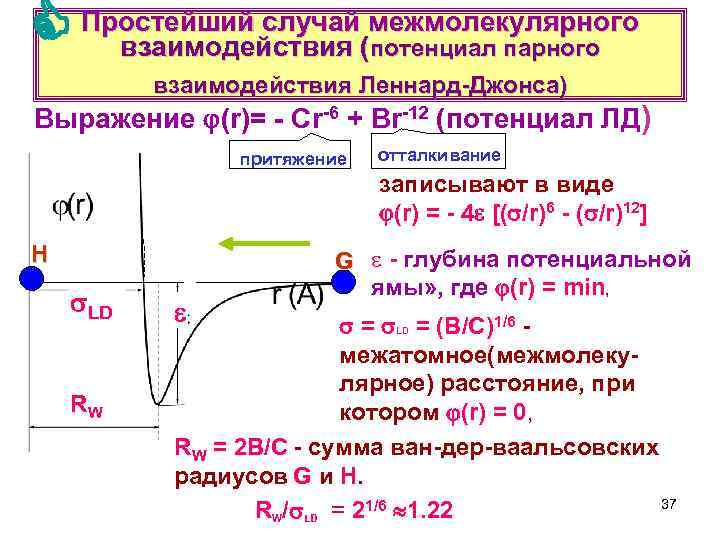
Простейший случай межмолекулярного взаимодействия (потенциал парного взаимодействия Леннард-Джонса) Выражение (r)= - Сr-6 + Br-12 (потенциал ЛД) притяжение отталкивание записывают в виде (r) = - 4 [( /r)6 - ( /r)12] H LD RW G - глубина потенциальной ямы» , где (r) = min, = LD = (В/С)1/6 межатомное(межмолекулярное) расстояние, при котором (r) = 0, RW = 2 В/С - сумма ван-дер-ваальсовских радиусов G и H. 37 RW/ LD = 21/6 1. 22
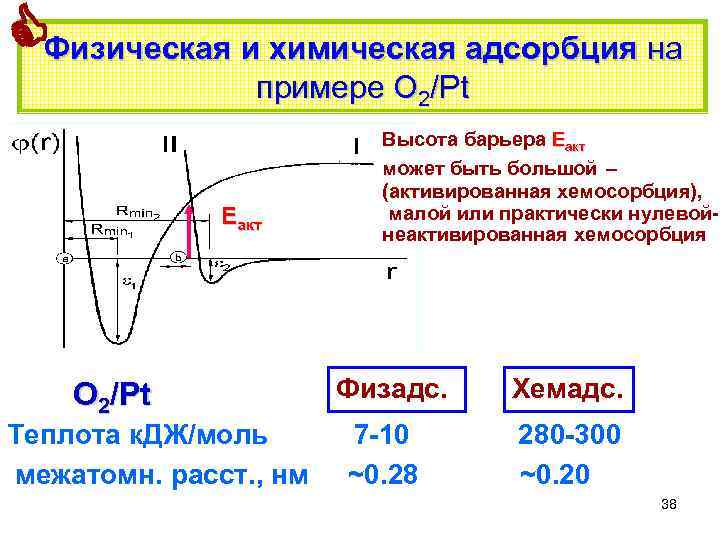
Физическая и химическая адсорбция на примере О 2/Pt Еакт О 2/Pt Теплота к. ДЖ/моль межатомн. расст. , нм Высота барьера Еакт может быть большой – (активированная хемосорбция), малой или практически нулевойнеактивированная хемосорбция Физадс. 7 -10 ~0. 28 Хемадс. 280 -300 ~0. 20 38
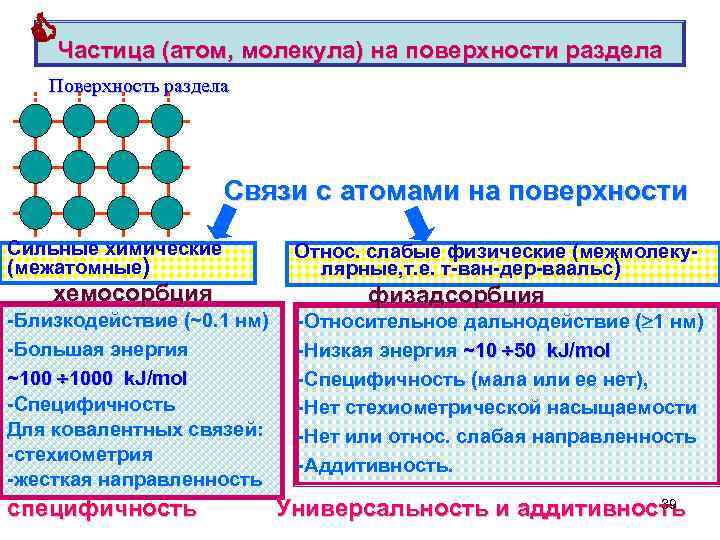
Частица (атом, молекула) на поверхности раздела Поверхность раздела Связи с атомами на поверхности Cильные химические (межатомные) хемосорбция -Близкодействие (~0. 1 нм) -Большая энергия ~100 1000 k. J/mol -Специфичность Для ковалентных связей: -стехиометрия -жесткая направленность специфичность Относ. слабые физические (межмолекулярные, т. е. т-ван-дер-ваальс) физадсорбция -Относительное дальнодействие ( 1 нм) -Низкая энергия ~10 50 k. J/mol -Специфичность (мала или ее нет), -Нет стехиометрической насыщаемости -Нет или относ. слабая направленность -Аддитивность. 39 Универсальность и аддитивность
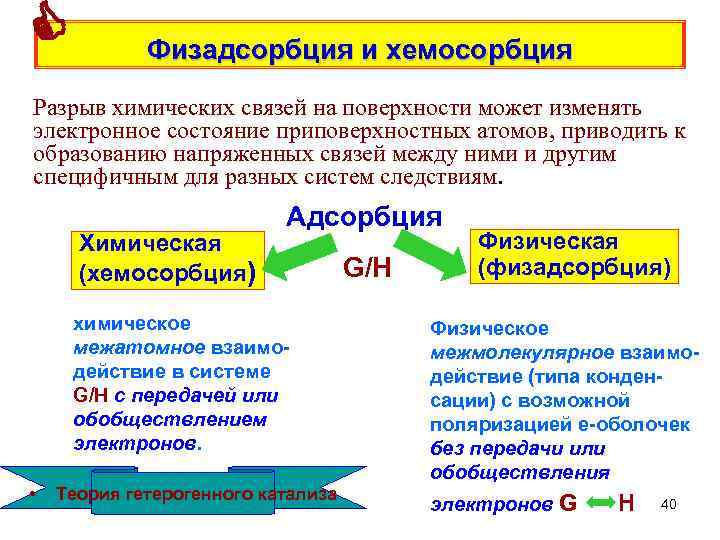
Физадсорбция и хемосорбция Разрыв химических связей на поверхности может изменять электронное состояние приповерхностных атомов, приводить к образованию напряженных связей между ними и другим специфичным для разных систем следствиям. Химическая (хемосорбция) Адсорбция химическое межатомное взаимодействие в системе G/H с передачей или обобществлением электронов. • Теория гетерогенного катализа G/H Физическая (физадсорбция) Физическое межмолекулярное взаимодействие (типа конденсации) с возможной поляризацией е-оболочек без передачи или обобществления электронов G H 40

Основные различия между типичной физической и химической адсорбцией Типовые ситуации Физ. адс. Хим. адс. специфичность Слабая или нет Высокая Теплота к. Дж/моль до 10 -50 >100 - 1000 Повышение Т Снижает Может усиливать Обратимость Обратима Необратима при низких Т Покрытие поверхности Полислои + кап. конденсация Обычно - монослой Но существует много особых случаев…. 41

Тепловые эффекты -Минимальная теплота хемосорбции Н 2 на оксиде хрома ~ 13 к. Дж/моль, -Описана эндотермическая хемосорбция Н 2 на стекле, где рост энтропии при диссоциации Н 2 и миграции атомов Н компенсирует эндотермичность G<0. Н = G +T S 42

Температура • Обычно хемосорбция при высоких, а физадсорбция - низких Т. • Но постоянные газы (N 2, О 2 и др. ) сорбируются в заметных количествах при 273 К , превышающих Т кипения на ~ 200 K (на ~1500 выше критической), физадсорбция воды на цеолитах заметна даже при 400 -5000 С. • Описаны случаи хемосорбции при криогенных температурах. 43
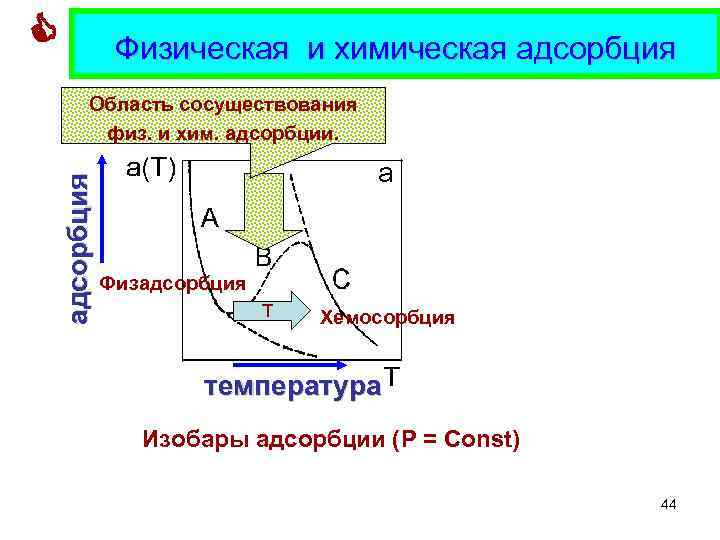
Физическая и химическая адсорбция Область сосуществования физ. и хим. адсорбции. Цеолит Na. A 0. 38 нм Физадсорбция T 0. 33 нм Хемосорбция температура Изобары адсорбции (P = Const) 44
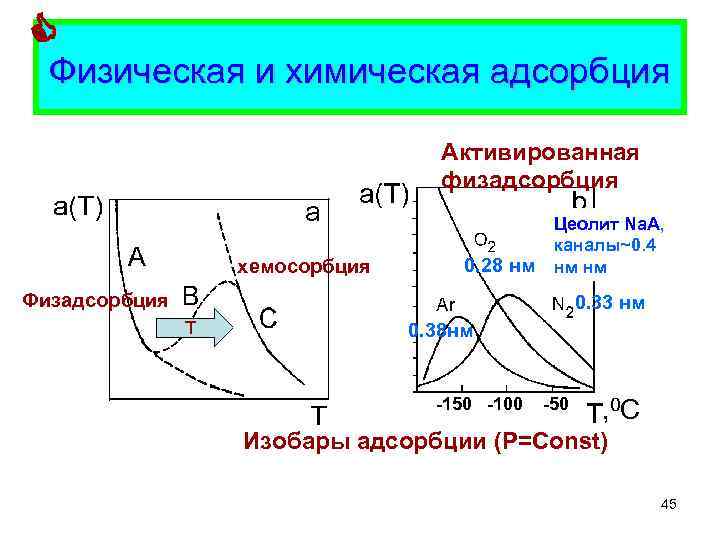
Физическая и химическая адсорбция Активированная физадсорбция хемосорбция 0. 28 нм Цеолит Na. A, каналы~0. 4 нм нм Физадсорбция 0. 33 нм T 0. 38 нм -150 -100 -50 , 0 С Изобары адсорбции (P=Const) 45

Физическая и химическая адсорбция Детальное исследование типов адсорбционных взаимодействий базируется на комплексных экспериментальных (ИКС, ЯМР, ЭПР, ЭСХА и др. ) и теоретических (квантовомеханические и др. подходы) исследованиях. 46

Супрамолекулярная структура пористых материалов В заключение –некоторые примеры разнообразия морфологии пористых материалов, которая для систем с идентичным химическим составом может изменяться в очень широком диапазоне. Проиллюстрируем на примере систем, состоящих из Si. O 2 47

Примеры морфологии силикатных материалов c нерегулярной текстурой Силикагель (2 -200 нм) силикагель после гидротермальной обработки b стекловолокно пористое стекло ценосфера 48

Примеры морфологии силикатных материалов c регулярной структурой Опал -регулярная упаковка аморфных частиц 10 -30 мкм Кварц (без размола) в МСМ 41 Структура некоторых цеолитов Тип А Фожазит (тип Х) ZSM-5 МСМ-41 МСМ 48 49
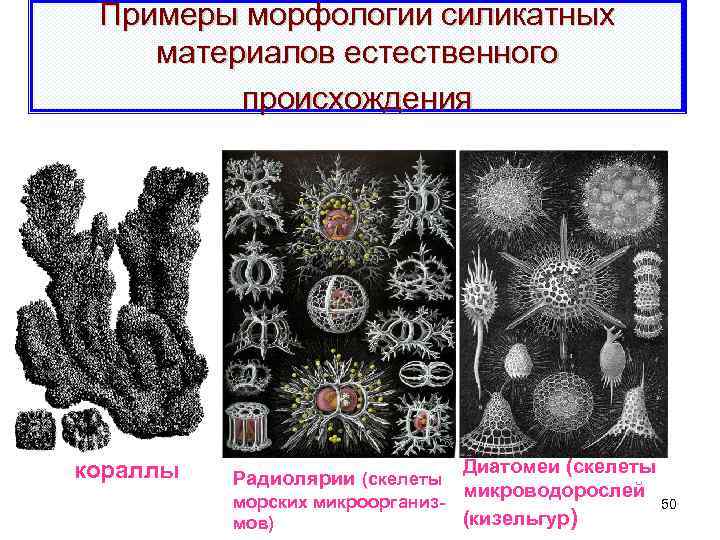
Примеры морфологии силикатных материалов естественного происхождения кораллы Диатомеи (скелеты микроводорослей морских микроорганиз 50 (кизельгур) мов) Радиолярии (скелеты
Научные основы приготовления катализаторов Формирование химического состава Формирование текстуры 51

Стратегия направленного синтеза современных катализаторов сложного состава должна быть подобна игре на фортепи-ано, где синхронно выполняются партии правой и левой рук- управление составом и текстурой (т. е. молекулярной и 52

• Спасибо за внимание 53

Дисперсность При малом вкладе «особых» атомов соотношение N = а(A/V) применимо к выпуклым частицам различной формы. Определим NА=А/ и NV = V/v, где и v – средние значения поверхности и объема на один атом в частице: N = NA/NV = (v/ )(A/V), В достаточно общем случае ячейку для одного атома можно представить призмой высотой а, при этом v/ = а, в результате N = а(A/V) 54

Лабиринт каркаса и лабиринт пор М Модель пористого стекла Модель Vпор/ Vпористого (пористость) о = стекла, = 47%. Средний тела размер пор 3. 23 нм д 0. 31 %. Средний размер е пор 4. 63 нм Vкаркаса / Vтела = 1 - (относительная плотность) л ь 55

Содержание курса Лекции 1 -9: основы физической адсорбции и термодинамики поверхностных явлений; Лекции 10 -11: элементы моделирования текстуры катализаторов и других пористых материалов; Лекции 12 -18: фундаментальные механизмы формирования текстуры типичных пористых материалов, саморегулируемое формирование нанопористых систем; Лекции 19 -20: элементы прикладной адсорбции и др. В результате вы должны знать: -Фундаментальные закономерности поверхностных явлений; -особенности разных типов адсорбции; -их использование для расчета удельной поверхности, размера и распределения пор; -подходы к моделированию текстуры, включая структуру нанопористых материалов ; -типовые механизмы формирования и регулирования текстуры, включая нанопористые материалы; -уметь использовать эти знания в практической работе. 56

Формирование супрамолекулярной структуры (текстуры): b a Top down Организованное Bottom up Самоорганизованное наличием шаблона (темплата, template), структуроуправляющего Основа многих совре- агента или другим способом. менных технологий 57 Основа «технологий» в природе внешним воздействием.

Роль текстуры катализатора Эффективность использования промышленного катализатора определяется активностью единицы объема слоя катализатора в реакторе: W v = ak A X аk- активность единицы активной поверхности или единичного центра; А - суммарная удельная поверхность; X - доля активной поверхности (или акт. компон. ); - степень использования предельной активности в условиях реактора с учетом диффузии; - насыпная плотность (вес ед объема слоя): = (1 - сл), г/см 3; сл- суммарная пористость зерна и слоя катализатора с истинной плотностью . 58

Роль текстуры катализатора Для модельного катализатора с тем же хим. и фазовым составом, но предельно оптимизированными текстурными характеристиками Wv, опт = ak, опт Aопт Xопт опт Активность промышленного катализатора Wv, / Wv, опт = J J = (А/Aопт)(Х/Xопт)( / опт) = JAJXJ J В катализаторах идентичного хим. и фаз. состава ak=const, ~Const, но при Ji < 1 значения J < 1 : При Ji= 0. 9 величина J = (0. 9)4 = 0. 65 при Ji= 0. 7 имеем J = (0. 7)4 = 0. 24, при Ji= 0. 5 величина J = (0. 5)4 ~ 0. 062 и т. д. Поэтому неоптимальная текстура может загубить любой потенциально высокоэффективный катализатор. 59

Научные основы приготовления катализаторов Формирование химического состава Формирование текстуры 60

Лекция 1. Введение в общую теорию поверхностных явлений -адсорбционная терминология, -типы физико-химических межмолекулярных взаимодействий, -главные различия между физической и химической адсорбцией, -определения дисперсности, 61

Ван-дер-ваальсовские (физические) взаимодействия -При моделировании их сводят к взаимодействию индуцированных и постоянных диполей с выделением 3 основных типов: Дисперсионное взаимодействие, которое происходит вне зависимости от наличия или отсутствия постоянных зарядов, дипольных моментов и т. д. Это наиболее универсальное взаимодействие, сохраняющееся при наличии всех других типов взаимодействия. Ориентационное взаимодействие - между постоянными диполями или диполем и зарядом Индукционное взаимодействие – между постоянным диполем или зарядом и индуцированным ими диполем. 62

Взаимодействие диполь/квадруполь и квадруполь/квадруполь В условиях свободного вращения диполь (µА) / квадруполь (QB) потенциал взаимодействия (r) = -(1/k. T)µА 2 QB 2/r 8 квадруполь (QА) /квадруполь (QB) (r)= (7/40 k. T) -(QА 2 QB 2/r 10 Эти вклады малы и их часто игнорируют 63
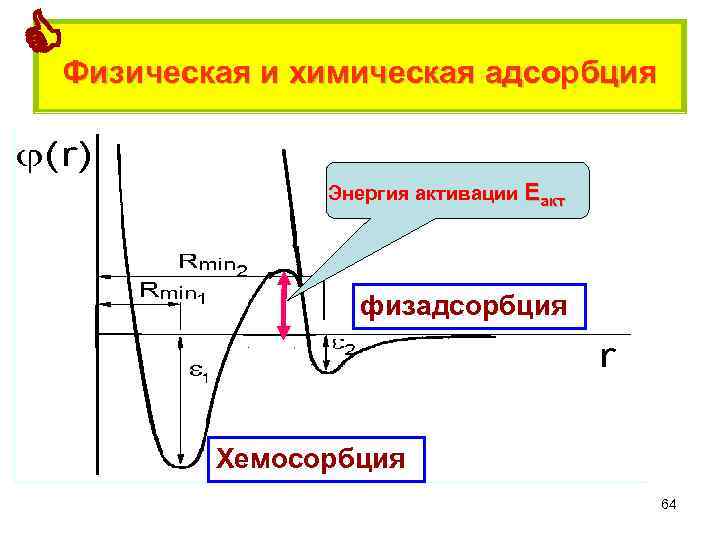
Физическая и химическая адсорбция Энергия активации Еакт физадсорбция Хемосорбция 64
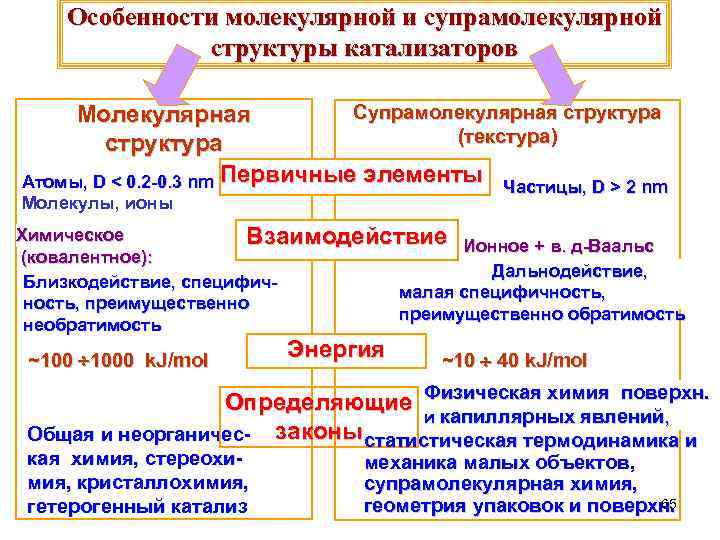
Особенности молекулярной и супрамолекулярной структуры катализаторов Супрамолекулярная структура Moлекулярная (текстура) (текстура структура Атомы, D < 0. 2 -0. 3 nm Первичные элементы Частицы, D > 2 nm Молекулы, ионы Химическое Взаимодействие Ионное + в. д-Ваальс (ковалентное): Дальнодействие, Близкодействие, специфичмалая специфичность, преимущественно обратимость необратимость ~100 1000 k. J/mol Энергия ~10 40 k. J/mol Определяющие Физическая химия поверхн. и капиллярных явлений, Общая и неорганичес- законы статистическая термодинамика и кая химия, стереохимия, кристаллохимия, гетерогенный катализ механика малых объектов, супрамолекулярная химия, 65 геометрия упаковок и поверхн.
Лекция 1 2013 вводная.ppt