Адсорбция_3.ppt
- Количество слайдов: 45

Адсорбция физико–химия поверхностных явлений

Биологические системы - гетерогенны. К поверхностям раздела фаз в организме относятся : • поверхность кожи человека ~1, 5 м 2 • поверхность всех эритроцитов 2500 – 3800 м 2 • поверхность скелета 2000 км 2 • стенки сосудов, мембраны клеток, ядер, митохондрий, слизистые оболочки.

Основные понятия • Сорбция – процесс поглощения одного вещества другим. • Сорбент (адсорбент) – поглотитель. • Сорбтив (адсорбтив) – поглощаемое вещество. • Адсорбция – самопроизвольный процесс накопления (изменения концентрации) вещества на поверхности раздела фаз

Основные понятия • Абсорбция – поглощение всем объемом сорбента ( СО 2 поглощается водой) • Хемосорбция – поглощение вещества за счет химического взаимодействия с адсорбентом • поглощение СО 2 на Са. О =Са. СО 3 О 2 на АL = АL 2 О 3

Поверхности раздела в зависимости от агрегатного состояния фаз : 1 подвижные: жидкость / газ; жидкость / жидкость 2 неподвижные: твердая / газ; твердая / жидкость; твердая / твердая
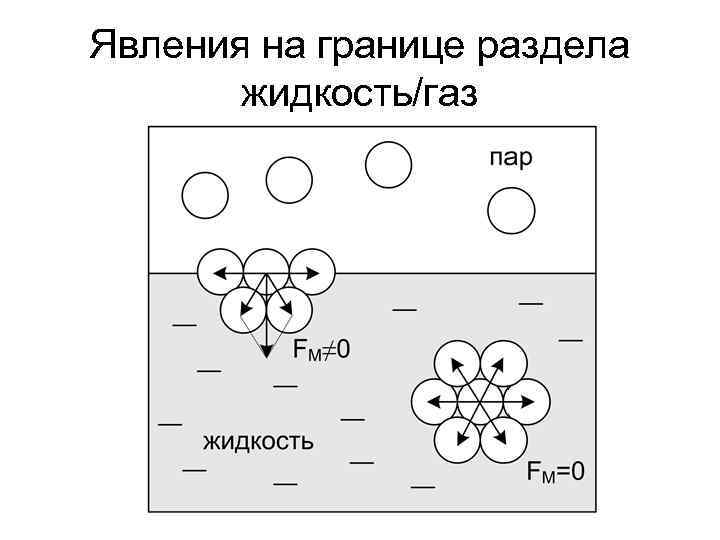
Явления на границе раздела жидкость/газ

Поверхностное натяжение - работа, которую необходимо совершить для образования единицы поверхности (Дж/м 2) GS – поверхностная энергия Гиббса, Дж; S – межфазная поверхность, м 2

Поверхностное натяжение зависит: 1. От природы жидкости Жидкость желчь этанол сыворотка крови вода ртуть σ, м. Дж/м 2 1 22, 3 45, 4 72, 8 436 σорг < σводы σнеорг > σводы 2. От температуры (↑t ↓σ , при tкрит σ =0). 3. От давления (↑p ↓σ ). 4. От концентрации растворенного вещества

Изменение σ используется в диагностике: • изменяется при некоторых заболеваниях ( рак, шок, травма) • влияет на деление клеток, проницаемость клеточных мембран • с возрастом уменьшается для сыворотки крови

Избыточная поверхностная энергия Гиббса GS = σ • S уменьшается: • В чистых растворителях за счет уменьшения S (S => min у шара, поэтому капли дождя, тумана, эмульсии имеют форму шара) • В растворах за счет уменьшения σ путем перераспределения молекул растворенных веществ в объеме и на поверхности

Адсорбция на жидкой поверхности Количественно величину адсорбции на жидкой поверхности вычисляют по уравнению Гиббса Г – количество адсорбированного вещества (моль/м 2) С – молярная концентрация раствора (моль/л) R – универсальная газовая постоянная = 8, 31 Дж/моль • К – поверхностная активность растворенного вещества.

– поверхностная активность – способность растворенных веществ изменять поверхностное натяжение растворителя

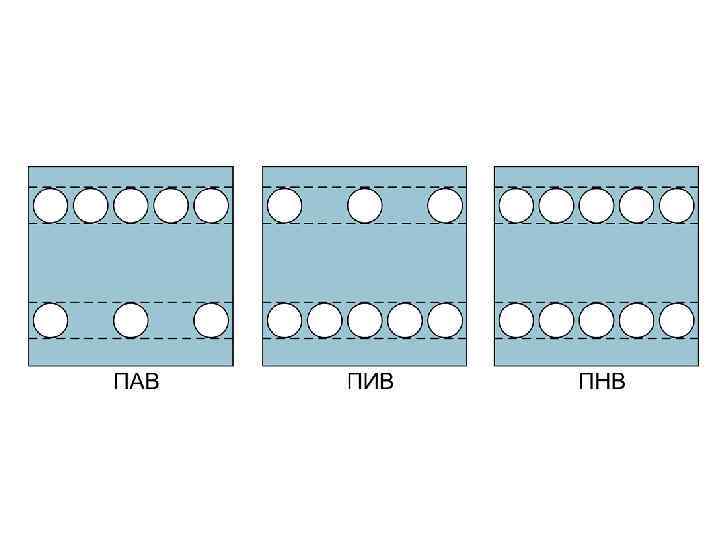
ПАВ Поверхностно-активные вещества (ПАВ) уменьшают σ растворителя, т. к. сами имеют низкие значения σ, меньше, чем у воды. ПАВ : спирты, органические кислоты, сложные эфиры, белки, холестерин, липиды, мыла. σраствора < σрастворителя, Δσ = σраствора – σрастворителя < 0 g > 0, Г > 0, т. е. вещество накапливается в поверхностном слое

ПИВ Поверхностно-инактивные вещества (ПИВ) незначительно повышают σ растворителя ПИВ : неорганические кислоты, соли, основания, глицерин, α – аминокислоты. σраствора > σрастворителя, Δσ = σраствора – σрастворителя > 0 g < 0, Г < 0, т. е. вещество накапливается внутри объема, а не на поверхности

ПНВ Поверхностно-неактивные вещества (ПНВ) не изменяют σ растворителя. ПНВ : сахароза σраствора = σрастворителя, Δσ = 0 g = 0, Г = 0 , т. е. вещество равномерно распределено во всем объеме жидкости.
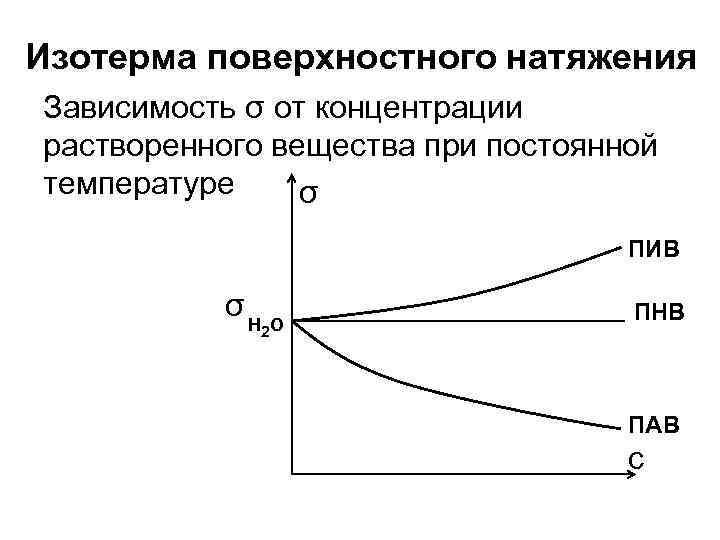
Изотерма поверхностного натяжения Зависимость σ от концентрации растворенного вещества при постоянной температуре σ ПИВ σH O 2 ПНВ ПАВ с
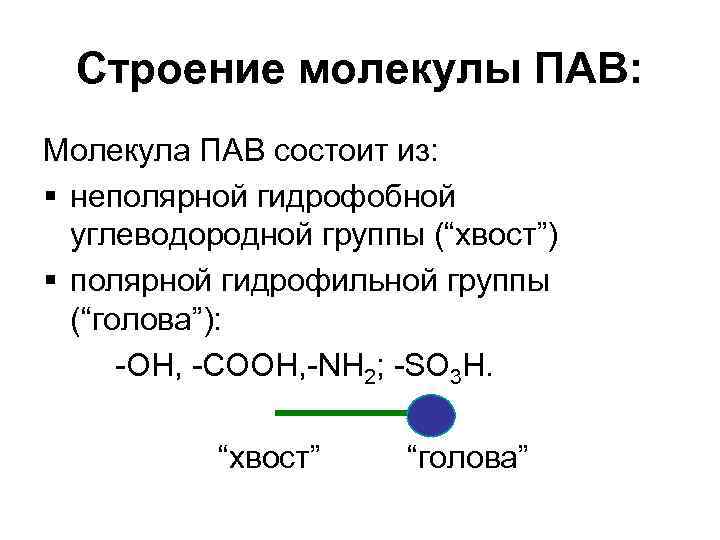
Строение молекулы ПАВ: Молекула ПАВ состоит из: § неполярной гидрофобной углеводородной группы (“хвост”) § полярной гидрофильной группы (“голова”): -ОН, -СООН, -NН 2; -SО 3 H. “хвост” “голова”
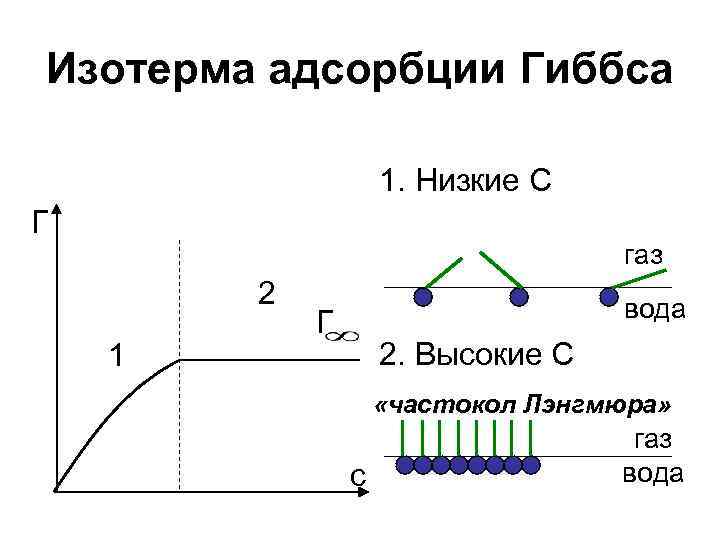
Изотерма адсорбции Гиббса 1. Низкие С Г газ 2 1 вода Г 2. Высокие С «частокол Лэнгмюра» c газ вода
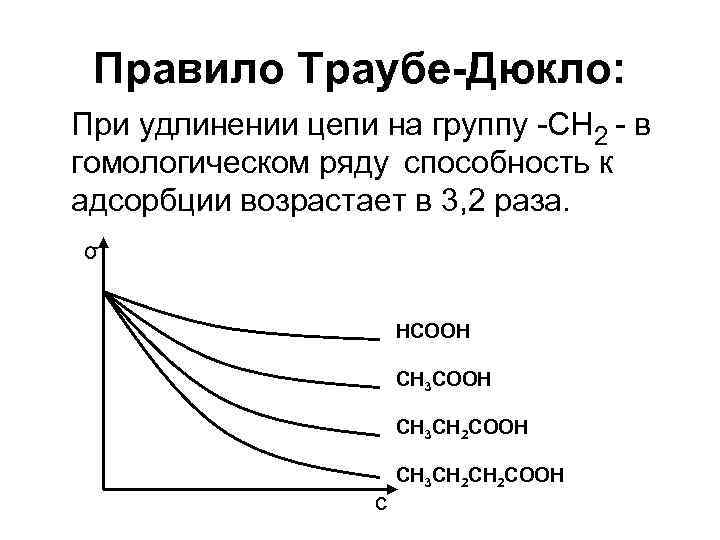
Правило Траубе-Дюкло: При удлинении цепи на группу -СН 2 - в гомологическом ряду способность к адсорбции возрастает в 3, 2 раза. σ НСООН СН 3 СН 2 СООН с СН 3 СН 2 СООН
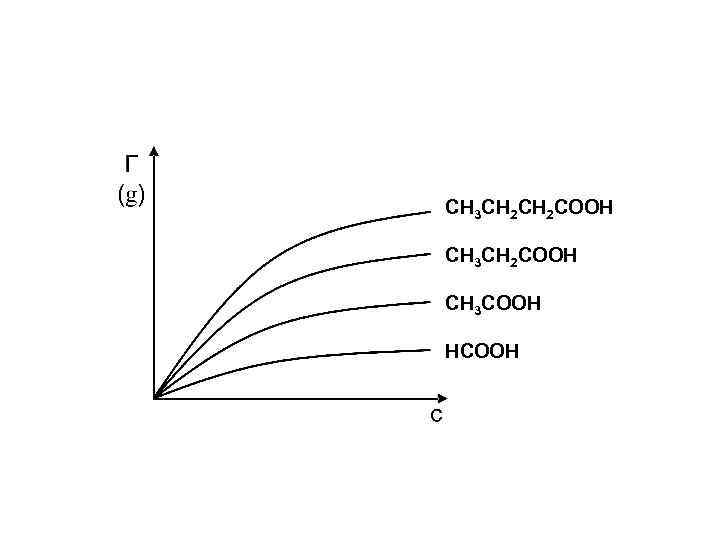
СН 3 СН 2 СООН СН 3 СООН НСООН

Значение ПАВ • В организме липиды, жирные кислоты накапливаются у стенок сосудов, мембран, а затем проникают через них в кровь, в протоплазму. • ПАВ-антисептики накапливаются на поверхности клеточных мембран микроорганизмов, нарушается их проницаемость, клетки гибнут. • Желчь адсорбируется на поверхности жира, ↓σ, дробит жир на капли, превращает в эмульсию, улучшается усвоение пищи.

Адсорбция твердыми телами Величина адсорбции зависит от: 1. Размера поверхности адсорбента чем > Sповерхности, тем > адсорбция. 2. Температуры (↑t ↓Г ). 3. Типа адсорбента, его сродства к растворителю. - гидрофильные адсорбенты (силикагель Si. O 2, глина, пористое стекло) для адсорбции полярных веществ из неполярных (неводных) растворителей. - гидрофобные адсорбенты (активированный уголь, графит, тальк) для адсорбции неполярных веществ из полярных растворителей. 4. Заряда адсорбента и адсорбтива. 5. Концентрации адсорбтива.

Основные положения теории Лэнгмюра • • • Адсорбция идет только на активных центрах (выступах, ребрах) Каждый активный центр удерживает только одну молекулу адсорбтива. При больших концентрациях (давлении) образуется мономолекулярный слой (предельная адсорбция). Адсорбированные молекулы удерживаются доли секунды (время жизни) и отрываются. При равновесии Vадсорбции = Vдесорбции

Уравнение Фрейндлиха • • Г = x/m = КФ · Cn х – количество вещества адсорбтива (моль) m – масса адсорбента С – равновесная концентрация, при которой Vадсорбции = Vдесорбции • КФ – константа Фрейндлиха, КФ = Г при С = 1 моль/л • n – эмпирическая константа, 0, 1– 0, 6.

Уравнение Ленгмюра Г - количество адсорбированного вещества, моль/кг Г∞ - предельная адсорбция С - концентрация Р - давление газа К - константа адсорбционного равновесия
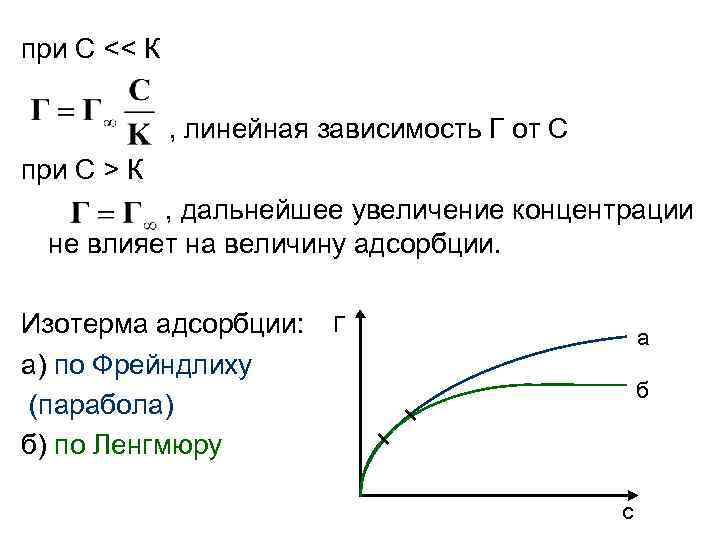
при С << К , линейная зависимость Г от С при С > К , дальнейшее увеличение концентрации не влияет на величину адсорбции. Изотерма адсорбции: а) по Фрейндлиху (парабола) б) по Ленгмюру Г а б с

Адсорбция электролитов Молекулярная (эквивалентная) - характерна для неэлектролитов, слабых электролитов. Ионная (избирательная, ионообменная) - характерна для сильных электролитов

Правило Панета-Фаянса Из раствора адсорбируются те ионы, которые входят в состав кристаллической решетки адсорбента или образуют с ним малорастворимое соединение. Определить знак заряда поверхности Ag. I(крист. ) полученного по реакции: Аg. NО 3(р) + КI(р) = Аg. I(крист. ) + KNO 3(р) а) n. Аg. NО 3 = n. КI : поверхность осадка не заряжена; б) n. Аg. NO 3 > n. КI : в) n. Аg. NО 3 < n. КI : избыток Аg. NO 3 Аg+ + NО 3 избыток КI К+ + IАg. I + + + Аg. I -

В организме избирательная адсорбция токсинов различными тканями: • возбудители столбняка на клетках ЦНС • возбудители дизентерии на клетках вегетативной нервной системы • CN- ионы блокируют дыхательные ферменты

Ионообменная адсорбция – процесс, в котором адсорбент и раствор обмениваются между собой в эквивалентных количествах одноименно заряженными ионами. RM 1 + М 2+ → RM 2 + M 1+ обмен катионов катионит RА 1 + А 2 - → RА 2 + А 1 - обмен анионов анионит

иониты используются: для обессоливания воды для очистки сточных вод для выделения и очистки аминокислот для консервирования крови для восстановления электролитного баланса

Хроматография - динамический метод анализа, основанный на многократно повторяющихся процессах сорбции и десорбции. А+В А В

Хроматография применяется: - разделение смесей аминокислот; - очистка лекарственных препаратов; - количественное определение витаминов, гормонов; - диагностика заболеваний; - анализ крови на присутствие наркотиков, алкоголя - метод для допинг-контроля

Медико-биологическое значение адсорбции: 1. Усвоение питательных и лекарственных веществ 2. Перенос О 2 и СО 2 из лёгких к тканям 3. Действие ферментов 4. Детоксикация организма: а) Гемосорбция - очистка крови б) Лимфосорбция - очистка лимфы. 5. Поглощение ядовитых веществ в желудочнокишечном тракте. 6. Адсорбционная терапия: активированный уголь (КМ, СКН) энтеросорбент (СКН) полисорб МП – кремний, обогащенный О 2

ВЭЖХ Agilent Technologies

ВЭЖХ Милихром

ВЭЖХ HP

ВЭЖХ Люмекс

ВЭЖХ Чешский прибор

ГЖХ

ГЖХ “Agilent Technologies”

ГЖХ “Кристалл”

ГЖХ “Хромос”

ХМС НР
Адсорбция_3.ppt