адсорбция 2 новая.pptx
- Количество слайдов: 24

Адсорбция 1777 – Фонтана. Свежеприготовленный уголь поглощает разные газы Шееле: «воздух, поглощённый углём, при нагревании и выделяется и вновь поглощается при охлаждении» Сосюр 1814 Митгерлих 1848

ТЕРМИН АДСОРБЦИЯ Термин адсорбция (Кайзер 1881 г. ) – концентрирование вещества на границе раздела фаз (твёрдое – газ, твёрдое – жидкость) Адсорбция, абсорбция, капиллярная конденсация в порах Адсорбат адсорбент Сорбция осуществляется за счёт физических сил взаимодействия или хемосорбция
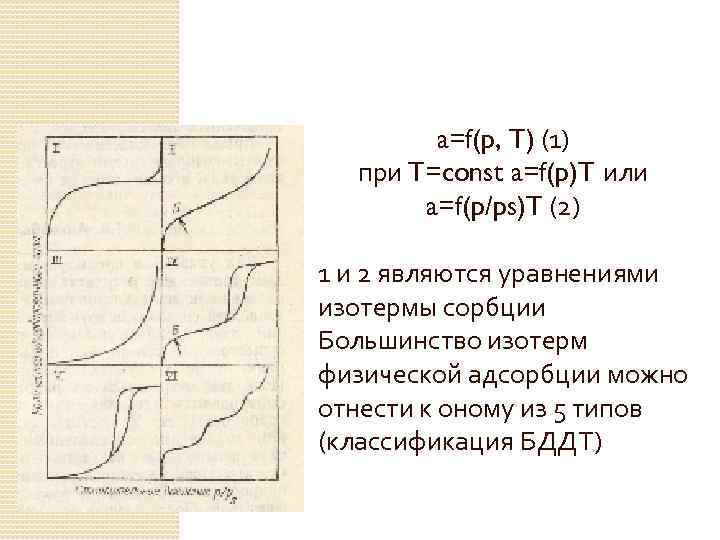
a=f(p, T) (1) при T=const a=f(p)T или a=f(p/ps)T (2) 1 и 2 являются уравнениями изотермы сорбции Большинство изотерм физической адсорбции можно отнести к оному из 5 типов (классификация БДДТ)

ПОВЕРХНОСТЬ РАЗДЕЛА ФАЗ тенденция – к сокращению поверхности твёрдого тела поверхностное натяжение твёрдого тела больше, чем жидкого. σ(Н 2 О)=72, 75 дн/см, σ(С 6 Н 6)=28, 8 дн/см, σ(Ba. SO 4)=310 дн/см Любой процесс, ведущий к уменьшению поверхностной энергии σS , протекает самопроизвольно и ведёт к уменьшению изобарно-изотермического потенциала (ΔG<0). Адсорбированные молекулы могут быть связаны с активными центрами неподвижно, или могут перемещаться вдоль поверхности ΔSгаз>Δsадс т. е. при адсорбции энтропия уменьшается ΔG=ΔH-TΔS <0 <0 т. е. ΔH<0

МЕЖМОЛЕКУЛЯРНЫЕ ВЗАИМОДЕЙСТВИЯ неспецифические Дисперсионные взаимодействия специфические Ø Индукционные взаимодействия, Ø Ориентационные взаимодействия Ø Донорно-акцепторные взаимодействия (водородная связь)

КЛАССИФИКАЦИЯ МОЛЕКУЛ И АДСОРБЕНТОВ А. В. КИСЕЛЁВА молекулы Группа А адсорбенты Тип III Неспецифические взаимодействия, определяемые в основном дисперсионными силами Группа В Группа С Группа D Неспецифические взаимодействия Неспецифические+специфические взаимодействия
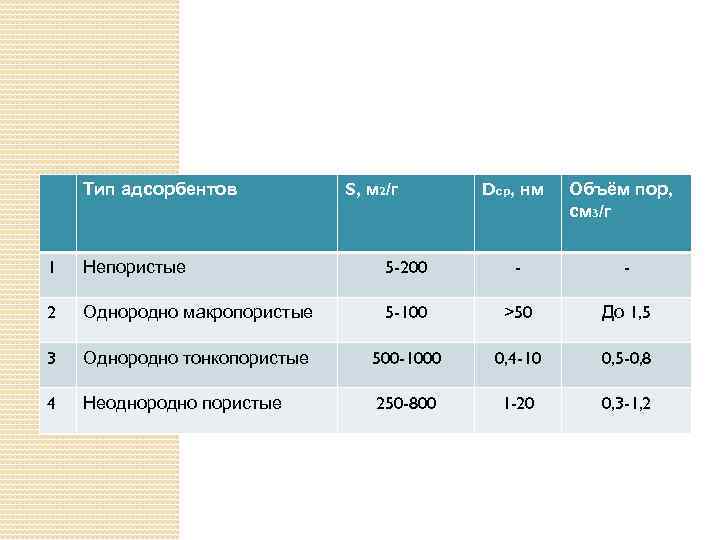
Тип адсорбентов 1 2 S, м 2/г Dср, нм Объём пор, см 3/г КЛАССИФИКАЦИЯ ПО Непористые 5 -200 ГЕОМЕТРИЧЕСКОЙ Однородно макропористые 5 -100 >50 СТРУКТУРЕ До 1, 5 3 Однородно тонкопористые 500 -1000 0, 4 -10 0, 5 -0, 8 4 Неоднородно пористые 250 -800 1 -20 0, 3 -1, 2

ЭНЕРГИЯ АДСОРБЦИОННЫХ СИЛ 1. Адсорбция простых неполярных молекул на неполярных адсорбентах При этом действуют лишь дисперсионные силы притяжения и отталкивания (1) (2) m=9, 1*10 -28 г. с=3, 0*1010 см/сек

(3) Рассмотрим адсорбцию Ar на базисной грани графита (4) (5) чтобы провести дифференцирование величин ∑r-6 и ∑r-12 надо выразить в функции z
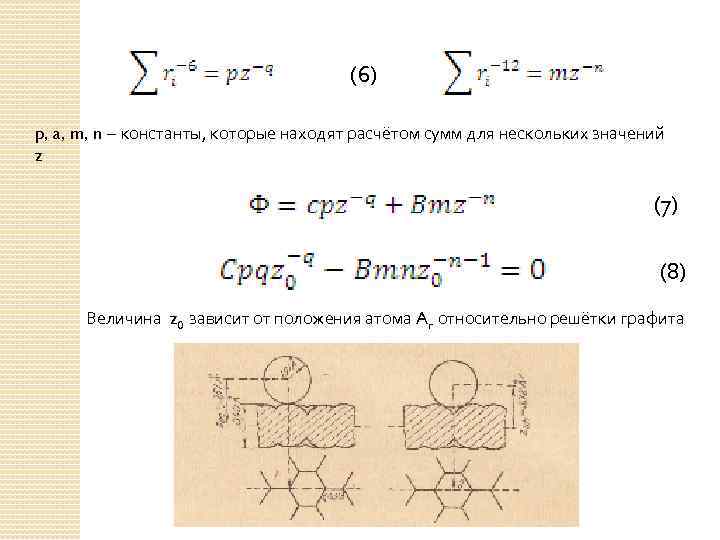
(6) p, a, m, n – константы, которые находят расчётом сумм для нескольких значений z (7) (8) Величина z 0 зависит от положения атома Ar относительно решётки графита
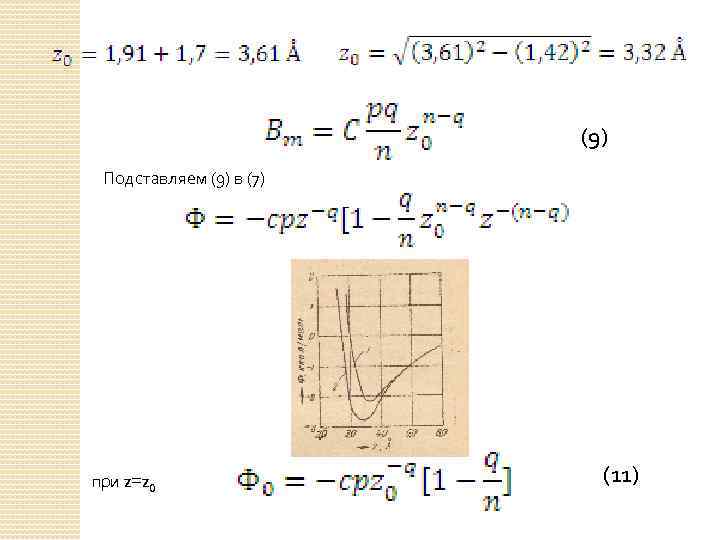
(9) Подставляем (9) в (7) при z=z 0 (11)
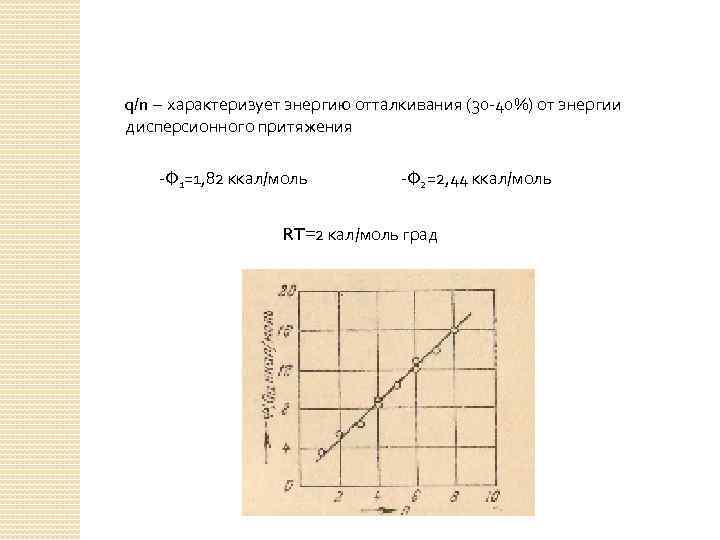
q/n – характеризует энергию отталкивания (30 -40%) от энергии дисперсионного притяжения -Ф 1=1, 82 ккал/моль -Ф 2=2, 44 ккал/моль RT=2 кал/моль град

АДСОРБЦИЯ СЛОЖНЫХ НЕПОЛЯРНЫХ МОЛЕКУЛ НА НЕПОЛЯРНОМ СОРБЕНТЕ н-алканы, звенья СН 3 и СН 2 -Ф=0, 85+1, 88 n ккал/моль

ЭЛЕКТРОСТАТИЧЕСКИЕ СИЛЫ 1) Адсорбция неполярных молекул на поверхности ионных решёток. Возникают индукционные силы взаимодействия, притяжение диполя, индуцированного в молекуле адсорбата электрическим полем, создаваемым решётки сорбента (12) FI зависят от заряда иона, типов решётки и грани. В случае грани [100] – чередование ионов противоположны знаков

2) Адсорбция полярных молекул на неполярном адсорбенте Постоянный дипольный момент адсорбата поляризует атомы адсорбента, т. е. индуцирует в них электрические моменты. Возникает индукционное притяжение, которое добавляется к дисперсионному (13) на графите с поляризуемостью α 1 сорбция сорбата с дипольным моментом μ 2. Предельный случай – сорбция диполей на металлах. .

АДСОРБЦИЯ ПОЛЯРНЫХ МОЛЕКУЛ НА ПОВЕРХНОСТЯХ, ИМЕЮЩИХ ЭЛЕКТРИЧЕСКИЕ ЗАРЯДЫ Возникают ориентационные взаимодействия (кулоновские) v – валентность иона ε – заряд электрона l – расстояние между зарядами

В расчёте на моль При адсорбции спиртов с большим углеводородным радикалом или фенола энергия дисперсионных сил больше энергии электростатического взаимодействия.

Так, например, фенол ориентируется плоскостью бензольного кольца параллельно поверхности адсорбента. Ось диполя оказывается расположенной под углом к направлению электростатического поля поверхности. Водородная связь при адсорбции Если адсорбент содержит –ОН группы, то при адсорбции R-ОН, NH 3 R-NH 2 возникают водородные связи

При водородной связи общая энергия взаимодействия увеличивается Взаимодействие неполярных молекул, обладающих π–электронными связями с ОН-группами и ионами поверхности сорбента Непредельные углеводороды, ароматические углеводороды - это мультидиполи, т. Е. молекула в целом неполярна, однако в некоторых местах распределения электронной плотности является неравномерным. При адсорбции С 2 Н 4 или С 6 Н 6 располагаются на поверхности плоско. Возникают специфические взаимодействия, аналогичные водородной связи. Эта энергия на силикагеле 2 -4 ккал/моль Если брать С 6 Н 14 и С 6 Н 6 и рассмотреть теплоты адсорбции на графитированной саже при одинаковой степени заполнения, то они близки.

Если рассмотреть теплоты адсорбции на силикагеле (гидроксилированная поверхность) или цеолите, то они сильно различаются. Молекулы N 2, CO 2 – обладают большим квадрупольным моментом Для таких молекул, как и для органических соединений с π-связями сорбция зависит от наличия гидроксильных групп или зарядов на поверхности Например: Адсорбаты: А) сферически симметричные оболочки или σ-связи, например, углеводороды Б) π-связи, например ненасыщенные или ароматические углеводороды или свободные пары электронов (эфиры, третичные амины) В) положительные заряды, сосредоточенные на периферии молекул Г) функциональные группы с электронной плотностью или положительным зарядом, сосредоточенном на периферии молекулы с например –ОН или =NH группами
Теплоты адсорбции Q, к. Дж/моль ΔQ Ar N 2 графит. сажа 11, 3 неспец. Полипропилен 6, 7 7, 1 неспец. γ-Al 2 O 3 8, 4 11, 3 2, 9 гидрокс. силикагель 8, 8 11, 7 2, 9
Реальные твёрдые тела Пористые и непористые твёрдые тела
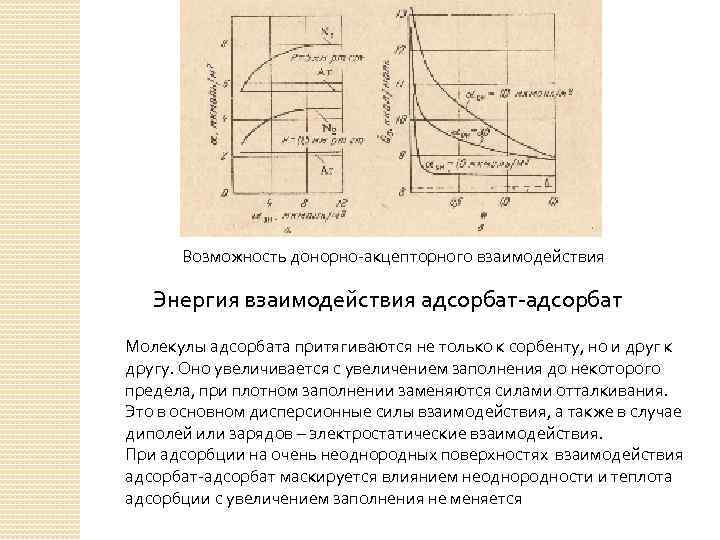
Возможность донорно-акцепторного взаимодействия Энергия взаимодействия адсорбат-адсорбат Молекулы адсорбата притягиваются не только к сорбенту, но и друг к другу. Оно увеличивается с увеличением заполнения до некоторого предела, при плотном заполнении заменяются силами отталкивания. Это в основном дисперсионные силы взаимодействия, а также в случае диполей или зарядов – электростатические взаимодействия. При адсорбции на очень неоднородных поверхностях взаимодействия адсорбат-адсорбат маскируется влиянием неоднородности и теплота адсорбции с увеличением заполнения не меняется

Специфическая и неспецифическая адсорбция Киселёв А. В. разделил адсорбцию на неспецифическую (дисперсионные силы взаимодействия и специфическую (ещё и кулоновские взаимодействия). Адсорбенты на: I графитированная термическа сажа (нет на поверхности никаких групп) II гидроксилированные оксиды. На них сосредоточенн + заряд, например –ОН -группа III на поверхности сосредоточен отрицат. Заряд, например =О; =СО
адсорбция 2 новая.pptx