Ацидоз и алкалоз.pptx
- Количество слайдов: 24
 Ацидоз и алкалоз Выполнила: Антропова Анастасия 121 группа Преподаватель: Сраго И. А.
Ацидоз и алкалоз Выполнила: Антропова Анастасия 121 группа Преподаватель: Сраго И. А.
 Большинство реакций в организме протекает при строго контролируемых значениях p. Н. Буферная система это равновесная система, способная поддерживать примерно на постоянном уровне какой либо параметр при определенных внешних воздействиях. Раствор, содержащий одну или несколько буферных систем, называется буферным раствором.
Большинство реакций в организме протекает при строго контролируемых значениях p. Н. Буферная система это равновесная система, способная поддерживать примерно на постоянном уровне какой либо параметр при определенных внешних воздействиях. Раствор, содержащий одну или несколько буферных систем, называется буферным раствором.
 Буферные системы организма. 1. Гидрокарбонатная система образована оксидом углерода(IV) (кислота) и гидрокарбонат – ионом (сопряженное основание). Уравнение применительно к гидрокарбонатной буферной системе носит название уравнения Гендерсона – Гассельбаха и имеет следующий вид:
Буферные системы организма. 1. Гидрокарбонатная система образована оксидом углерода(IV) (кислота) и гидрокарбонат – ионом (сопряженное основание). Уравнение применительно к гидрокарбонатной буферной системе носит название уравнения Гендерсона – Гассельбаха и имеет следующий вид:
 Если в кровь поступает кислота и увеличивается концентрация иона водорода, то он, взаимодействуя с НСОз, смещает равновесие в сторону Н 2 СО 3 и приводит к выделению газооб разного СО 2 При поступлении в кровь оснований, они связываются угольной кислотой, и равновесие смещается в сторону HCO 3 :
Если в кровь поступает кислота и увеличивается концентрация иона водорода, то он, взаимодействуя с НСОз, смещает равновесие в сторону Н 2 СО 3 и приводит к выделению газооб разного СО 2 При поступлении в кровь оснований, они связываются угольной кислотой, и равновесие смещается в сторону HCO 3 :
 2. Гемоглобиновая система представлена двумя слабыми кислотами – гемоглобином и оксигемоглобином и сопряженными им основания – собственно гемоглобинат – и оксигемоглобинат – ионами. Гемоглобиновый буфер – главная буферная система эритроцитов, на долю которой приходится около 35% всей буферной емкости крови.
2. Гемоглобиновая система представлена двумя слабыми кислотами – гемоглобином и оксигемоглобином и сопряженными им основания – собственно гемоглобинат – и оксигемоглобинат – ионами. Гемоглобиновый буфер – главная буферная система эритроцитов, на долю которой приходится около 35% всей буферной емкости крови.
 3. Фосфатная система функционирует в основном в плазме. Она представлена дигидрофосфат – ионом (кислота) и гидрофосфат – ионом (основание). В отличие от гидрокарбонатной фосфатная система более консервативна, так как избыточные продукты нейтрализации выводятся через почки. 4. Кроме уже указанных, в организме функционируют следующие буферные системы: белковая, аминокислотная и аммиачная (в почках).
3. Фосфатная система функционирует в основном в плазме. Она представлена дигидрофосфат – ионом (кислота) и гидрофосфат – ионом (основание). В отличие от гидрокарбонатной фосфатная система более консервативна, так как избыточные продукты нейтрализации выводятся через почки. 4. Кроме уже указанных, в организме функционируют следующие буферные системы: белковая, аминокислотная и аммиачная (в почках).
 Взаимосвязь буферных систем. Все буферные системы в организме взаимосвязаны!
Взаимосвязь буферных систем. Все буферные системы в организме взаимосвязаны!
 В процессе газообмена в легких кислород поступает в эритроциты, где протекает следующая реакция: По мере перемещения крови в переферические отделы кровеносной системы происходит отдача кислорода ионизированной формой оксигемоглобина: В эритроцитах в присутствии карбоангидразы со значительной скоростью протекает следующая реакция: Образующийся избыток протонов (стадия 3) связывается с гемоглобинат – ионами, образовавшимися на стадии 2, в слабую кислоту:
В процессе газообмена в легких кислород поступает в эритроциты, где протекает следующая реакция: По мере перемещения крови в переферические отделы кровеносной системы происходит отдача кислорода ионизированной формой оксигемоглобина: В эритроцитах в присутствии карбоангидразы со значительной скоростью протекает следующая реакция: Образующийся избыток протонов (стадия 3) связывается с гемоглобинат – ионами, образовавшимися на стадии 2, в слабую кислоту:
 Поступающие в плазму гидрокарбонат – ионы нейтрализуют накапливающийся там избыток протонов, возникающий в результате метаболических процессов: Образовавшийся углекислый газ взаимодействует с компонентами белковой буферной системы: Избыток протонов нейтрализуется фосфатным буфером: После того как кровь вновь попадает в легкие, в ней увеличивается концентрация оксигемоглобина ( стадия 1) , который реагирует с гидрокарбонат – ионами, не диффундировавшими в плазму:
Поступающие в плазму гидрокарбонат – ионы нейтрализуют накапливающийся там избыток протонов, возникающий в результате метаболических процессов: Образовавшийся углекислый газ взаимодействует с компонентами белковой буферной системы: Избыток протонов нейтрализуется фосфатным буфером: После того как кровь вновь попадает в легкие, в ней увеличивается концентрация оксигемоглобина ( стадия 1) , который реагирует с гидрокарбонат – ионами, не диффундировавшими в плазму:
 Буферная емкость (Ва ) – это расчетная величина, равная числу молярных масс эквивалента сильной кислоты или сильного основания, которое нужно добавить к 1 л. Буферного раствора, чтобы р. Н изменился на единицу.
Буферная емкость (Ва ) – это расчетная величина, равная числу молярных масс эквивалента сильной кислоты или сильного основания, которое нужно добавить к 1 л. Буферного раствора, чтобы р. Н изменился на единицу.
 Ацидоз это уменьшение кислотной буферной емкости физиологической системы по сравнению с нормой. Алкалоз это увеличение кислотной буферной емкости физиологической системы по сравнению с нормой. Состояния, характеризующиеся отклонением значения р. Н крови от нормы называют ацидемией ( уменьшение р. Н) и алкалиемией (увеличение р. Н).
Ацидоз это уменьшение кислотной буферной емкости физиологической системы по сравнению с нормой. Алкалоз это увеличение кислотной буферной емкости физиологической системы по сравнению с нормой. Состояния, характеризующиеся отклонением значения р. Н крови от нормы называют ацидемией ( уменьшение р. Н) и алкалиемией (увеличение р. Н).
 Причины нарушения кислотноосновного состояния Увеличение содержания кислот, или уменьшение содержания буферных оснований в системе по сравнению с нормой.
Причины нарушения кислотноосновного состояния Увеличение содержания кислот, или уменьшение содержания буферных оснований в системе по сравнению с нормой.
 Негазовый ацидоз. Экзогенный ацидоз возникает при употреблении излишне кислой пищи (избыточное содержание кислот: лимонной, уксусной и др. ); Эндогенный ацидоз возникает при изменении концентрации протолитически активных продуктов обмена вследствие увеличения синтеза, изменения скорости выведения или потери.
Негазовый ацидоз. Экзогенный ацидоз возникает при употреблении излишне кислой пищи (избыточное содержание кислот: лимонной, уксусной и др. ); Эндогенный ацидоз возникает при изменении концентрации протолитически активных продуктов обмена вследствие увеличения синтеза, изменения скорости выведения или потери.
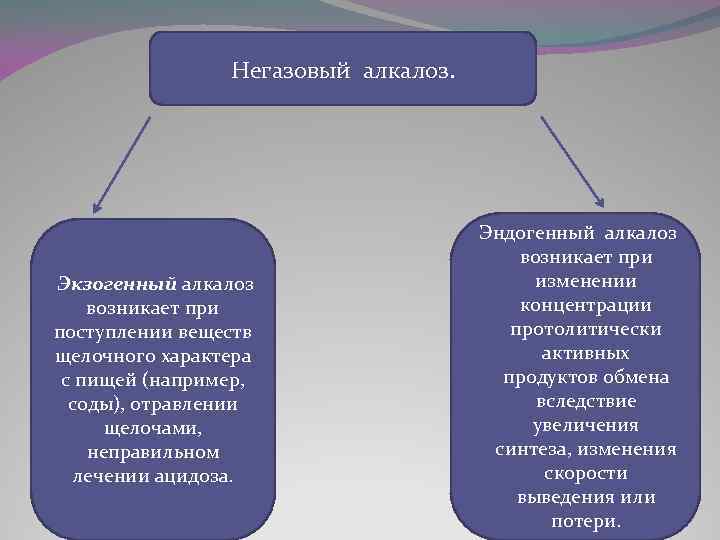 Негазовый алкалоз. Экзогенный алкалоз возникает при поступлении веществ щелочного характера с пищей (например, соды), отравлении щелочами, неправильном лечении ацидоза. Эндогенный алкалоз возникает при изменении концентрации протолитически активных продуктов обмена вследствие увеличения синтеза, изменения скорости выведения или потери.
Негазовый алкалоз. Экзогенный алкалоз возникает при поступлении веществ щелочного характера с пищей (например, соды), отравлении щелочами, неправильном лечении ацидоза. Эндогенный алкалоз возникает при изменении концентрации протолитически активных продуктов обмена вследствие увеличения синтеза, изменения скорости выведения или потери.
 Ацидоз и алкалоз. Компенсированный Некомпесированный Изменение значения р. Н крови на 0, 6 единицы в любую сторону приводит к летальному исходу!
Ацидоз и алкалоз. Компенсированный Некомпесированный Изменение значения р. Н крови на 0, 6 единицы в любую сторону приводит к летальному исходу!
 При компенсированном ацидозе (алкалозе), несмотря на отклонения от нормы кислотной буферной емкости, р. Н крови сохраняет значение в пределах 7, 35 < р. Н < 7, 45. Некомпенсированный ацидоз сопровождается уменьшением кислотной буферной емкости и снижением р. Н крови (6, 8 < р. Н < 7, 35), а некомпенсированный алкалоз увеличением кислотной буферной емкости и повышением р. Н крови (7, 45 < р. Н < 7, 9). Снижение р. Н крови по сравнению с нормой называется ацидемией, а повышение р. Н крови алкалиемией.
При компенсированном ацидозе (алкалозе), несмотря на отклонения от нормы кислотной буферной емкости, р. Н крови сохраняет значение в пределах 7, 35 < р. Н < 7, 45. Некомпенсированный ацидоз сопровождается уменьшением кислотной буферной емкости и снижением р. Н крови (6, 8 < р. Н < 7, 35), а некомпенсированный алкалоз увеличением кислотной буферной емкости и повышением р. Н крови (7, 45 < р. Н < 7, 9). Снижение р. Н крови по сравнению с нормой называется ацидемией, а повышение р. Н крови алкалиемией.
 Метаболические показатели, характеризующие кислотноосновное состояние крови Величина р. Н плазмы крови 7, 35 < р. Н < 7, 45.
Метаболические показатели, характеризующие кислотноосновное состояние крови Величина р. Н плазмы крови 7, 35 < р. Н < 7, 45.
 Парциальное напряжение углекислоты p(СО 2) = (40 + 5) мм рт. ст. (5, 3 к. Па). Предельные значения парциального давления С 02 составляют при алкалозе 10 мм рт. ст. , а при ацидозе 130 мм рт. ст.
Парциальное напряжение углекислоты p(СО 2) = (40 + 5) мм рт. ст. (5, 3 к. Па). Предельные значения парциального давления С 02 составляют при алкалозе 10 мм рт. ст. , а при ацидозе 130 мм рт. ст.
 Содержание буферных оснований в плазме крови (ВВ) нормальное значение для плазмы ВВ = (42 ± 3) ммоль/л
Содержание буферных оснований в плазме крови (ВВ) нормальное значение для плазмы ВВ = (42 ± 3) ммоль/л
 Виды первичного нарушения кислотноосновного баланса Метаболический ацидоз. Причины: нарушение кровообращения, кислородное голодание тка ней, диарея (понос), нарушение выделительной функции почек, диабет. Метаболический алкалоз. Причины: неукротимая рвота, удаление кислых продуктов из же лудка, запор (накопление щелочных продуктов в кишечнике), дли тельный прием щелочной пищи и минеральной воды.
Виды первичного нарушения кислотноосновного баланса Метаболический ацидоз. Причины: нарушение кровообращения, кислородное голодание тка ней, диарея (понос), нарушение выделительной функции почек, диабет. Метаболический алкалоз. Причины: неукротимая рвота, удаление кислых продуктов из же лудка, запор (накопление щелочных продуктов в кишечнике), дли тельный прием щелочной пищи и минеральной воды.
 Респираторный (газовый) ацидоз Причины: заболевания органов дыхания, гиповентиляция легких, угнетение дыхательного центра некоторыми препаратами, например барбитуратами. Респираторный (газовый) алкалоз Причины: вдыхание разреженного воздуха, чрезмерное возбужде ние дыхательного
Респираторный (газовый) ацидоз Причины: заболевания органов дыхания, гиповентиляция легких, угнетение дыхательного центра некоторыми препаратами, например барбитуратами. Респираторный (газовый) алкалоз Причины: вдыхание разреженного воздуха, чрезмерное возбужде ние дыхательного
 Коррекция кислотно – основногого состояния организма В качестве экстренной меры при ацидозе применяют внутривенное вливание растворов гидрокарбоната натрия Трисамин эффективен только при внутривенном введении. В качестве средства, корригирующего ацидоз, используется также лактат натрия в виде 11% раствора для внутривенного введения.
Коррекция кислотно – основногого состояния организма В качестве экстренной меры при ацидозе применяют внутривенное вливание растворов гидрокарбоната натрия Трисамин эффективен только при внутривенном введении. В качестве средства, корригирующего ацидоз, используется также лактат натрия в виде 11% раствора для внутривенного введения.
 Для устранения алкалоза в некоторых случаях вводят 5% раствор аскорбиновой кислоты. При пониженной кислотности желудочного сока назначают разбавленную соляную кислоту, при повышенной кислотности – различные антацидные препараты. В основе фармакологического действия всех перечисленных средств лежит реакция нейтрализации!
Для устранения алкалоза в некоторых случаях вводят 5% раствор аскорбиновой кислоты. При пониженной кислотности желудочного сока назначают разбавленную соляную кислоту, при повышенной кислотности – различные антацидные препараты. В основе фармакологического действия всех перечисленных средств лежит реакция нейтрализации!
 За счет сбалансированности процессов поступления и выведе ния кислот и оснований, а также за счет равновесного характе ра протолитических процессов, определяющих взаимодействие этих двух противоположностей, в организме поддерживается состояние протолитического (кислотно основного) гомеостаза, то есть нашего хорошего самочувствия!
За счет сбалансированности процессов поступления и выведе ния кислот и оснований, а также за счет равновесного характе ра протолитических процессов, определяющих взаимодействие этих двух противоположностей, в организме поддерживается состояние протолитического (кислотно основного) гомеостаза, то есть нашего хорошего самочувствия!


