Лекция 7 ацетилен.pptx
- Количество слайдов: 36
 Ацетилен и синтезы на его основе Производство ацетилена из карбида кальция Лекция 9 Лектор: доцент каф. НХТ, к. т. н. Давыдова О. В.
Ацетилен и синтезы на его основе Производство ацетилена из карбида кальция Лекция 9 Лектор: доцент каф. НХТ, к. т. н. Давыдова О. В.
 Общие сведения Ацетиле н (по ИЮПАК — этин) — СН≡СН первый член ряда ацетиленовых углеводородов, содержащих реакционноспособную тройную связь между углеродными атомами. Впервые СН≡СН получил в 1836 г. Эдмунд Дэви, действем воды на карбид калия: К 2 С 2 + 2 Н 2 О С 2 Н 2 + 2 КОН Новый газ он назвал двууглеродистым водородом. СН≡СН - бесцветный газ, обладающий слабым эфирным запахом. Ткип= 83, 8ºС; Ткрит= +35, 5ºС; Ркрит= -61, 6 атм.
Общие сведения Ацетиле н (по ИЮПАК — этин) — СН≡СН первый член ряда ацетиленовых углеводородов, содержащих реакционноспособную тройную связь между углеродными атомами. Впервые СН≡СН получил в 1836 г. Эдмунд Дэви, действем воды на карбид калия: К 2 С 2 + 2 Н 2 О С 2 Н 2 + 2 КОН Новый газ он назвал двууглеродистым водородом. СН≡СН - бесцветный газ, обладающий слабым эфирным запахом. Ткип= 83, 8ºС; Ткрит= +35, 5ºС; Ркрит= -61, 6 атм.
 Общие сведения o Ацетилен образует с воздухом взрывоопасные смеси от 2 до 81 % об. , в связи с этим нельзя допускать проникновения ацетилена в атмосферу производственных помещений и необходимо исключить попадание воздуха в технологическую аппаратуру и трубопроводы, содержащие ацетилен. В отличие от многих газообразных углеводородов и Н 2 ацетилен хорошо растворим в Н 2 О: в 1 объёме Н 2 О при 20ºС растворяется 1 объём ацетилена. o Значительно лучше растворяется в органических веществах (в объёмах газа на 1 объём жидкости): бензин – 5 ДМФА – 32 СН 3 ОН – 15, 5 ацетон – 23 N-метилпирролидон – 39
Общие сведения o Ацетилен образует с воздухом взрывоопасные смеси от 2 до 81 % об. , в связи с этим нельзя допускать проникновения ацетилена в атмосферу производственных помещений и необходимо исключить попадание воздуха в технологическую аппаратуру и трубопроводы, содержащие ацетилен. В отличие от многих газообразных углеводородов и Н 2 ацетилен хорошо растворим в Н 2 О: в 1 объёме Н 2 О при 20ºС растворяется 1 объём ацетилена. o Значительно лучше растворяется в органических веществах (в объёмах газа на 1 объём жидкости): бензин – 5 ДМФА – 32 СН 3 ОН – 15, 5 ацетон – 23 N-метилпирролидон – 39
 Общие сведения o Благодаря высокой растворимости ацетилена в ацетоне можно хранить и транспортировать этот газ в баллонах в сжатом состоянии, что не возможно для чистого ацетилена ввиду его взрывоопасности. В ацетиленовых баллонах имеется насадка из активированного угля, обильно пропитанного ацетоном. o Ацетилен в виде раствора в ацетоне находится в баллоне под давлением 15 атм.
Общие сведения o Благодаря высокой растворимости ацетилена в ацетоне можно хранить и транспортировать этот газ в баллонах в сжатом состоянии, что не возможно для чистого ацетилена ввиду его взрывоопасности. В ацетиленовых баллонах имеется насадка из активированного угля, обильно пропитанного ацетоном. o Ацетилен в виде раствора в ацетоне находится в баллоне под давлением 15 атм.
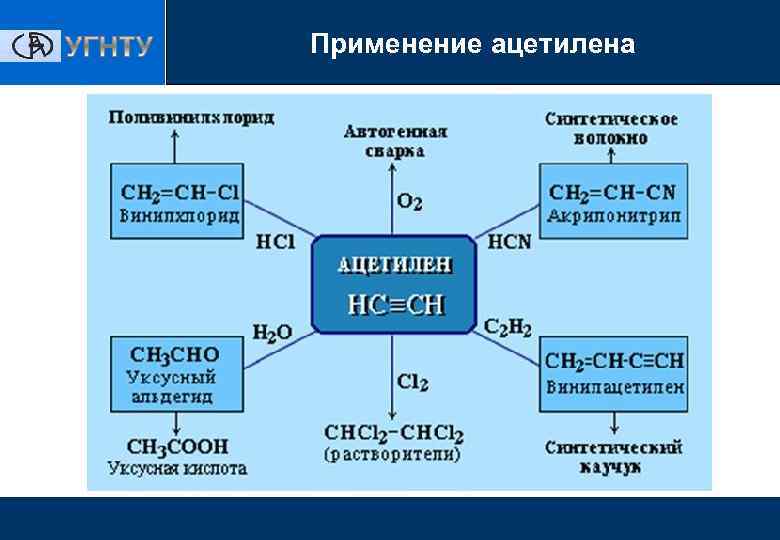 Применение ацетилена
Применение ацетилена
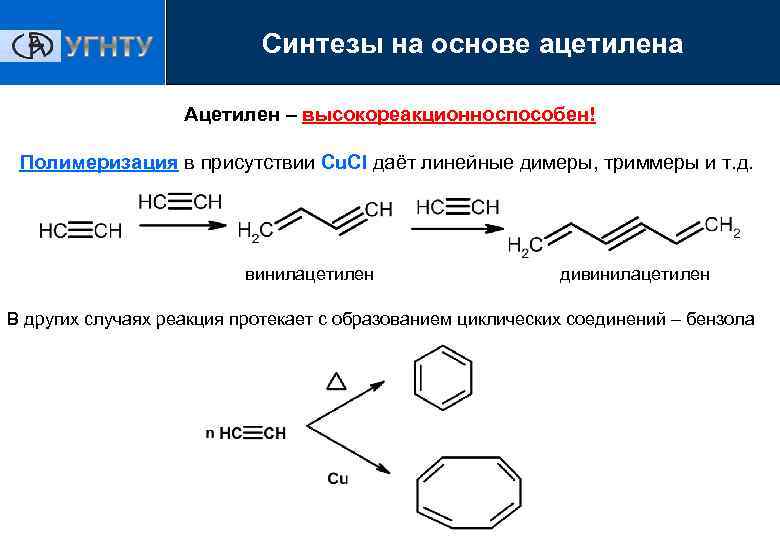 Синтезы на основе ацетилена Ацетилен – высокореакционноспособен! Полимеризация в присутствии Cu. Cl даёт линейные димеры, триммеры и т. д. винилацетилен дивинилацетилен В других случаях реакция протекает с образованием циклических соединений – бензола
Синтезы на основе ацетилена Ацетилен – высокореакционноспособен! Полимеризация в присутствии Cu. Cl даёт линейные димеры, триммеры и т. д. винилацетилен дивинилацетилен В других случаях реакция протекает с образованием циклических соединений – бензола
 Синтезы на основе ацетилена Хлорирование: Симм-тетрахлорэтан используют для синтеза трихлорэтилена и тетрахлорэтилена. Гидрохлорирование: Хлорвини л — органическое вещество; бесцветный газ со слабым сладковатым запахом, представляющий собой простейшее хлорпроизводное этилена. Вещество является чрезвычайно огне- и взрывоопасным, выделяя при горении токсичные вещества.
Синтезы на основе ацетилена Хлорирование: Симм-тетрахлорэтан используют для синтеза трихлорэтилена и тетрахлорэтилена. Гидрохлорирование: Хлорвини л — органическое вещество; бесцветный газ со слабым сладковатым запахом, представляющий собой простейшее хлорпроизводное этилена. Вещество является чрезвычайно огне- и взрывоопасным, выделяя при горении токсичные вещества.
 Синтезы на основе ацетилена Гидратация: Ацетальдеги д (уксусный альдегид) — один из наиболее важных альдегидов, широко встречающийся в природе и производящийся в больших количествах индустриально. Получают уксусный альдегид гидратацией ацетилена в присутствии солей ртути (реакция Кучерова), с образованием енола, который изомеризуется в альдегид. Этот метод раньше доминировал до появления процесса Вакера с окислением или дегидрированием этилового спирта на медном или серебряном катализаторе.
Синтезы на основе ацетилена Гидратация: Ацетальдеги д (уксусный альдегид) — один из наиболее важных альдегидов, широко встречающийся в природе и производящийся в больших количествах индустриально. Получают уксусный альдегид гидратацией ацетилена в присутствии солей ртути (реакция Кучерова), с образованием енола, который изомеризуется в альдегид. Этот метод раньше доминировал до появления процесса Вакера с окислением или дегидрированием этилового спирта на медном или серебряном катализаторе.
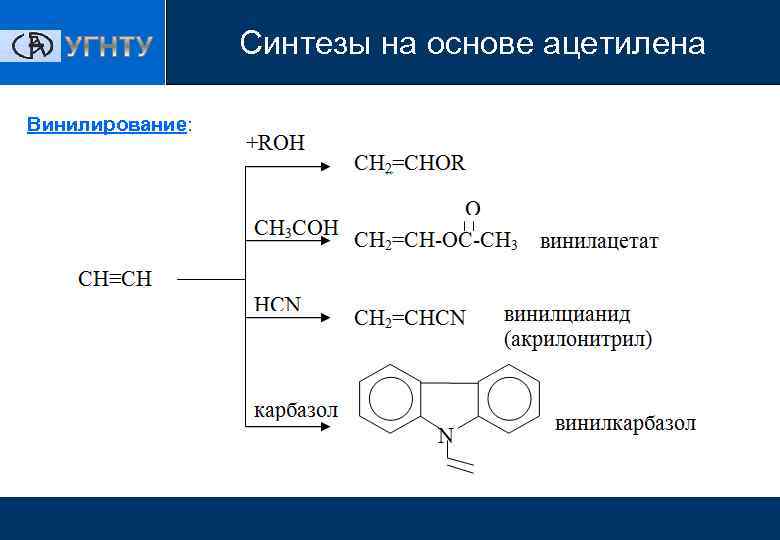 Синтезы на основе ацетилена Винилирование:
Синтезы на основе ацетилена Винилирование:
 Синтезы на основе ацетилена Конденсация с карбонильными соединениями: Нитрование азотной кислотой : идёт с расщеплением тройной связи
Синтезы на основе ацетилена Конденсация с карбонильными соединениями: Нитрование азотной кислотой : идёт с расщеплением тройной связи
 Получение ацетилена из карбида кальция Промышленный метод получения ацетилена из Ca. C 2 существует с конца XIX века, актуален и сейчас. Ca. C 2 получают из негашеной извести Са. О и кокса в электродуговых печах: Реакция сильно эндотермичная, что составляет существенный элемент в себестоимости производимого ацетилена. При разложении водой карбида кальция по экзотермической реакции получают ацетилен: Из реакционной зоны нужно постоянно отводить тепло, чтобы исключить разложение и полимеризацию ацетилена. Из 1 кг Ca. C 2 получают 230÷ 280 л CH≡CH, теоретически должно быть – 380 л.
Получение ацетилена из карбида кальция Промышленный метод получения ацетилена из Ca. C 2 существует с конца XIX века, актуален и сейчас. Ca. C 2 получают из негашеной извести Са. О и кокса в электродуговых печах: Реакция сильно эндотермичная, что составляет существенный элемент в себестоимости производимого ацетилена. При разложении водой карбида кальция по экзотермической реакции получают ацетилен: Из реакционной зоны нужно постоянно отводить тепло, чтобы исключить разложение и полимеризацию ацетилена. Из 1 кг Ca. C 2 получают 230÷ 280 л CH≡CH, теоретически должно быть – 380 л.
 Ацетиленовые генераторы По принципу отвода тепла генераторы ацетилена можно разделить на две группы: 1. «Мокрого» типа: реакционное тепло воспринимается избыточной водой, нагревающейся до 50 -60°С. На 1 кг Са. С 2 расходуется 10 кг воды, при этом Са(ОН)2 образуется в виде малопригодной для утилизации суспензии. 2. «Сухого» типа: тепло отводится небольшим количеством избыточной воды за счёт её испарения. Са(ОН)2 получается в виде извести-пушонки, которую используют для приготовления строительных материалов.
Ацетиленовые генераторы По принципу отвода тепла генераторы ацетилена можно разделить на две группы: 1. «Мокрого» типа: реакционное тепло воспринимается избыточной водой, нагревающейся до 50 -60°С. На 1 кг Са. С 2 расходуется 10 кг воды, при этом Са(ОН)2 образуется в виде малопригодной для утилизации суспензии. 2. «Сухого» типа: тепло отводится небольшим количеством избыточной воды за счёт её испарения. Са(ОН)2 получается в виде извести-пушонки, которую используют для приготовления строительных материалов.
 Ацетиленовые генераторы Генераторы «мокрого» типа делят по способу загрузки реагентов на следующие системы: «карбид в воду» , «вода на карбид» и контактные, в которых вода и карбид кальция находятся в постоянном соприкосновении. Наиболее безопасными и применимыми для производства ацетилена в крупных масштабах являются генераторы типа «карбид в воду» . В этих аппаратах куски карбида сразу погружаются в избыток воды, чем исключаются перегревы и создаются условия для лучшего отвода реакционного тепла. Производительность генераторов «карбид в воду» – до 500 м 3/ч.
Ацетиленовые генераторы Генераторы «мокрого» типа делят по способу загрузки реагентов на следующие системы: «карбид в воду» , «вода на карбид» и контактные, в которых вода и карбид кальция находятся в постоянном соприкосновении. Наиболее безопасными и применимыми для производства ацетилена в крупных масштабах являются генераторы типа «карбид в воду» . В этих аппаратах куски карбида сразу погружаются в избыток воды, чем исключаются перегревы и создаются условия для лучшего отвода реакционного тепла. Производительность генераторов «карбид в воду» – до 500 м 3/ч.
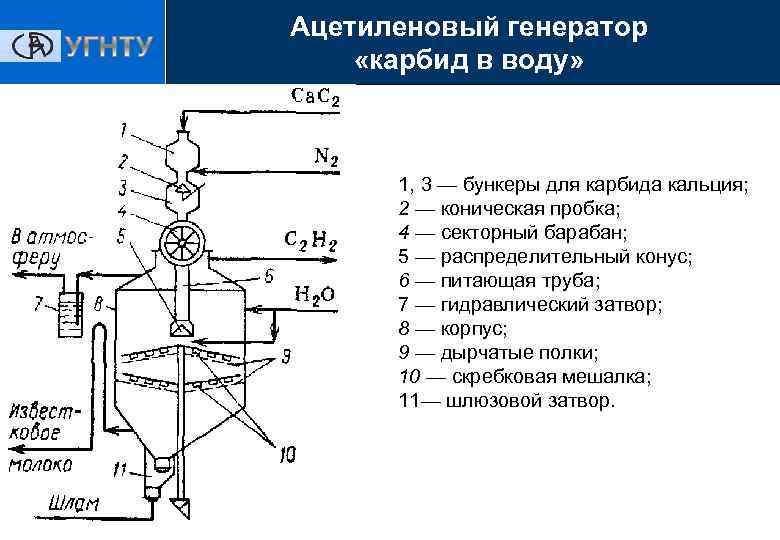 Ацетиленовый генератор «карбид в воду» 1, 3 — бункеры для карбида кальция; 2 — коническая пробка; 4 — секторный барабан; 5 — распределительный конус; 6 — питающая труба; 7 — гидравлический затвор; 8 — корпус; 9 — дырчатые полки; 10 — скребковая мешалка; 11— шлюзовой затвор.
Ацетиленовый генератор «карбид в воду» 1, 3 — бункеры для карбида кальция; 2 — коническая пробка; 4 — секторный барабан; 5 — распределительный конус; 6 — питающая труба; 7 — гидравлический затвор; 8 — корпус; 9 — дырчатые полки; 10 — скребковая мешалка; 11— шлюзовой затвор.
 Ацетиленовые генераторы Мощность у «сухих» генераторов больше, чем у генераторов «мокрого типа» . В них перерабатывают карбидную мелочь. Основным условием их успешной работы является тесный контакт между частицами карбида кальция и небольшим количеством воды. Это достигается введением воды через специальные разбрызгиватели и наличием в генераторе перемешивающих устройств (вращающиеся барабаны, скребковые мешалки). Благодаря этому исключается перегрев ацетилена и поддерживается равномерная температура 110— 115°С.
Ацетиленовые генераторы Мощность у «сухих» генераторов больше, чем у генераторов «мокрого типа» . В них перерабатывают карбидную мелочь. Основным условием их успешной работы является тесный контакт между частицами карбида кальция и небольшим количеством воды. Это достигается введением воды через специальные разбрызгиватели и наличием в генераторе перемешивающих устройств (вращающиеся барабаны, скребковые мешалки). Благодаря этому исключается перегрев ацетилена и поддерживается равномерная температура 110— 115°С.
 Примеси и очистка ацетилена Ацетилен, полученный карбидным методом, имеет высокую концентрацию (свыше 99 % об. ), но содержит небольшие примеси NH 3, H 2 S, фосфористого водорода и др. Они образуются при разложении водой соединений, всегда присутствующих в Са. С 2: нитридов, сульфидов и фосфидов Са и др. металлов: Присутствие этих веществ не допустимо при химической переработке ацетилена. Раньше очистку проводили «сухим» методом» , пропуская ацетилен через твёрдую очистительную массу «гератол» - Ge. O 3, который окислял примеси в сульфаты, фосфаты и т. д. Известен так же «мокрый» способ, заключающийся в промывке ацетилена в насадочных скрубберах. Для этого используют гипохлорит Na:
Примеси и очистка ацетилена Ацетилен, полученный карбидным методом, имеет высокую концентрацию (свыше 99 % об. ), но содержит небольшие примеси NH 3, H 2 S, фосфористого водорода и др. Они образуются при разложении водой соединений, всегда присутствующих в Са. С 2: нитридов, сульфидов и фосфидов Са и др. металлов: Присутствие этих веществ не допустимо при химической переработке ацетилена. Раньше очистку проводили «сухим» методом» , пропуская ацетилен через твёрдую очистительную массу «гератол» - Ge. O 3, который окислял примеси в сульфаты, фосфаты и т. д. Известен так же «мокрый» способ, заключающийся в промывке ацетилена в насадочных скрубберах. Для этого используют гипохлорит Na:
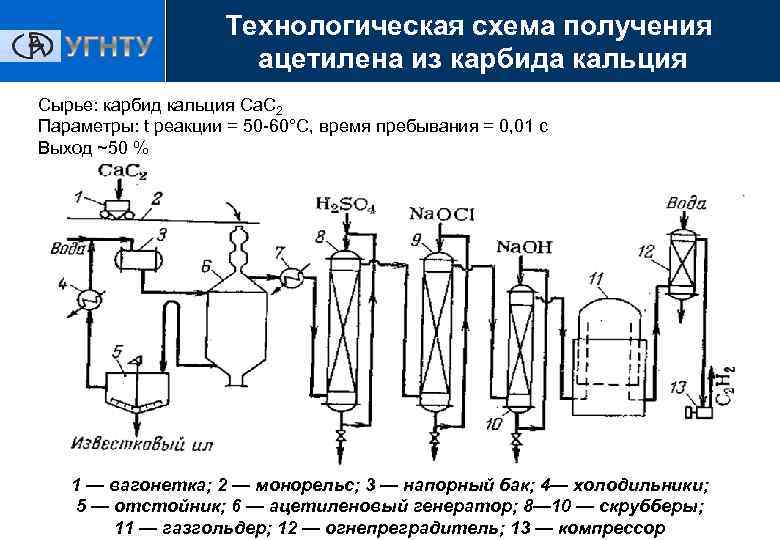 Технологическая схема получения ацетилена из карбида кальция Сырье: карбид кальция Ca. C 2 Параметры: t реакции = 50 -60°С, время пребывания = 0, 01 с Выход ~50 % 1 — вагонетка; 2 — монорельс; 3 — напорный бак; 4— холодильники; 5 — отстойник; 6 — ацетиленовый генератор; 8— 10 — скрубберы; 11 — газгольдер; 12 — огнепреградитель; 13 — компрессор
Технологическая схема получения ацетилена из карбида кальция Сырье: карбид кальция Ca. C 2 Параметры: t реакции = 50 -60°С, время пребывания = 0, 01 с Выход ~50 % 1 — вагонетка; 2 — монорельс; 3 — напорный бак; 4— холодильники; 5 — отстойник; 6 — ацетиленовый генератор; 8— 10 — скрубберы; 11 — газгольдер; 12 — огнепреградитель; 13 — компрессор
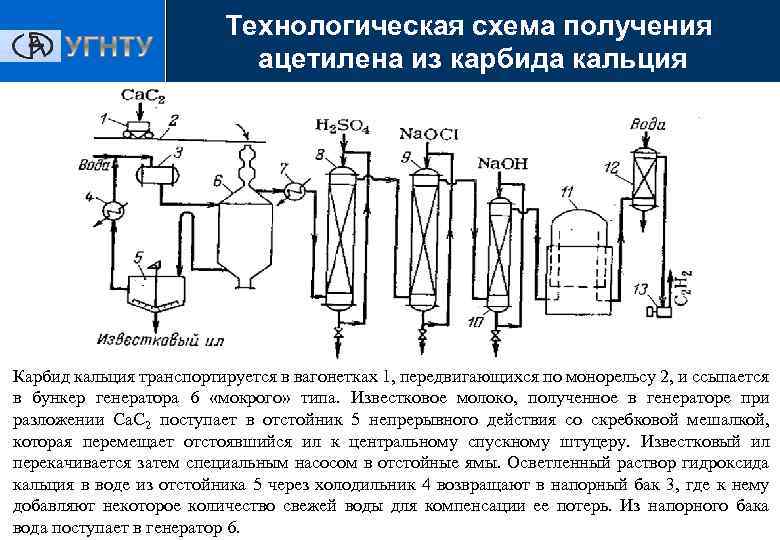 Технологическая схема получения ацетилена из карбида кальция Карбид кальция транспортируется в вагонетках 1, передвигающихся по монорельсу 2, и ссыпается в бункер генератора 6 «мокрого» типа. Известковое молоко, полученное в генераторе при разложении Са. С 2 поступает в отстойник 5 непрерывного действия со скребковой мешалкой, которая перемещает отстоявшийся ил к центральному спускному штуцеру. Известковый ил перекачивается затем специальным насосом в отстойные ямы. Осветленный раствор гидроксида кальция в воде из отстойника 5 через холодильник 4 возвращают в напорный бак 3, где к нему добавляют некоторое количество свежей воды для компенсации ее потерь. Из напорного бака вода поступает в генератор 6.
Технологическая схема получения ацетилена из карбида кальция Карбид кальция транспортируется в вагонетках 1, передвигающихся по монорельсу 2, и ссыпается в бункер генератора 6 «мокрого» типа. Известковое молоко, полученное в генераторе при разложении Са. С 2 поступает в отстойник 5 непрерывного действия со скребковой мешалкой, которая перемещает отстоявшийся ил к центральному спускному штуцеру. Известковый ил перекачивается затем специальным насосом в отстойные ямы. Осветленный раствор гидроксида кальция в воде из отстойника 5 через холодильник 4 возвращают в напорный бак 3, где к нему добавляют некоторое количество свежей воды для компенсации ее потерь. Из напорного бака вода поступает в генератор 6.
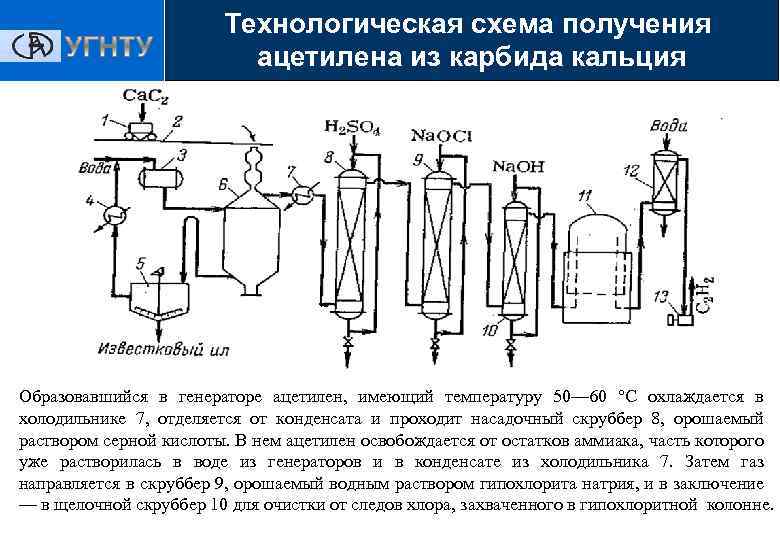 Технологическая схема получения ацетилена из карбида кальция Образовавшийся в генераторе ацетилен, имеющий температуру 50— 60 °С охлаждается в холодильнике 7, отделяется от конденсата и проходит насадочный скруббер 8, орошаемый раствором серной кислоты. В нем ацетилен освобождается от остатков аммиака, часть которого уже растворилась в воде из генераторов и в конденсате из холодильника 7. Затем газ направляется в скруббер 9, орошаемый водным раствором гипохлорита натрия, и в заключение — в щелочной скруббер 10 для очистки от следов хлора, захваченного в гипохлоритной колонне.
Технологическая схема получения ацетилена из карбида кальция Образовавшийся в генераторе ацетилен, имеющий температуру 50— 60 °С охлаждается в холодильнике 7, отделяется от конденсата и проходит насадочный скруббер 8, орошаемый раствором серной кислоты. В нем ацетилен освобождается от остатков аммиака, часть которого уже растворилась в воде из генераторов и в конденсате из холодильника 7. Затем газ направляется в скруббер 9, орошаемый водным раствором гипохлорита натрия, и в заключение — в щелочной скруббер 10 для очистки от следов хлора, захваченного в гипохлоритной колонне.
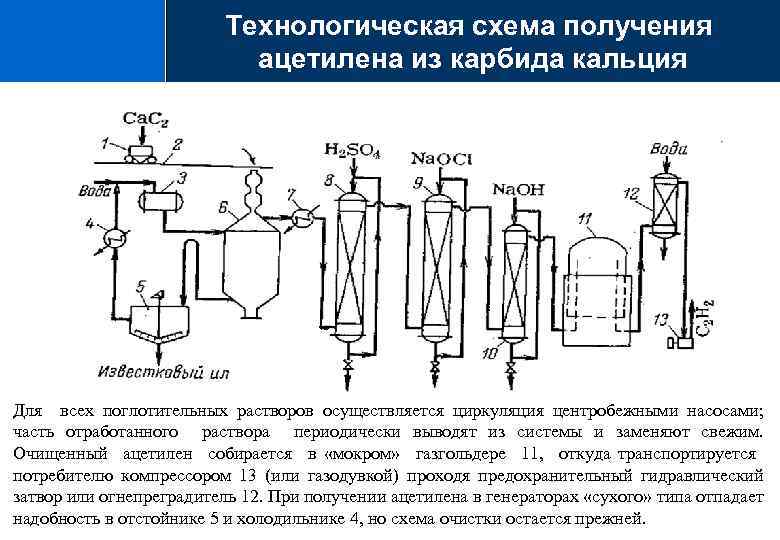 Технологическая схема получения ацетилена из карбида кальция Для всех поглотительных растворов осуществляется циркуляция центробежными насосами; часть отработанного раствора периодически выводят из системы и заменяют свежим. Очищенный ацетилен собирается в «мокром» газгольдере 11, откуда транспортируется потребителю компрессором 13 (или газодувкой) проходя предохранительный гидравлический затвор или огнепреградитель 12. При получении ацетилена в генераторах «сухого» типа отпадает надобность в отстойнике 5 и холодильнике 4, но схема очистки остается прежней.
Технологическая схема получения ацетилена из карбида кальция Для всех поглотительных растворов осуществляется циркуляция центробежными насосами; часть отработанного раствора периодически выводят из системы и заменяют свежим. Очищенный ацетилен собирается в «мокром» газгольдере 11, откуда транспортируется потребителю компрессором 13 (или газодувкой) проходя предохранительный гидравлический затвор или огнепреградитель 12. При получении ацетилена в генераторах «сухого» типа отпадает надобность в отстойнике 5 и холодильнике 4, но схема очистки остается прежней.
 Производство Общие сведения ацетилена из углеводородов Значительный интерес как источник сырья представляют дешевые нефтяные остатки. Установлено, что при пиролизе тяжелых углеводородов можно получать с высоким выходом ацетилен, концентрация которого в продуктах реакции достигает 31 - 33 %; кроме ацетилена, в них содержится 54 - 58 % водорода и 10 - 12 % олефинов, главным образом этилена. При переработке же газообразных углеводородов содержание ацетилена в продуктах реакции составляет от 7 до 16 %. Однако промышленная технология переработки гудрона и других нефтяных остатков еще полностью не разработана, из-за чего это сырье пока не используется.
Производство Общие сведения ацетилена из углеводородов Значительный интерес как источник сырья представляют дешевые нефтяные остатки. Установлено, что при пиролизе тяжелых углеводородов можно получать с высоким выходом ацетилен, концентрация которого в продуктах реакции достигает 31 - 33 %; кроме ацетилена, в них содержится 54 - 58 % водорода и 10 - 12 % олефинов, главным образом этилена. При переработке же газообразных углеводородов содержание ацетилена в продуктах реакции составляет от 7 до 16 %. Однако промышленная технология переработки гудрона и других нефтяных остатков еще полностью не разработана, из-за чего это сырье пока не используется.
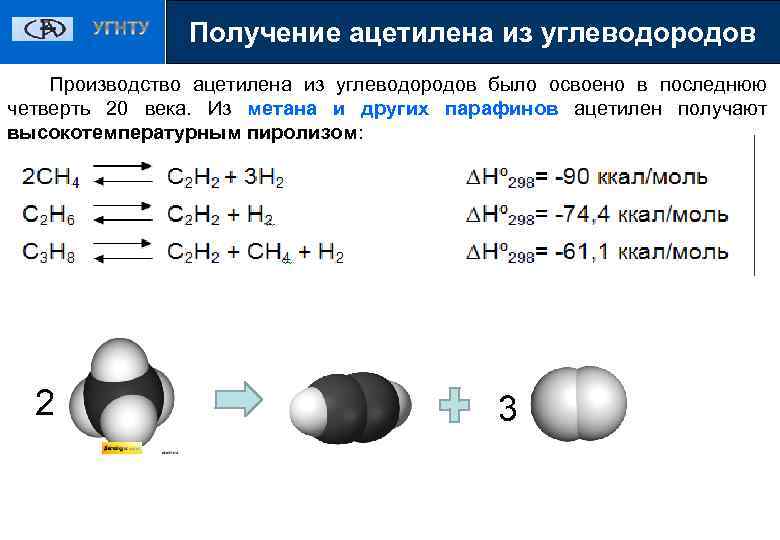 Получение ацетилена из углеводородов Получение ацетилена Производство ацетилена из углеводородов было освоено в последнюю четверть 20 века. Из метана и других парафинов ацетилен получают высокотемпературным пиролизом: 2 3
Получение ацетилена из углеводородов Получение ацетилена Производство ацетилена из углеводородов было освоено в последнюю четверть 20 века. Из метана и других парафинов ацетилен получают высокотемпературным пиролизом: 2 3
 Получение ацетилена из углеводородов Получение ацетилена Все реакции эндотермичны и равновесие смещается вправо только при Т=1000÷ 1300ºС, причём высокая степень конверсии достигается для метана при 1400÷ 1500ºС для этана – 900÷ 1000ºС. Для практического осуществления, с целью ускорения процесса, требуется более высокая температура от 1200 до 1300ºС для пропана и 1500÷ 1600ºС для СН 4. Реакция имеет радикально-цепной механизм: .
Получение ацетилена из углеводородов Получение ацетилена Все реакции эндотермичны и равновесие смещается вправо только при Т=1000÷ 1300ºС, причём высокая степень конверсии достигается для метана при 1400÷ 1500ºС для этана – 900÷ 1000ºС. Для практического осуществления, с целью ускорения процесса, требуется более высокая температура от 1200 до 1300ºС для пропана и 1500÷ 1600ºС для СН 4. Реакция имеет радикально-цепной механизм: .
 Получение ацетилена из углеводородов В полученном газе содержаться: СН 4, СН 2=СН 2, их гомологи, в небольших количествах бензол и углеводороды ацетиленового ряда: метилацетилен (пропин) СН 3 -С≡СН, винилацетилен СН 2=СН-С≡СН и диацетилен СН≡С-С≡СН. Получение ацетилена данным методом значительно осложняется экзотермической реакцией его распада на углерод и водород. Этот распад становится заметен при 1000ºС и достигает значительной величины при 1200÷ 1600ºС, т. е. при температуре требуемой для получения самого ацетилена. В результате наблюдается система последовательных превращений: Регулирование выхода промежуточных продуктов может быть достигнуто уменьшением конверсии в результате снижения времени контакта. Оптимальной является конверсия 50% и время 0, 01 сек. Затем необходима «закалка» реакционных газов (впрыскивание воды) – температура резко снижается до величины, при которой распада ацетилена не происходит.
Получение ацетилена из углеводородов В полученном газе содержаться: СН 4, СН 2=СН 2, их гомологи, в небольших количествах бензол и углеводороды ацетиленового ряда: метилацетилен (пропин) СН 3 -С≡СН, винилацетилен СН 2=СН-С≡СН и диацетилен СН≡С-С≡СН. Получение ацетилена данным методом значительно осложняется экзотермической реакцией его распада на углерод и водород. Этот распад становится заметен при 1000ºС и достигает значительной величины при 1200÷ 1600ºС, т. е. при температуре требуемой для получения самого ацетилена. В результате наблюдается система последовательных превращений: Регулирование выхода промежуточных продуктов может быть достигнуто уменьшением конверсии в результате снижения времени контакта. Оптимальной является конверсия 50% и время 0, 01 сек. Затем необходима «закалка» реакционных газов (впрыскивание воды) – температура резко снижается до величины, при которой распада ацетилена не происходит.
 Методы пиролиза углеводородов в ацетилен По способу подвода тепла, необходимого для нагревания исходных газов до 1200÷ 1600ºС, различают три метода. q Электрокрекинг углеводородов при помощи вольтовой дуги в электродуговых печах постоянного тока. Расход электроэнергии на 1 кг снижается по сравнению с карбидным методом с 11, 5 до 9÷ 11 к. Вт∙ч, но всё же является значительным. q Высокотемпературный пиролиз углеводородов в регенеративных печах с термостойкой насадкой из глинозёма. Печи работают периодически. Сначала насадка нагревается до нужной температуры горячими газами, получаемыми в специальной топке при сжигании смеси метана с воздухом. Затем в печь подают подогретое углеводородное сырьё. После охлаждения насадки до нижней допустимой температуры печь снова переключают на стадию подогрева. q Окислительный пиролиз углеводородов, при котором эндотермичность реакции образования ацетилена компенсируется экзотермической реакцией окисления части углеводородов кислородом
Методы пиролиза углеводородов в ацетилен По способу подвода тепла, необходимого для нагревания исходных газов до 1200÷ 1600ºС, различают три метода. q Электрокрекинг углеводородов при помощи вольтовой дуги в электродуговых печах постоянного тока. Расход электроэнергии на 1 кг снижается по сравнению с карбидным методом с 11, 5 до 9÷ 11 к. Вт∙ч, но всё же является значительным. q Высокотемпературный пиролиз углеводородов в регенеративных печах с термостойкой насадкой из глинозёма. Печи работают периодически. Сначала насадка нагревается до нужной температуры горячими газами, получаемыми в специальной топке при сжигании смеси метана с воздухом. Затем в печь подают подогретое углеводородное сырьё. После охлаждения насадки до нижней допустимой температуры печь снова переключают на стадию подогрева. q Окислительный пиролиз углеводородов, при котором эндотермичность реакции образования ацетилена компенсируется экзотермической реакцией окисления части углеводородов кислородом
 Методы термического расщепления Реакции окислительного пиролиза: Причём все реакции протекают одновременно. Ввиду непрерывности процесса и снижения энергозатрат, этот метод представляет наибольший интерес из всех перечисленных, хотя при нём содержание ацетилена в получаемом газе ниже, чем при электрокрекинге. Наряду с основными реакциями расщепления и сгорания метана при окислительном пиролизе происходит конверсия угдеводорода двуокисью углерода и водяным паром:
Методы термического расщепления Реакции окислительного пиролиза: Причём все реакции протекают одновременно. Ввиду непрерывности процесса и снижения энергозатрат, этот метод представляет наибольший интерес из всех перечисленных, хотя при нём содержание ацетилена в получаемом газе ниже, чем при электрокрекинге. Наряду с основными реакциями расщепления и сгорания метана при окислительном пиролизе происходит конверсия угдеводорода двуокисью углерода и водяным паром:
 Методы термического расщепления Несмотря на то, что эти реакции обратимы, при высокой температуре процесса равновесие полностью сдвинуто вправо. В реакцию конверсии способен вступать и образующийся ацетилен: На практике около 1/3 кислорода расходуется на образование воды, 10÷ 15% на СО 2 и 50÷ 55% на СО. Поэтому для поддержания автотермических условий реакции соотношения объёмов СН 4 и О 2 в исходной смеси должно составлять 100 : 65, что находится за верхним пределом взрывоопасности смеси. Использование воздуха вместо О 2 нерационально ввиду дополнительных затрат тепла на нагревание азота и значительного разбавления реакционных газов, что осложняет выделение из них ацетилена.
Методы термического расщепления Несмотря на то, что эти реакции обратимы, при высокой температуре процесса равновесие полностью сдвинуто вправо. В реакцию конверсии способен вступать и образующийся ацетилен: На практике около 1/3 кислорода расходуется на образование воды, 10÷ 15% на СО 2 и 50÷ 55% на СО. Поэтому для поддержания автотермических условий реакции соотношения объёмов СН 4 и О 2 в исходной смеси должно составлять 100 : 65, что находится за верхним пределом взрывоопасности смеси. Использование воздуха вместо О 2 нерационально ввиду дополнительных затрат тепла на нагревание азота и значительного разбавления реакционных газов, что осложняет выделение из них ацетилена.
 Реактор окислительного пиролиза СН 4 до С 2 Н 2 При нормальном режиме окислительного пиролиза на горение расходуется 55% метана, на образование ацетилена 23— 25 %, на образование сажи степень конверсии метана достигает 90%, степень конверсии кислорода превышает 99%. 1 — камера смешения; 2 - корпус; 3 – предохранительная мембрана; 4 — камера горения; 5 — нижняя камера; 6 —форсунка; 7 — горелочная плита; 8 — диффузор
Реактор окислительного пиролиза СН 4 до С 2 Н 2 При нормальном режиме окислительного пиролиза на горение расходуется 55% метана, на образование ацетилена 23— 25 %, на образование сажи степень конверсии метана достигает 90%, степень конверсии кислорода превышает 99%. 1 — камера смешения; 2 - корпус; 3 – предохранительная мембрана; 4 — камера горения; 5 — нижняя камера; 6 —форсунка; 7 — горелочная плита; 8 — диффузор
 Гомогенный пиролиз Методы термического расщепления Видоизменением описанного метода является гомогенный пиролиз углеводородных газов или жидкостей. СН 4 или другой углеводород сжигают в смеси с кислородом в топке печи, газ приобретает температуру 2000ºС. Реакции пиролиза с разрывом связей С—С сопровождаются значительным поглощением тепла. В средней части печи в газовый поток вводят исходное сырьё, предварительно подогретое до 500ºС. При высокой температуре происходят процессы расщепления и конверсии с образованием С 2 Н 2, других газов и сажи. Преимущество этого метода по сравнению с окислительным пиролизом состоит в большей безопасности и надёжности работы печи, однако для её работы требуются огнеупорные материалы. Установка пиролиза
Гомогенный пиролиз Методы термического расщепления Видоизменением описанного метода является гомогенный пиролиз углеводородных газов или жидкостей. СН 4 или другой углеводород сжигают в смеси с кислородом в топке печи, газ приобретает температуру 2000ºС. Реакции пиролиза с разрывом связей С—С сопровождаются значительным поглощением тепла. В средней части печи в газовый поток вводят исходное сырьё, предварительно подогретое до 500ºС. При высокой температуре происходят процессы расщепления и конверсии с образованием С 2 Н 2, других газов и сажи. Преимущество этого метода по сравнению с окислительным пиролизом состоит в большей безопасности и надёжности работы печи, однако для её работы требуются огнеупорные материалы. Установка пиролиза
 Выделение ацетилена из реакционных газов Реакционные газы имеют сложный состав при любом методе высокотемпературного расщепления углеводородов и содержат: Ø 7÷ 9% об. С 2 Н 2 (при регенеративном и окислительном пиролизе) и Ø 11÷ 14% об. С 2 Н 2 (при электрокрекинге). Остальные газы: Регенеративный пиролиз: Ø Н 2 – 45÷ 55%, Ø СН 4 - 25÷ 40% Ø небольшие количества С 2 Н 4, С 2 Н 6 и их гомологи; Ø бензол, Ø метилвинил- и диацетилен. Окислительный пиролиз: Ø СН 4 и С 2 Н 4 – 5÷ 7%, Ø СО 2 – 3÷ 4% и СО – 25%, Ø Н 2 – 55%. Ø Гомологи ацетилена – 0, 2÷ 0, 3%.
Выделение ацетилена из реакционных газов Реакционные газы имеют сложный состав при любом методе высокотемпературного расщепления углеводородов и содержат: Ø 7÷ 9% об. С 2 Н 2 (при регенеративном и окислительном пиролизе) и Ø 11÷ 14% об. С 2 Н 2 (при электрокрекинге). Остальные газы: Регенеративный пиролиз: Ø Н 2 – 45÷ 55%, Ø СН 4 - 25÷ 40% Ø небольшие количества С 2 Н 4, С 2 Н 6 и их гомологи; Ø бензол, Ø метилвинил- и диацетилен. Окислительный пиролиз: Ø СН 4 и С 2 Н 4 – 5÷ 7%, Ø СО 2 – 3÷ 4% и СО – 25%, Ø Н 2 – 55%. Ø Гомологи ацетилена – 0, 2÷ 0, 3%.
 Выделение ацетилена из реакционных газов Для выделения и очистки ацетилена используют его свойство лучше, чем другие компоненты реакционных газов, растворяться в некоторых агентах. Для выделения ацетилена их газов термического расщепления углеводородов используют: Ø Н 2 О (под давлением), Ø жидкий аммиак, Ø метиловый спирт (при -70°С) , Ø ацетон (при -70°С), Ø диметилформамид (ДМФА) и Ø N-метилпирролидон. Обычно газ в начале освобождают от сажи, затем от ароматических соединений и диацетилена абсорбцией минеральным маслом или основным растворителем, в котором диацетилен растворяется значительно лучше ацетилена, после чего поглощают ацетилен. Затем проводят абсорбцию ацетилена при повышенном давлении и десорбируют его при снижении давления и нагревании. В заключении очищают ацетилен от СО 2, например, этанолалкилом.
Выделение ацетилена из реакционных газов Для выделения и очистки ацетилена используют его свойство лучше, чем другие компоненты реакционных газов, растворяться в некоторых агентах. Для выделения ацетилена их газов термического расщепления углеводородов используют: Ø Н 2 О (под давлением), Ø жидкий аммиак, Ø метиловый спирт (при -70°С) , Ø ацетон (при -70°С), Ø диметилформамид (ДМФА) и Ø N-метилпирролидон. Обычно газ в начале освобождают от сажи, затем от ароматических соединений и диацетилена абсорбцией минеральным маслом или основным растворителем, в котором диацетилен растворяется значительно лучше ацетилена, после чего поглощают ацетилен. Затем проводят абсорбцию ацетилена при повышенном давлении и десорбируют его при снижении давления и нагревании. В заключении очищают ацетилен от СО 2, например, этанолалкилом.
 Технологическая схема окислительного пиролиза 1 – подогреватель; 3 – печь пиролиза; 4 – водяной скруббер; 5 – масляный фильтр; 6 – компрессор; 7 – холодильник; 8 – сепаратор; 9, 10 – скрубберы; 11 – дроссельные вентили; 12, 13 – десорберы. Выход С 2 Н 2 – 99%.
Технологическая схема окислительного пиролиза 1 – подогреватель; 3 – печь пиролиза; 4 – водяной скруббер; 5 – масляный фильтр; 6 – компрессор; 7 – холодильник; 8 – сепаратор; 9, 10 – скрубберы; 11 – дроссельные вентили; 12, 13 – десорберы. Выход С 2 Н 2 – 99%.
 Технологическая схема окислительного пиролиза Вода, стекающая из гидравлического затвора реактора и из сажеулавливающих аппаратов, содержит 2— 3 % сажи, а также малолетучие ароматические соединения. Она поступает в отстойник 9, с верха которого сажу и смолы собирают скребками и направляют на сжигание. Воду из отстойника возвращают в реактор как «закалочный агент» , а ее избыток идет на очистку, чем создается замкнутая система водооборота без сбрасывания токсичных сточных вод. Газ из газгольдера 8 сжимается компрессором 10 до давления ≈ 1 МПа, проходя после каждой ступени холодильники и сепараторы, не показанные на схеме. В абсорбере 11 он промывается диметилформамидом или N-метилпирролидоном, а непоглотившийся газ (Н 2, СН 4, СО 2) проходит скруббер 12, где при орошении водным конденсатом улавливается унесенный им растворитель. После этого газ можно использовать в качестве синтез-газа или топлива.
Технологическая схема окислительного пиролиза Вода, стекающая из гидравлического затвора реактора и из сажеулавливающих аппаратов, содержит 2— 3 % сажи, а также малолетучие ароматические соединения. Она поступает в отстойник 9, с верха которого сажу и смолы собирают скребками и направляют на сжигание. Воду из отстойника возвращают в реактор как «закалочный агент» , а ее избыток идет на очистку, чем создается замкнутая система водооборота без сбрасывания токсичных сточных вод. Газ из газгольдера 8 сжимается компрессором 10 до давления ≈ 1 МПа, проходя после каждой ступени холодильники и сепараторы, не показанные на схеме. В абсорбере 11 он промывается диметилформамидом или N-метилпирролидоном, а непоглотившийся газ (Н 2, СН 4, СО 2) проходит скруббер 12, где при орошении водным конденсатом улавливается унесенный им растворитель. После этого газ можно использовать в качестве синтез-газа или топлива.
 Технологическая схема окислительного пиролиза Раствор в кубе абсорбера 11 содержит ацетилен и его гомологи, а также значительное количество близкого к ним по растворимости диоксида углерода с примесью других газов. Он проходит дроссельный вентиль 13 и поступает в десорбер 14 первой ступени. За счет снижения давления до ~0, 15 МПа и нагревания куба до 40°С из раствора десорбируются ацетилен и менее растворимые газы. Ацетилен при своем движении вверх вытесняет из раствора диоксид углерода, который вместе с другими газами и частью ацетилена выходит с верха десорбера, предварительно отмываясь от растворителя водным конденсатом. Эти газы возвращают на компримирование. Концентрированный ацетилен выводят из средней части десорбера 14, промывают в скруббере 15 водой и через огнепреградитель 16 выводят с установки.
Технологическая схема окислительного пиролиза Раствор в кубе абсорбера 11 содержит ацетилен и его гомологи, а также значительное количество близкого к ним по растворимости диоксида углерода с примесью других газов. Он проходит дроссельный вентиль 13 и поступает в десорбер 14 первой ступени. За счет снижения давления до ~0, 15 МПа и нагревания куба до 40°С из раствора десорбируются ацетилен и менее растворимые газы. Ацетилен при своем движении вверх вытесняет из раствора диоксид углерода, который вместе с другими газами и частью ацетилена выходит с верха десорбера, предварительно отмываясь от растворителя водным конденсатом. Эти газы возвращают на компримирование. Концентрированный ацетилен выводят из средней части десорбера 14, промывают в скруббере 15 водой и через огнепреградитель 16 выводят с установки.
 Технологическая схема окислительного пиролиза Кубовую жидкость десорбера 14, содержащую некоторое количество ацетилена и его гомологов, направляют в десорбер 18 второй ступени, подогревая предварительно в теплообменнике 17. За счет нагревания куба до 100 °С из раствора отгоняются все газы, причем из средней части колонны уходят гомологи ацетилена, направляемые затем на сжигание, а с верха — ацетилен с примесью его гомологов, возвращаемый в десорбер первой ступени. В растворителе постепенно накапливаются вода и полимеры, от которых его освобождают на установке регенерации, не изображенной на схеме. Полученный на установке концентрированный ацетилен содержит 99, 0 — 99, 5 % основного вещества с примесью метилацетилена, пропадиена и диоксида углерода (по 0, 1— 0, 3 %).
Технологическая схема окислительного пиролиза Кубовую жидкость десорбера 14, содержащую некоторое количество ацетилена и его гомологов, направляют в десорбер 18 второй ступени, подогревая предварительно в теплообменнике 17. За счет нагревания куба до 100 °С из раствора отгоняются все газы, причем из средней части колонны уходят гомологи ацетилена, направляемые затем на сжигание, а с верха — ацетилен с примесью его гомологов, возвращаемый в десорбер первой ступени. В растворителе постепенно накапливаются вода и полимеры, от которых его освобождают на установке регенерации, не изображенной на схеме. Полученный на установке концентрированный ацетилен содержит 99, 0 — 99, 5 % основного вещества с примесью метилацетилена, пропадиена и диоксида углерода (по 0, 1— 0, 3 %).
 Сравнение методов получения С 2 Н 2 Карбидный метод (–) большой расход электроэнергии и сырья (известняк и кокс). (+) получение концентрированного С 2 Н 2 с лёгкой очисткой. Термическое расщепление (+) меньшее количество сырья, побочно получают смесь Н 2 + СН 4 или СО, утилизация которых снижает себестоимость С 2 Н 2, (–) ацетилен разбавленный и требуется сложная система очистки и концентрирования. Удельные капитальные вложения, энергетические затраты и себестоимость С 2 Н 2 снижаются, по сравнению с карбидным способом, при электрокрекинге до 60÷ 80%, а при регенеративном и окислительном пиролизе углеводородов до 30÷ 55%. Однако карбидный способ сохраняет своё значение для районов, удалённых от нефтяных, и газовых месторождений, и богатых электроэнергией. Для оценки перспектив органического синтеза на основе С 2 Н 2 существенно, что С 2 Н 2 втрое дороже олефинов.
Сравнение методов получения С 2 Н 2 Карбидный метод (–) большой расход электроэнергии и сырья (известняк и кокс). (+) получение концентрированного С 2 Н 2 с лёгкой очисткой. Термическое расщепление (+) меньшее количество сырья, побочно получают смесь Н 2 + СН 4 или СО, утилизация которых снижает себестоимость С 2 Н 2, (–) ацетилен разбавленный и требуется сложная система очистки и концентрирования. Удельные капитальные вложения, энергетические затраты и себестоимость С 2 Н 2 снижаются, по сравнению с карбидным способом, при электрокрекинге до 60÷ 80%, а при регенеративном и окислительном пиролизе углеводородов до 30÷ 55%. Однако карбидный способ сохраняет своё значение для районов, удалённых от нефтяных, и газовых месторождений, и богатых электроэнергией. Для оценки перспектив органического синтеза на основе С 2 Н 2 существенно, что С 2 Н 2 втрое дороже олефинов.


