40cca973752c69096123b9041ead5ec5.ppt
- Количество слайдов: 35
 9 класс Кремний и его соединения Учитель химии Анзина С. М. МКОУ СОШ № 8 с. Манычское 1
9 класс Кремний и его соединения Учитель химии Анзина С. М. МКОУ СОШ № 8 с. Манычское 1
 Выделив только заглавную букву слов ответов, составьте из этих букв слово. n n n n Положительно заряженный ион Элемент 5 периода периодической системы химических элементов, щелочной металл Лантаноид, в ядре его атома 63 протона Автор периодического закона Вещества, которые не проводят электрический ток Разновидность атомов элементов с одинаковым зарядом ядра Твердое вещество серого цвета, галоген 2
Выделив только заглавную букву слов ответов, составьте из этих букв слово. n n n n Положительно заряженный ион Элемент 5 периода периодической системы химических элементов, щелочной металл Лантаноид, в ядре его атома 63 протона Автор периодического закона Вещества, которые не проводят электрический ток Разновидность атомов элементов с одинаковым зарядом ядра Твердое вещество серого цвета, галоген 2
 Ответы n n n n Катион Рубидий Европий Менделеев Неэлектролиты Изотопы Йод 3
Ответы n n n n Катион Рубидий Европий Менделеев Неэлектролиты Изотопы Йод 3
 Кремень – камень Открыт Ж. Гей Люссаком и Л. Тенаром в 1811 г. Получил в 1825 г. Я. Берцелиус Русское название “кремний” введено в 1834 году российским химиком Германом Ивановичем Гессом. В переводе с греческого kremnos – “утес, гора ”. 4
Кремень – камень Открыт Ж. Гей Люссаком и Л. Тенаром в 1811 г. Получил в 1825 г. Я. Берцелиус Русское название “кремний” введено в 1834 году российским химиком Германом Ивановичем Гессом. В переводе с греческого kremnos – “утес, гора ”. 4
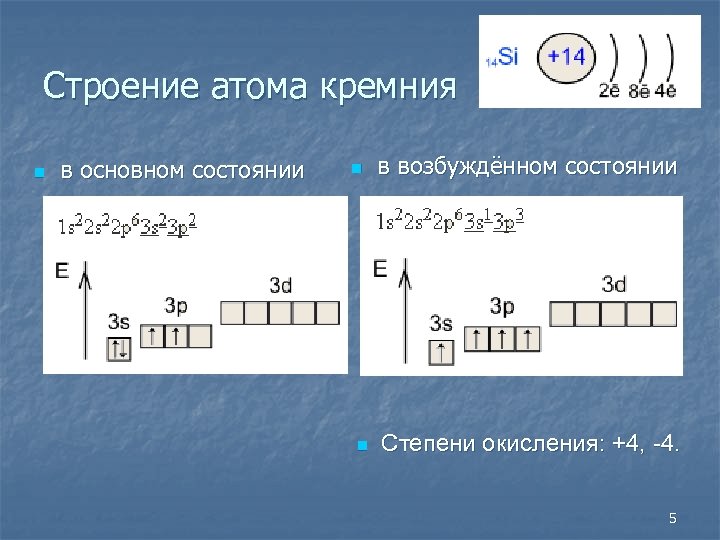 Строение атома кремния n в основном состоянии n n в возбуждённом состоянии Степени окисления: +4, -4. 5
Строение атома кремния n в основном состоянии n n в возбуждённом состоянии Степени окисления: +4, -4. 5
 Кремний в природе Второй после кислорода n ¼ состава земной коры n Наиболее распространен Si. O 2 кремнезем (основная часть песка) и Al 2 O 3 • 2 Si. O 2 • 2 H 2 O каолинит (основная часть глины). n 6
Кремний в природе Второй после кислорода n ¼ состава земной коры n Наиболее распространен Si. O 2 кремнезем (основная часть песка) и Al 2 O 3 • 2 Si. O 2 • 2 H 2 O каолинит (основная часть глины). n 6
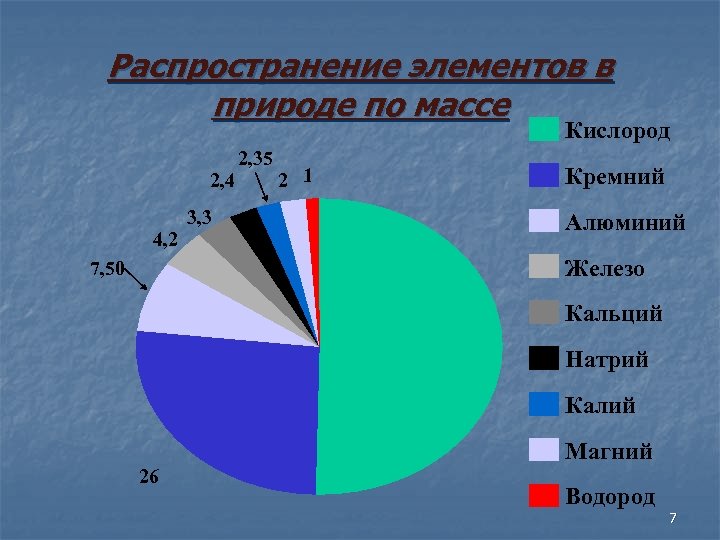 Распространение элементов в природе по массе Кислород 2, 35 2, 4 4, 2 3, 3 2 1 Кремний Алюминий Железо 7, 50 Кальций Натрий Калий Магний 26 Водород 7
Распространение элементов в природе по массе Кислород 2, 35 2, 4 4, 2 3, 3 2 1 Кремний Алюминий Железо 7, 50 Кальций Натрий Калий Магний 26 Водород 7
 Песок – самое распространенное соединение кремния n n Есть повсюду в почве Песчаные пустыни Величайшие пустыни Мира: Ливийская на северо-востоке Африки, на Аравийском полуострове, Большая песчаная и пустыня Виктория в Австралии, Кызылкум в Узбекистане 8
Песок – самое распространенное соединение кремния n n Есть повсюду в почве Песчаные пустыни Величайшие пустыни Мира: Ливийская на северо-востоке Африки, на Аравийском полуострове, Большая песчаная и пустыня Виктория в Австралии, Кызылкум в Узбекистане 8
 Горный хрусталь – окаменевшая вода? Куски кварца Кусок горного хрусталя в виде головы животного 9
Горный хрусталь – окаменевшая вода? Куски кварца Кусок горного хрусталя в виде головы животного 9
 К в а р ц Кварц имеет формулу Si. O 2. Встречается в природе в виде песка. При накаливании смеси песка с углем получают карборунд, служащий для изготовления точильных камней. 10
К в а р ц Кварц имеет формулу Si. O 2. Встречается в природе в виде песка. При накаливании смеси песка с углем получают карборунд, служащий для изготовления точильных камней. 10
 Кварц-драгоценный камень Прозрачные, как вода, и бесцветные кристаллы кварца называют горным хрусталем. Окрашенные разновидности кварца являются драгоценными камнями. Это аметист(фиолетовый), рубин(красный), морион(коричневый), сердолик(полупрозрачный розовый), раухтопаз( дымчатый прозрачный). 11
Кварц-драгоценный камень Прозрачные, как вода, и бесцветные кристаллы кварца называют горным хрусталем. Окрашенные разновидности кварца являются драгоценными камнями. Это аметист(фиолетовый), рубин(красный), морион(коричневый), сердолик(полупрозрачный розовый), раухтопаз( дымчатый прозрачный). 11
 Драгоценные камни всего лишь оксиды кремния? Сердолик Аметист лиловый Агат Ваза из оникса (разновидности агата) Яшма Халцедон Розовый аметист 12
Драгоценные камни всего лишь оксиды кремния? Сердолик Аметист лиловый Агат Ваза из оникса (разновидности агата) Яшма Халцедон Розовый аметист 12
 Силикаты – соли кремниевой кислоты n n Гранит( наиболее прочная магматическая порода, состоящая в основном из кварца) Глина (Si. O 2 30 80%, 2 Al 2 O 3 10 40%, Н О 2 2 до 1%) Гранитный горный массив 13
Силикаты – соли кремниевой кислоты n n Гранит( наиболее прочная магматическая порода, состоящая в основном из кварца) Глина (Si. O 2 30 80%, 2 Al 2 O 3 10 40%, Н О 2 2 до 1%) Гранитный горный массив 13
 Г р а н и т Гранит самая распространенная горная порода. Состоит из кварца, полевого шпата и слюды. Содержит до 70% кремнезема. Гранит прекрасный строительный материал. 14
Г р а н и т Гранит самая распространенная горная порода. Состоит из кварца, полевого шпата и слюды. Содержит до 70% кремнезема. Гранит прекрасный строительный материал. 14
 Г л и н а Состав глины выражается формулой Al 2 O 3*2 Si. O 2*2 H 2 O. Глина служит основным сырьем в керамической промышленности, производящей фарфор и фаянс. 15
Г л и н а Состав глины выражается формулой Al 2 O 3*2 Si. O 2*2 H 2 O. Глина служит основным сырьем в керамической промышленности, производящей фарфор и фаянс. 15
 А с б е с т Асбест 3 Mg. O*2 H 2 O*2 Si. O 3 природный силикат магния отличается огнестойкостью. Применяется в качестве тепло и электроизоляционно го материала. 16
А с б е с т Асбест 3 Mg. O*2 H 2 O*2 Si. O 3 природный силикат магния отличается огнестойкостью. Применяется в качестве тепло и электроизоляционно го материала. 16
 Т а л ь к Тальк 3 Mg. O*H 2 O*4 Si. O 2 природный силикат магния. Применяется в бумажной, парфюмерной промышленности, в медицине. 17
Т а л ь к Тальк 3 Mg. O*H 2 O*4 Si. O 2 природный силикат магния. Применяется в бумажной, парфюмерной промышленности, в медицине. 17
 Соединения кремния в живой природе n n n Прочность стебля растений Защитные покровы Стебли злаков животных Гладкость и прочность костей Чешуя рыб Шерсть животных Перья птиц Крылья бабочек Панцирь жуков 18
Соединения кремния в живой природе n n n Прочность стебля растений Защитные покровы Стебли злаков животных Гладкость и прочность костей Чешуя рыб Шерсть животных Перья птиц Крылья бабочек Панцирь жуков 18
 Физические свойства кремния n n Кристаллический кремний это вещество темно серого цвета со стальным блеском. Структура кремния аналогична структуре алмаза: кристаллическая решетка кубическая гранецентрированная, но из за большей длины связи между атомами Si Si по сравнению с длиной связи C C твердость кремния значительно меньше, чем алмаза. Кремний очень хрупок, его плотность 2, 33 г/см 3. Как и уголь, относится к тугоплавким веществам. 19
Физические свойства кремния n n Кристаллический кремний это вещество темно серого цвета со стальным блеском. Структура кремния аналогична структуре алмаза: кристаллическая решетка кубическая гранецентрированная, но из за большей длины связи между атомами Si Si по сравнению с длиной связи C C твердость кремния значительно меньше, чем алмаза. Кремний очень хрупок, его плотность 2, 33 г/см 3. Как и уголь, относится к тугоплавким веществам. 19
 Аллотропия кремния n n n Известен аморфный и кристаллический кремний. Кристаллический – тёмно серое вещество с металлическим блеском, большая твёрдость, хрупок, полупроводник; ρ = 2, 33 г/см 3, t°пл. =1415°C; t°кип. = 2680°C. Имеет алмазоподобную структуру и образует прочные ковалентные связи. Инертен. Аморфный бурый порошок, гигроскопичен, алмазоподобная структура, ρ = 2 г/см 3, более реакционноспособен. 20
Аллотропия кремния n n n Известен аморфный и кристаллический кремний. Кристаллический – тёмно серое вещество с металлическим блеском, большая твёрдость, хрупок, полупроводник; ρ = 2, 33 г/см 3, t°пл. =1415°C; t°кип. = 2680°C. Имеет алмазоподобную структуру и образует прочные ковалентные связи. Инертен. Аморфный бурый порошок, гигроскопичен, алмазоподобная структура, ρ = 2 г/см 3, более реакционноспособен. 20
 Получение кремния n n 1) Промышленность – нагревание угля с песком: 2 C + Si. O 2 t Si + 2 CO 2) Лаборатория 2 Mg + Si. O 2 t Si + 2 Mg. O 21
Получение кремния n n 1) Промышленность – нагревание угля с песком: 2 C + Si. O 2 t Si + 2 CO 2) Лаборатория 2 Mg + Si. O 2 t Si + 2 Mg. O 21
 Химические свойства кремния. n Как восстановитель: 1) С кислородом n Si 0 + O 2 t Si+4 O 2 n n 2) С фтором (без нагревания) n Si 0 + 2 F 2 → Si. F 4 n n 3) С углеродом Si 0 + C t Si+4 C (Si. C - карборунд - твёрдый; используется для точки и шлифовки) 4) С водородом не взаимодействует. 22
Химические свойства кремния. n Как восстановитель: 1) С кислородом n Si 0 + O 2 t Si+4 O 2 n n 2) С фтором (без нагревания) n Si 0 + 2 F 2 → Si. F 4 n n 3) С углеродом Si 0 + C t Si+4 C (Si. C - карборунд - твёрдый; используется для точки и шлифовки) 4) С водородом не взаимодействует. 22
 n n n 5) С кислотами не реагирует (только с плавиковой кислотой Si+4 HF=Si. F 4+2 H 2) Растворяется только в смеси азотной и плавиковой кислот: 3 Si + 4 HNO 3 + 18 HF → 3 H 2[Si. F 6] + 4 NO + 8 H 2 O n 6) Со щелочами (при нагревании): n Si 0 + 2 Na. OH + H 2 O t Na 2 Si+4 O 3+ 2 H 2 n n n Как окислитель: 7) С металлами (образуются силициды): Si 0 + 2 Mg t Mg 2 Si 4 23
n n n 5) С кислотами не реагирует (только с плавиковой кислотой Si+4 HF=Si. F 4+2 H 2) Растворяется только в смеси азотной и плавиковой кислот: 3 Si + 4 HNO 3 + 18 HF → 3 H 2[Si. F 6] + 4 NO + 8 H 2 O n 6) Со щелочами (при нагревании): n Si 0 + 2 Na. OH + H 2 O t Na 2 Si+4 O 3+ 2 H 2 n n n Как окислитель: 7) С металлами (образуются силициды): Si 0 + 2 Mg t Mg 2 Si 4 23
 Силан - Si. H 4 n Физические свойства: Бесцветный газ, ядовит, t°пл. = 185°C, t°кип. = 112°C. n Получение: Mg 2 Si + 4 HCl → 2 Mg. Cl 2 + Si. H 4↑ n Химические свойства: 1) Окисление: Si. H 4 + 2 O 2 t Si. O 2 + 2 H 2 O n 2) Разложение: Si. H 4 → Si + 2 H 2 n 24
Силан - Si. H 4 n Физические свойства: Бесцветный газ, ядовит, t°пл. = 185°C, t°кип. = 112°C. n Получение: Mg 2 Si + 4 HCl → 2 Mg. Cl 2 + Si. H 4↑ n Химические свойства: 1) Окисление: Si. H 4 + 2 O 2 t Si. O 2 + 2 H 2 O n 2) Разложение: Si. H 4 → Si + 2 H 2 n 24
 Оксид кремния (IV) - (Si. O 2)n n n Кристаллическая решётка оксида кремния (IV) – атомная Физические свойства: Твёрдое, кристаллическое, тугоплавкое вещество, t°пл. = 1728°C, t°кип. = 2590°C 25
Оксид кремния (IV) - (Si. O 2)n n n Кристаллическая решётка оксида кремния (IV) – атомная Физические свойства: Твёрдое, кристаллическое, тугоплавкое вещество, t°пл. = 1728°C, t°кип. = 2590°C 25
 Химические свойства: Si. O 2 n n n Кислотный оксид. При сплавлении взаимодействует с основными оксидами, щелочами, а также с карбонатами щелочных и щелочноземельных металлов: Изучение свойств оксида кремния (IV) 1) С основными оксидами: Si. O 2 + Ca. O t Ca. Si. O 3 n 2) Со щелочами: Si. O 2 + 2 Na. OH t Na 2 Si. O 3 + H 2 O n 3) С водой не реагирует 4) С солями: n 5) С плавиковой кислотой: n Si. O 2 + Ca. CO 3 t Ca. Si. O 3 + CO 2 Si. O 2 + K 2 CO 3 t K 2 Si. O 3 + CO 2 Si. O 2 + 4 HF t Si. F 4 + 2 HO 2 Si. O 2 + 6 HF t H 2[Si. F 6] (гексафторкремниевая кислота) + 2 H 2 O (реакции лежат в основе процесса травления стекла). 26
Химические свойства: Si. O 2 n n n Кислотный оксид. При сплавлении взаимодействует с основными оксидами, щелочами, а также с карбонатами щелочных и щелочноземельных металлов: Изучение свойств оксида кремния (IV) 1) С основными оксидами: Si. O 2 + Ca. O t Ca. Si. O 3 n 2) Со щелочами: Si. O 2 + 2 Na. OH t Na 2 Si. O 3 + H 2 O n 3) С водой не реагирует 4) С солями: n 5) С плавиковой кислотой: n Si. O 2 + Ca. CO 3 t Ca. Si. O 3 + CO 2 Si. O 2 + K 2 CO 3 t K 2 Si. O 3 + CO 2 Si. O 2 + 4 HF t Si. F 4 + 2 HO 2 Si. O 2 + 6 HF t H 2[Si. F 6] (гексафторкремниевая кислота) + 2 H 2 O (реакции лежат в основе процесса травления стекла). 26
 n n Кремниевые кислоты x • Si. O 2 • y H 2 O x = 1, y = 1 H 2 Si. O 3 метакремниевая кислота x = 1, y = 2 H 4 Si. O 4 ортокремниевая кислота и т. д. Физические свойства: H 2 Si. O 3 очень слабая (слабее угольной), непрочная, в воде малорастворима (образует коллоидный раствор), не имеет кислого вкуса. n n Получение: Действие сильных кислот на силикаты Na 2 Si. O 3 + 2 HCl → 2 Na. Cl + H 2 Si. O 3↓ 27
n n Кремниевые кислоты x • Si. O 2 • y H 2 O x = 1, y = 1 H 2 Si. O 3 метакремниевая кислота x = 1, y = 2 H 4 Si. O 4 ортокремниевая кислота и т. д. Физические свойства: H 2 Si. O 3 очень слабая (слабее угольной), непрочная, в воде малорастворима (образует коллоидный раствор), не имеет кислого вкуса. n n Получение: Действие сильных кислот на силикаты Na 2 Si. O 3 + 2 HCl → 2 Na. Cl + H 2 Si. O 3↓ 27
 Химические свойства При нагревании разлагается: H 2 Si. O 3 t H 2 O + Si. O 2 n Соли кремниевой кислоты силикаты. n 1) с кислотами Na 2 Si. O 3+H 2 O+CO 2=Na 2 CO 3+H 2 Si. O 3 n 2) с солями Na 2 Si. O 3+Ca. Cl 2=2 Na. Cl+Ca. Si. O 3↓ n 3) Силикаты, входящие в состав минералов, в природных условиях разрушаются под действием воды и оксида углерода (IV) выветривание горных пород: (K 2 O • Al 2 O 3 • 6 Si. O 2)(полевой шпат) + CO 2 + 2 H 2 O → (Al 2 O 3 • 2 Si. O 2 • 2 H 2 O)(каолинит (глина)) + 4 Si. O 2(кремнезём (песок)) + K 2 CO 3 n 28
Химические свойства При нагревании разлагается: H 2 Si. O 3 t H 2 O + Si. O 2 n Соли кремниевой кислоты силикаты. n 1) с кислотами Na 2 Si. O 3+H 2 O+CO 2=Na 2 CO 3+H 2 Si. O 3 n 2) с солями Na 2 Si. O 3+Ca. Cl 2=2 Na. Cl+Ca. Si. O 3↓ n 3) Силикаты, входящие в состав минералов, в природных условиях разрушаются под действием воды и оксида углерода (IV) выветривание горных пород: (K 2 O • Al 2 O 3 • 6 Si. O 2)(полевой шпат) + CO 2 + 2 H 2 O → (Al 2 O 3 • 2 Si. O 2 • 2 H 2 O)(каолинит (глина)) + 4 Si. O 2(кремнезём (песок)) + K 2 CO 3 n 28
 Соединения кремния и древние люди n n n Каменный век – век кремневых орудий труда Распространен и доступен На сколе очень острый 29
Соединения кремния и древние люди n n n Каменный век – век кремневых орудий труда Распространен и доступен На сколе очень острый 29
 Кремний полупроводник n n Солнечные батарейки Солнечные батареи Фотоэлементы Электроника 30
Кремний полупроводник n n Солнечные батарейки Солнечные батареи Фотоэлементы Электроника 30
 Стекло древнейшее изобретение человечества n n Оконное стекло Кварцевое стекло Хрустальное стекло Цветное стекло Витраж в Венском соборе 16 век Хрустальные вазы 18 век Царские кубки 17 век Стеклянные изделия Древнего Египта Стеклянные ландыши 20 век 31
Стекло древнейшее изобретение человечества n n Оконное стекло Кварцевое стекло Хрустальное стекло Цветное стекло Витраж в Венском соборе 16 век Хрустальные вазы 18 век Царские кубки 17 век Стеклянные изделия Древнего Египта Стеклянные ландыши 20 век 31
 Керамика – значит глина, а там тоже кремний n n n Кирпич Керамическая посуда Фарфор Фаянс Статуэтки Отделочная плитка 32
Керамика – значит глина, а там тоже кремний n n n Кирпич Керамическая посуда Фарфор Фаянс Статуэтки Отделочная плитка 32
 Цемент – это тоже соединения кремния n n Бетон Железобетон Плотина Братской ГЭС Дом из бетонных панелей 33
Цемент – это тоже соединения кремния n n Бетон Железобетон Плотина Братской ГЭС Дом из бетонных панелей 33
 Ответьте на вопросы n n n Почему углерод называют элементом живой природы, а кремний основным элементом неживой природы? Почему физические свойства оксидов кремния и углерода резко отличаются друга? Почему нельзя хранить плавиковую кислоту в стеклянной посуде? 34
Ответьте на вопросы n n n Почему углерод называют элементом живой природы, а кремний основным элементом неживой природы? Почему физические свойства оксидов кремния и углерода резко отличаются друга? Почему нельзя хранить плавиковую кислоту в стеклянной посуде? 34
 Задания для закрепления n n Осуществите превращения по схеме: 1) Si → Si. O 2 → Na 2 Si. O 3 → H 2 Si. O 3 →Si. O 2 2) Si → Mg 2 Si → Si. H 4 → Si. O 2 3) Si → Na 2 Si. O 3 35
Задания для закрепления n n Осуществите превращения по схеме: 1) Si → Si. O 2 → Na 2 Si. O 3 → H 2 Si. O 3 →Si. O 2 2) Si → Mg 2 Si → Si. H 4 → Si. O 2 3) Si → Na 2 Si. O 3 35


