9 класс Карбоновые кислоты


9 класс Карбоновые кислоты

План урока. 1. Повторение спирты 2. Понятие о карбоновых кислотах. 3. Уксусная кислота. 4. Стеариновая кислота. 5. Вопросы и упражнения. Д/З: § 36. В. 1.

Что такое спирты? Спирты (устаревшее алкого ли) — органические соединения, содержащие одну или несколько гидроксильных групп (гидроксил, OH), непосредственно связанных с атомом углерода в углеводородном радикале. Общая формула спиртов Сx. Hy(OH)n.
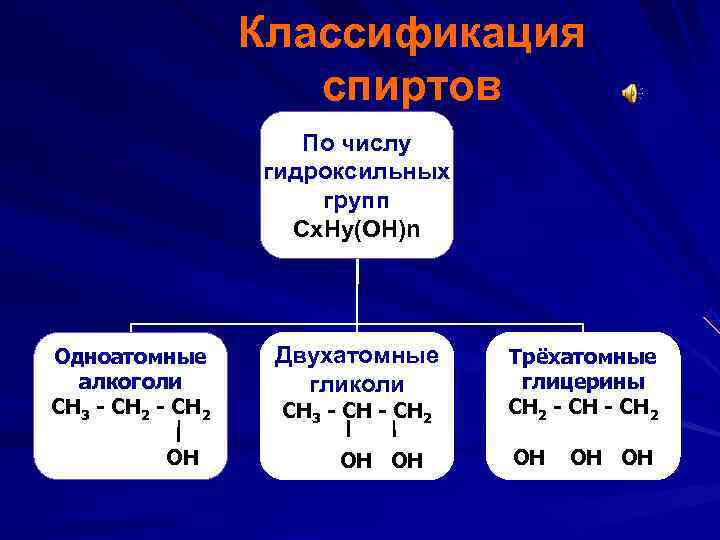
Классификация спиртов По числу гидроксильных групп Cx. Hy(OH)n Одноатомные Двухатомные Трёхатомные алкоголи гликоли глицерины CH 3 - CH 2 CH 2 - CH 2 OH OH OH
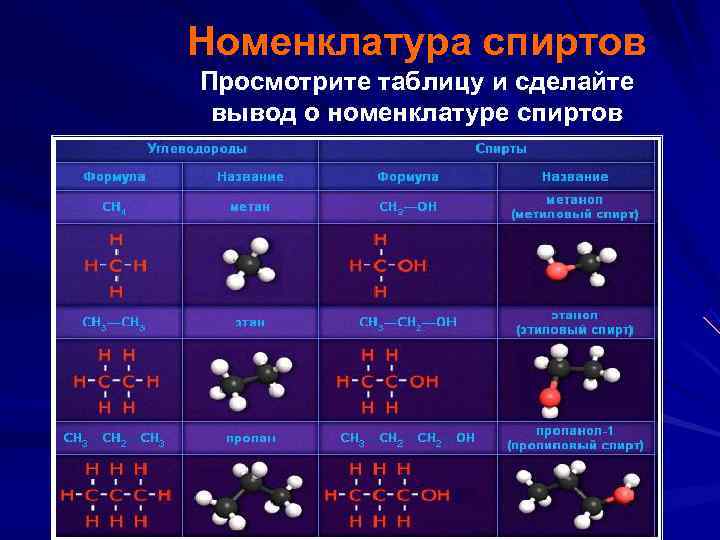
Номенклатура спиртов Просмотрите таблицу и сделайте вывод о номенклатуре спиртов

Метанол - яд Ядовитое действие метанола основано на поражении нервной и сосудистой системы. Приём внутрь 5— 10 мл метанола приводит к тяжёлому отравлению, а 30 мл и более — к смерти.

Применение этанола n Этиловый спирт употребляется приготовлении различных спиртных напитков. n В медицине для приготовления экстрактов из лекарственных растений, а также для дезинфекции. n В косметике и парфюмерии этанол — растворитель для духов и лосьонов.

Вредное воздействие этанола Алкоголь крайне неблагоприятно влияет на сосуды головного мозга. В начале опьянения они расширяются, кровоток в них замедляется, что приводит к застойным явлениям в головном мозге. Затем, когда в крови помимо алкоголя начинают накапливаться вредные продукты его неполного распада, наступает резкий спазм, сужение сосудов, развиваются такие опасные осложнения, как мозговые инсульты, приводящие к тяжелой инвалидности и даже смерти.

Вредное воздействие этанола Изменения структуры мозга, вызванные многолетней алкогольной интоксикацией, почти необратимы, и даже после длительного воздержания от употребления спиртных напитков они сохраняются. Если же человек не может остановиться, то органические и, следовательно, психические отклонения от нормы идут по нарастающей.

. Названия одноатомных спиртов образуются из названия углеводорода с самой длинной углеродной цепью, содержащей гидроксильную группу, путём добавления суффикса -ол. Для многоатомных спиртов перед суффиксом -ол по-гречески (-ди-, -три- , . . . ) указывается количество гидроксильных групп. Например: CH 3 -CH 2 -OH этанол

1. Понятие о карбоновых кислотах. Среди органических веществ большую группу образуют органические кислоты, такие как молочная, муравьиная, яблочная, щавелевая, лимонная, уксусная, аскорбиновая и многие другие. Названия этих кислот указывают откуда они были получены химиками. Все эти вещества содержат карбоксильную группу – СООН. Карбоксильная группа –СООН – это функциональная группа карбоновых кислот.

Органические кислоты в природе

Карбоновые кислоты – это органические вещества, содержащие одну или несколько карбоксильных групп -СООН , связанных с углеводородным радикалом. Структурная формула карбоксильной группы имеет вид: О С О Н

Общая формула одноосновных карбоновых кислот (содержат одну карбоксильную группу) - RCOOH, где R – углеводородный радикал. Все карбоновые кислоты относятся к слабым электролитам, в водной среде диссоциируют частично: RCOOH RCOO- + H+ Карбоновая Карбоксилат кислота - анион

Среди карбоновых кислот Известных «лиц» невпроворот. В кислотах - группы карбоксильные, Но все кислоты здесь - несильные.

2. Уксусная кислота СН 3 СООН– самая древняя из органических кислот. Аптекари – алхимики средневековья получали её из перебродившего вина. Чистая уксусная кислота – б/ц жидкость с резким запахом. Она используется в пищевых целях, при консервировании пищевых продуктов.

Уксусная кислота в больших количествах применяется в химической промышленности. Основную часть уксусной кислоты используют для получения искусственных волокон и пластмасс на основе целлюлозы. Уксусную кислоту применяют в производстве красителей, медикаментов, ядохимикатов, органического стекла.

Уксусная кислота проявляет все типичные свойства кислот. Она диссоциирует и реагирует с: 1. металлами 2. оксидами металлов 3. основаниями 4. солями. Кроме того, уксусная кислота реагирует со спиртами ( эта реакция будет изучена позже).

Диссоциация кислот

Взаимодействие с металлами

Взаимодействие с оксидами металлов

Взаимодействие с солями более слабых кислот
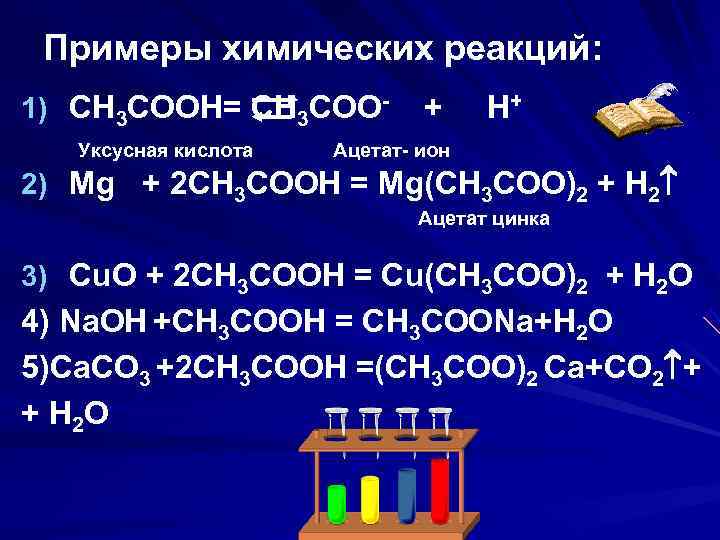
Примеры химических реакций: 1) CH 3 COOH= CH 3 COO- + H+ Уксусная кислота Ацетат- ион 2) Mg + 2 CH 3 COOH = Mg(CH 3 COO)2 + H 2 Ацетат цинка 3) Cu. O + 2 CH 3 COOH = Cu(CH 3 COO)2 + H 2 O 4) Na. OH +CH 3 COOH = CH 3 COONa+H 2 O 5)Ca. CO 3 +2 CH 3 COOH =(CH 3 COO)2 Ca+CO 2 + + H 2 O

3. Стеариновая кислота относится к высшим карбоновым кислотам и имеет формулу С 17 Н 35 СООН. Она является одной из наиболее распространённых в природе высших жирных кислот. Стеариновая кислота — главная составная часть многих жиров и масел, из которых её выделяют гидролизом.

Соли стеариновой кислоты называются стеаратами. Стеараты кальция, магния или железа, так же как сама стеариновая кислота, в воде нерастворимы. Стеараты щелочных металлов, например стеарат натрия С 17 Н 35 СООNa, хорошо растворимы в воде. Они являются основой мыл: хозяйственного, банного, туалетного, детского.

Мыло - стеарат натрия

4. Вопросы и задания. (тетради на проверку) 1. Что называется карбоновыми кислотами? 2. Напишите молекулярную и структурную формулу карбоксильной функциональной группы. 3. Напишите структурную формулу уксусной кислоты. Каковы её физические свойства и где она применяется?

4. С какими из ниже перечисленных веществ будет реагировать уксусная кислота? Напишите уравнения воз- можных реакций и назовите вещества. Zn(OH)2, Cu, Na. Cl, Mg, Ba. CO 3, Fe. O, CO 2, KOH. 6. Назовите формулу известной вам жирной карбоновой кислоты. 7. Где применяются стеараты натрия и калия?

Сдайте тетради на проверку Домашнее задание: Изучить § 36 до сложных эфиров

