7(2011).ppt
- Количество слайдов: 23
 7. Квантовая физика в современных технологиях. Неклассические концепции в химии. 7. 1. Ядерная энергетика. 7. 2. Физика полупроводников. 7. 3. Квантовые генераторы - лазеры. 7. 4. Учение о химическом процессе. КСЕ
7. Квантовая физика в современных технологиях. Неклассические концепции в химии. 7. 1. Ядерная энергетика. 7. 2. Физика полупроводников. 7. 3. Квантовые генераторы - лазеры. 7. 4. Учение о химическом процессе. КСЕ
 7. 1. Ядерная энергетика Z – порядковый номер элемента, число протонов в ядре; А – массовое число, общее число протонов и нейтронов (нуклонов). Изотопы – ядра с одинаковым Z, но разным А. Дефект массы ядра: Энергия связи ядра - энергия, необходимая для расщепления ядра на составляющие его нуклоны: КСЕ
7. 1. Ядерная энергетика Z – порядковый номер элемента, число протонов в ядре; А – массовое число, общее число протонов и нейтронов (нуклонов). Изотопы – ядра с одинаковым Z, но разным А. Дефект массы ядра: Энергия связи ядра - энергия, необходимая для расщепления ядра на составляющие его нуклоны: КСЕ
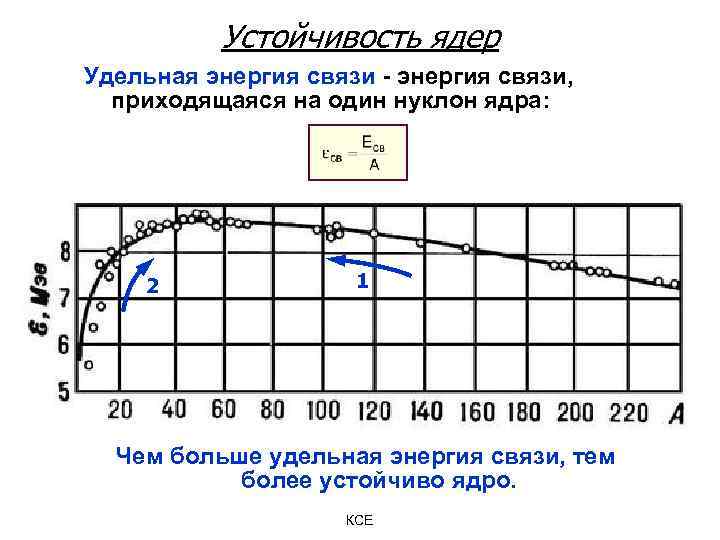 Устойчивость ядер Удельная энергия связи - энергия связи, приходящаяся на один нуклон ядра: 2 1 Чем больше удельная энергия связи, тем более устойчиво ядро. КСЕ
Устойчивость ядер Удельная энергия связи - энергия связи, приходящаяся на один нуклон ядра: 2 1 Чем больше удельная энергия связи, тем более устойчиво ядро. КСЕ
 1. Реакция деления. а) Ядерные реакторы. Первые реакторы – 1942 г. , Э. Ферми, США и 1949 г. , И. В. Курчатов, Россия. Делящееся вещество – смесь изотопов урана U 238 и U 235 (или плутоний Рu 239). При попадании в ядро нейтрона оно делится, испуская два или три вторичных нейтрона. Может возникнуть цепная реакция. В зависимости от скорости нейтроны делятся на быстрые и медленные. Медленными нейтронами делится только изотоп урана U 235. Природный уран U 238 «обогащают» и используют их смесь. КСЕ
1. Реакция деления. а) Ядерные реакторы. Первые реакторы – 1942 г. , Э. Ферми, США и 1949 г. , И. В. Курчатов, Россия. Делящееся вещество – смесь изотопов урана U 238 и U 235 (или плутоний Рu 239). При попадании в ядро нейтрона оно делится, испуская два или три вторичных нейтрона. Может возникнуть цепная реакция. В зависимости от скорости нейтроны делятся на быстрые и медленные. Медленными нейтронами делится только изотоп урана U 235. Природный уран U 238 «обогащают» и используют их смесь. КСЕ
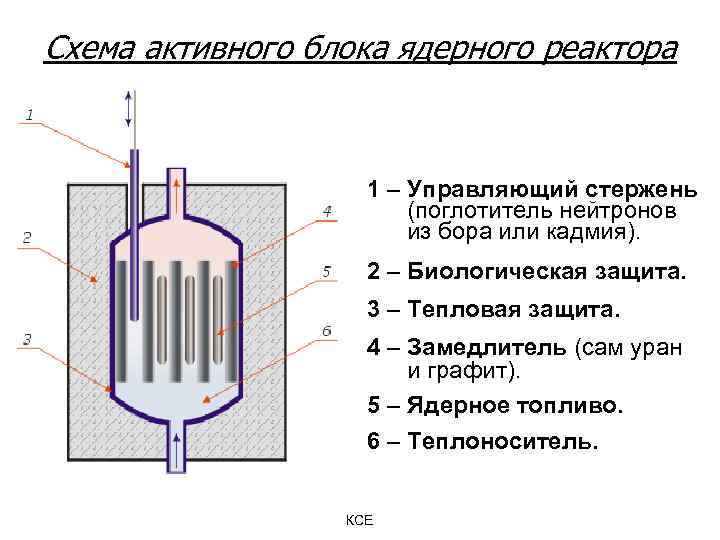 Схема активного блока ядерного реактора 1 – Управляющий стержень (поглотитель нейтронов из бора или кадмия). 2 – Биологическая защита. 3 – Тепловая защита. 4 – Замедлитель (сам уран и графит). 5 – Ядерное топливо. 6 – Теплоноситель. КСЕ
Схема активного блока ядерного реактора 1 – Управляющий стержень (поглотитель нейтронов из бора или кадмия). 2 – Биологическая защита. 3 – Тепловая защита. 4 – Замедлитель (сам уран и графит). 5 – Ядерное топливо. 6 – Теплоноситель. КСЕ
 б) Атомная бомба. После взрыва пороха масса активного вещества становится больше критической и происходит неуправляемая цепная реакция. КСЕ
б) Атомная бомба. После взрыва пороха масса активного вещества становится больше критической и происходит неуправляемая цепная реакция. КСЕ
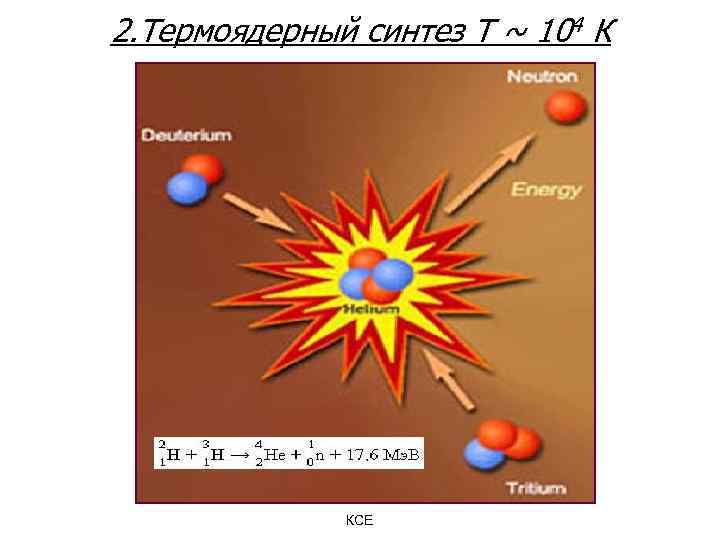 2. Термоядерный синтез T ~ 104 К КСЕ
2. Термоядерный синтез T ~ 104 К КСЕ
 7. 2. Полупроводники Все твердые тела по их способности проводить электрический ток делятся на проводники (металлы), диэлектрики (изоляторы) и полупроводники. – В проводниках валентные (внешние) электроны обобществляются всем объемом материала – являются свободными носителями заряда. – В диэлектриках электроны связаны каждый со своим атомом. – В полупроводниках при низких температурах (Т 0 К) электроны связаны каждый со своим атомом, а уже при комнатных температурах появляются свободные носители заряда. КСЕ
7. 2. Полупроводники Все твердые тела по их способности проводить электрический ток делятся на проводники (металлы), диэлектрики (изоляторы) и полупроводники. – В проводниках валентные (внешние) электроны обобществляются всем объемом материала – являются свободными носителями заряда. – В диэлектриках электроны связаны каждый со своим атомом. – В полупроводниках при низких температурах (Т 0 К) электроны связаны каждый со своим атомом, а уже при комнатных температурах появляются свободные носители заряда. КСЕ
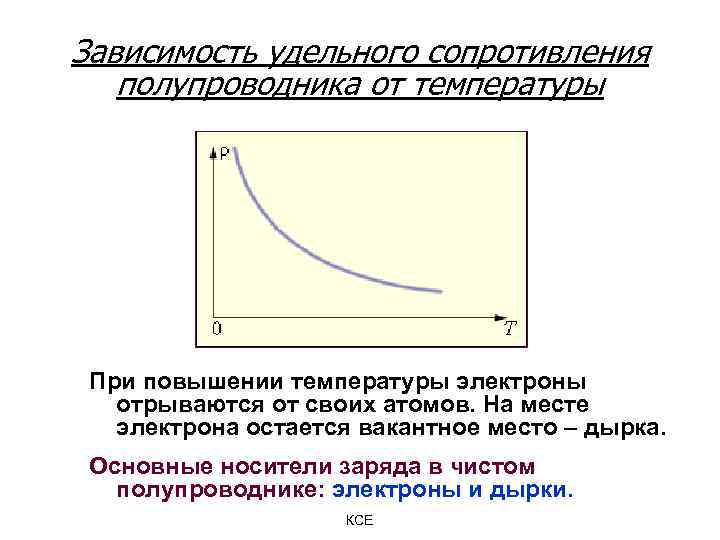 Зависимость удельного сопротивления полупроводника от температуры При повышении температуры электроны отрываются от своих атомов. На месте электрона остается вакантное место – дырка. Основные носители заряда в чистом полупроводнике: электроны и дырки. КСЕ
Зависимость удельного сопротивления полупроводника от температуры При повышении температуры электроны отрываются от своих атомов. На месте электрона остается вакантное место – дырка. Основные носители заряда в чистом полупроводнике: электроны и дырки. КСЕ
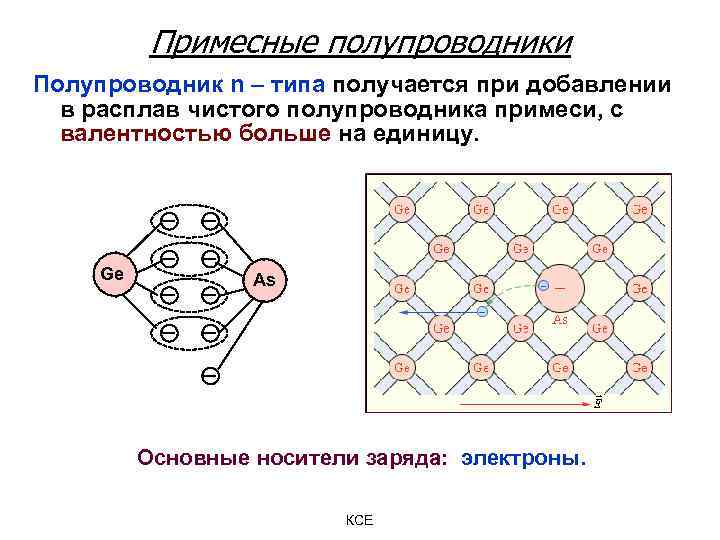 Примесные полупроводники Полупроводник n – типа получается при добавлении в расплав чистого полупроводника примеси, с валентностью больше на единицу. Ge As Основные носители заряда: электроны. КСЕ
Примесные полупроводники Полупроводник n – типа получается при добавлении в расплав чистого полупроводника примеси, с валентностью больше на единицу. Ge As Основные носители заряда: электроны. КСЕ
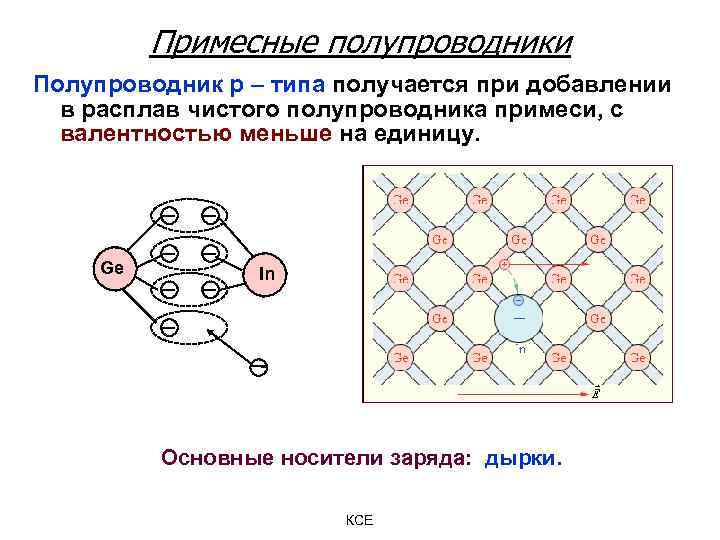 Примесные полупроводники Полупроводник р – типа получается при добавлении в расплав чистого полупроводника примеси, с валентностью меньше на единицу. Ge In Основные носители заряда: дырки. КСЕ
Примесные полупроводники Полупроводник р – типа получается при добавлении в расплав чистого полупроводника примеси, с валентностью меньше на единицу. Ge In Основные носители заряда: дырки. КСЕ
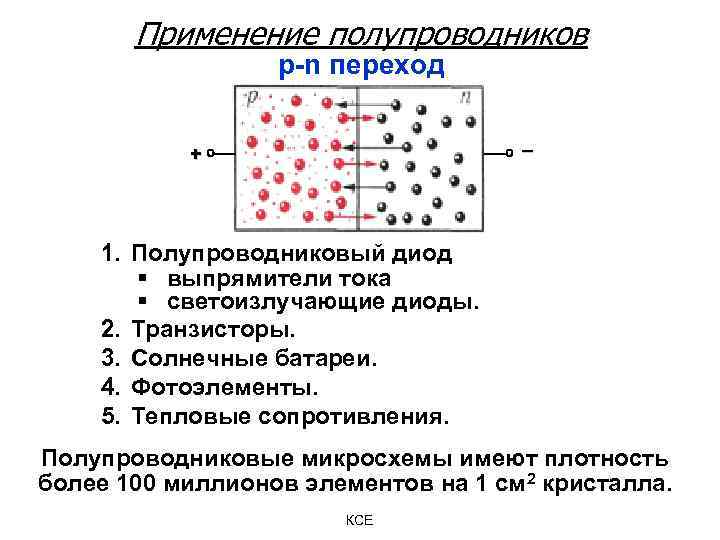 Применение полупроводников р-n переход _ + 1. Полупроводниковый диод § выпрямители тока § светоизлучающие диоды. 2. Транзисторы. 3. Солнечные батареи. 4. Фотоэлементы. 5. Тепловые сопротивления. Полупроводниковые микросхемы имеют плотность более 100 миллионов элементов на 1 см 2 кристалла. КСЕ
Применение полупроводников р-n переход _ + 1. Полупроводниковый диод § выпрямители тока § светоизлучающие диоды. 2. Транзисторы. 3. Солнечные батареи. 4. Фотоэлементы. 5. Тепловые сопротивления. Полупроводниковые микросхемы имеют плотность более 100 миллионов элементов на 1 см 2 кристалла. КСЕ
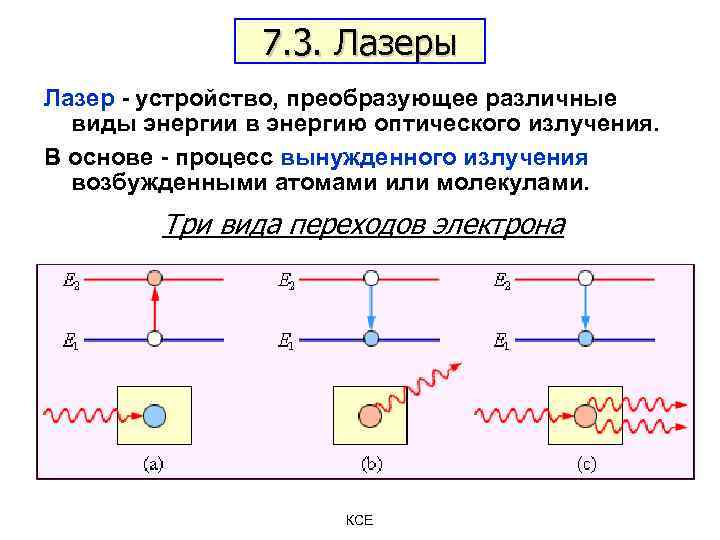 7. 3. Лазеры Лазер - устройство, преобразующее различные виды энергии в энергию оптического излучения. В основе - процесс вынужденного излучения возбужденными атомами или молекулами. Три вида переходов электрона КСЕ
7. 3. Лазеры Лазер - устройство, преобразующее различные виды энергии в энергию оптического излучения. В основе - процесс вынужденного излучения возбужденными атомами или молекулами. Три вида переходов электрона КСЕ
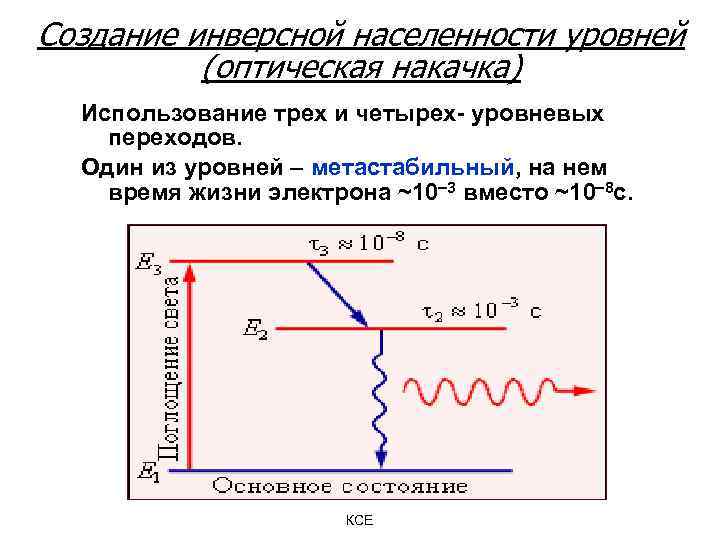 Создание инверсной населенности уровней (оптическая накачка) Использование трех и четырех- уровневых переходов. Один из уровней – метастабильный, на нем время жизни электрона ~10 3 вместо ~10 8 с. КСЕ
Создание инверсной населенности уровней (оптическая накачка) Использование трех и четырех- уровневых переходов. Один из уровней – метастабильный, на нем время жизни электрона ~10 3 вместо ~10 8 с. КСЕ
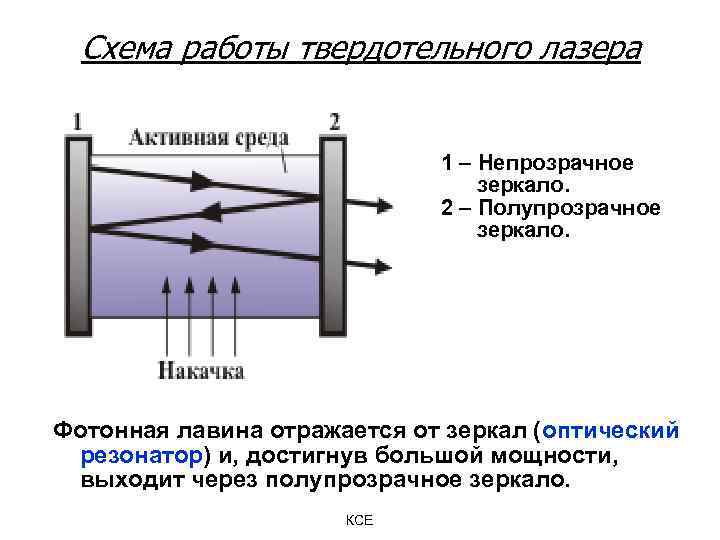 Схема работы твердотельного лазера 1 – Непрозрачное зеркало. 2 – Полупрозрачное зеркало. Фотонная лавина отражается от зеркал (оптический резонатор) и, достигнув большой мощности, выходит через полупрозрачное зеркало. КСЕ
Схема работы твердотельного лазера 1 – Непрозрачное зеркало. 2 – Полупрозрачное зеркало. Фотонная лавина отражается от зеркал (оптический резонатор) и, достигнув большой мощности, выходит через полупрозрачное зеркало. КСЕ
 Применение лазеров 1. Наука § § § спектроскопия фотохимия лазерное намагничивание и охлаждение. 2. Вооружение § § § лазерное оружие лазерный прицел лазерное наведение на цель. 3. Контроль качества микросхем оптическими методами. 4. Медицина. 5. Лазеры в быту § § § проигрыватели указки, голография освещение. 6. Обработка материалов в промышленности. КСЕ
Применение лазеров 1. Наука § § § спектроскопия фотохимия лазерное намагничивание и охлаждение. 2. Вооружение § § § лазерное оружие лазерный прицел лазерное наведение на цель. 3. Контроль качества микросхем оптическими методами. 4. Медицина. 5. Лазеры в быту § § § проигрыватели указки, голография освещение. 6. Обработка материалов в промышленности. КСЕ
 7. 4. Учение о химическом процессе Это третий уровень химического познания. Н. Н. Семенов, русский ученый, (1896 – 1986 г. ) основоположник физической химии. Основные параметры химического процесса: I. Тепловой эффект реакции. II. Химическое равновесие реакции – состояние, в котором скорости прямой и обратной реакций одинаковы. III. Скорость протекания реакции – количество вещества, прореагировавшего в единицу времени в единице объема. КСЕ
7. 4. Учение о химическом процессе Это третий уровень химического познания. Н. Н. Семенов, русский ученый, (1896 – 1986 г. ) основоположник физической химии. Основные параметры химического процесса: I. Тепловой эффект реакции. II. Химическое равновесие реакции – состояние, в котором скорости прямой и обратной реакций одинаковы. III. Скорость протекания реакции – количество вещества, прореагировавшего в единицу времени в единице объема. КСЕ
 I. Тепловой эффект реакции. Герман Гесс, русский химик (1802– 1850). Закон Гесса: Тепловой эффект Q химической реакции зависит от состояния исходных веществ и продуктов реакции, но не зависит от промежуточных стадий реакции. Qi — теплоты образования конечных и исходных веществ; ri — стехиометрические коэффициенты реакции. КСЕ
I. Тепловой эффект реакции. Герман Гесс, русский химик (1802– 1850). Закон Гесса: Тепловой эффект Q химической реакции зависит от состояния исходных веществ и продуктов реакции, но не зависит от промежуточных стадий реакции. Qi — теплоты образования конечных и исходных веществ; ri — стехиометрические коэффициенты реакции. КСЕ
 II. Химическое равновесие реакции. Химическое равновесие может быть смещено как в сторону прямой, так и в сторону обратной реакции. Принцип подвижного равновесия Ле Шателье (французский ученый 1850– 1936 г. ): Внешнее воздействие на систему, находящуюся в состоянии химического равновесия, приводит к смещению этого равновесия в направлении, при котором эффект произведенного воздействия ослабляется. Пример: при повышении температуры равновесие смещается в сторону реакции, идущей с поглощением тепла. КСЕ
II. Химическое равновесие реакции. Химическое равновесие может быть смещено как в сторону прямой, так и в сторону обратной реакции. Принцип подвижного равновесия Ле Шателье (французский ученый 1850– 1936 г. ): Внешнее воздействие на систему, находящуюся в состоянии химического равновесия, приводит к смещению этого равновесия в направлении, при котором эффект произведенного воздействия ослабляется. Пример: при повышении температуры равновесие смещается в сторону реакции, идущей с поглощением тепла. КСЕ
 III. Скорость протекания реакции. Факторы, определяющие скорость реакции: 1. Природа реагирующих веществ. 2. Площадь поверхности реагирования. Для веществ в твердом состоянии скорость реакции прямо пропорциональна поверхности реагирующих веществ. 3. Концентрация веществ. Закон действующих масс: скорость реакции жидких и газообразных веществ пропорциональна произведению их концентраций. КСЕ
III. Скорость протекания реакции. Факторы, определяющие скорость реакции: 1. Природа реагирующих веществ. 2. Площадь поверхности реагирования. Для веществ в твердом состоянии скорость реакции прямо пропорциональна поверхности реагирующих веществ. 3. Концентрация веществ. Закон действующих масс: скорость реакции жидких и газообразных веществ пропорциональна произведению их концентраций. КСЕ
 4. Температура. Правило Вант-Гоффа: при повышении температуры на 10 о. С скорость реакции возрастает в 2 - 4 раза. Более точно: формула Аррениуса: КСЕ
4. Температура. Правило Вант-Гоффа: при повышении температуры на 10 о. С скорость реакции возрастает в 2 - 4 раза. Более точно: формула Аррениуса: КСЕ
 5. Катализатор – активатор молекул реагента исходных химических веществ. Катализ открыл в 1812 г. русский химик Кирхгоф К. С. • гетерогенный катализ – жидкие или газообразные реагенты на поверхности твердого катализатора; • гомогенный катализ - газы или жидкости; • электрокатализ - на поверхности электрода; • фотокатализ – под действием излучения. Синтез аммиака: катализатор – железо; температура ~ 450 С, давление 30 -100 МПа. Учет каталитического действия среды есть одно из проявлений неклассического подхода в химии. КСЕ
5. Катализатор – активатор молекул реагента исходных химических веществ. Катализ открыл в 1812 г. русский химик Кирхгоф К. С. • гетерогенный катализ – жидкие или газообразные реагенты на поверхности твердого катализатора; • гомогенный катализ - газы или жидкости; • электрокатализ - на поверхности электрода; • фотокатализ – под действием излучения. Синтез аммиака: катализатор – железо; температура ~ 450 С, давление 30 -100 МПа. Учет каталитического действия среды есть одно из проявлений неклассического подхода в химии. КСЕ
 Новейшие направления: химия экстремальных состояний • Плазмохимия (в низкотемпературной плазме при температурах 1000 -100000 С) • Радиационная химия (элионные технологии в направленных электронных или ионных пучках) • Химия высоких давлений и температур (деформируются электронные оболочки атомов, повышается реакционная способность веществ) КСЕ
Новейшие направления: химия экстремальных состояний • Плазмохимия (в низкотемпературной плазме при температурах 1000 -100000 С) • Радиационная химия (элионные технологии в направленных электронных или ионных пучках) • Химия высоких давлений и температур (деформируются электронные оболочки атомов, повышается реакционная способность веществ) КСЕ


