ГАЛОГЕНИРОВАНИЕ.ppt
- Количество слайдов: 41

7. ГАЛОГЕНИРОВАНИЕ Область примене нияреакции. Хлорирование. Агенты хлорирования. Основные факторы хлорирования ароматических соединений. Механизм и кинетика процесса. Особенности галогенирования производных бензола, нафталина и антрахинона. Хлорирование толуола в ядро и в боковую цепь. Технология процесса. Бромирование. Агенты. Прямое и косвенное бромирование. Особенности технологического оформления процесса. Фторирование органических соединений. Современная практика и перспективы промышленного применения фторпроизводных
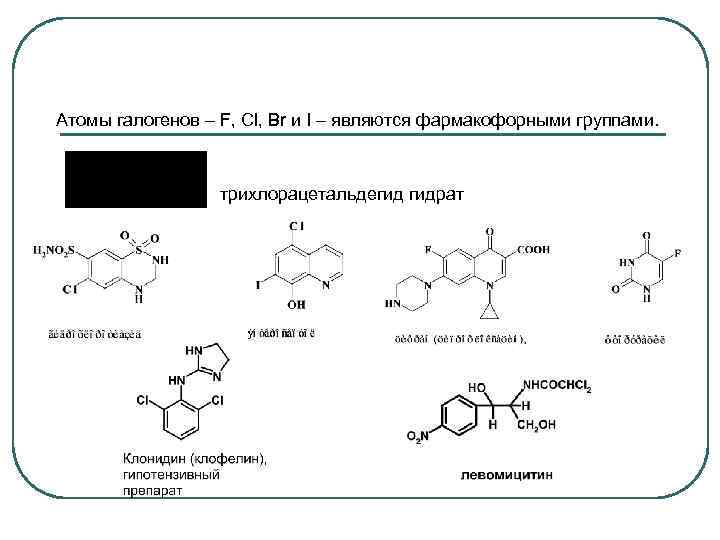
Атомы галогенов – F, Cl, Br и I – являются фармакофорными группами. трихлорацетальдегид гидрат
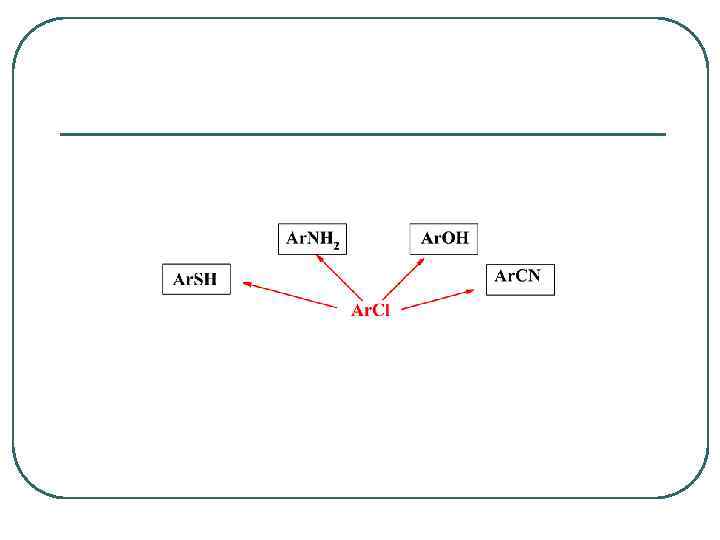

Реагенты реакций галогенирования: Cl 2, Br 2, I 2 (но не F 2) Cl. F, ICl HOCl, HOBr, ROCl, R-SO 2 NHCl, SO 2 Cl 2, 2 H 2 SO 4 + 2 Na. Br = Br 2 + Na 2 SO 4 + 2 H 2 O + SO 2 Катализаторы: Fe. Cl 3, I 2, H 2 SO 4, NH 4 Cl, Ti. Cl 4, Sb. Cl 5

Механизм реакции Реакционноспособная частица Hal+, как считалось ранее, образуется в результате следующих реакций: Однако при более подробном изучении было найдено, что действительным реагенто в хлорировании является оксид хлора Cl O Cl, который возникает по следующей реакции:
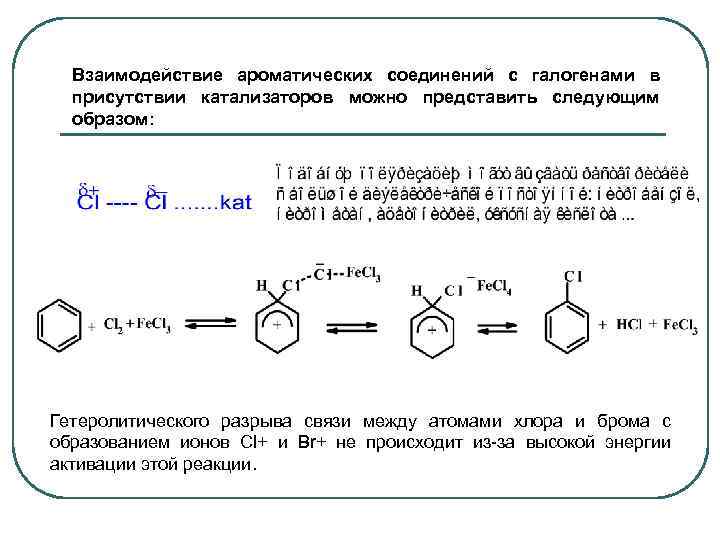
Взаимодействие ароматических соединений с галогенами в присутствии катализаторов можно представить следующим образом: Гетеролитического разрыва связи между атомами хлора и брома с образованием ионов Cl+ и Br+ не происходит из за высокой энергии активации этой реакции.

При действии хлористого сульфурила восстановительная реакция. идет окислительно- Реакция ускоряется в присутствии перекисей и при облучении ультрафиолетом. Присоединение атома хлора к ароматическому ядру с образованием комплекса идет по свободнорадикальному механизму.
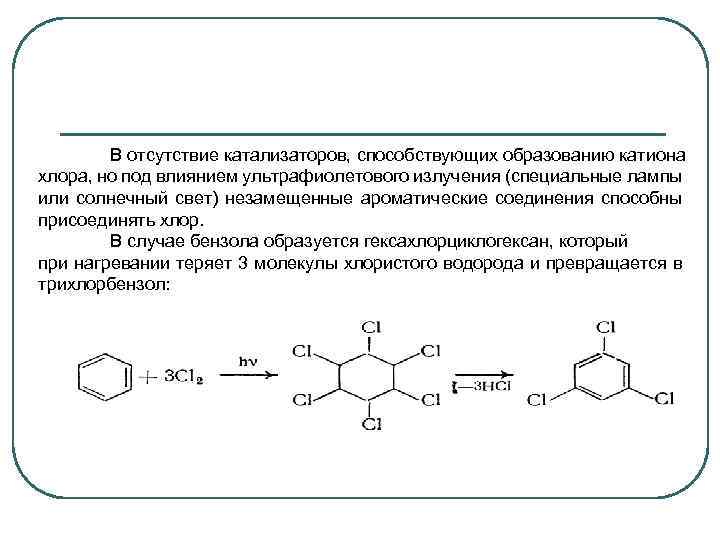
В отсутствие катализаторов, способствующих образованию катиона хлора, но под влиянием ультрафиолетового излучения (специальные лампы или солнечный свет) незамещенные ароматические соединения способны присоединять хлор. В случае бензола образуется гексахлорциклогексан, который при нагревании теряет 3 молекулы хлористого водорода и превращается в трихлорбензол:
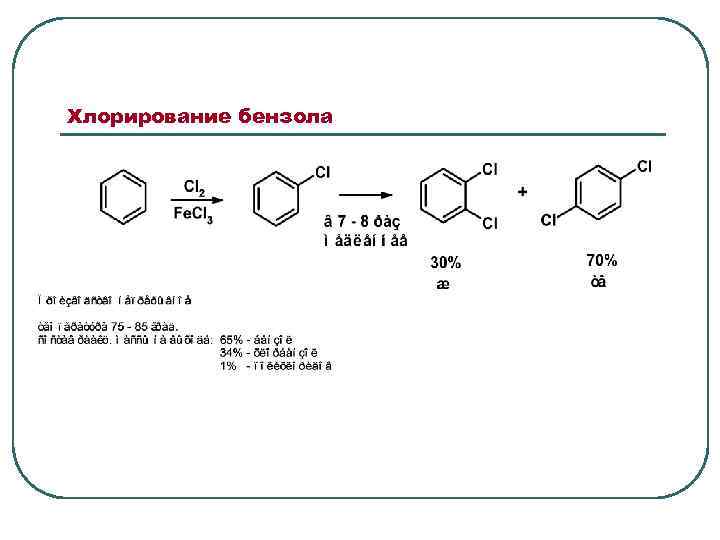
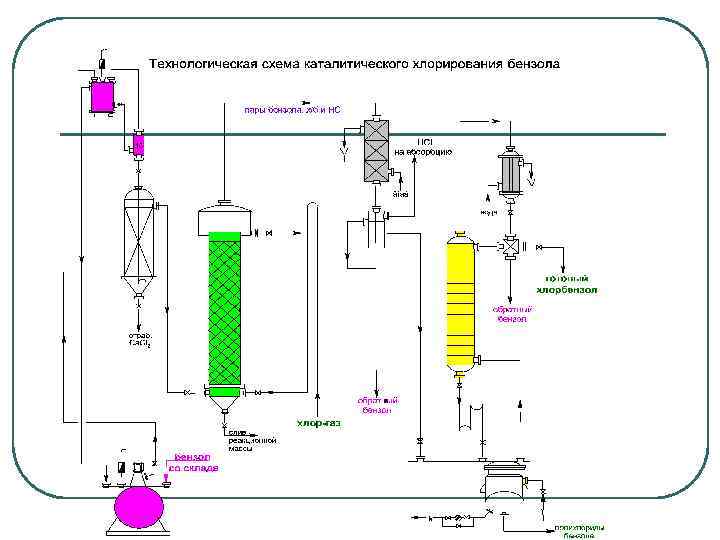
Хлорирование бензола
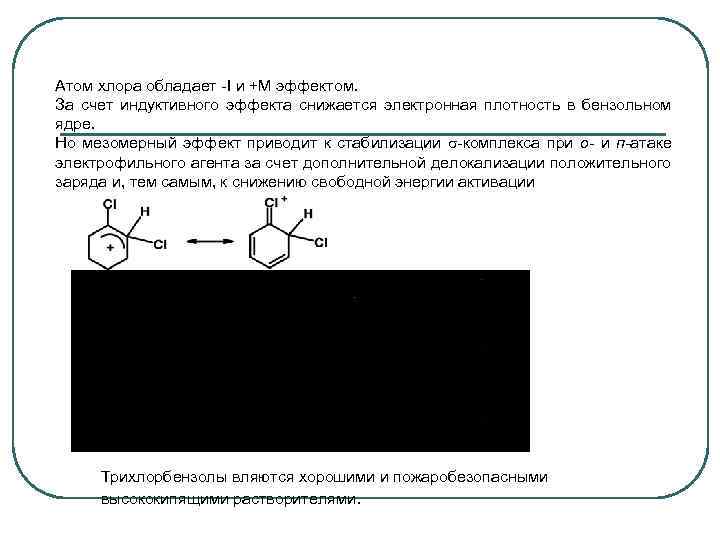
Атом хлора обладает I и +М эффектом. За счет индуктивного эффекта снижается электронная плотность в бензольном ядре. Но мезомерный эффект приводит к стабилизации комплекса при о- и п-атаке электрофильного агента за счет дополнительной делокализации положительного заряда и, тем самым, к снижению свободной энергии активации Трихлорбензолы вляются хорошими и пожаробезопасными высококипящими растворителями.

При наличии в ароматическом ядре электроноакцепторного заместителя региоселективность процесса увеличивается, так как общая скорость реакции хлорирования уменьшается. При хлорировании нитробензола образуется в основном мнитрохлорбензол. Небольшая примесь м-дихлорбензола возникает в результате ипсо-замещения нитрогруппы.
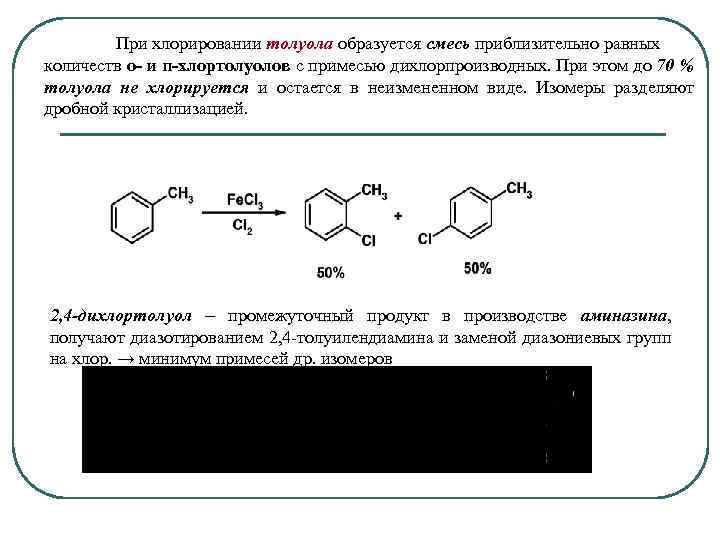
При хлорировании толуола образуется смесь приблизительно равных количеств о- и п-хлортолуолов с примесью дихлорпроизводных. При этом до 70 % толуола не хлорируется и остается в неизмененном виде. Изомеры разделяют дробной кристаллизацией. 2, 4 -дихлортолуол ‒ промежуточный продукт в производстве аминазина, получают диазотированием 2, 4 -толуилендиамина и заменой диазониевых групп на хлор. → минимум примесей др. изомеров
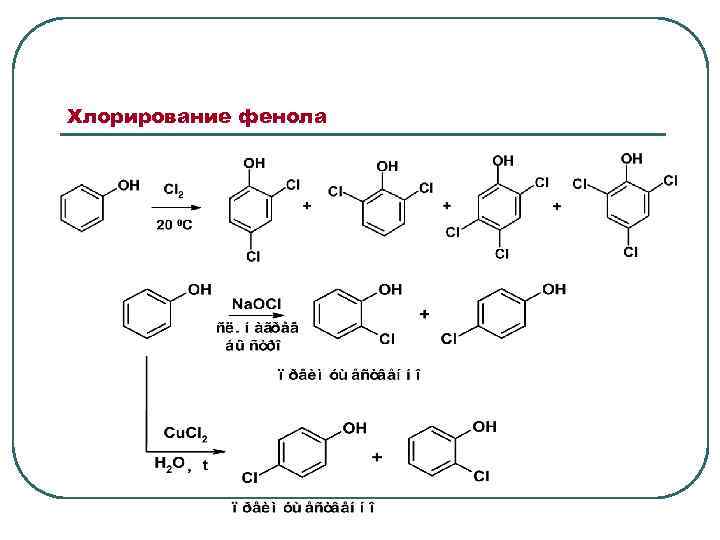
Хлорирование фенола

Хлорирование анилина 4 -амино-3, 5 -дихлорбензолсульфокислота При прямом хлорировании анилина образуется сложная смесь соединений. Поэтому для синтеза индивидуального 2, 6 дихлоранилина блокируют п-положение анилина за счет введения сульфогруппы, которая выполняет функцию защитной группировки. При хлорировании сульфаниловой кислоты образуется только один продукт 4 амино 3, 5 дихлорбензолсульфокислота. Индивидуальный 2, 6 дихлоранилин получают с помощью десульфирования
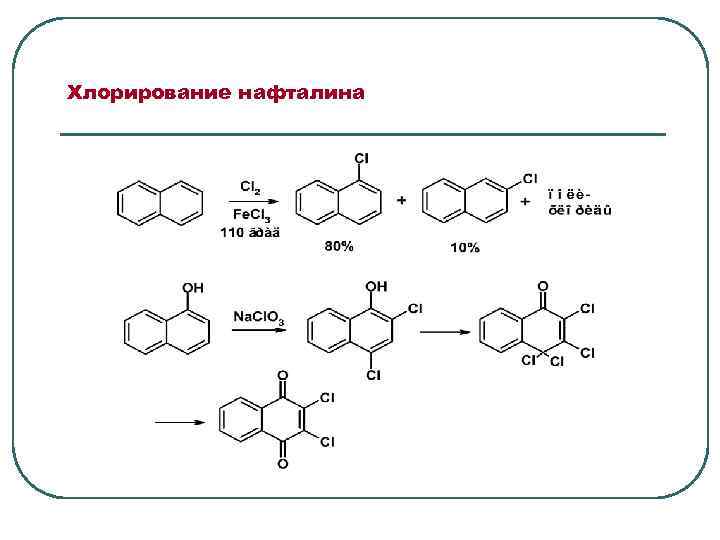
Хлорирование нафталина
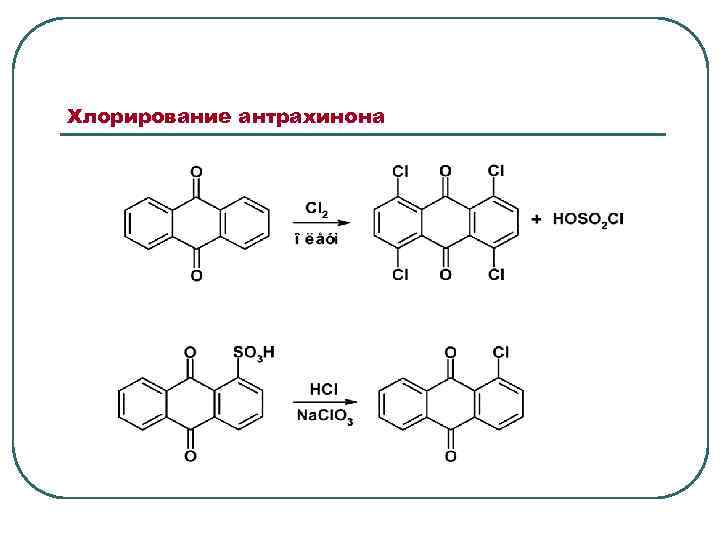
Хлорирование антрахинона

7. 2 Бромирование, йодирование Бром менее сильный электрофил, чем хлор. Реакция более селективна, что позволяет использовать ее в производстве 4 бром о ксилола, промежуточного продукта в синтезе 4 амино о ксилола, который далее используют для получения рибофлавина. хлорирующие агенты не обеспечивают селективность процесса.


Бром является дефицитным сырьем. Улавливание выделяющегося в процессе реакции бромида водорода не является достаточной мерой для утилизации последнего, так как потребность в бромистоводородной кислоте невелика. Для использования всего брома, загружаемого в реактор, можно проводить бромирование в присутствии окислителей. Например: 6 RH + ЗВг 2 + КСl 3 > 6 RBr + КСl + ЗН 2 О Как правило, бромирование ведут молекулярным бромом, выделяющийся бромистый водород улавливают и регенерируют из него бром действием окислителей: 2 НВг + Сl 2 >- 2 НСl + Вг 2 а

противовирусный препарат теброфен
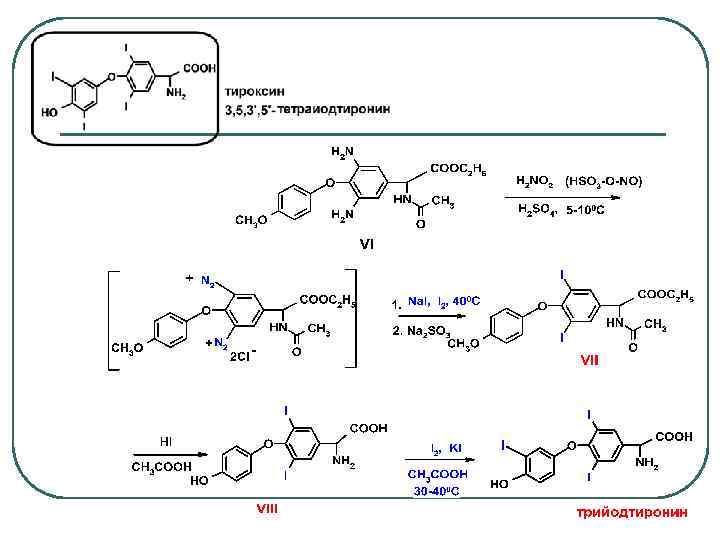

Присоединение галогенов к С=С двойной связи 1. В присутствии инициаторов радикальных реакций в неполярном растворителе реакция идет преимущественно по радикальному механизму. 2. В полярных растворителях основной механизм превращения – гетеролитический –реакция электрофильного присоединения Медленная стадия ‒ образование карбокатиона l Быстро реагирует с анионом брома (X = Br) (при наличии в растворе других анионов или нуклеофилов заместитель Х может отличаться от атома брома) l
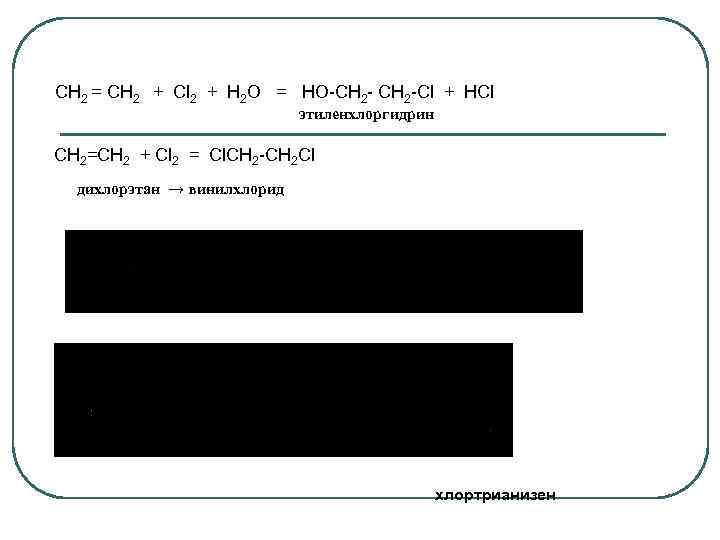
CH 2 = CH 2 + Cl 2 + H 2 O = HO CH 2 Cl + HCl этиленхлоргидрин СН 2=СН 2 + Cl 2 = Cl. СН 2 Cl дихлорэтан → винилхлорид хлортрианизен
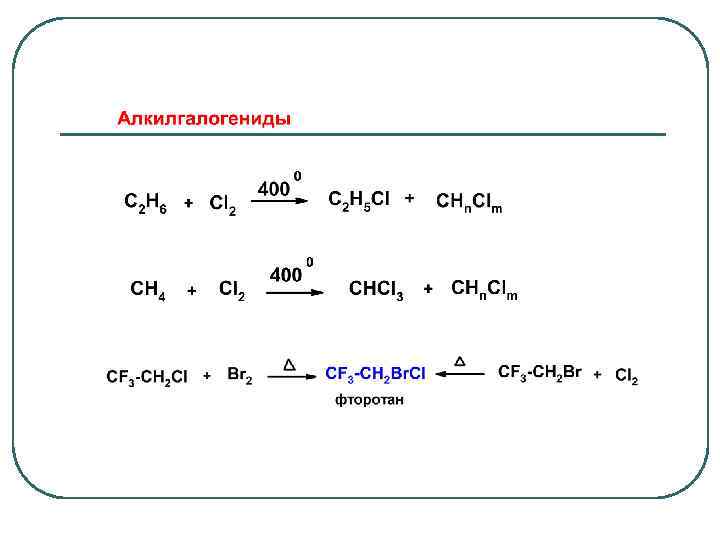
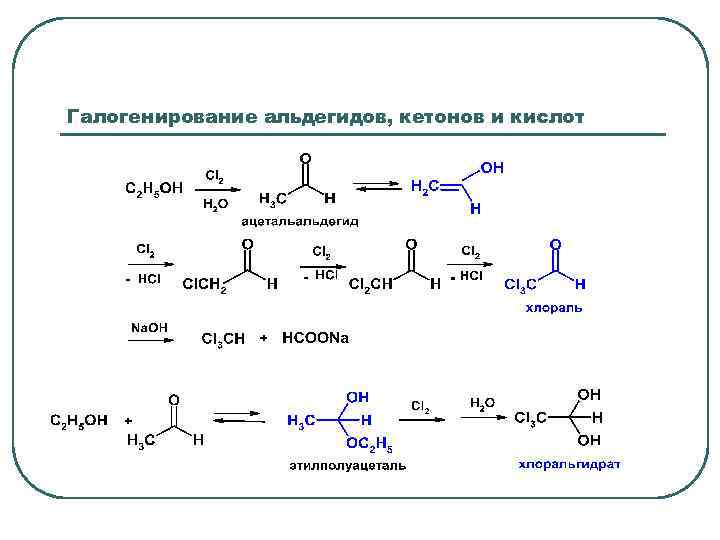
Галогенирование альдегидов, кетонов и кислот

Получение галоидокетонов Фенилэфрин, левомицетин

Галогенирование в боковую цепь

7. 3 Получение фторорганических соединений l C F 0. 139 нм C Cl 0. 177 нм l C H l 0. 109 нм «эффект маскировки» Энергия связи C F 116 ккал связи С Н – 99 ккал. В процессах дегидрирования или замещения водорода фермент не может разорвать связь C F. Аналогично, CF 3 группа мало отличается от СН 3 группы. Но метильная группа обладает слабым электронодонорным эффектом, а трифторметильная группа сильным электроноакцепторным действием. В результате этого в молекуле резко изменяется распределение электронной плотности.

CF 3 CHCl. Br СН 3 OCF 2 CHCl 2 Фторотан метоксифлуран CHF 2 OCF 2 CHFCl энфлуран CF 3 CH 2 OCH=CH 2 FOCH(CF 3)2 флуроксен севофлуран МЕТОДЫ l Низкотемпературное взаимодействие алканов и алкенов с фтором, разбавленным инертным газом. Окислительное фторирование фторидами металлов высшей валентности. l Электрохимическое фторирование в среде фтороводорода. l Получение фторорганических соединений с помощью фтороводорода и соединений общей формулы X Fn. l Превращение кето и карбоксигрупп в дифтор и трифторметильные группы. l Замещение галогенов на фтороводородом или фторидами металлов. l Замещение диазониевой группы. l Синтез новых веществ, исходя из реакционноспособных фторорганических соединений.

перфторированные кетоны Реактор из горизонтально расположенных никелевых трубок, заполненных медными стружками. Реактор имел несколько температурных зон от – 78 0 С до 0 0 С. Внутри трубок небольшое количество субстрата контактирует с фтором, разбавленным гелием или азотом. Время контакта от нескольких дней до недели с постепенным повышением концентрации фтора. Так был получен перфторадамантан, перфторизобутан. Однако способ не позволяет получать вещества в достаточно больших количествах. Лучшие результаты дает аэрозольное низкотемпературное фторирование. Субстрат реакции наносится в виде аэрозоля на микрогранулы фторида калия и фторируется разбавленным фтором. Реактор состоит из модулей с различным температурным режимом. ,
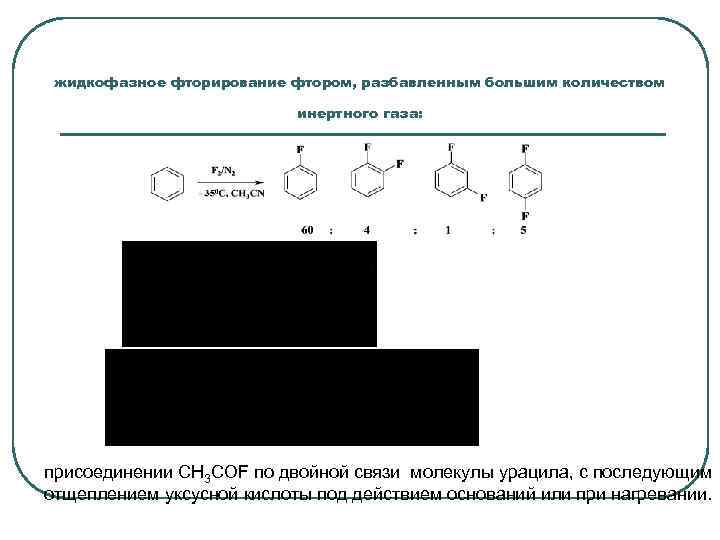
жидкофазное фторирование фтором, разбавленным большим количеством инертного газа: присоединении СH 3 COF по двойной связи молекулы урацила, с последующим отщеплением уксусной кислоты под действием оснований или при нагревании.

Для получения перфторированных углеводородов широко используют фторирование соединений при высокой температуре в парах фторидами металлов высшей валентности. Co. F 3 При этом трифторид превращается в дифторид кобальта. Обратный переход осуществляется пуском слабого тока фтора. Процесс ведут в псевдоожиженном слое. перфторгептан Гептан пропускают первый раз через слой трифторида кобальта при температуре 175 – 2000 С. Конденсируют пары полученного продукта и при слабом токе фтора пропускают через псевдоожиженный слой второй раз при температуре 3000 С.

препараты фторхинолонового ряда Для замещения двух атомов хлора приходится повышать температуру. Исходный 2, 4 дихлор 3 фторнитробензол получают из аминопроизводного с помощью реакции Шимана.


замещение диазониевой группы на фтор – реакция Шимана диазотирование ароматического амина в концентрированной плавиковой кислоте с последующим нагреванием выход целевого продукта незначителен. в основном образуются соответствующие фенолы, так как гидратированный фторид ион является очень слабым нуклеофилом. Применяют твердый нитрит натрия в безводной HF выход фторбензола составляет 75%.

Диазогруппу удалось заменить на фтор с помощью разложения триазена Фенилдиазоний хлорид на первой стадии реагирует с пиперидином, триазен выделяют и проводят реакцию при низкой температуре в концентрированной HF

ПРОВЕДЕНИЕ ПРОЦЕССОВ ГАЛОГЕНИРОВАНИЯ l l l Температура Катализатор Природа растворителя Основные стадии: а) подготовка хлорирующего агента; б) подготовка хлорируемого сырья; в) хлорирование; г) обработка продуктов хлорирования; д) утилизация и очистка отходящих газов.
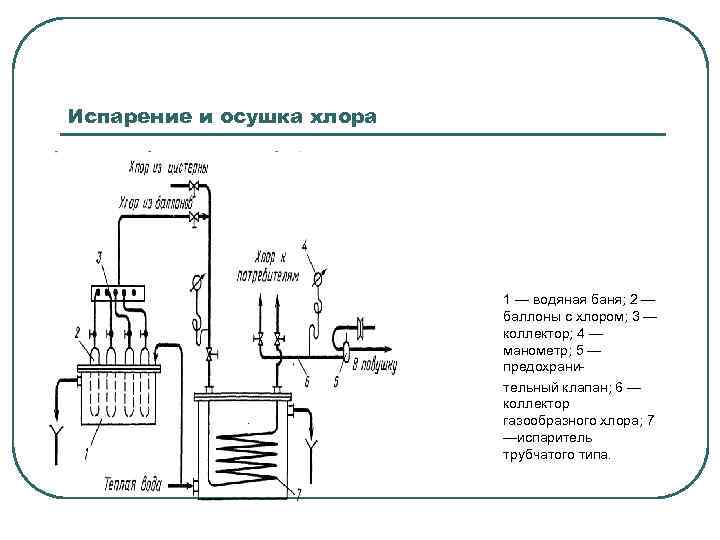
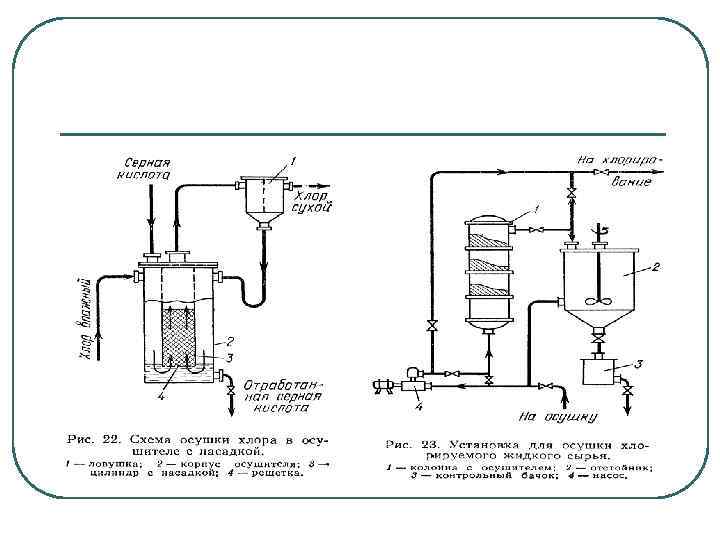
Испарение и осушка хлора 1 — водяная баня; 2 — баллоны с хлором; 3 — коллектор; 4 — манометр; 5 — предохрани тельный клапан; 6 — коллектор газообразного хлора; 7 —испаритель трубчатого типа.
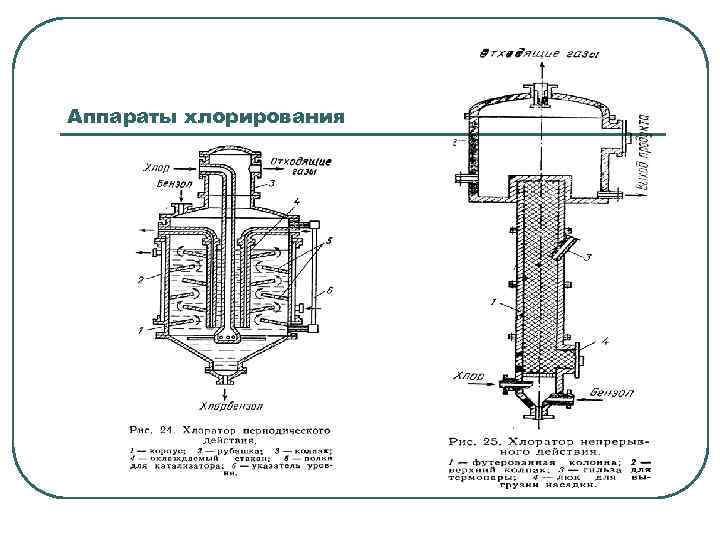
Аппараты хлорирования
ГАЛОГЕНИРОВАНИЕ.ppt