7 ДИСПЕРСНЫЕ СИСТЕМЫ
7 ДИСПЕРСНЫЕ СИСТЕМЫ
 7. 1 7. 2 7. 3 7. 4 Классификация дисперсных систем. Параметры дисперсных систем. Способы выражения концентрации. Методы получения дисперсных систем. 7. 4. 1 Получение лиофильных дисперсных систем 7. 4. 2 Получение лиофобных дисперсных систем 7. 5 Методы очистки. 7. 6 Свойства дисперсных систем. 7. 6. 1 Молекулярно-кинетические свойства. 7. 6. 2 Оптические свойства. 7. 6. 3 Устойчивость дисперсных систем. 7. 6. 4 Нарушение устойчивости дисперсных систем. 7. 6. 5 Электрокинетические свойства
7. 1 7. 2 7. 3 7. 4 Классификация дисперсных систем. Параметры дисперсных систем. Способы выражения концентрации. Методы получения дисперсных систем. 7. 4. 1 Получение лиофильных дисперсных систем 7. 4. 2 Получение лиофобных дисперсных систем 7. 5 Методы очистки. 7. 6 Свойства дисперсных систем. 7. 6. 1 Молекулярно-кинетические свойства. 7. 6. 2 Оптические свойства. 7. 6. 3 Устойчивость дисперсных систем. 7. 6. 4 Нарушение устойчивости дисперсных систем. 7. 6. 5 Электрокинетические свойства
 Дополнительная литература: 1. Мягченков В. А. Поверхностные явления и дисперсные системы. - М. : Колос. С, 2007. – 187 с. 2. Дерягин Б. В. «Успехи химии» , 1979, т. 48, вып. 4, с. 675 -721 3. www. youtube. com/watch? v=8 w 3 Ndyz. Fg. H 8 Дисперсная система (ДС) – это система, в которой хотя бы одно вещество находится в диспергированном (раздробленном) состоянии. Дисперсная фаза (ДФ) – это то, что находится в диспергированном состоянии. Дисперсионная среда – это сплошная однородная среда, в объеме которой распределена дисперсная фаза.
Дополнительная литература: 1. Мягченков В. А. Поверхностные явления и дисперсные системы. - М. : Колос. С, 2007. – 187 с. 2. Дерягин Б. В. «Успехи химии» , 1979, т. 48, вып. 4, с. 675 -721 3. www. youtube. com/watch? v=8 w 3 Ndyz. Fg. H 8 Дисперсная система (ДС) – это система, в которой хотя бы одно вещество находится в диспергированном (раздробленном) состоянии. Дисперсная фаза (ДФ) – это то, что находится в диспергированном состоянии. Дисперсионная среда – это сплошная однородная среда, в объеме которой распределена дисперсная фаза.
 7. 1 Классификация дисперсных систем 1. По размеру частиц ДФ • молекулярно-ионные дисперсные системы Ø < 0, 001 мкм; • коллоидно-дисперсные системы 0, 001< Ø < 0, 1 мкм ; • микрогетерогенные системы 0, 1 < Ø < 10 мкм ; • грубодисперсные системы Ø > 10 мкм. 2. По агрегатному состоянию дисперсной фазы и дисперсионной среды: • с газовой дисперсионной средой: ж/г, т/г, ((ж+т)/г; • с жидкой дисперсионной средой: г/ж, ж/ж, т/ж; • с твердой дисперсионной средой: г/т, ж/т, т/т. 3. По характеру взаимодействия частиц ДФ и молекул дисперсионной среды: • лиофильные системы; • лиофобные системы. 4. По характеру взаимодействия частиц ДФ: • свободнодисперсные (бесструктурные) системы; • связнодисперсные (структурированные) системы.
7. 1 Классификация дисперсных систем 1. По размеру частиц ДФ • молекулярно-ионные дисперсные системы Ø < 0, 001 мкм; • коллоидно-дисперсные системы 0, 001< Ø < 0, 1 мкм ; • микрогетерогенные системы 0, 1 < Ø < 10 мкм ; • грубодисперсные системы Ø > 10 мкм. 2. По агрегатному состоянию дисперсной фазы и дисперсионной среды: • с газовой дисперсионной средой: ж/г, т/г, ((ж+т)/г; • с жидкой дисперсионной средой: г/ж, ж/ж, т/ж; • с твердой дисперсионной средой: г/т, ж/т, т/т. 3. По характеру взаимодействия частиц ДФ и молекул дисперсионной среды: • лиофильные системы; • лиофобные системы. 4. По характеру взаимодействия частиц ДФ: • свободнодисперсные (бесструктурные) системы; • связнодисперсные (структурированные) системы.
 ПИЩЕВЫЕ ДИСПЕРСНЫЕ СИСТЕМЫ Пищевые эмульсии: ж/ж: молоко, сливочное масло, сметана, кремы, желток яичный. Пищевые пены: г/ж: молочный коктейль, газированные напитки, пиво. г/т: хлеб, кондитерские изделия, зефир. Пищевые аэрозоли (образуются в технологическом процессе): ж/г: молоко в процессе распылительной сушки. т/г: мучная пыль, сахарная пыль. Пищевые порошки: т/г: мука, сахарный песок и пудра, сухой кисель, яичный порошок Пищевые суспензии, золи, пасты и др. : т/ж: нерафинированное масло, кетчуп, протертые супы, растворы крахмала и белков ж/т: колбасный фарш, сырковая масса, пасты, паштеты. т/т: мышечная ткань, шоколад, замороженное сливочное масло
ПИЩЕВЫЕ ДИСПЕРСНЫЕ СИСТЕМЫ Пищевые эмульсии: ж/ж: молоко, сливочное масло, сметана, кремы, желток яичный. Пищевые пены: г/ж: молочный коктейль, газированные напитки, пиво. г/т: хлеб, кондитерские изделия, зефир. Пищевые аэрозоли (образуются в технологическом процессе): ж/г: молоко в процессе распылительной сушки. т/г: мучная пыль, сахарная пыль. Пищевые порошки: т/г: мука, сахарный песок и пудра, сухой кисель, яичный порошок Пищевые суспензии, золи, пасты и др. : т/ж: нерафинированное масло, кетчуп, протертые супы, растворы крахмала и белков ж/т: колбасный фарш, сырковая масса, пасты, паштеты. т/т: мышечная ткань, шоколад, замороженное сливочное масло
 7. 2 Параметры дисперсных систем 1. Поперечный размер (d). 2. Дисперсность (D) 3. Удельная поверхность (Sуд): • для шарообразных или • для цилиндрических • для пластинчатых 4. Кривизна поверхности (Н) :
7. 2 Параметры дисперсных систем 1. Поперечный размер (d). 2. Дисперсность (D) 3. Удельная поверхность (Sуд): • для шарообразных или • для цилиндрических • для пластинчатых 4. Кривизна поверхности (Н) :
 7. 3 Способы выражения концентрации дисперсных систем 1. Численная : 2. Массовая : 3. Объемная:
7. 3 Способы выражения концентрации дисперсных систем 1. Численная : 2. Массовая : 3. Объемная:
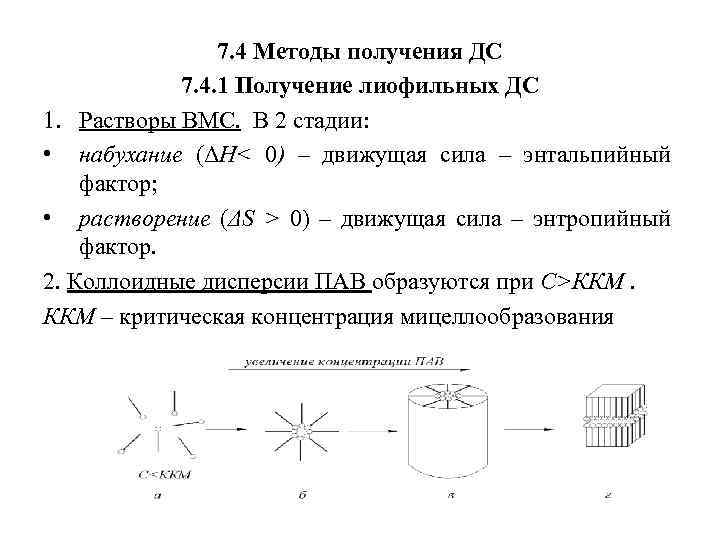 7. 4 Методы получения ДС 7. 4. 1 Получение лиофильных ДС 1. Растворы ВМС. В 2 стадии: • набухание (ΔН< 0) – движущая сила – энтальпийный фактор; • растворение (ΔS > 0) – движущая сила – энтропийный фактор. 2. Коллоидные дисперсии ПАВ образуются при С>ККМ. ККМ – критическая концентрация мицеллообразования
7. 4 Методы получения ДС 7. 4. 1 Получение лиофильных ДС 1. Растворы ВМС. В 2 стадии: • набухание (ΔН< 0) – движущая сила – энтальпийный фактор; • растворение (ΔS > 0) – движущая сила – энтропийный фактор. 2. Коллоидные дисперсии ПАВ образуются при С>ККМ. ККМ – критическая концентрация мицеллообразования
 7. 4. 2 Методы получения лиофобных дисперсных систем A. Метод диспергирования. Правило Кирпичева-Кика: Wдр=k. V Правило Риттингера: Wизм= σ*ΔS Wдисп = Wдр + Wизм= k. V + σ*ΔS
7. 4. 2 Методы получения лиофобных дисперсных систем A. Метод диспергирования. Правило Кирпичева-Кика: Wдр=k. V Правило Риттингера: Wизм= σ*ΔS Wдисп = Wдр + Wизм= k. V + σ*ΔS
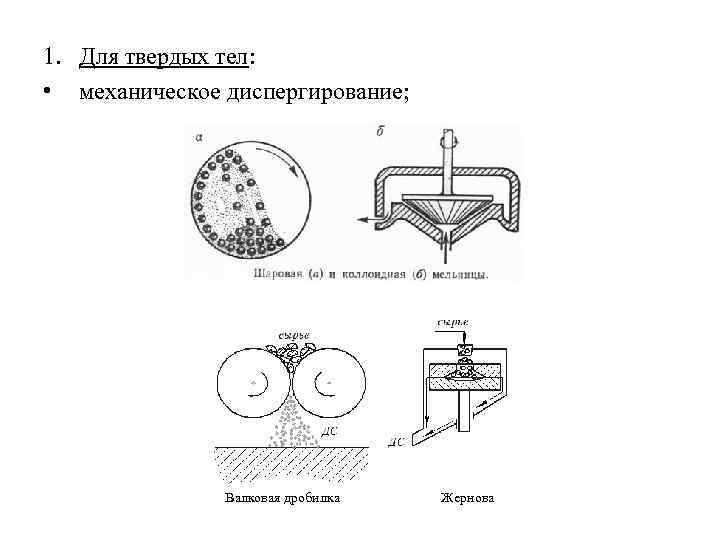 1. Для твердых тел: • механическое диспергирование; Валковая дробилка Жернова
1. Для твердых тел: • механическое диспергирование; Валковая дробилка Жернова
 • действие ультразвуком (ν > 20 к. Гц);
• действие ультразвуком (ν > 20 к. Гц);
 • электрогидравлическое диспергирование металлов (метод Бредига); • химическое диспергирование (пептизация). 2. Для жидкостей: • встряхивание; • применение перемешивающих устройств (смесителей);
• электрогидравлическое диспергирование металлов (метод Бредига); • химическое диспергирование (пептизация). 2. Для жидкостей: • встряхивание; • применение перемешивающих устройств (смесителей);
 • использование гомогенизаторов;
• использование гомогенизаторов;
 • электрическое диспергирование; • самопроизвольное диспергирование жидкости при температурах, близких к КТР; • введение в систему из двух несмешивающихся жидкостей специальных эмульгаторов – поверхностно -активных веществ.
• электрическое диспергирование; • самопроизвольное диспергирование жидкости при температурах, близких к КТР; • введение в систему из двух несмешивающихся жидкостей специальных эмульгаторов – поверхностно -активных веществ.
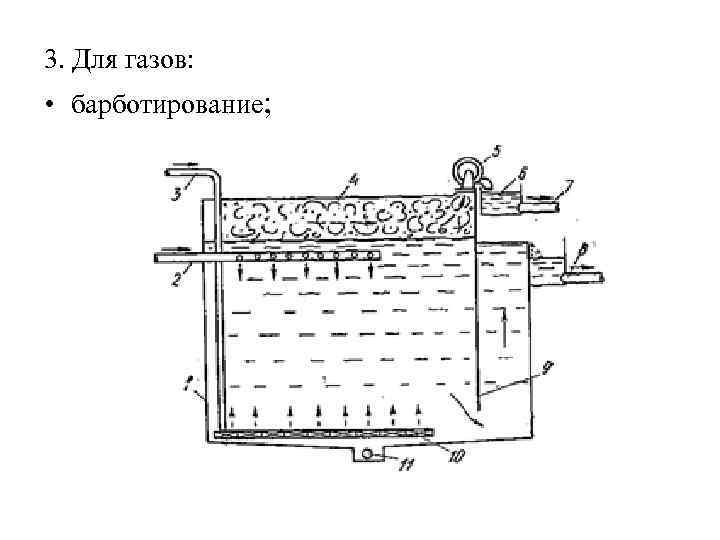 3. Для газов: • барботирование;
3. Для газов: • барботирование;
 • одновременное течение жидкости и газа под давлением через диспергирующие устройства – пористые фильтры, тонкие трубки, сопла и т. д. Б. Метод конденсации 1. Химический метод. 2. Физико-химический метод: • метод замены растворителя; • создание пересыщенной системы путем понижения температуры или путем повышения давления; • двухстадийный метод изменения температуры, при котором вещество или раствор нагревают с образованием пара, затем охлаждают (аэрозольный метод, распылительная сушка и другие).
• одновременное течение жидкости и газа под давлением через диспергирующие устройства – пористые фильтры, тонкие трубки, сопла и т. д. Б. Метод конденсации 1. Химический метод. 2. Физико-химический метод: • метод замены растворителя; • создание пересыщенной системы путем понижения температуры или путем повышения давления; • двухстадийный метод изменения температуры, при котором вещество или раствор нагревают с образованием пара, затем охлаждают (аэрозольный метод, распылительная сушка и другие).
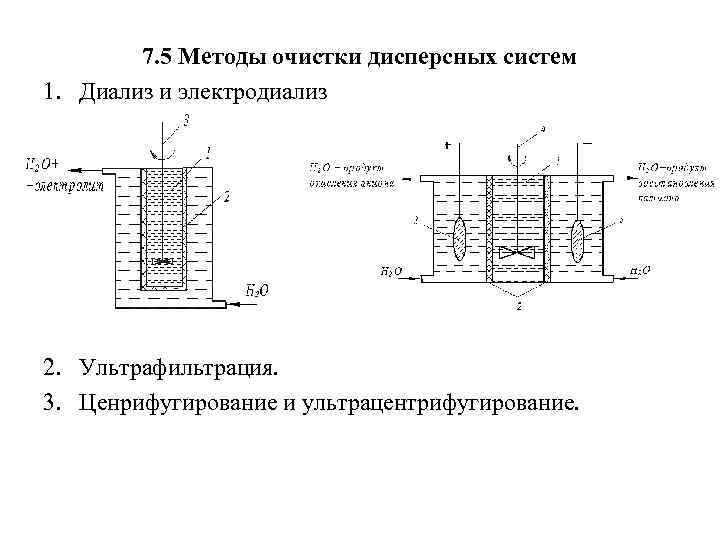 7. 5 Методы очистки дисперсных систем 1. Диализ и электродиализ 2. Ультрафильтрация. 3. Ценрифугирование и ультрацентрифугирование.
7. 5 Методы очистки дисперсных систем 1. Диализ и электродиализ 2. Ультрафильтрация. 3. Ценрифугирование и ультрацентрифугирование.
 7. 6 Факторы устойчивости дисперсных систем При проведении технологических процессов с участием ДС всегда приходится решать противоположные задачи – стабилизировать ДС или, наоборот, разрушать ее. Несмотря на особенности методов стабилизации и разрушения для каждого типа ДС, все они опираются на определенные общие принципы. Различают 2 вида устойчивости ДС (Н. Н. Песков 1917 г. ): • агрегативная устойчивость – это способность ДС противостоять процессам, приводящим к уменьшению ее свободной поверхностной энергии путем сохранения степени дисперсности; • седиментационная устойчивость – это способность частиц ДФ находиться во взвешенном состоянии под действием броуновского движения.
7. 6 Факторы устойчивости дисперсных систем При проведении технологических процессов с участием ДС всегда приходится решать противоположные задачи – стабилизировать ДС или, наоборот, разрушать ее. Несмотря на особенности методов стабилизации и разрушения для каждого типа ДС, все они опираются на определенные общие принципы. Различают 2 вида устойчивости ДС (Н. Н. Песков 1917 г. ): • агрегативная устойчивость – это способность ДС противостоять процессам, приводящим к уменьшению ее свободной поверхностной энергии путем сохранения степени дисперсности; • седиментационная устойчивость – это способность частиц ДФ находиться во взвешенном состоянии под действием броуновского движения.
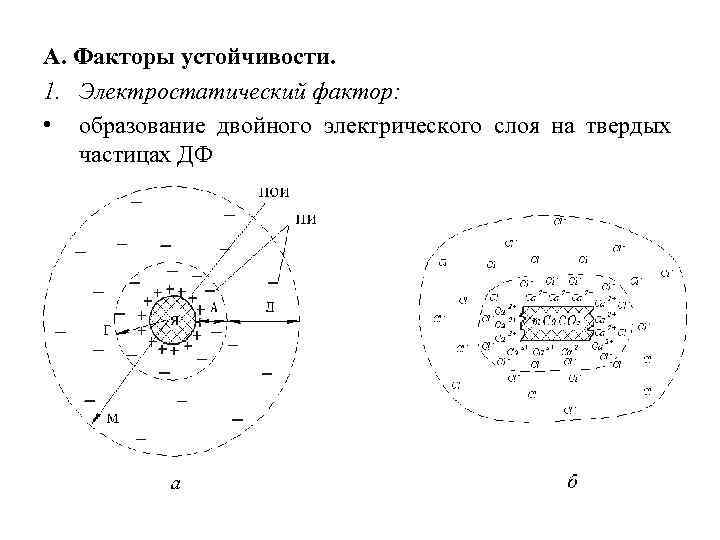 А. Факторы устойчивости. 1. Электростатический фактор: • образование двойного электрического слоя на твердых частицах ДФ
А. Факторы устойчивости. 1. Электростатический фактор: • образование двойного электрического слоя на твердых частицах ДФ
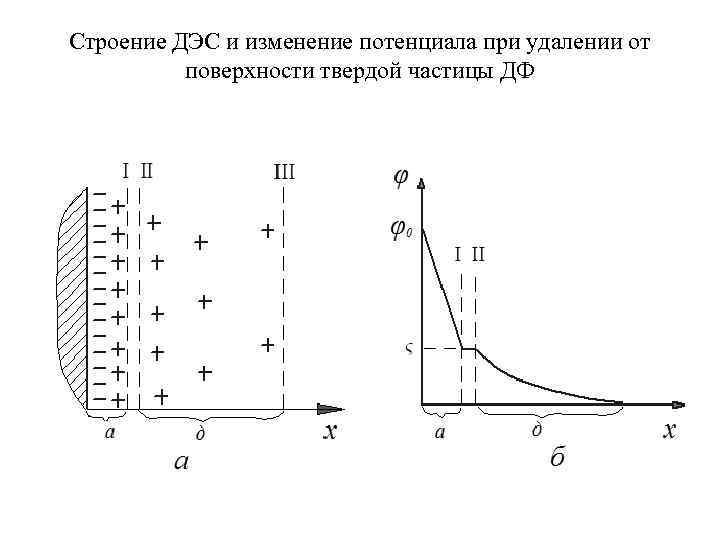 Строение ДЭС и изменение потенциала при удалении от поверхности твердой частицы ДФ
Строение ДЭС и изменение потенциала при удалении от поверхности твердой частицы ДФ
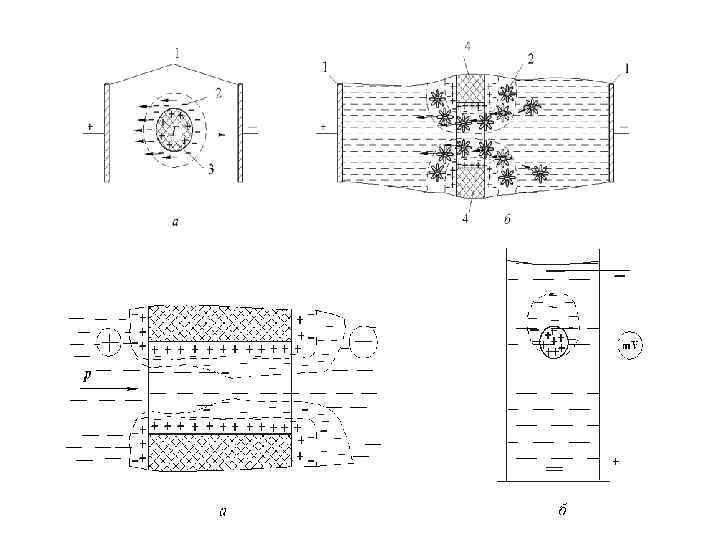
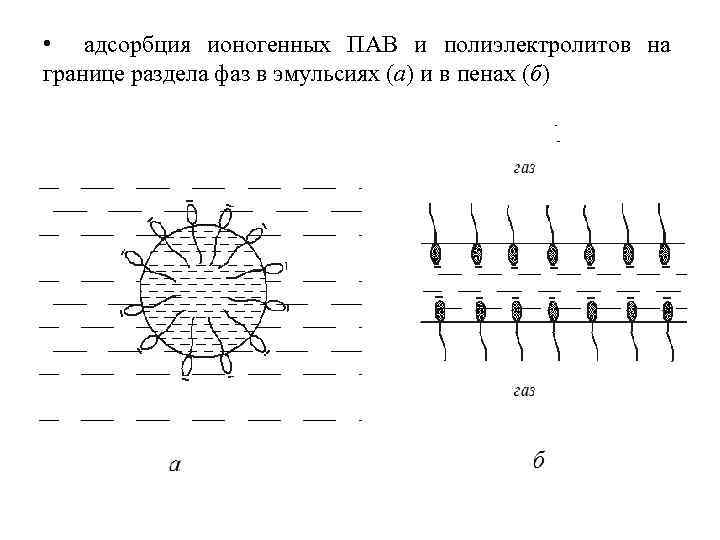 • адсорбция ионогенных ПАВ и полиэлектролитов на границе раздела фаз в эмульсиях (а) и в пенах (б)
• адсорбция ионогенных ПАВ и полиэлектролитов на границе раздела фаз в эмульсиях (а) и в пенах (б)
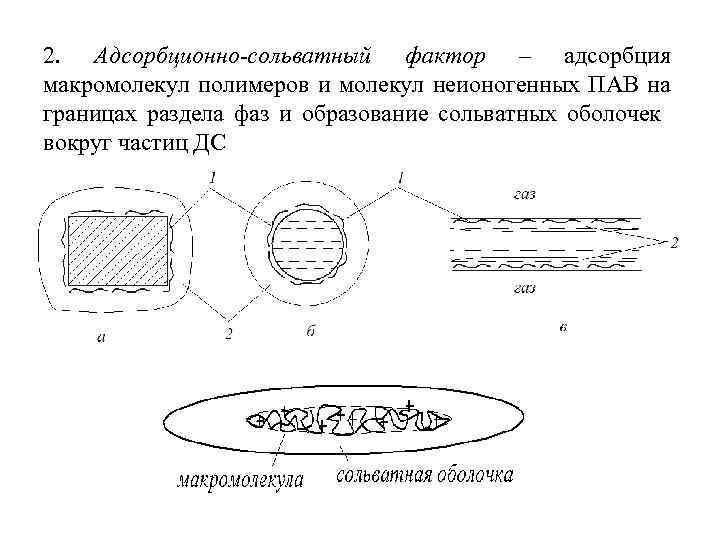 2. Адсорбционно-сольватный фактор – адсорбция макромолекул полимеров и молекул неионогенных ПАВ на границах раздела фаз и образование сольватных оболочек вокруг частиц ДС
2. Адсорбционно-сольватный фактор – адсорбция макромолекул полимеров и молекул неионогенных ПАВ на границах раздела фаз и образование сольватных оболочек вокруг частиц ДС
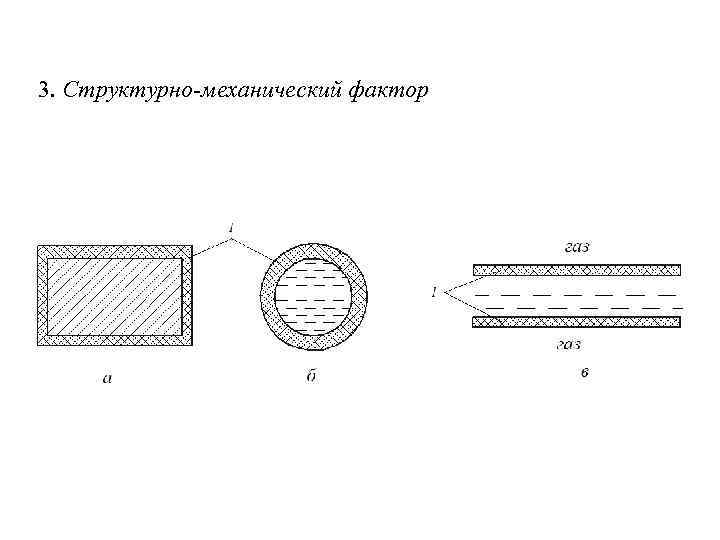 3. Структурно-механический фактор
3. Структурно-механический фактор
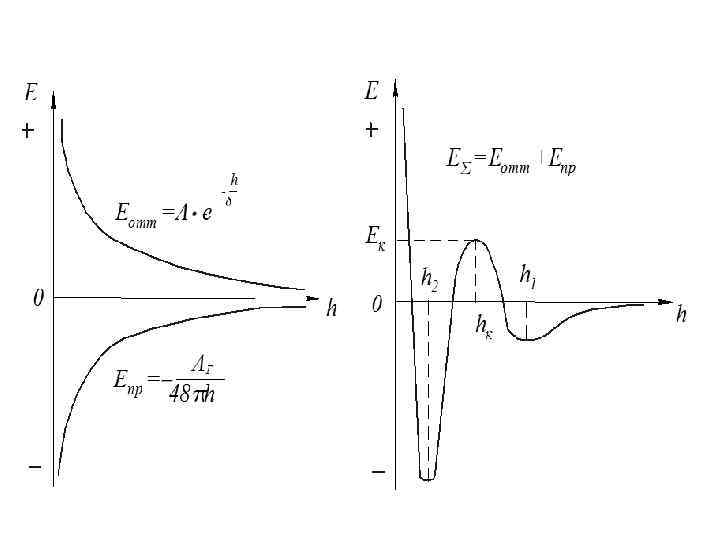
 4. Энтропийный фактор S = R∙ln w 5. Гидродинамический фактор. Б. Разрушение ДС происходит при ослаблении факторов устойчивости Теория ДЛФО (Б. В. Дерягин, Л. Д. Ландау, Е. Фервей, Дж. Овербек) Агрегативная устойчивость ДС определяется балансом сил: • электростатического отталкивания с энергией Еотт˃0; • ван-дер-ваальсовы силы притяжения с энергией Епр˂0.
4. Энтропийный фактор S = R∙ln w 5. Гидродинамический фактор. Б. Разрушение ДС происходит при ослаблении факторов устойчивости Теория ДЛФО (Б. В. Дерягин, Л. Д. Ландау, Е. Фервей, Дж. Овербек) Агрегативная устойчивость ДС определяется балансом сил: • электростатического отталкивания с энергией Еотт˃0; • ван-дер-ваальсовы силы притяжения с энергией Епр˂0.
 • Действие электростатического фактора стабилизации может быть снижено или нейтрализовано путем добавления электролитов, ионы которых вызывают существенные изменения в структуре ДЭС. • Адсорбционно-сольватный фактор можно исключить, если разрушить сольватные оболочки частиц ДФ путем лиофобизации их поверхности, а также осуществив десорбцию стабилизатора - молекул ПАВ – из поверхности. • Структурно-механический фактор может быть устранен путем разрушения пленок на поверхности частиц ДФ. Для этой цели в ДС добавляют растворитель, который растворяет пленку, или химически реагент, который реагирует с веществом пленки и разрушает ее. • Действие гидродинамического фактора можно снижать путем уменьшения вязкости ДС. Для этого ДС нагревают или добавляют растворитель, имеющий меньшую вязкость.
• Действие электростатического фактора стабилизации может быть снижено или нейтрализовано путем добавления электролитов, ионы которых вызывают существенные изменения в структуре ДЭС. • Адсорбционно-сольватный фактор можно исключить, если разрушить сольватные оболочки частиц ДФ путем лиофобизации их поверхности, а также осуществив десорбцию стабилизатора - молекул ПАВ – из поверхности. • Структурно-механический фактор может быть устранен путем разрушения пленок на поверхности частиц ДФ. Для этой цели в ДС добавляют растворитель, который растворяет пленку, или химически реагент, который реагирует с веществом пленки и разрушает ее. • Действие гидродинамического фактора можно снижать путем уменьшения вязкости ДС. Для этого ДС нагревают или добавляют растворитель, имеющий меньшую вязкость.
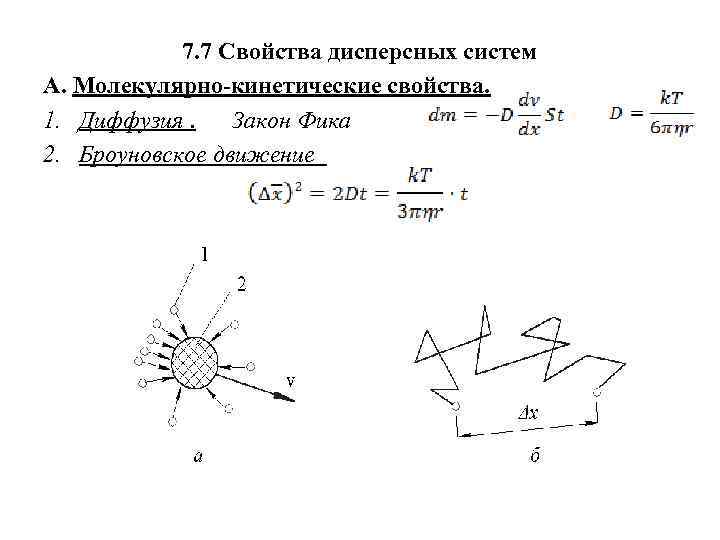 7. 7 Свойства дисперсных систем А. Молекулярно-кинетические свойства. 1. Диффузия. Закон Фика 2. Броуновское движение
7. 7 Свойства дисперсных систем А. Молекулярно-кинетические свойства. 1. Диффузия. Закон Фика 2. Броуновское движение
 3. Диффузионно-седиментационное равновесие. Формула Стокса: Гипсометрический закон Лапласа: , где 4. Осмотическое давление.
3. Диффузионно-седиментационное равновесие. Формула Стокса: Гипсометрический закон Лапласа: , где 4. Осмотическое давление.
 5. Мембранное равновесие Доннана.
5. Мембранное равновесие Доннана.
 Б. Оптические свойства. Видимая часть спектра излучения 400… 700 нм. Рассеяние ‒ при r / λ< 0, 05; отражение ‒ при r> λ ; поглощение ‒ при окрашенных частицах ДФ.
Б. Оптические свойства. Видимая часть спектра излучения 400… 700 нм. Рассеяние ‒ при r / λ< 0, 05; отражение ‒ при r> λ ; поглощение ‒ при окрашенных частицах ДФ.
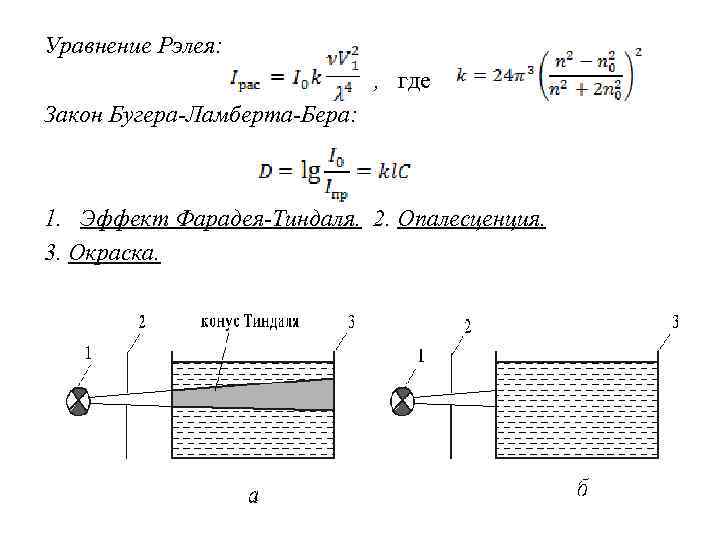 Уравнение Рэлея: , где Закон Бугера-Ламберта-Бера: 1. Эффект Фарадея-Тиндаля. 2. Опалесценция. 3. Окраска.
Уравнение Рэлея: , где Закон Бугера-Ламберта-Бера: 1. Эффект Фарадея-Тиндаля. 2. Опалесценция. 3. Окраска.
 В. Электрокинетические свойства. 1. Электрофорез. 2. Электроосмос. 3. Эффект Дорна (возникновение потенциала седиментации). 4. Эффект Квинке (возникновение потенциала течения).
В. Электрокинетические свойства. 1. Электрофорез. 2. Электроосмос. 3. Эффект Дорна (возникновение потенциала седиментации). 4. Эффект Квинке (возникновение потенциала течения).