 « 7 ЧУДЕС В ЖИВОЙ И НЕЖИВОЙ ПРИРОДЕ » « 7 WONDERS OF THE LIVING AND NON-LIVING NATURE”
« 7 ЧУДЕС В ЖИВОЙ И НЕЖИВОЙ ПРИРОДЕ » « 7 WONDERS OF THE LIVING AND NON-LIVING NATURE”
 «Жить – это значит узнавать… Жить – это значит творить, трудясь без устали, с неисчерпаемым вдохновением!» Д. И. Менделеев «Live means learning to live. . . – it means to create, working tirelessly, with endless inspiration!» D. I. Mendeleev
«Жить – это значит узнавать… Жить – это значит творить, трудясь без устали, с неисчерпаемым вдохновением!» Д. И. Менделеев «Live means learning to live. . . – it means to create, working tirelessly, with endless inspiration!» D. I. Mendeleev
 Oxidation-reduction reactions belong to more common chemical reactions and they have a huge meaning in theory and practice- because oxidation regeneration (reconstruction) is one of the most important process in Nature. The life of any living creature is connected with these reactions: the process of metabolism, fermentation, breathing, photosynthesis which provides oxygen; decomposition of organic residues-which provides humus, burning (combustion). Many natural phenomena are accompanied with oxidation-reduction processes, such as: lightning, volcanic eruption. Also oxidationreduction processes can be observed during explosions, combustion of fuels, metal corrosion, electrolysis and metal smelting. People use them to get alkalis, acids and many other valuable chemicals. The same reactions are the basis of conversion(transformation) of chemical energy into electric in galvanic and fuel elements. So, we can consider, that the world around us is giant chemical laboratory where different chemical reactions take place each second, mainly oxidation -reduction reactions.
Oxidation-reduction reactions belong to more common chemical reactions and they have a huge meaning in theory and practice- because oxidation regeneration (reconstruction) is one of the most important process in Nature. The life of any living creature is connected with these reactions: the process of metabolism, fermentation, breathing, photosynthesis which provides oxygen; decomposition of organic residues-which provides humus, burning (combustion). Many natural phenomena are accompanied with oxidation-reduction processes, such as: lightning, volcanic eruption. Also oxidationreduction processes can be observed during explosions, combustion of fuels, metal corrosion, electrolysis and metal smelting. People use them to get alkalis, acids and many other valuable chemicals. The same reactions are the basis of conversion(transformation) of chemical energy into electric in galvanic and fuel elements. So, we can consider, that the world around us is giant chemical laboratory where different chemical reactions take place each second, mainly oxidation -reduction reactions.
 Объект изучения: ОКИСЛИТЕЛЬНОВОССТАНОВИТЕЛЬНЫЕ РЕАКЦИИ
Объект изучения: ОКИСЛИТЕЛЬНОВОССТАНОВИТЕЛЬНЫЕ РЕАКЦИИ
 Цель урока Выявить положительные и отрицательные стороны воздействия окислительновосстановительных реакций в природе
Цель урока Выявить положительные и отрицательные стороны воздействия окислительновосстановительных реакций в природе
 Задачи • дать определение ОВР; • рассмотреть алгоритм проставления степени окисления в веществах; • рассмотреть алгоритм проставления коэффициентов методом электронного и электронно-ионного баланса; • рассмотреть ОВР, протекающие в природе; • выявить плюсы и минусы ОВР, протекающих в природе.
Задачи • дать определение ОВР; • рассмотреть алгоритм проставления степени окисления в веществах; • рассмотреть алгоритм проставления коэффициентов методом электронного и электронно-ионного баланса; • рассмотреть ОВР, протекающие в природе; • выявить плюсы и минусы ОВР, протекающих в природе.
 Chemical terms Oxidation-reduction reactions belong to more common chemical reactions and they have a huge meaning in theory and practice- because oxidation regeneration (reconstruction) is one of the most important process in Nature. The life of any living creature is connected with these reactions: the process of metabolism, fermentation, breathing, photosynthesis which provides oxygen; decomposition of organic residues-which provides humus, burning (combustion). Many natural phenomena are accompanied with oxidation-reduction processes, such as: lightning, volcanic eruption. Also oxidation-reduction processes can be observed during explosions, combustion of fuels, metal corrosion, electrolysis and metal smelting. People use them to get alkalis, acids and many other valuable chemicals. The same reactions are the basis of conversion(transformation) of chemical energy into electric in galvanic and fuel elements. So, we can consider, that the world around us is giant chemical laboratory where different chemical reactions take place each second, mainly oxidation-reduction reactions.
Chemical terms Oxidation-reduction reactions belong to more common chemical reactions and they have a huge meaning in theory and practice- because oxidation regeneration (reconstruction) is one of the most important process in Nature. The life of any living creature is connected with these reactions: the process of metabolism, fermentation, breathing, photosynthesis which provides oxygen; decomposition of organic residues-which provides humus, burning (combustion). Many natural phenomena are accompanied with oxidation-reduction processes, such as: lightning, volcanic eruption. Also oxidation-reduction processes can be observed during explosions, combustion of fuels, metal corrosion, electrolysis and metal smelting. People use them to get alkalis, acids and many other valuable chemicals. The same reactions are the basis of conversion(transformation) of chemical energy into electric in galvanic and fuel elements. So, we can consider, that the world around us is giant chemical laboratory where different chemical reactions take place each second, mainly oxidation-reduction reactions.
 Окислительно-восстановительные процессы принадлежат к числу наиболее распространенных химических реакций. Окислительно–восстановительные процессы в живом организме играют важную роль. С ним связаны дыхание и обмен веществ в живых организмах, брожение, фотосинтез в зеленых частях растений и нервная деятельность человека и животных. Они основа жизни на Земле.
Окислительно-восстановительные процессы принадлежат к числу наиболее распространенных химических реакций. Окислительно–восстановительные процессы в живом организме играют важную роль. С ним связаны дыхание и обмен веществ в живых организмах, брожение, фотосинтез в зеленых частях растений и нервная деятельность человека и животных. Они основа жизни на Земле.
 НИИ «Химические отношения» . Срочно. Просим представить информацию об окислительно-восстановительных реакциях, происходящих на планете Земля, для расширения научных контактов с учеными планеты Марс.
НИИ «Химические отношения» . Срочно. Просим представить информацию об окислительно-восстановительных реакциях, происходящих на планете Земля, для расширения научных контактов с учеными планеты Марс.
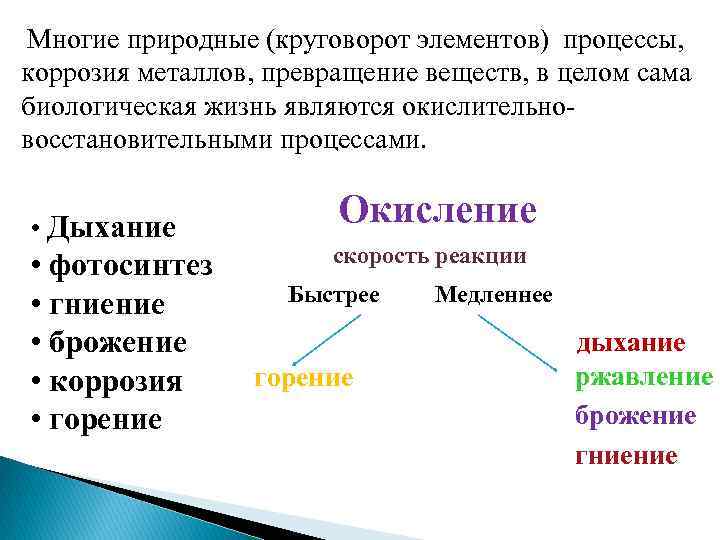 Многие природные (круговорот элементов) процессы, коррозия металлов, превращение веществ, в целом сама биологическая жизнь являются окислительновосстановительными процессами. • Дыхание • фотосинтез • гниение • брожение • коррозия • горение Окисление скорость реакции Быстрее горение Медленнее дыхание ржавление брожение гниение
Многие природные (круговорот элементов) процессы, коррозия металлов, превращение веществ, в целом сама биологическая жизнь являются окислительновосстановительными процессами. • Дыхание • фотосинтез • гниение • брожение • коррозия • горение Окисление скорость реакции Быстрее горение Медленнее дыхание ржавление брожение гниение

 Окислительно-восстановительные реакции (ОВР) - это такие реакции, при которых происходит изменение степеней окисления атомов химических элементов или ионов, образующих реагирующие вещества. Окисление – это процесс отдачи электронов. Восстановление – это процесс принятия электронов.
Окислительно-восстановительные реакции (ОВР) - это такие реакции, при которых происходит изменение степеней окисления атомов химических элементов или ионов, образующих реагирующие вещества. Окисление – это процесс отдачи электронов. Восстановление – это процесс принятия электронов.
 Окислитель – это атом или нейтральная молекула, которая в процессе реакции принимает электроны. Восстановитель - это атом или нейтральная молекула, которая в процессе реакции отдает электроны.
Окислитель – это атом или нейтральная молекула, которая в процессе реакции принимает электроны. Восстановитель - это атом или нейтральная молекула, которая в процессе реакции отдает электроны.
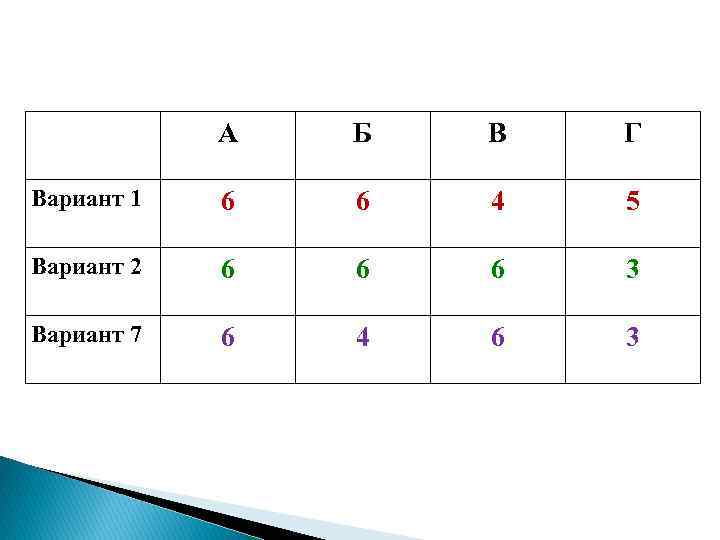 А Б В Г Вариант 1 6 6 4 5 Вариант 2 6 6 6 3 Вариант 7 6 4 6 3
А Б В Г Вариант 1 6 6 4 5 Вариант 2 6 6 6 3 Вариант 7 6 4 6 3
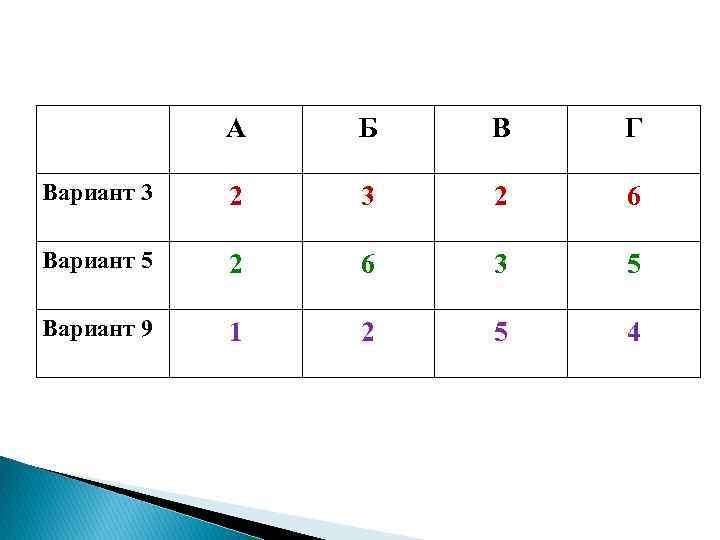 А Б В Г Вариант 3 2 6 Вариант 5 2 6 3 5 Вариант 9 1 2 5 4
А Б В Г Вариант 3 2 6 Вариант 5 2 6 3 5 Вариант 9 1 2 5 4
 Химики прошлого прозвали перманганат калия «таинственный хамелеон» . В подкисленном растворе образуются бесцветные катионы Mn 2+ : 2 KMn. O 4 + 5 Na 2 SO 3 + 3 H 2 SO 4 = 2 Mn. SO 4 + 5 Na 2 SO 4 + K 2 SO 4 + 3 H 2 O В сильнощелочной среде образуются манганат-анионы Mn. O 42 - зеленого цвета: 2 KMn. O 4 + Na 2 SO 3 + 2 KOH = 2 K 2 Mn. O 4 + Na 2 SO 4 + H 2 O Перманганат калия, попадая на кожу, разлагается с выделением бурого осадка диоксида марганца Mn. O 2. В зависимости от концентрации раствора, а значит, – от количества осадка, диоксид марганца оказывает вяжущее либо прижигающее действие. 2 KMn. O 4 + 3 Na 2 SO 3 + H 2 O = 2 Mn. O 2 + 3 Na 2 SO 4 + 2 KOH
Химики прошлого прозвали перманганат калия «таинственный хамелеон» . В подкисленном растворе образуются бесцветные катионы Mn 2+ : 2 KMn. O 4 + 5 Na 2 SO 3 + 3 H 2 SO 4 = 2 Mn. SO 4 + 5 Na 2 SO 4 + K 2 SO 4 + 3 H 2 O В сильнощелочной среде образуются манганат-анионы Mn. O 42 - зеленого цвета: 2 KMn. O 4 + Na 2 SO 3 + 2 KOH = 2 K 2 Mn. O 4 + Na 2 SO 4 + H 2 O Перманганат калия, попадая на кожу, разлагается с выделением бурого осадка диоксида марганца Mn. O 2. В зависимости от концентрации раствора, а значит, – от количества осадка, диоксид марганца оказывает вяжущее либо прижигающее действие. 2 KMn. O 4 + 3 Na 2 SO 3 + H 2 O = 2 Mn. O 2 + 3 Na 2 SO 4 + 2 KOH
 HOW DOES REDOX REACTION EFFECT PEOPLE’S LIVES? DOES IT HAVE ONLY POSITIVE EFFECT? ASK THESE QUESTIONS TO REACTIONS THEMSELVES AND GUESS THEIR NAMES!
HOW DOES REDOX REACTION EFFECT PEOPLE’S LIVES? DOES IT HAVE ONLY POSITIVE EFFECT? ASK THESE QUESTIONS TO REACTIONS THEMSELVES AND GUESS THEIR NAMES!
 WHO AM I ?
WHO AM I ?
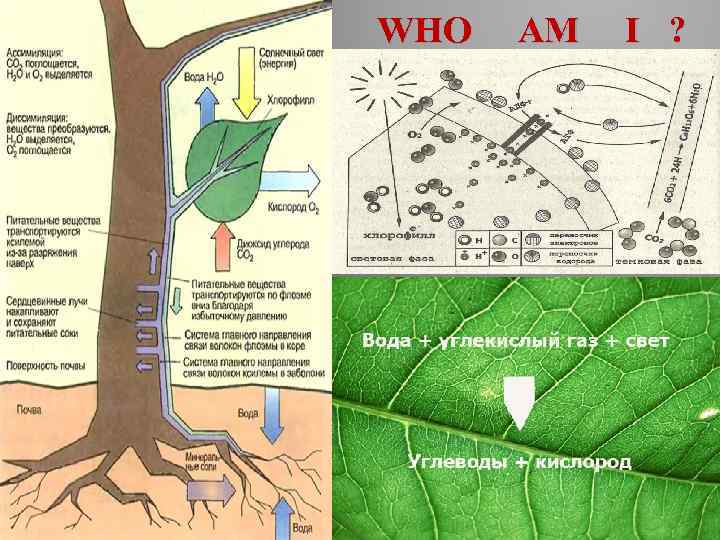
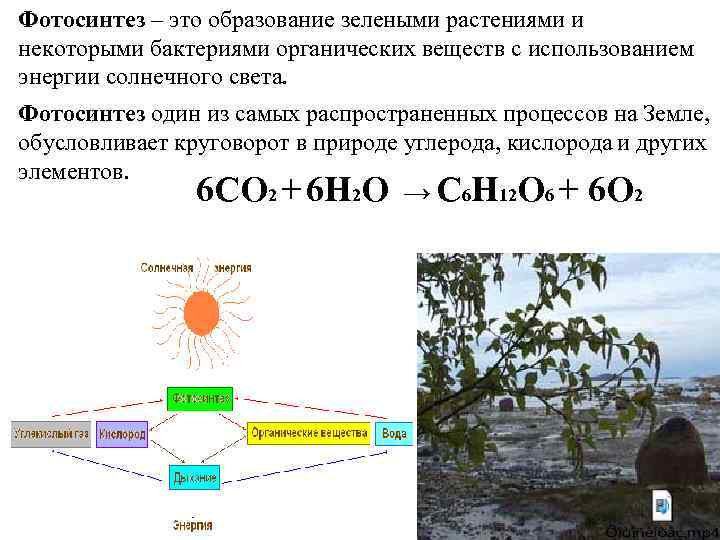 Фотосинтез – это образование зелеными растениями и некоторыми бактериями органических веществ с использованием энергии солнечного света. Фотосинтез один из самых распространенных процессов на Земле, обусловливает круговорот в природе углерода, кислорода и других элементов. 6 CO 2 + 6 H 2 O → C 6 H 12 O 6 + 6 O 2
Фотосинтез – это образование зелеными растениями и некоторыми бактериями органических веществ с использованием энергии солнечного света. Фотосинтез один из самых распространенных процессов на Земле, обусловливает круговорот в природе углерода, кислорода и других элементов. 6 CO 2 + 6 H 2 O → C 6 H 12 O 6 + 6 O 2
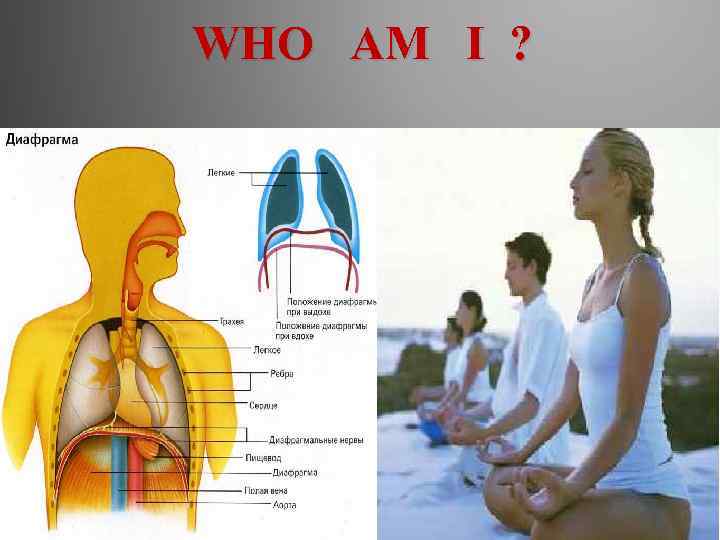 WHO AM I ?
WHO AM I ?
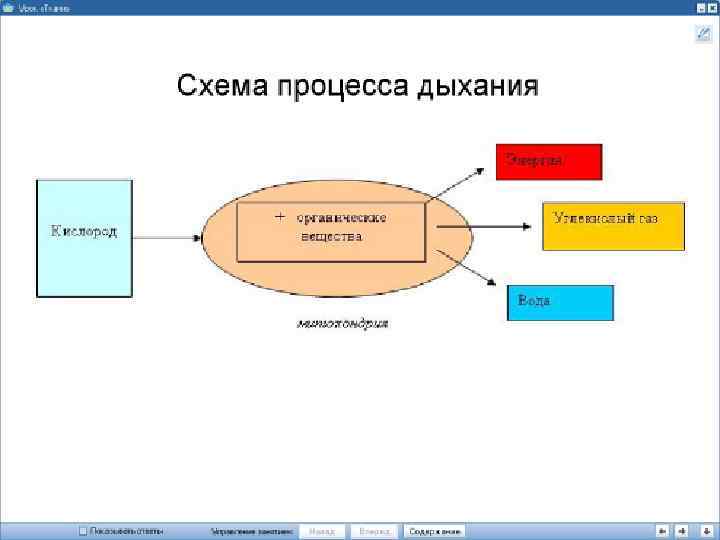
 Плюсы: Дыхание С 6 Н 1206 + 6 Н 20 + 12 R → 6 С 02 + 12 RH 2 + 6 O 2 → 12 R + 12 Н 20 С 6 Н 1206 + 602 - 4 6 С 02 + 6 Н 20 Символом R обозначают дыхательный пигмент, способный к обратимым окислительно-восстановительным превращениям. 1. Непременным участником дыхания является вода. 2. Вода наряду с окисляемым субстратом выполняет роль донора водорода. 3. Молекулярный кислород используется на заключительном этапе дыхания для регенерации акцепторов водорода с образованием воды.
Плюсы: Дыхание С 6 Н 1206 + 6 Н 20 + 12 R → 6 С 02 + 12 RH 2 + 6 O 2 → 12 R + 12 Н 20 С 6 Н 1206 + 602 - 4 6 С 02 + 6 Н 20 Символом R обозначают дыхательный пигмент, способный к обратимым окислительно-восстановительным превращениям. 1. Непременным участником дыхания является вода. 2. Вода наряду с окисляемым субстратом выполняет роль донора водорода. 3. Молекулярный кислород используется на заключительном этапе дыхания для регенерации акцепторов водорода с образованием воды.
 WHO AM I ?
WHO AM I ?
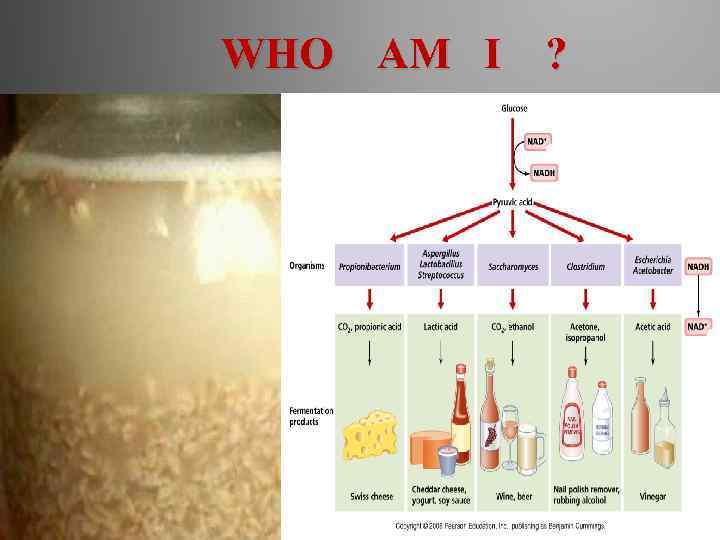
 Плюсы: Брожение Это особый химический процесс, вызываемый ферментами. При процессе брожения сложная частица органического вещества распадается на более простые. Спиртовое брожение: C 6 H 12 O 6 → 2 C 2 H 5 OH + 2 CO 2 А также кисломолочное брожение: С 6 Н 12 О 6 → 2 СН 3─CНОН─СООН + 21, 8 -104 Дж выделяется: глюкоза, молочная кислота, энергия
Плюсы: Брожение Это особый химический процесс, вызываемый ферментами. При процессе брожения сложная частица органического вещества распадается на более простые. Спиртовое брожение: C 6 H 12 O 6 → 2 C 2 H 5 OH + 2 CO 2 А также кисломолочное брожение: С 6 Н 12 О 6 → 2 СН 3─CНОН─СООН + 21, 8 -104 Дж выделяется: глюкоза, молочная кислота, энергия
 Плюсы Превращение, например, сока в вино, зерна и других исходных продуктов в пиво, а углеводов в углекислый газ приготовлении хлебного теста. Широко используется человеком также молочнокислое брожение для приготовления кисломолочных продуктов, квашения овощей и приготовления силоса.
Плюсы Превращение, например, сока в вино, зерна и других исходных продуктов в пиво, а углеводов в углекислый газ приготовлении хлебного теста. Широко используется человеком также молочнокислое брожение для приготовления кисломолочных продуктов, квашения овощей и приготовления силоса.
 WH 0 AM I ?
WH 0 AM I ?
 Плюсы: Горение – это окислительно-восстановительная реакция, сопровождающаяся выделением тепла и света. Cn. H 2 n+2 + 3 n + 1/2 O 2 = n. CO 2 + n +1 H 2 O Например: горение бутана, пропана, ацетилена, водорода, метана и пр.
Плюсы: Горение – это окислительно-восстановительная реакция, сопровождающаяся выделением тепла и света. Cn. H 2 n+2 + 3 n + 1/2 O 2 = n. CO 2 + n +1 H 2 O Например: горение бутана, пропана, ацетилена, водорода, метана и пр.
 Плюсы: Горение Получение тепла, возможность приготовления пищи и материалов нужных для жизнедеятельности человека.
Плюсы: Горение Получение тепла, возможность приготовления пищи и материалов нужных для жизнедеятельности человека.
 Минусы: Горение Загрязнение атмосферы углекислым газом, влияние на здоровье человека. Пожары.
Минусы: Горение Загрязнение атмосферы углекислым газом, влияние на здоровье человека. Пожары.
 WHO AM I ?
WHO AM I ?
 Плюсы: Гниение - это сложный биохимический процесс с образованием углекислого газа, воды и азота. • При гниении без доступа воздуха преобладают восстановительные процессы и накапливаются многие указанные продукты. • При свободном доступе воздуха гниение проходит до конца, углерод в органических соединениях выделяется в виде углекислого газа.
Плюсы: Гниение - это сложный биохимический процесс с образованием углекислого газа, воды и азота. • При гниении без доступа воздуха преобладают восстановительные процессы и накапливаются многие указанные продукты. • При свободном доступе воздуха гниение проходит до конца, углерод в органических соединениях выделяется в виде углекислого газа.
 Минусы: Гниение Распад белковых и других азотистых веществ под влиянием гнилостных бактерий , сопровождающийся образованием зловонных продуктов. Микробактерии портят различные продукты питания. Плюсы: Гниение Обогащение почвы при гниении органических веществ. Перегной - самый плодородный слой почвы, так как в нем много полезных микроорганизмов.
Минусы: Гниение Распад белковых и других азотистых веществ под влиянием гнилостных бактерий , сопровождающийся образованием зловонных продуктов. Микробактерии портят различные продукты питания. Плюсы: Гниение Обогащение почвы при гниении органических веществ. Перегной - самый плодородный слой почвы, так как в нем много полезных микроорганизмов.
 WHO AM I ?
WHO AM I ?
 Коррозия - это окислительно-восстановительная реакция, протекающая на поверхности металла под воздействием внешней среды. В результате коррозии металлы переходят в устойчивые соединения - оксиды или соли, в виде которых они находятся в природе. 4 Fe + 3 O 2 + 2 H 2 О = 2 Fe 2 O 3·H 2 О Минусы: Разрушение металлический конструкций и изделий, что приводит ежегодно к миллиардным убыткам в промышленно развитых странах.
Коррозия - это окислительно-восстановительная реакция, протекающая на поверхности металла под воздействием внешней среды. В результате коррозии металлы переходят в устойчивые соединения - оксиды или соли, в виде которых они находятся в природе. 4 Fe + 3 O 2 + 2 H 2 О = 2 Fe 2 O 3·H 2 О Минусы: Разрушение металлический конструкций и изделий, что приводит ежегодно к миллиардным убыткам в промышленно развитых странах.
 WHO AM I ?
WHO AM I ?
 O 2 = 2 O N 2 + O 2 = 2 NO, 2 NO + O 2 = 2 NO 2 O + O 2= O 3 Природные явления Минусы: Это явление приносит разрушения и сопровождается выделением ядовитых газов: N 2 + O 2 = 2 NO 2 Разряд молнии Гром и молния Плюсы: Образуется озон, а он защищает растения и животных от жёсткого ультрафиолетового излучения. O 2 = 2 O O + O 2= O 3
O 2 = 2 O N 2 + O 2 = 2 NO, 2 NO + O 2 = 2 NO 2 O + O 2= O 3 Природные явления Минусы: Это явление приносит разрушения и сопровождается выделением ядовитых газов: N 2 + O 2 = 2 NO 2 Разряд молнии Гром и молния Плюсы: Образуется озон, а он защищает растения и животных от жёсткого ультрафиолетового излучения. O 2 = 2 O O + O 2= O 3
 Природные явления Извержение вулкана Плюсы: Минусы: • Вулканы привели Это явление приносит разрушения и сопровождается практически к полной выделением ядовитых газов: остановке еще более мощного источника 2 H 2 S + 3 O 2 = 2 SO 2 +2 H 2 O углекислого газа - современных 2 SO 2 + O 2= 2 SO 3 авиалайнеров. 2 CO + O 2 = 2 CO 2 • Кроме этого, пепел вулкана это очень хорошее удобрение. Извержение вулкана
Природные явления Извержение вулкана Плюсы: Минусы: • Вулканы привели Это явление приносит разрушения и сопровождается практически к полной выделением ядовитых газов: остановке еще более мощного источника 2 H 2 S + 3 O 2 = 2 SO 2 +2 H 2 O углекислого газа - современных 2 SO 2 + O 2= 2 SO 3 авиалайнеров. 2 CO + O 2 = 2 CO 2 • Кроме этого, пепел вулкана это очень хорошее удобрение. Извержение вулкана
 TRUE OR FALSE GAME
TRUE OR FALSE GAME
 Corrosion is the destruction of metals and their alloys under the influence of the environment. (TRUE)
Corrosion is the destruction of metals and their alloys under the influence of the environment. (TRUE)
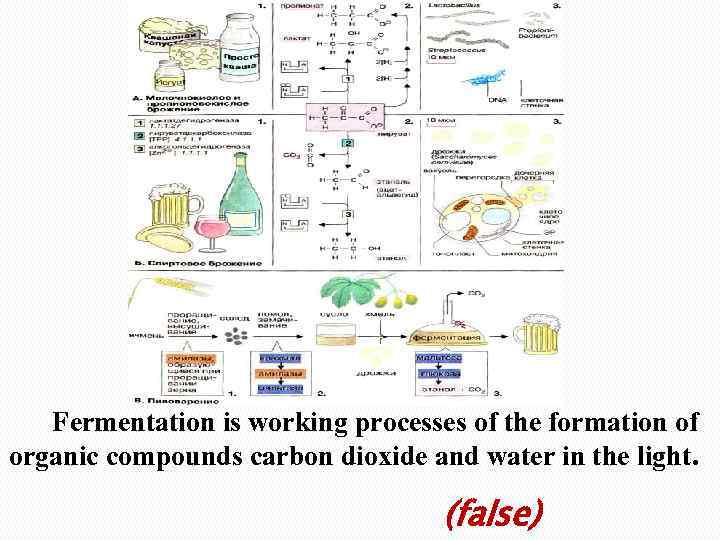 Fermentation is working processes of the formation of organic compounds carbon dioxide and water in the light. (false)
Fermentation is working processes of the formation of organic compounds carbon dioxide and water in the light. (false)
 Decomposition is the decay of proteins under the influence of bacteria characterized by a fetid (unpleasant)odor. (true)
Decomposition is the decay of proteins under the influence of bacteria characterized by a fetid (unpleasant)odor. (true)
 Eruption is not a redox (oxidationreduction ) reaction. (false)
Eruption is not a redox (oxidationreduction ) reaction. (false)
 Oxidant is an atom that donates (gives) electrons. (false)
Oxidant is an atom that donates (gives) electrons. (false)
 Recovery is the process of taking the electron. (true)
Recovery is the process of taking the electron. (true)
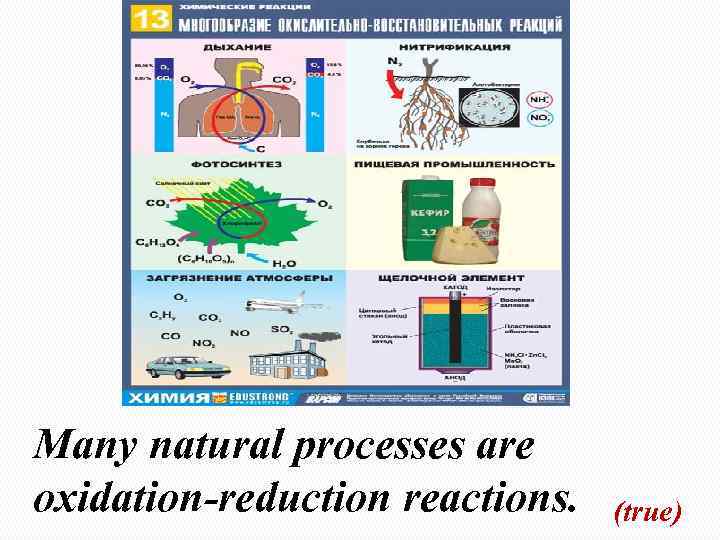 Many natural processes are oxidation-reduction reactions. (true)
Many natural processes are oxidation-reduction reactions. (true)
 Сombustion is a complex physicochemical process, characterized by the release of heat. (true)
Сombustion is a complex physicochemical process, characterized by the release of heat. (true)
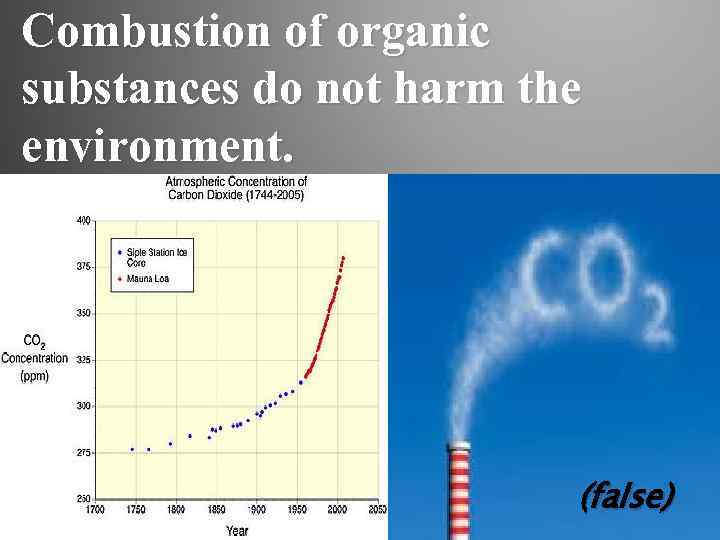 Combustion of organic substances do not harm the environment. (false)
Combustion of organic substances do not harm the environment. (false)
 Тhe most common are the types of fermentation, which takes place during the decomposition of organic substances. (true)
Тhe most common are the types of fermentation, which takes place during the decomposition of organic substances. (true)
 Значение ОВР в природе 1. При реакции фотосинтеза в зеленых растениях образуется кислород. 2. Реакция дыхания является основой жизни. 3. Реакции горения применяются для получения тепла, света, механической энергии. 4. ОВР в природе – извержение вулканов, грозовой разряд, образование перегноя, брожение овощей и фруктов, коррозия металлов и др. 5. В металлургии с помощью ОВР получают металлы.
Значение ОВР в природе 1. При реакции фотосинтеза в зеленых растениях образуется кислород. 2. Реакция дыхания является основой жизни. 3. Реакции горения применяются для получения тепла, света, механической энергии. 4. ОВР в природе – извержение вулканов, грозовой разряд, образование перегноя, брожение овощей и фруктов, коррозия металлов и др. 5. В металлургии с помощью ОВР получают металлы.
 Спасибо за внимание!
Спасибо за внимание!


