 5. План характеристики: • Определение класса • Классификация • Изомерия • Свойства • Получение • Применение
5. План характеристики: • Определение класса • Классификация • Изомерия • Свойства • Получение • Применение
 • Дайте свое определение класса. • Аминокислоты – гетерофункциональные соединения, которые обязательно содержат две функциональные группы: аминогруппу – NH 2 и карбоксильную группу –COOH, связанные с углеводородным радикалом (стр. 220 учебника) • Аминокислоты – производные кислот, которые можно рассматривать как продукты замещения одного или более атомов водорода в их радикалах на одну или более аминогрупп (“Курс органической химии”, стр. 371) • Общая формула NH 2 – CH – COOH R
• Дайте свое определение класса. • Аминокислоты – гетерофункциональные соединения, которые обязательно содержат две функциональные группы: аминогруппу – NH 2 и карбоксильную группу –COOH, связанные с углеводородным радикалом (стр. 220 учебника) • Аминокислоты – производные кислот, которые можно рассматривать как продукты замещения одного или более атомов водорода в их радикалах на одну или более аминогрупп (“Курс органической химии”, стр. 371) • Общая формула NH 2 – CH – COOH R
 • По взаимному расположению функциональных групп: α , β , γ… С – С- С – С – СООН С – С- С – СООН | | | NH 2 • По количеству функциональных групп : • моноаминомонокарбоновые • диаминомонокарбоновые С-С-С -СООН ׀ ׀ NH 2 лизин 2, 6 – диаминогексановая кислота • моноаминодикарбоновые 2 -аминопентандиовая кислота НООС-С-СООН | NH 2 глутаминовая
• По взаимному расположению функциональных групп: α , β , γ… С – С- С – С – СООН С – С- С – СООН | | | NH 2 • По количеству функциональных групп : • моноаминомонокарбоновые • диаминомонокарбоновые С-С-С -СООН ׀ ׀ NH 2 лизин 2, 6 – диаминогексановая кислота • моноаминодикарбоновые 2 -аминопентандиовая кислота НООС-С-СООН | NH 2 глутаминовая
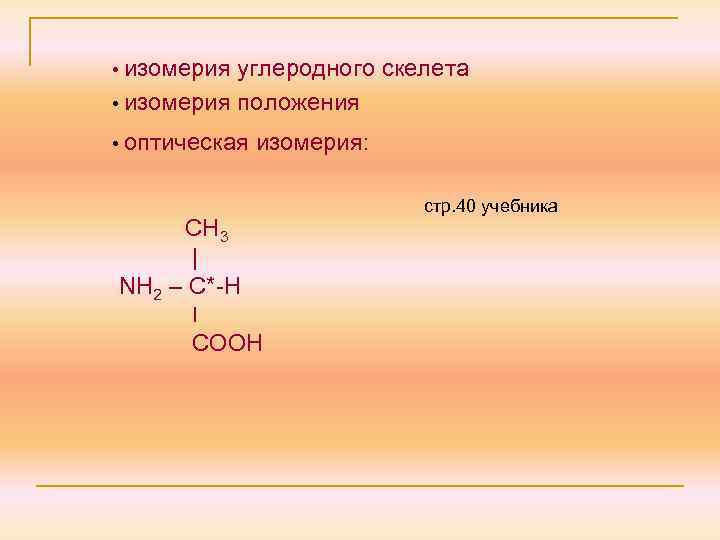 • изомерия углеродного скелета • изомерия положения • оптическая изомерия: СН 3 | NH 2 – C*-Н ׀ СООН стр. 40 учебника
• изомерия углеродного скелета • изомерия положения • оптическая изомерия: СН 3 | NH 2 – C*-Н ׀ СООН стр. 40 учебника
 Свойства: n. Физические : сладкие, безвкусные, горькие Почему? Вывод: зависит от радикала n. Химические : 1) Растворимость в воде N+H 3 – CH – COOH N+H 3 – CH – COO NH 2 – CH – COO| | | R R R Биполярный ион 2) С кислотами NH 2 – COOH + НС| → [NH 3 – CH 2 – COOH ] С| хлорид как основание 3) С основаниями NH 2 – COOH + Na OH → NH 2 – COONa + H 2 O как кислота Вывод : органические амфотерные соединения 4) Специфическое - взаимодействие между собой NH 2 – COOH + НNH – CH 2 – COOH → NH 2 – CO- NH – CH 2 –COOH пептидная связь Вывод: α-аминокислоты – элементарные частицы природных полимеров- белков
Свойства: n. Физические : сладкие, безвкусные, горькие Почему? Вывод: зависит от радикала n. Химические : 1) Растворимость в воде N+H 3 – CH – COOH N+H 3 – CH – COO NH 2 – CH – COO| | | R R R Биполярный ион 2) С кислотами NH 2 – COOH + НС| → [NH 3 – CH 2 – COOH ] С| хлорид как основание 3) С основаниями NH 2 – COOH + Na OH → NH 2 – COONa + H 2 O как кислота Вывод : органические амфотерные соединения 4) Специфическое - взаимодействие между собой NH 2 – COOH + НNH – CH 2 – COOH → NH 2 – CO- NH – CH 2 –COOH пептидная связь Вывод: α-аминокислоты – элементарные частицы природных полимеров- белков
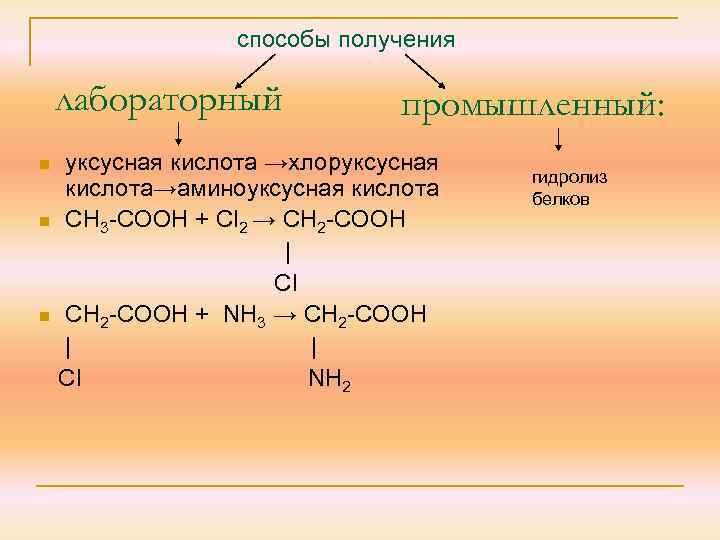 способы получения лабораторный n n n промышленный: уксусная кислота →хлоруксусная кислота→аминоуксусная кислота СН 3 -СООН + Сl 2 → СН 2 -СООН | Cl СН 2 -СООН + NH 3 → СН 2 -СООН | | Сl NH 2 гидролиз белков
способы получения лабораторный n n n промышленный: уксусная кислота →хлоруксусная кислота→аминоуксусная кислота СН 3 -СООН + Сl 2 → СН 2 -СООН | Cl СН 2 -СООН + NH 3 → СН 2 -СООН | | Сl NH 2 гидролиз белков
 • В живых организмах: • Природные аминокислоты (около 150) • Протеиногенные аминокислоты (около 20) в белках • Незаменимые: валин, лейцин, лизин, треонин, цистеин и др. • Антибиотики (пенициллин) • Полиамидные смолы (капрон, нейлон) • *Добавка к корму
• В живых организмах: • Природные аминокислоты (около 150) • Протеиногенные аминокислоты (около 20) в белках • Незаменимые: валин, лейцин, лизин, треонин, цистеин и др. • Антибиотики (пенициллин) • Полиамидные смолы (капрон, нейлон) • *Добавка к корму