5_alkany_2011_S_R.ppt
- Количество слайдов: 49

№ 5. ОСОБЕННОСТИ СТРОЕНИЯ, РЕАКЦИОННОЙ СПОСОБНОСТИ И МЕТОДЫ СИНТЕЗА АЛКАНОВ
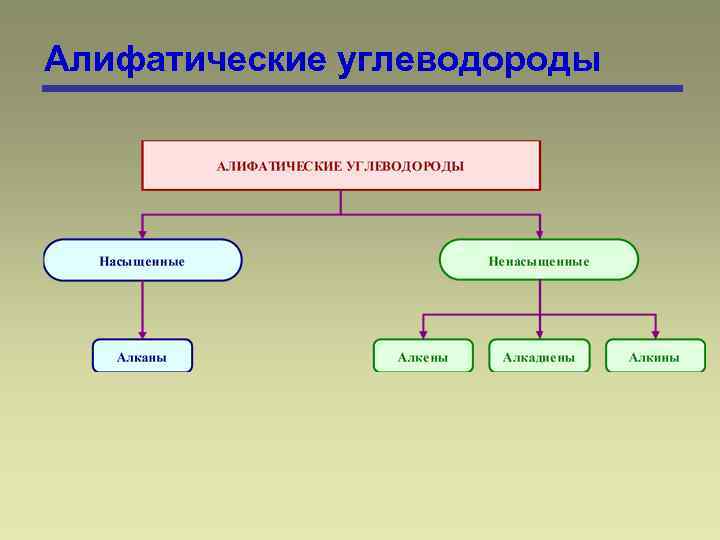
Алифатические углеводороды

Алканы Алканами называются насыщенные углеводороды, молекулы которых состоят из атомов углерода и водорода, связанных между собой только -связями.
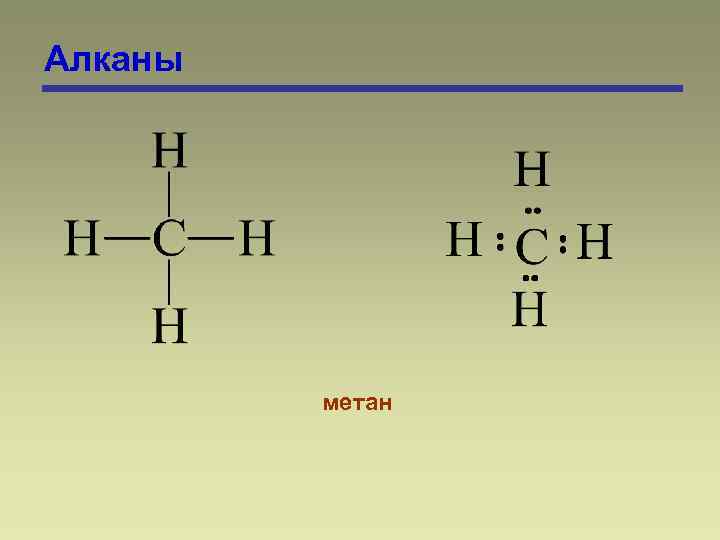
Алканы метан
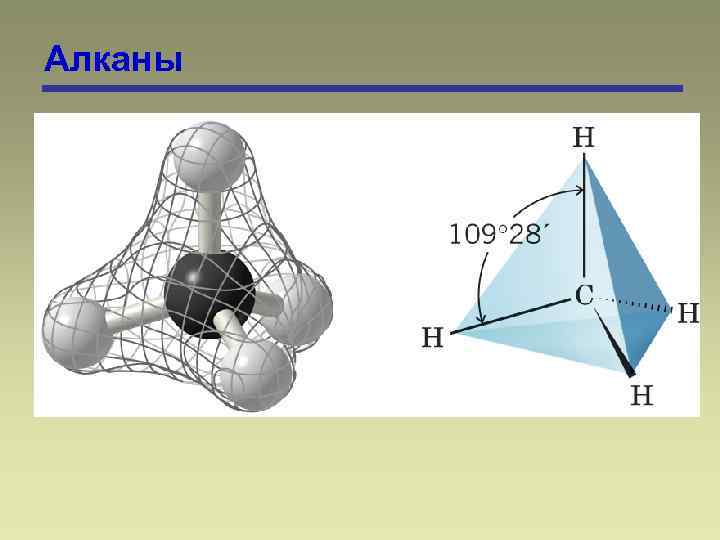
Алканы
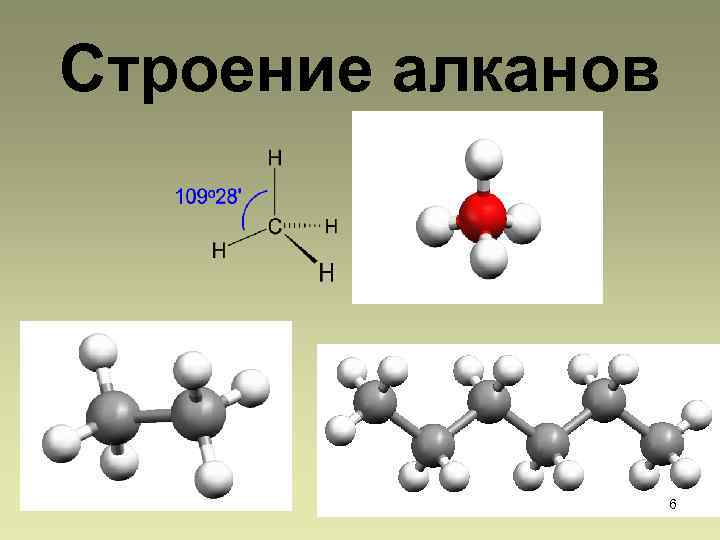
Строение алканов 6
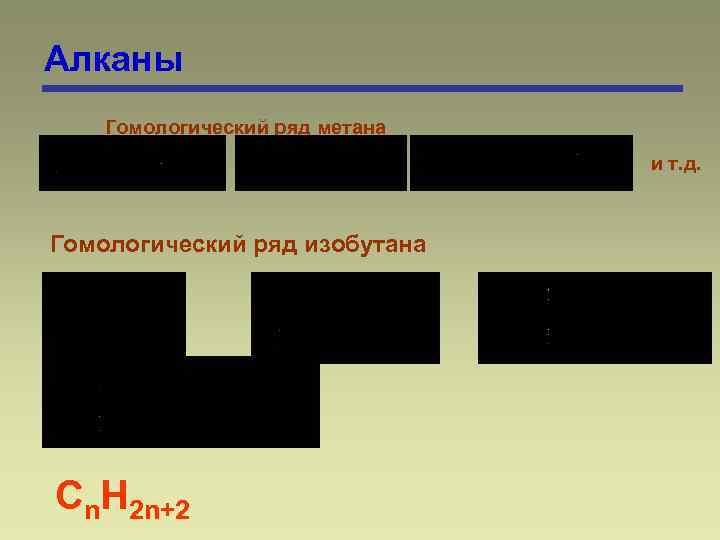
Алканы Гомологический ряд метана и т. д. Гомологический ряд изобутана Сn. Н 2 n+2
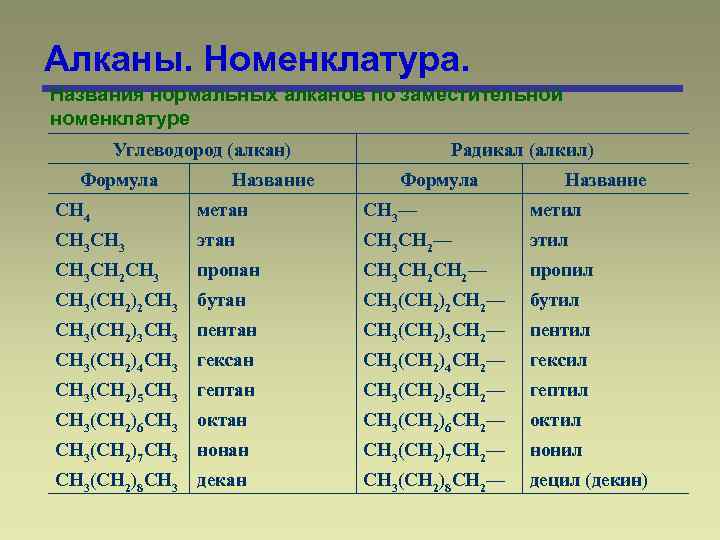
Алканы. Номенклатура. Названия нормальных алканов по заместительной номенклатуре Углеводород (алкан) Формула Название Радикал (алкил) Формула Название CH 4 метан CH 3— метил CH 3 этан CH 3 CH 2— этил CH 3 CH 2 CH 3 пропан CH 3 CH 2— пропил CH 3(CH 2)2 CH 3 бутан CH 3(CH 2)2 CH 2— бутил CH 3(CH 2)3 CH 3 пентан CH 3(CH 2)3 CH 2— пентил CH 3(CH 2)4 CH 3 гексан CH 3(CH 2)4 CH 2— гексил CH 3(CH 2)5 CH 3 гептан CH 3(CH 2)5 CH 2— гептил CH 3(CH 2)6 CH 3 октан CH 3(CH 2)6 CH 2— октил CH 3(CH 2)7 CH 3 нонан CH 3(CH 2)7 CH 2— нонил CH 3(CH 2)8 CH 3 декан CH 3(CH 2)8 CH 2— децил (декин)
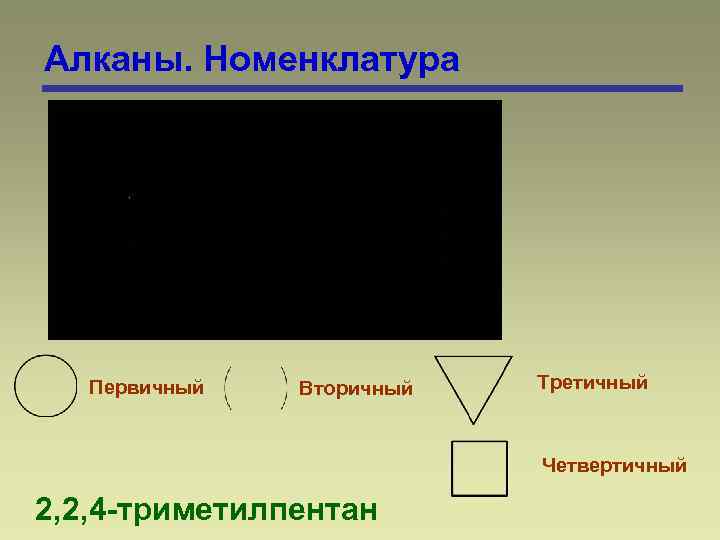
Алканы. Номенклатура Первичный Вторичный Третичный Четвертичный 2, 2, 4 -триметилпентан
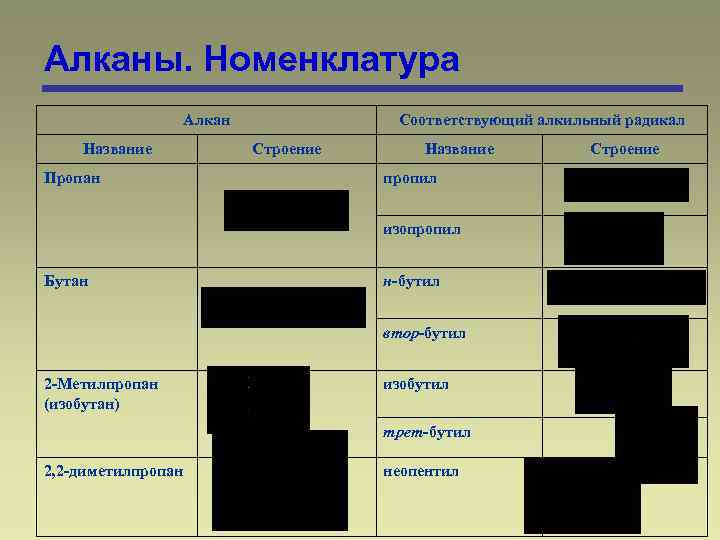
Алканы. Номенклатура Алкан Название Пропан Соответствующий алкильный радикал Строение Название пропил изопропил Бутан н-бутил втор-бутил 2 -Метилпропан (изобутан) изобутил трет-бутил 2, 2 -диметилпропан неопентил Строение

Алканы. Номенклатура Систематическая номенклатура ИЮПАК 1) определяют самую длинную цепь атомов углерода. Число атомов углерода в этой цепи служит основой названия; 2) нумеруют главную цепь с того конца, ближе к которому находится заместитель (углеводородный радикал); 3) перед основой названия указывают цифровой номер того атома углерода в главной цепи, у которого находится заместитель, а затем в виде префикса называют этот заместитель;

Алканы. Номенклатура 4) при наличии двух и более заместителей нумерацию цепи производят так, чтобы заместители получили наименьшие номера. В названии алкана радикалы перечисляются в алфавитном порядке. Перед названием каждого радикала ставят цифру, обозначающую его положение в главной углеродной цепи. Если заместители одинаковые, то к их названию добавляют умножительные приставки ди-, три-, тетра-, пента- и т. д. 5) если в главной цепи на равном расстоянии от концов стоят одинаковые радикалы, то нумерацию производят таким образом, чтобы радикалы получили наименьшие номера.
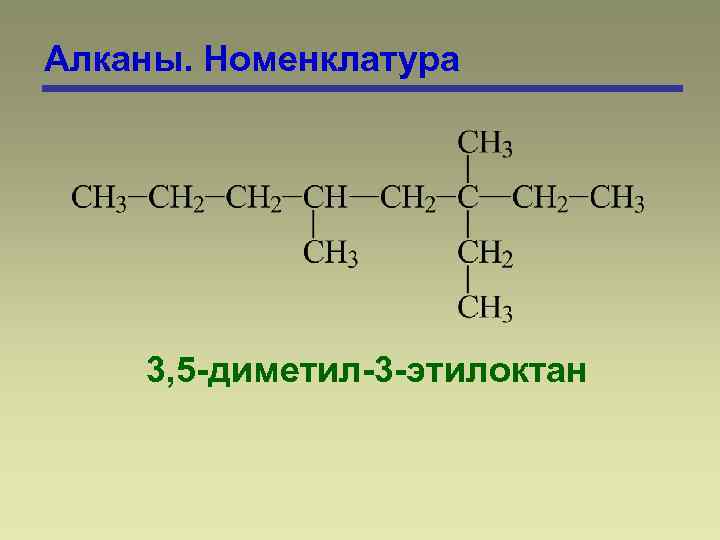
Алканы. Номенклатура 3, 5 -диметил-3 -этилоктан

Алканы. Номенклатура 2, 3, 6 -триметилгептан
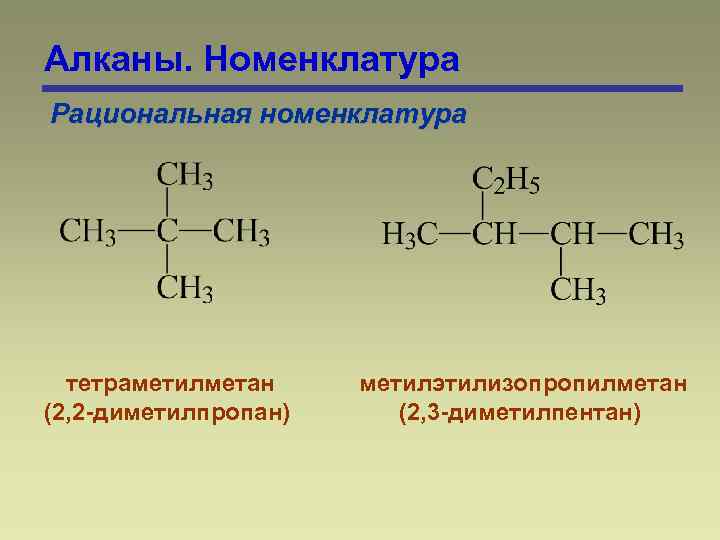
Алканы. Номенклатура Рациональная номенклатура тетраметилметан (2, 2 -диметилпропан) метилэтилизопропилметан (2, 3 -диметилпентан)
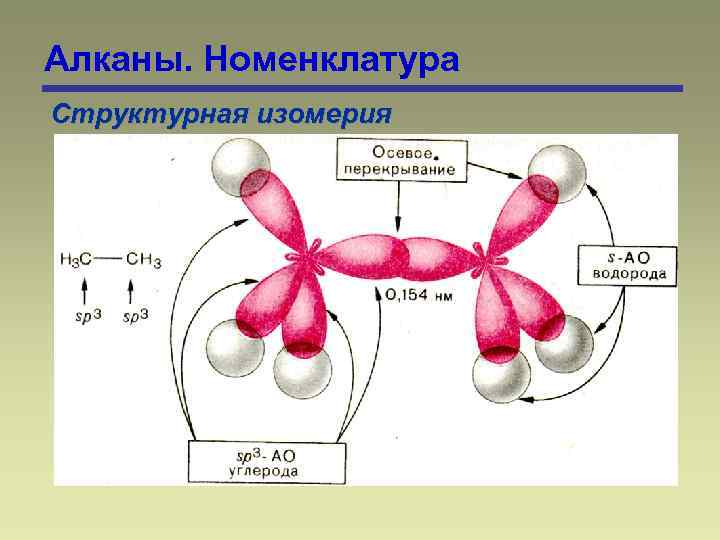
Алканы. Номенклатура Структурная изомерия
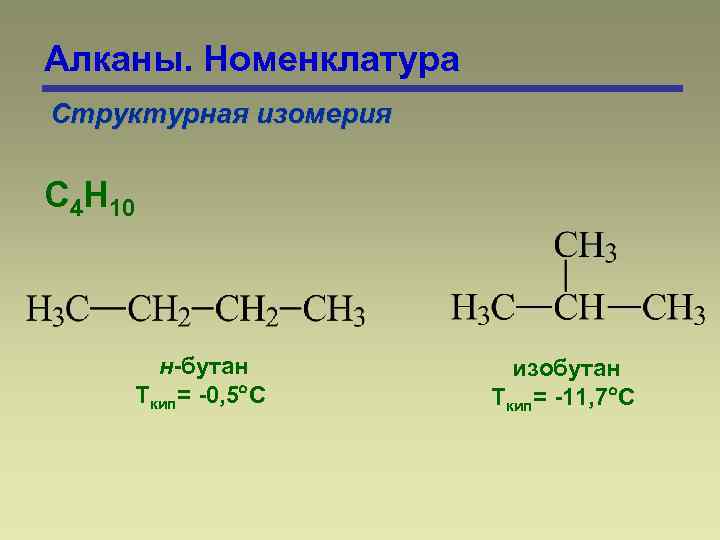
Алканы. Номенклатура Структурная изомерия С 4 Н 10 н-бутан Ткип= -0, 5 С изобутан Ткип= -11, 7 С
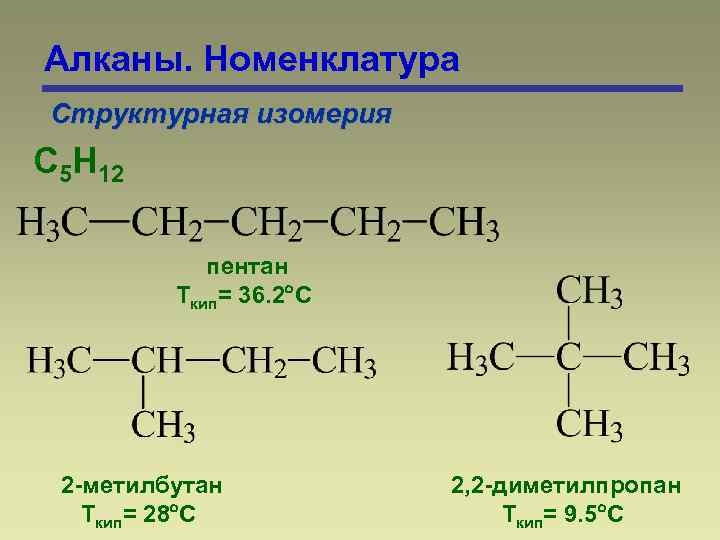
Алканы. Номенклатура Структурная изомерия С 5 Н 12 пентан Ткип= 36. 2 С 2 -метилбутан Ткип= 28 С 2, 2 -диметилпропан Ткип= 9. 5 С
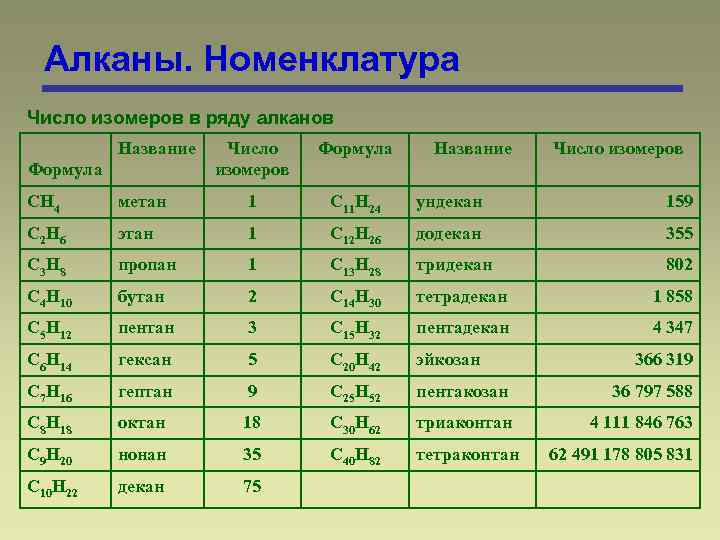
Алканы. Номенклатура Число изомеров в ряду алканов Название Формула Число изомеров Формула Название Число изомеров CH 4 метан 1 C 11 H 24 ундекан 159 C 2 H 6 этан 1 C 12 H 26 додекан 355 C 3 H 8 пропан 1 C 13 H 28 тридекан 802 C 4 H 10 бутан 2 C 14 H 30 тетрадекан 1 858 C 5 H 12 пентан 3 C 15 H 32 пентадекан 4 347 C 6 H 14 гексан 5 C 20 H 42 эйкозан C 7 H 16 гептан 9 C 25 H 52 пентакозан 36 797 588 C 8 H 18 октан 18 C 30 H 62 триаконтан 4 111 846 763 C 9 H 20 нонан 35 C 40 H 82 тетраконтан C 10 H 22 декан 75 366 319 62 491 178 805 831

Алканы. Способы получения Получение из ненасыщенных углеводородов Получение из галогенопроизводных (Реакция Вюрца)

ВЮРЦ (Wurtz), Шарль Адольф Французский химик-органик и педагог 26 ноября 1817 г. – 12 мая 1884 г. 21
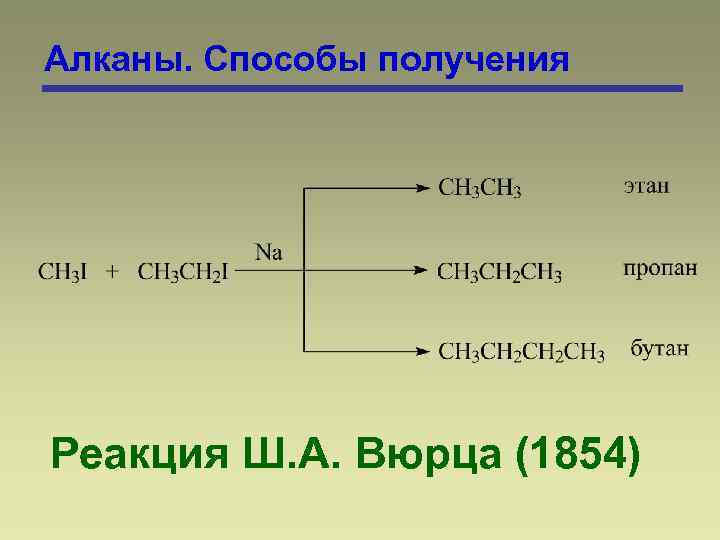
Алканы. Способы получения Реакция Ш. А. Вюрца (1854)

Алканы. Способы получения Получение из солей карбоновых кислот ( сплавление) (реакция Дюма) Электролиз солей щелочных металлов и карбоновых кислот (реакция Кольбе)

Адольф Вильгельм Герман Кольбе нем. Adolph Wilhelm Hermann Kolbe немецкий химикорганик. 24

Реакция электролиза по Кольбе: 25
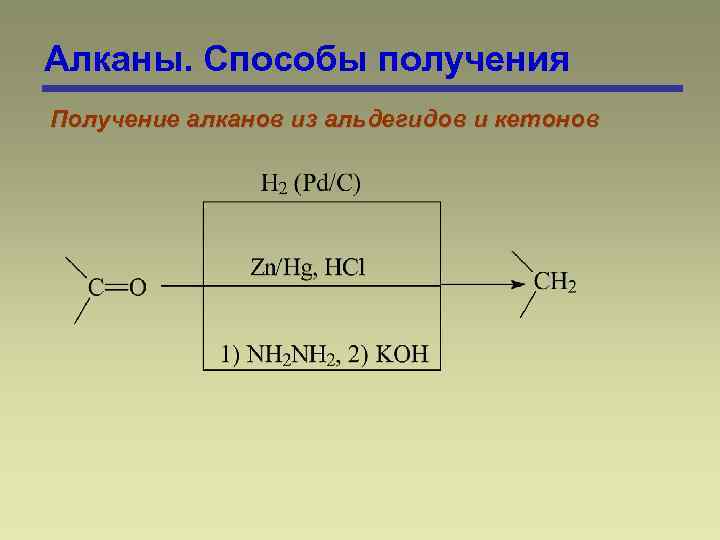
Алканы. Способы получения Получение алканов из альдегидов и кетонов

Алканы. Химические свойства Галогенирование
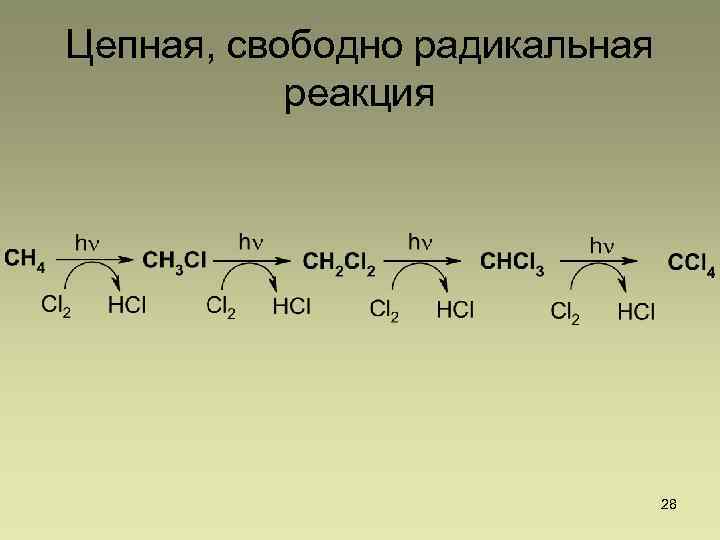
Цепная, свободно радикальная реакция 28

• Механизм радикального замещения (SR) на примере монохлорирования метана Реакция галогенирования алканов протекает по радикальному цепному механизму, т. е. как цепь повторяющихся реакций с участием свободнорадикальных частиц. Цепные реакции – химические реакции, идущие путем последовательного протекания одних и тех же элементарных стадий. Н. Н. Семёнов (справа) и П. Л. Капица (слева), портрет работы Б. М. Кустодиева, 1921 29 29
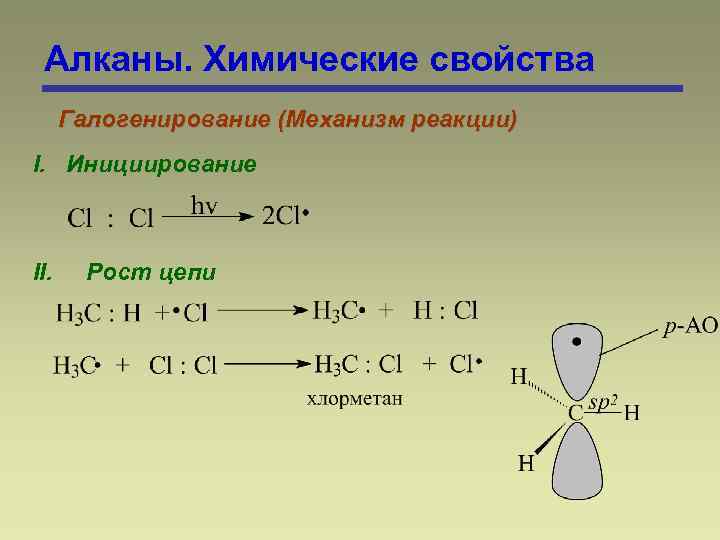
Алканы. Химические свойства Галогенирование (Механизм реакции) I. Инициирование II. Рост цепи
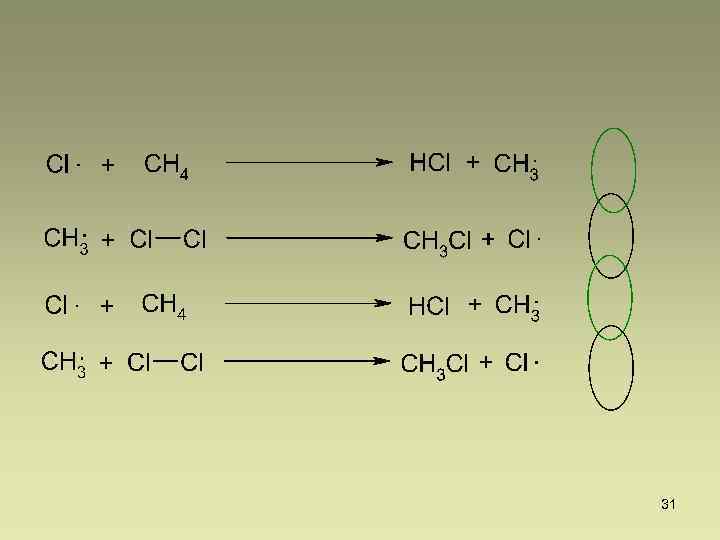
31

Алканы. Химические свойства Галогенирование (Механизм реакции) III. Обрыв цепи

Галогенирование (Механизм реакции) 1. Галогенирование начинается только под действием инициатора радикальных реакций : 1)нагреванием до температур 200 300 С термолиз (тепловая энергия) 2) облучением фотолиз (лучистая энергия, кванты света h ) 3) введением веществ, достаточно легко генерирующих свободные радикалы. Pb(C 2 H 5)4 Pb + C 2 H 5 • ; Cl • • Cl + C 2 H 5 • Cl • + C 2 H 5 Cl

Алканы. Химические свойства Галогенирование (Механизм реакции) При реакциях SR с углеводородами, содержащими атомы С с различной степенью замещения, наблюдается региоселективность реакции

Региоселективность реакции, т. е. предпочтительное протекание реакции по одному из нескольких возможных реакционных центров молекулы: 35

Селективность реакции SR объясняется : • 1) различиями в прочности первичных, вторичных и третичных С Н связей (ниже приведены значения энергий диссоциации этих связей): Едис. 406 к. Дж/моль (97 ккал/моль) 393, 5 к. Дж/моль (94 ккал/моль) 381 к. Дж/моль (91 ккал/моль). 36

• 2) предпочтительной становится та первичная атака субстрата реагентом, которая приводит к образованию наиболее стабильного свободного радикала Стабильность радикалов: R 3 C • R 2 CH • RCH 2 • H 3 C • 37

Галоген в реакции СН 4 + Х • СН 3 • + НХ Изменение энтальпии (ккал/моль) F 2 Cl 2 Br 2 J 2 32 1 +15 +33 Реакционная способность в ряду галогенов уменьшается слева направо: F 2 > Cl 2 > Br 2 > I 2 Галогенирование под действием фтора может выйти из под контроля и приобрести взрывной характер. Региоселективность любой органической реакции понижается с увеличением активности реагента 38

На результат реакции SR оказывают влияние и электронные эффекты тех заместителей, которые имеются в цепи алкана. • при фотохимическом хлорировании 1 -хлорбутана при 35 С региоселективность реакции такова: СН 3 СН 2 Cl. 25% 50% 17% 3% 39

Пропен хлорируется при температуре 450 С по механизму SR : • СН 2=СН СН 3 + Cl • НCl + СН 2=СН СН 2 • Cl 2 • • СН 2 СН=СН 2 СН СН 2 • СН 2=СН СН 2 Cl + Cl • Реакция Львова 40
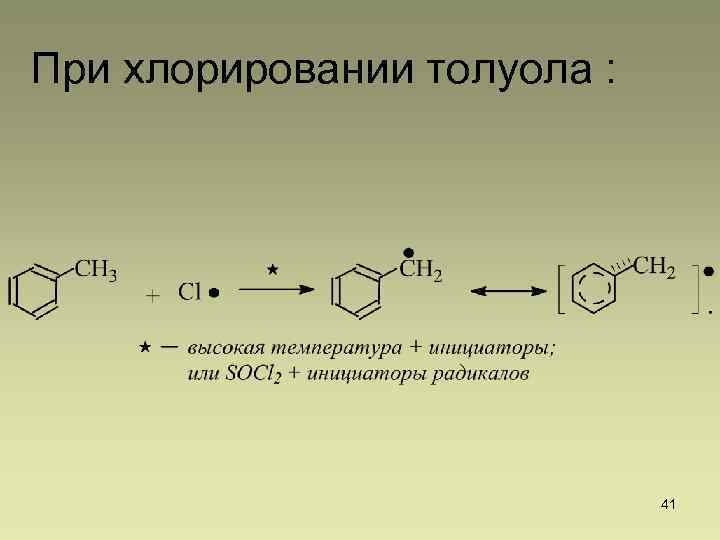
При хлорировании толуола : 41
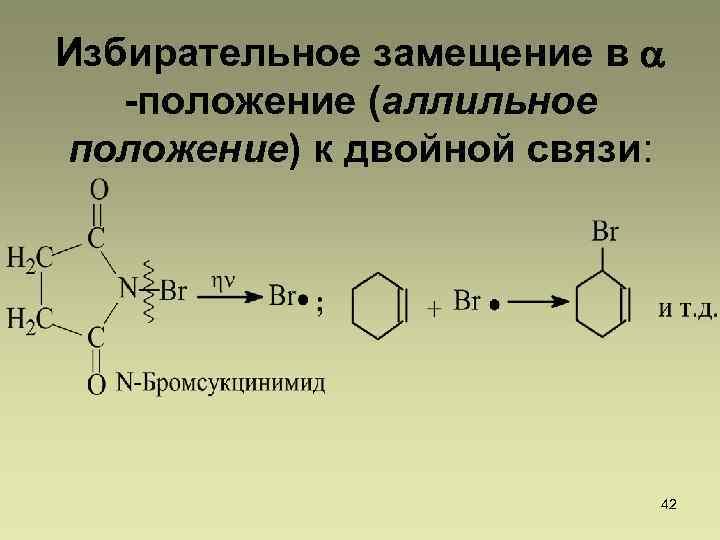
Избирательное замещение в -положение (аллильное положение) к двойной связи: 42

Алканы. Химические свойства Нитрование обработка 10 – 20 %-ной азотной кислотой в паровой фазе при температуре не выше 140 °С. Реакция М. И. Коновалова

Алканы. Химические свойства Сульфохлорирование hν RH + Cl 2 + SO 2 → RSO 2 Cl + HCl . С 10 H 22 + SO 2 + Cl 2 C 10 H 21 SO 2 Cl + HCl декан сульфохлорид декана C 10 H 21 SO 2 Cl + 2 Na. OH C 10 H 21 SO 3 Na + Na. Cl + H 2 O алкилсульфонат
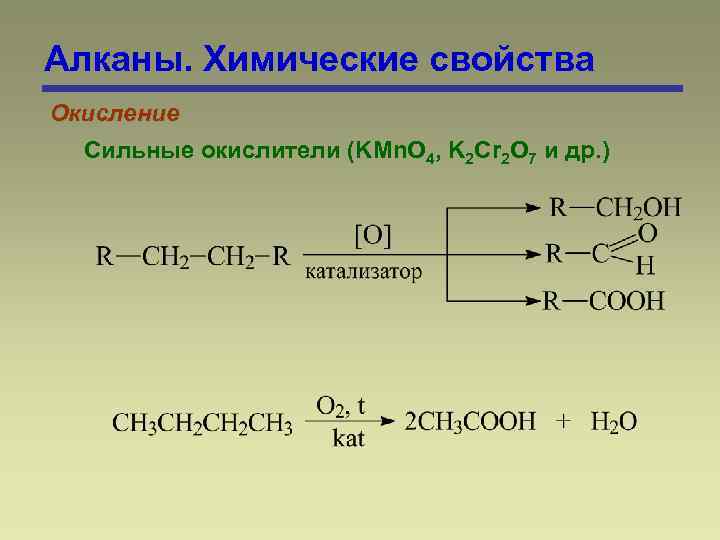
Алканы. Химические свойства Окисление Сильные окислители (KMn. O 4, K 2 Cr 2 O 7 и др. )
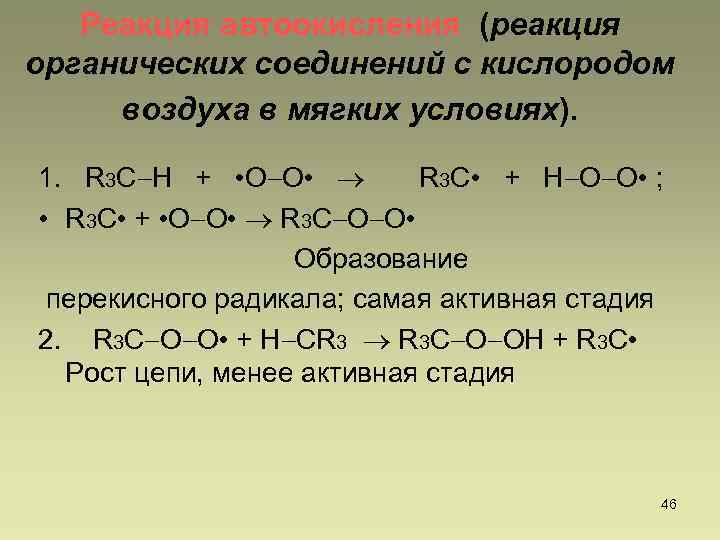
Реакция автоокисления (реакция органических соединений с кислородом воздуха в мягких условиях). 1. R 3 C H + • O O • R 3 C • + H O O • ; • R 3 C • + • O O • R 3 C O O • Образование перекисного радикала; самая активная стадия 2. R 3 C O O • + H CR 3 R 3 C O OH + R 3 C • Рост цепи, менее активная стадия 46
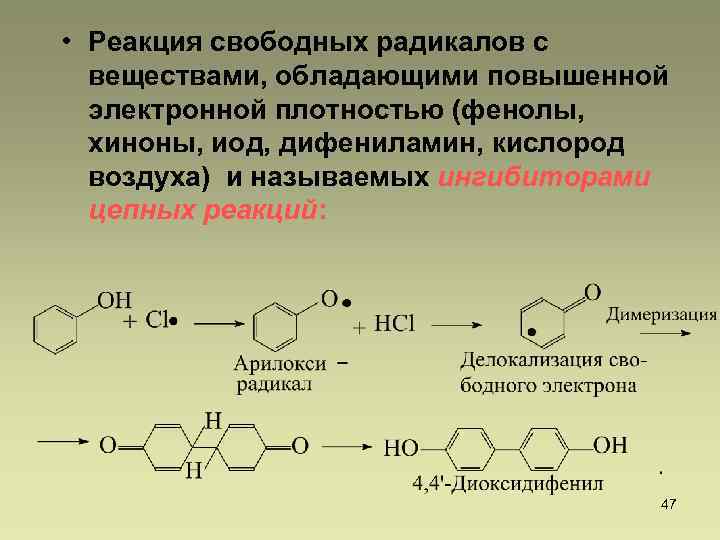
• Реакция свободных радикалов с веществами, обладающими повышенной электронной плотностью (фенолы, хиноны, иод, дифениламин, кислород воздуха) и называемых ингибиторами цепных реакций: 47
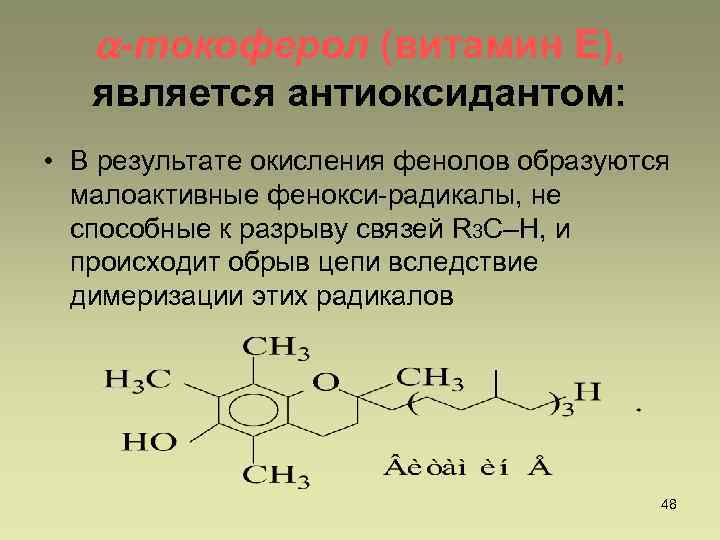
-токоферол (витамин Е), является антиоксидантом: • В результате окисления фенолов образуются малоактивные фенокси-радикалы, не способные к разрыву связей R 3 C–H, и происходит обрыв цепи вследствие димеризации этих радикалов 48

49
5_alkany_2011_S_R.ppt