5_alkany_2014__S_R.pptx
- Количество слайдов: 36
№ 5. Общие закономерности реакционной способности органических соединений как химическая основа их биологического функционирования.

Радикальное замещение у насыщенного атома углерода, SR у C sp 3. 2
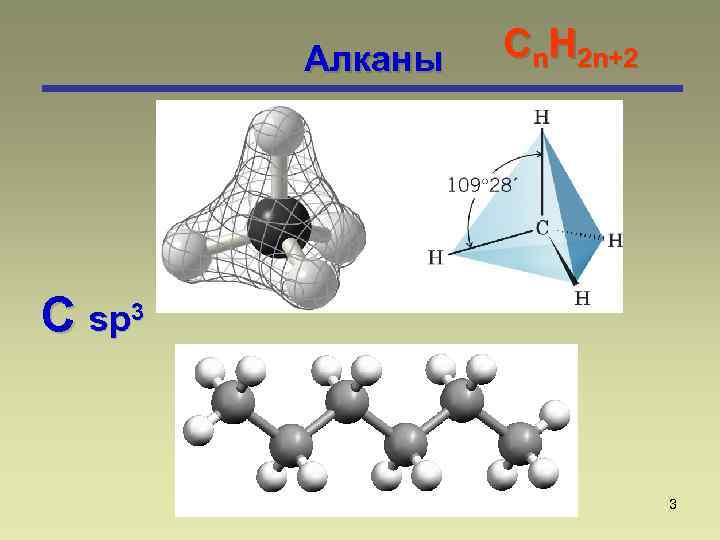
Алканы Сn. Н 2 n+2 C sp 3 3
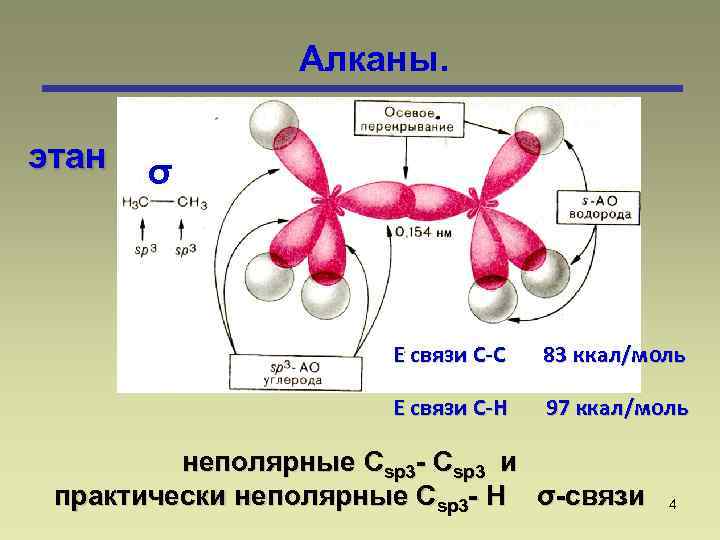
Алканы. этан σ Е связи С-С 83 ккал/моль Е связи С-Н 97 ккал/моль неполярные Csp 3 - Csp 3 и практически неполярные Csp 3 - H σ-связи 4
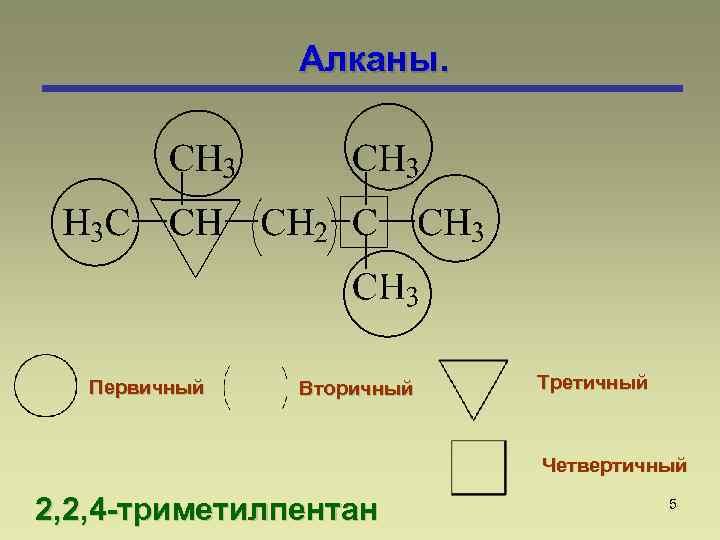
Алканы. Первичный Вторичный Третичный Четвертичный 2, 2, 4 -триметилпентан 5

Алканы. Способы получения 1. Получение из галогенопроизводных (Реакция Вюрца) t Симметричные галогеналканы Реакция Ш. А. Вюрца (1854) 6

ВЮРЦ (Wurtz), Шарль Адольф Французский химик-органик и педагог 1817 г. – 1884 г. 7
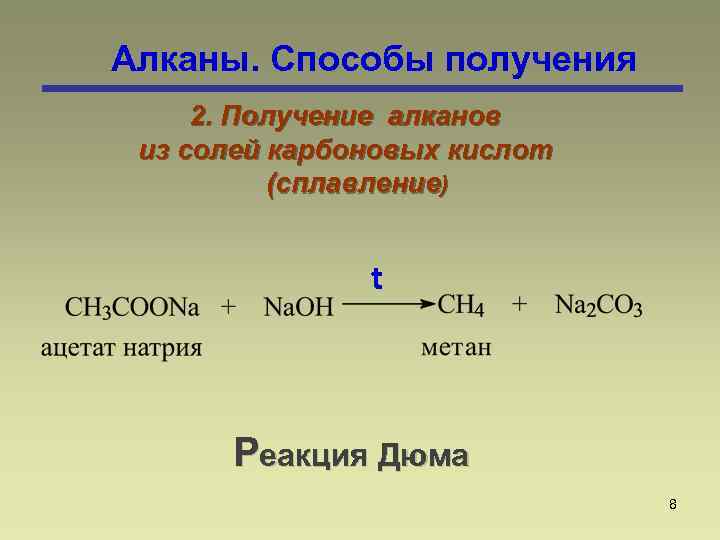
Алканы. Способы получения 2. Получение алканов из солей карбоновых кислот (сплавление) t Реакция Дюма 8

3. Электролиз солей щелочных металлов и карбоновых кислот (реакция Кольбе) 1849 г. 9

Адольф Вильгельм Герман Кольбе (Adolph Wilhelm Hermann Kolbe) немецкий химик-органик 1818 г. – 1884 г. 10

Гомолитическое замещение, SR. 11
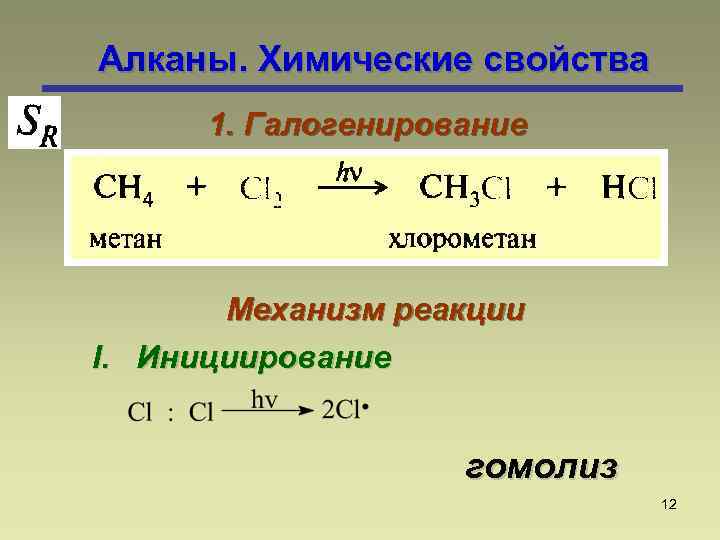
Алканы. Химические свойства 1. Галогенирование Механизм реакции I. Инициирование гомолиз 12

Инициирование радикальных реакций : 1) термолиз (> 300 С) 2) фотолиз (лучистая энергия, кванты света h ) 3) химическое инициирование Веществa, достаточно легко генерирующие свободные радикалы: Pb(C 2 H 5)4 Pb + C 2 H 5 • Тетраэтилат свинца Cl • • Cl + C 2 H 5 • Cl • + C 2 H 5 Cl 13
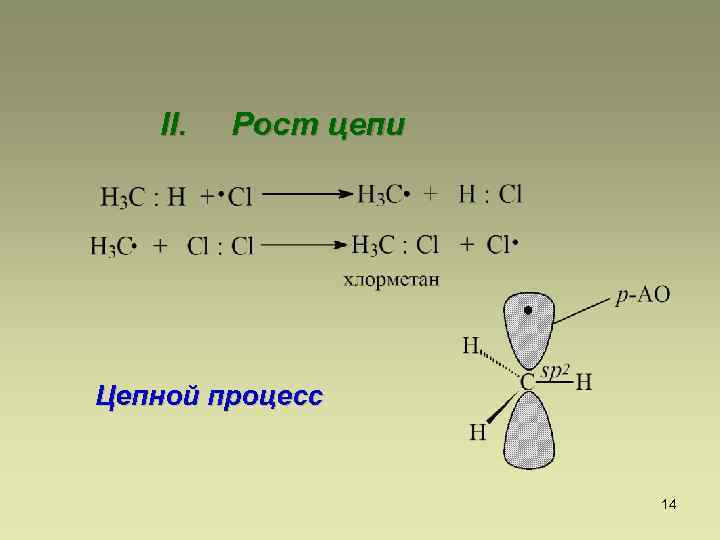
II. Рост цепи Цепной процесс 14
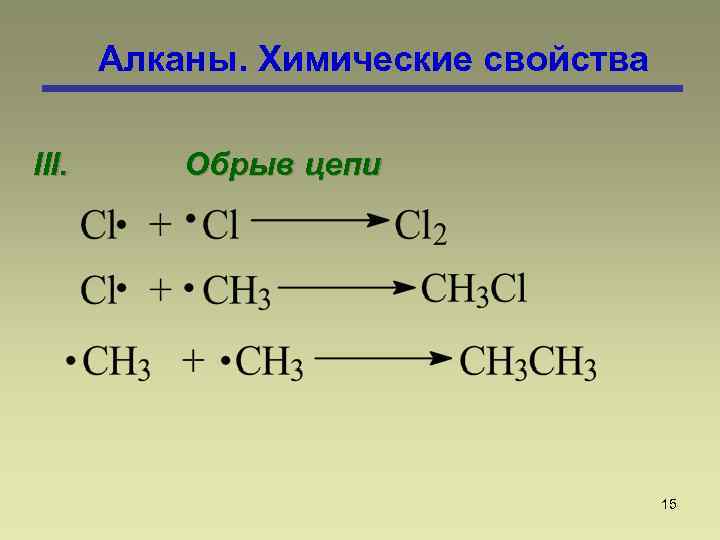
Алканы. Химические свойства III. Обрыв цепи 15
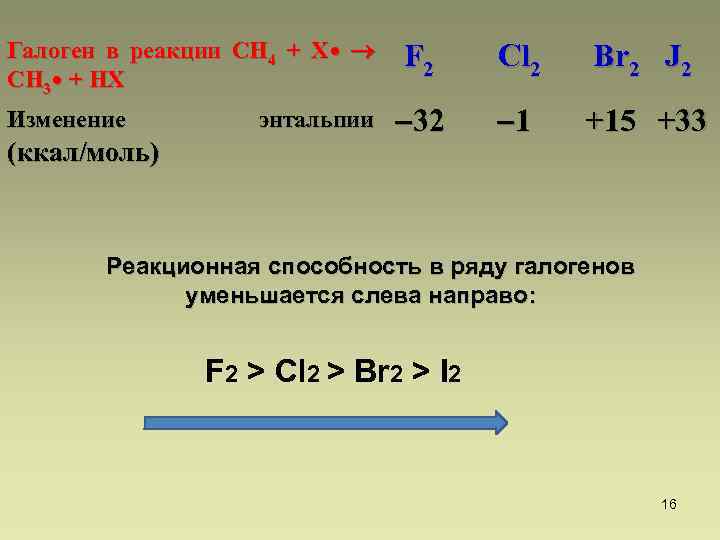
Галоген в реакции СН 4 + Х • СН 3 • + НХ Изменение (ккал/моль) энтальпии F 2 Cl 2 Br 2 J 2 32 1 +15 +33 Реакционная способность в ряду галогенов уменьшается слева направо: F 2 > Cl 2 > Br 2 > I 2 16
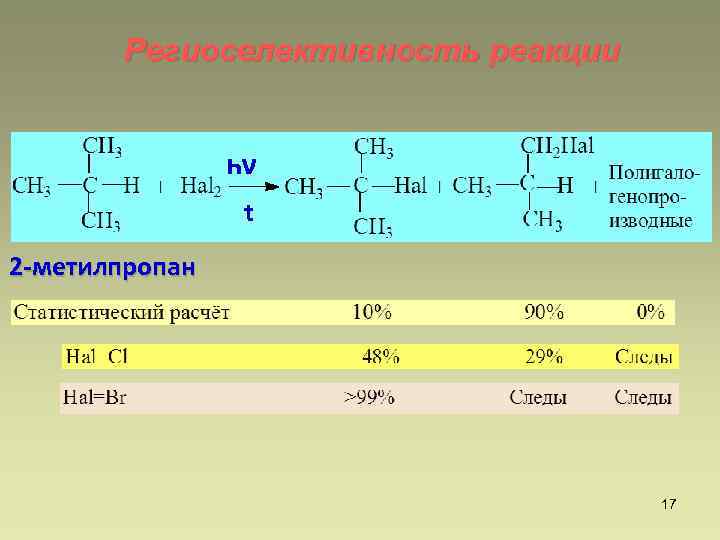
Региоселективность реакции һν t 2 -метилпропан 17

трет. Н : втор. Н : перв. Н Бром 1600 : 82 : 1 Хлор 5. 0 : 3. 8 : 1 Br 2 менее реакционноспособен, чем Cl 2 поэтому более селективен ! и 18
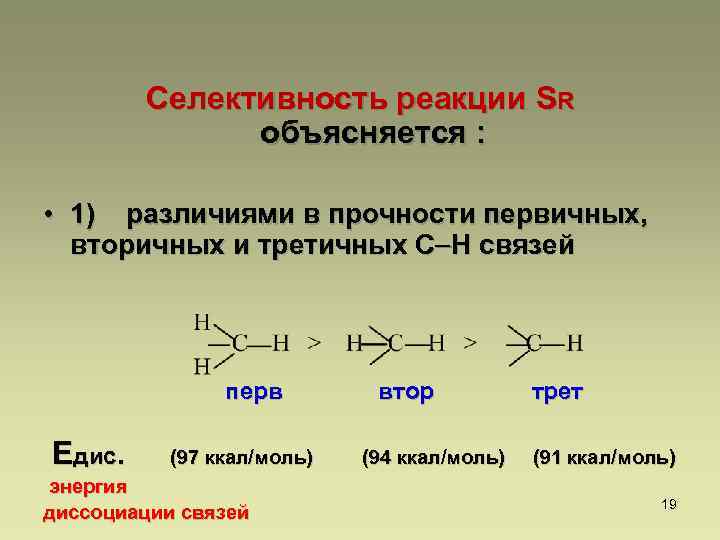
Селективность реакции SR объясняется : • 1) различиями в прочности первичных, вторичных и третичных С Н связей перв втор трет Едис. (97 ккал/моль) (94 ккал/моль) (91 ккал/моль) энергия диссоциации связей 19

• 2. образованием наиболее стабильного промежуточного свободного радикала Стабильность радикалов: 20
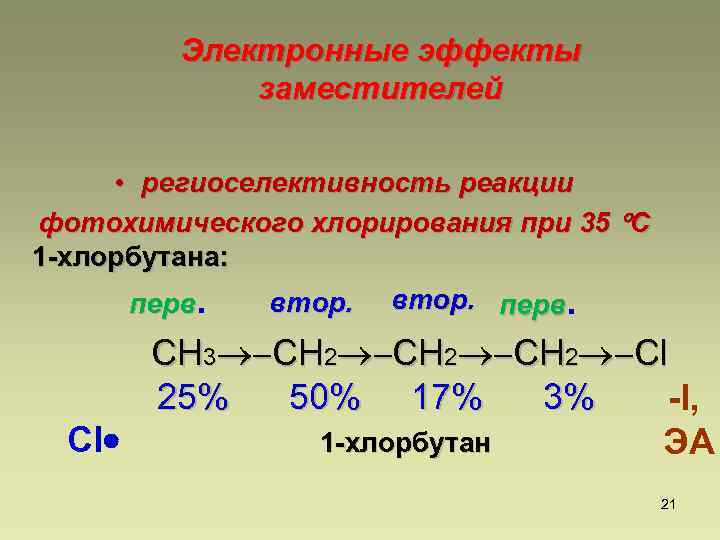
Электронные эффекты заместителей • региоселективность реакции фотохимического хлорирования при 35 С 1 -хлорбутана: втор. перв. СН 3 СН 2 Cl 25% 50% 17% 3% -I, Cl 1 -хлорбутан ЭА 21

Хлорирование в аллильное положение, SR Cl 2 450 С СН 2=СН СН 3 + Cl • НCl + СН 2=СН СН 2 • Пропен Cl 2 • СН 2 СН=СН 2 СН СН 2 • СН 2=СН СН 2 Cl + Cl • 1883 г. Реакция М. Д. Львова (ученик и ближайший помощник А. М. Бутлерова) 22
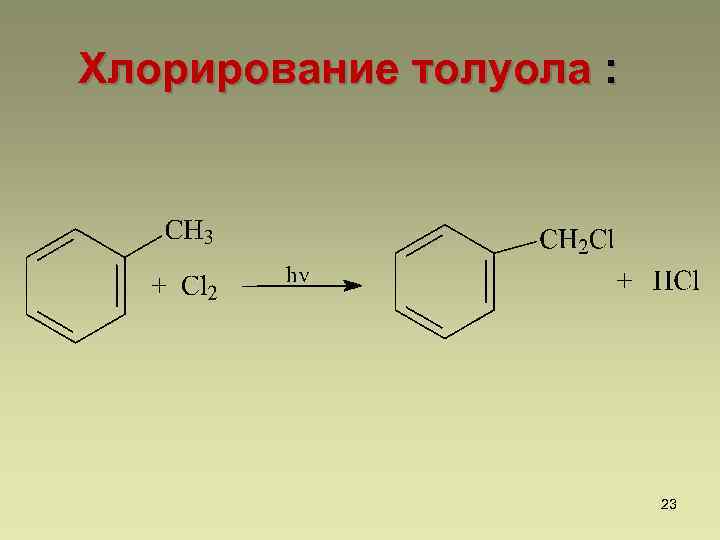
Хлорирование толуола : 23
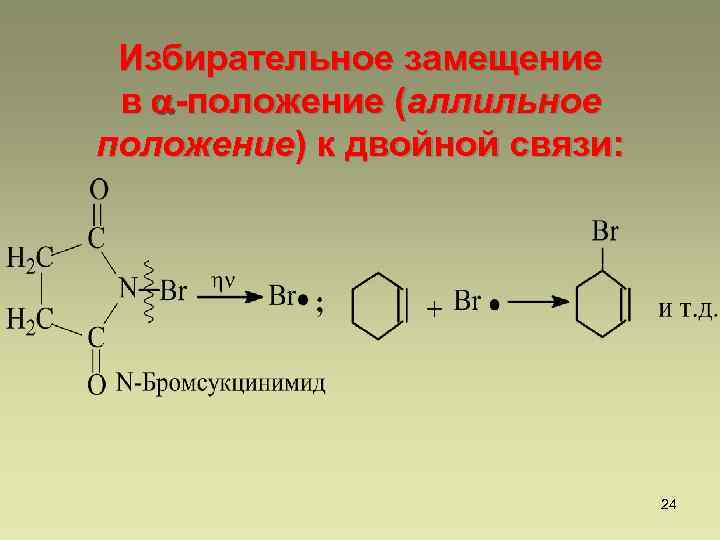
Избирательное замещение в -положение (аллильное положение) к двойной связи: 24

Алканы. Химические свойства 2. Нитрование разб. Р обработка 10 – 20 %-ной азотной кислотой в паровой фазе при температуре не выше 140 °С. Реакция М. И. Коновалова 25

Алканы. Химические свойства 3. Сульфохлорирование hν RH + Cl 2 + SO 2 → RSO 2 Cl + HCl . сульфохлорид Втор. С > перв. С 26

Реакция органических соединений с кислородом воздуха в мягких условиях- Реакция автоокисления 27
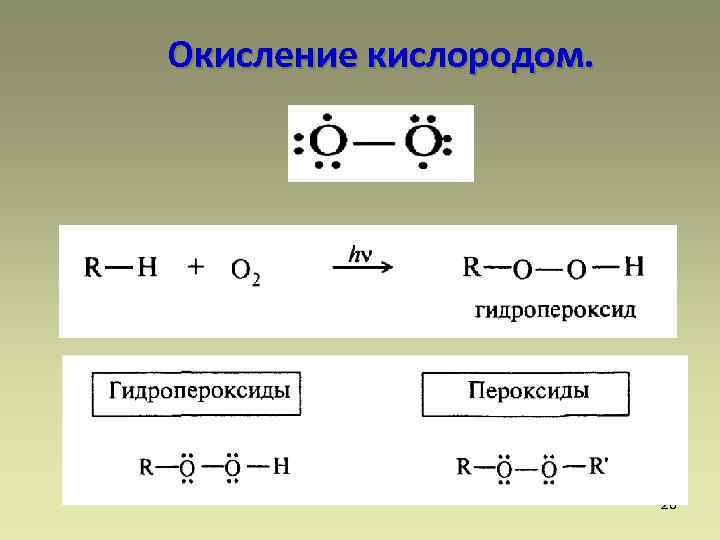
Окисление кислородом. 28

В условиях организма: 29
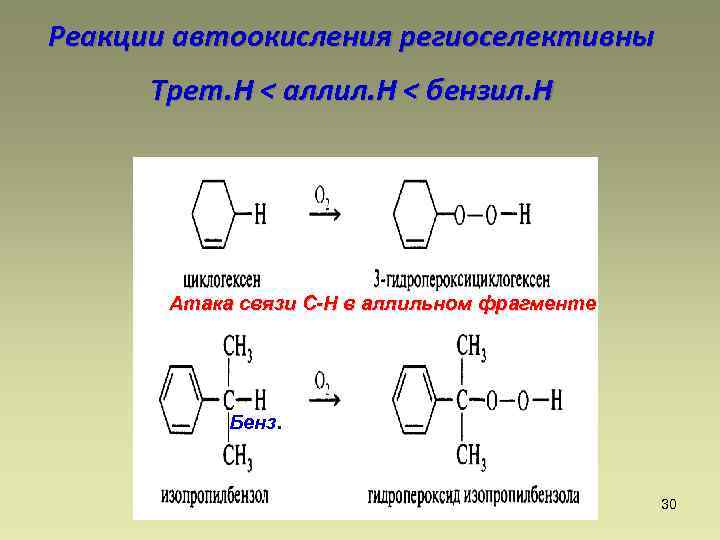
Реакции автоокисления региоселективны Трет. Н < аллил. Н < бензил. Н Атака связи С-Н в аллильном фрагменте Бенз. 30
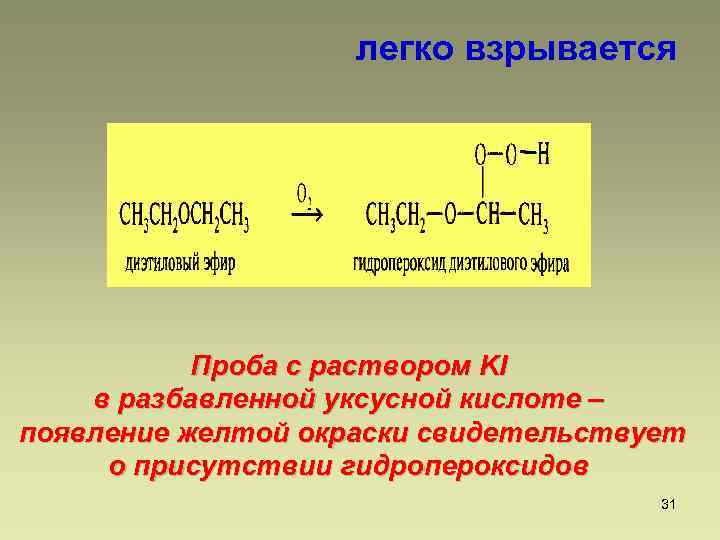
легко взрываeтся Проба с раствором KI в разбавленной уксусной кислоте – появление желтой окраски свидетельствует о присутствии гидропероксидов 31
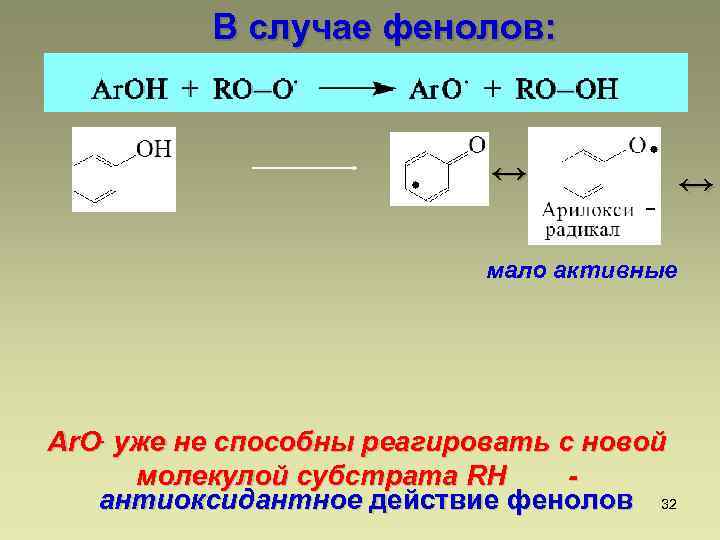
В случае фенолов: ↔ мало активные Ar. O. уже не способны реагировать с новой молекулой субстрата RH антиоксидантное действие фенолов 32 ↔
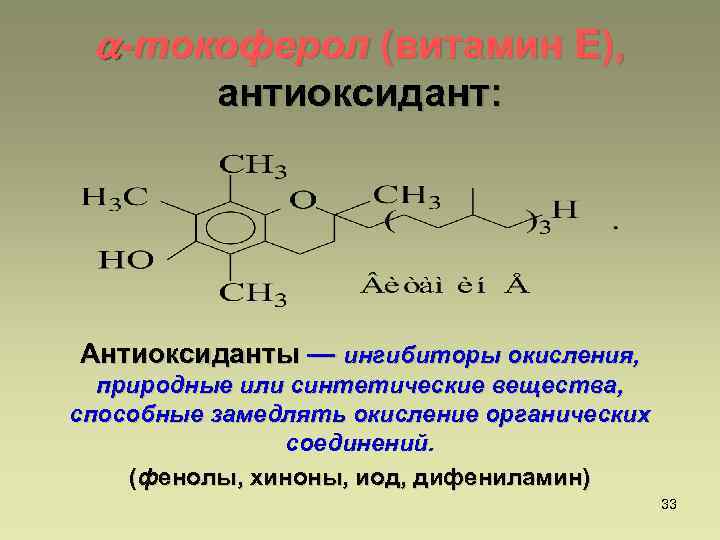
-токоферол (витамин Е), антиоксидант: Антиоксиданты — ингибиторы окисления, природные или синтетические вещества, способные замедлять окисление органических соединений. (фенолы, хиноны, иод, дифениламин) 33

Сравнительно малоактивны 34
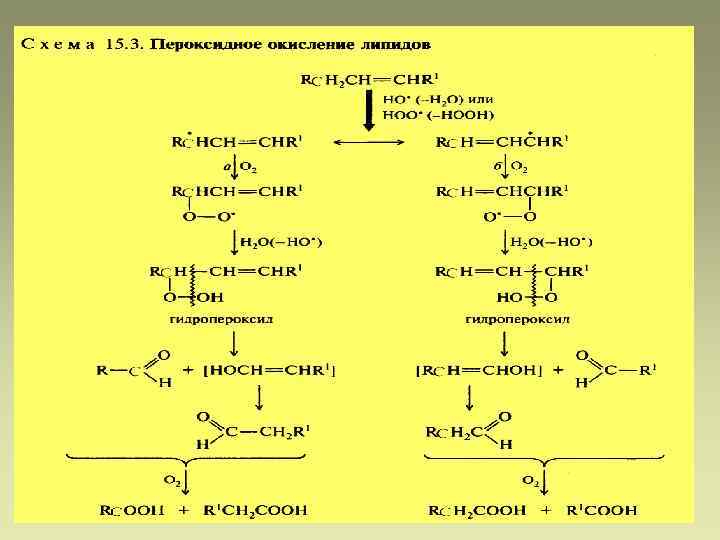
35

Спасибо за Ваше внимание! 36
5_alkany_2014__S_R.pptx