5. Микромир. Эволюция представлений о строении атома. Строение










































30784-estestvennonauchnaya_kartina_mira_4.ppt
- Количество слайдов: 44
 5. Микромир. Эволюция представлений о строении атома. Строение атомного ядра и периодическая система Д.И. Менделеева. Ядерные реакции. Радиоактивность. Элементарные частицы. Физика высоких энергий. Многообразие химических соединений. Химические связи.
5. Микромир. Эволюция представлений о строении атома. Строение атомного ядра и периодическая система Д.И. Менделеева. Ядерные реакции. Радиоактивность. Элементарные частицы. Физика высоких энергий. Многообразие химических соединений. Химические связи.
 Эволюция представлений о строении атома А́том (от др.-греч. ἄτομος — неделимый) — наименьшая химически неделимая часть химического элемента, являющаяся носителем его свойств. Атом состоит из атомного ядра и электронов. Ядро атома состоит из положительно заряженных протонов и незаряженных нейтронов. Если число протонов в ядре совпадает с числом электронов, то атом в целом оказывается электрически нейтральным. В противном случае он обладает некоторым положительным или отрицательным зарядом и называется ионом. Атомы классифицируются по количеству протонов и нейтронов в ядре: количество протонов определяет принадлежность атома некоторому химическому элементу, а число нейтронов — изотопу этого элемента.
Эволюция представлений о строении атома А́том (от др.-греч. ἄτομος — неделимый) — наименьшая химически неделимая часть химического элемента, являющаяся носителем его свойств. Атом состоит из атомного ядра и электронов. Ядро атома состоит из положительно заряженных протонов и незаряженных нейтронов. Если число протонов в ядре совпадает с числом электронов, то атом в целом оказывается электрически нейтральным. В противном случае он обладает некоторым положительным или отрицательным зарядом и называется ионом. Атомы классифицируются по количеству протонов и нейтронов в ядре: количество протонов определяет принадлежность атома некоторому химическому элементу, а число нейтронов — изотопу этого элемента.
 Эволюция представлений о строении атома Кусочки материи. Демокрит полагал, что свойства того или иного вещества определяются формой, массой, и пр. характеристиками образующих его атомов. Так, скажем, у огня атомы остры, поэтому огонь способен обжигать, у твёрдых тел они шероховаты, поэтому накрепко сцепляются друг с другом, у воды — гладки, поэтому она способна течь. Даже душа человека, согласно Демокриту, состоит из атомов.
Эволюция представлений о строении атома Кусочки материи. Демокрит полагал, что свойства того или иного вещества определяются формой, массой, и пр. характеристиками образующих его атомов. Так, скажем, у огня атомы остры, поэтому огонь способен обжигать, у твёрдых тел они шероховаты, поэтому накрепко сцепляются друг с другом, у воды — гладки, поэтому она способна течь. Даже душа человека, согласно Демокриту, состоит из атомов.
 Эволюция представлений о строении атома Корпускулярно-кинетическая теория тепла. М. В. Ломоносов утверждает, что все вещества состоят из «корпускул» — «молекул», которые являются «собраниями» «элементов» — «атомов»: «Элемент есть часть тела, не состоящая из каких-либо других меньших и отличающихся от него тел... Корпускула есть собрание элементов, образующее одну малую массу» . «Элементу» он придаёт современное ему значение — в смысле предела делимости тел — последней составной их части. Учёный указывает на шарообразную его форму. Именно М. В. Ломоносову принадлежит мысль о «внутреннем вращательном („коловратном“) движении частиц» — скорость вращения сказывается повышением температуры. При всех издержках такой модели, важно придание учёным понятию движения более глубокой физической значимости
Эволюция представлений о строении атома Корпускулярно-кинетическая теория тепла. М. В. Ломоносов утверждает, что все вещества состоят из «корпускул» — «молекул», которые являются «собраниями» «элементов» — «атомов»: «Элемент есть часть тела, не состоящая из каких-либо других меньших и отличающихся от него тел... Корпускула есть собрание элементов, образующее одну малую массу» . «Элементу» он придаёт современное ему значение — в смысле предела делимости тел — последней составной их части. Учёный указывает на шарообразную его форму. Именно М. В. Ломоносову принадлежит мысль о «внутреннем вращательном („коловратном“) движении частиц» — скорость вращения сказывается повышением температуры. При всех издержках такой модели, важно придание учёным понятию движения более глубокой физической значимости
 Эволюция представлений о строении атома Модель атома Томсона (модель «Пудинг с изюмом», англ. Plum pudding model). Дж. Дж. Томсон предложил рассматривать атом как некоторое положительно заряженное тело с заключёнными внутри него электронами. Согласно пудинговой модели, предложенной английским физиком Джозефом Джоном Томсоном, положительный заряд как бы размазан внутри объема атома. В атом как бы вкраплены отдельные электроны, нейтрализующие положительный заряд.
Эволюция представлений о строении атома Модель атома Томсона (модель «Пудинг с изюмом», англ. Plum pudding model). Дж. Дж. Томсон предложил рассматривать атом как некоторое положительно заряженное тело с заключёнными внутри него электронами. Согласно пудинговой модели, предложенной английским физиком Джозефом Джоном Томсоном, положительный заряд как бы размазан внутри объема атома. В атом как бы вкраплены отдельные электроны, нейтрализующие положительный заряд.
 Эволюция представлений о строении атома Ранняя планетарная модель атома Нагаоки. В 1904 году японский физик Хантаро Нагаока предложил модель атома, построенную по аналогии с планетой Сатурн. В этой модели вокруг маленького положительного ядра по орбитам вращались электроны, объединённые в кольца. Модель оказалось ошибочной, но некоторые важные её положения вошли в модель Резерфорда
Эволюция представлений о строении атома Ранняя планетарная модель атома Нагаоки. В 1904 году японский физик Хантаро Нагаока предложил модель атома, построенную по аналогии с планетой Сатурн. В этой модели вокруг маленького положительного ядра по орбитам вращались электроны, объединённые в кольца. Модель оказалось ошибочной, но некоторые важные её положения вошли в модель Резерфорда
 Эволюция представлений о строении атома Планетарная модель атома Бора-Резерфорда. В 1911 году Эрнест Резерфорд, проделав ряд экспериментов, пришёл к выводу, что атом представляет собой подобие планетной системы, в которой электроны движутся по орбитам вокруг расположенного в центре атома тяжёлого положительно заряженного ядра («модель атома Резерфорда»). Опыт Резерфорда Размер атомного ядра 10-15-10-14 м Размер электронной оболочки ~10-10 м
Эволюция представлений о строении атома Планетарная модель атома Бора-Резерфорда. В 1911 году Эрнест Резерфорд, проделав ряд экспериментов, пришёл к выводу, что атом представляет собой подобие планетной системы, в которой электроны движутся по орбитам вокруг расположенного в центре атома тяжёлого положительно заряженного ядра («модель атома Резерфорда»). Опыт Резерфорда Размер атомного ядра 10-15-10-14 м Размер электронной оболочки ~10-10 м
 Такое описание атома вошло в противоречие с классической электродинамикой. Дело в том, что, согласно классической электродинамике, электрон при движении с центростремительным ускорением должен излучать электромагнитные волны, а, следовательно, терять энергию. Расчеты показывали, что время, за которое электрон в таком атоме упадёт на ядро, совершенно ничтожно. Эволюция представлений о строении атома
Такое описание атома вошло в противоречие с классической электродинамикой. Дело в том, что, согласно классической электродинамике, электрон при движении с центростремительным ускорением должен излучать электромагнитные волны, а, следовательно, терять энергию. Расчеты показывали, что время, за которое электрон в таком атоме упадёт на ядро, совершенно ничтожно. Эволюция представлений о строении атома
 Эволюция представлений о строении атома Для объяснения стабильности атомов Нильсу Бору пришлось ввести постулаты, которые сводились к тому, что электрон в атоме, находясь в некоторых специальных энергетических состояниях, не излучает энергию («модель атома Бора-Резерфорда»).
Эволюция представлений о строении атома Для объяснения стабильности атомов Нильсу Бору пришлось ввести постулаты, которые сводились к тому, что электрон в атоме, находясь в некоторых специальных энергетических состояниях, не излучает энергию («модель атома Бора-Резерфорда»).
 Эволюция представлений о строении атома Теория Бора для атома водорода ПОСТУЛАТЫ БОРА: 1. В атоме электроны могут двигаться только по определенным, так называемым разрешенным, или стационарным, круговым орбитам 2. Атом излучает или поглощает квант электромагнитной энергии при переходе электрона с одной стационарной орбиты на другую 3. На стационарных орбитах момент импульса электрона Ln= meυnrn кратен величине h/(2π)
Эволюция представлений о строении атома Теория Бора для атома водорода ПОСТУЛАТЫ БОРА: 1. В атоме электроны могут двигаться только по определенным, так называемым разрешенным, или стационарным, круговым орбитам 2. Атом излучает или поглощает квант электромагнитной энергии при переходе электрона с одной стационарной орбиты на другую 3. На стационарных орбитах момент импульса электрона Ln= meυnrn кратен величине h/(2π)
 Эволюция представлений о строении атома Постулаты Бора показали, что для описания атома классическая механика неприменима. Дальнейшее изучение излучения атома привело к созданию квантовой механики, которая позволила объяснить подавляющее большинство наблюдаемых фактов.
Эволюция представлений о строении атома Постулаты Бора показали, что для описания атома классическая механика неприменима. Дальнейшее изучение излучения атома привело к созданию квантовой механики, которая позволила объяснить подавляющее большинство наблюдаемых фактов.
 Эволюция представлений о строении атома Законы Ньютона продержались у власти 250 лет и были свергнуты в 1925 г., когда Вернер Гейзенберг, Эрвин Шрёдингер и их коллеги разработали квантовую теорию. Анализируя странные свойства атомов, физики обнаружили, что электрон ведет себя как волна и в кажущейся хаотичности своего движения внутри атома может совершать квантовые скачки. Теснее всего с представлением о квантовых волнах связан венский физик Эрвин Шрёдингер, создатель знаменитого волнового уравнения, названного его именем, — одного из важнейших уравнений физики и химии. Целые институтские курсы посвящены решению этого знаменитого уравнения; целые стены физических библиотек заняты книгами, в которых подробно исследуются его глубокие следствия. В принципе вся сумма знаний по химии может быть сведена к решениям этого уравнения.
Эволюция представлений о строении атома Законы Ньютона продержались у власти 250 лет и были свергнуты в 1925 г., когда Вернер Гейзенберг, Эрвин Шрёдингер и их коллеги разработали квантовую теорию. Анализируя странные свойства атомов, физики обнаружили, что электрон ведет себя как волна и в кажущейся хаотичности своего движения внутри атома может совершать квантовые скачки. Теснее всего с представлением о квантовых волнах связан венский физик Эрвин Шрёдингер, создатель знаменитого волнового уравнения, названного его именем, — одного из важнейших уравнений физики и химии. Целые институтские курсы посвящены решению этого знаменитого уравнения; целые стены физических библиотек заняты книгами, в которых подробно исследуются его глубокие следствия. В принципе вся сумма знаний по химии может быть сведена к решениям этого уравнения.
 Эволюция представлений о строении атома В 1905 г. Эйнштейн показал, что световые волны могут вести себя наподобие частиц; это значит, что они могут быть описаны как пакеты энергии, известные под названием фотонов. Но примерно к 1920 г. Шрёдингеру стало очевидно, что обратное тоже верно: частицы, к примеру электроны, могут вести себя подобно волнам. Эту идею первым высказал французский физик Луи де Бройль, удостоенный за эту гипотезу Нобелевской премии. Как-то Шрёдингер читал лекцию об этом любопытном феномене. Один из присутствовавших в зале коллег-физиков Питер Дебай задал вопрос: «Если электрон можно описать как волну; то как выглядит его волновое уравнение?» Луи Виктор Пьер Раймон де Бройль (1892 - 1987) Питер Дебай (1884 - 1966)
Эволюция представлений о строении атома В 1905 г. Эйнштейн показал, что световые волны могут вести себя наподобие частиц; это значит, что они могут быть описаны как пакеты энергии, известные под названием фотонов. Но примерно к 1920 г. Шрёдингеру стало очевидно, что обратное тоже верно: частицы, к примеру электроны, могут вести себя подобно волнам. Эту идею первым высказал французский физик Луи де Бройль, удостоенный за эту гипотезу Нобелевской премии. Как-то Шрёдингер читал лекцию об этом любопытном феномене. Один из присутствовавших в зале коллег-физиков Питер Дебай задал вопрос: «Если электрон можно описать как волну; то как выглядит его волновое уравнение?» Луи Виктор Пьер Раймон де Бройль (1892 - 1987) Питер Дебай (1884 - 1966)
 Эволюция представлений о строении атома Шредингер, к немалому своему удивлению, обнаружил, что энергетические уровни электронов уже до него были точно установлены и опубликованы другими физиками. После этого он понял, что старая модель атома, принадлежащая Нильсу Бору, — та самая, где электроны носятся вокруг ядра и которую до сих пор рисуют в книгах и рекламных проспектах как символ современной науки — на самом деле неверна. Круговые орбиты электронов вокруг ядра атома необходимо заменить волнами.
Эволюция представлений о строении атома Шредингер, к немалому своему удивлению, обнаружил, что энергетические уровни электронов уже до него были точно установлены и опубликованы другими физиками. После этого он понял, что старая модель атома, принадлежащая Нильсу Бору, — та самая, где электроны носятся вокруг ядра и которую до сих пор рисуют в книгах и рекламных проспектах как символ современной науки — на самом деле неверна. Круговые орбиты электронов вокруг ядра атома необходимо заменить волнами.
 Эволюция представлений о строении атома Макс Бор (1882 - 1970) Но оставался еще один вопрос, который не дает физикам покоя даже сегодня. Если электрон описывается как волна, то что же в нем колеблется? Ответ на этот вопрос дал физик Макс Борн; он сказал, что эти волны представляют собой не что иное, как волны вероятности. Они сообщают только о том, с какой вероятностью вы обнаружите конкретный электрон в определенное время в определенной точке. Другими словами, электрон — это частица, но вероятность обнаружить эту частицу задается волной Шрёдингера. И чем выше волна, тем больше шансов обнаружить частицу именно в этой точке. Получается, что внезапно в самом сердце физики — науки, которая прежде давала нам точные предсказания и подробные траектории любых объектов, начиная с планет и комет и кончая пушечными ядрами, — оказались понятия шанса и вероятности.
Эволюция представлений о строении атома Макс Бор (1882 - 1970) Но оставался еще один вопрос, который не дает физикам покоя даже сегодня. Если электрон описывается как волна, то что же в нем колеблется? Ответ на этот вопрос дал физик Макс Борн; он сказал, что эти волны представляют собой не что иное, как волны вероятности. Они сообщают только о том, с какой вероятностью вы обнаружите конкретный электрон в определенное время в определенной точке. Другими словами, электрон — это частица, но вероятность обнаружить эту частицу задается волной Шрёдингера. И чем выше волна, тем больше шансов обнаружить частицу именно в этой точке. Получается, что внезапно в самом сердце физики — науки, которая прежде давала нам точные предсказания и подробные траектории любых объектов, начиная с планет и комет и кончая пушечными ядрами, — оказались понятия шанса и вероятности.
 Эволюция представлений о строении атома Вернер Карл Гейзенберг (1901 - 1976) Гейзенберг сумел формализовать этот факт, предложив принцип неопределенности (По иронии судьбы и Эйнштейн, крестный отец квантовой теории, принимавший участие в революционных преобразованиях 1905 г., и Шрёдингер, автор волнового уравнения, пришли в ужас от появления случайных процессов в фундаментальной физике. Эйнштейн писал: «Квантовая механика вызывает огромное уважение. Но внутренний голос подсказывает мне, что это не то, что нужно. Эта теория многое объясняет, но едва ли приближает нас хоть сколько-то к тайне Бога. По крайней мере о себе могу сказать точно: я убежден, что Он не играет в кости».) Теория Гейзенберга была революционной и противоречивой, но работала. С ее помощью физикам удалось одним махом объяснить огромное число загадочных явлений, включая законы химии.
Эволюция представлений о строении атома Вернер Карл Гейзенберг (1901 - 1976) Гейзенберг сумел формализовать этот факт, предложив принцип неопределенности (По иронии судьбы и Эйнштейн, крестный отец квантовой теории, принимавший участие в революционных преобразованиях 1905 г., и Шрёдингер, автор волнового уравнения, пришли в ужас от появления случайных процессов в фундаментальной физике. Эйнштейн писал: «Квантовая механика вызывает огромное уважение. Но внутренний голос подсказывает мне, что это не то, что нужно. Эта теория многое объясняет, но едва ли приближает нас хоть сколько-то к тайне Бога. По крайней мере о себе могу сказать точно: я убежден, что Он не играет в кости».) Теория Гейзенберга была революционной и противоречивой, но работала. С ее помощью физикам удалось одним махом объяснить огромное число загадочных явлений, включая законы химии.
 Эволюция представлений о строении атома Невозможно точно определить скорость и точное положение электрона в один и тот же момент. Невозможно точно определить и его энергию в заданный промежуток времени. Пример: частица с определённым значением энергии, находящаяся в коробке с идеально отражающими стенками; она не характеризуется ни каким-либо определённым «положением» или пространственной координатой (волновая функция частицы делокализована на всё пространство коробки, то есть ее координаты не имеют определенного значения, локализация частицы осуществлена не точнее размеров коробки), ни определённым значением импульса (учитывая его направление)!
Эволюция представлений о строении атома Невозможно точно определить скорость и точное положение электрона в один и тот же момент. Невозможно точно определить и его энергию в заданный промежуток времени. Пример: частица с определённым значением энергии, находящаяся в коробке с идеально отражающими стенками; она не характеризуется ни каким-либо определённым «положением» или пространственной координатой (волновая функция частицы делокализована на всё пространство коробки, то есть ее координаты не имеют определенного значения, локализация частицы осуществлена не точнее размеров коробки), ни определённым значением импульса (учитывая его направление)!
 Энергия связи и дефект массы. Ядерные реакции Тот факт, что электроны, по-видимому, могут находиться во многих местах одновременно, составляет фундамент всей химии. Мы думаем, что электроны обращаются вокруг ядра атома, как тела миниатюрной Солнечной системы. Но между атомом и Солнечной системой есть принципиальные различия. При столкновении в космосе двух Солнечных систем они неизбежно развалятся, планеты при этом отбросит в разных направлениях. Атомы же, сталкиваясь, часто делятся друг с другом электронами и образуют вполне стабильные молекулы. В старших классах школы учитель часто говорит ученикам про «размазанный электрон», напоминающий продолговатый мяч для регби; он соединяет два атома между собой. Но вот о чем учителя химии почти никогда не рассказывают ученикам. Электрон, о котором идет речь, вовсе не «размазан» между двумя атомами. На самом деле этот «мяч для регби» представляет вероятность того, что электрон находится одновременно во множестве мест внутри данного объема. Другими словами, вся химия, изучающая и объясняющая строение молекул, из которых состоят наши тела, основана на представлении о том, что электроны могут находиться одновременно в нескольких местах; именно такое «совместное владение» электронами, которые умудряются одновременно принадлежать двум атомам, удерживает на месте атомы в молекулах нашего тела. Без квантовой теории наши молекулы и атомы распались бы в мгновение ока.
Энергия связи и дефект массы. Ядерные реакции Тот факт, что электроны, по-видимому, могут находиться во многих местах одновременно, составляет фундамент всей химии. Мы думаем, что электроны обращаются вокруг ядра атома, как тела миниатюрной Солнечной системы. Но между атомом и Солнечной системой есть принципиальные различия. При столкновении в космосе двух Солнечных систем они неизбежно развалятся, планеты при этом отбросит в разных направлениях. Атомы же, сталкиваясь, часто делятся друг с другом электронами и образуют вполне стабильные молекулы. В старших классах школы учитель часто говорит ученикам про «размазанный электрон», напоминающий продолговатый мяч для регби; он соединяет два атома между собой. Но вот о чем учителя химии почти никогда не рассказывают ученикам. Электрон, о котором идет речь, вовсе не «размазан» между двумя атомами. На самом деле этот «мяч для регби» представляет вероятность того, что электрон находится одновременно во множестве мест внутри данного объема. Другими словами, вся химия, изучающая и объясняющая строение молекул, из которых состоят наши тела, основана на представлении о том, что электроны могут находиться одновременно в нескольких местах; именно такое «совместное владение» электронами, которые умудряются одновременно принадлежать двум атомам, удерживает на месте атомы в молекулах нашего тела. Без квантовой теории наши молекулы и атомы распались бы в мгновение ока.
 Эволюция представлений о строении атома Согласно квантовой механике, не существует определенных круговых орбит электронов, как в теории Бора. В силу волновой природы электрон «размазан» в пространстве, подобно «облаку» отрицательного заряда.
Эволюция представлений о строении атома Согласно квантовой механике, не существует определенных круговых орбит электронов, как в теории Бора. В силу волновой природы электрон «размазан» в пространстве, подобно «облаку» отрицательного заряда.
 Энергия связи и дефект массы. Ядерные реакции А́томное ядро́ — центральная часть атома, в которой сосредоточена основная его масса (более 99,9 %). Атомное ядро состоит из нуклонов — положительно заряженных протонов и нейтральных нейтронов, которые связаны между собой при помощи сильного взаимодействия Ядро заряжено положительно, и величина заряда определяется количеством протонов в ядре Заряд ядра определяет химический элемент, к которому относится атом. Размеры ядер различных атомов составляют несколько фемтометров, что в более чем в 10 тысяч раз меньше размеров самого атома. Ядра с одинаковыми количествами протонов Z и разными количествами нейтронов A называются изотопами Ядра с одинаковым числом нейтронов, но разным числом протонов — называются изотонами Число протонов в ядре (зарядовое число, также порядковый номер элемента) принято обозначать через Z, число нейтронов — через N. Их сумма A = Z + N называется массовым числом ядра.
Энергия связи и дефект массы. Ядерные реакции А́томное ядро́ — центральная часть атома, в которой сосредоточена основная его масса (более 99,9 %). Атомное ядро состоит из нуклонов — положительно заряженных протонов и нейтральных нейтронов, которые связаны между собой при помощи сильного взаимодействия Ядро заряжено положительно, и величина заряда определяется количеством протонов в ядре Заряд ядра определяет химический элемент, к которому относится атом. Размеры ядер различных атомов составляют несколько фемтометров, что в более чем в 10 тысяч раз меньше размеров самого атома. Ядра с одинаковыми количествами протонов Z и разными количествами нейтронов A называются изотопами Ядра с одинаковым числом нейтронов, но разным числом протонов — называются изотонами Число протонов в ядре (зарядовое число, также порядковый номер элемента) принято обозначать через Z, число нейтронов — через N. Их сумма A = Z + N называется массовым числом ядра.
 Энергия связи и дефект массы. Ядерные реакции Дефект массы - заряд ядра равен сумме зарядов входящих в него протонов, масса ядра не равна сумме масс отдельных свободных протонов и нейтронов (нуклонов), она несколько меньше ее Нуклоны в ядре прочно удерживаются ядерными силами. Для того чтобы удалить нуклон из ядра, надо совершить большую работу, т. е. сообщить ядру значительную энергию. Энергия связи атомного ядра Есв характеризует интенсивность взаимодействия нуклонов в ядре и равна той максимальной энергии, которую необходимо затратить, чтобы разделить ядро на отдельные невзаимодействующие нуклоны без сообщения им кинетической энергии. У каждого ядра своя энергия связи. Чем больше эта энергия, тем более устойчиво атомное ядро. Точные измерения масс ядра показывают, что масса покоя ядра m0 всегда меньше суммы масс покоя, составляющих его протонов и нейтронов. Эту разность масс называют дефектом массы:
Энергия связи и дефект массы. Ядерные реакции Дефект массы - заряд ядра равен сумме зарядов входящих в него протонов, масса ядра не равна сумме масс отдельных свободных протонов и нейтронов (нуклонов), она несколько меньше ее Нуклоны в ядре прочно удерживаются ядерными силами. Для того чтобы удалить нуклон из ядра, надо совершить большую работу, т. е. сообщить ядру значительную энергию. Энергия связи атомного ядра Есв характеризует интенсивность взаимодействия нуклонов в ядре и равна той максимальной энергии, которую необходимо затратить, чтобы разделить ядро на отдельные невзаимодействующие нуклоны без сообщения им кинетической энергии. У каждого ядра своя энергия связи. Чем больше эта энергия, тем более устойчиво атомное ядро. Точные измерения масс ядра показывают, что масса покоя ядра m0 всегда меньше суммы масс покоя, составляющих его протонов и нейтронов. Эту разность масс называют дефектом массы:
 1896-1899гг.-А. Беккерель и супруги Кюри открыли радиоактивность. Радиоактивность – способность вещества испускать невидимые лучи: альфа, бета и гамма лучи. При этом происходит изменение химических свойств вещества. Атомы радиоактивных элементов, излучая превращаются в атомы другого вещества. распад: ядро самопроизвольно выделяет альфа-частицу, которые представляют ядра гелия, состоящие из двух протонов (Н++) Ядерные реакции
1896-1899гг.-А. Беккерель и супруги Кюри открыли радиоактивность. Радиоактивность – способность вещества испускать невидимые лучи: альфа, бета и гамма лучи. При этом происходит изменение химических свойств вещества. Атомы радиоактивных элементов, излучая превращаются в атомы другого вещества. распад: ядро самопроизвольно выделяет альфа-частицу, которые представляют ядра гелия, состоящие из двух протонов (Н++) Ядерные реакции
 Ядерные реакции распад: излучение электронов е-или позитронов е+ Бе́та-распа́д — тип радиоактивного распада, обусловленного слабым взаимодействием и изменяющего заряд ядра на единицу. При этом ядро может излучать бета-частицу (электрон или позитрон). В случае испускания электрона он называется «бета-минус» (β − ), а в случае испускания позитрона — «бета-плюс-распадом» (β + ). Кроме β − и β + -распадов, к бета-распадам относят также электронный захват, когда ядро захватывает атомный электрон. Во всех типах бета-распада ядро излучает электронное нейтрино (β + -распад, электронный захват) или антинейтрино (β − -распад).
Ядерные реакции распад: излучение электронов е-или позитронов е+ Бе́та-распа́д — тип радиоактивного распада, обусловленного слабым взаимодействием и изменяющего заряд ядра на единицу. При этом ядро может излучать бета-частицу (электрон или позитрон). В случае испускания электрона он называется «бета-минус» (β − ), а в случае испускания позитрона — «бета-плюс-распадом» (β + ). Кроме β − и β + -распадов, к бета-распадам относят также электронный захват, когда ядро захватывает атомный электрон. Во всех типах бета-распада ядро излучает электронное нейтрино (β + -распад, электронный захват) или антинейтрино (β − -распад).
 Ядерные реакции Развитие квантовой механики в 1920-х годах привело к пониманию дискретности энергетических уровней в атомном ядре: это предположение было высказано австрийским физиком Лизой Мейтнер в 1922 году. То есть, спектр вылетающих при распаде ядра частиц должен быть дискретным, и показывать энергии, равные разницам энергий уровней, между которыми происходит переход при распаде. Таковым, например, является спектр альфа-частиц при альфа-распаде. Таким образом, непрерывность спектра электронов β-распада ставила под сомнение закон сохранения энергии. Вопрос стоял настолько остро, что в 1931 г. знаменитый датский физик Н. Бор на Римской конференции выступил с идеей о несохранении энергии! Однако было и другое объяснение — потерянную энергию уносит какая-то неизвестная и незаметная частица. Гипотезу о существовании чрезвычайно слабо взаимодействующей с веществом частицы выдвинул 4 декабря 1930 г. Паули — не в статье, а в неформальном письме участникам физической конференции в Тюбингене: …имея в виду … непрерывный β-спектр, я предпринял отчаянную попытку спасти «обменную статистику» и закон сохранения энергии. Именно имеется возможность того, что в ядрах существуют электрически нейтральные частицы, которые я буду называть «нейтронами» и которые обладают спином 1/2… Масса «нейтрона» по порядку величины должна быть сравнимой с массой электрона и во всяком случае не более 0,01 массы протона. Непрерывный β-спектр тогда стал бы понятным, если предположить, что при β-распаде вместе с электроном испускается ещё и «нейтрон», таким образом, что сумма энергий «нейтрона» и электрона остаётся постоянной. Я признаю, что такой выход может показаться на первый взгляд маловероятным… Однако, не рискнув, не выиграешь; серьёзность положения с непрерывным β-спектром хорошо проиллюстрировал мой уважаемый предшественник г-н Дебай, который недавно заявил мне в Брюсселе: «О… об этом лучше не думать вовсе, как о новых налогах». Нейтри́но — нейтральная фундаментальная частица с полуцелым спином, участвующая только в слабом и гравитационном взаимодействиях, и относящаяся к классу лептонов. Нейтрино малой энергии чрезвычайно слабо взаимодействуют с веществом: так, нейтрино с энергией порядка 3-10 МэВ имеют в воде длину свободного пробега порядка 1018 м (около 100 св. лет). Также известно, что каждую секунду через площадку на Земле в 1 см² проходит около 6×1010 нейтрино, испущенных Солнцем.
Ядерные реакции Развитие квантовой механики в 1920-х годах привело к пониманию дискретности энергетических уровней в атомном ядре: это предположение было высказано австрийским физиком Лизой Мейтнер в 1922 году. То есть, спектр вылетающих при распаде ядра частиц должен быть дискретным, и показывать энергии, равные разницам энергий уровней, между которыми происходит переход при распаде. Таковым, например, является спектр альфа-частиц при альфа-распаде. Таким образом, непрерывность спектра электронов β-распада ставила под сомнение закон сохранения энергии. Вопрос стоял настолько остро, что в 1931 г. знаменитый датский физик Н. Бор на Римской конференции выступил с идеей о несохранении энергии! Однако было и другое объяснение — потерянную энергию уносит какая-то неизвестная и незаметная частица. Гипотезу о существовании чрезвычайно слабо взаимодействующей с веществом частицы выдвинул 4 декабря 1930 г. Паули — не в статье, а в неформальном письме участникам физической конференции в Тюбингене: …имея в виду … непрерывный β-спектр, я предпринял отчаянную попытку спасти «обменную статистику» и закон сохранения энергии. Именно имеется возможность того, что в ядрах существуют электрически нейтральные частицы, которые я буду называть «нейтронами» и которые обладают спином 1/2… Масса «нейтрона» по порядку величины должна быть сравнимой с массой электрона и во всяком случае не более 0,01 массы протона. Непрерывный β-спектр тогда стал бы понятным, если предположить, что при β-распаде вместе с электроном испускается ещё и «нейтрон», таким образом, что сумма энергий «нейтрона» и электрона остаётся постоянной. Я признаю, что такой выход может показаться на первый взгляд маловероятным… Однако, не рискнув, не выиграешь; серьёзность положения с непрерывным β-спектром хорошо проиллюстрировал мой уважаемый предшественник г-н Дебай, который недавно заявил мне в Брюсселе: «О… об этом лучше не думать вовсе, как о новых налогах». Нейтри́но — нейтральная фундаментальная частица с полуцелым спином, участвующая только в слабом и гравитационном взаимодействиях, и относящаяся к классу лептонов. Нейтрино малой энергии чрезвычайно слабо взаимодействуют с веществом: так, нейтрино с энергией порядка 3-10 МэВ имеют в воде длину свободного пробега порядка 1018 м (около 100 св. лет). Также известно, что каждую секунду через площадку на Земле в 1 см² проходит около 6×1010 нейтрино, испущенных Солнцем.
 Ядерные реакции излучение. Вторичное излучение, следующее за альфа и бета распадом. При альфа и бета распаде ядро может перейти в возбуждённое состояние, избыток энергии удаляется при выделении гамма-излучения. Изоме́рный перехо́д (га́мма-распа́д) — радиоактивный распад атомного ядра, происходящий из возбуждённого метастабильного состояния с излучением одного или нескольких гамма-квантов. Га́мма-излуче́ние (гамма-лучи, γ-лучи) — вид электромагнитного излучения с чрезвычайно малой длиной волны — < 5×10−3 нм и, вследствие этого, ярко выраженными корпускулярными и слабо выраженными волновыми свойствами. Гамма-квантами являются фотоны с высокой энергией. Считается, что энергии квантов гамма-излучения превышают 105 эВ, хотя резкая граница между гамма- и рентгеновским излучением не определена. На шкале электромагнитных волн гамма-излучение граничит с рентгеновским излучением, занимая диапазон более высоких частот и энергий. В области 1-100 кэВ гамма-излучение и рентгеновское излучение различаются только по источнику: если квант излучается в ядерном переходе, то его принято относить к гамма-излучению; если при взаимодействиях электронов или при переходах в атомной электронной оболочке — к рентгеновскому излучению. С точки зрения физики, кванты электромагнитного излучения с одинаковой энергией не отличаются, поэтому такое разделение условно
Ядерные реакции излучение. Вторичное излучение, следующее за альфа и бета распадом. При альфа и бета распаде ядро может перейти в возбуждённое состояние, избыток энергии удаляется при выделении гамма-излучения. Изоме́рный перехо́д (га́мма-распа́д) — радиоактивный распад атомного ядра, происходящий из возбуждённого метастабильного состояния с излучением одного или нескольких гамма-квантов. Га́мма-излуче́ние (гамма-лучи, γ-лучи) — вид электромагнитного излучения с чрезвычайно малой длиной волны — < 5×10−3 нм и, вследствие этого, ярко выраженными корпускулярными и слабо выраженными волновыми свойствами. Гамма-квантами являются фотоны с высокой энергией. Считается, что энергии квантов гамма-излучения превышают 105 эВ, хотя резкая граница между гамма- и рентгеновским излучением не определена. На шкале электромагнитных волн гамма-излучение граничит с рентгеновским излучением, занимая диапазон более высоких частот и энергий. В области 1-100 кэВ гамма-излучение и рентгеновское излучение различаются только по источнику: если квант излучается в ядерном переходе, то его принято относить к гамма-излучению; если при взаимодействиях электронов или при переходах в атомной электронной оболочке — к рентгеновскому излучению. С точки зрения физики, кванты электромагнитного излучения с одинаковой энергией не отличаются, поэтому такое разделение условно
 Реакция деления и синтеза. Основы ядерной энергетики Термоядерный синтез При нормальной температуре слияние ядер невозможно, так как положительно заряженные ядра испытывают огромные силы кулоновского отталкивания. Для синтеза легких ядер необходимо сблизить их на расстояние порядка 10−15 м, на котором действие ядерных сил притяжения будет превышать кулоновские силы отталкивания. Для того чтобы произошло слияние ядер, необходимо увеличить их подвижность, то есть увеличить их кинетическую энергию. Это достигается повышением температуры. За счет полученной тепловой энергии увеличивается подвижность ядер, и они могут подойти друг к другу на такие близкие расстояния, что под действием ядерных сил сцепления сольются в новое более сложное ядро. В результате слияния легких ядер освобождается большая энергия, так как образовавшееся новое ядро имеет большую удельную энергию связи, чем исходные ядра. Термоядерная реакция — это экзоэнергетическая реакция слияния легких ядер при очень высокой температуре (107 К). Прежде всего, среди них следует отметить реакцию между двумя изотопами (дейтерий и тритий) весьма распространенного на Земле водорода, в результате которой образуется гелий и выделяется нейтрон. Реакция может быть записана в виде
Реакция деления и синтеза. Основы ядерной энергетики Термоядерный синтез При нормальной температуре слияние ядер невозможно, так как положительно заряженные ядра испытывают огромные силы кулоновского отталкивания. Для синтеза легких ядер необходимо сблизить их на расстояние порядка 10−15 м, на котором действие ядерных сил притяжения будет превышать кулоновские силы отталкивания. Для того чтобы произошло слияние ядер, необходимо увеличить их подвижность, то есть увеличить их кинетическую энергию. Это достигается повышением температуры. За счет полученной тепловой энергии увеличивается подвижность ядер, и они могут подойти друг к другу на такие близкие расстояния, что под действием ядерных сил сцепления сольются в новое более сложное ядро. В результате слияния легких ядер освобождается большая энергия, так как образовавшееся новое ядро имеет большую удельную энергию связи, чем исходные ядра. Термоядерная реакция — это экзоэнергетическая реакция слияния легких ядер при очень высокой температуре (107 К). Прежде всего, среди них следует отметить реакцию между двумя изотопами (дейтерий и тритий) весьма распространенного на Земле водорода, в результате которой образуется гелий и выделяется нейтрон. Реакция может быть записана в виде
 Реакция деления и синтеза. Основы ядерной энергетики Деление тяжелого ядра на два более легких (средних ) при бомбардировке ядра урана свободным нейтроном Деле́ние ядра́ — процесс расщепления атомного ядра на два (реже три) ядра с близкими массами, называемых осколками деления. В результате деления могут возникать и другие продукты реакции: лёгкие ядра (в основном альфа-частицы), нейтроны и гамма-кванты. Деление бывает спонтанным (самопроизвольным) и вынужденным (в результате взаимодействия с другими частицами, прежде всего, с нейтронами). Деление тяжёлых ядер — экзотермический процесс, в результате которого высвобождается большое количество энергии в виде кинетической энергии продуктов реакции, а также излучения. Деление ядер служит источником энергии в ядерных реакторах и ядерном оружии.
Реакция деления и синтеза. Основы ядерной энергетики Деление тяжелого ядра на два более легких (средних ) при бомбардировке ядра урана свободным нейтроном Деле́ние ядра́ — процесс расщепления атомного ядра на два (реже три) ядра с близкими массами, называемых осколками деления. В результате деления могут возникать и другие продукты реакции: лёгкие ядра (в основном альфа-частицы), нейтроны и гамма-кванты. Деление бывает спонтанным (самопроизвольным) и вынужденным (в результате взаимодействия с другими частицами, прежде всего, с нейтронами). Деление тяжёлых ядер — экзотермический процесс, в результате которого высвобождается большое количество энергии в виде кинетической энергии продуктов реакции, а также излучения. Деление ядер служит источником энергии в ядерных реакторах и ядерном оружии.
 Элементарные частицы Все элементарные частицы делятся по величине спина на два класса: фермионы — частицы с полуцелым спином (например, электрон, протон, нейтрон, нейтрино); бозоны — частицы с целым спином (например, фотон, глюон, мезоны). По видам взаимодействий элементарные частицы делятся на следующие группы: Составные частицы адроны — частицы, участвующие во всех видах фундаментальных взаимодействий. Они состоят из кварков Фундаментальные (бесструктурные) частицы лептоны — фермионы, которые имеют вид точечных частиц (не участвуют в сильных взаимодействиях). Известны 6 типов лептонов. кварки — дробнозаряженные частицы, входящие в состав адронов. В свободном состоянии не наблюдались. Как и лептоны, делятся на 6 типов и считаются бесструктурными, однако, в отличие от лептонов, участвуют в сильном взаимодействии. калибровочные бозоны — частицы, посредством обмена которыми осуществляются взаимодействия: фотон — частица, переносящая электромагнитное взаимодействие; восемь глюонов — частиц, переносящих сильное взаимодействие; три промежуточных векторных бозона W+, W− и Z0, переносящие слабое взаимодействие;
Элементарные частицы Все элементарные частицы делятся по величине спина на два класса: фермионы — частицы с полуцелым спином (например, электрон, протон, нейтрон, нейтрино); бозоны — частицы с целым спином (например, фотон, глюон, мезоны). По видам взаимодействий элементарные частицы делятся на следующие группы: Составные частицы адроны — частицы, участвующие во всех видах фундаментальных взаимодействий. Они состоят из кварков Фундаментальные (бесструктурные) частицы лептоны — фермионы, которые имеют вид точечных частиц (не участвуют в сильных взаимодействиях). Известны 6 типов лептонов. кварки — дробнозаряженные частицы, входящие в состав адронов. В свободном состоянии не наблюдались. Как и лептоны, делятся на 6 типов и считаются бесструктурными, однако, в отличие от лептонов, участвуют в сильном взаимодействии. калибровочные бозоны — частицы, посредством обмена которыми осуществляются взаимодействия: фотон — частица, переносящая электромагнитное взаимодействие; восемь глюонов — частиц, переносящих сильное взаимодействие; три промежуточных векторных бозона W+, W− и Z0, переносящие слабое взаимодействие;
 Элементарные частицы Всё вещество состоит из 12 фундаментальных частиц-фермионов: 6 лептонов (электрон, мюон, тау-лептон, и три сорта нейтрино) и 6 кварков (u, d, s, c, b, t), которые можно объединить в три поколения фермионов.
Элементарные частицы Всё вещество состоит из 12 фундаментальных частиц-фермионов: 6 лептонов (электрон, мюон, тау-лептон, и три сорта нейтрино) и 6 кварков (u, d, s, c, b, t), которые можно объединить в три поколения фермионов.
 Физика высоких энергий ФИЗИКА ВЫСОКИХ ЭНЕРГИЙ — раздел физики элементарных частиц, изучающий взаимодействия элементарных частиц и/или ядер атомов при энергиях столкновения, существенно выше, чем массы самих сталкивающихся частиц. Эксперименты по физике высоких энергий проводятся с помощью ускорителей заряженных частиц и ядерных реакторов. Также источником частиц высоких энергий являются космические лучи. В неускорительных экспериментах с космическими лучами изучают, в основном, свойства нейтрино и поведение частиц при сверхвысоких энергиях (широкие космические ливни). Основа любого эксперимента в области физики высоких энергий — детекторы ионизирующего излучения и гамма-лучей.
Физика высоких энергий ФИЗИКА ВЫСОКИХ ЭНЕРГИЙ — раздел физики элементарных частиц, изучающий взаимодействия элементарных частиц и/или ядер атомов при энергиях столкновения, существенно выше, чем массы самих сталкивающихся частиц. Эксперименты по физике высоких энергий проводятся с помощью ускорителей заряженных частиц и ядерных реакторов. Также источником частиц высоких энергий являются космические лучи. В неускорительных экспериментах с космическими лучами изучают, в основном, свойства нейтрино и поведение частиц при сверхвысоких энергиях (широкие космические ливни). Основа любого эксперимента в области физики высоких энергий — детекторы ионизирующего излучения и гамма-лучей.
 Физика высоких энергий Ускори́тель заря́женных части́ц — класс устройств для получения заряженных частиц (элементарных частиц, ионов) высоких энергий. Современные ускорители, подчас, являются огромными дорогостоящими комплексами, которые не может позволить себе даже крупное государство. В основе работы ускорителя заложено взаимодействие заряженных частиц с электрическим и магнитным полями. Электрическое поле способно напрямую совершать работу над частицей, то есть увеличивать её энергию. Магнитное же поле, создавая силу Лоренца, только отклоняет частицу, не изменяя её энергии, и задаёт орбиту, по которой движутся частицы
Физика высоких энергий Ускори́тель заря́женных части́ц — класс устройств для получения заряженных частиц (элементарных частиц, ионов) высоких энергий. Современные ускорители, подчас, являются огромными дорогостоящими комплексами, которые не может позволить себе даже крупное государство. В основе работы ускорителя заложено взаимодействие заряженных частиц с электрическим и магнитным полями. Электрическое поле способно напрямую совершать работу над частицей, то есть увеличивать её энергию. Магнитное же поле, создавая силу Лоренца, только отклоняет частицу, не изменяя её энергии, и задаёт орбиту, по которой движутся частицы
 Физика высоких энергий Большой адро́нный колла́йдер, сокр. БАК (англ. Large Hadron Collider, сокр. LHC) — ускоритель заряженных частиц на встречных пучках, предназначенный для разгона протонов и тяжёлых ионов (ионов свинца) и изучения продуктов их соударений. Коллайдер построен в научно-исследовательском центре Европейского совета ядерных исследований (фр. Conseil Européen pour la Recherche Nucléaire, сокр. CERN), на границе Швейцарии и Франции, недалеко от Женевы. БАК является самой крупной экспериментальной установкой в мире. Руководитель проекта — Лин Эванс. В строительстве и исследованиях участвовали и участвуют более 10 000 учёных и инженеров из более чем 100 стран. Большим назван из-за своих размеров: длина основного кольца ускорителя составляет 26 659 м; адронным — из-за того, что он ускоряет адроны, то есть тяжёлые частицы, состоящие из кварков; коллайдером (англ. collider — сталкиватель) — из-за того, что пучки частиц ускоряются в противоположных направлениях и сталкиваются в специальных точках столкновения
Физика высоких энергий Большой адро́нный колла́йдер, сокр. БАК (англ. Large Hadron Collider, сокр. LHC) — ускоритель заряженных частиц на встречных пучках, предназначенный для разгона протонов и тяжёлых ионов (ионов свинца) и изучения продуктов их соударений. Коллайдер построен в научно-исследовательском центре Европейского совета ядерных исследований (фр. Conseil Européen pour la Recherche Nucléaire, сокр. CERN), на границе Швейцарии и Франции, недалеко от Женевы. БАК является самой крупной экспериментальной установкой в мире. Руководитель проекта — Лин Эванс. В строительстве и исследованиях участвовали и участвуют более 10 000 учёных и инженеров из более чем 100 стран. Большим назван из-за своих размеров: длина основного кольца ускорителя составляет 26 659 м; адронным — из-за того, что он ускоряет адроны, то есть тяжёлые частицы, состоящие из кварков; коллайдером (англ. collider — сталкиватель) — из-за того, что пучки частиц ускоряются в противоположных направлениях и сталкиваются в специальных точках столкновения
 Физика высоких энергий На границе Швейцарии и Франции, в туннеле длиной 27 километров, охлажденном до 271°C, 9300 сверхмощных магнитов разгоняют до скорости света и сталкивают между собой пучки элементарных частиц – протонов. Путешествие на 13,7 миллиардов лет назад, которое могло бы пролить свет на загадки Вселенной. Это – не фантастика, это – ЦЕРН, Европейская организация по ядерным исследованиям.
Физика высоких энергий На границе Швейцарии и Франции, в туннеле длиной 27 километров, охлажденном до 271°C, 9300 сверхмощных магнитов разгоняют до скорости света и сталкивают между собой пучки элементарных частиц – протонов. Путешествие на 13,7 миллиардов лет назад, которое могло бы пролить свет на загадки Вселенной. Это – не фантастика, это – ЦЕРН, Европейская организация по ядерным исследованиям.
 Физика высоких энергий
Физика высоких энергий
 Периодическая система элементов 18 (6) марта 1869 г. На заседании Русского химического общества было сделано сообщение об открытии Д.И. Менделеевым соотношения свойств с атомным весом элементов: «Элементы, расположенные по величине их атомного веса представляют явственную периодичность их свойств…» «Физические и химические свойства элементов…стоят в периодической зависимости от их атомного веса»
Периодическая система элементов 18 (6) марта 1869 г. На заседании Русского химического общества было сделано сообщение об открытии Д.И. Менделеевым соотношения свойств с атомным весом элементов: «Элементы, расположенные по величине их атомного веса представляют явственную периодичность их свойств…» «Физические и химические свойства элементов…стоят в периодической зависимости от их атомного веса»
 Физический смысл периодического закона обнаружился в 1913г., когда английский физик Г.Мозли экспериментально доказал, что не атомный вес, а порядковый номер и связанный с ним электрический заряд ядра определяют место элемента в периодической системе Периодическая система химических элементов (табли́ца Менделе́ева)
Физический смысл периодического закона обнаружился в 1913г., когда английский физик Г.Мозли экспериментально доказал, что не атомный вес, а порядковый номер и связанный с ним электрический заряд ядра определяют место элемента в периодической системе Периодическая система химических элементов (табли́ца Менделе́ева)
 Периодическая система химических элементов (табли́ца Менделе́ева) В начале XX века с открытием строения атома было установлено, что периодичность изменения свойств элементов определяется не атомным весом, а зарядом ядра, равным атомному номеру и числу электронов, распределение которых по электронным оболочкам атома элемента определяет его химические свойства. Дальнейшее развитие периодической системы связано с заполнением пустых клеток таблицы, в которые помещались всё новые и новые элементы: благородные газы, природные и искусственно полученные радиоактивные элементы. В 2010 году, с синтезом 117 элемента, седьмой период периодической системы был завершён, проблема нижней границы таблицы Менделеева остаётся одной из важнейших в современной теоретической химии
Периодическая система химических элементов (табли́ца Менделе́ева) В начале XX века с открытием строения атома было установлено, что периодичность изменения свойств элементов определяется не атомным весом, а зарядом ядра, равным атомному номеру и числу электронов, распределение которых по электронным оболочкам атома элемента определяет его химические свойства. Дальнейшее развитие периодической системы связано с заполнением пустых клеток таблицы, в которые помещались всё новые и новые элементы: благородные газы, природные и искусственно полученные радиоактивные элементы. В 2010 году, с синтезом 117 элемента, седьмой период периодической системы был завершён, проблема нижней границы таблицы Менделеева остаётся одной из важнейших в современной теоретической химии
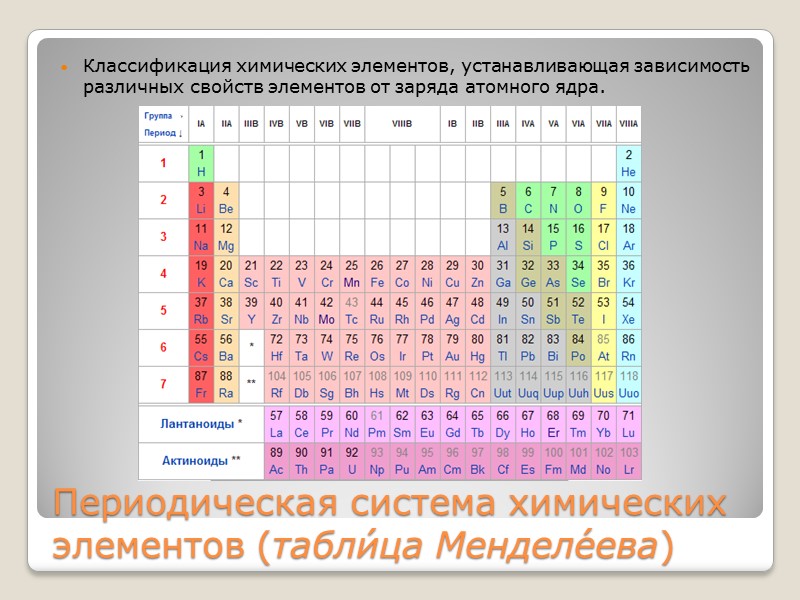
 Периодическая система химических элементов (табли́ца Менделе́ева) Классификация химических элементов, устанавливающая зависимость различных свойств элементов от заряда атомного ядра.
Периодическая система химических элементов (табли́ца Менделе́ева) Классификация химических элементов, устанавливающая зависимость различных свойств элементов от заряда атомного ядра.
 Молекулы. Химические связи Химическое соединение — это вещество, в котором атомы двух и более различных химических элементов соединены при помощи химических связей. Молекула – это наименьшая частица химического соединения, обладающая его химическими свойствами. В форме молекул могут быть не только соединения, но и простые вещества. Молекулы химического соединения, т. е. сложного вещества, многоэлементны (H2O, NH3, CO2, H2SO4), молекулы простых веществ – одноэлементны (H2, O2, N2, Cl2, S8, P4 и др.). Поэтому в приведенном выше определении молекулы речь идет о многоэлементных молекулах. Молекула – это электронейтральная наименьшая совокупность атомов, образующих структуру посредством химических связей. Шаро-стержневая модель молекулы диборана B2H6. Атомы бора показаны розовым, водорода — серым. Центральные «мостиковые» атомы одновалентного водорода образуют с соседними атомами бора трёхцентровые связи.
Молекулы. Химические связи Химическое соединение — это вещество, в котором атомы двух и более различных химических элементов соединены при помощи химических связей. Молекула – это наименьшая частица химического соединения, обладающая его химическими свойствами. В форме молекул могут быть не только соединения, но и простые вещества. Молекулы химического соединения, т. е. сложного вещества, многоэлементны (H2O, NH3, CO2, H2SO4), молекулы простых веществ – одноэлементны (H2, O2, N2, Cl2, S8, P4 и др.). Поэтому в приведенном выше определении молекулы речь идет о многоэлементных молекулах. Молекула – это электронейтральная наименьшая совокупность атомов, образующих структуру посредством химических связей. Шаро-стержневая модель молекулы диборана B2H6. Атомы бора показаны розовым, водорода — серым. Центральные «мостиковые» атомы одновалентного водорода образуют с соседними атомами бора трёхцентровые связи.
 Химические связи Химическая связь — явление взаимодействия атомов, обусловленное перекрыванием электронных облаков связывающихся частиц, которое сопровождается уменьшением полной энергии системы.
Химические связи Химическая связь — явление взаимодействия атомов, обусловленное перекрыванием электронных облаков связывающихся частиц, которое сопровождается уменьшением полной энергии системы.
 Химические связи Ионная химическая связь это связь, образовавшаяся за счет электростатического притяжения катионов к анионам
Химические связи Ионная химическая связь это связь, образовавшаяся за счет электростатического притяжения катионов к анионам
 Химические связи Металлическая связь связь в металлах и сплавах, которую выполняют относительно свободные электроны между ионами металлов в металлической кристаллической решетке
Химические связи Металлическая связь связь в металлах и сплавах, которую выполняют относительно свободные электроны между ионами металлов в металлической кристаллической решетке
 Химические связи Водородная связь Химическая связь между положительно поляризованными атомами водорода одной молекулы (или ее части) и отрицательно поляризованными атомами сильно электроотрицательных элементов, имеющих неподеленные электронные пары (F, О, N и реже С1 и S) другой молекулы (или ее части) O H…..O H…..O H…. H H H
Химические связи Водородная связь Химическая связь между положительно поляризованными атомами водорода одной молекулы (или ее части) и отрицательно поляризованными атомами сильно электроотрицательных элементов, имеющих неподеленные электронные пары (F, О, N и реже С1 и S) другой молекулы (или ее части) O H…..O H…..O H…. H H H
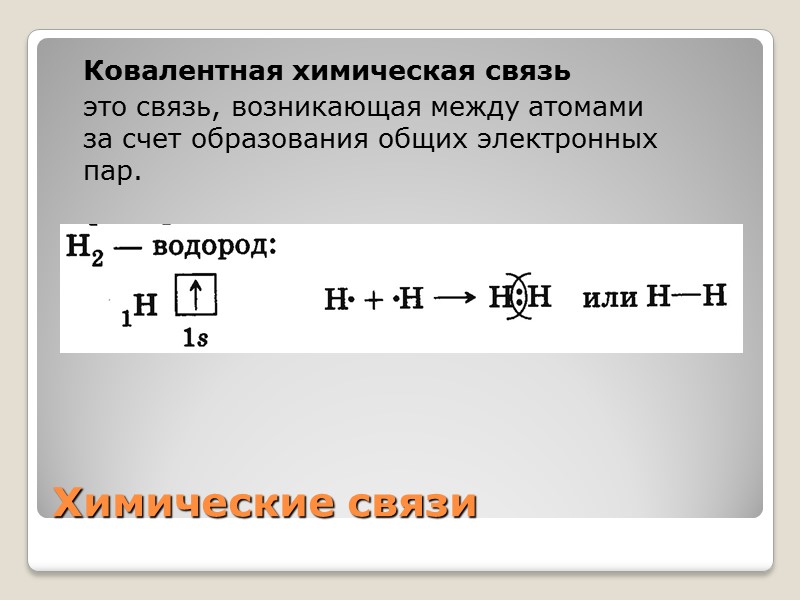
 Химические связи Ковалентная химическая связь это связь, возникающая между атомами за счет образования общих электронных пар.
Химические связи Ковалентная химическая связь это связь, возникающая между атомами за счет образования общих электронных пар.

