Презентация по КСЕ 5.ppt
- Количество слайдов: 26

5. Концепции классической химии и биологии. 5. 1. Учение о составе вещества. 5. 2. Концепция структуры веществ. 5. 3. Периодический закон Менделеева. 5. 4. Натуралистический этап развития биологии. 5. 5. Теория эволюции в биологии. 5. 6. Молекулярно - генетический этап развития биологии. КСЕ

5. 1. Учение о составе вещества Химия – наука о превращениях веществ, с изменением их состава или строения. Основная цель – это получение веществ с заданными свойствами. Д. И. Менделеев: «Химия в значительной мере сама создает свой объект изучения» . Роберт Бойль, английский физик и химик (1627 – 1691 г. ) - анализ состава тел. Химический элемент – совокупность атомов с одинаковым зарядом ядра. Молекула – микрочастица, образованная из атомов, и способная к самостоятельному существованию. КСЕ

Основные законы: 1. Закон Ломоносова: массы начальных и конечных веществ, участвующих в реакции, одинаковы. 2. Закон Пруста: любое чистое вещество имеет всегда один и тот же состав. 3. Законы Дальтона: а) количества вещества элементов в химических соединениях относятся между собой, как целые числа (АВ, АВ 2, …) б) любое химическое соединение имеет неизменное соотношение компонентов. 4. Закон Авогадро: при одинаковых давлении и температуре в одном и том же объеме любого газа содержится одинаковое количество молекул. КСЕ

5. Закон сохранения энергии: количество тепловой энергии, принесенной в зону взаимодействия веществ, равно количеству энергии, вынесенной веществами из этой зоны. Экзотермические – реакции, идущие с выделением тепла; Эндотермические – реакции, идущие с поглощением тепла. Qвнеш - теплота, введенная в процесс извне, Qэкзотерм - теплота, выделившаяся при экзотермической реакции, Qпотерь - потери теплоты в окружающую среду. КСЕ

5. 2. Концепция структуры веществ Структура – это устойчивая пространственная и энергетическая упорядоченность молекулы. Йенс Берцелиус, шведский химик (1779 – 1848 г. ): • точное измерение атомных весов элементов; • символика химических элементов, формулы химических соединений и уравнений; • исследования в области электрохимии; • введение понятия «органическая химия» - наука, изучающая соединения углерода с другими элементами. КСЕ

Фридрих Кекуле, немецкий химик (1829 – 1896 г. ): • • сформулировал теорию валентности ввел изображение молекул в виде наглядных формул: Кекуле предложил создавать химические соединения на основе их структурных формул. Но формульный схематизм Кекуле не учитывал реакционную способность реагентов. КСЕ
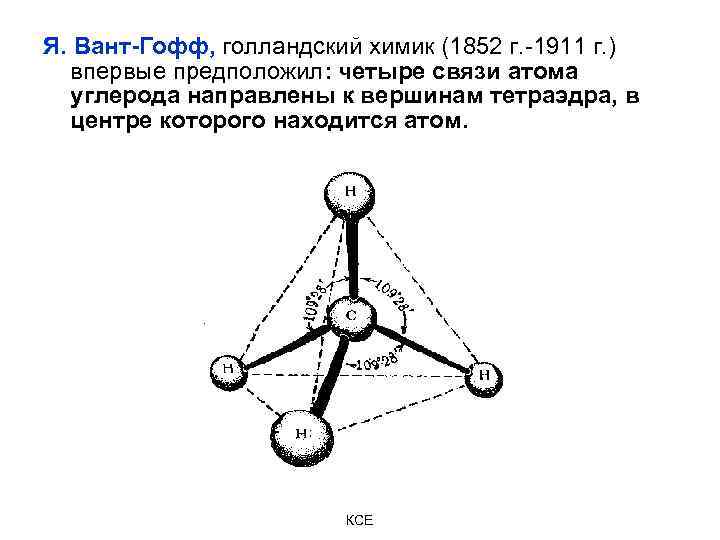
Я. Вант-Гофф, голландский химик (1852 г. -1911 г. ) впервые предположил: четыре связи атома углерода направлены к вершинам тетраэдра, в центре которого находится атом. КСЕ
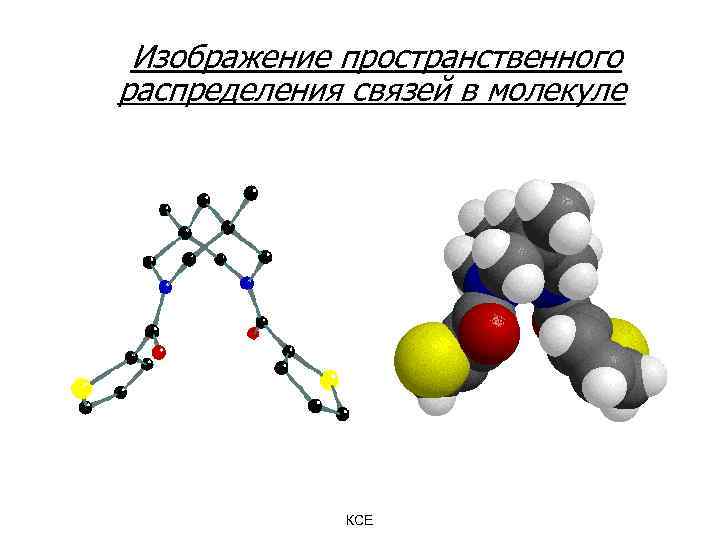
Изображение пространственного распределения связей в молекуле КСЕ

Теория А. М. Бутлерова (1861 г. ): 1. Химические и физические свойства соединений зависят как от природы и числа входящих в их состав атомов, так и от структуры и конфигурации молекул. 2. В молекулах существует взаимное влияние как связанных, так и непосредственно не связанных друг с другом атомов. 3. Для каждой формулы можно вывести определенное число теоретически возможных структур (изомеров). КСЕ

Изомеры – химические соединения, одинаковые по молярной массе и составу, но различающиеся расположением атомов в пространстве. 1. Структурные изомеры - молекулы, отличающиеся порядком связей атомов, т. е. химическим строением. КСЕ
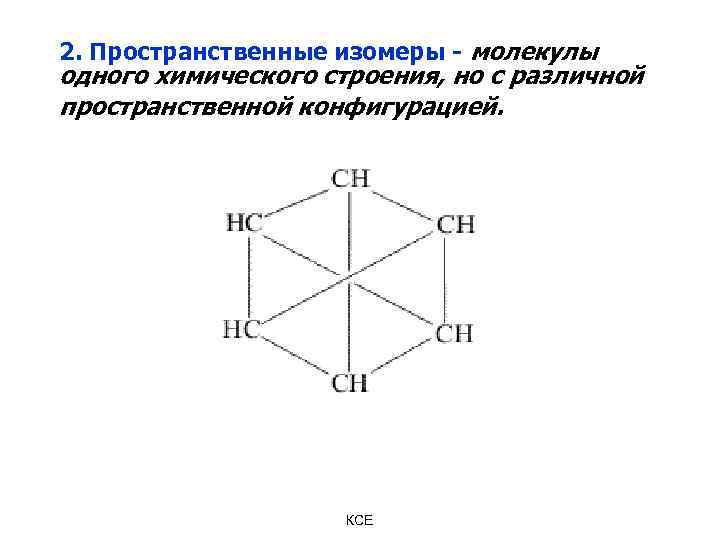
2. Пространственные изомеры - молекулы одного химического строения, но с различной пространственной конфигурацией. КСЕ
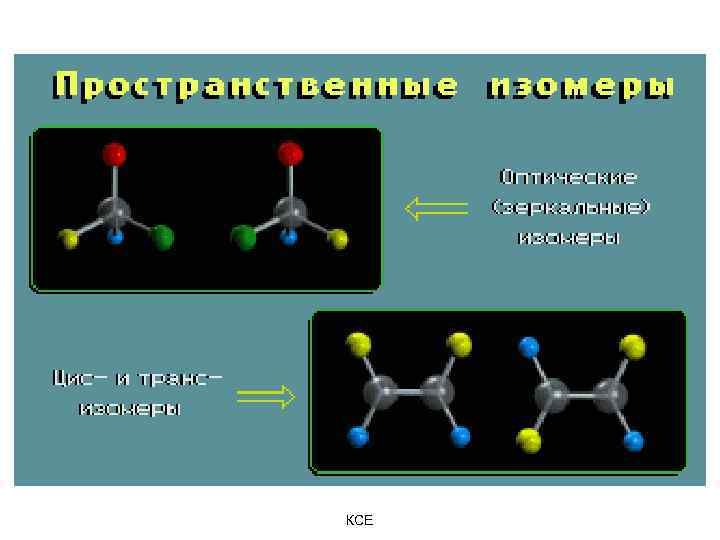
КСЕ

5. 3. Периодический закон Менделеева. • Формулировка Менделеева (1869 г. ): Свойства простых тел, а также формы и свойства соединений находятся в периодической зависимости от атомных весов элементов. (67 элементов). • Современная формулировка: строение и свойства химических элементов находятся в периодической зависимости от зарядов атомных ядер элементов и определяются периодически повторяющимися электронными конфигурациями их атомов. Известно 117 элементов, в природе обнаружено 89. КСЕ
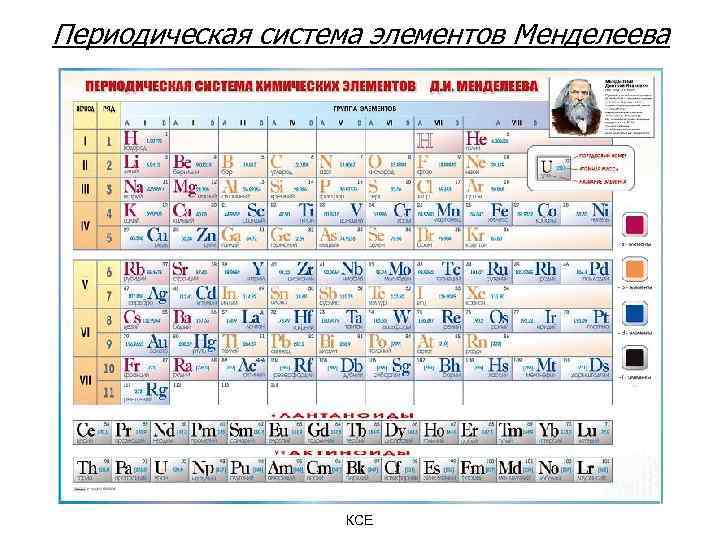
Периодическая система элементов Менделеева КСЕ
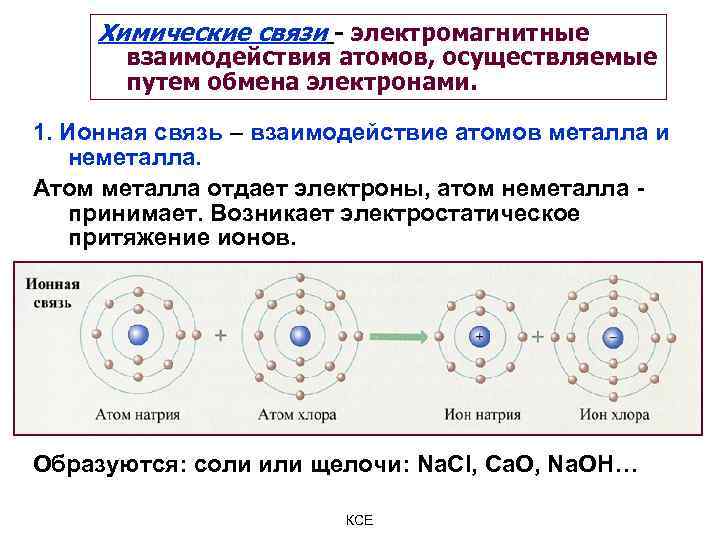
Химические связи - электромагнитные взаимодействия атомов, осуществляемые путем обмена электронами. 1. Ионная связь – взаимодействие атомов металла и неметалла. Атом металла отдает электроны, атом неметалла принимает. Возникает электростатическое притяжение ионов. Образуются: соли или щелочи: Na. Cl, Ca. O, Na. OH… КСЕ
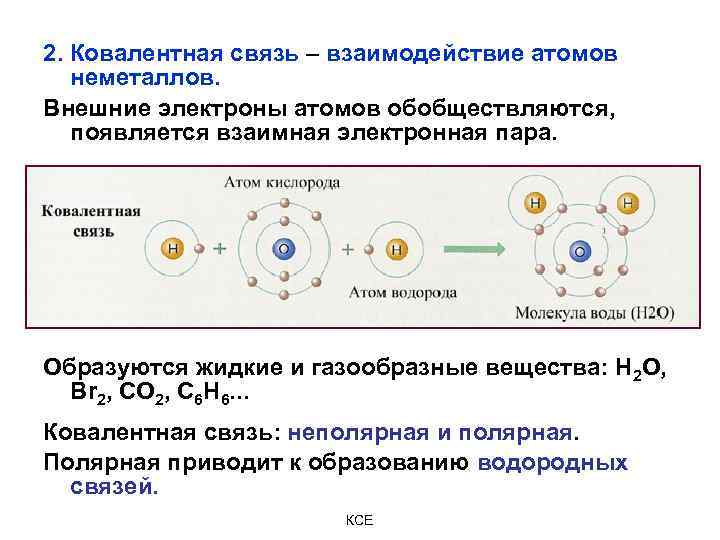
2. Ковалентная связь – взаимодействие атомов неметаллов. Внешние электроны атомов обобществляются, появляется взаимная электронная пара. Образуются жидкие и газообразные вещества: Н 2 О, Br 2, CO 2, C 6 H 6. . . Ковалентная связь: неполярная и полярная. Полярная приводит к образованию водородных связей. КСЕ

3. Металлическая связь. Каждый атом отдает один или два внешних электрона. Образуется атомная решетка, внутри которой находятся свободные электроны. КСЕ

Основные направления современной структурной химии - создание кристаллов с максимальным приближением к идеальной решетке для получения материалов с высокими техническими показателями: максимальной прочностью, термической стойкостью и др. ; - создание кристаллов с запрограммированными дефектами решетки для производства материалов с заданными электрическими, магнитными и другими свойствами. КСЕ
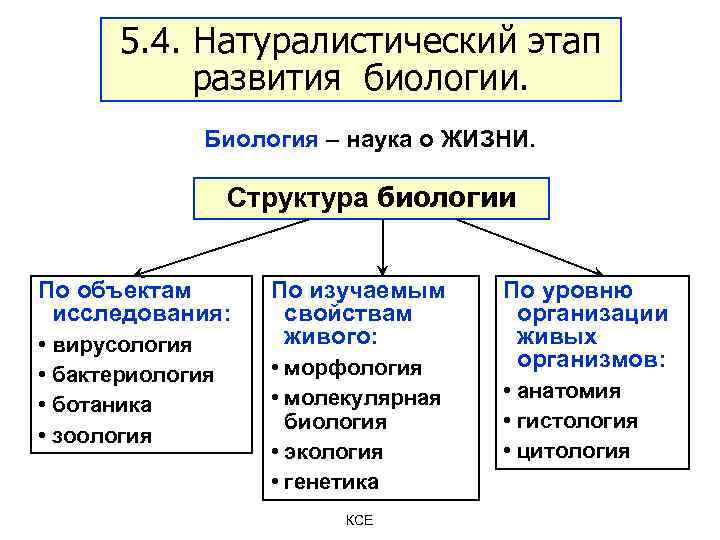
5. 4. Натуралистический этап развития биологии. Биология – наука о ЖИЗНИ. Структура биологии По объектам исследования: • вирусология • бактериология • ботаника • зоология По изучаемым свойствам живого: • морфология • молекулярная биология • экология • генетика КСЕ По уровню организации живых организмов: • анатомия • гистология • цитология

Классификация Линнея Первые попытки классификации – Аристотель. Карл Линней, шведский биолог-натуралист (1707 – 1778 г. ) - основоположник общепринятой системы классификации. В систему классификации входят: 1. 2. 3. 4. 5. 6. 7. Царство (5 царств) Тип (отдел - у растений) Класс (4 класса) Отряд (порядок – у растений) Семейство Род Вид (особи, способные к скрещиванию между собой). КСЕ

5. 5. Теория эволюции в биологии. Жан Ламарк, французский биолог (1744 – 1829 г. ) – основоположник эволюционной теории. Две основные причины эволюции: 1. Стремление живой природы к совершенствованию своей организации, заложенное Творцом. 2. Изменение видов под влиянием внешней среды. Эти изменения передаются по наследству. КСЕ

Чарльз Дарвин, английский ученый, (1809 -1882 г. ) – создатель теории эволюции «Происхождение видов путем естественного отбора» (1859 г. ) КСЕ

Теория Дарвина 1. В пределах каждого вида существует индивидуальная наследственная изменчивость: - определенная изменчивость: способность особей одинаковым образом реагировать на изменения внешних условий; - неопределенная изменчивость (мутация), не связанная с изменениям внешних условий. 2. Живые организмы размножаются в геометрической прогрессии. 3. Борьба за существование: борьба особи за жизнь и борьба за успех в размножении. 4. Естественный отбор: выживают и дают потомство наиболее приспособленные особи. 5. Естественный отбор особей в разных условиях ведет к расхождению их признаков и к видообразованию. КСЕ

5. 6. Молекулярно - генетический этап развития биологии. Иоганн Мендель, австрийский монах, естествоиспытатель, (1822 – 1884 г. ) - основатель генетики. «Опыты по гибридизации растений» , 1866 г: … наследственность передается дискретными частицами - генами. КСЕ

Законы Менделя 1. Закон единообразия первого поколения: при скрещивании двух особей, различающихся по одной паре альтернативных признаков, первое поколение единообразно, в нем проявляется только один признак. Этот признак называется доминантным. Второй признак называемый рецессивным, в первом поколении подавляется. 2. Закон расщепления: при скрещивании особей первого поколения второе поколение дает расщепление по анализируемому признаку в отношении 3 : 1. 3. Закон независимого комбинирования признаков: при скрещивании особей, отличающихся по двум и более парам альтернативных признаков, гены и соответствующие им признаки наследуются независимо друг от друга и комбинируются во всех возможных сочетаниях. КСЕ
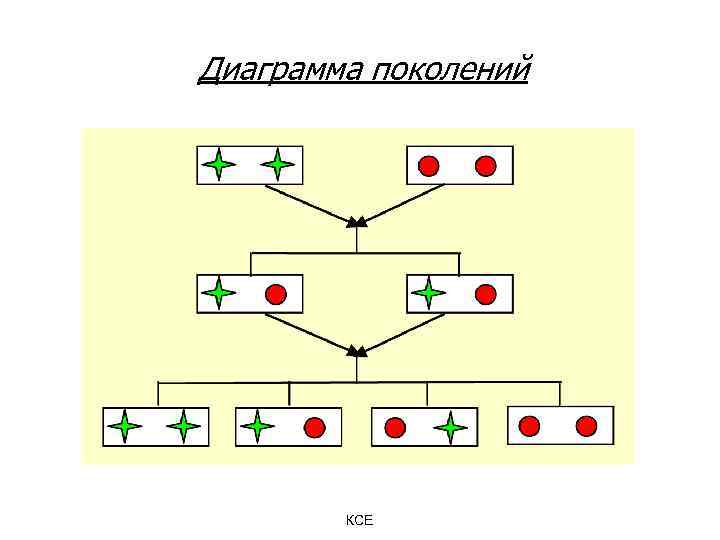
Диаграмма поколений КСЕ
Презентация по КСЕ 5.ppt