ММТП часть 5-2. Протоонкогены и СТ.ppt
- Количество слайдов: 153

5. 2. 1. Ассоциированные с мембраной белки (на примере RAS и SRC)

Фосфорилирование рецептора приводит к двум последствиям: • • • 1. Фосфорилирование усиливает киназную активность рецептора по типу положительной обратной связи. 2. Фосфорилирование тирозиновых остатков в цитоплазматических доменах обеспечивает прохождение сигнала к следующему этапу сигнальной трансдукции. Различают 3 типа белков, с которыми может взаимодействовать активированный рецептор: - Белок может быть мишенью для рецептора, если он сам не фосфорилирован. Мишень может быть также адаптерной молекулой, т. е. сама не обладать каталитической активностью (например, Grb-2) или быть ферментом, который активируется связыванием с рецептором (например, PI-3 киназа). - Белок является субстратом для фермента, который его фосфорилирует. Если субстрат сам является ферментом, то он активируется фосфорилированием (например, c-src, PLCγ). Иногда субстрат – это киназа, тогда сигнальная трансдукции продолжается каскадом киназ. - Некоторые субстраты могут быть концевыми мишенями, как в случае с цитоскелетными белками, которые фосфорилируются с изменением их биохимических свойств, что сопровождается появлением новых клеточных структур. Этот механизм работает, например, в митозе, когда появляется веретено для разделения хромосом.

Семейство Src-киназ • Прототипом семейства Src-киназ является белок c-Src (pp 60 c-src), впервые открытый как онкоген. Однако считается, что оригинальным белком этого семейства был его вирусный аналог, открытый Раусом в ранние 1900 -ые годы. Раус описал трансформирующий фактор, присутствующий в тканях саркомы цыплят, который индуцировал опухоль у здоровых цыплят после инъекции тканевого гомогената. Этот фактор позднее стал известен как вирус саркомы Рауса, содержащий вирусный онкоген Scr. Клеточный аналог этого онкогена или протоонкоген впервые был охарактеризован Майклом Бишопом и Гарольдом Вармусом, за открытие которого в 1989 г. они получили Нобелевскую премию.
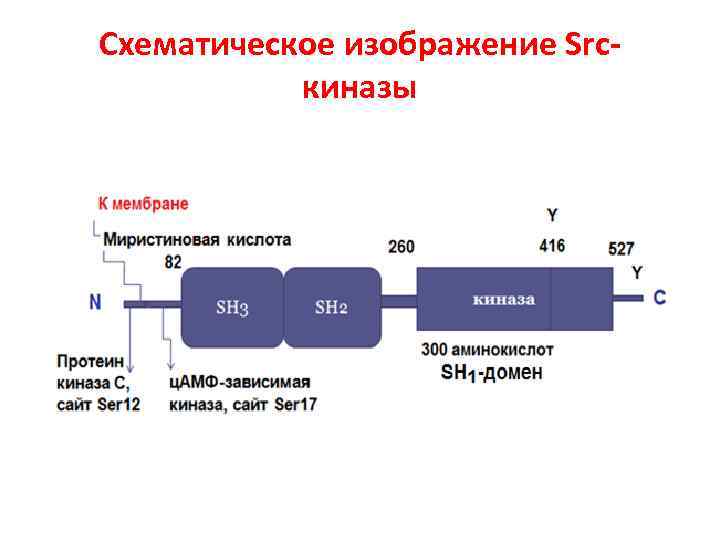
Схематическое изображение Srcкиназы
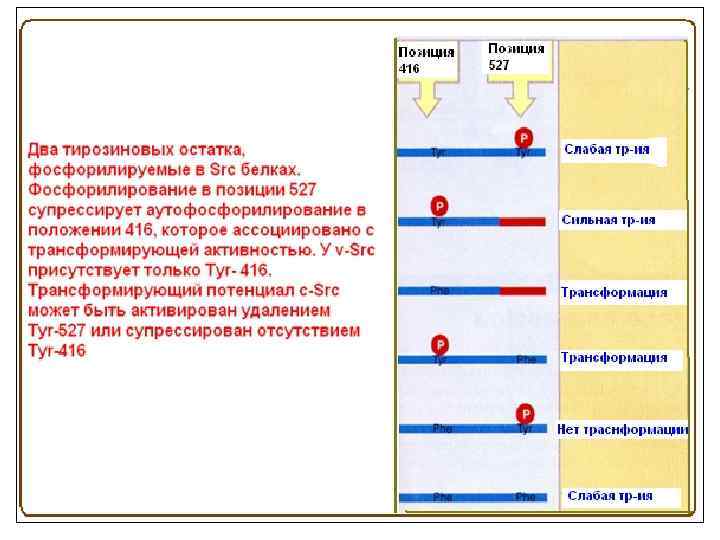
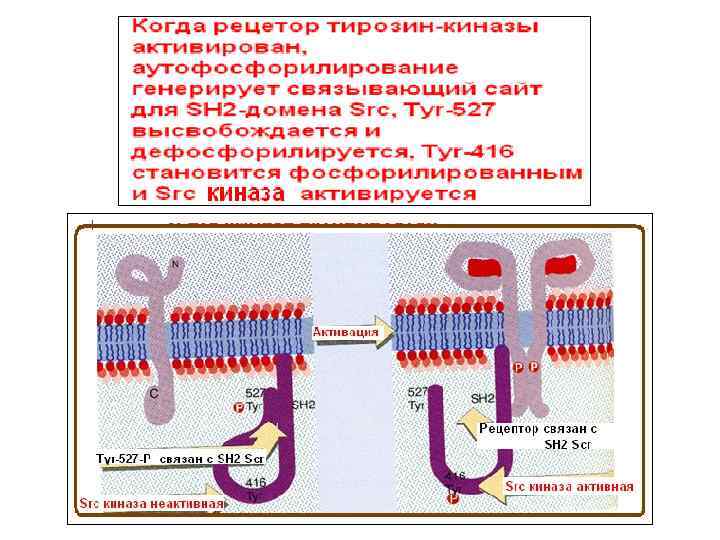
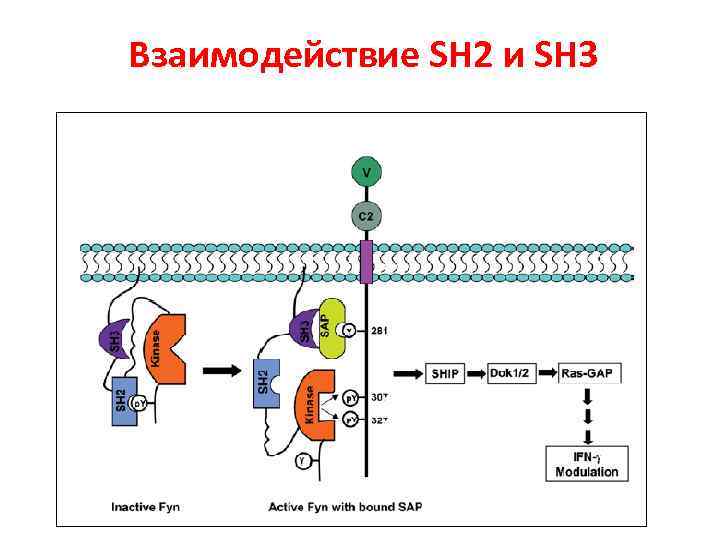
Взаимодействие SH 2 и SH 3
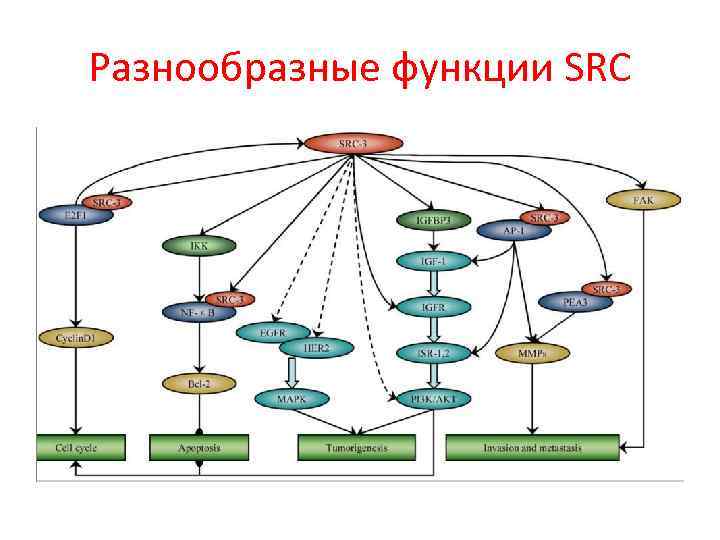
Разнообразные функции SRC

G-белки в сигнальной трансдукции

Семейство белков RAS • • Суперсемейство RAS состоит из нескольких семейств белков: RAS, RHO, RAB, ARF, RAC и RAN. Наиболее изученным из низ являются белки RAS. Геном млекопитающих содержит 3 гена RAS, кодирующих небольшие ГТФ-азные белки молекулярной массой 21 k. Da, обозначаемые как H-RAS (Harvey-RAS), N-RAS (neuroblastoma-RAS) и K-RAS (Kristen-RAS), последний имеет две изоформы K-RAS 4 A и K-RAS 4 B, образуемые через альтернативный сплайсинг. KRAS 4 A слабо экспрессируется в клетках человека, в отличие от KRAS 4 B, который является доминантной формой. Кроме того, в геноме млекопитающих было идентифицировано более чем 150 RAS-подобных гена. Белки этого семейства также регулируют многие физиологические процессы, пролиферацию, дифференцировку и выживание клетки.
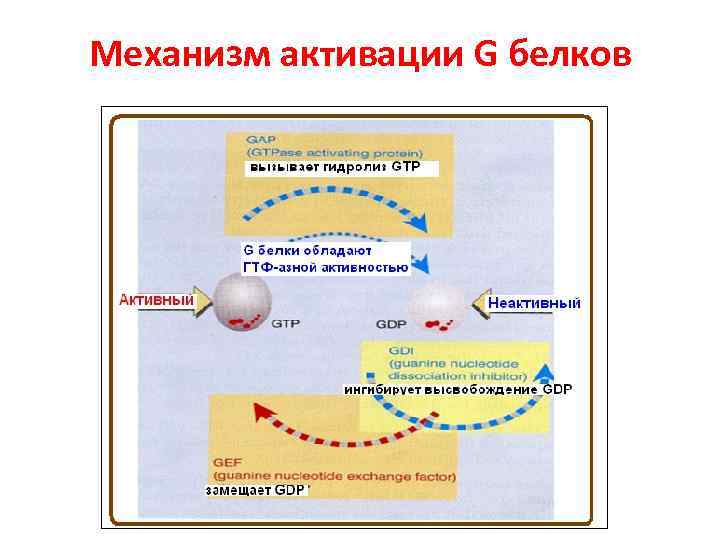
Механизм активации G белков
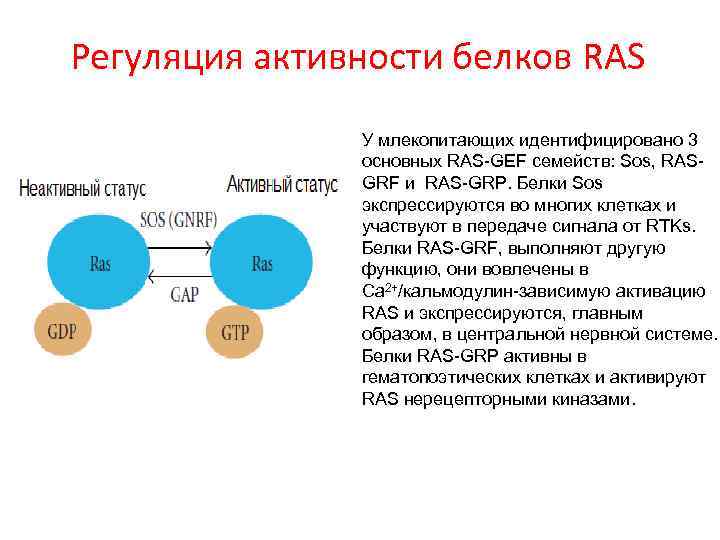
Регуляция активности белков RAS У млекопитающих идентифицировано 3 основных RAS-GEF семейств: Sos, RASGRF и RAS-GRP. Белки Sos экспрессируются во многих клетках и участвуют в передаче сигнала от RTKs. Белки RAS-GRF, выполняют другую функцию, они вовлечены в Са 2+/кальмодулин-зависимую активацию RAS и экспрессируются, главным образом, в центральной нервной системе. Белки RAS-GRP активны в гематопоэтических клетках и активируют RAS нерецепторными киназами.
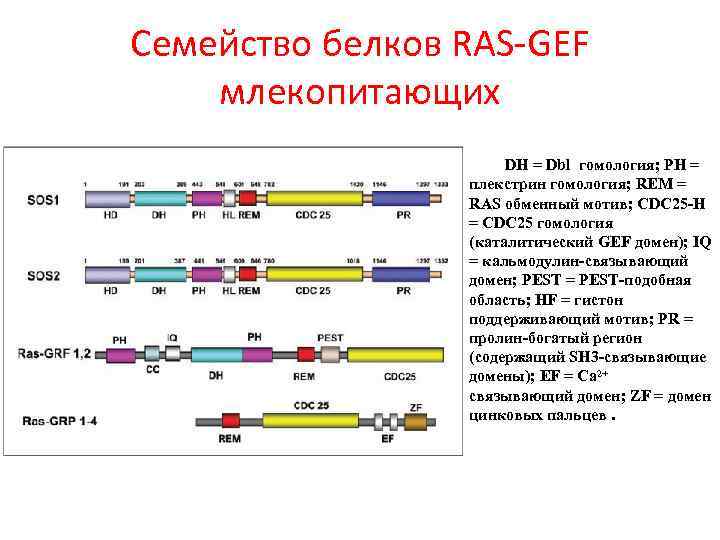
Семейство белков RAS-GEF млекопитающих DH = Dbl гомология; PH = плекстрин гомология; REM = RAS обменный мотив; CDC 25 -H = CDC 25 гомология (каталитический GEF домен); IQ = кальмодулин-связывающий домен; PEST = PEST-подобная область; HF = гистон поддерживающий мотив; PR = пролин-богатый регион (содержащий SH 3 -связывающие домены); EF = Ca 2+ связывающий домен; ZF = домен цинковых пальцев.
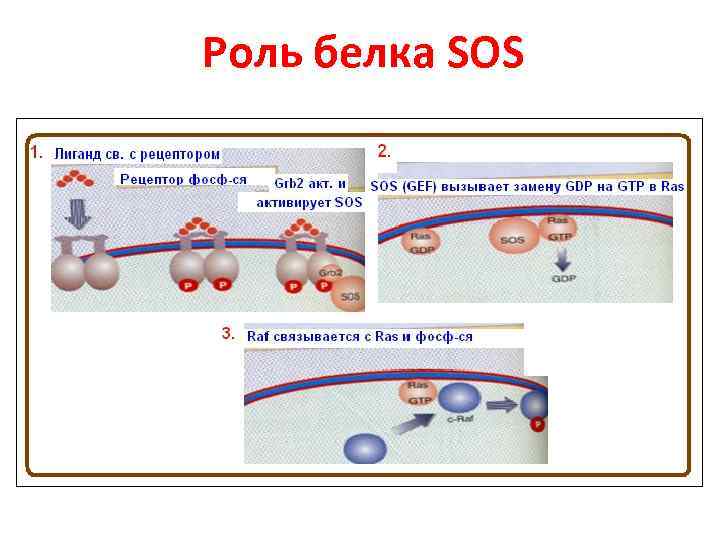
Роль белка SOS
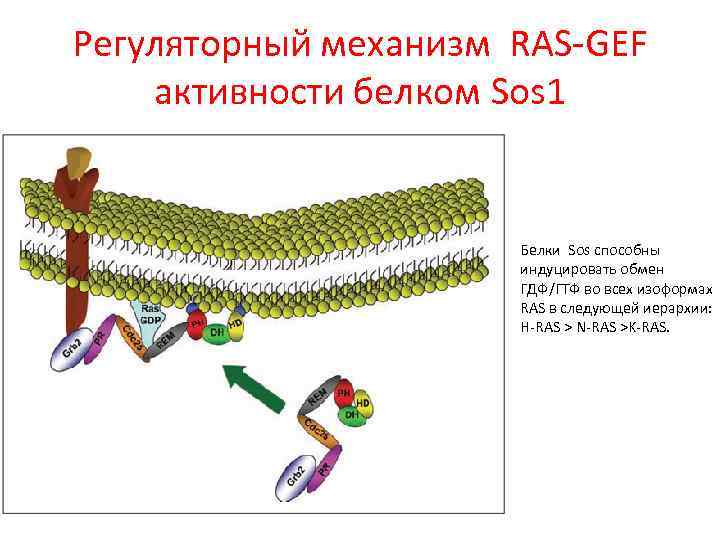
Регуляторный механизм RAS-GEF активности белком Sos 1 Белки Sos способны индуцировать обмен ГДФ/ГТФ во всех изоформах RAS в следующей иерархии: H-RAS > N-RAS >K-RAS.
Активация Ras Пролиферация Выживаемость Дифференцировка
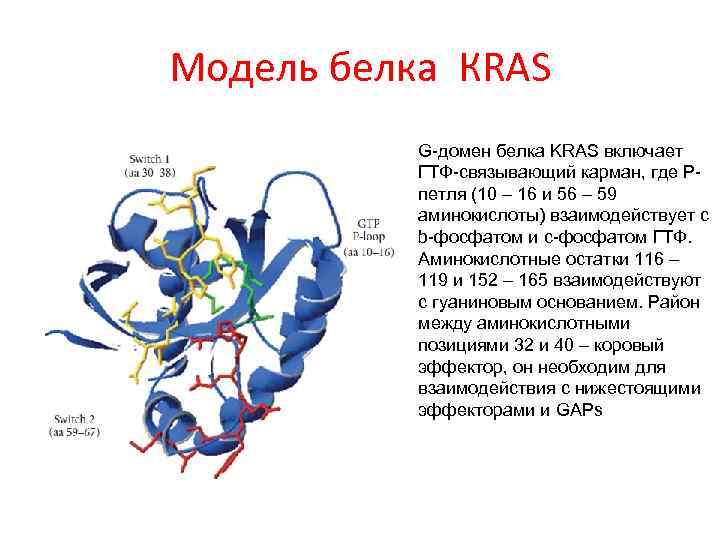
Модель белка КRAS G-домен белка KRAS включает ГТФ-связывающий карман, где Рпетля (10 – 16 и 56 – 59 аминокислоты) взаимодействует с b-фосфатом и c-фосфатом ГТФ. Аминокислотные остатки 116 – 119 и 152 – 165 взаимодействуют с гуаниновым основанием. Район между аминокислотными позициями 32 и 40 – коровый эффектор, он необходим для взаимодействия с нижестоящими эффекторами и GAPs
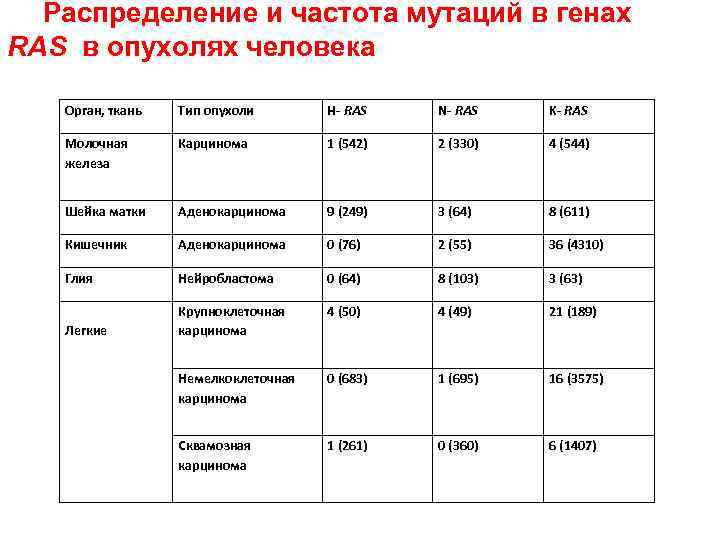
Распределение и частота мутаций в генах RAS в опухолях человека Орган, ткань Тип опухоли H- RAS N- RAS K- RAS Молочная железа Карцинома 1 (542) 2 (330) 4 (544) Шейка матки Аденокарцинома 9 (249) 3 (64) 8 (611) Кишечник Аденокарцинома 0 (76) 2 (55) 36 (4310) Глия Нейробластома 0 (64) 8 (103) 3 (63) 4 (50) 4 (49) 21 (189) Легкие Крупноклеточная карцинома Немелкоклеточная карцинома 0 (683) 1 (695) 16 (3575) Сквамозная карцинома 1 (261) 0 (360) 6 (1407)
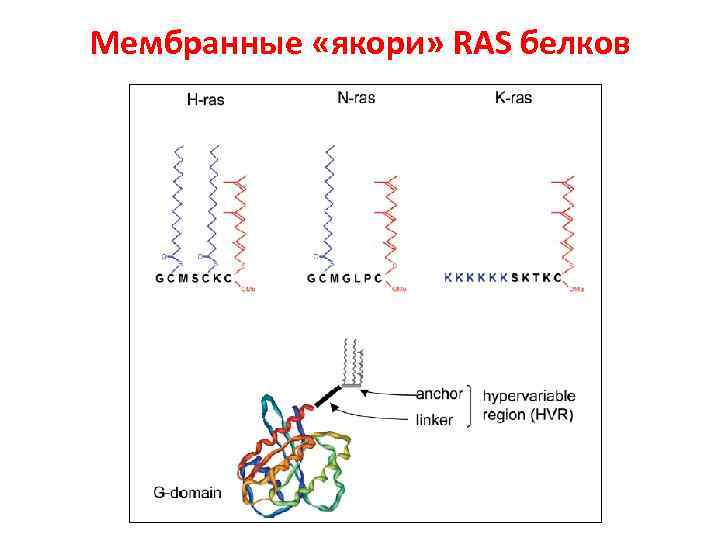
Мембранные «якори» RAS белков
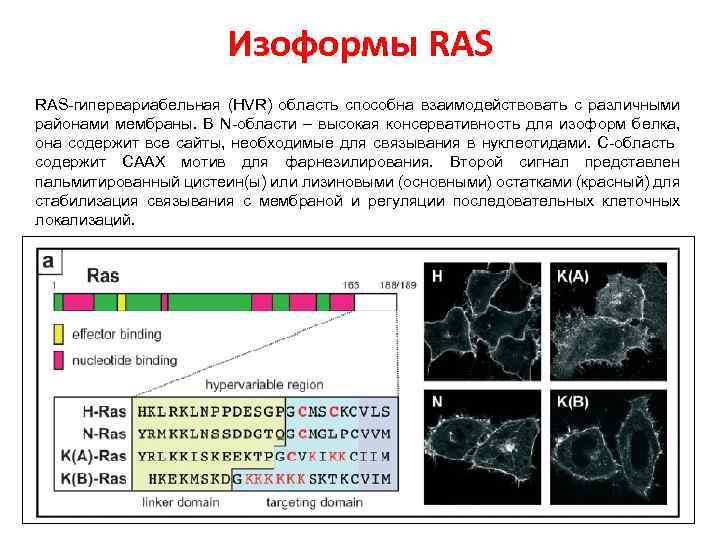
Изоформы RAS-гипервариабельная (HVR) область способна взаимодействовать с различными районами мембраны. В N-области – высокая консервативность для изоформ белка, она содержит все сайты, необходимые для связывания в нуклеотидами. C-область содержит СААХ мотив для фарнезилирования. Второй сигнал представлен пальмитированный цистеин(ы) или лизиновыми (основными) остатками (красный) для стабилизация связывания с мембраной и регуляции последовательных клеточных локализаций.
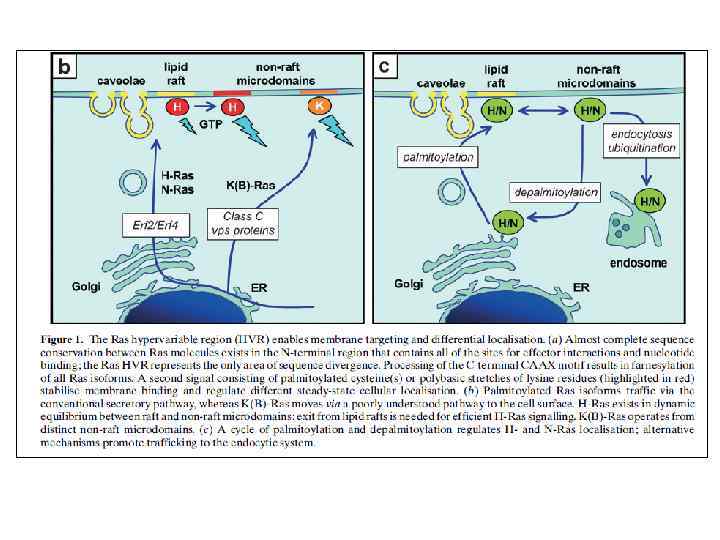
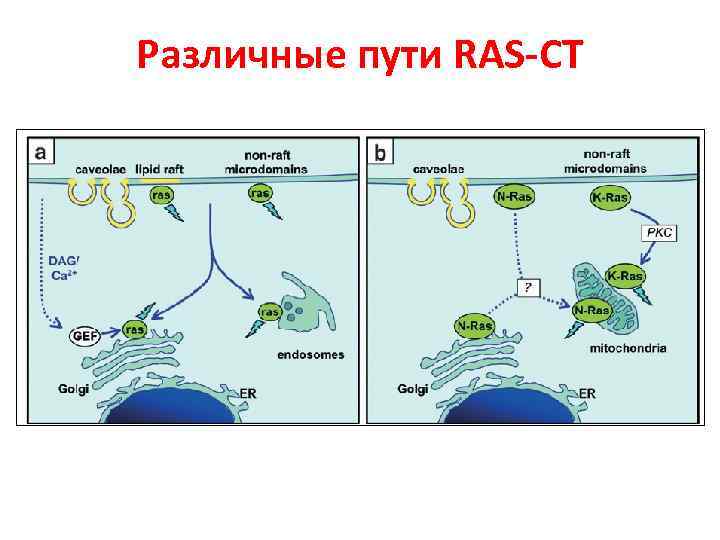
Различные пути RAS-СТ

Регуляция RAS
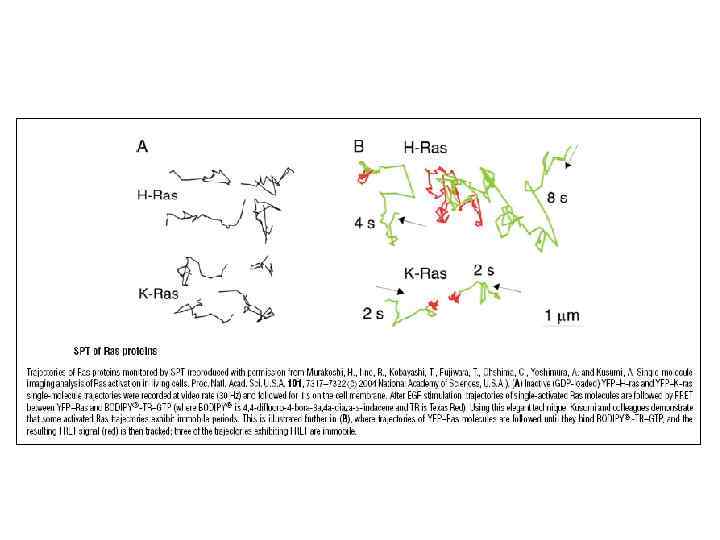
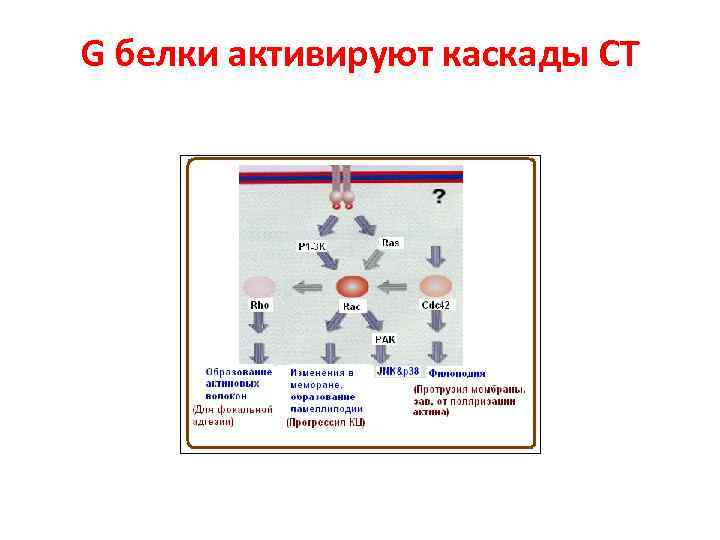
G белки активируют каскады СТ

5. 2. 2. Цитозольные белки (RAF и MAP) Цитозольные белки принимают сигнал от вышестоящих мембраноассоциированных белков, от рецепторов или адаптеров.
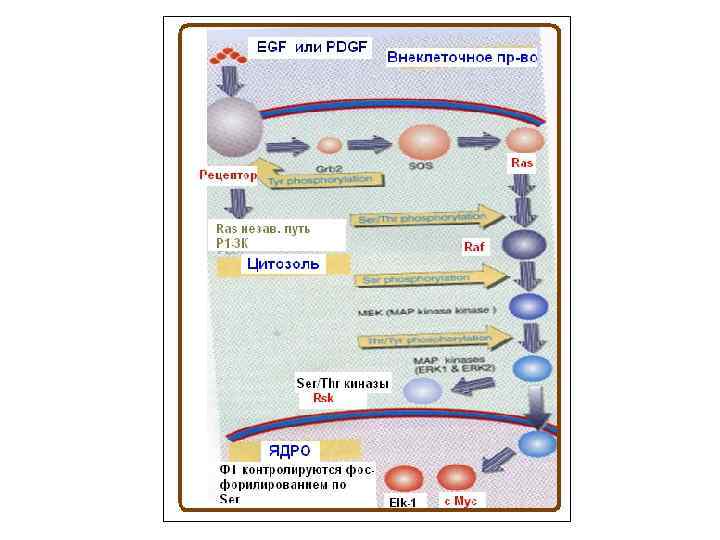
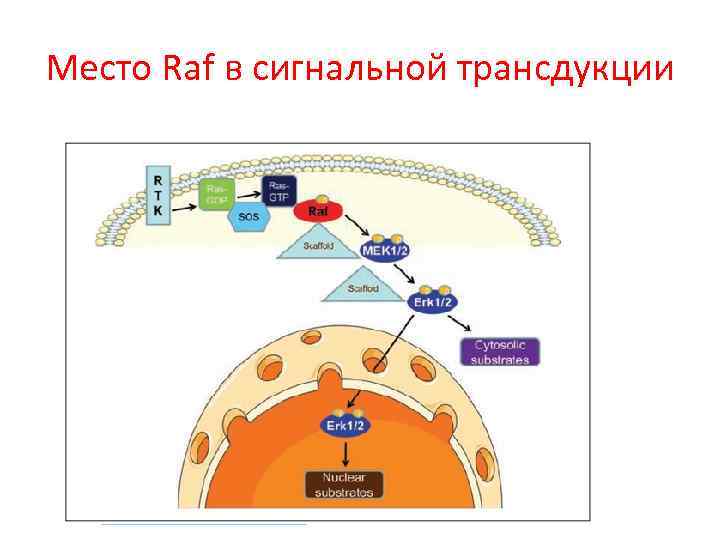
Место Raf в сигнальной трансдукции
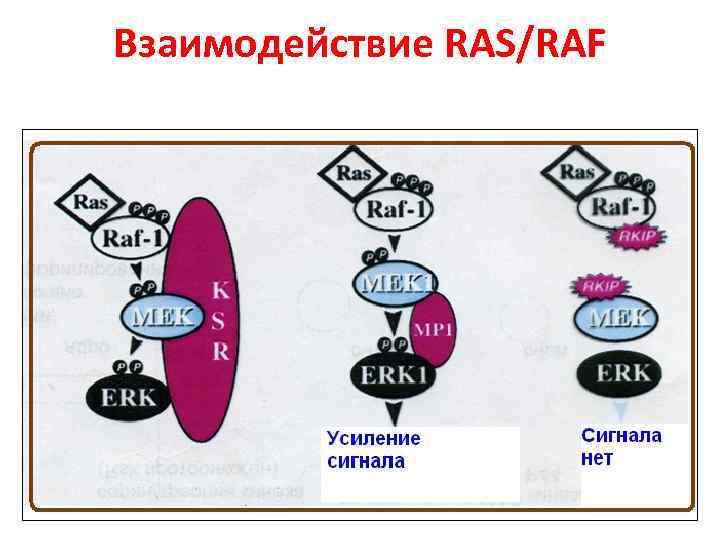
Взаимодействие RAS/RAF

Семейство белков Raf • Белки Raf были идентифицированы как прямые активаторы белков MEK и эффекторы Ras. • Таким образом, стало ясно, что Raf являются основным связывающим звеном между Ras- и MEK-ERK-сигнальными участками. Интересно, что у дрожжей нет Raf-киназы, а филогенетически древняя изоформа этого белка B-Raf появилась у позвоночных. У млекопитающих выявлено 3 изоформы Raf: Raf-1, B-Raf и A-Raf, которые имеют общую консервативную область (CR), но проявляют разные свойства. В свою очередь, CR область состоит из 3 -х участков: CR 1, CR 2, CR 3.
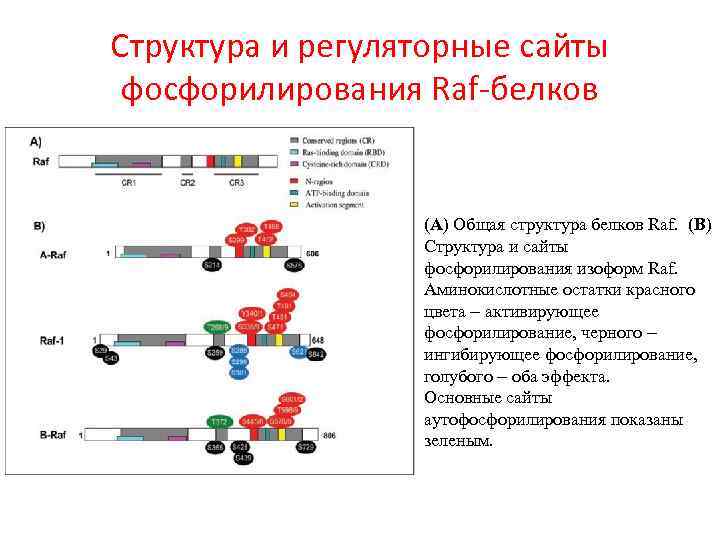
Структура и регуляторные сайты фосфорилирования Raf-белков (A) Общая структура белков Raf. (B) Структура и сайты фосфорилирования изоформ Raf. Аминокислотные остатки красного цвета – активирующее фосфорилирование, черного – ингибирующее фосфорилирование, голубого – оба эффекта. Основные сайты аутофосфорилирования показаны зеленым.
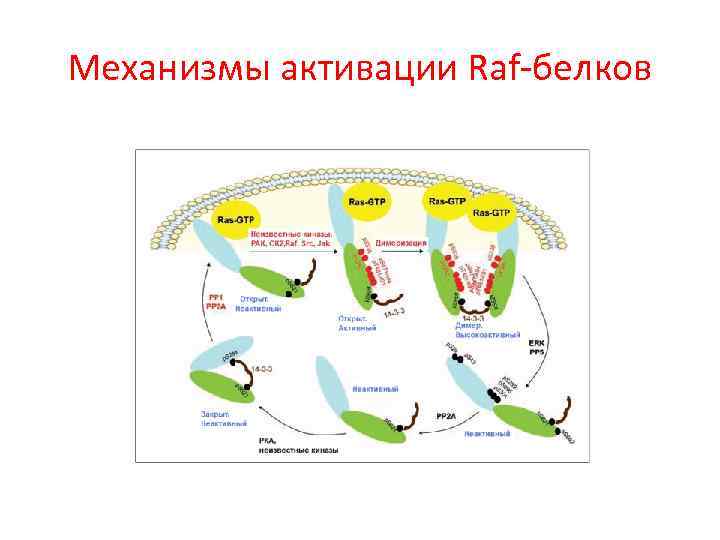
Механизмы активации Raf-белков
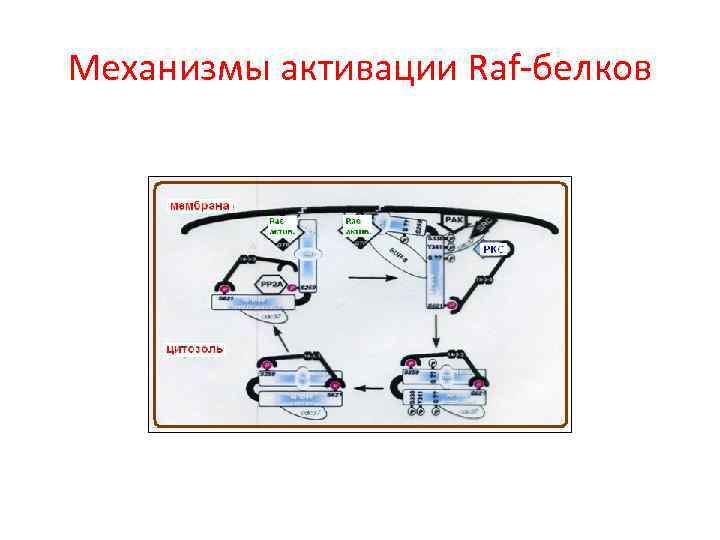
Механизмы активации Raf-белков
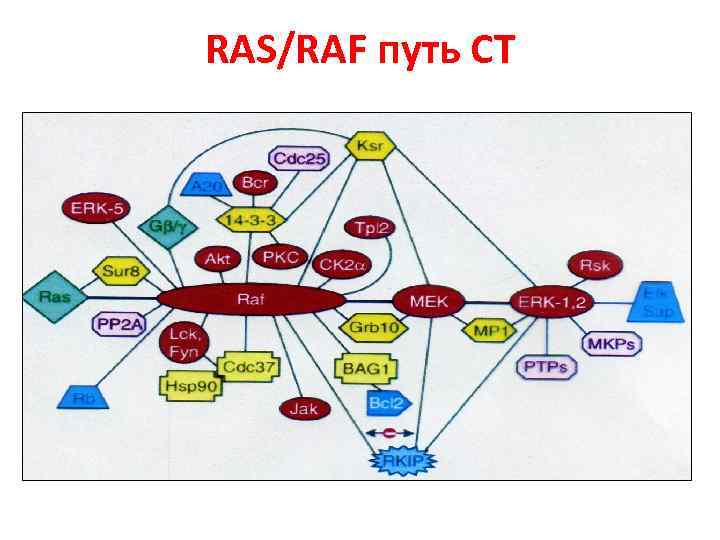
RAS/RAF путь СТ
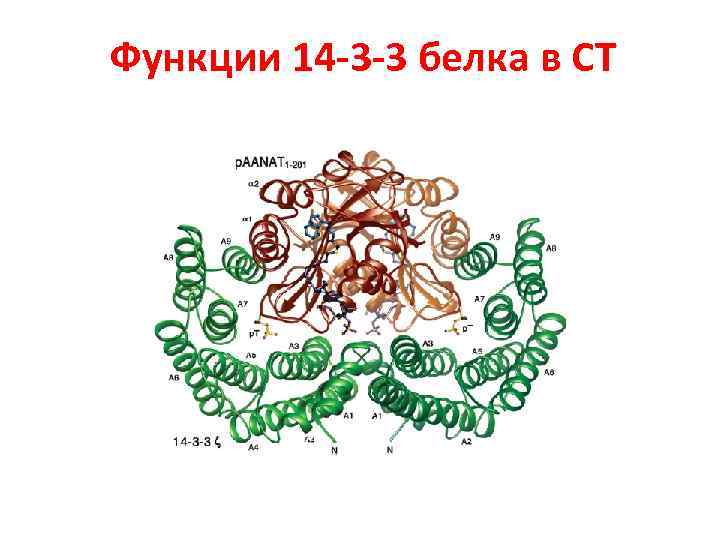
Функции 14 -3 -3 белка в СТ
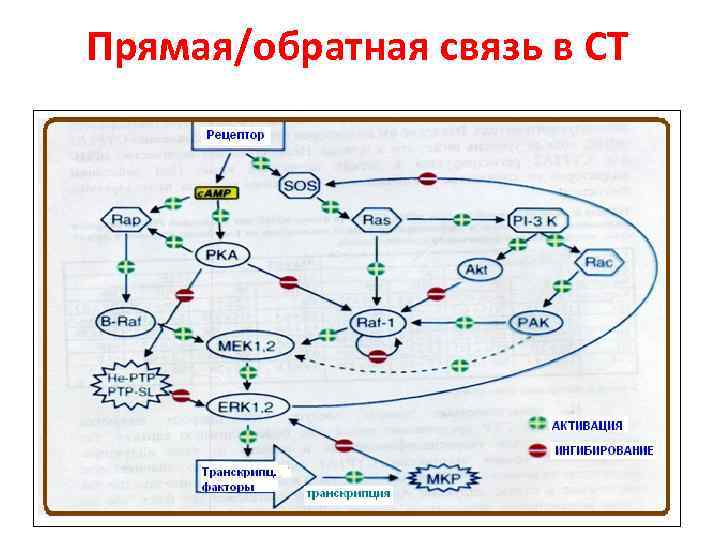
Прямая/обратная связь в СТ

BRAF inhibitors: From the laboratory to clinical trials BRAF M. A. Rahman, A. Salajegheh, R. A. Smith and A. K. -Y. Lam Critical Reviews in Oncology/Hematology DOI: 10. 1016/j. critrevonc. 2013. 12. 008 Copyright © Elsevier Ireland Ltd Terms and Conditions
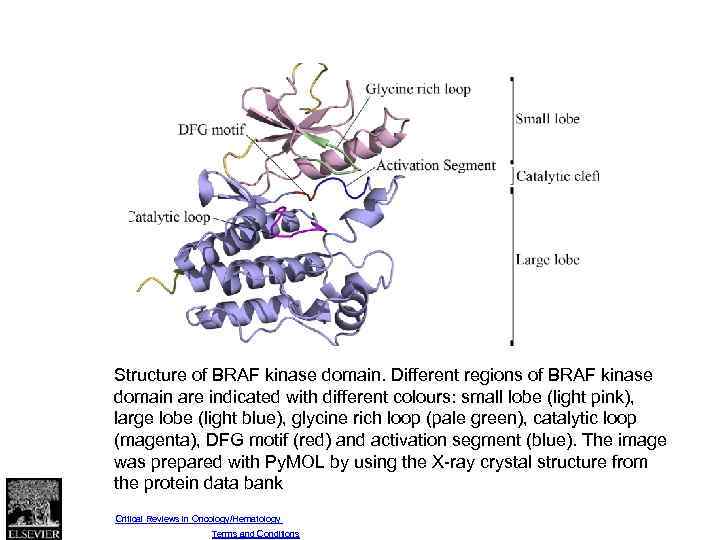
Fig. 1 Structure of BRAF kinase domain. Different regions of BRAF kinase domain are indicated with different colours: small lobe (light pink), large lobe (light blue), glycine rich loop (pale green), catalytic loop (magenta), DFG motif (red) and activation segment (blue). The image was prepared with Py. MOL by using the X-ray crystal structure from the protein data bank Source: Critical Reviews in Oncology/Hematology (DOI: 10. 1016/j. critrevonc. 2013. 12. 008 ) Copyright © Elsevier Ireland Ltd Terms and Conditions
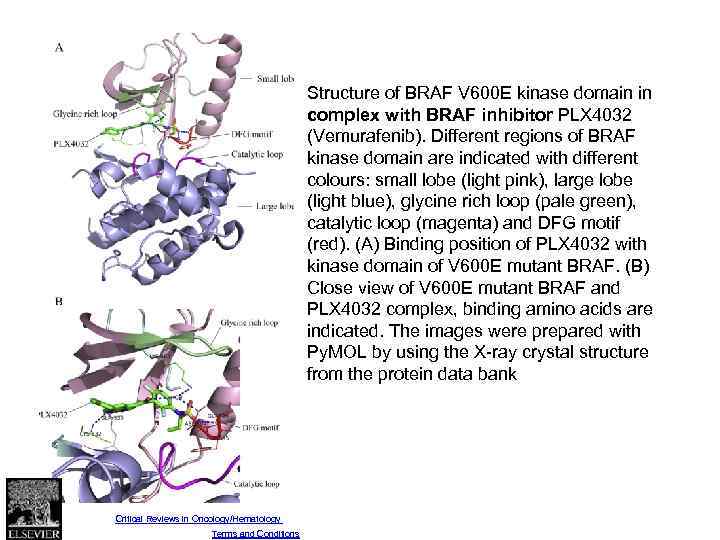
Fig. 2 Structure of BRAF V 600 E kinase domain in complex with BRAF inhibitor PLX 4032 (Vemurafenib). Different regions of BRAF kinase domain are indicated with different colours: small lobe (light pink), large lobe (light blue), glycine rich loop (pale green), catalytic loop (magenta) and DFG motif (red). (A) Binding position of PLX 4032 with kinase domain of V 600 E mutant BRAF. (B) Close view of V 600 E mutant BRAF and PLX 4032 complex, binding amino acids are indicated. The images were prepared with Py. MOL by using the X-ray crystal structure from the protein data bank Source: Critical Reviews in Oncology/Hematology (DOI: 10. 1016/j. critrevonc. 2013. 12. 008 ) Copyright © Elsevier Ireland Ltd Terms and Conditions
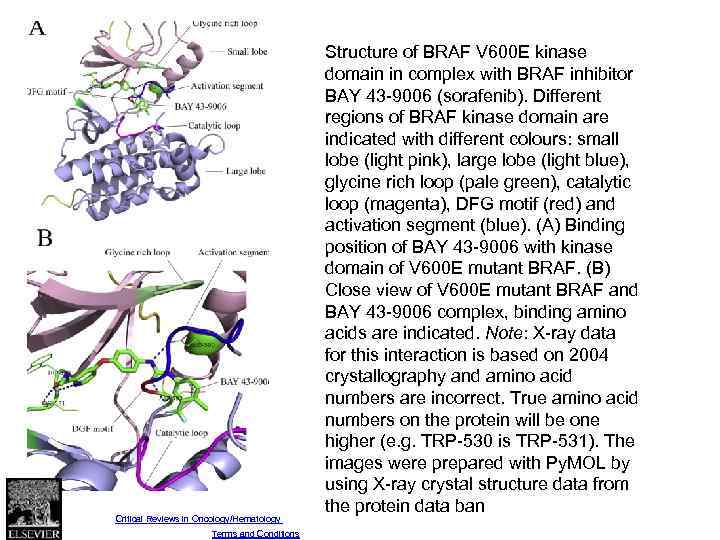
Fig. 3 Structure of BRAF V 600 E kinase domain in complex with BRAF inhibitor BAY 43 -9006 (sorafenib). Different regions of BRAF kinase domain are indicated with different colours: small lobe (light pink), large lobe (light blue), glycine rich loop (pale green), catalytic loop (magenta), DFG motif (red) and activation segment (blue). (A) Binding position of BAY 43 -9006 with kinase domain of V 600 E mutant BRAF. (B) Close view of V 600 E mutant BRAF and BAY 43 -9006 complex, binding amino acids are indicated. Note: X-ray data for this interaction is based on 2004 crystallography and amino acid numbers are incorrect. True amino acid numbers on the protein will be one higher (e. g. TRP-530 is TRP-531). The images were prepared with Py. MOL by using X-ray crystal structure data from the protein data ban Source: Critical Reviews in Oncology/Hematology (DOI: 10. 1016/j. critrevonc. 2013. 12. 008 ) Copyright © Elsevier Ireland Ltd Terms and Conditions

5. 2. 3. Этап МАР киназ

Активированные белки Raf передают сигнал к нижестоящим цитозольным белкам MAP (mitogen active protein) или MAPK (MAP kinase), которые объединяются в семейство МЕК. Эта группа включает 4 различных каскада, которые называются по компоненте, стоящей после МАР киназы. Характеристика МАР киназ N 1 Белки MAPK Тип сигнального пути ERK 1/2 3 Внеклеточная сигналрегулируемая киназа 1 и 2 (МЕК 1 и МЕК 2) c-Jun N-терминальная киназа 1 JNK 1 -3 – 3 p 38 MAPK α, β, γ, δ p 38α-δ 4 ERK 5 2 Большая MAPK ERK 1/2 каскад передает, г. о. , митогенные сигналы, P 38 и JNK – активированные стрессом, ERK 5 – оба пути
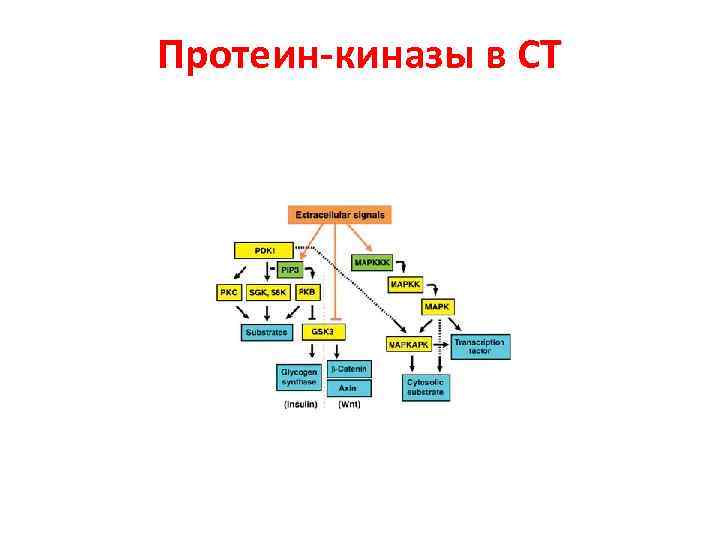
Протеин-киназы в СТ
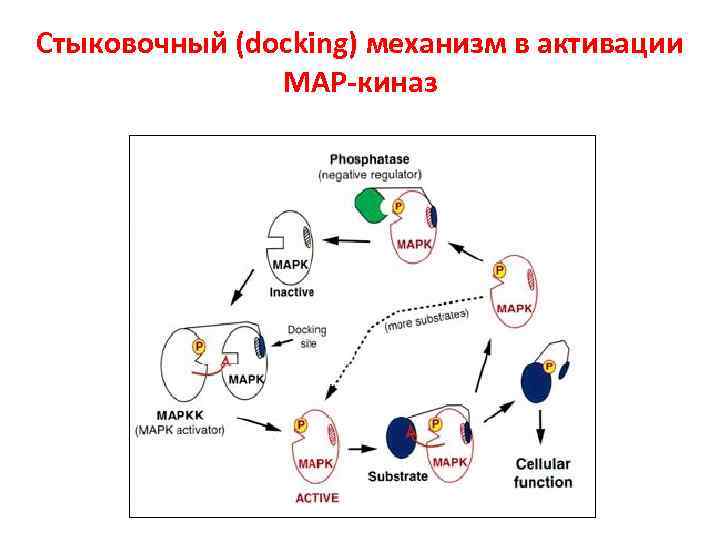
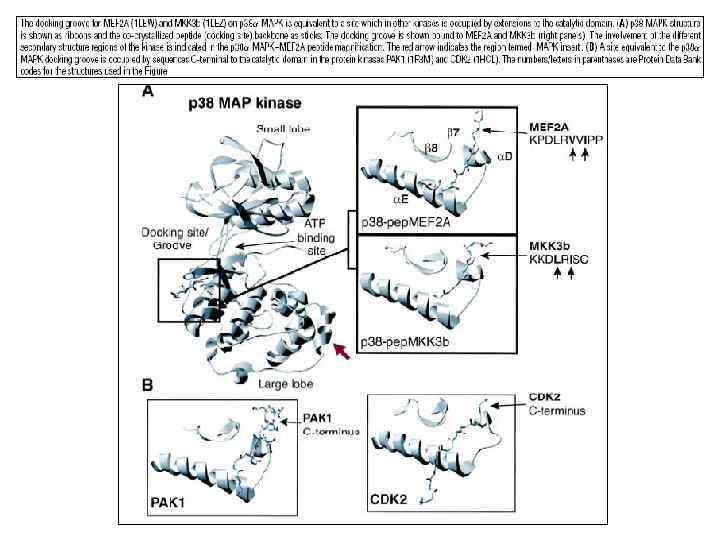
Стыковочный (docking) механизм в активации МАР-киназ
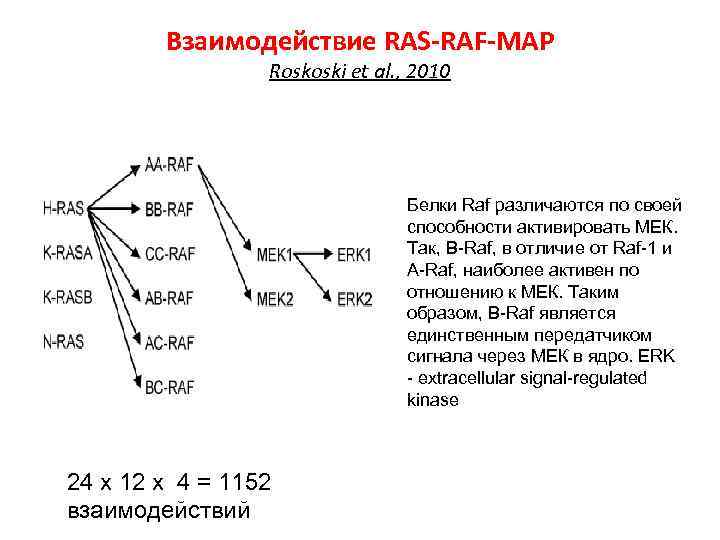
Взаимодействие RAS-RAF-MAP Roskoski et al. , 2010 Белки Raf различаются по своей способности активировать МЕК. Так, B-Raf, в отличие от Raf-1 и A-Raf, наиболее активен по отношению к МЕК. Таким образом, B-Raf является единственным передатчиком сигнала через МЕК в ядро. ERK - extracellular signal-regulated kinase 24 х 12 х 4 = 1152 взаимодействий

ERK 1/2 киназы • ERK 1/2 – генные продукты ERK 1 (MAPK 3) и ERK 2 (MAPK 1). • MEK 1/2 -опосредованное фосфорилирование ERK 1/2 (Thr и Tyr в последовательности Thr-Xaa-Tyr) • Известно более 200 субстратов ERK 1/2, в том числе ФТ Elk 1, c-Fos и c-Jun.
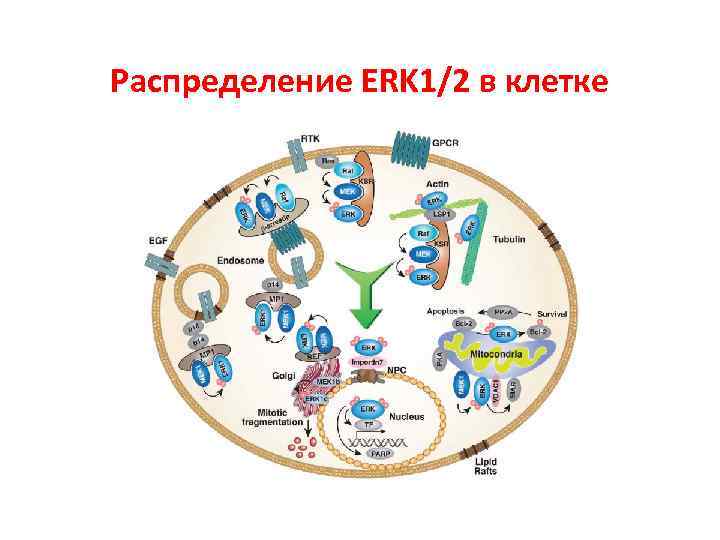
Распределение ERK 1/2 в клетке
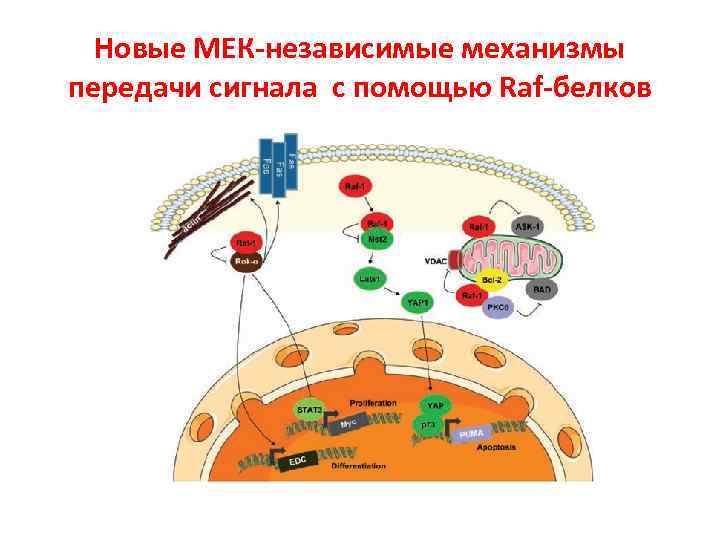
Новые МЕК-независимые механизмы передачи сигнала с помощью Raf-белков
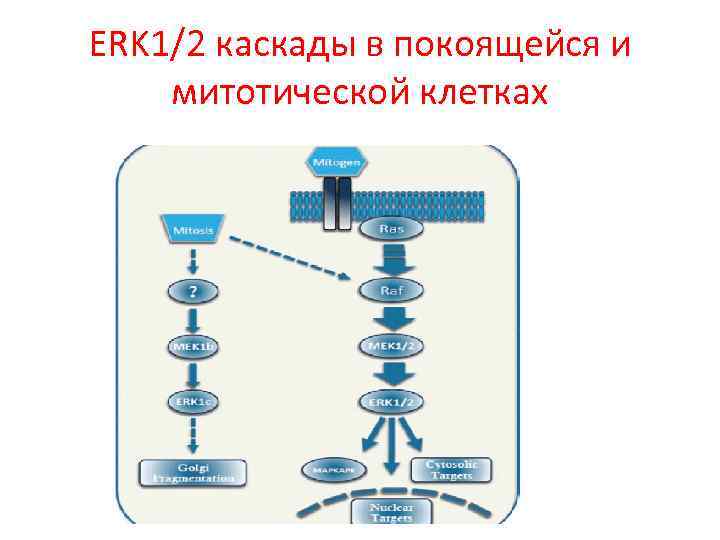
ERK 1/2 каскады в покоящейся и митотической клетках
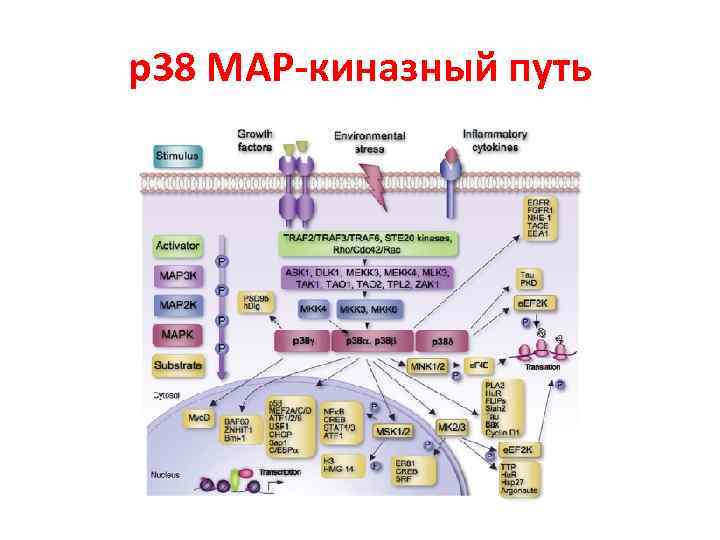
р38 МАР-киназный путь
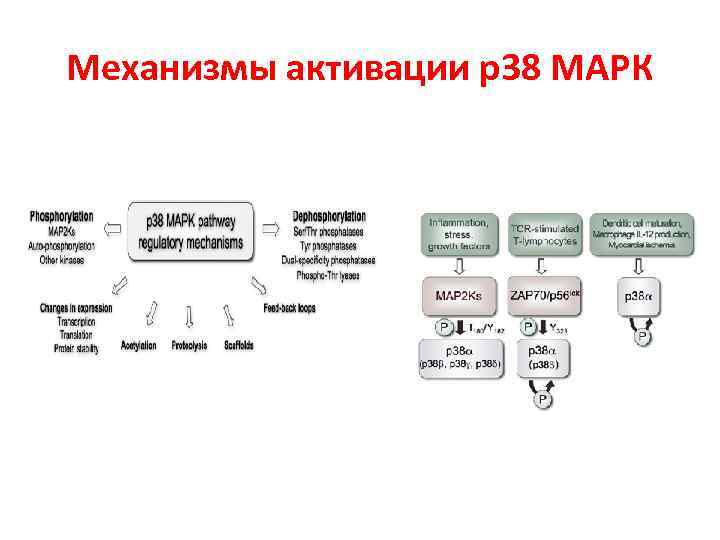
Механизмы активации р38 МАРК
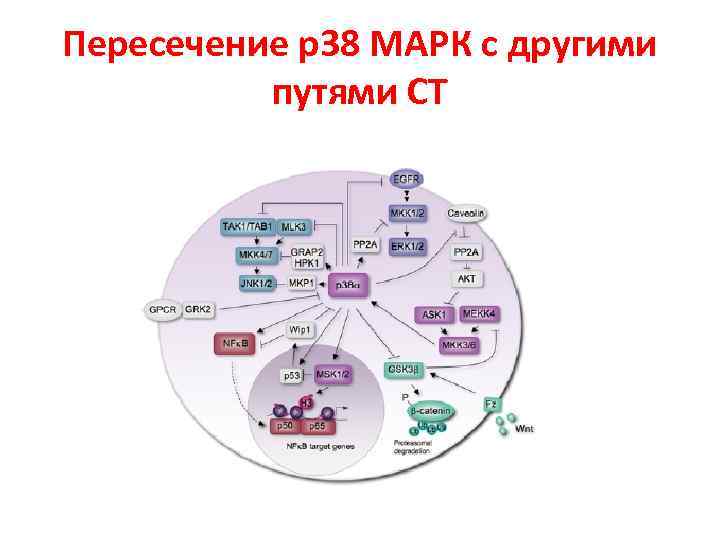
Пересечение р38 МАРК с другими путями СТ
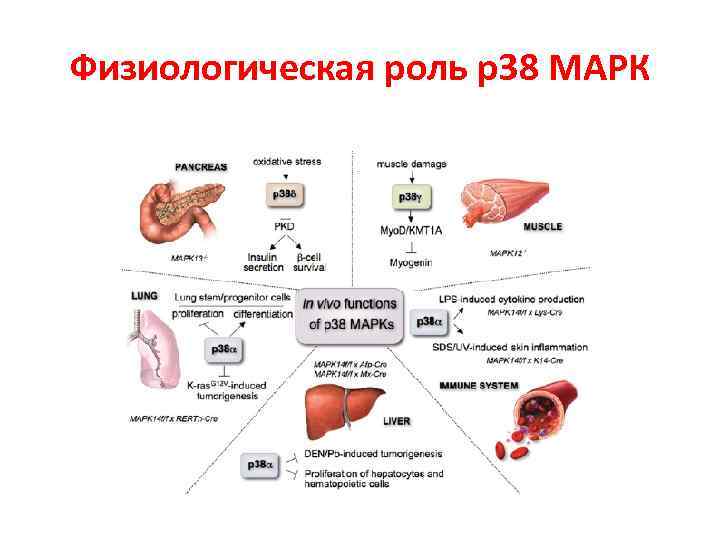
Физиологическая роль р38 МАРК

Другие пути СТ
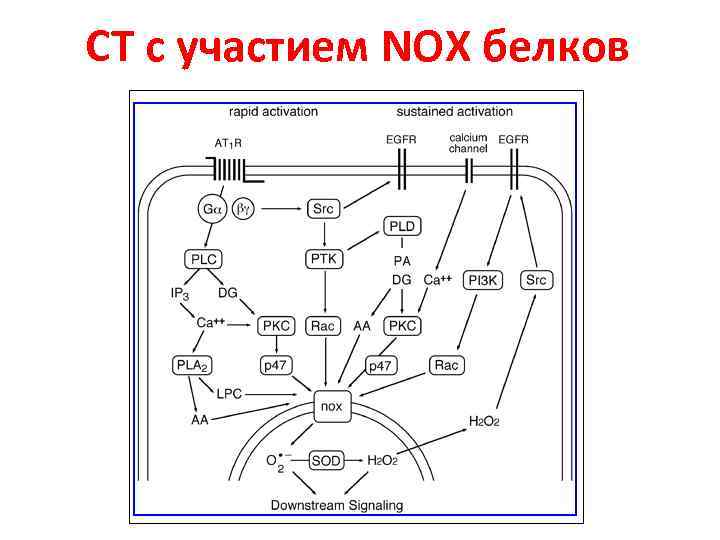
СТ с участием NOX белков

PI 3 K путь СТ

Липидная киназа PI 3 K • Существует 3 класса киназ PI 3 K, различающихся по структуре и функциям. Класс IA PI 3 K чаще всего ассоциирован с возникновением рака. Известно 3 гена этого класса: PIK 3 R 1, PIK 3 R 2 и PIK 3 R 3, активирующие мутации в которых находят в опухолевых клетках человека.
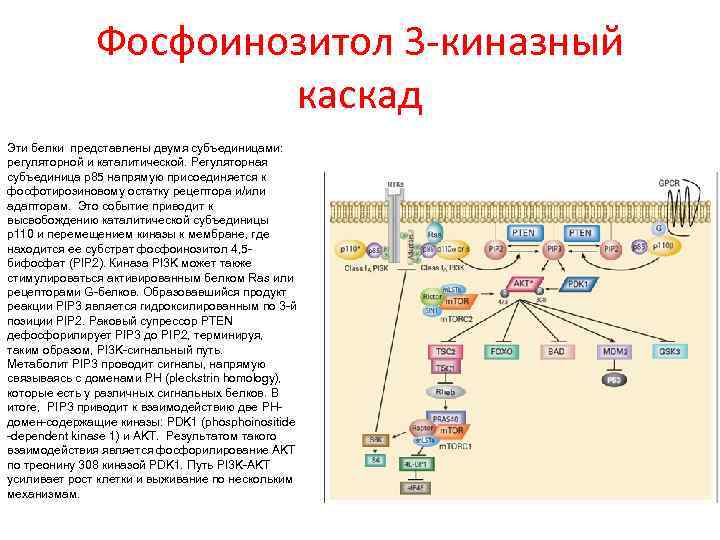
Фосфоинозитол 3 -киназный каскад Эти белки представлены двумя субъединицами: регуляторной и каталитической. Регуляторная субъединица p 85 напрямую присоединяется к фосфотирозиновому остатку рецептора и/или адапторам. Это событие приводит к высвобождению каталитической субъединицы p 110 и перемещением киназы к мембране, где находится ее субстрат фосфоинозитол 4, 5 бифосфат (PIP 2). Киназа PI 3 K может также стимулироваться активированным белком Ras или рецепторами G-белков. Образовавшийся продукт реакции PIP 3 является гидроксилированным по 3 -й позиции PIP 2. Раковый супрессор PTEN дефосфорилирует PIP 3 до PIP 2, терминируя, таким образом, PI 3 K-сигнальный путь. Метаболит PIP 3 проводит сигналы, напрямую связываясь с доменами PH (pleckstrin homology), которые есть у различных сигнальных белков. В итоге, PIP 3 приводит к взаимодействию две PHдомен-содержащие киназы: PDK 1 (phosphoinositide -dependent kinase 1) и AKT. Результатом такого взаимодействия является фосфорилирование AKT по треонину 308 киназой PDK 1. Путь PI 3 K-AKT усиливает рост клетки и выживание по нескольким механизмам.
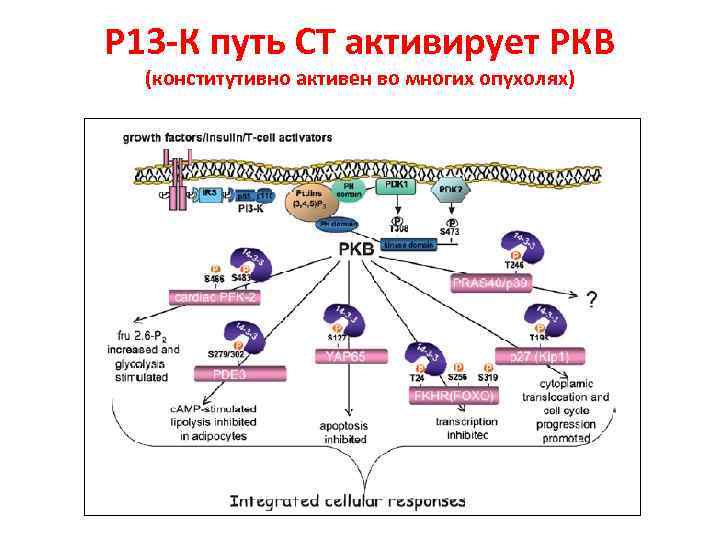
Р 13 -К путь СТ активирует РКВ (конститутивно активен во многих опухолях)

m. TOR путь СТ

m. TOR • Этот путь играет ключевую роль в росте и питании клетки. Чтобы избежать дефицита энергии и гибель, клетки достаточно быстро ингибируют программы биосинтеза, увеличивая рециркуляцию «старых» белков и органелл как источников метаболитов, в результате чего пролиферация замедляется или вообще останавливается. Киназа TOR (target of rapamycin) является своеобразным интерфейсом между ростом и голодом клетки. Появление этой киназы у ранних эукариот сделало возможным для одноклеточных организмов реагировать на питательные вещества и расти в комфортных условиях. У многоклеточных организмов у TOR появилась еще одна функция: контролировать рост и гомеостаз. TOR млекопитающих (m. TOR) играет ключевую роль в старении, а также в развитии таких болезней человека, как рак, метаболические болезни, включая диабет.

С помощью генетических и биохимических подходов TOR была открыта у дрожжей и млекопитающих как мишень для иммуносупрессора рапамицина, макролидного препарата, синтезируемого почвенной бактерией острова Пасхи. Белок TOR принадлежит к семейству phospho inositide 3 -kinase (PI 3 K)-related protein kinases (PIKK), которое представлено большим семейством белков, контролирующим стресс, вызванный метаболическими, генетическими нарушениями в окружающей среде. Установлено, что m. TOR является каталитической субъединицей двух различных комплексов: m. TOR complex 1 (m. TORC 1) и m. TORC 2
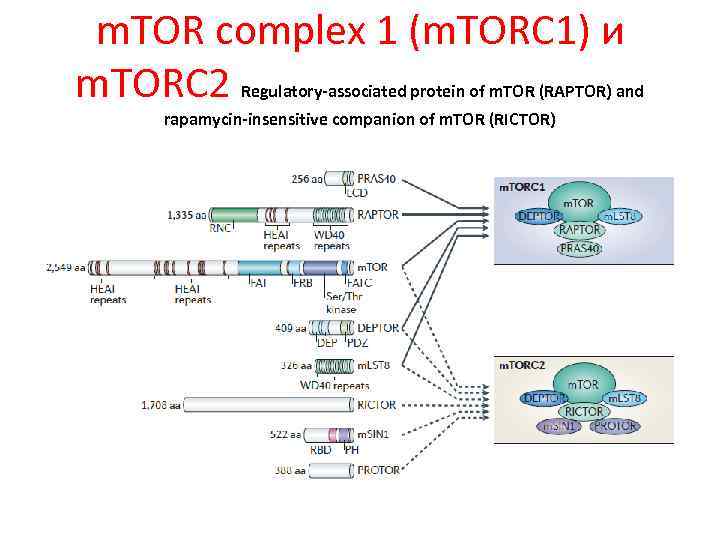
m. TOR complex 1 (m. TORC 1) и m. TORC 2 Regulatory-associated protein of m. TOR (RAPTOR) and rapamycin-insensitive companion of m. TOR (RICTOR)

У дрожжей и млекопитающих рапамицин ингибирует способность m. TORC 1, но не m. TORC 2 фосфорилировать субстраты. Рапамицин связывает небольшие молекулы с м. м. 12 k. Da, такие как белок FKBP 1, и ингибирует связывание с белком RAPTOR
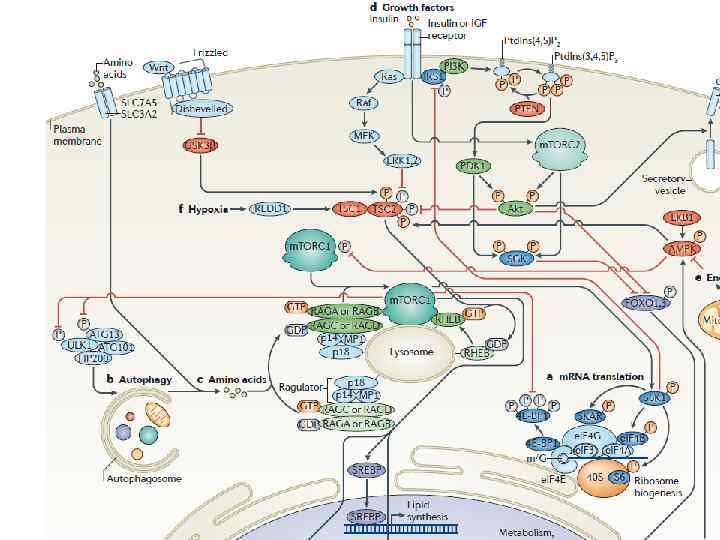
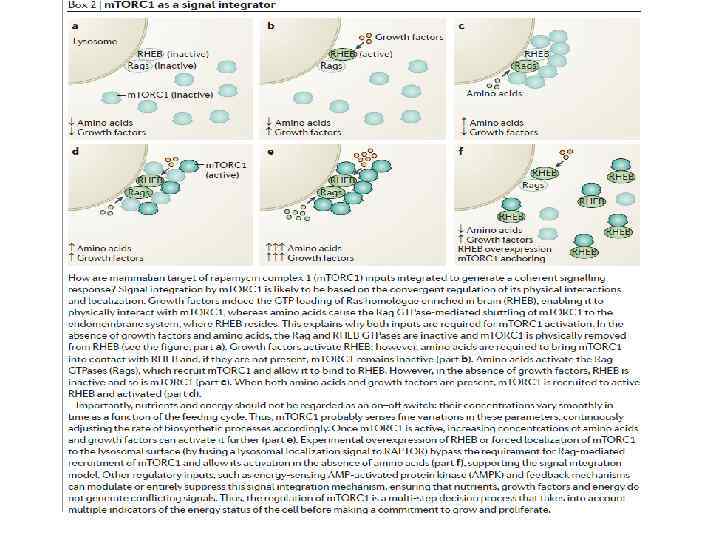
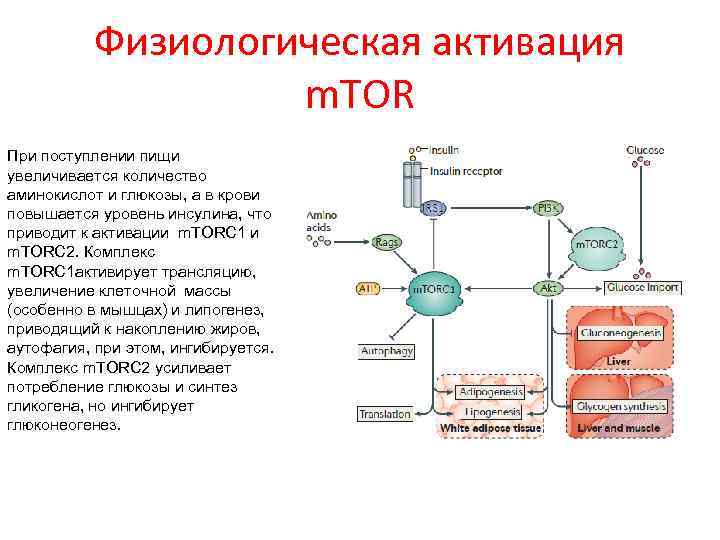
Физиологическая активация m. TOR При поступлении пищи увеличивается количество аминокислот и глюкозы, а в крови повышается уровень инсулина, что приводит к активации m. TORC 1 и m. TORC 2. Комплекс m. TORC 1 активирует трансляцию, увеличение клеточной массы (особенно в мышцах) и липогенез, приводящий к накоплению жиров, аутофагия, при этом, ингибируется. Комплекс m. TORC 2 усиливает потребление глюкозы и синтез гликогена, но ингибирует глюконеогенез.
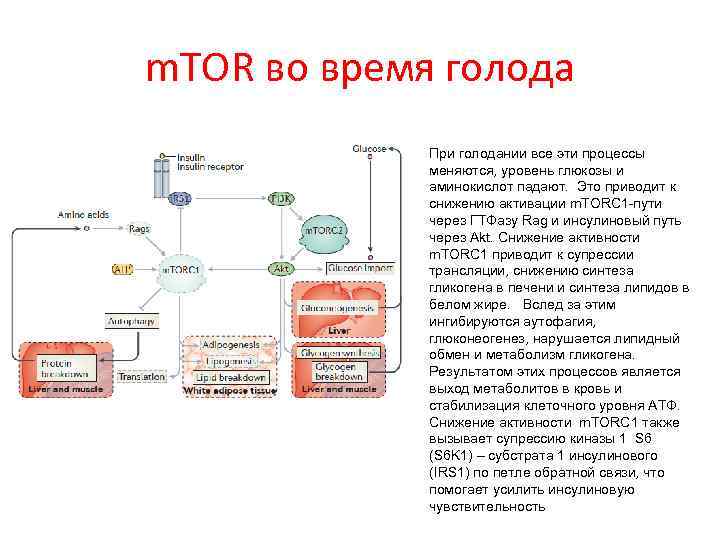
m. TOR во время голода При голодании все эти процессы меняются, уровень глюкозы и аминокислот падают. Это приводит к снижению активации m. TORC 1 -пути через ГТФазу Rag и инсулиновый путь через Akt. Снижение активности m. TORC 1 приводит к супрессии трансляции, снижению синтеза гликогена в печени и синтеза липидов в белом жире. Вслед за этим ингибируются аутофагия, глюконеогенез, нарушается липидный обмен и метаболизм гликогена. Результатом этих процессов является выход метаболитов в кровь и стабилизация клеточного уровня АТФ. Снижение активности m. TORC 1 также вызывает супрессию киназы 1 S 6 (S 6 K 1) – субстрата 1 инсулинового (IRS 1) по петле обратной связи, что помогает усилить инсулиновую чувствительность
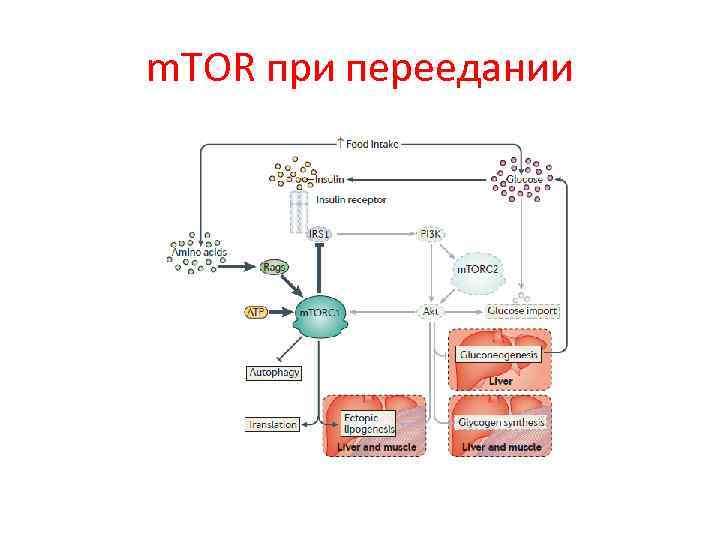
m. TOR при переедании
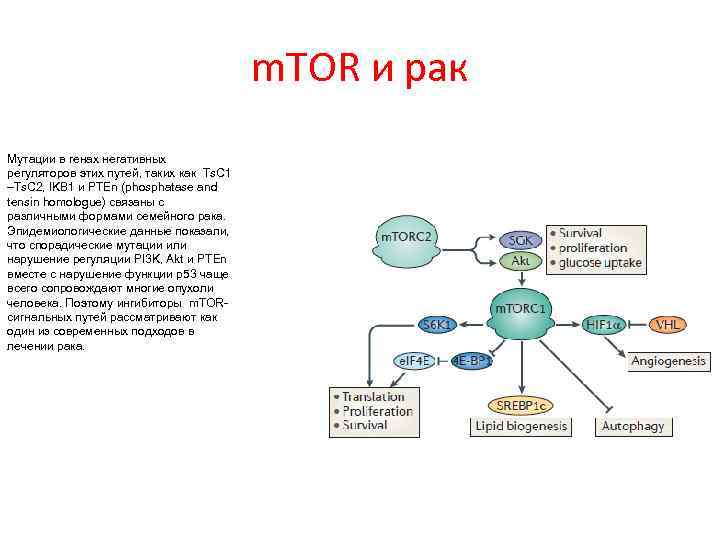
m. TOR и рак Мутации в генах негативных регуляторов этих путей, таких как Ts. C 1 –Ts. C 2, l. KB 1 и PTEn (phosphatase and tensin homologue) связаны с различными формами семейного рака. Эпидемиологические данные показали, что спорадические мутации или нарушение регуляции PI 3 K, Akt и PTEn вместе с нарушение функции p 53 чаще всего сопровождают многие опухоли человека. Поэтому ингибиторы m. TORсигнальных путей рассматривают как один из современных подходов в лечении рака.
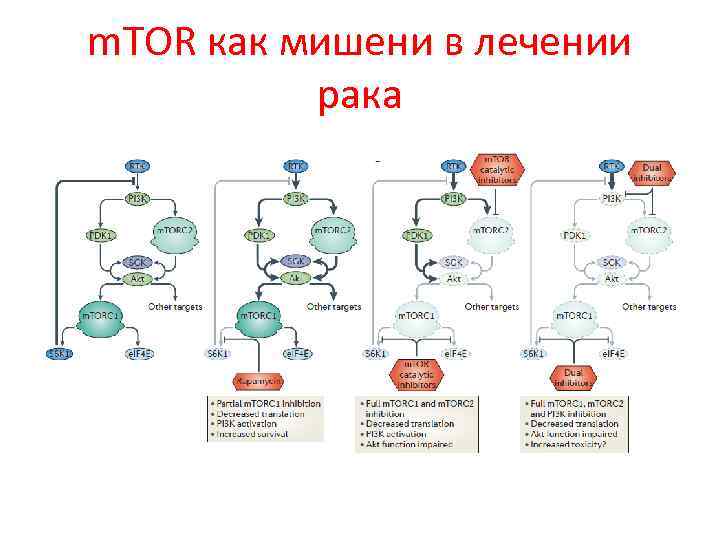
m. TOR как мишени в лечении рака
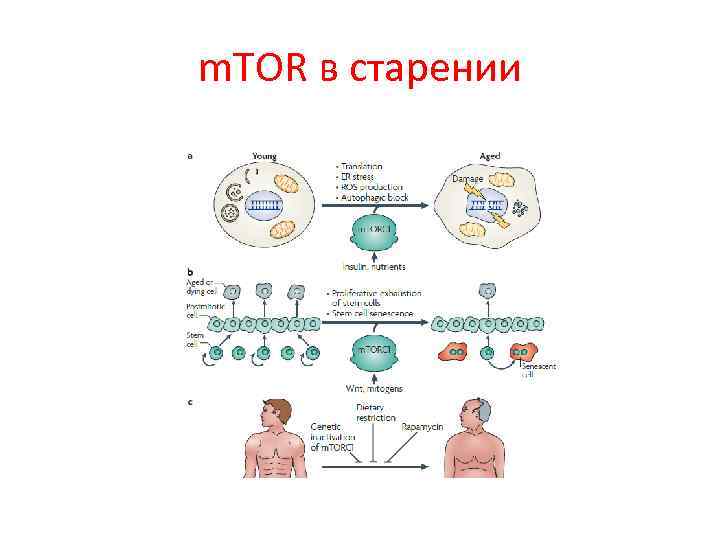
m. TOR в старении
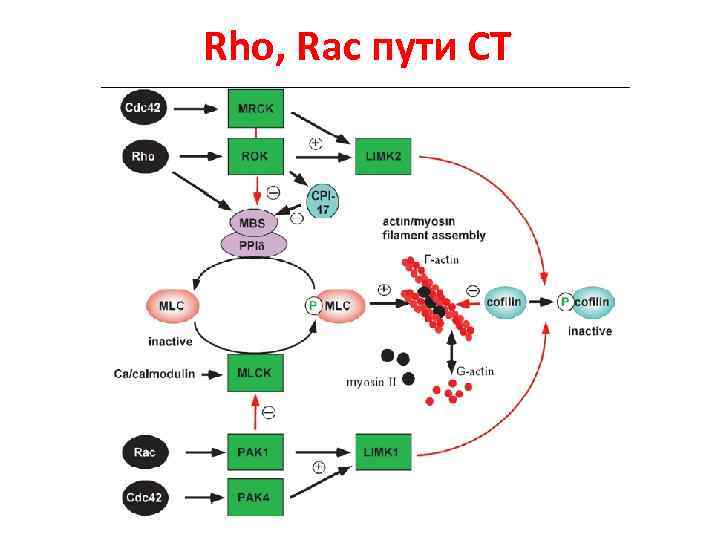
Rho, Rac пути СТ
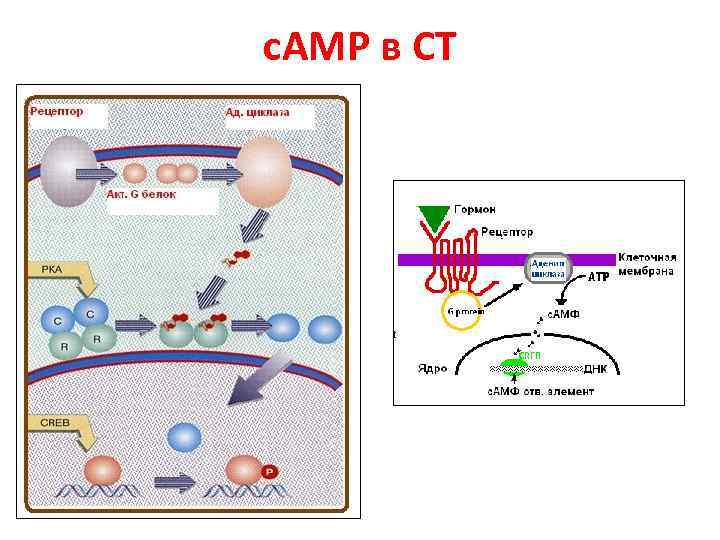
c. АМP в СТ

NOTCH 1 -сигнальный путь
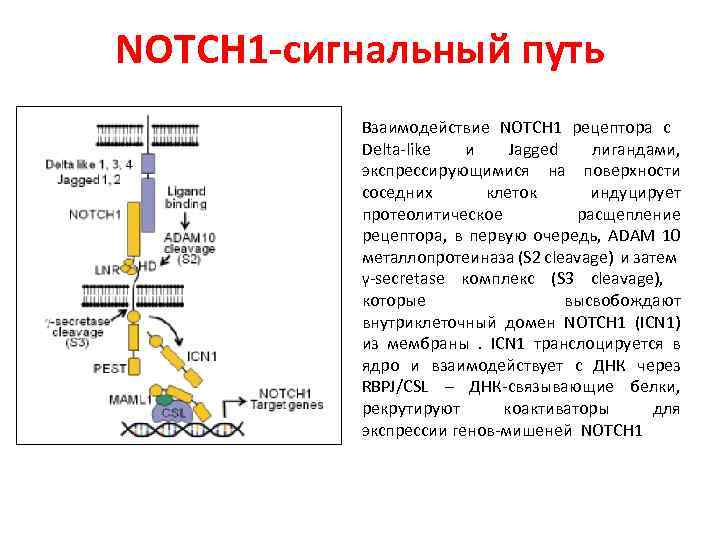
NOTCH 1 -сигнальный путь Взаимодействие NOTCH 1 рецептора с Delta-like и Jagged лигандами, экспрессирующимися на поверхности соседних клеток индуцирует протеолитическое расщепление рецептора, в первую очередь, ADAM 10 металлопротеиназа (S 2 cleavage) и затем γ-secretase комплекс (S 3 cleavage), которые высвобождают внутриклеточный домен NOTCH 1 (ICN 1) из мембраны. ICN 1 транслоцируется в ядро и взаимодействует с ДНК через RBPJ/CSL – ДНК-связывающие белки, рекрутируют коактиваторы для экспрессии генов-мишеней NOTCH 1
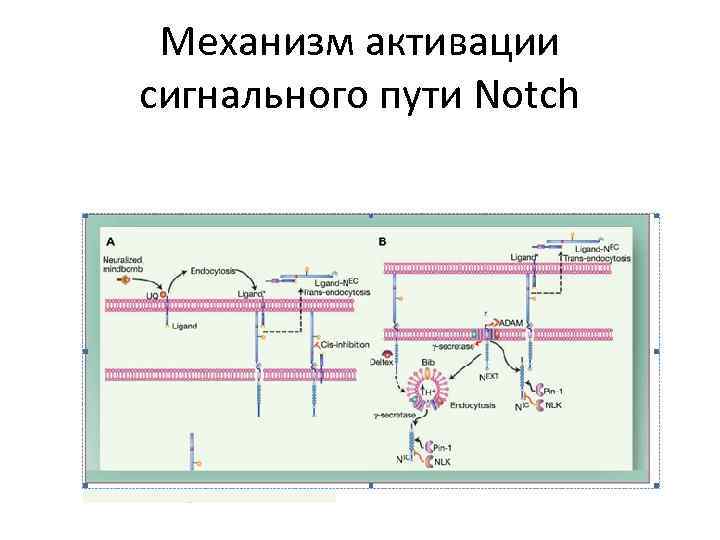
Механизм активации сигнального пути Notch
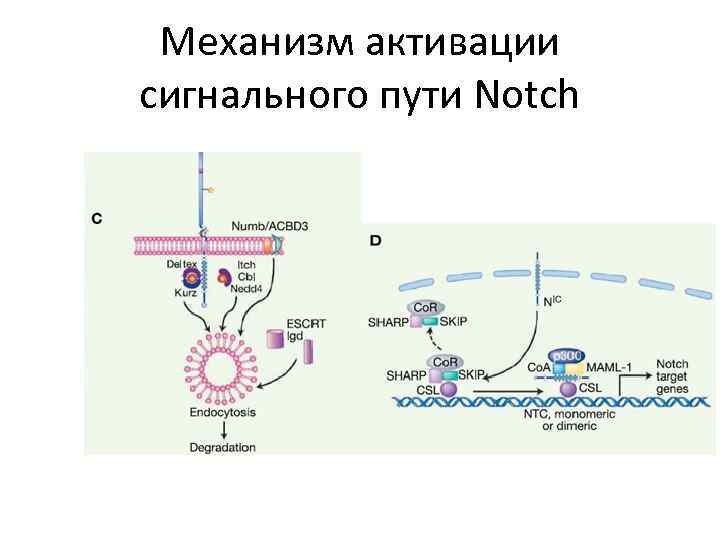
Механизм активации сигнального пути Notch

Онкогенные формы NOTCH 1 при T-ALL Аберрантная активация NOTCH может происходить из-за мутаций. (А) рецептор дикого типа; (b) Транслокация NOTCH 1 в TCR локус индуцирует усеченные формы NOTCH 1. (c) NOTCH 1 HD мутации класса 1 дестабилизируют структуру HD-LNR повторов, ответственных за поддержание конфигурации рецептора (d) NOTCH 1 H 1545 P мутации повреждают защиту от S 2 расщепления у HD-LNR (e) NOTCH 1 HD мутации класса 2 располагают S 2 МР сайт расщепления вне HD-LNR комплекса (f) NOTCH 1 JME усиливает выделение HD-LNR повторного комплекса из мембраны (g) NOTCH 1 ΔPEST у C-конца рецептора нарушает деградацию активного NOTCH 1 в ядре.

Распределение мутаций при лейкемии (TALL)

WNT (АРС) путь СТ
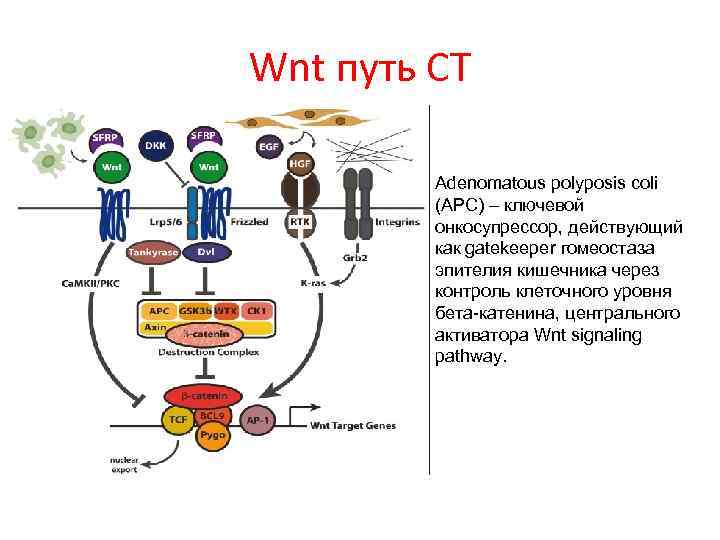
Wnt путь СТ Adenomatous polyposis coli (APC) – ключевой онкосупрессор, действующий как gatekeeper гомеостаза эпителия кишечника через контроль клеточного уровня бета-катенина, центрального активатора Wnt signaling pathway.

Канонический Wnts исгнал проходит через активатор транскрипции β-catenin. В отсутствие лигандов цитоплазматический β-catenin находтся в составе комплекса «деструктивных» белков: APC, glycogen synthase kinase 3 -β (GSK-3β), Axin и др. В этом состоянии β-catenin фосфорилирован, убиквитинирован и деградирован, что предотвращает его транслокация в ядро и взаимодействие с семйеством ФТ семейства LEF/TCF (LEF-1/LEF 1, TCF-1/TCF 7, TCF-3/TCF 7 L 1 и TCF-4/TCF 7 L 2. Когда присутствуют лиганды Wnt, они связываются с рецепторным комплексом, состоящем из 7 -ми трансмембранных белков Frizzled (Fz) и дного рецептора LRP 5/6 (lipoprotein-related protein 5 or 6). Связывание с этими рецепторами рекрутирует скаффолд-белок Dishevelled (Dvl), что приводит к фосфорилированию LRP 5/6 и рекрутированию Axin и. GSK-3β в стороне от комплекса деструкции. Это событие ведет к освобождению β-catenin и накоплению его в ядре вместе с LEF/TCFs. Когда возрастает его ядерная концентрация, LEF/TCFs направляет β-catenin к генаммишеням и способствует взаимодействию с корегуляторами Pygopus, BCL 9/Legless и активации транскрипционных комплексов, таких как CDK 8 module of Mediator и TRRAP.

Структура АРС белка
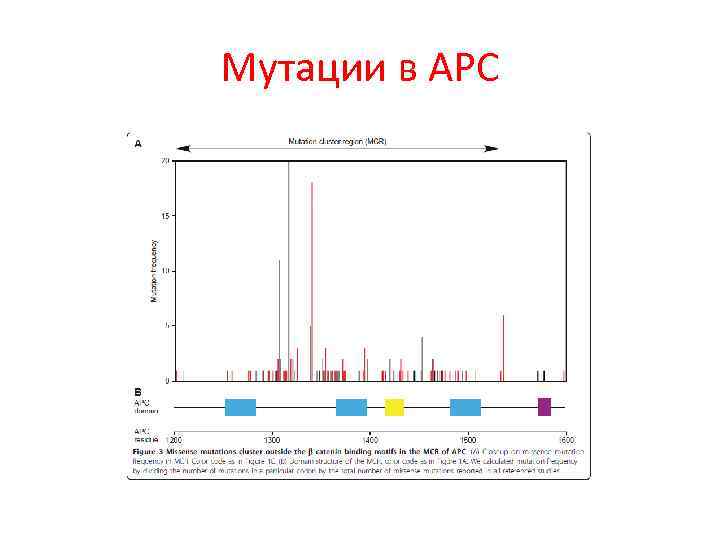
Мутации в АРС
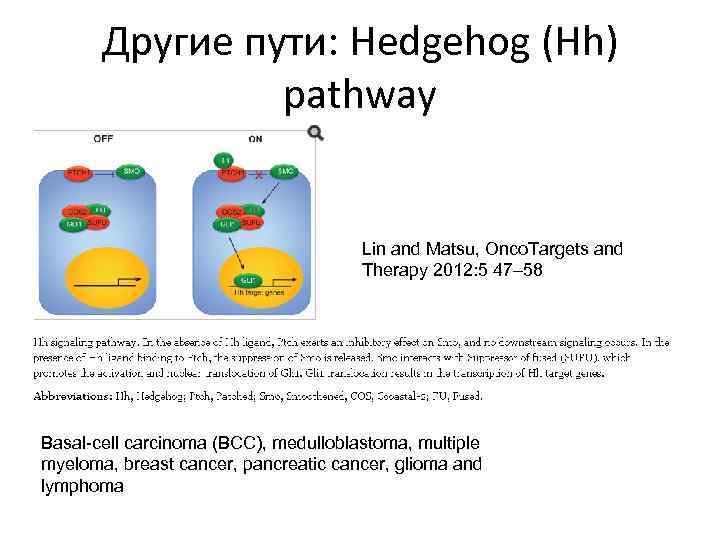
Другие пути: Hedgehog (Hh) pathway Lin and Matsu, Onco. Targets and Therapy 2012: 5 47– 58 Basal-cell carcinoma (BCC), medulloblastoma, multiple myeloma, breast cancer, pancreatic cancer, glioma and lymphoma

Стратегия таргетной терапии Currently a newer drug, vismodegib acting through inhibition of the Hh pathway has been approved by the US Food and Drug Administration's (US FDA) priority review program on January 30, 2012, for the treatment of advanced form of basal-cell carcinoma
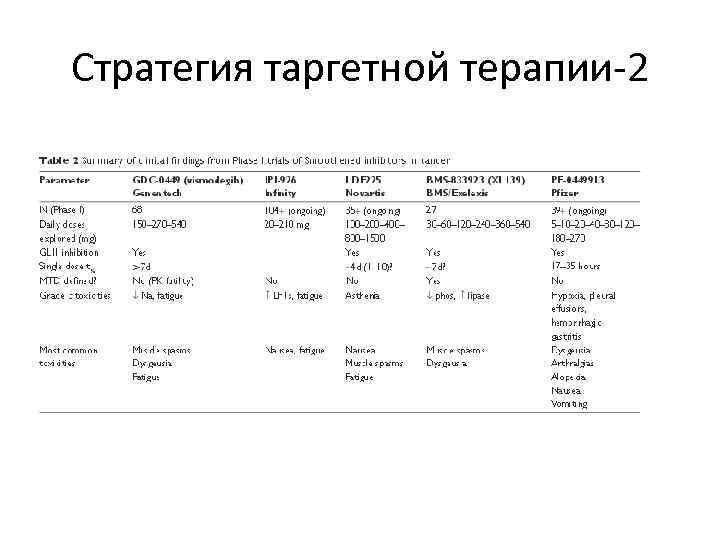
Стратегия таргетной терапии-2
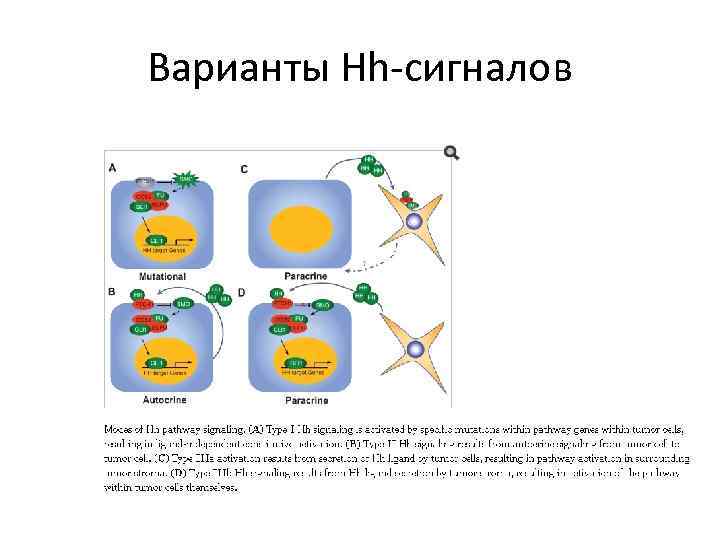
Варианты Hh-сигналов

Стероидные рецепторы в сигнальной трансдукции
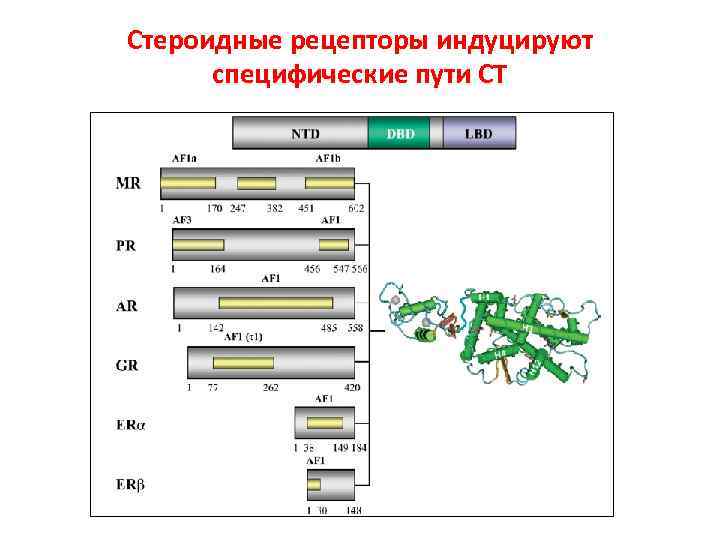
Стероидные рецепторы индуцируют специфические пути СТ

Суперсемейство NRs
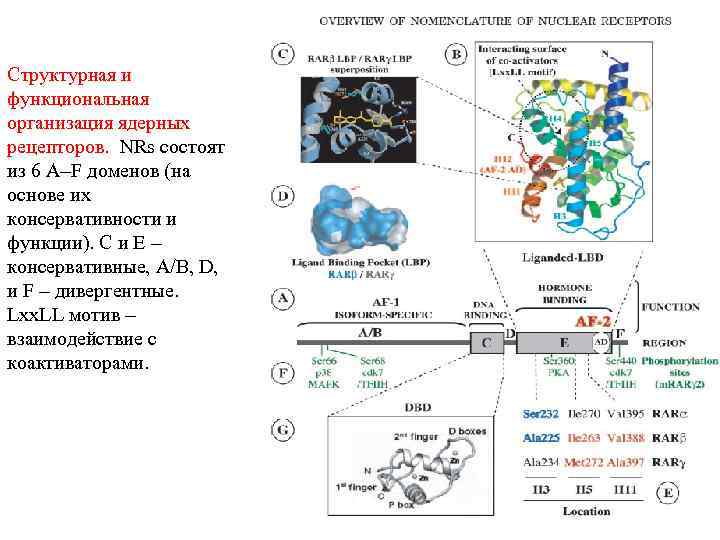
Структурная и функциональная организация ядерных рецепторов. NRs состоят из 6 A–F доменов (на основе их консервативности и функции). C и E – консервативные, A/B, D, и F – дивергентные. Lxx. LL мотив – взаимодействие с коактиваторами.
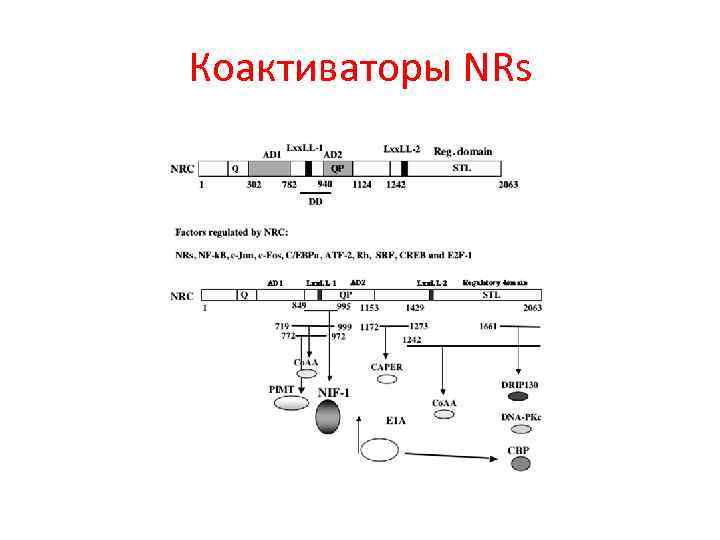
Коактиваторы NRs
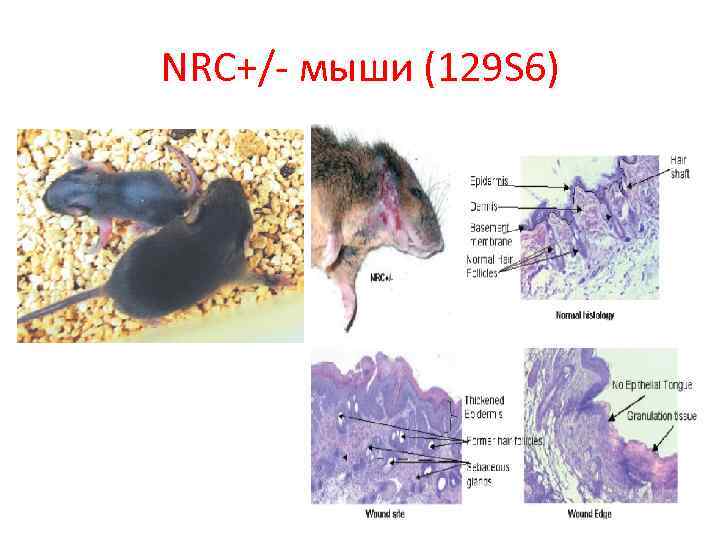
NRC+/- мыши (129 S 6)

Эстрогеновые рецепторы в канцерогенезе
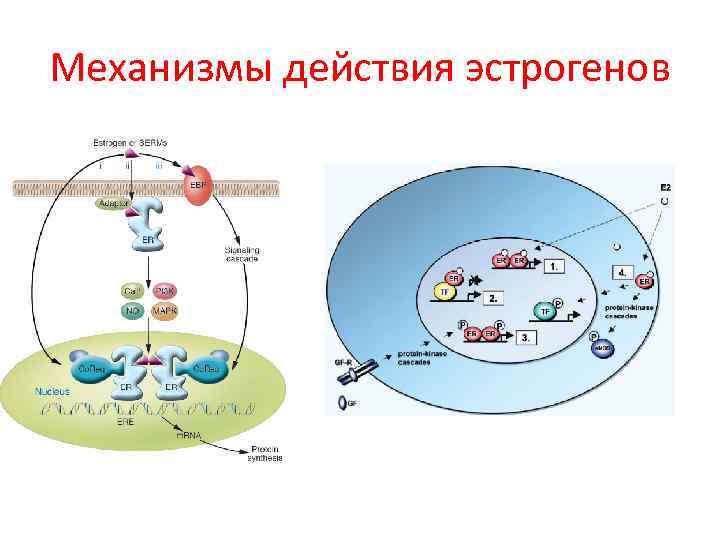
Механизмы действия эстрогенов
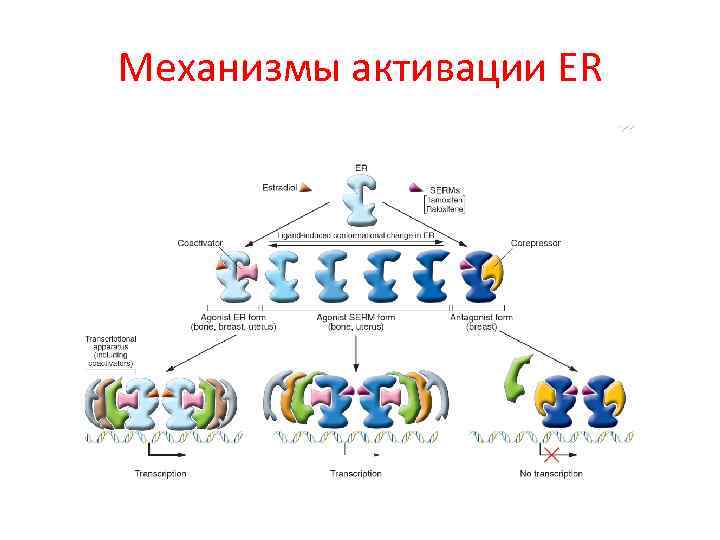
Механизмы активации ER
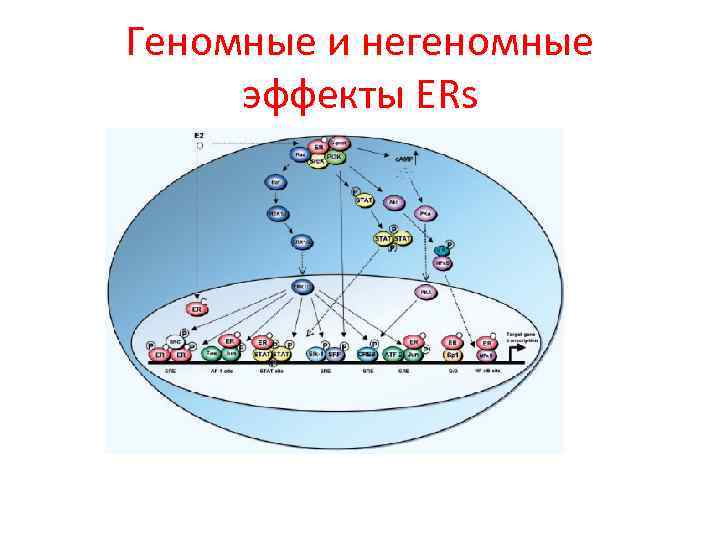
Геномные и негеномные эффекты ERs
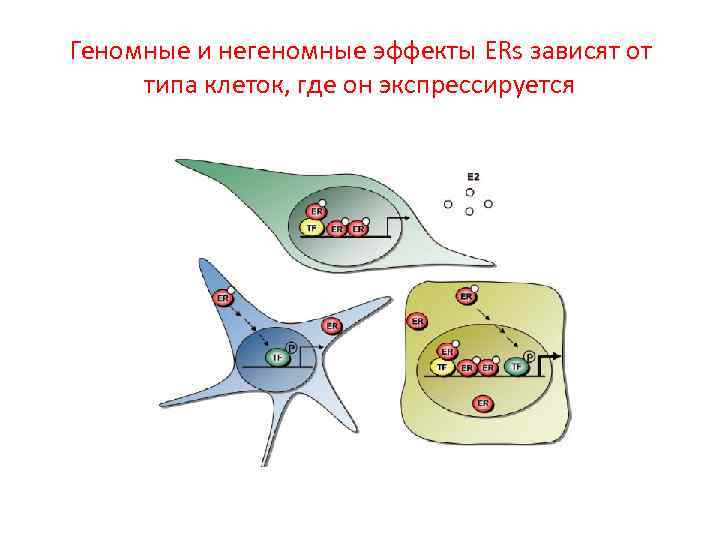
Геномные и негеномные эффекты ERs зависят от типа клеток, где он экспрессируется

5. 2. 4. Факторы транскрипции
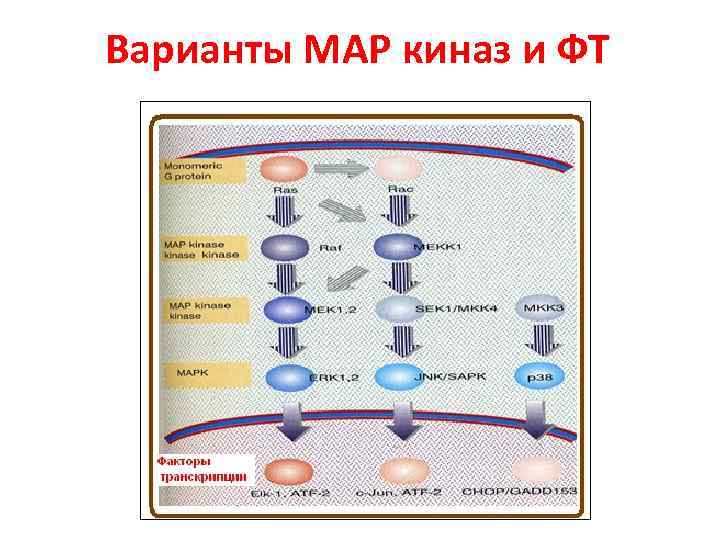
Варианты МАР киназ и ФТ
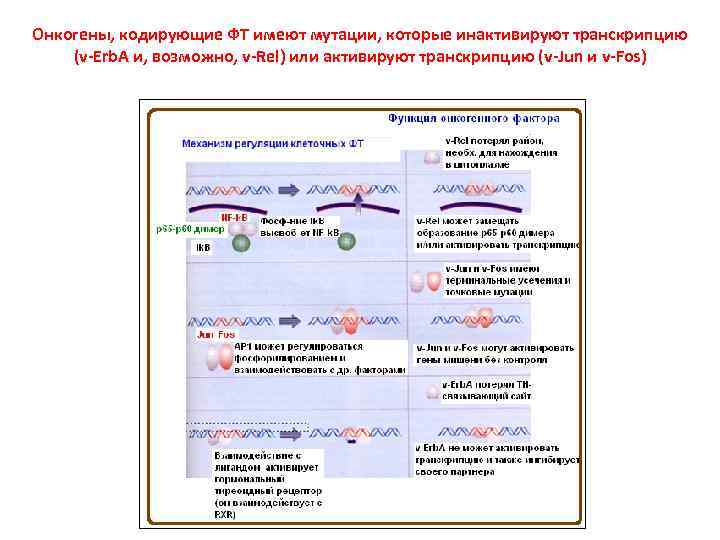
Онкогены, кодирующие ФТ имеют мутации, которые инактивируют транскрипцию (v-Erb. A и, возможно, v-Rel) или активируют транскрипцию (v-Jun и v-Fos)
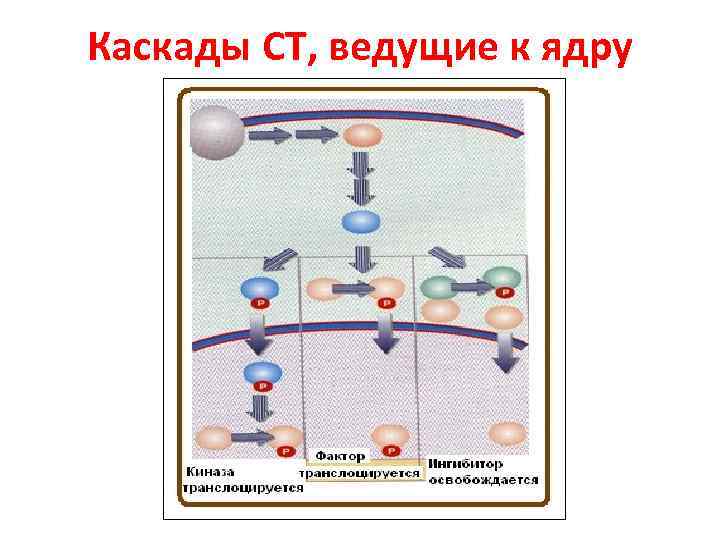
Каскады СТ, ведущие к ядру
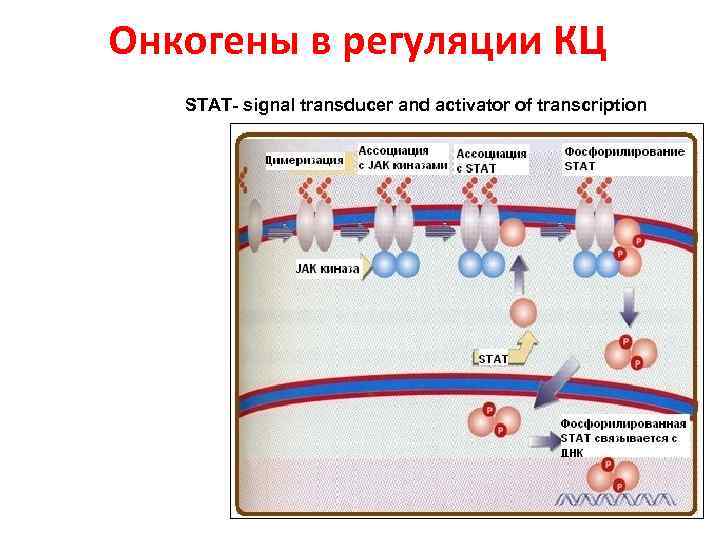
Онкогены в регуляции КЦ STAT- signal transducer and activator of transcription
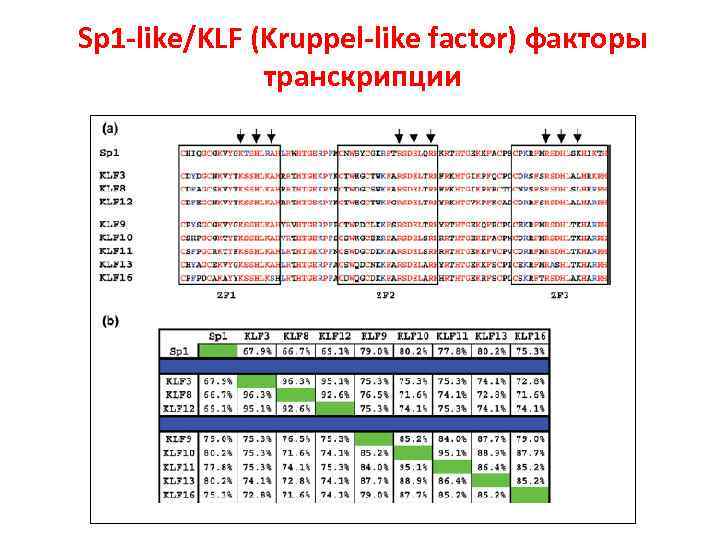
Sp 1 -like/KLF (Kruppel-like factor) факторы транскрипции
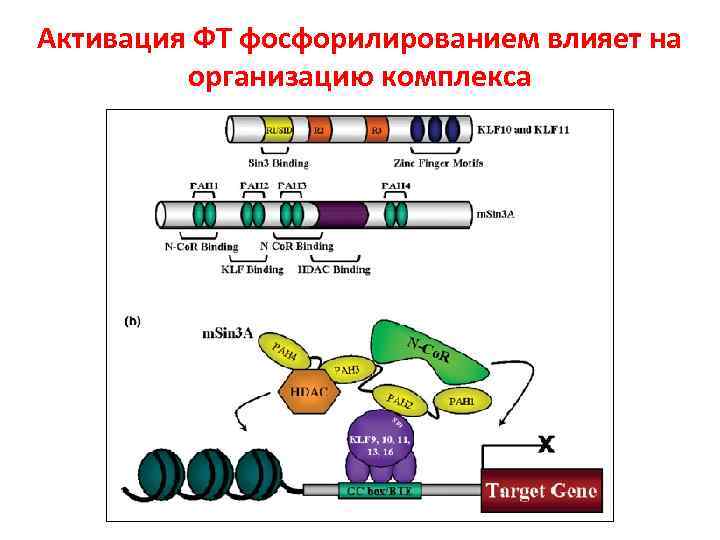
Активация ФТ фосфорилированием влияет на организацию комплекса
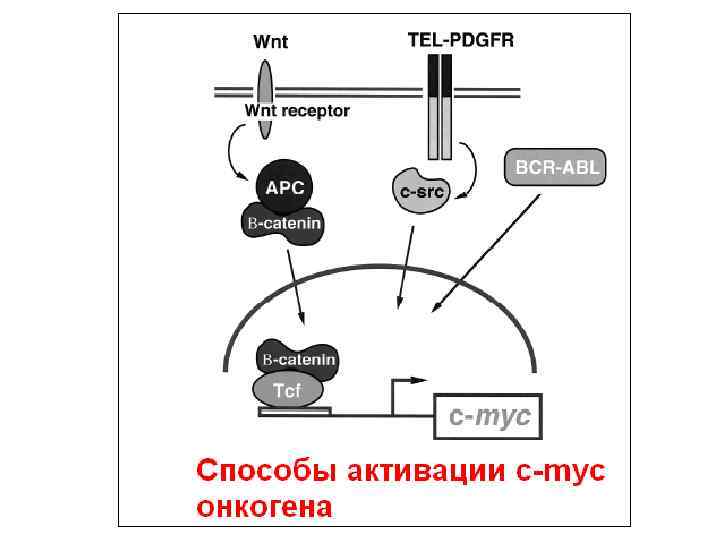
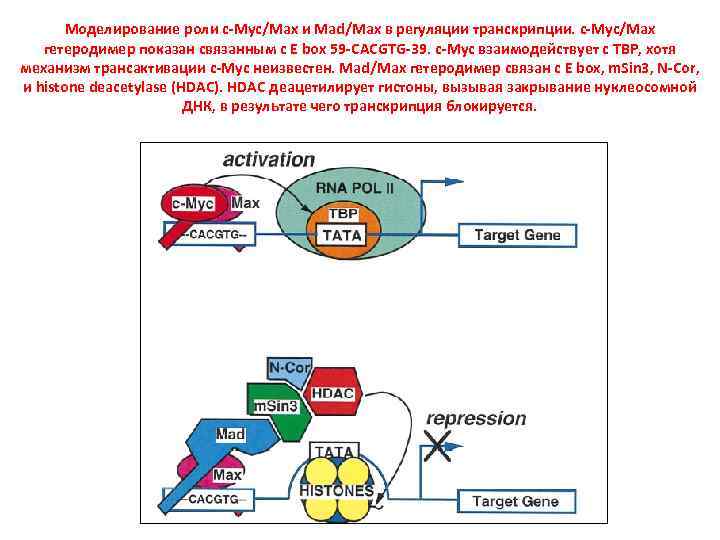
Моделирование роли c-Myc/Max и Mad/Max в регуляции транскрипции. c-Myc/Max гетеродимер показан связанным с E box 59 -CACGTG-39. c-Myc взаимодействует с TBP, хотя механизм трансактивации c-Myc неизвестен. Mad/Max гетеродимер связан с E box, m. Sin 3, N-Cor, и histone deacetylase (HDAC). HDAC деацетилирует гистоны, вызывая закрывание нуклеосомной ДНК, в результате чего транскрипция блокируется.
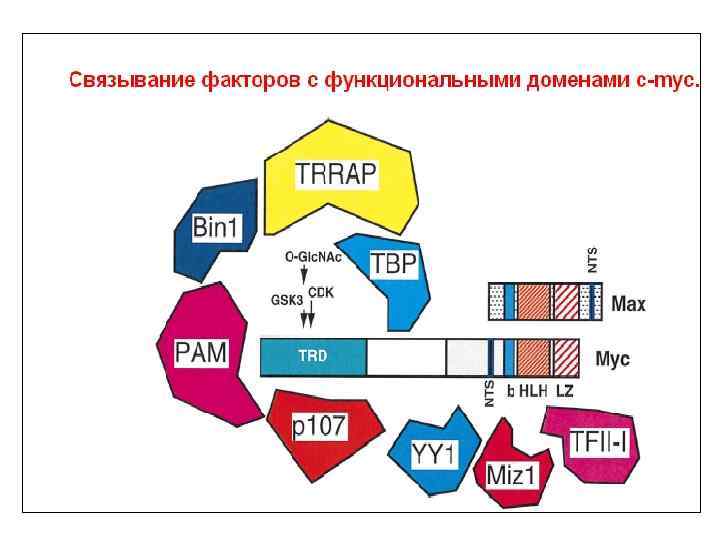
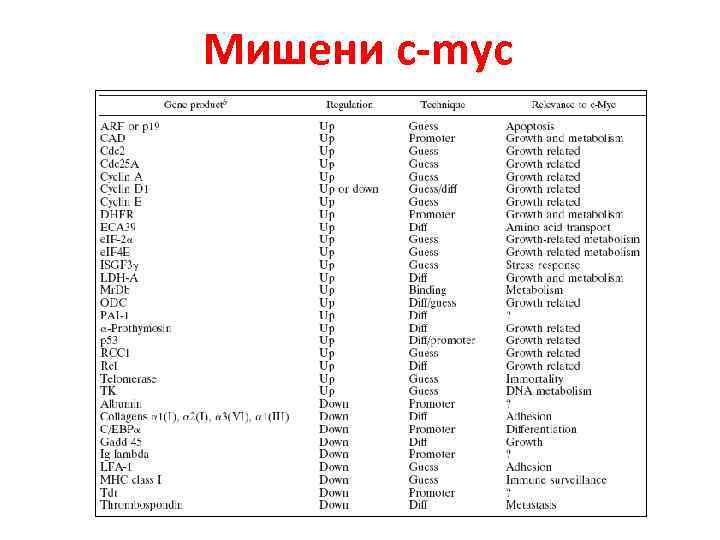
Мишени c-myc
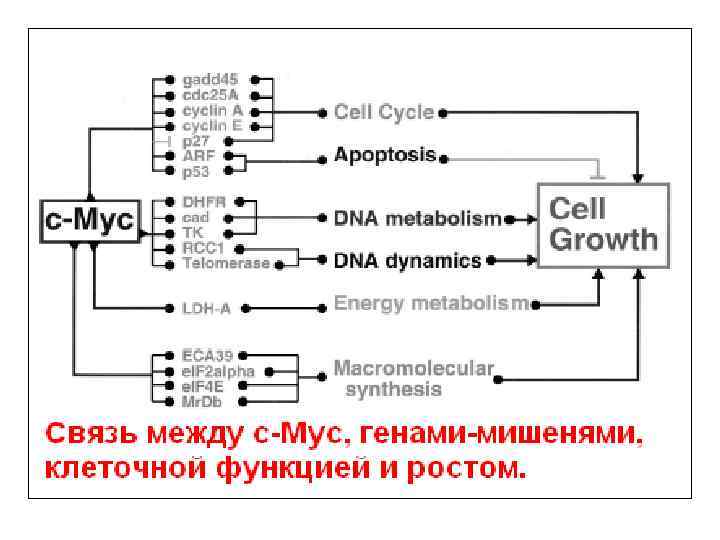

NF-k. B семейство • (p 50/p 105), NF-k. B 2 (p 52/ p 100), Rel. A (p 65), Rel (c-Rel) и Rel. B. • Для них характерно: Rel homology domain (RHD), который опосредует связывание с ДНК, димеризацию и связывание с группой ингибиторов Ik. B • Ik. B киназный комплекс (IKK) состоит из 3 -х субъединиц: IKKa, IKKb и IKKg/NEMO и убиквитина.
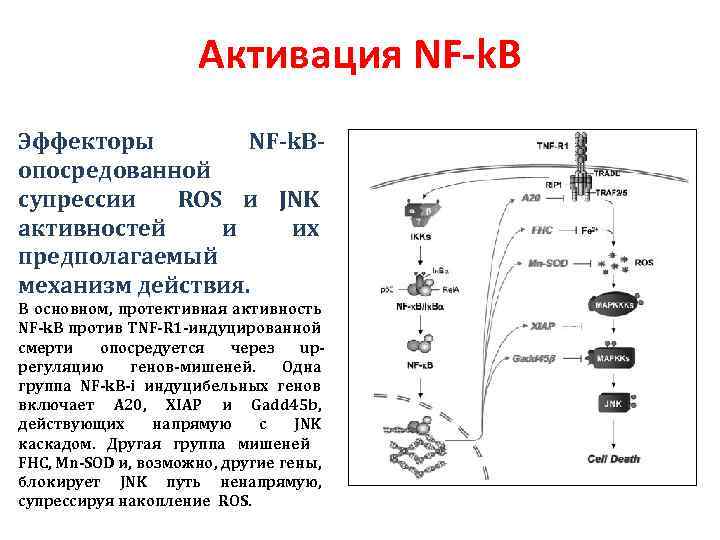
Активация NF-k. B Эффекторы NF-k. Bопосредованной супрессии ROS и JNK активностей и их предполагаемый механизм действия. В основном, протективная активность NF-k. B против TNF-R 1 -индуцированной смерти опосредуется через upрегуляцию генов-мишеней. Одна группа NF-k. B-i индуцибельных генов включает A 20, XIAP и Gadd 45 b, действующих напрямую с JNK каскадом. Другая группа мишеней FHC, Mn-SOD и, возможно, другие гены, блокирует JNK путь ненапрямую, супрессируя накопление ROS.
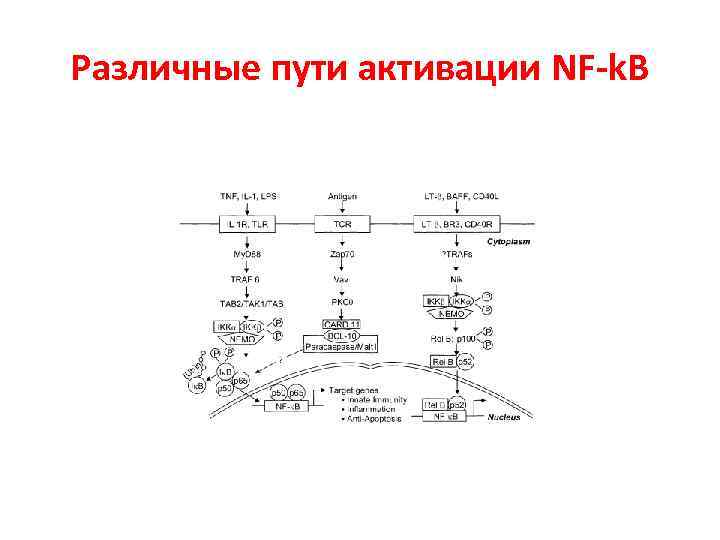
Различные пути активации NF-k. B
Пространственная структура фактора транскрипции NF-к. B
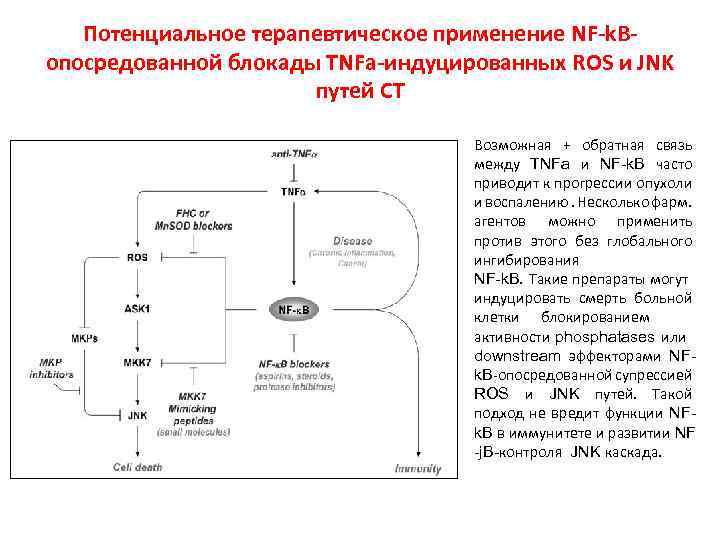
Потенциальное терапевтическое применение NF-k. Bопосредованной блокады TNFa-индуцированных ROS и JNK путей СТ Возможная + обратная связь между TNFa и NF-k. B часто приводит к прогрессии опухоли и воспалению. Несколько фарм. агентов можно применить против этого без глобального ингибирования NF-k. B. Такие препараты могут индуцировать смерть больной клетки блокированием активности phosphatases или downstream эффекторами NFk. B-опосредованной супрессией ROS и JNK путей. Такой подход не вредит функции NFk. B в иммунитете и развитии NF -j. B-контроля JNK каскада.

АР 1 семейство Activator protein 1 (AP-1) семейство белков – содержат лейциновый зиппер (b. ZIP). Они регулируют многие клеточные процессы, включая пролиферацию, выживание, рост, дифференцировку, апоптоз, трансформацию. У млекопитающих это гомоили гетеродимеры, которые формируются jun (c-jun, jun. B, jun. D), fos (c-fos, fra-1, fra-2) или atf белками.
Структура АР 1

АР 1 и его гены-мишени
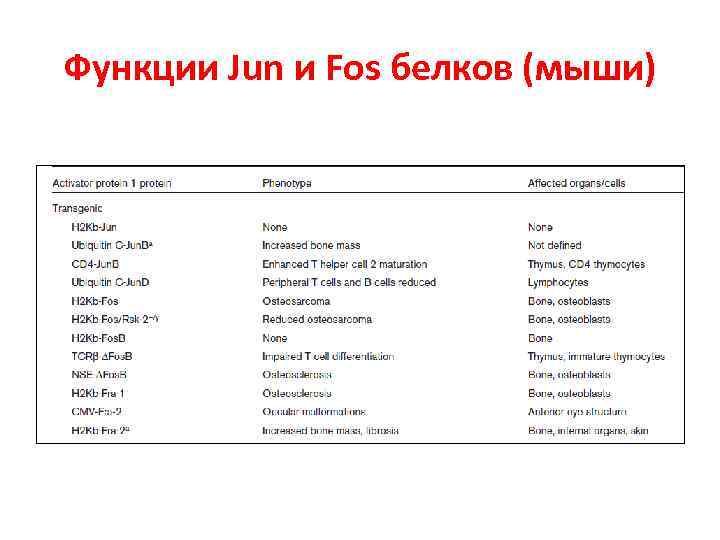
Функции Jun и Fos белков (мыши)

Функции Jun и Fos белков (мыши) продолжение
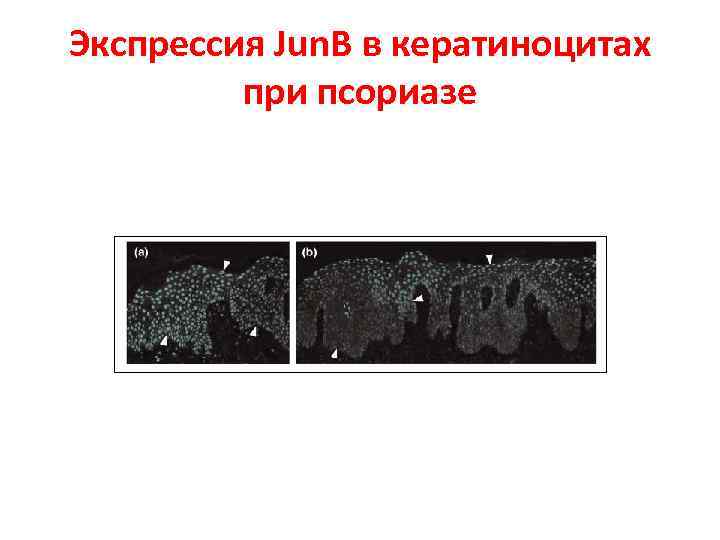
Экспрессия Jun. B в кератиноцитах при псориазе
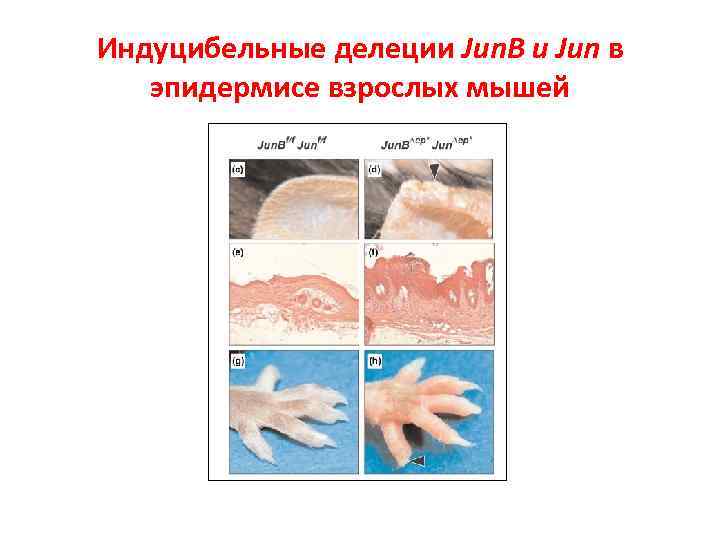
Индуцибельные делеции Jun. B и Jun в эпидермисе взрослых мышей
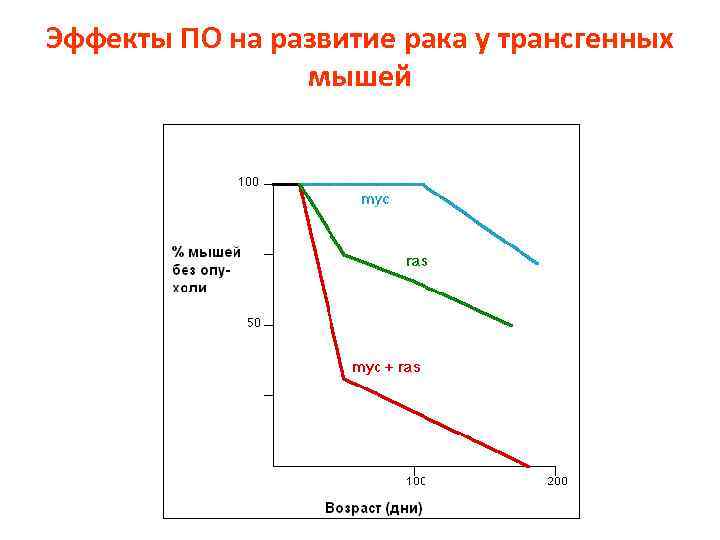
Эффекты ПО на развитие рака у трансгенных мышей
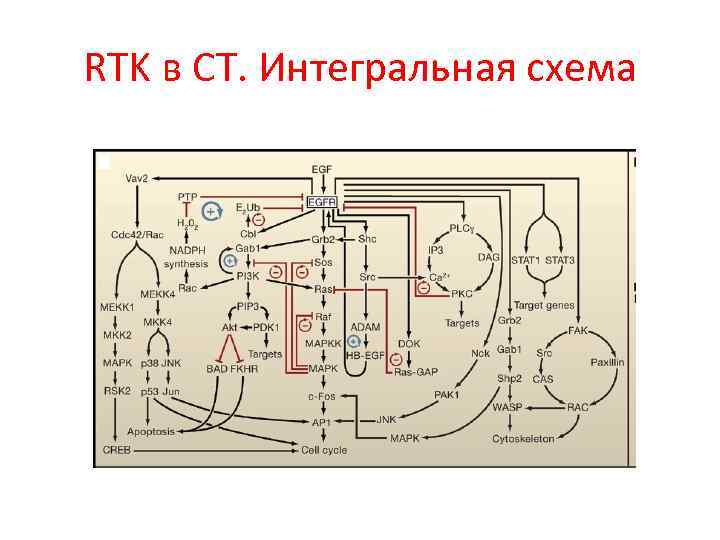
RTK в СТ. Интегральная схема

Мировая статистика рака

• Сигнальные молекулы – мишени в терапии рака
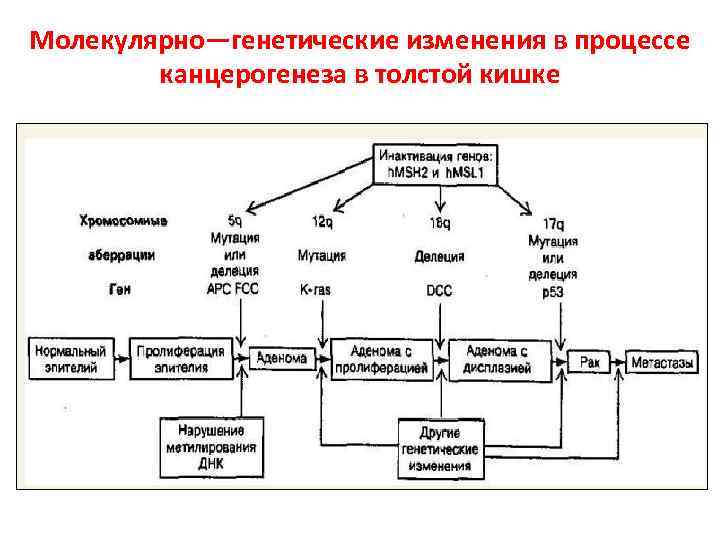
Молекулярно—генетические изменения в процессе канцерогенеза в толстой кишке
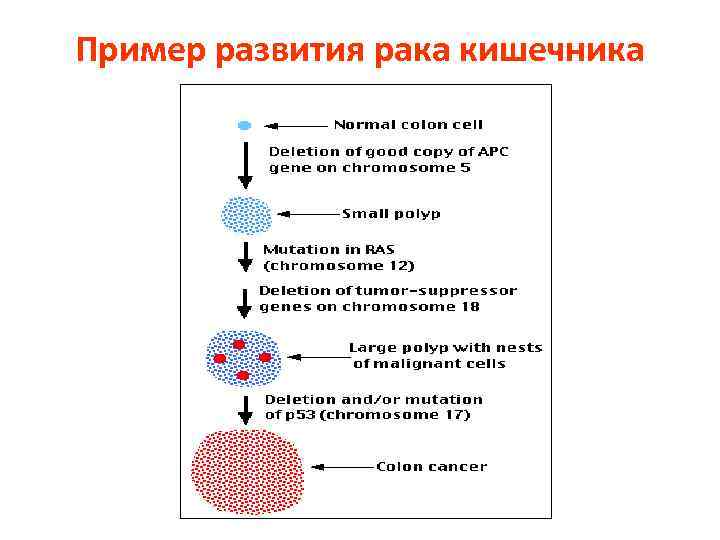
Пример развития рака кишечника
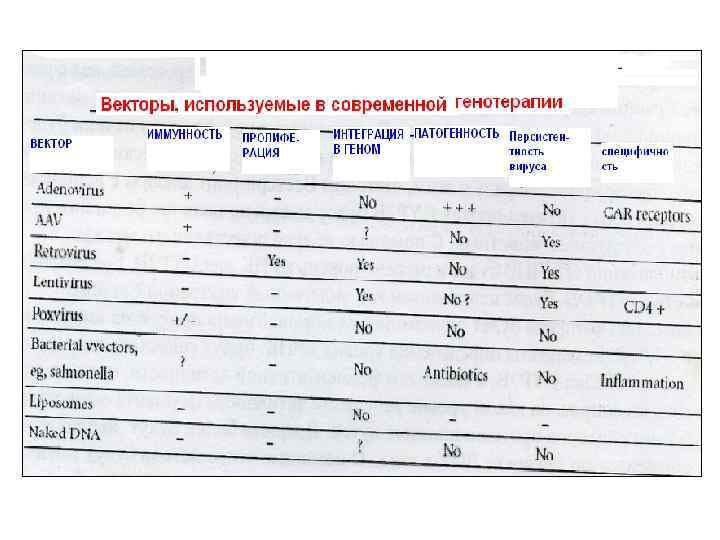
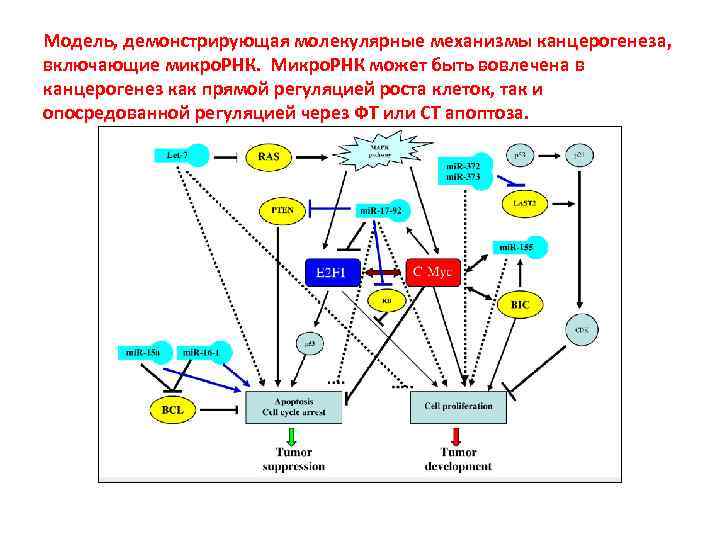
Модель, демонстрирующая молекулярные механизмы канцерогенеза, включающие микро. РНК. Микро. РНК может быть вовлечена в канцерогенез как прямой регуляцией роста клеток, так и опосредованной регуляцией через ФТ или СТ апоптоза.
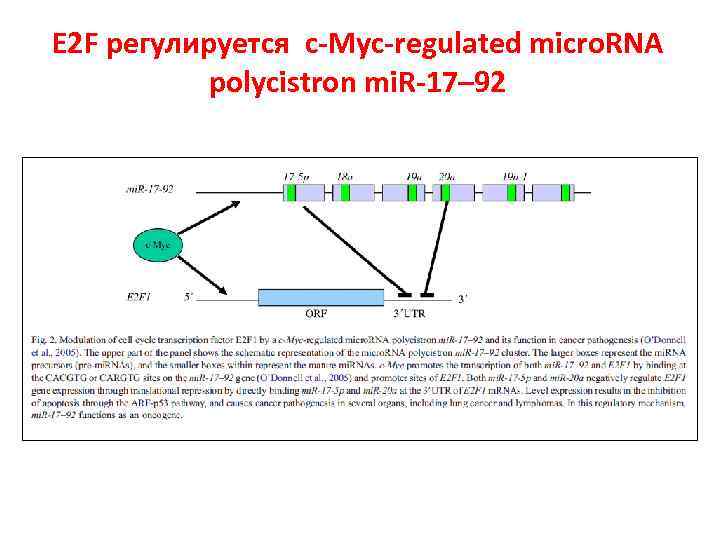
E 2 F регулируется c-Myc-regulated micro. RNA polycistron mi. R-17– 92
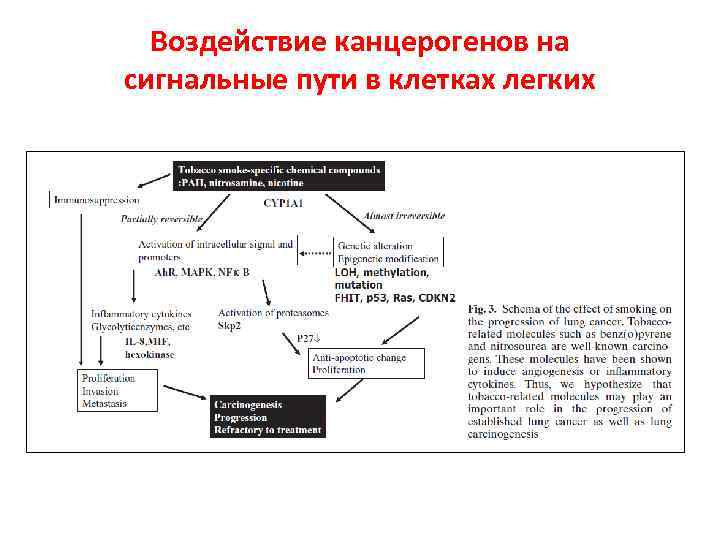
Воздействие канцерогенов на сигнальные пути в клетках легких
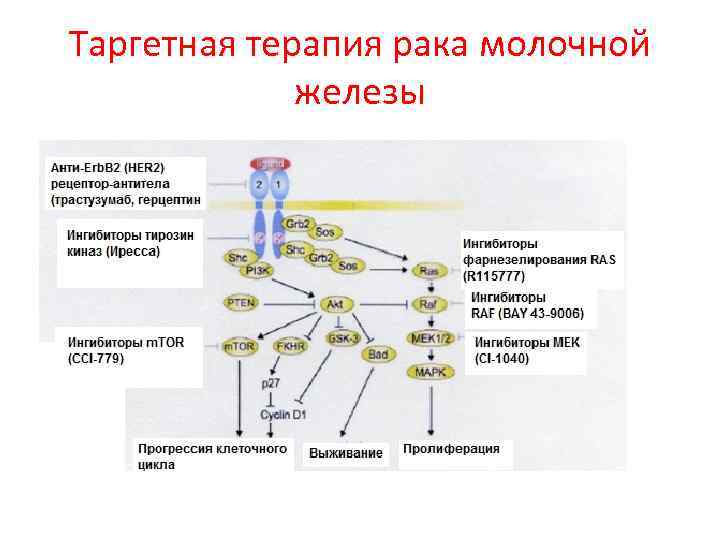
Таргетная терапия рака молочной железы
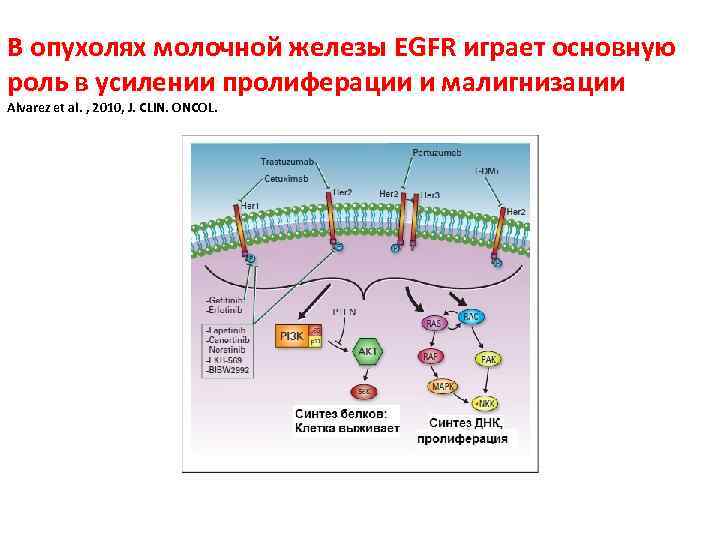
В опухолях молочной железы EGFR играет основную роль в усилении пролиферации и малигнизации Alvarez et al. , 2010, J. CLIN. ONCOL.
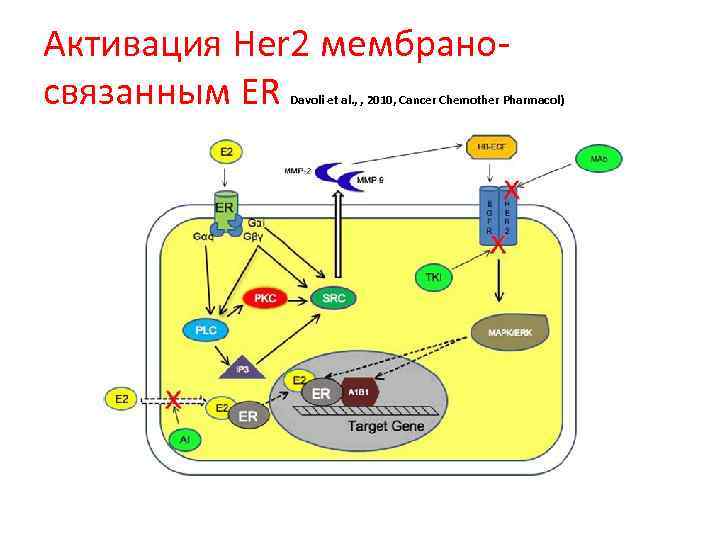
Активация Her 2 мембраносвязанным ER Davoli et al. , , 2010, Cancer Chemother Pharmacol)
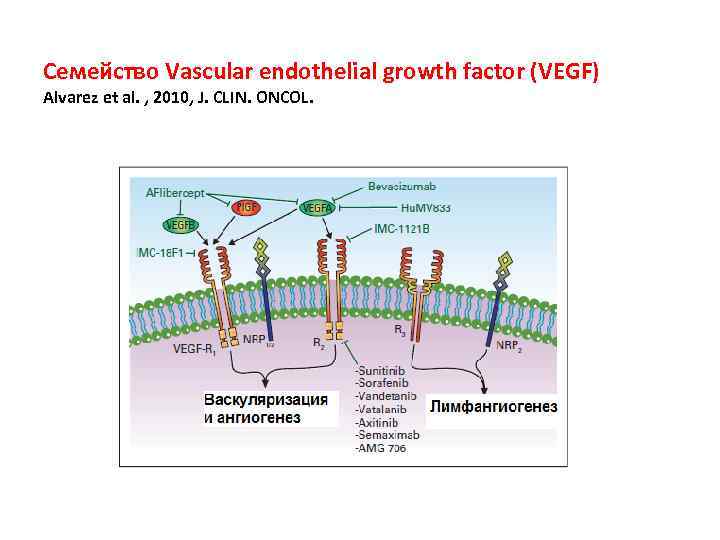
Семейство Vascular endothelial growth factor (VEGF) Alvarez et al. , 2010, J. CLIN. ONCOL.
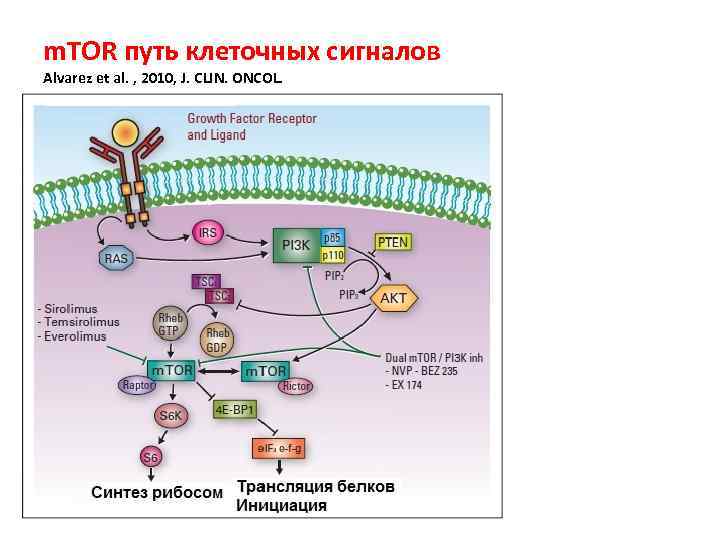
m. TOR путь клеточных сигналов Alvarez et al. , 2010, J. CLIN. ONCOL.

Таргетная терапия в лечении рака легкого • NSCLC – немелкоклеточный рак легкого • • • vascular endothelial growth factor (VEGF) Bevacizumab ингибирует VEGF Cetuximab – Mab против epidermal growth factor receptor (EGFR) Gefitinib и erlotinib - монотерапия
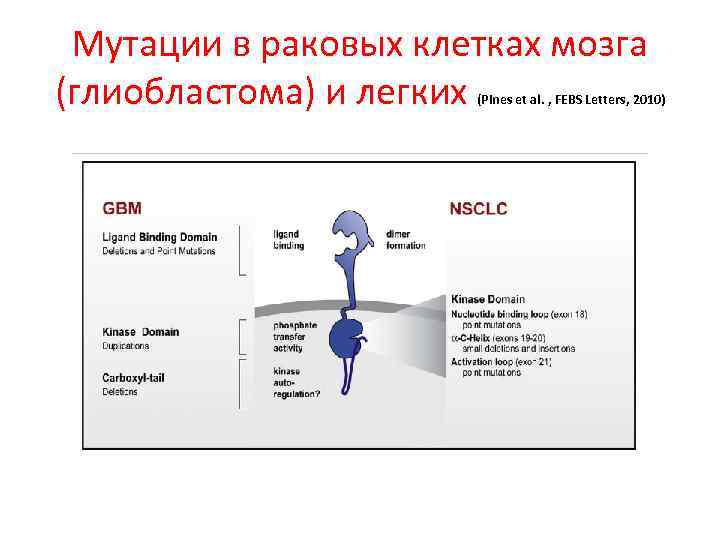
Мутации в раковых клетках мозга (глиобластома) и легких (Pines et al. , FEBS Letters, 2010)

Таргетная терапия EGFR-СТ (Pines et al. , FEBS Letters, 2010)
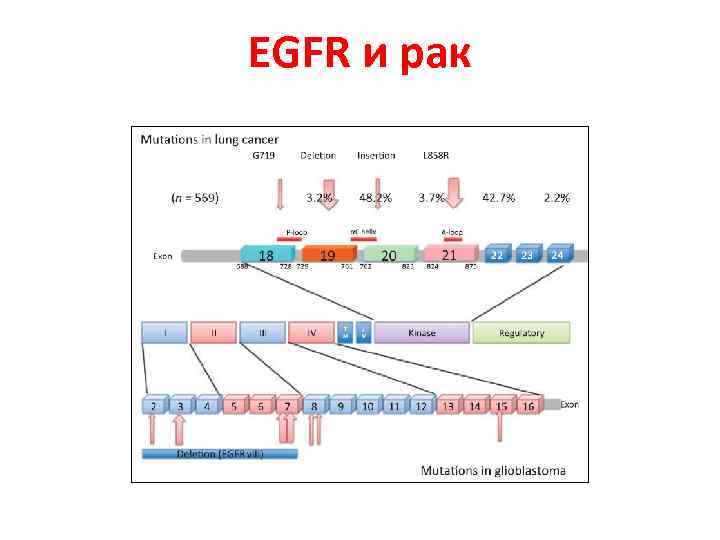
EGFR и рак

Таргетная терапия в лечении рака кишечника • Panitumumab – антитела против EGFR, связывают лиганд-связывающий экстраклеточный домен, ингибируя димеризацию рецептора

Мутации в опухолях кишечника (586 случаев) Kopper L. Pathol. Oncol. Res. (2010) PIK 3 CA KRAS (p 110 каталитическая субъединица ) PI 3 K BRAF 35– 45% <20%, <15% Среди 208 больных, принимавших панитумумаб, 17% с диким типом KRAS показали объективный ответ, но не пациенты с мутациями (84 больных)

Ренальная карцинома • 2 категории терапии: • (1) vascular endothelial growth factor receptor (VEGFR)-направленная терапия • (2) Ингибиторы m. TOR (аналоги рапамицина).
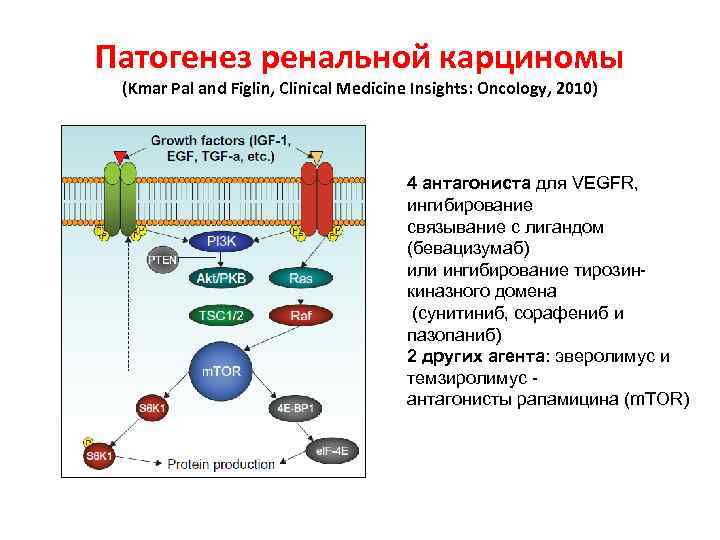
Патогенез ренальной карциномы (Kmar Pal and Figlin, Clinical Medicine Insights: Oncology, 2010) 4 антагониста для VEGFR, ингибирование связывание с лигандом (бевацизумаб) или ингибирование тирозинкиназного домена (сунитиниб, сорафениб и пазопаниб) 2 других агента: эверолимус и темзиролимус антагонисты рапамицина (m. TOR)
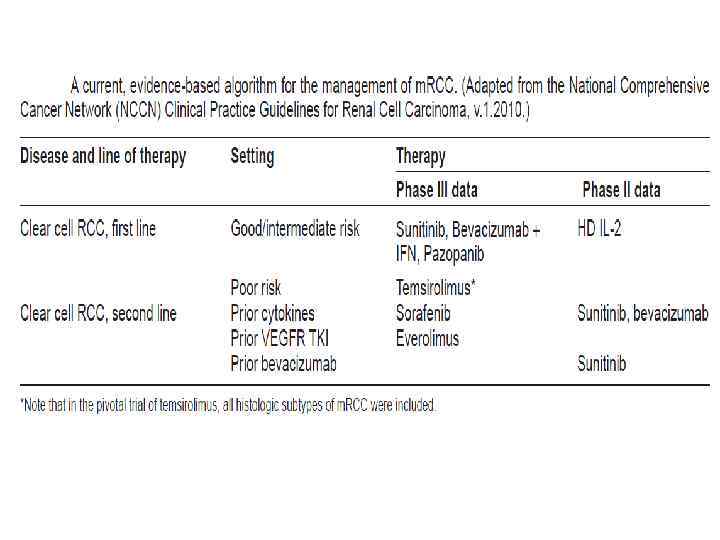
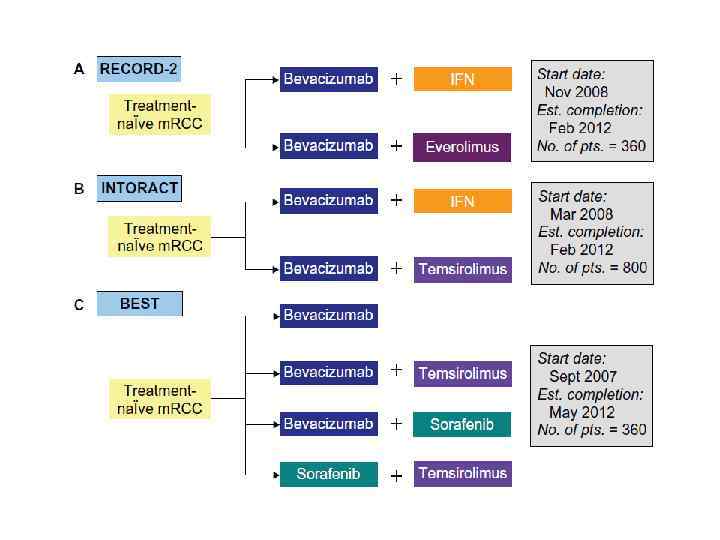

Применение ингибиторов RAF • B-RAF мутации встречаются в 30– 60% меланом, 30– 50% тиреоидного рака, 5– 20% рака кишечника • Ингибиторы RAF киназ (Sorafenib) эффективно блокируют MEK 1/2 и ERK 1/2 активацию в клетках, содержащих онкогенный B-RAF Val 600 Glu (активирующая мутация). • Ингибиторы RAF киназ приводят к парадоксальному увеличению активности RAF в клетках, содержащих дикий тип B-RAF или активированный мутантный RAS. C-RAF играет ключевую роль в усилении MEK-ERK активации.
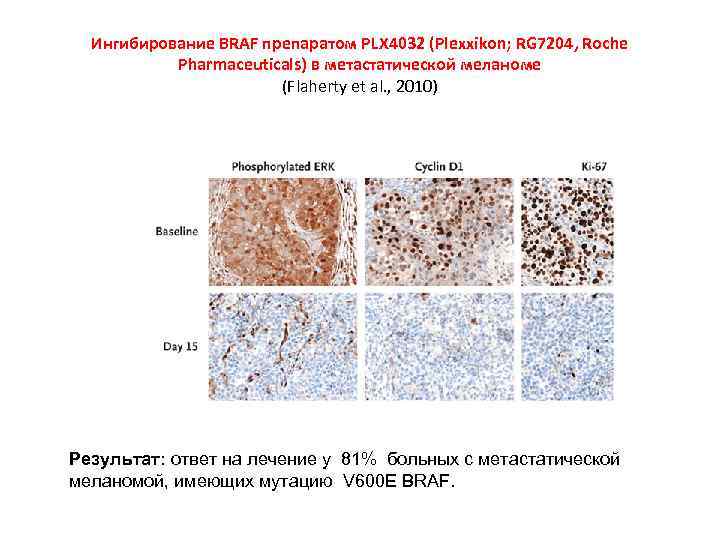
Ингибирование BRAF препаратом PLX 4032 (Plexxikon; RG 7204, Roche Pharmaceuticals) в метастатической меланоме (Flaherty et al. , 2010) Результат: ответ на лечение у 81% больных с метастатической меланомой, имеющих мутацию V 600 E BRAF.
Перспективы изучения СТ Сигнальная трансдукция Фундаментальные механизмы в клеточной биологии Патологии человека (рак, нейродегенеративные болезни и др. ) Применение стволовых клеток в медицине
ММТП часть 5-2. Протоонкогены и СТ.ppt