ЛЕКЦИИ_Химия(2016-17)(2 сем.)4-ТЕРМОДИНАМИКА.ppt
- Количество слайдов: 29
 4. Термодинамика наука, изучающая • превращения (переходы) энергии из одной формы в другую, от одной части системы к другой • энергетические эффекты, сопровождающие физические и химические процессы • возможность, направления и предел самопроизвольного протекания процессов. Химическая термодинамика - термодинамика химических процессов. Описывает статистически значимые процессы (большое число частиц или случаев)
4. Термодинамика наука, изучающая • превращения (переходы) энергии из одной формы в другую, от одной части системы к другой • энергетические эффекты, сопровождающие физические и химические процессы • возможность, направления и предел самопроизвольного протекания процессов. Химическая термодинамика - термодинамика химических процессов. Описывает статистически значимые процессы (большое число частиц или случаев)
 Основные понятия 4. 1 Термодинамическая система m Q>0 Окружающая (внешняя) среда W<0 Термодинамическая система W>0 Q<0 Обмен энергией - E Окружающая среда Передача теплоты - Q Совершение работы - W • изолированные m=0; E=0 • закрытые m=0; E 0 • открытые m 0; E 0
Основные понятия 4. 1 Термодинамическая система m Q>0 Окружающая (внешняя) среда W<0 Термодинамическая система W>0 Q<0 Обмен энергией - E Окружающая среда Передача теплоты - Q Совершение работы - W • изолированные m=0; E=0 • закрытые m=0; E 0 • открытые m 0; E 0
 Термодинамическая система. От свойств и состояния её образующих физических. тел: Гомогенная (однофазная) Гетерогенная (многофазная) фаза 1 фаза 2 граница раздела фаз Фаза: совокупность частей системы с одинаковыми физико- химическими свойствами. Отделена от другой фазы поверхностью раздела(граница раздела фаз)
Термодинамическая система. От свойств и состояния её образующих физических. тел: Гомогенная (однофазная) Гетерогенная (многофазная) фаза 1 фаза 2 граница раздела фаз Фаза: совокупность частей системы с одинаковыми физико- химическими свойствами. Отделена от другой фазы поверхностью раздела(граница раздела фаз)
 Состояние системы Совокупность всех физических и химических свойств системы(состояние системы), определяется основными термодинамическими параметрами (параметрами состояния системы – независимые свойства системы) термодинамические параметры системы : P; T; V; ij; Сij; . . . Термодинамическое равновесие - постулат параметры–const во времени (механическое, термическое и химическое равновесия) Т/д функции состояния системы (определяют через т/д параметры) Внутренняя энергия U Энтальпия H Энтропия S Энергия Гиббса G Энергия Гельмгольца A Уравнение состояния (функциональная зависимость параметров равновесной системы, например, идеального газа) P V = R T ур. Менделеева-Клапейрона
Состояние системы Совокупность всех физических и химических свойств системы(состояние системы), определяется основными термодинамическими параметрами (параметрами состояния системы – независимые свойства системы) термодинамические параметры системы : P; T; V; ij; Сij; . . . Термодинамическое равновесие - постулат параметры–const во времени (механическое, термическое и химическое равновесия) Т/д функции состояния системы (определяют через т/д параметры) Внутренняя энергия U Энтальпия H Энтропия S Энергия Гиббса G Энергия Гельмгольца A Уравнение состояния (функциональная зависимость параметров равновесной системы, например, идеального газа) P V = R T ур. Менделеева-Клапейрона
 4. 2 Термодинамический процесс (изменяется хотя бы один из параметров равновесной системы) Внешнее воздействие: E, i время -t Состояние равновесия 1 T 1; P 1; V 1; i 1 Термодинамический процесс - (переход) из состояния равновесия 1 в 2 время - Состояние равновесия 2 T 2; P 2; V 2; i 2 самопроизвольный Термодинамический процесс (не требуют внешних затрат энергии) переход теплоты от нагретого тела к холодному несамопроизвольный (вынужденный) – разделение газовой смеси
4. 2 Термодинамический процесс (изменяется хотя бы один из параметров равновесной системы) Внешнее воздействие: E, i время -t Состояние равновесия 1 T 1; P 1; V 1; i 1 Термодинамический процесс - (переход) из состояния равновесия 1 в 2 время - Состояние равновесия 2 T 2; P 2; V 2; i 2 самопроизвольный Термодинамический процесс (не требуют внешних затрат энергии) переход теплоты от нагретого тела к холодному несамопроизвольный (вынужденный) – разделение газовой смеси
 Термодинамический процесс (при постоянстве одного из т/д параметра) изотермический -Т=const изохорический - V=const изобарический -Р= const Термодин. процесс по характеру перехода из состояний равновесия равновесный (обратимый); t - время воздействия, τ- время установления равновесия (релаксаци) τ τ t - бесконечная последовательность отдельных состояний равновесия неравновесный (необратимый) t
Термодинамический процесс (при постоянстве одного из т/д параметра) изотермический -Т=const изохорический - V=const изобарический -Р= const Термодин. процесс по характеру перехода из состояний равновесия равновесный (обратимый); t - время воздействия, τ- время установления равновесия (релаксаци) τ τ t - бесконечная последовательность отдельных состояний равновесия неравновесный (необратимый) t
 Термодинамический процесс (t-время воздействия на систему, τ-время перехода системы в новое сост. равновесия) Равновесный(обратимый)процесс Неравновесный(необратимый) процесс t t W 12 < Wравн W 21 > Wравн W равн = W 12 = W 21 Р Р 1 (1) T-const Равновесие(1 -2 -1) P∙V = ·R·T d. W P d. V R T d. V V mg V 2 W R T P 2, V 2, T (2) Р 2 P 1, V 1, T V 1 V 2 V 1 V d. V V
Термодинамический процесс (t-время воздействия на систему, τ-время перехода системы в новое сост. равновесия) Равновесный(обратимый)процесс Неравновесный(необратимый) процесс t t W 12 < Wравн W 21 > Wравн W равн = W 12 = W 21 Р Р 1 (1) T-const Равновесие(1 -2 -1) P∙V = ·R·T d. W P d. V R T d. V V mg V 2 W R T P 2, V 2, T (2) Р 2 P 1, V 1, T V 1 V 2 V 1 V d. V V
 Химическая реакция а A + b B с C + d D продукты исходные вещества(реагенты) реакции количество исходных веществ уменьшается количество продуктов увеличивается-прямая реакция количество продуктов уменьшается количество исходных веществ увеличиваетсяобратная реакция C + D A + B с d а b
Химическая реакция а A + b B с C + d D продукты исходные вещества(реагенты) реакции количество исходных веществ уменьшается количество продуктов увеличивается-прямая реакция количество продуктов уменьшается количество исходных веществ увеличиваетсяобратная реакция C + D A + B с d а b
 4. 3 Первое начало термодинамики (закон сохранения энергии) - Джеймс Джоуль Теплота ( Q), сообщенная термодинамической системе, идет на увеличение внутренней энергии ( U) системы и на совершение системой работы( W). Q Q = U + W U Термодинамическая система T; P; V; Сi Q = d. U + W W Q = d. U + P d. V
4. 3 Первое начало термодинамики (закон сохранения энергии) - Джеймс Джоуль Теплота ( Q), сообщенная термодинамической системе, идет на увеличение внутренней энергии ( U) системы и на совершение системой работы( W). Q Q = U + W U Термодинамическая система T; P; V; Сi Q = d. U + W W Q = d. U + P d. V
 Т/Д функции состояния I. Внутренняя энергия U U - это сумма всех видов энергии ТДС, за исключением кинетической и потенциальной энергии системы в целом. U [к. Дж]; [к. Дж моль], [ к. Дж кг] U функция состояния системы беск. мал. изменение –полн. дифф-л к (d. U) U к U Внутренняя энергия ΔU d. U н в химическом процессе н U-изменение 2 -х составл. Химическая(Е связей) Тепловая(кинет. Е) d. U 0 для кругового процесса Величину U характеризует Т. Если Т 2 > Т 1, то UТ 2 >UТ 1 Термодинамическая шкала температур Т, К > 0
Т/Д функции состояния I. Внутренняя энергия U U - это сумма всех видов энергии ТДС, за исключением кинетической и потенциальной энергии системы в целом. U [к. Дж]; [к. Дж моль], [ к. Дж кг] U функция состояния системы беск. мал. изменение –полн. дифф-л к (d. U) U к U Внутренняя энергия ΔU d. U н в химическом процессе н U-изменение 2 -х составл. Химическая(Е связей) Тепловая(кинет. Е) d. U 0 для кругового процесса Величину U характеризует Т. Если Т 2 > Т 1, то UТ 2 >UТ 1 Термодинамическая шкала температур Т, К > 0
 II. Энтальпия (теплосодержание системы) Q = d. U + W W = P d. V Q V = U V =const P =const Q = d. U + P d. V QP = U+ P V Н= U + P V – энтальпия [к. Дж]; [к. Дж моль], [к. Дж кг] Q V = d. U QP = d. U + P d. V QP = d(U + P V) QP = d. Н
II. Энтальпия (теплосодержание системы) Q = d. U + W W = P d. V Q V = U V =const P =const Q = d. U + P d. V QP = U+ P V Н= U + P V – энтальпия [к. Дж]; [к. Дж моль], [к. Дж кг] Q V = d. U QP = d. U + P d. V QP = d(U + P V) QP = d. Н
 Тепловой эффект химической реакции Э - то количество теплоты Q при условии экзо термические Хим ическая реакция Q процесс необратим при P =const или V=const только работа расширения Т-одинакова для реагентов и продуктов реакции эндо термические Изохорный тепловой эффект химической реакции - QV = r U Изобарный тепловой эффект химической реакции - QP = r Н r. Н - экзотермические реакции(+Q) 0 r. Н - эндотермические реакции(-Q) 0
Тепловой эффект химической реакции Э - то количество теплоты Q при условии экзо термические Хим ическая реакция Q процесс необратим при P =const или V=const только работа расширения Т-одинакова для реагентов и продуктов реакции эндо термические Изохорный тепловой эффект химической реакции - QV = r U Изобарный тепловой эффект химической реакции - QP = r Н r. Н - экзотермические реакции(+Q) 0 r. Н - эндотермические реакции(-Q) 0
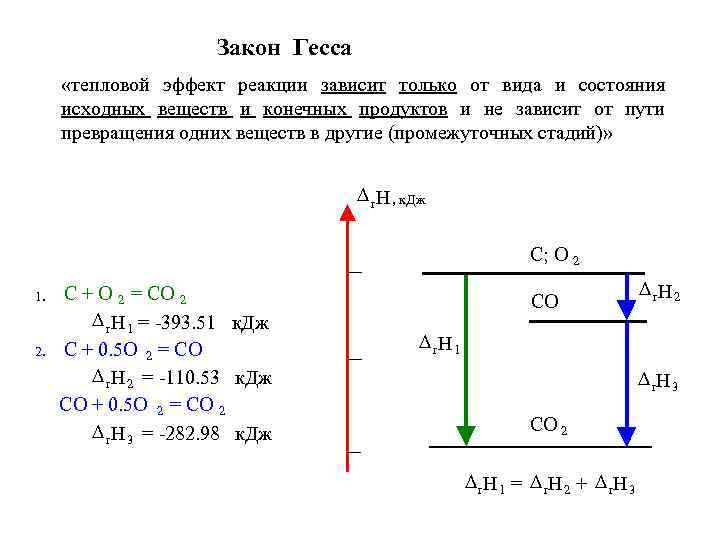 Закон Гесса «тепловой эффект реакции зависит только от вида и состояния исходных веществ и конечных продуктов и не зависит от пути превращения одних веществ в другие (промежуточных стадий)» r. Н , к. Дж C; O 2 C + O 2 = CO 2 r. Н 1 = -393. 51 к. Дж 2. C + 0. 5 O 2 = CO r. Н 2 = -110. 53 к. Дж CO + 0. 5 O 2 = CO 2 r. Н 3 = -282. 98 к. Дж 1. CO r. Н 2 r. Н 1 r. Н 3 CO 2 r. Н 1 = r. Н 2 + r. Н 3
Закон Гесса «тепловой эффект реакции зависит только от вида и состояния исходных веществ и конечных продуктов и не зависит от пути превращения одних веществ в другие (промежуточных стадий)» r. Н , к. Дж C; O 2 C + O 2 = CO 2 r. Н 1 = -393. 51 к. Дж 2. C + 0. 5 O 2 = CO r. Н 2 = -110. 53 к. Дж CO + 0. 5 O 2 = CO 2 r. Н 3 = -282. 98 к. Дж 1. CO r. Н 2 r. Н 1 r. Н 3 CO 2 r. Н 1 = r. Н 2 + r. Н 3
 Термохимические уравнения (включают тепловой эффект реакции) 4 Al + 3 O 2 = 2 Al 2 O 3 + r. Н = -3352. 2 [к. Дж] 2 Al + 3 2 O 2 = 1 Al 2 O 3 + f. Н = -1676, 1 [ к. Дж моль] Превращение одного моля f Н - образование одного моля в-ва 1 Al + 3 4 O 2 = 1 2 Al 2 O 3 + c. Н = -838, 05 [к. Дж моль] c. Н – сгорание одного моля в-ва
Термохимические уравнения (включают тепловой эффект реакции) 4 Al + 3 O 2 = 2 Al 2 O 3 + r. Н = -3352. 2 [к. Дж] 2 Al + 3 2 O 2 = 1 Al 2 O 3 + f. Н = -1676, 1 [ к. Дж моль] Превращение одного моля f Н - образование одного моля в-ва 1 Al + 3 4 O 2 = 1 2 Al 2 O 3 + c. Н = -838, 05 [к. Дж моль] c. Н – сгорание одного моля в-ва
 Термохимические расчеты (расчет тепловых эффектов реакций) Стандартная (молярная) энтальпия образования • Стандартные условия: Р 0 = 1, 013 105 Па Т 0 = 298, 15 К С 0 = 1 моль/л r. Н 0298 стандартная энтальпия(тепловой эффект) хим. реакции f. Н 0298 –Стандартная энтальпия образования веществ: 1. простые в-ва f. Н 0298= 0 к. Дж/моль 2. сложные в-ва f. Н 0298= - QР к. Дж/моль 1/2 А 2 + 1/2 В 2 = АВ + f. Н 0298 1. Газообразный водород f. Н 0298= 0 к. Дж/моль. 2. Ртуть жидкость f. Н 0298= 0 к. Дж/моль. 3. Углерод твердый графит f. Н 0298 = 0 к. Дж/моль, алмаз f. Н 0298 = 1, 83 к. Дж/моль 2. При сгорании сложных веществ – продукты окисления СО 2 , Н 2 О, HHal, N 2, Mex. Oy 1.
Термохимические расчеты (расчет тепловых эффектов реакций) Стандартная (молярная) энтальпия образования • Стандартные условия: Р 0 = 1, 013 105 Па Т 0 = 298, 15 К С 0 = 1 моль/л r. Н 0298 стандартная энтальпия(тепловой эффект) хим. реакции f. Н 0298 –Стандартная энтальпия образования веществ: 1. простые в-ва f. Н 0298= 0 к. Дж/моль 2. сложные в-ва f. Н 0298= - QР к. Дж/моль 1/2 А 2 + 1/2 В 2 = АВ + f. Н 0298 1. Газообразный водород f. Н 0298= 0 к. Дж/моль. 2. Ртуть жидкость f. Н 0298= 0 к. Дж/моль. 3. Углерод твердый графит f. Н 0298 = 0 к. Дж/моль, алмаз f. Н 0298 = 1, 83 к. Дж/моль 2. При сгорании сложных веществ – продукты окисления СО 2 , Н 2 О, HHal, N 2, Mex. Oy 1.
 Следствие из закона Гесса: r. Н 0298 = ( i f. Н 0 i)продукты – ( i f. Н 0 i)исходные вещества Для реакции а. A + b. B = с. C + d. D r. Н 0298 = ( c f. Н 0 C + d f. Н 0 D ) – ( a f. Н 0 A + b f. Н 0 B) Пример. реакция : CH 4 (газ) + CO 2 (газ) = 2 CO (газ) + 2 H 2 (газ) f. Н 0298, к. Дж/моль – 74, 85 – 393, 51 – 110, 5 0 Расчет теплового эффекта реакции: r. Н 0298 = [2 (– 110, 5) + 2 0] – [(– 74, 85) + (– 393, 51)] = 247, 36 [к. Дж]
Следствие из закона Гесса: r. Н 0298 = ( i f. Н 0 i)продукты – ( i f. Н 0 i)исходные вещества Для реакции а. A + b. B = с. C + d. D r. Н 0298 = ( c f. Н 0 C + d f. Н 0 D ) – ( a f. Н 0 A + b f. Н 0 B) Пример. реакция : CH 4 (газ) + CO 2 (газ) = 2 CO (газ) + 2 H 2 (газ) f. Н 0298, к. Дж/моль – 74, 85 – 393, 51 – 110, 5 0 Расчет теплового эффекта реакции: r. Н 0298 = [2 (– 110, 5) + 2 0] – [(– 74, 85) + (– 393, 51)] = 247, 36 [к. Дж]
![Зависимость теплового эффекта реакции от температуры cp – молярная изобарная теплоемкость [Дж/моль. К] Если Зависимость теплового эффекта реакции от температуры cp – молярная изобарная теплоемкость [Дж/моль. К] Если](https://present5.com/presentation/-126646561_442057130/image-17.jpg) Зависимость теплового эффекта реакции от температуры cp – молярная изобарная теплоемкость [Дж/моль. К] Если в интервале Т 1 - Т 2 фазовые переходы: плавление Тпл, кипение Ткип m. Н 0 [к. Дж/моль] – энтальпия плавления v. Н 0 [к. Дж/моль] – энтальпия испарения čр - const HТ 2 – HТ 1 = čр (T 2 – T 1) cp(Т) = а + b Т + c Т 2 +…
Зависимость теплового эффекта реакции от температуры cp – молярная изобарная теплоемкость [Дж/моль. К] Если в интервале Т 1 - Т 2 фазовые переходы: плавление Тпл, кипение Ткип m. Н 0 [к. Дж/моль] – энтальпия плавления v. Н 0 [к. Дж/моль] – энтальпия испарения čр - const HТ 2 – HТ 1 = čр (T 2 – T 1) cp(Т) = а + b Т + c Т 2 +…
 пример - Н 2 О f. H T (cp) пар v. H (cp) жидкость f. H 0 (cp) лед T 1 m. H 273 298 373 T 2 Т, К
пример - Н 2 О f. H T (cp) пар v. H (cp) жидкость f. H 0 (cp) лед T 1 m. H 273 298 373 T 2 Т, К
 Второе начало термодинамики Q 1 Q 2 T 1 T 2 Q 1 T 1 δQ 1 δQ 2 0 T 1 T 2 η d. Qравн T Q 1 Q 2 0 T 1 T 2 0 Под интегралом - функция состояния S=Q равн/T – энтропия (Рудольф Клаузиус) Qнеравн Qравн d. U = Q + W d. Uравн=d. Uнеравн Wнеравн < Wравн d. U + p d. V -T d. S 0 - 1 -ое начало, d. U=d. V=0 → Td. S≥ 0 → d. S≥ 0 в изолированной системе самопроизвольно протекают процессы с увеличением энтропии (d. S При равновесии - S максимальна (d. S = 0) > 0)
Второе начало термодинамики Q 1 Q 2 T 1 T 2 Q 1 T 1 δQ 1 δQ 2 0 T 1 T 2 η d. Qравн T Q 1 Q 2 0 T 1 T 2 0 Под интегралом - функция состояния S=Q равн/T – энтропия (Рудольф Клаузиус) Qнеравн Qравн d. U = Q + W d. Uравн=d. Uнеравн Wнеравн < Wравн d. U + p d. V -T d. S 0 - 1 -ое начало, d. U=d. V=0 → Td. S≥ 0 → d. S≥ 0 в изолированной системе самопроизвольно протекают процессы с увеличением энтропии (d. S При равновесии - S максимальна (d. S = 0) > 0)
 I W 1= 1 II ловинам (макросостояния системы) Wi – число способов (микросостояний) W 2= 4 III IV III. Энтропия и т/д вероятность I – V варианты распределения по двум по- реализации макросостояний ΣWi=16 - всего способов размещения 4 -х молекул по двум половинам W 3= 6 P=6/16 математическая вероятность Max W 3=6 W – термодинамическая вероятность W 4= 4 0≤P≤ 1 V W 5= 1 1≤W≤∞
I W 1= 1 II ловинам (макросостояния системы) Wi – число способов (микросостояний) W 2= 4 III IV III. Энтропия и т/д вероятность I – V варианты распределения по двум по- реализации макросостояний ΣWi=16 - всего способов размещения 4 -х молекул по двум половинам W 3= 6 P=6/16 математическая вероятность Max W 3=6 W – термодинамическая вероятность W 4= 4 0≤P≤ 1 V W 5= 1 1≤W≤∞
 Энтропия. Уравнение Больцмана S = k ln. W k = 1, 38 10 -23 Дж К – константа Больцмана (k = R/NА) W – термодинамическая вероятность состояния системы число микросостояний, которым можно реализовать данное макросостояние системы W 1 Второе начало термодинамики В изолированной системе самопроизвольно идут только процессы в которых реализуется более вероятное состояние системы, т. е. процессы сопровождающиеся увеличением термодинамической вероятности W и следовательно энтропии S. Т. о. в изолированной системе для самопроизвольного процесса ΔS>0
Энтропия. Уравнение Больцмана S = k ln. W k = 1, 38 10 -23 Дж К – константа Больцмана (k = R/NА) W – термодинамическая вероятность состояния системы число микросостояний, которым можно реализовать данное макросостояние системы W 1 Второе начало термодинамики В изолированной системе самопроизвольно идут только процессы в которых реализуется более вероятное состояние системы, т. е. процессы сопровождающиеся увеличением термодинамической вероятности W и следовательно энтропии S. Т. о. в изолированной системе для самопроизвольного процесса ΔS>0
 Второе начало термодинамики В изолированной системе самопроизвольно будут протекать процессы с увеличением термодинамической вероятности, а состояние равновесия соответствует состоянию с максимальной вероятностью. *Энтропия идеального кристалла при 0 К равна нулю -3 -е начало термодинамики (Постулат Планка), поэтому энтропия любого вeщества абсолютна и положительна 2 -е начало т/д описывает системы: • число частиц должно быть велико, статистически значимо(>1012 -1014) • число частиц – конечно • не распространяется на неограниченную(бесконечную) систему [W становится неопределенной(бесконечное число состояний)]
Второе начало термодинамики В изолированной системе самопроизвольно будут протекать процессы с увеличением термодинамической вероятности, а состояние равновесия соответствует состоянию с максимальной вероятностью. *Энтропия идеального кристалла при 0 К равна нулю -3 -е начало термодинамики (Постулат Планка), поэтому энтропия любого вeщества абсолютна и положительна 2 -е начало т/д описывает системы: • число частиц должно быть велико, статистически значимо(>1012 -1014) • число частиц – конечно • не распространяется на неограниченную(бесконечную) систему [W становится неопределенной(бесконечное число состояний)]
![Факторы влияющие на величину энтропии S [Дж К] [Дж моль К] стандартная - S Факторы влияющие на величину энтропии S [Дж К] [Дж моль К] стандартная - S](https://present5.com/presentation/-126646561_442057130/image-23.jpg) Факторы влияющие на величину энтропии S [Дж К] [Дж моль К] стандартная - S 0298 • Фазовый переход • Состав, структура Фаза S 0298, Дж моль К лед 39, 33 жидкая вода 69, 95 водяной пар 188, 72 • Химическая реакция r. S 0 = ( i S 0 i)продукты – ( i S 0 i)исх. вещества • Температура d. S=δQ/T δQ=cd. T d. S=c d. T/T
Факторы влияющие на величину энтропии S [Дж К] [Дж моль К] стандартная - S 0298 • Фазовый переход • Состав, структура Фаза S 0298, Дж моль К лед 39, 33 жидкая вода 69, 95 водяной пар 188, 72 • Химическая реакция r. S 0 = ( i S 0 i)продукты – ( i S 0 i)исх. вещества • Температура d. S=δQ/T δQ=cd. T d. S=c d. T/T
 IV. Энергия Гиббса. Направление химического процесса T d. S d. U + p d. V -T d. S 0 d. U + p d. V - T d. S < 0 - самопр. процесс d. U + p d. V - T d. S =0 - равновесие • Изобарно-изотермический процесс (p–const, Т–const). d. U + p d. V - T d. S 0 d. H – T d. S = d(H – T S) = d. G 0 G H – T S - энергия Гиббса [к. Дж; к. Дж моль] • Изохорно-изотермический процесс (V–const, Т–const). d. U - T d. S = d(U – T S) = d. А 0 A U – T S - энергия Гельмгольца [к. Дж; к. Дж моль]
IV. Энергия Гиббса. Направление химического процесса T d. S d. U + p d. V -T d. S 0 d. U + p d. V - T d. S < 0 - самопр. процесс d. U + p d. V - T d. S =0 - равновесие • Изобарно-изотермический процесс (p–const, Т–const). d. U + p d. V - T d. S 0 d. H – T d. S = d(H – T S) = d. G 0 G H – T S - энергия Гиббса [к. Дж; к. Дж моль] • Изохорно-изотермический процесс (V–const, Т–const). d. U - T d. S = d(U – T S) = d. А 0 A U – T S - энергия Гельмгольца [к. Дж; к. Дж моль]
 Стандартная энергия Гиббса (образования) вещества ΔG 0298 Энергия Гиббса реакции r. G 0298 = ( i f. G 0 i)продукты – ( i f. G 0 i)исходные вещества а. A + b. B = с. C + d. D r. G 0= ( c f. G 0 C + d f. G 0 D) – ( a f. G 0 A + b f. G 0 B) r. G 0298= f. H 0 i – 298 r. S 0 r. G 0 298 = [ i ( f. H 0 i – 298 S 0 i]продукты –[ i( f. H 0 i – 298 S 0 i]исходные вещества= = [( i f. Н 0 i)прод. –( i f. Н 0 i)исх. в. ]– 298 [( i S 0 i)прод. – ( i S 0 i)исх. в. ] = r. G 0298 = r. H 0 – 298 r. S 0
Стандартная энергия Гиббса (образования) вещества ΔG 0298 Энергия Гиббса реакции r. G 0298 = ( i f. G 0 i)продукты – ( i f. G 0 i)исходные вещества а. A + b. B = с. C + d. D r. G 0= ( c f. G 0 C + d f. G 0 D) – ( a f. G 0 A + b f. G 0 B) r. G 0298= f. H 0 i – 298 r. S 0 r. G 0 298 = [ i ( f. H 0 i – 298 S 0 i]продукты –[ i( f. H 0 i – 298 S 0 i]исходные вещества= = [( i f. Н 0 i)прод. –( i f. Н 0 i)исх. в. ]– 298 [( i S 0 i)прод. – ( i S 0 i)исх. в. ] = r. G 0298 = r. H 0 – 298 r. S 0
 Температурная зависимость r. G(T) r. H 0 – T r. S 0 r. G(T) = r. H(T) – T r. S(T) r. G 0 - самопроизвольный процесс r. G(T) r. H 0 – T r. S 0 0 энтальпийный и энтропийный факторы Направление протекания химической реакции r. G 0 при любой Т r. S 0 0 r. H 0 0 r. G 0 при r. S 0 0 r. H 0 0 r. S 0 0 r. G 0 при любой Т
Температурная зависимость r. G(T) r. H 0 – T r. S 0 r. G(T) = r. H(T) – T r. S(T) r. G 0 - самопроизвольный процесс r. G(T) r. H 0 – T r. S 0 0 энтальпийный и энтропийный факторы Направление протекания химической реакции r. G 0 при любой Т r. S 0 0 r. H 0 0 r. G 0 при r. S 0 0 r. H 0 0 r. S 0 0 r. G 0 при любой Т
 Энергия Гиббса реакции в нестандартных условиях реакция а. A + b. B = с. C + d. D r. G 0 = ( c f. G 0 C + d f. G 0 D ) – ( a f. G 0 A + b f. G 0 B ) С 0 =1 моль/л С С 0 r. Gi = r. G 0 i + R T ln. Ci – безразмерная концентрация – мольная доля; Сi – [ моль/л ] – относительное парциальное давление [атм], p 0 =1, 013. 105 Па r. G = ( c f. G 0 C+ d f. G 0 D ) – ( a f. G 0 A+ b f. G 0 B) + R T ( c ln. СC+ d ln. CD– a ln. CA– b ln. CB)
Энергия Гиббса реакции в нестандартных условиях реакция а. A + b. B = с. C + d. D r. G 0 = ( c f. G 0 C + d f. G 0 D ) – ( a f. G 0 A + b f. G 0 B ) С 0 =1 моль/л С С 0 r. Gi = r. G 0 i + R T ln. Ci – безразмерная концентрация – мольная доля; Сi – [ моль/л ] – относительное парциальное давление [атм], p 0 =1, 013. 105 Па r. G = ( c f. G 0 C+ d f. G 0 D ) – ( a f. G 0 A+ b f. G 0 B) + R T ( c ln. СC+ d ln. CD– a ln. CA– b ln. CB)
 4. 7 Равновесие Стандартная(термодинамическая) константа равновесия хим. реакции r. G 0 T + R T ln. K 0 = 0 r. G 0 T = r. Н 0 T – Т r. S 0 T
4. 7 Равновесие Стандартная(термодинамическая) константа равновесия хим. реакции r. G 0 T + R T ln. K 0 = 0 r. G 0 T = r. Н 0 T – Т r. S 0 T
 Сдвиг равновесия Изобара реакции Р-const r. Н 0 0 (экзотермич. реакция) – ln. K 0 - убывающая функция r. Н 0 0 (эндотермич. реакция) – ln. K 0 - возрастающая функция Изотерма реакции T-const r. G 0 T = – R T ln. K 0 r. G<0 r. G>0 r. G=0
Сдвиг равновесия Изобара реакции Р-const r. Н 0 0 (экзотермич. реакция) – ln. K 0 - убывающая функция r. Н 0 0 (эндотермич. реакция) – ln. K 0 - возрастающая функция Изотерма реакции T-const r. G 0 T = – R T ln. K 0 r. G<0 r. G>0 r. G=0


