Л 3 Фураны 2012.ppt
- Количество слайдов: 36
 4 курс - 2012 Лекция 3 Гетероциклические лекарственные средства. Производные фурана
4 курс - 2012 Лекция 3 Гетероциклические лекарственные средства. Производные фурана
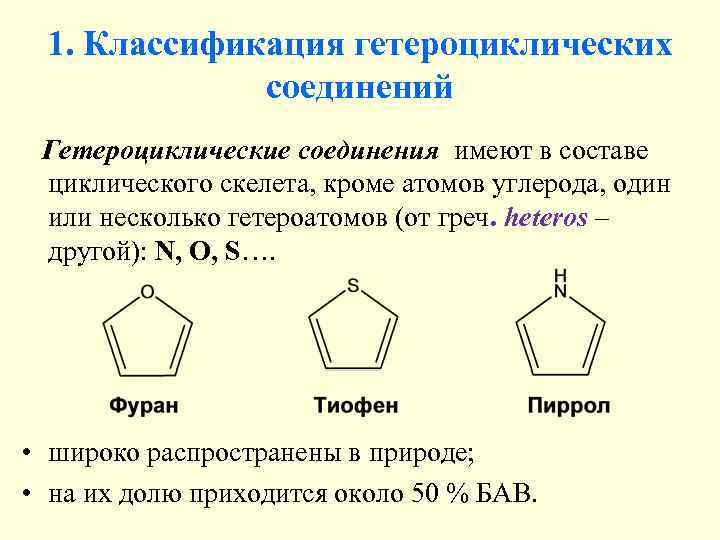 1. Классификация гетероциклических соединений Гетероциклические соединения имеют в составе циклического скелета, кроме атомов углерода, один или несколько гетероатомов (от греч. heteros – другой): N, O, S…. • широко распространены в природе; • на их долю приходится около 50 % БАВ.
1. Классификация гетероциклических соединений Гетероциклические соединения имеют в составе циклического скелета, кроме атомов углерода, один или несколько гетероатомов (от греч. heteros – другой): N, O, S…. • широко распространены в природе; • на их долю приходится около 50 % БАВ.
 Гетероциклы различаются: • Природой гетероатома. • Числом гетероатомов в цикле: • Положением гетероатомов в цикле (структурная изомерия):
Гетероциклы различаются: • Природой гетероатома. • Числом гетероатомов в цикле: • Положением гетероатомов в цикле (структурная изомерия):
 • Размером цикла (число атомных звеньев в цикле):
• Размером цикла (число атомных звеньев в цикле):
 Краунэфиры – макрогетероциклические соединения, содержащие в своих циклах более 11 атомов, из которых не менее четырёх — гетероатомы, которые связаны между собой этиленовыми мостиками формула I — 12 -краун-4; (1, 4, 7, 10 тетраоксоциклододекан) формула II — 1, 10 -диаза-18 -краун-6; (1, 4, 10, 13 -тетраокса-7, 16 диазациклооктадекан) формула III — 1, 7 -дитиа-15 -краун-5 формула IV — дибензо-18 -краун-6 формула V — циклогексано-15 -краун-5 3 курс: Валиномицин – переносчик ионов К+
Краунэфиры – макрогетероциклические соединения, содержащие в своих циклах более 11 атомов, из которых не менее четырёх — гетероатомы, которые связаны между собой этиленовыми мостиками формула I — 12 -краун-4; (1, 4, 7, 10 тетраоксоциклододекан) формула II — 1, 10 -диаза-18 -краун-6; (1, 4, 10, 13 -тетраокса-7, 16 диазациклооктадекан) формула III — 1, 7 -дитиа-15 -краун-5 формула IV — дибензо-18 -краун-6 формула V — циклогексано-15 -краун-5 3 курс: Валиномицин – переносчик ионов К+
 Числом ядер (одно- и многоядерные циклы) Фенотиазин
Числом ядер (одно- и многоядерные циклы) Фенотиазин
 Присутствие гетероатома в цикле обусловливает высокую химическую реакционную способность и биологическую активность молекул гетероциклических соединений (в первую очередь ароматических соединенгий). OSAR (ККСА) - метод
Присутствие гетероатома в цикле обусловливает высокую химическую реакционную способность и биологическую активность молекул гетероциклических соединений (в первую очередь ароматических соединенгий). OSAR (ККСА) - метод
 2. Лекарственные средства, производные фурана 2. 1. Перечень программных ЛС • Амиодарон; • Гризеофульвин. • ЛС нитрофуранового ряда: Нитрофурал (Фурацилин), Фуразолидон, Нитрофурантоин (фурадонин), фурагин. (! Синтезированы в Институте органической химии АН Латвии)
2. Лекарственные средства, производные фурана 2. 1. Перечень программных ЛС • Амиодарон; • Гризеофульвин. • ЛС нитрофуранового ряда: Нитрофурал (Фурацилин), Фуразолидон, Нитрофурантоин (фурадонин), фурагин. (! Синтезированы в Институте органической химии АН Латвии)
 2. 2. Применение в медицине • Амиодарон (Кардиодарон. R)– антиаритмический препарат. Обладает также антиангинальным, коронародилатирующим, альфа- и бетаадреноблокирующим и гипотензивным действием. • Гризеофульвин – антибиотическое ЛС- нарушает формирование и деление грибковой клетки. • Нитрофурал (фурацилин), фуразолидон, нитрофурантоин (фурадонин), фурагин – антибактериальные ЛС, молекулярные механизмы действия – нарушение синтеза ДНК и белка микробных клеток;
2. 2. Применение в медицине • Амиодарон (Кардиодарон. R)– антиаритмический препарат. Обладает также антиангинальным, коронародилатирующим, альфа- и бетаадреноблокирующим и гипотензивным действием. • Гризеофульвин – антибиотическое ЛС- нарушает формирование и деление грибковой клетки. • Нитрофурал (фурацилин), фуразолидон, нитрофурантоин (фурадонин), фурагин – антибактериальные ЛС, молекулярные механизмы действия – нарушение синтеза ДНК и белка микробных клеток;
 2. 3. Химическое строение фурана В основе химической структуры лежит пятичленный кислородсодержащий гетероцикл: α Критерии ароматичности: • • • Плоский циклический σ-скелет; Сопряженная замкнутая π-электронная система, охватывающая все атомы цикла; Правило Хюккеля: число π электронов: (4 n+2)π (n=0, 1, 2, 3…). Фуран является ароматическим гетероциклическим соединением. π-избыточный гетероцикл (повышенная электронная плотность внутри кольца) – число электронов, образующих ароматическую систему (6) превышает общее число атомов в цикле (5) легко вступает в реакции электрофильного замещения (преимущественно в α-положение); легко окисляется.
2. 3. Химическое строение фурана В основе химической структуры лежит пятичленный кислородсодержащий гетероцикл: α Критерии ароматичности: • • • Плоский циклический σ-скелет; Сопряженная замкнутая π-электронная система, охватывающая все атомы цикла; Правило Хюккеля: число π электронов: (4 n+2)π (n=0, 1, 2, 3…). Фуран является ароматическим гетероциклическим соединением. π-избыточный гетероцикл (повышенная электронная плотность внутри кольца) – число электронов, образующих ароматическую систему (6) превышает общее число атомов в цикле (5) легко вступает в реакции электрофильного замещения (преимущественно в α-положение); легко окисляется.
 2. 4. Amiodarone Hydrochloride/Амиодарон C 25 H 30 Cl. I 2 NO 3 Mr 682 (2 -Бутил-3 -бензофуранил) [4 -[(2 -диэтиламино)этокси]-3, 5 -дийодфенил] метан-он (и в виде гидрохлорида) 2 -Бутил-3 -(3, 5 -дийодо-4 -(2 -диэтиламино)-этокси) бензоил)бензофуран Содержание действующего вещества: не менее 97% и не более 103% (сухое вещество). Третичная алифатическая аминогруппа в боковой цепи придает молекуле основные свойства, следовательно, способность солеобразования и растворимость в воде. Присутствие в молекуле эпокси- и простой эфирной- групп обусловливает значительную лабильность вещества Условия хранения: в хорошо укупоренных контейнерах, в защищенном от света месте, при температуре, не превышающей 30 0 С.
2. 4. Amiodarone Hydrochloride/Амиодарон C 25 H 30 Cl. I 2 NO 3 Mr 682 (2 -Бутил-3 -бензофуранил) [4 -[(2 -диэтиламино)этокси]-3, 5 -дийодфенил] метан-он (и в виде гидрохлорида) 2 -Бутил-3 -(3, 5 -дийодо-4 -(2 -диэтиламино)-этокси) бензоил)бензофуран Содержание действующего вещества: не менее 97% и не более 103% (сухое вещество). Третичная алифатическая аминогруппа в боковой цепи придает молекуле основные свойства, следовательно, способность солеобразования и растворимость в воде. Присутствие в молекуле эпокси- и простой эфирной- групп обусловливает значительную лабильность вещества Условия хранения: в хорошо укупоренных контейнерах, в защищенном от света месте, при температуре, не превышающей 30 0 С.
 Фармакокинетика Биодоступность 20 – 55% Метаболизм – печенью Период полувыведения - 58 сут (от 15 до 142 дней) Экскреция - с желчью Лекарственные формы - таблетки, раствор для внутривенного введения Способ введения - перорально, внутривенно Торговые названия: Амиодарон, Амиокордин, Кардиодарон, Кордарон, Ритморест, Седакорон
Фармакокинетика Биодоступность 20 – 55% Метаболизм – печенью Период полувыведения - 58 сут (от 15 до 142 дней) Экскреция - с желчью Лекарственные формы - таблетки, раствор для внутривенного введения Способ введения - перорально, внутривенно Торговые названия: Амиодарон, Амиокордин, Кардиодарон, Кордарон, Ритморест, Седакорон
 Применение: антиаритмическое, антиангинальное ЛС Исследования кафедры факультетской терапии СПб. ГМУ им. акад. И. П. Павлова: Препарат является эфффективным и безопасным средством для профилактики злокачественных аритмий сердца и внезапной смерти у больных с ИБС. Но! WHO Pharmaceuticals Newsletter No. 4, 2011: Служба медицинской безопасности Новой Зеландии сообщила, что применение амиодарона сопровождалось (51 пациент) развитием побочных эффектов - оптическая нейропатия (что случается редко) и corneal deposits уплотнение роговицы (которые возникают у большинства пациентов). Все пациенты испытывают вновь появившиеся симптомы зрительных нарушений или ухудшение имеющихся. Если зрительная невропатия подтверждается, лечение амиодароном должно быть остановлено из-за возможной потери зрения. Prescriber Update Vol. 32 No. 2, June 2011 (www. medsafe. aovt. nz).
Применение: антиаритмическое, антиангинальное ЛС Исследования кафедры факультетской терапии СПб. ГМУ им. акад. И. П. Павлова: Препарат является эфффективным и безопасным средством для профилактики злокачественных аритмий сердца и внезапной смерти у больных с ИБС. Но! WHO Pharmaceuticals Newsletter No. 4, 2011: Служба медицинской безопасности Новой Зеландии сообщила, что применение амиодарона сопровождалось (51 пациент) развитием побочных эффектов - оптическая нейропатия (что случается редко) и corneal deposits уплотнение роговицы (которые возникают у большинства пациентов). Все пациенты испытывают вновь появившиеся симптомы зрительных нарушений или ухудшение имеющихся. Если зрительная невропатия подтверждается, лечение амиодароном должно быть остановлено из-за возможной потери зрения. Prescriber Update Vol. 32 No. 2, June 2011 (www. medsafe. aovt. nz).
 World J Hepatol 2012 June 27; 4(6): 196 -198 (Случай из практики – 29 -летняя пациентка, внутривенное введение препарата) Аланинаминотрансфераза. Норма АЛТ (норма Ал. АТ) для женщин — до 31 Ед/л для мужчин норма Ал. АТ — до 41 Ед/л.
World J Hepatol 2012 June 27; 4(6): 196 -198 (Случай из практики – 29 -летняя пациентка, внутривенное введение препарата) Аланинаминотрансфераза. Норма АЛТ (норма Ал. АТ) для женщин — до 31 Ед/л для мужчин норма Ал. АТ — до 41 Ед/л.
 • Амиодарон терапии у взрослых с врожденными пороками сердца (ИБС) связана со значительным риском амиодарон-индуцированной тиреотоксикоз
• Амиодарон терапии у взрослых с врожденными пороками сердца (ИБС) связана со значительным риском амиодарон-индуцированной тиреотоксикоз
 • Описание: Белый или почти белый кристаллический порошок, очень мало растворим в воде, растворим в метаноле, мало растворим в этаноле (96%). • Т 0 С плавления: от 159°C дo 163°C.
• Описание: Белый или почти белый кристаллический порошок, очень мало растворим в воде, растворим в метаноле, мало растворим в этаноле (96%). • Т 0 С плавления: от 159°C дo 163°C.
 2. 4. 2. Подлинность (Ph. Eur) А. ИК – спектрофотомерия (электромагнитный спектр в интервале от 0, 76 мкм до ~ 1000 мкм). ! Инфракрасные спектры характеризуются сериями полос поглощения, определяемые волновым числом и интенсивностью. На оси абсцисс откладывается в линейной шкале значение волнового числа (см -1), на оси ординат - величина светопропускания Т (%). (А=lg 1/T) Диски с KBr: навеску твердого вещества (1 -3 мг) тщательно смешивают в вибромельнице или в ступке со спектроскопически чистым калия бромидом (150 -200 мг) и смесь прессуют. Спектр полученного образца получают относительно воздуха или относительно диска, приготовленного из чистого КВr, помещенного во второй канал прибора.
2. 4. 2. Подлинность (Ph. Eur) А. ИК – спектрофотомерия (электромагнитный спектр в интервале от 0, 76 мкм до ~ 1000 мкм). ! Инфракрасные спектры характеризуются сериями полос поглощения, определяемые волновым числом и интенсивностью. На оси абсцисс откладывается в линейной шкале значение волнового числа (см -1), на оси ординат - величина светопропускания Т (%). (А=lg 1/T) Диски с KBr: навеску твердого вещества (1 -3 мг) тщательно смешивают в вибромельнице или в ступке со спектроскопически чистым калия бромидом (150 -200 мг) и смесь прессуют. Спектр полученного образца получают относительно воздуха или относительно диска, приготовленного из чистого КВr, помещенного во второй канал прибора.
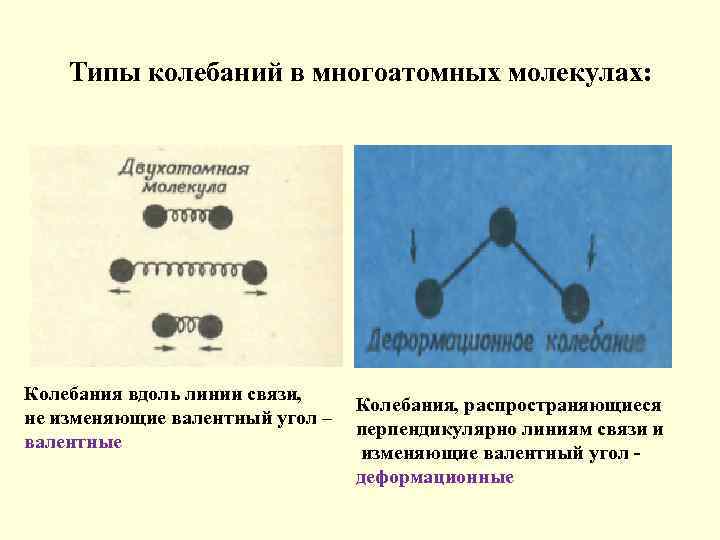 Типы колебаний в многоатомных молекулах: Колебания вдоль линии связи, не изменяющие валентный угол – валентные Колебания, распространяющиеся перпендикулярно линиям связи и изменяющие валентный угол деформационные
Типы колебаний в многоатомных молекулах: Колебания вдоль линии связи, не изменяющие валентный угол – валентные Колебания, распространяющиеся перпендикулярно линиям связи и изменяющие валентный угол деформационные
 ИК-абсорбционный спектр амиодарона 15 % раствора в дихлорметане На ИК- спектре амиодарона появляются полосы поглощения, обусловленные: • валентными колебаниями (ν) сопряженных связей С=С в интервале частот 1585 -1620 см-1 ; • деформационными колебаниями (δ) связей С-Н в интервале частот 1430 -1470 см-1 ; • валентными колебаниями связей С-О (простые эфиры) в интервале частот -1.
ИК-абсорбционный спектр амиодарона 15 % раствора в дихлорметане На ИК- спектре амиодарона появляются полосы поглощения, обусловленные: • валентными колебаниями (ν) сопряженных связей С=С в интервале частот 1585 -1620 см-1 ; • деформационными колебаниями (δ) связей С-Н в интервале частот 1430 -1470 см-1 ; • валентными колебаниями связей С-О (простые эфиры) в интервале частот -1.
 • В. ЛВ дает реакцию на хлориды. (It gives reaction (b) of chlorides)
• В. ЛВ дает реакцию на хлориды. (It gives reaction (b) of chlorides)
 2. 4. 3. Чистота ЛВ • Прозрачность раствора: раствор ЛВ в метаноле должен быть прозрачным и по цветности соответствовать эталонному раствору. • p. H водного раствора от 3. 2 до 3. 8. (1, 0 г субстанции растворить в воде при нагревании до 80 о. С и разбавить до 20 мл тем же растворителем). Родственные примеси: Методы ТСХ (испытуемый раствор: растворить 0, 500 г субстанции в 5, 0 мл метиленхлорида) и ВЭЖХ. Йодиды: максимум 150 ppm. Тяжелые металлы: максимум 20 ppm (стандартный раствор – 10 ppm Pb). Потеря в массе при высушивании: максимум 0, 5% (1, 000 г при высушивании при 50 о. С и давлении 0, 3 к. Па в течение 4 ч. ). Сульфатная зола – максимум 0, 1 % (навеска 1, 0 г).
2. 4. 3. Чистота ЛВ • Прозрачность раствора: раствор ЛВ в метаноле должен быть прозрачным и по цветности соответствовать эталонному раствору. • p. H водного раствора от 3. 2 до 3. 8. (1, 0 г субстанции растворить в воде при нагревании до 80 о. С и разбавить до 20 мл тем же растворителем). Родственные примеси: Методы ТСХ (испытуемый раствор: растворить 0, 500 г субстанции в 5, 0 мл метиленхлорида) и ВЭЖХ. Йодиды: максимум 150 ppm. Тяжелые металлы: максимум 20 ppm (стандартный раствор – 10 ppm Pb). Потеря в массе при высушивании: максимум 0, 5% (1, 000 г при высушивании при 50 о. С и давлении 0, 3 к. Па в течение 4 ч. ). Сульфатная зола – максимум 0, 1 % (навеска 1, 0 г).
 Обнаружение пятен Облучатель УФС-254/365
Обнаружение пятен Облучатель УФС-254/365
 Горизонтальная хроматографическая камера Более быстрое насыщение камеры парами подвижной фазы; Постоянная скорость движения фронта элюента; Эффективность разделения – способность системы предотвращать размывание пятен Воспроизводимость результатов;
Горизонтальная хроматографическая камера Более быстрое насыщение камеры парами подвижной фазы; Постоянная скорость движения фронта элюента; Эффективность разделения – способность системы предотвращать размывание пятен Воспроизводимость результатов;
 2. 4. 4. Количественное определение (Assay) • Растворить 0, 600 г в смеси: 5, 0 мл 0, 01 моль/л HCl и 75 мл спирта. Точка эквивалентности – потенциометрически. Титрант - 0, 1 моль/л Na. OH. Отмечают объем титранта между двумя точками перегиба на кривой титрования. 1 мл 0, 1 моль/л Na. OH эквивалентен 68, 18 мг C 25 H 30 Cl. I 2 NO 3. Потенциометрическое титрование основано на определении точки эквивалентности по результатам измерений потенциала электрода, связанного с концентрацией участника электродной реакции (Н+). Рабочий (индикаторный) электрод - стеклянный. Электрод сравнения - сереброхлоридный.
2. 4. 4. Количественное определение (Assay) • Растворить 0, 600 г в смеси: 5, 0 мл 0, 01 моль/л HCl и 75 мл спирта. Точка эквивалентности – потенциометрически. Титрант - 0, 1 моль/л Na. OH. Отмечают объем титранта между двумя точками перегиба на кривой титрования. 1 мл 0, 1 моль/л Na. OH эквивалентен 68, 18 мг C 25 H 30 Cl. I 2 NO 3. Потенциометрическое титрование основано на определении точки эквивалентности по результатам измерений потенциала электрода, связанного с концентрацией участника электродной реакции (Н+). Рабочий (индикаторный) электрод - стеклянный. Электрод сравнения - сереброхлоридный.
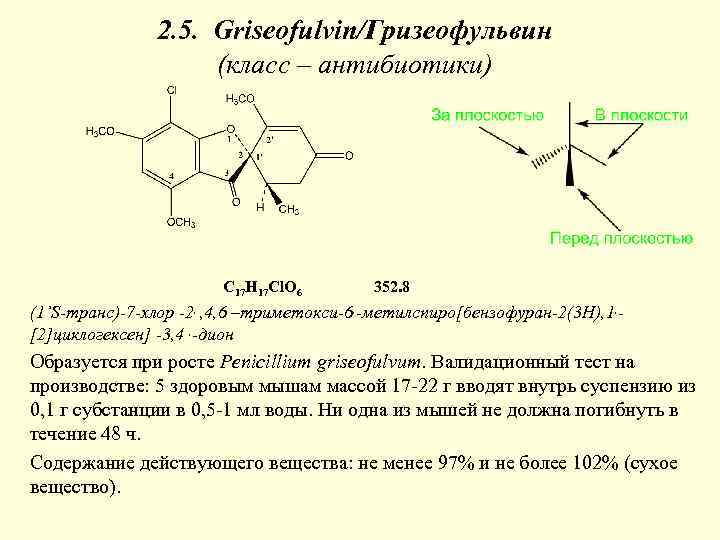 2. 5. Griseofulvin/Гризеофульвин (класс – антибиотики) C 17 H 17 Cl. O 6 352. 8 (1’S-транс)-7 -хлор -2, , 4, 6 –триметокси-6, -метилспиро[бензофуран-2(3 Н), 1, [2]циклогексен] -3, 4 , -дион Образуется при росте Penicillium griseofulvum. Валидационный тест на производстве: 5 здоровым мышам массой 17 -22 г вводят внутрь суспензию из 0, 1 г субстанции в 0, 5 -1 мл воды. Ни одна из мышей не должна погибнуть в течение 48 ч. Содержание действующего вещества: не менее 97% и не более 102% (сухое вещество).
2. 5. Griseofulvin/Гризеофульвин (класс – антибиотики) C 17 H 17 Cl. O 6 352. 8 (1’S-транс)-7 -хлор -2, , 4, 6 –триметокси-6, -метилспиро[бензофуран-2(3 Н), 1, [2]циклогексен] -3, 4 , -дион Образуется при росте Penicillium griseofulvum. Валидационный тест на производстве: 5 здоровым мышам массой 17 -22 г вводят внутрь суспензию из 0, 1 г субстанции в 0, 5 -1 мл воды. Ни одна из мышей не должна погибнуть в течение 48 ч. Содержание действующего вещества: не менее 97% и не более 102% (сухое вещество).
 • 2. 5. 1. Описание Белый или желтовато-белый высокодисперсный кристаллический порошок (размеры частиц от 5 мкм до 30 мкм) Практически нерастворим в воде, легко растворим в ДМФА и тетрахлорэтане, мало растворим в этаноле (МФ: ~750 г/л) и метаноле. Легко растворим в тетрахлорэтане • Тпл ~ 200 о. С • Применение: противогрибковое (фунгистатическое) ЛС, (от лат. fungus – гриб) • ЛФ: таблетки, мазь. •
• 2. 5. 1. Описание Белый или желтовато-белый высокодисперсный кристаллический порошок (размеры частиц от 5 мкм до 30 мкм) Практически нерастворим в воде, легко растворим в ДМФА и тетрахлорэтане, мало растворим в этаноле (МФ: ~750 г/л) и метаноле. Легко растворим в тетрахлорэтане • Тпл ~ 200 о. С • Применение: противогрибковое (фунгистатическое) ЛС, (от лат. fungus – гриб) • ЛФ: таблетки, мазь. •
 Размер частиц (МФ) • В ступке растереть 10 мг субстанции с 10 каплями гидроксиэтилцеллюлозы, добавить еще 3, 50 мл гидроксиэтилцеллюлозы и растереть еще раз. Перенести каплю суспензии в счетную камеру глубиной 10 мм, прикрыть покровным стеклом, и исследовать под микроскопом 10 областей по 0, 04 мм 2 каждая, используя увеличение 600 ×. Должно быть не более 30 кристаллов размером более 5 мкм в поле зрения. • Метод лазерной дифракции – распределение частиц по объему(V) и размеру (r).
Размер частиц (МФ) • В ступке растереть 10 мг субстанции с 10 каплями гидроксиэтилцеллюлозы, добавить еще 3, 50 мл гидроксиэтилцеллюлозы и растереть еще раз. Перенести каплю суспензии в счетную камеру глубиной 10 мм, прикрыть покровным стеклом, и исследовать под микроскопом 10 областей по 0, 04 мм 2 каждая, используя увеличение 600 ×. Должно быть не более 30 кристаллов размером более 5 мкм в поле зрения. • Метод лазерной дифракции – распределение частиц по объему(V) и размеру (r).
 2. 5. 2. Подлинность A. ИК- спектрофотометрия ИК- спектр гризеофульвина 1, 5 % раствора в хлороформе В ИК- спектре гризеофульвина имеется сильная полоса валентных колебаний группы С=О, соответствующая ~1620 см-1
2. 5. 2. Подлинность A. ИК- спектрофотометрия ИК- спектр гризеофульвина 1, 5 % раствора в хлороформе В ИК- спектре гризеофульвина имеется сильная полоса валентных колебаний группы С=О, соответствующая ~1620 см-1
 B. Окрашенные продукты окисления • При растворении ЛC (5 мг) в серной кислоте (~1760 г/л) с добавлением 5 мг порошка K 2 Cr 2 O 7 (калия дихромата) приводит к появлению винно-красной окраски.
B. Окрашенные продукты окисления • При растворении ЛC (5 мг) в серной кислоте (~1760 г/л) с добавлением 5 мг порошка K 2 Cr 2 O 7 (калия дихромата) приводит к появлению винно-красной окраски.
 МФ-2011: ТСХ Подвижная фаза – 1 объем этилметилкетона и 1 объем ксилена. Исследуемый раствор - 0, 5 мг тестируемой субстанции в 1 мл хлороформа Раствор сравнения - 0, 5 мг CRS гризеофульвина в 1 мл хлороформа. Проявление - УФ-лампа (254 нм) По положению, виду и интенсивности пятна не должны отличаться
МФ-2011: ТСХ Подвижная фаза – 1 объем этилметилкетона и 1 объем ксилена. Исследуемый раствор - 0, 5 мг тестируемой субстанции в 1 мл хлороформа Раствор сравнения - 0, 5 мг CRS гризеофульвина в 1 мл хлороформа. Проявление - УФ-лампа (254 нм) По положению, виду и интенсивности пятна не должны отличаться
 2. 5. 3. Чистота ЛВ При проведении фармацевтического анализа контролируют: Прозрачность (сравнение с эталоном) – растворить 0, 75 г в ДМФА и довести объем до 10 мл. Кислотность - приготовить суспензию из 0, 25 г в 20 мл этанола (96%) и добавить - 0, 1 мл раствора фенолфталеина (в этаноле). Для изменения окраски индикатора должно пойти не более 1, 0 мл 0, 02 М раствора Na. OH. Какое количество (моль) кислоты допустимо в навеске субстанции 250 мг?
2. 5. 3. Чистота ЛВ При проведении фармацевтического анализа контролируют: Прозрачность (сравнение с эталоном) – растворить 0, 75 г в ДМФА и довести объем до 10 мл. Кислотность - приготовить суспензию из 0, 25 г в 20 мл этанола (96%) и добавить - 0, 1 мл раствора фенолфталеина (в этаноле). Для изменения окраски индикатора должно пойти не более 1, 0 мл 0, 02 М раствора Na. OH. Какое количество (моль) кислоты допустимо в навеске субстанции 250 мг?
![• Удельное вращение - [α]D 20 от +354° до +364° для раствора , • Удельное вращение - [α]D 20 от +354° до +364° для раствора ,](https://present5.com/presentation/41666315_131779607/image-32.jpg) • Удельное вращение - [α]D 20 от +354° до +364° для раствора , полученного растворением 250 мг субстанции 25 мл ДМФА (При определении удельного вращения используют натриевую лампу, дающую монохроматический свет с длиной волны 589 нм (D-линия спектра). • Чему равна ω% (масса/объем) исследуемого раствора? • Сколько асимметрических атомов углерода в молекуле ЛВ?
• Удельное вращение - [α]D 20 от +354° до +364° для раствора , полученного растворением 250 мг субстанции 25 мл ДМФА (При определении удельного вращения используют натриевую лампу, дающую монохроматический свет с длиной волны 589 нм (D-линия спектра). • Чему равна ω% (масса/объем) исследуемого раствора? • Сколько асимметрических атомов углерода в молекуле ЛВ?
 • Родственные примеси - газовая хроматография. • Внутренний стандарт – 0, 2 г дифенилантрацена растворяют в 100 мл ацетона. • Тестовый раствор (а) – 0, 10 г исследуемой субстанции растворяют в 10 мл ацетона • Тестовый раствор (b) – 0, 10 г исследуемой субстанции растворяют в 1, 0 мл раствора внутреннего стандарта и объем доводят до 10 мл ацетоном. • Раствор сравнения – растворить 5, 0 мг CRS гризеофульвина в ацетоне, добавить 1, 0 мл раствора внутреннего стандарта и доводят объем до 10, 0 мл ацетоном.
• Родственные примеси - газовая хроматография. • Внутренний стандарт – 0, 2 г дифенилантрацена растворяют в 100 мл ацетона. • Тестовый раствор (а) – 0, 10 г исследуемой субстанции растворяют в 10 мл ацетона • Тестовый раствор (b) – 0, 10 г исследуемой субстанции растворяют в 1, 0 мл раствора внутреннего стандарта и объем доводят до 10 мл ацетоном. • Раствор сравнения – растворить 5, 0 мг CRS гризеофульвина в ацетоне, добавить 1, 0 мл раствора внутреннего стандарта и доводят объем до 10, 0 мл ацетоном.
 I. R - отношение площади пика гризеофульвина к площади пика внутреннего стандарта (раствора сравнения). II. Допустимые примеси: Дехлоро-гризеофульвин (рассчитывают отношение площади пика к площади пика внутреннего стандарта в растворе b) - не более 0, 6 R (3, 0%). Дегидро-гризеофульвин не более 0, 15 R (0, 75%).
I. R - отношение площади пика гризеофульвина к площади пика внутреннего стандарта (раствора сравнения). II. Допустимые примеси: Дехлоро-гризеофульвин (рассчитывают отношение площади пика к площади пика внутреннего стандарта в растворе b) - не более 0, 6 R (3, 0%). Дегидро-гризеофульвин не более 0, 15 R (0, 75%).
 • Потеря в массе при высушивании – максимум 1, 0%. Определяется для 1, 00 г при высушивании в печи при 105 о. С. • Сульфатная зола - максимум 0, 2 % (для навески в 1, 00 г). • Вещества, растворимые в легком бензине – максимум 0, 2% (2 мг в 1, 0 г субстанции.
• Потеря в массе при высушивании – максимум 1, 0%. Определяется для 1, 00 г при высушивании в печи при 105 о. С. • Сульфатная зола - максимум 0, 2 % (для навески в 1, 00 г). • Вещества, растворимые в легком бензине – максимум 0, 2% (2 мг в 1, 0 г субстанции.
 2. 5. 4. Количественное определение Измерение абсорбции раствора субстанции (80, 0 мг в 200 мл безводного этанола; 2 мл полученного раствора развести до 100 мл тем же растворителем) при длине волны λ=291 нм. 1% A=E 1 см · Cх · l Рассчитать удельное поглощение (E 1%1 см ), если абсорбция А =0, 548.
2. 5. 4. Количественное определение Измерение абсорбции раствора субстанции (80, 0 мг в 200 мл безводного этанола; 2 мл полученного раствора развести до 100 мл тем же растворителем) при длине волны λ=291 нм. 1% A=E 1 см · Cх · l Рассчитать удельное поглощение (E 1%1 см ), если абсорбция А =0, 548.


