Лекция 6 2013 LAST.pptx
- Количество слайдов: 54
 4 к - 2013 Лекция 6 Производные пиримидина – ч. 2
4 к - 2013 Лекция 6 Производные пиримидина – ч. 2
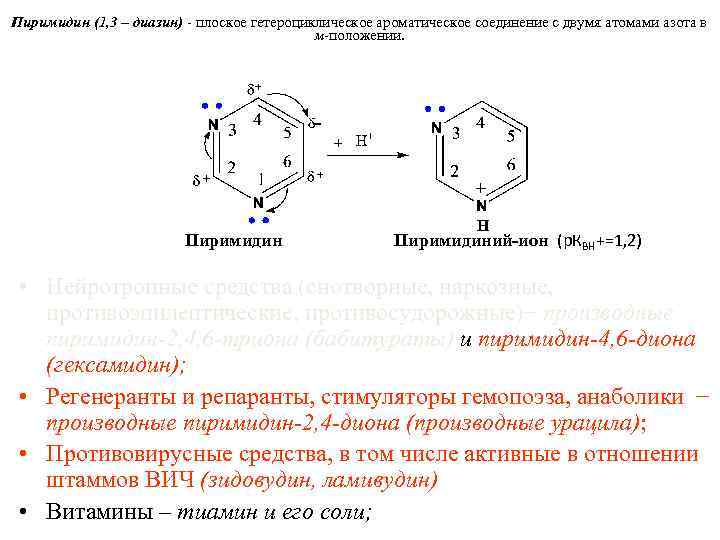 Пиримидин (1, 3 – диазин) - плоское гетероциклическое ароматическое соединение с двумя атомами азота в м-положении. Пиримидин Пиримидиний-ион (р. КВН+=1, 2) • Нейротропные средства (снотворные, наркозные, противоэпилептические, противосудорожные)− производные пиримидин-2, 4, 6 -триона (бабитураты) и пиримидин-4, 6 -диона (гексамидин); • Регенеранты и репаранты, стимуляторы гемопоэза, анаболики − производные пиримидин-2, 4 -диона (производные урацила); • Противовирусные средства, в том числе активные в отношении штаммов ВИЧ (зидовудин, ламивудин) • Витамины – тиамин и его соли;
Пиримидин (1, 3 – диазин) - плоское гетероциклическое ароматическое соединение с двумя атомами азота в м-положении. Пиримидин Пиримидиний-ион (р. КВН+=1, 2) • Нейротропные средства (снотворные, наркозные, противоэпилептические, противосудорожные)− производные пиримидин-2, 4, 6 -триона (бабитураты) и пиримидин-4, 6 -диона (гексамидин); • Регенеранты и репаранты, стимуляторы гемопоэза, анаболики − производные пиримидин-2, 4 -диона (производные урацила); • Противовирусные средства, в том числе активные в отношении штаммов ВИЧ (зидовудин, ламивудин) • Витамины – тиамин и его соли;
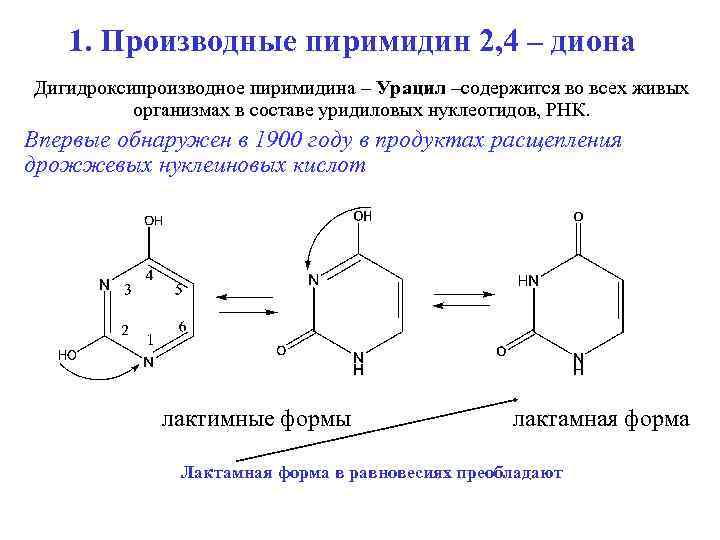 1. Производные пиримидин 2, 4 – диона Дигидроксипроизводное пиримидина – Урацил –содержится во всех живых организмах в составе уридиловых нуклеотидов, РНК. Впервые обнаружен в 1900 году в продуктах расщепления дрожжевых нуклеиновых кислот лактимные формы лактамная форма Лактамная форма в равновесиях преобладают
1. Производные пиримидин 2, 4 – диона Дигидроксипроизводное пиримидина – Урацил –содержится во всех живых организмах в составе уридиловых нуклеотидов, РНК. Впервые обнаружен в 1900 году в продуктах расщепления дрожжевых нуклеиновых кислот лактимные формы лактамная форма Лактамная форма в равновесиях преобладают
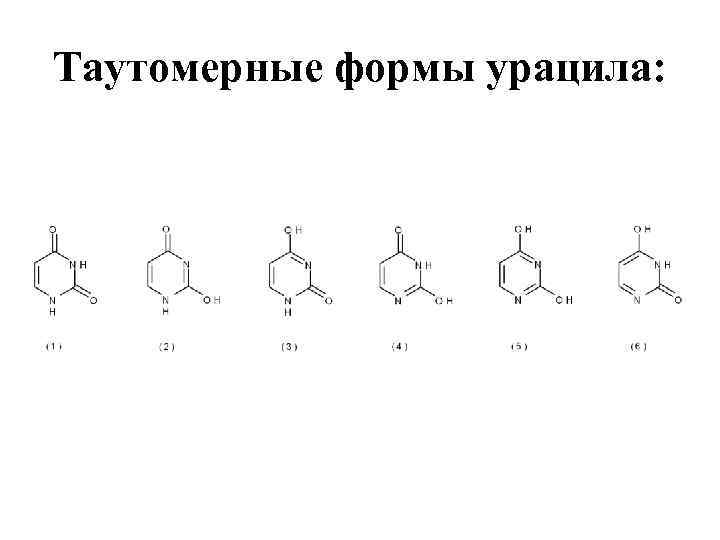 Таутомерные формы урацила:
Таутомерные формы урацила:
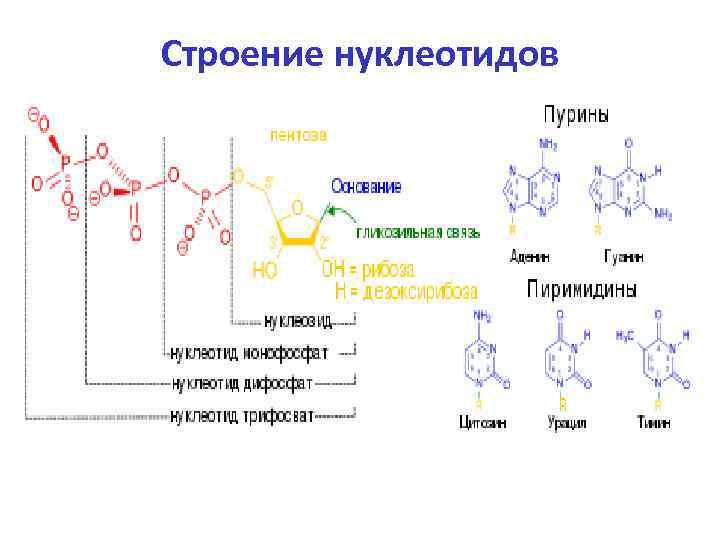 Строение нуклеотидов
Строение нуклеотидов
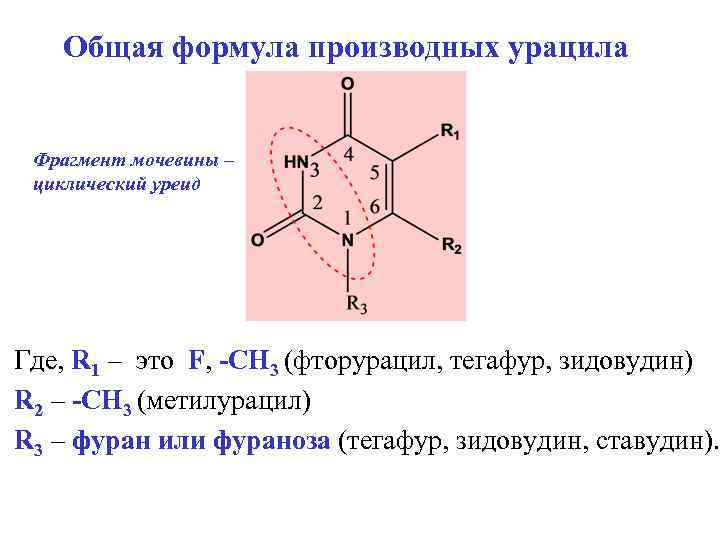 Общая формула производных урацила Фрагмент мочевины – циклический уреид Где, R 1 – это F, -СН 3 (фторурацил, тегафур, зидовудин) R 2 – -СН 3 (метилурацил) R 3 – фуран или фураноза (тегафур, зидовудин, ставудин).
Общая формула производных урацила Фрагмент мочевины – циклический уреид Где, R 1 – это F, -СН 3 (фторурацил, тегафур, зидовудин) R 2 – -СН 3 (метилурацил) R 3 – фуран или фураноза (тегафур, зидовудин, ставудин).
 Применение в медицине • На основе урацила синтезированы лекарственные вещества, являющиеся метаболитами (метилурацил) и антиметаболитами (фторурацил, тегафур) нуклеиновых оснований. Метаболит (метилурацил) - исходное соединение для синтеза нуклеиновых кислот. • Препараты-антиметаболиты применяются как противоопухолевые лекарственные средства. Они ингибируют синтез ДНК нарушается процесс деления опухолевых клеток и происходит их гибель. • Противоретровирусные лекарственные средства (зидовудин, ставудин) эффективны при ВИЧ-инфекции • Ретрови русы — семейство РНК-содержащих вирусов, заражающих преимущественно позвоночных. Наиболее известный и активно изучаемый представитель — вирус иммунодефицита человека.
Применение в медицине • На основе урацила синтезированы лекарственные вещества, являющиеся метаболитами (метилурацил) и антиметаболитами (фторурацил, тегафур) нуклеиновых оснований. Метаболит (метилурацил) - исходное соединение для синтеза нуклеиновых кислот. • Препараты-антиметаболиты применяются как противоопухолевые лекарственные средства. Они ингибируют синтез ДНК нарушается процесс деления опухолевых клеток и происходит их гибель. • Противоретровирусные лекарственные средства (зидовудин, ставудин) эффективны при ВИЧ-инфекции • Ретрови русы — семейство РНК-содержащих вирусов, заражающих преимущественно позвоночных. Наиболее известный и активно изучаемый представитель — вирус иммунодефицита человека.
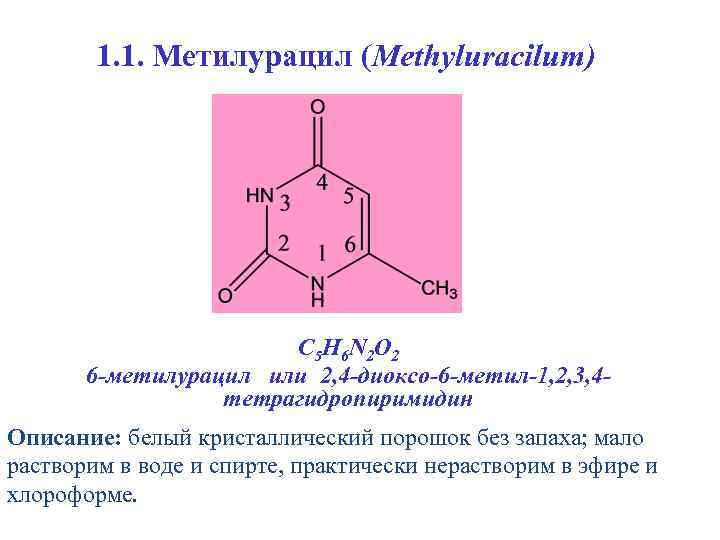 1. 1. Метилурацил (Methyluracilum) С 5 Н 6 N 2 O 2 6 -метилурацил или 2, 4 -диоксо-6 -метил-1, 2, 3, 4 тетрагидропиримидин Описание: белый кристаллический порошок без запаха; мало растворим в воде и спирте, практически нерастворим в эфире и хлороформе.
1. 1. Метилурацил (Methyluracilum) С 5 Н 6 N 2 O 2 6 -метилурацил или 2, 4 -диоксо-6 -метил-1, 2, 3, 4 тетрагидропиримидин Описание: белый кристаллический порошок без запаха; мало растворим в воде и спирте, практически нерастворим в эфире и хлороформе.
 Фармакологическое действие: анаболическое, гемопоэтическое (греч. póiesis – сотворение), лейкопоэтическое, регенерирующее, ранозаживляющее, противовоспалительное ЛС • ЛФ: метилурациловая мазь 10 % (при ранах, ожогах, трофических язвах) • Свечи с метилурацилом 0, 5 г (ректиты, язвенные колиты) • Таблетки 0, 5 г – лейкопения, переломы костей, болезни ЖКТ Анаболические средства — ЛС, действие которых направлено на усиление анаболических процессов в организме, т. е. ускорение образования и обновления структурных частей клеток, тканей и мышечных структур.
Фармакологическое действие: анаболическое, гемопоэтическое (греч. póiesis – сотворение), лейкопоэтическое, регенерирующее, ранозаживляющее, противовоспалительное ЛС • ЛФ: метилурациловая мазь 10 % (при ранах, ожогах, трофических язвах) • Свечи с метилурацилом 0, 5 г (ректиты, язвенные колиты) • Таблетки 0, 5 г – лейкопения, переломы костей, болезни ЖКТ Анаболические средства — ЛС, действие которых направлено на усиление анаболических процессов в организме, т. е. ускорение образования и обновления структурных частей клеток, тканей и мышечных структур.
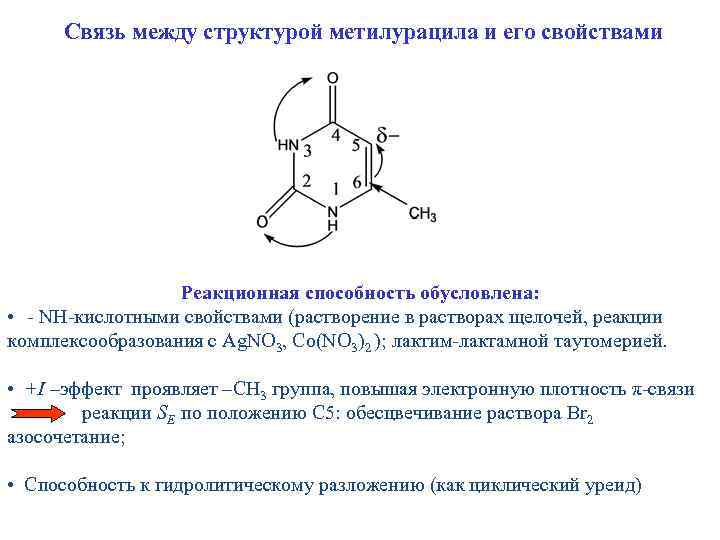 Связь между структурой метилурацила и его свойствами Реакционная способность обусловлена: • - NH-кислотными свойствами (растворение в растворах щелочей, реакции комплексообразования с Ag. NO 3, Co(NO 3)2 ); лактим-лактамной таутомерией. • +I –эффект проявляет –CH 3 группа, повышая электронную плотность π-связи реакции SE по положению С 5: обесцвечивание раствора Br 2 азосочетание; • Способность к гидролитическому разложению (как циклический уреид)
Связь между структурой метилурацила и его свойствами Реакционная способность обусловлена: • - NH-кислотными свойствами (растворение в растворах щелочей, реакции комплексообразования с Ag. NO 3, Co(NO 3)2 ); лактим-лактамной таутомерией. • +I –эффект проявляет –CH 3 группа, повышая электронную плотность π-связи реакции SE по положению С 5: обесцвечивание раствора Br 2 азосочетание; • Способность к гидролитическому разложению (как циклический уреид)
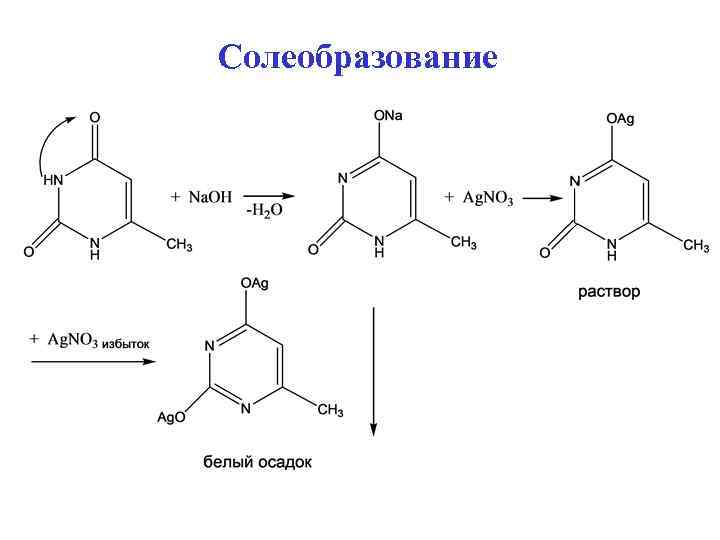 Солеобразование
Солеобразование
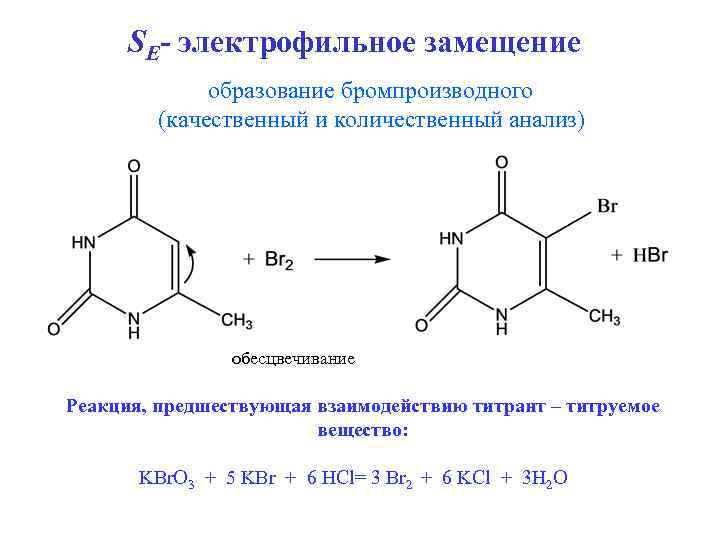 SE- электрофильное замещение образование бромпроизводного (качественный и количественный анализ) обесцвечивание Реакция, предшествующая взаимодействию титрант – титруемое вещество: KBr. O 3 + 5 KBr + 6 HCl= 3 Br 2 + 6 KCl + 3 H 2 O
SE- электрофильное замещение образование бромпроизводного (качественный и количественный анализ) обесцвечивание Реакция, предшествующая взаимодействию титрант – титруемое вещество: KBr. O 3 + 5 KBr + 6 HCl= 3 Br 2 + 6 KCl + 3 H 2 O
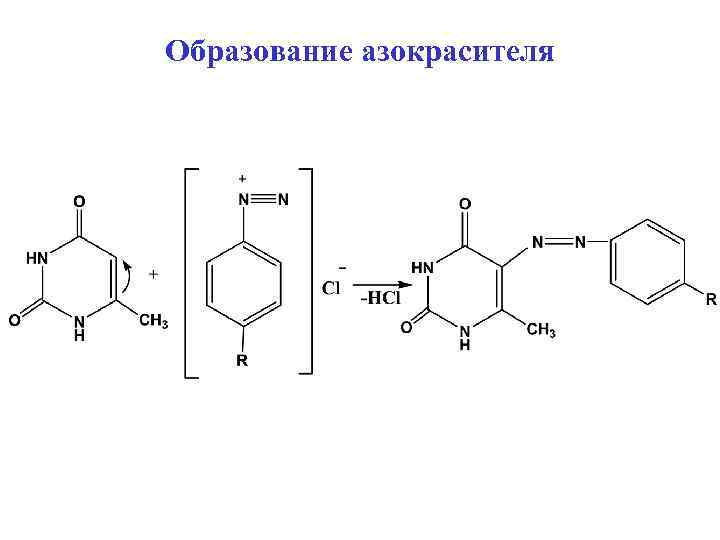 Образование азокрасителя
Образование азокрасителя
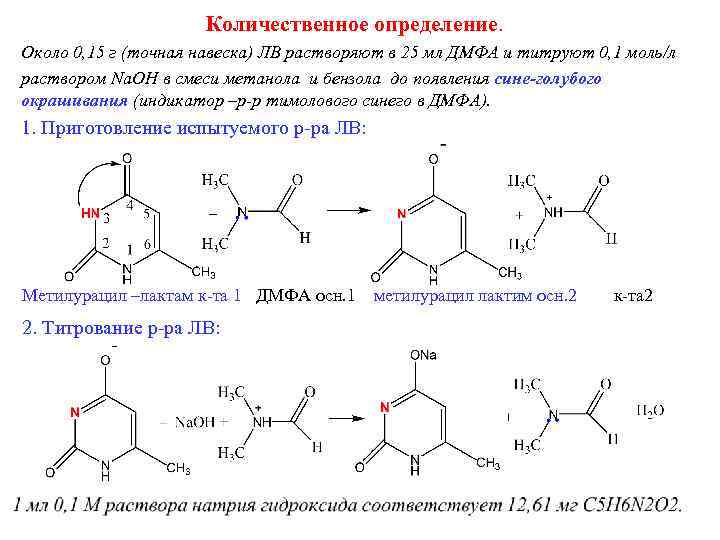 Количественное определение. Около 0, 15 г (точная навеска) ЛВ растворяют в 25 мл ДМФА и титруют 0, 1 моль/л раствором Na. OH в смеси метанола и бензола до появления сине-голубого окрашивания (индикатор –р-р тимолового синего в ДМФА). 1. Приготовление испытуемого р-ра ЛВ: Метилурацил –лактам к-та 1 ДМФА осн. 1 метилурацил лактим осн. 2 к-та 2 2. Титрование р-ра ЛВ:
Количественное определение. Около 0, 15 г (точная навеска) ЛВ растворяют в 25 мл ДМФА и титруют 0, 1 моль/л раствором Na. OH в смеси метанола и бензола до появления сине-голубого окрашивания (индикатор –р-р тимолового синего в ДМФА). 1. Приготовление испытуемого р-ра ЛВ: Метилурацил –лактам к-та 1 ДМФА осн. 1 метилурацил лактим осн. 2 к-та 2 2. Титрование р-ра ЛВ:
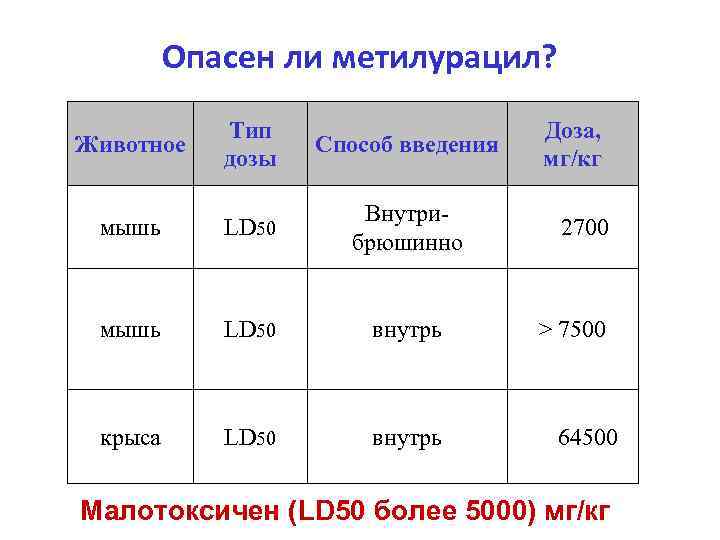 Опасен ли метилурацил? Животное Тип дозы Способ введения Доза, мг/кг мышь LD 50 Внутрибрюшинно 2700 мышь LD 50 внутрь > 7500 крыса LD 50 внутрь 64500 Малотоксичен (LD 50 более 5000) мг/кг
Опасен ли метилурацил? Животное Тип дозы Способ введения Доза, мг/кг мышь LD 50 Внутрибрюшинно 2700 мышь LD 50 внутрь > 7500 крыса LD 50 внутрь 64500 Малотоксичен (LD 50 более 5000) мг/кг
 1. 2. Фторурацил (Ftorouracilum) С 4 Н 3 N 2 O 2 F 5 -фторурацил или 2, 4 -диоксо-5 -фтор-1, 2, 3, 4 -тетрагидропиримидин Описание: белый или белый с желтоватым оттенком кристаллический порошок; мало растворим в воде и спирте, умеренно растворим в растворах щелочей, мало растворим в 0, 1 М растворе HCl. Фармакологическое действие – антагонист естественных метаболитов (антиметаболит) - цитостатическое (противоопухолевое) лекарственное средство. ЛФ: 5% водный раствор в ампулах 5 мл (в виде Na-соли)
1. 2. Фторурацил (Ftorouracilum) С 4 Н 3 N 2 O 2 F 5 -фторурацил или 2, 4 -диоксо-5 -фтор-1, 2, 3, 4 -тетрагидропиримидин Описание: белый или белый с желтоватым оттенком кристаллический порошок; мало растворим в воде и спирте, умеренно растворим в растворах щелочей, мало растворим в 0, 1 М растворе HCl. Фармакологическое действие – антагонист естественных метаболитов (антиметаболит) - цитостатическое (противоопухолевое) лекарственное средство. ЛФ: 5% водный раствор в ампулах 5 мл (в виде Na-соли)
 Особенности фармацевтического анализа - обусловлены присутствием в структуре молекулы атома фтора F: После минерализации (сжигание в колбе с кислородом, спекание с кристаллической щелочью): - + Ca+2 Ca. F 1. F 2 2.
Особенности фармацевтического анализа - обусловлены присутствием в структуре молекулы атома фтора F: После минерализации (сжигание в колбе с кислородом, спекание с кристаллической щелочью): - + Ca+2 Ca. F 1. F 2 2.
 1. 3. Тегафур (Фторафур) Fluorofur, Futraful С 8 Н 9 FN 2 O 3 Мr 200, 17 5 -фтор-1[(R, S)-тетрагидрофуран-2 -ил]пиримидин-2, 4 (1 Н, 3 Н) дион Содержание действующего вещества: не менее 98, 0% Описание: белый кристаллический порошок; растворим в метаноле, умеренно в воде (30 г-100 мл ), мало в диэтиловом эфире (10 г-100 мл); растворим в растворе Na. OH разв. Применение в медицине: рак желудка, толстой и прямой кишки, молочной железы; диффузный нейродермит, кожные лимфомы.
1. 3. Тегафур (Фторафур) Fluorofur, Futraful С 8 Н 9 FN 2 O 3 Мr 200, 17 5 -фтор-1[(R, S)-тетрагидрофуран-2 -ил]пиримидин-2, 4 (1 Н, 3 Н) дион Содержание действующего вещества: не менее 98, 0% Описание: белый кристаллический порошок; растворим в метаноле, умеренно в воде (30 г-100 мл ), мало в диэтиловом эфире (10 г-100 мл); растворим в растворе Na. OH разв. Применение в медицине: рак желудка, толстой и прямой кишки, молочной железы; диффузный нейродермит, кожные лимфомы.
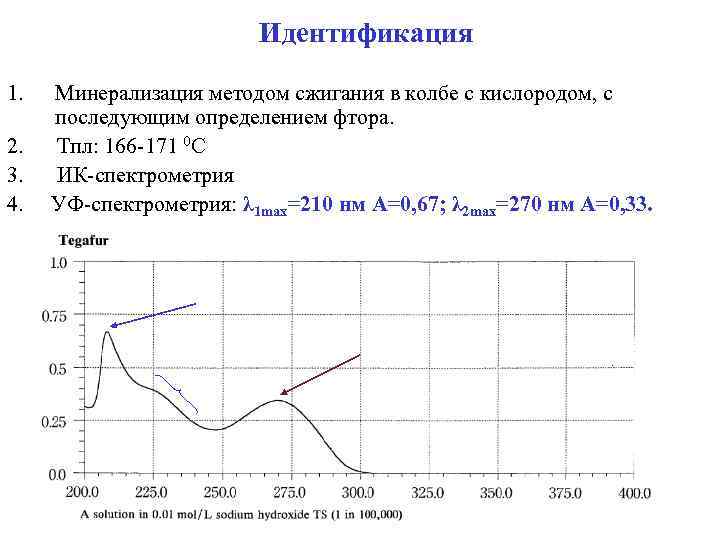 Идентификация 1. Минерализация методом сжигания в колбе с кислородом, с последующим определением фтора. 2. Тпл: 166 -171 0 С 3. ИК-спектрометрия 4. УФ-спектрометрия: λ 1 max=210 нм А=0, 67; λ 2 max=270 нм А=0, 33.
Идентификация 1. Минерализация методом сжигания в колбе с кислородом, с последующим определением фтора. 2. Тпл: 166 -171 0 С 3. ИК-спектрометрия 4. УФ-спектрометрия: λ 1 max=210 нм А=0, 67; λ 2 max=270 нм А=0, 33.
 Оценка чистоты • Прозрачность раствора: раствор ЛВ в Na. OH разв. должен быть прозрачным и бесцветным. • Хлориды – не более 0, 011% • Тяжелые металлы – не более 10 ррm • Мышьяк – не более 2 ррm • Related substances (родственные примеси): метод ТСХ ( thin-layer chromatography), используя silica gel (силикагель) GF 254 в качестве неподвижной фазы. • Потеря в массе при высушивании – не более 0, 5 % (1 г, 105 0 С, 4 часа) • Остаток после сжигания/сульфатная зола – 0, 10% (1 г).
Оценка чистоты • Прозрачность раствора: раствор ЛВ в Na. OH разв. должен быть прозрачным и бесцветным. • Хлориды – не более 0, 011% • Тяжелые металлы – не более 10 ррm • Мышьяк – не более 2 ррm • Related substances (родственные примеси): метод ТСХ ( thin-layer chromatography), используя silica gel (силикагель) GF 254 в качестве неподвижной фазы. • Потеря в массе при высушивании – не более 0, 5 % (1 г, 105 0 С, 4 часа) • Остаток после сжигания/сульфатная зола – 0, 10% (1 г).
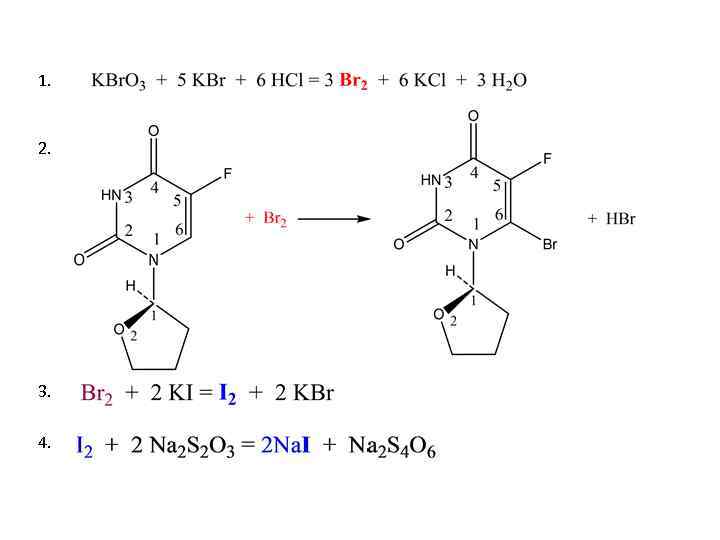
 Количественное определение Методика JP: Около 0, 15 г ЛС, предварительно высушенной, перенести в темную колбу, растворить в 75 мл воды, добавить точно 25 мл 0, 01 моль/л KBr. О 3; Добавить 1, 0 г KBr и 12 мл HCl; встряхнуть, оставить на 30 мин. К этому раствору добавить 1, 6 г KI, встряхнуть, оставить на 5 минут. Титровать выделяющийся йод 0, 1 моль/л раствором Na 2 S 2 O 3.
Количественное определение Методика JP: Около 0, 15 г ЛС, предварительно высушенной, перенести в темную колбу, растворить в 75 мл воды, добавить точно 25 мл 0, 01 моль/л KBr. О 3; Добавить 1, 0 г KBr и 12 мл HCl; встряхнуть, оставить на 30 мин. К этому раствору добавить 1, 6 г KI, встряхнуть, оставить на 5 минут. Титровать выделяющийся йод 0, 1 моль/л раствором Na 2 S 2 O 3.
 1. 2. 3. 4.
1. 2. 3. 4.
 0, 01 моль/л раствор KBr. O 3 эквивалентен 10, 008 мг С 8 Н 9 FN 2 O 3
0, 01 моль/л раствор KBr. O 3 эквивалентен 10, 008 мг С 8 Н 9 FN 2 O 3
 Противоретровирусные лекарственные средства (зидовудин, ставудин) эффективны при ВИЧ -инфекции • Ретрови русы — семейство РНК-содержащих вирусов, заражающих преимущественно позвоночных. Наиболее известный и активно изучаемый представитель — вирус иммунодефицита человека. После инфицирования клетки ретровирусом в цитоплазме начинается синтез вирусного ДНКгенома с использованием вирионной РНК в качестве матрицы. зидовудин, ставудин
Противоретровирусные лекарственные средства (зидовудин, ставудин) эффективны при ВИЧ -инфекции • Ретрови русы — семейство РНК-содержащих вирусов, заражающих преимущественно позвоночных. Наиболее известный и активно изучаемый представитель — вирус иммунодефицита человека. После инфицирования клетки ретровирусом в цитоплазме начинается синтез вирусного ДНКгенома с использованием вирионной РНК в качестве матрицы. зидовудин, ставудин
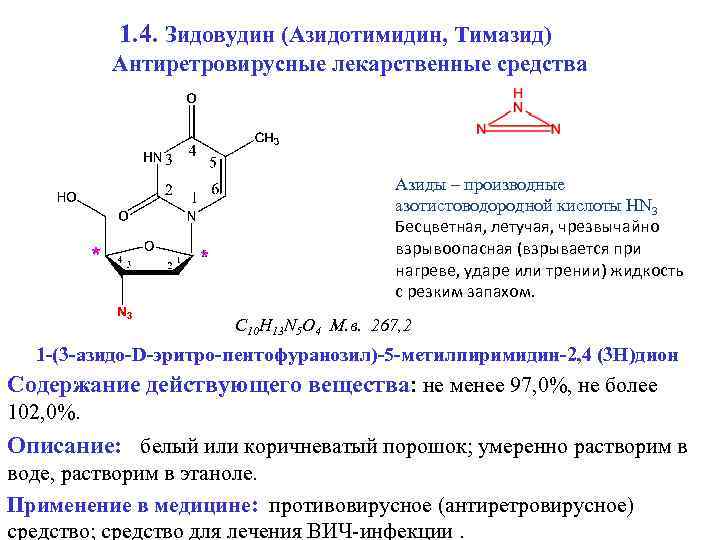 1. 4. Зидовудин (Азидотимидин, Тимазид) Антиретровирусные лекарственные средства Азиды – производные азотистоводородной кислоты HN 3 Бесцветная, летучая, чрезвычайно взрывоопасная (взрывается при нагреве, ударе или трении) жидкость с резким запахом. С 10 Н 13 N 5 O 4 М. в. 267, 2 1 -(3 -азидо-D-эритро-пентофуранозил)-5 -метилпиримидин-2, 4 (3 Н)дион Содержание действующего вещества: не менее 97, 0%, не более 102, 0%. Описание: белый или коричневатый порошок; умеренно растворим в воде, растворим в этаноле. Применение в медицине: противовирусное (антиретровирусное) средство; средство для лечения ВИЧ-инфекции.
1. 4. Зидовудин (Азидотимидин, Тимазид) Антиретровирусные лекарственные средства Азиды – производные азотистоводородной кислоты HN 3 Бесцветная, летучая, чрезвычайно взрывоопасная (взрывается при нагреве, ударе или трении) жидкость с резким запахом. С 10 Н 13 N 5 O 4 М. в. 267, 2 1 -(3 -азидо-D-эритро-пентофуранозил)-5 -метилпиримидин-2, 4 (3 Н)дион Содержание действующего вещества: не менее 97, 0%, не более 102, 0%. Описание: белый или коричневатый порошок; умеренно растворим в воде, растворим в этаноле. Применение в медицине: противовирусное (антиретровирусное) средство; средство для лечения ВИЧ-инфекции.
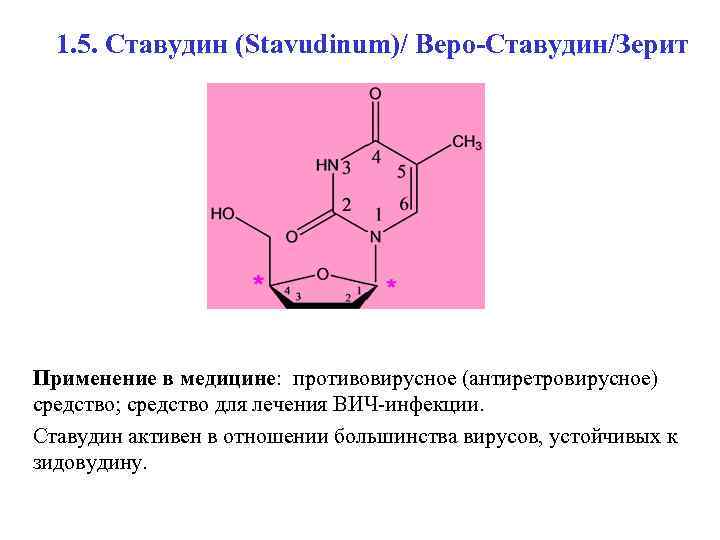 1. 5. Ставудин (Stavudinum)/ Веро-Ставудин/Зерит Применение в медицине: противовирусное (антиретровирусное) средство; средство для лечения ВИЧ-инфекции. Ставудин активен в отношении большинства вирусов, устойчивых к зидовудину.
1. 5. Ставудин (Stavudinum)/ Веро-Ставудин/Зерит Применение в медицине: противовирусное (антиретровирусное) средство; средство для лечения ВИЧ-инфекции. Ставудин активен в отношении большинства вирусов, устойчивых к зидовудину.
 AIDS Res Ther. 2006 Jul 22; 3: 19. The effect of different combination therapies on oxidative stress markers in HIV infected patients in Cameroon. Ngondi JL, Oben J, Forkah DM, Etame LH, Mbanya D. Source Nutrition, HIV and Health Research Unit, Department of Biochemistry, University of Yaounde I, Cameroon. jlngondi@yahoo. com • • Abstract The study assessed the effect of some highly active antiretroviral therapies (HAART), used in the management of HIV/AIDS in Cameroon, on oxidative stress markers such as malondialdehyde (as TBARs), albumin, protein carbonyl content and protein sulfhydryls groups. 85 HIV positive patients (34. 8 +/- 9. 3 years) were on three different highly active antiretroviral therapies (HAART patients). 65 HIV positive patients (32. 2 +/- 10. 9 years) on no treatment (Pre-HAART patients), and 90 non-HIV infected patients (32. 6 +/- 9. 3 years), were the control groups. Plasma TBARs as well as carbonyl levels were significantly higher in HIV patients on HAART compared to pre-HAART patients or non-HIV infected controls. On the other hand, the protein sulfhydryl group content was not different for patients on HAART compared to pre-HAART patients, but both were significantly lower than non-HIV infected controls (P < 0. 0001, 0. 001). The combination treatment Therapy I [stavudin (80 mg) + Lamivudin (600 mg) + Nevirapin + (400 mg) zidovudin (600 mg)] brought about a significant (p < 0. 05) reduction in the plasma concentration of protein sulfhydrl groups as well as TBARs compared to Therapy II [stavudin (80 mg) + Lamivudin (300 mg) + nevirapin (400 mg)] or with combination Therapy III of [zidovudine (600 mg) + lamivudin(300 mg) with efavirenz (600 mg)] (P < 0. 05). The content of the antioxidant, Vitamin C was lower in the plasma of patients on Therapy I compared to those on Therapy II (P < 0. 01) and Therapy III (P < 0. 001). HIV infection therefore increases the oxidative stress process, while antiretroviral combination therapy increased protein oxidation as well as the level of oxidative stress already present in HIV infection.
AIDS Res Ther. 2006 Jul 22; 3: 19. The effect of different combination therapies on oxidative stress markers in HIV infected patients in Cameroon. Ngondi JL, Oben J, Forkah DM, Etame LH, Mbanya D. Source Nutrition, HIV and Health Research Unit, Department of Biochemistry, University of Yaounde I, Cameroon. jlngondi@yahoo. com • • Abstract The study assessed the effect of some highly active antiretroviral therapies (HAART), used in the management of HIV/AIDS in Cameroon, on oxidative stress markers such as malondialdehyde (as TBARs), albumin, protein carbonyl content and protein sulfhydryls groups. 85 HIV positive patients (34. 8 +/- 9. 3 years) were on three different highly active antiretroviral therapies (HAART patients). 65 HIV positive patients (32. 2 +/- 10. 9 years) on no treatment (Pre-HAART patients), and 90 non-HIV infected patients (32. 6 +/- 9. 3 years), were the control groups. Plasma TBARs as well as carbonyl levels were significantly higher in HIV patients on HAART compared to pre-HAART patients or non-HIV infected controls. On the other hand, the protein sulfhydryl group content was not different for patients on HAART compared to pre-HAART patients, but both were significantly lower than non-HIV infected controls (P < 0. 0001, 0. 001). The combination treatment Therapy I [stavudin (80 mg) + Lamivudin (600 mg) + Nevirapin + (400 mg) zidovudin (600 mg)] brought about a significant (p < 0. 05) reduction in the plasma concentration of protein sulfhydrl groups as well as TBARs compared to Therapy II [stavudin (80 mg) + Lamivudin (300 mg) + nevirapin (400 mg)] or with combination Therapy III of [zidovudine (600 mg) + lamivudin(300 mg) with efavirenz (600 mg)] (P < 0. 05). The content of the antioxidant, Vitamin C was lower in the plasma of patients on Therapy I compared to those on Therapy II (P < 0. 01) and Therapy III (P < 0. 001). HIV infection therefore increases the oxidative stress process, while antiretroviral combination therapy increased protein oxidation as well as the level of oxidative stress already present in HIV infection.
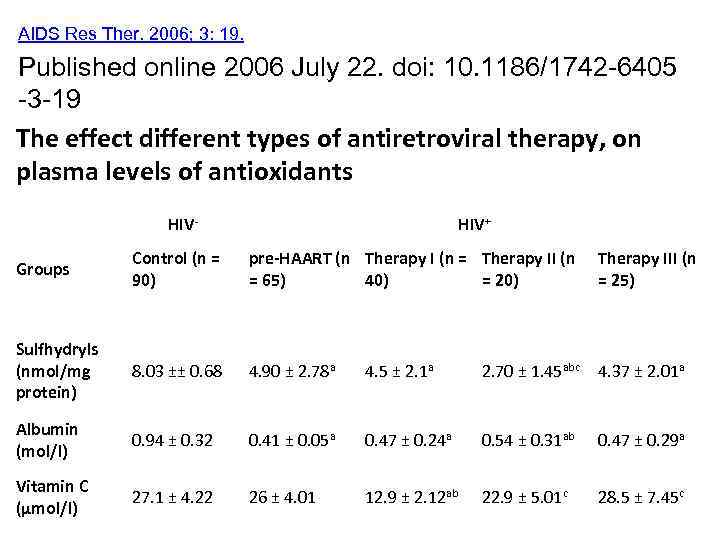 AIDS Res Ther. 2006; 3: 19. Published online 2006 July 22. doi: 10. 1186/1742 -6405 -3 -19 The effect different types of antiretroviral therapy, on plasma levels of antioxidants HIV- HIV+ Groups Control (n = 90) pre-HAART (n Therapy I (n = Therapy II (n = 65) 40) = 20) Therapy III (n = 25) Sulfhydryls (nmol/mg protein) 8. 03 ±± 0. 68 4. 90 ± 2. 78 a 4. 5 ± 2. 1 a 2. 70 ± 1. 45 abc 4. 37 ± 2. 01 a Albumin (mol/l) 0. 94 ± 0. 32 0. 41 ± 0. 05 a 0. 47 ± 0. 24 a 0. 54 ± 0. 31 ab 0. 47 ± 0. 29 a Vitamin C (μmol/l) 27. 1 ± 4. 22 26 ± 4. 01 12. 9 ± 2. 12 ab 22. 9 ± 5. 01 c 28. 5 ± 7. 45 c
AIDS Res Ther. 2006; 3: 19. Published online 2006 July 22. doi: 10. 1186/1742 -6405 -3 -19 The effect different types of antiretroviral therapy, on plasma levels of antioxidants HIV- HIV+ Groups Control (n = 90) pre-HAART (n Therapy I (n = Therapy II (n = 65) 40) = 20) Therapy III (n = 25) Sulfhydryls (nmol/mg protein) 8. 03 ±± 0. 68 4. 90 ± 2. 78 a 4. 5 ± 2. 1 a 2. 70 ± 1. 45 abc 4. 37 ± 2. 01 a Albumin (mol/l) 0. 94 ± 0. 32 0. 41 ± 0. 05 a 0. 47 ± 0. 24 a 0. 54 ± 0. 31 ab 0. 47 ± 0. 29 a Vitamin C (μmol/l) 27. 1 ± 4. 22 26 ± 4. 01 12. 9 ± 2. 12 ab 22. 9 ± 5. 01 c 28. 5 ± 7. 45 c
 Фармацевтический анализ – контроль качества (Ph. Eur) 1. ИК – спектрофотомерия (участок электромагнитного спектра в интервале от 0, 76 до ~ 1000 мкм). ! Инфракрасные спектры характеризуются сериями полос поглощения, определяемые волновым числом и интенсивностью. На оси абсцисс откладывается в линейной шкале значение волнового числа υ (см -1), на оси ординат величина светопропускания Т (%). (А=lg 1/T) Диски с KBr: навеску твердого вещества (1 -3 мг) тщательно смешивают в вибромельнице или в ступке со спектроскопически чистым калия бромидом (150 -200 мг) и смесь прессуют. Спектр полученного образца получают относительно воздуха или относительно диска, приготовленного из чистого КВr, помещенного во второй канал прибора.
Фармацевтический анализ – контроль качества (Ph. Eur) 1. ИК – спектрофотомерия (участок электромагнитного спектра в интервале от 0, 76 до ~ 1000 мкм). ! Инфракрасные спектры характеризуются сериями полос поглощения, определяемые волновым числом и интенсивностью. На оси абсцисс откладывается в линейной шкале значение волнового числа υ (см -1), на оси ординат величина светопропускания Т (%). (А=lg 1/T) Диски с KBr: навеску твердого вещества (1 -3 мг) тщательно смешивают в вибромельнице или в ступке со спектроскопически чистым калия бромидом (150 -200 мг) и смесь прессуют. Спектр полученного образца получают относительно воздуха или относительно диска, приготовленного из чистого КВr, помещенного во второй канал прибора.
![2. Удельное вращение [α]D 25 от + 60, 5° до + 63, 0°. (При 2. Удельное вращение [α]D 25 от + 60, 5° до + 63, 0°. (При](https://present5.com/presentation/41666315_166522381/image-30.jpg) 2. Удельное вращение [α]D 25 от + 60, 5° до + 63, 0°. (При определении удельного вращения используют натриевую лампу, дающую монохроматический свет с длиной волны 589 нм (D-линия спектра). 3. Тпл: около 124 0 С
2. Удельное вращение [α]D 25 от + 60, 5° до + 63, 0°. (При определении удельного вращения используют натриевую лампу, дающую монохроматический свет с длиной волны 589 нм (D-линия спектра). 3. Тпл: около 124 0 С
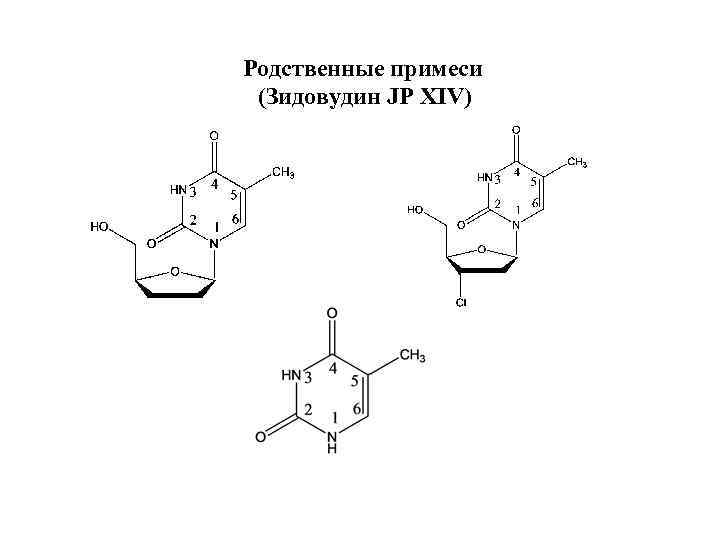 Родственные примеси (Зидовудин JP XIV)
Родственные примеси (Зидовудин JP XIV)
 Практически все антиретровирусные ЛС чрезвычайно токсичны Основное побочное действие зидовудина – угнетение кроветворения. Кроме того, приеме зидовудина отмечаются тошнота, головная боль, кардиомиопатия, миопатия.
Практически все антиретровирусные ЛС чрезвычайно токсичны Основное побочное действие зидовудина – угнетение кроветворения. Кроме того, приеме зидовудина отмечаются тошнота, головная боль, кардиомиопатия, миопатия.
 Количественное определение - метод ВЭЖХ - вариант колоночной жидкостной хроматографии, в которой подвижная фаза - элюент проходит через заполняющий колонку сорбент с большей скоростью за счет значительного давления на входе в хроматографическую колонку.
Количественное определение - метод ВЭЖХ - вариант колоночной жидкостной хроматографии, в которой подвижная фаза - элюент проходит через заполняющий колонку сорбент с большей скоростью за счет значительного давления на входе в хроматографическую колонку.
 Основные узлы жидкостного хроматографа: Насос высокого давления (до 200 -500 атм) - обеспечивает подачу элюента в колонку с заданной постоянной скоростью. Хроматографическая колонка (нержавеющая сталь, стекло): • l=10 -25 см, • d= 0, 3 -0, 8 см, • заполнена силикагелем (d=5 -10 мкм) - с привитыми к поверхности различными функциональными группами - неполярными алкильными остатками от C 8 до C 18 (обращенно-фазовый вариант ВЭЖХ) или • замещенными алкилхлорсиланами, содержащими полярные группы: нитрильная, диольная группы, аминогруппа (нормально-фазовый вариант ВЭЖХ);
Основные узлы жидкостного хроматографа: Насос высокого давления (до 200 -500 атм) - обеспечивает подачу элюента в колонку с заданной постоянной скоростью. Хроматографическая колонка (нержавеющая сталь, стекло): • l=10 -25 см, • d= 0, 3 -0, 8 см, • заполнена силикагелем (d=5 -10 мкм) - с привитыми к поверхности различными функциональными группами - неполярными алкильными остатками от C 8 до C 18 (обращенно-фазовый вариант ВЭЖХ) или • замещенными алкилхлорсиланами, содержащими полярные группы: нитрильная, диольная группы, аминогруппа (нормально-фазовый вариант ВЭЖХ);
 • для неполярной неподвижной фазы используются полярные элюэнты (смеси из таких растворителей, как ацетонитрил, метанол, вода, тетрагидрофуран), • для полярной – смеси неполярных органических компонентов (например, гексан, хлороформ, дихлорэтан). • Детектор - обычно используют спектрофотометрический детектор с переменной (190 -900 нм) или фиксированной (чаще 254 нм) длиной волны.
• для неполярной неподвижной фазы используются полярные элюэнты (смеси из таких растворителей, как ацетонитрил, метанол, вода, тетрагидрофуран), • для полярной – смеси неполярных органических компонентов (например, гексан, хлороформ, дихлорэтан). • Детектор - обычно используют спектрофотометрический детектор с переменной (190 -900 нм) или фиксированной (чаще 254 нм) длиной волны.
 Хроматографический анализ базируется на методе теоретических тарелок • хроматографическая колонка теоретически делится на ряд элементарных участков – «тарелок» ; • на каждой «тарелке» устанавливается равновесное распределение определяемого вещества между сорбентом и элюентом; • каждая новая порция элюента вызывает смещение этого равновесия, вследствие чего часть вещества переносится на следующую тарелку, на которой вновь устанавливается равновесие. • эффективность колонки тем выше, чем меньше высота, эквивалентная теоретической тарелке и больше число теоретических тарелок.
Хроматографический анализ базируется на методе теоретических тарелок • хроматографическая колонка теоретически делится на ряд элементарных участков – «тарелок» ; • на каждой «тарелке» устанавливается равновесное распределение определяемого вещества между сорбентом и элюентом; • каждая новая порция элюента вызывает смещение этого равновесия, вследствие чего часть вещества переносится на следующую тарелку, на которой вновь устанавливается равновесие. • эффективность колонки тем выше, чем меньше высота, эквивалентная теоретической тарелке и больше число теоретических тарелок.
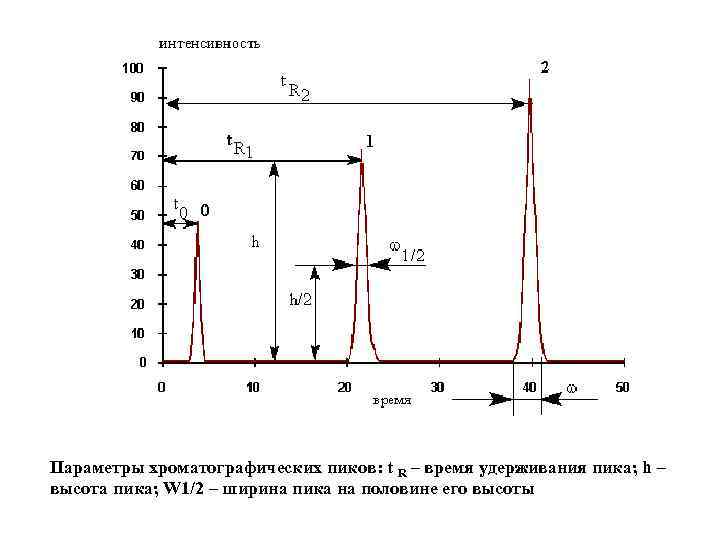 Параметры хроматографических пиков: t R – время удерживания пика; h – высота пика; W 1/2 – ширина пика на половине его высоты
Параметры хроматографических пиков: t R – время удерживания пика; h – высота пика; W 1/2 – ширина пика на половине его высоты
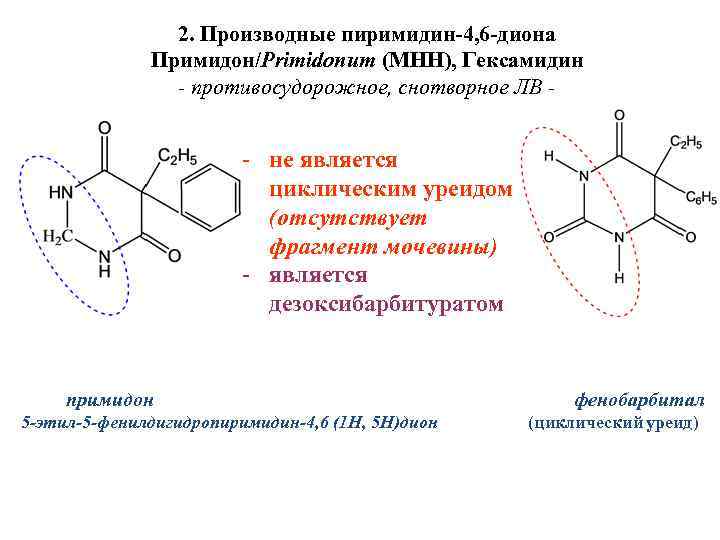 2. Производные пиримидин-4, 6 -диона Примидон/Primidonum (МНН), Гексамидин - противосудорожное, снотворное ЛВ - - не является циклическим уреидом (отсутствует фрагмент мочевины) - является дезоксибарбитуратом примидон 5 -этил-5 -фенилдигидропиримидин-4, 6 (1 Н, 5 Н)дион фенобарбитал (циклический уреид)
2. Производные пиримидин-4, 6 -диона Примидон/Primidonum (МНН), Гексамидин - противосудорожное, снотворное ЛВ - - не является циклическим уреидом (отсутствует фрагмент мочевины) - является дезоксибарбитуратом примидон 5 -этил-5 -фенилдигидропиримидин-4, 6 (1 Н, 5 Н)дион фенобарбитал (циклический уреид)
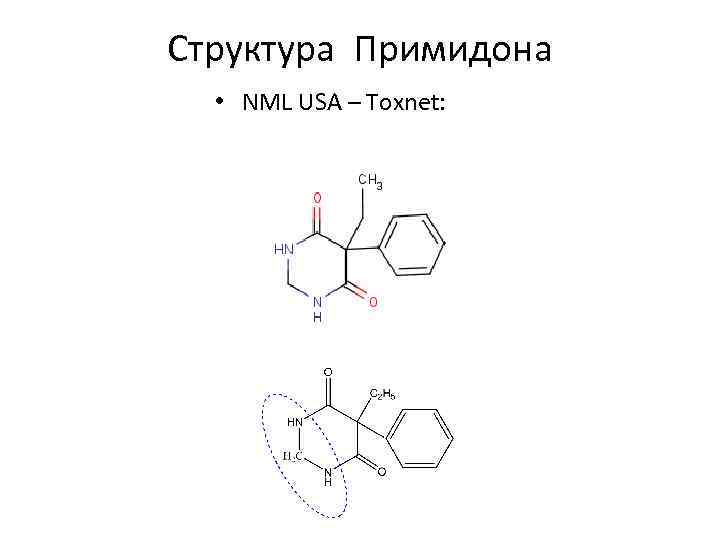 Структура Примидона • NML USA – Toxnet:
Структура Примидона • NML USA – Toxnet:
 NB! • За рубежом под этим же названием (Hexamidinum, Hexamidine) выпускается другой препарат — 4, 4 -(гексаметилендиокси)-дибензамидин, являющийся химиотерапевтическим антипротозойным средством.
NB! • За рубежом под этим же названием (Hexamidinum, Hexamidine) выпускается другой препарат — 4, 4 -(гексаметилендиокси)-дибензамидин, являющийся химиотерапевтическим антипротозойным средством.
 Показания: эпилепсия различного генеза, судорожные припадки • уступает по фармакологической активности фенобарбиталу; • менее токсичен; • может вызвать сонливость, головокружение, тошноту, атаксúю (греч. аtaxía – беспорядок) – нарушение координации движения; • при длительном зависимость. применении – лекарственная
Показания: эпилепсия различного генеза, судорожные припадки • уступает по фармакологической активности фенобарбиталу; • менее токсичен; • может вызвать сонливость, головокружение, тошноту, атаксúю (греч. аtaxía – беспорядок) – нарушение координации движения; • при длительном зависимость. применении – лекарственная
 Tremor Other Hyperkinet Mov (N Y). 2012; 2. 2012 Aug 6. • Methodological issues in clinical drug development for essential tremor. • Carranza MA, Snyder MR, Elble RJ, Boutzoukas AE, Zesiewicz TA. • Source • Department of Neurology, University of South Florida, Tampa, Florida, United States of America. • Abstract • Essential tremor (ET) (на фоне отсутствия других симптомов, как например, тремор при болезни Пркисона) is one of the most common tremor disorders in the world. Despite this, only two medications have received Level A recommendations from the American Academy of Neurology to treat it (primidone and propranolol). Even though these medications provide relief to a large group of ET patients, up to 50% of patients are non-responders. Additional medications to treat ET are needed. This review discusses some of the methodological issues that should be addressed for quality clinical drug development in ET.
Tremor Other Hyperkinet Mov (N Y). 2012; 2. 2012 Aug 6. • Methodological issues in clinical drug development for essential tremor. • Carranza MA, Snyder MR, Elble RJ, Boutzoukas AE, Zesiewicz TA. • Source • Department of Neurology, University of South Florida, Tampa, Florida, United States of America. • Abstract • Essential tremor (ET) (на фоне отсутствия других симптомов, как например, тремор при болезни Пркисона) is one of the most common tremor disorders in the world. Despite this, only two medications have received Level A recommendations from the American Academy of Neurology to treat it (primidone and propranolol). Even though these medications provide relief to a large group of ET patients, up to 50% of patients are non-responders. Additional medications to treat ET are needed. This review discusses some of the methodological issues that should be addressed for quality clinical drug development in ET.
 NML US –Toxnet: Максимальная доза: . . . не должна быть превышена суточная доза в 2 г Dose, mg/kg Organism Test Type child TDLo oral 625 women TDLo oral 5 women TDLo Route oral 450 38000 Effect BEHAVIORAL: GENERAL ANESTHETIC, SLEEP, CHANGES IN MOTOR ACTIVITY BEHAVIORAL: "HALLUCINATIO NS, DISTORTED PERCEPTIONS", TOXIC PSYCHOSIS Source British Medical Journal. Vol. 1, Pg. 90, 1957. Lancet. Vol. 266, Pg. 102, 1954. Archives of Neurology Vol. 30, Pg. 255, 1974. Drug Intelligence and Clinical Pharmacy. Vol. 17, Pg. 551, 1983.
NML US –Toxnet: Максимальная доза: . . . не должна быть превышена суточная доза в 2 г Dose, mg/kg Organism Test Type child TDLo oral 625 women TDLo oral 5 women TDLo Route oral 450 38000 Effect BEHAVIORAL: GENERAL ANESTHETIC, SLEEP, CHANGES IN MOTOR ACTIVITY BEHAVIORAL: "HALLUCINATIO NS, DISTORTED PERCEPTIONS", TOXIC PSYCHOSIS Source British Medical Journal. Vol. 1, Pg. 90, 1957. Lancet. Vol. 266, Pg. 102, 1954. Archives of Neurology Vol. 30, Pg. 255, 1974. Drug Intelligence and Clinical Pharmacy. Vol. 17, Pg. 551, 1983.
 Лекарственные формы Хранение РФ: таблетки по 0, 125 и 0, 25 г в упаковке по 50 штук. US: PRIMIDONE, USP (MYSOLINE) Таблетки по 50 и 250 мг Суспензия для приема внутрь (250 мг/5 мл). • список Б. В хорошо укупоренной таре Хранить таблетки ниже 40 о. С, предпочтительно между 15 и 30 о. С в закупоренных и защищенных от света емкостях. Защищать от замораживания (Primidone Oral Suspension USP/ Drug Information for the Health Care Professional. 17 th ed. Volume I. 1997, p. 2424).
Лекарственные формы Хранение РФ: таблетки по 0, 125 и 0, 25 г в упаковке по 50 штук. US: PRIMIDONE, USP (MYSOLINE) Таблетки по 50 и 250 мг Суспензия для приема внутрь (250 мг/5 мл). • список Б. В хорошо укупоренной таре Хранить таблетки ниже 40 о. С, предпочтительно между 15 и 30 о. С в закупоренных и защищенных от света емкостях. Защищать от замораживания (Primidone Oral Suspension USP/ Drug Information for the Health Care Professional. 17 th ed. Volume I. 1997, p. 2424).
 1. 2. Биофармацевтичексие характеристики примидона • Коэффициент распределения КN (октанол/вода) = 0. 91 (Растворимость выше в полярном или неполярном растворителе? ) • Тпл=281 -282 0 C • Метаболизм: образуются два активных метаболита – фенобарбитал и фенилэтилмалонамид. Пик концентрации в плазме крови наблюдается примерно через 3 ч. Биологический полупериод: t 1/2 (плазма крови) = 10 -21 ч. Для фенобарбитала-метаболита – 75 -126 ч; Для фенилэтилмалонамида-метаболита – 10 - 25 ч.
1. 2. Биофармацевтичексие характеристики примидона • Коэффициент распределения КN (октанол/вода) = 0. 91 (Растворимость выше в полярном или неполярном растворителе? ) • Тпл=281 -282 0 C • Метаболизм: образуются два активных метаболита – фенобарбитал и фенилэтилмалонамид. Пик концентрации в плазме крови наблюдается примерно через 3 ч. Биологический полупериод: t 1/2 (плазма крови) = 10 -21 ч. Для фенобарбитала-метаболита – 75 -126 ч; Для фенилэтилмалонамида-метаболита – 10 - 25 ч.
 • Описание: белый кристаллический порошок, практически нерастворим в воде, мало растворим в этаноле, ацетоне. • более выраженные противосудорожное и менее выраженное снотворное действие, чем у фенобарбитала; • может вызвать сонливость, головокружение, тошноту, атаксúю (греч. аtaxía – беспорядок) – нарушение координации движения; • при длительном применении – лекарственная зависимость. • умеренно опасен при введении в желудок, обладает умеренной кумулятивной активностью, в высоких дозах способен вызывать потенциальные тератогенные и канцерогенные эффекты, оказывает общетоксическое действие.
• Описание: белый кристаллический порошок, практически нерастворим в воде, мало растворим в этаноле, ацетоне. • более выраженные противосудорожное и менее выраженное снотворное действие, чем у фенобарбитала; • может вызвать сонливость, головокружение, тошноту, атаксúю (греч. аtaxía – беспорядок) – нарушение координации движения; • при длительном применении – лекарственная зависимость. • умеренно опасен при введении в желудок, обладает умеренной кумулятивной активностью, в высоких дозах способен вызывать потенциальные тератогенные и канцерогенные эффекты, оказывает общетоксическое действие.
 Контроль качества (Ph. Eur 6, 0) • First identification: В – ИК-СФ • Second identification: A, C, D А: УФ-СФ – λ 1 max 252 нм, λ 2 max 257 нм, λ 3 max 264 нм А 257/А 261 от 2, 00 до 2, 20 С: Раствор ЛВ в Na-соли хромотроповой к-ты с дбавлением H 2 O и H 2 SO 4 дает розовато-синее окрашивание при нагревании смеси. D: Смешать ЛВ с безводным Na 2 CO 3 или Na. OH нагреть до плавления – выделяется газ аммиак, окрашивающий влажную лакмусовую бумагу в синий цвет Количественный анализ: УФ-СФ 0, 06% спиртового р-ра при λ 2 max 257 нм, используя стандартный образец примидона.
Контроль качества (Ph. Eur 6, 0) • First identification: В – ИК-СФ • Second identification: A, C, D А: УФ-СФ – λ 1 max 252 нм, λ 2 max 257 нм, λ 3 max 264 нм А 257/А 261 от 2, 00 до 2, 20 С: Раствор ЛВ в Na-соли хромотроповой к-ты с дбавлением H 2 O и H 2 SO 4 дает розовато-синее окрашивание при нагревании смеси. D: Смешать ЛВ с безводным Na 2 CO 3 или Na. OH нагреть до плавления – выделяется газ аммиак, окрашивающий влажную лакмусовую бумагу в синий цвет Количественный анализ: УФ-СФ 0, 06% спиртового р-ра при λ 2 max 257 нм, используя стандартный образец примидона.
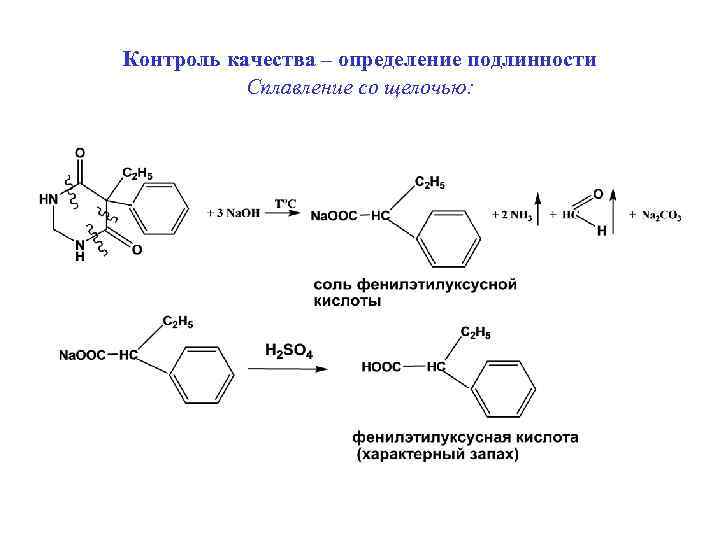 Контроль качества – определение подлинности Сплавление со щелочью:
Контроль качества – определение подлинности Сплавление со щелочью:
 Кислотный гидролиз
Кислотный гидролиз
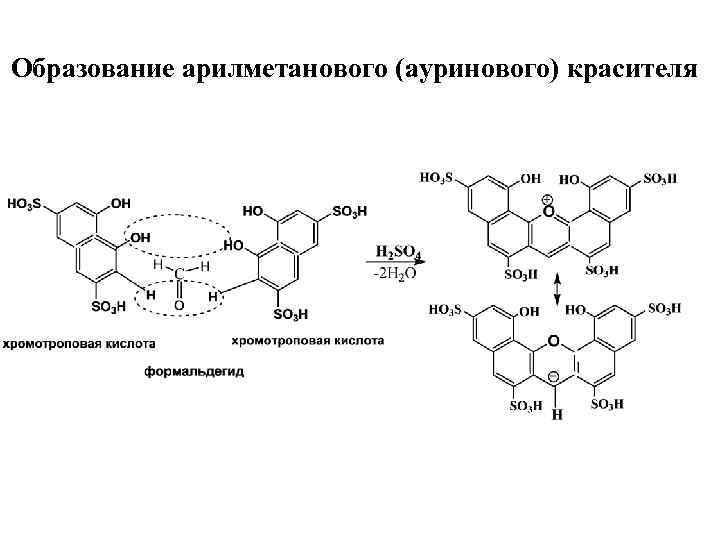 Образование арилметанового (ауринового) красителя
Образование арилметанового (ауринового) красителя
 Количественное определение • УФ-спектрометрия спиртового раствора примидона: λmax 1 = 255 нм, λmax 2 = 258 нм, λmax 3 = 262 нм. • Метод Кьельдаля - метод быстрого измерения пропорций азота в органическом соединении, названный в честь датского химика Йохана КЬЕЛЬДАЛЯ (1849 -1900). Азот при нагревании органического вещества с концентрированной H 2 SO 4 в присутствии катализатора переходит в (NH 4)2 SO 4. После добавления Na. OH смесь кипит, высвобождая NH 3 , который растворяется в кислоте. Аммиак, а значит и азот, определяется титрованием.
Количественное определение • УФ-спектрометрия спиртового раствора примидона: λmax 1 = 255 нм, λmax 2 = 258 нм, λmax 3 = 262 нм. • Метод Кьельдаля - метод быстрого измерения пропорций азота в органическом соединении, названный в честь датского химика Йохана КЬЕЛЬДАЛЯ (1849 -1900). Азот при нагревании органического вещества с концентрированной H 2 SO 4 в присутствии катализатора переходит в (NH 4)2 SO 4. После добавления Na. OH смесь кипит, высвобождая NH 3 , который растворяется в кислоте. Аммиак, а значит и азот, определяется титрованием.
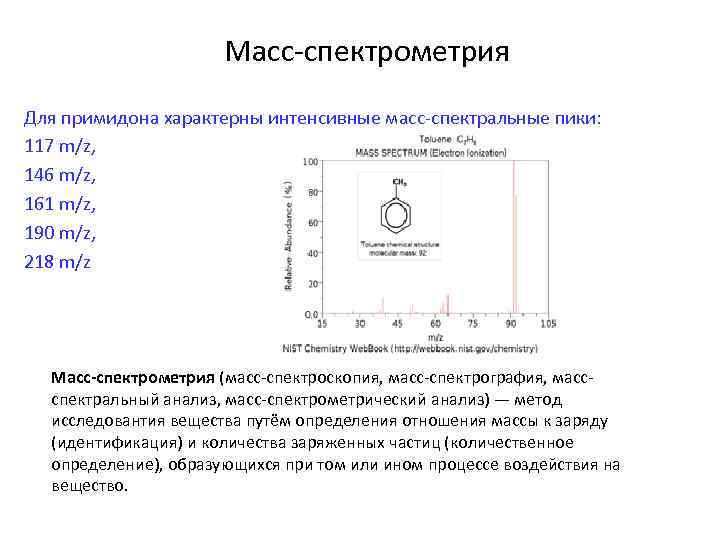 Масс-спектрометрия Для примидона характерны интенсивные масс-спектральные пики: 117 m/z, 146 m/z, 161 m/z, 190 m/z, 218 m/z Масс-спектрометрия (масс-спектроскопия, масс-спектрография, массспектральный анализ, масс-спектрометрический анализ) — метод исследовантия вещества путём определения отношения массы к заряду (идентификация) и количества заряженных частиц (количественное определение), образующихся при том или ином процессе воздействия на вещество.
Масс-спектрометрия Для примидона характерны интенсивные масс-спектральные пики: 117 m/z, 146 m/z, 161 m/z, 190 m/z, 218 m/z Масс-спектрометрия (масс-спектроскопия, масс-спектрография, массспектральный анализ, масс-спектрометрический анализ) — метод исследовантия вещества путём определения отношения массы к заряду (идентификация) и количества заряженных частиц (количественное определение), образующихся при том или ином процессе воздействия на вещество.
 J Anal Toxicol. 2000 Nov-Dec; 24(8): 685 -90. • Analysis of Six Anticonvulsant Drugs using Solid-Phase Extraction, Deuterated Internal Standards, and Gas Chromatography-Mass Spectrometry • D. J. Speed 1, S. J. Dickson 2, E. R. Cairns 3, N. D. Kim 1
J Anal Toxicol. 2000 Nov-Dec; 24(8): 685 -90. • Analysis of Six Anticonvulsant Drugs using Solid-Phase Extraction, Deuterated Internal Standards, and Gas Chromatography-Mass Spectrometry • D. J. Speed 1, S. J. Dickson 2, E. R. Cairns 3, N. D. Kim 1
 Количественное определение Кислотные свойства - менее выражены невозможность реакций кислотно-основного титрования. • УФ-спектрометрия спиртового раствора примидона: λmax 1 = 255 нм, λmax 2 = 258 нм, λmax 3 = 262 нм. • Метод Кьельдаля
Количественное определение Кислотные свойства - менее выражены невозможность реакций кислотно-основного титрования. • УФ-спектрометрия спиртового раствора примидона: λmax 1 = 255 нм, λmax 2 = 258 нм, λmax 3 = 262 нм. • Метод Кьельдаля


