4 Алкины.pptx
- Количество слайдов: 17
 4 АЦЕТИЛЕНОВЫЕ УГЛЕВОДОРОДЫ
4 АЦЕТИЛЕНОВЫЕ УГЛЕВОДОРОДЫ
 АЛКИНЫ Углеводороды, в цепи которых находится тройная связь называются ацетиленовыми или алкинами. Их общая формула Сn. H 2 n– 2. Родоначальник этого ряда – ацетилен. ИЗОМЕРИЯ. НОМЕНКЛАТУРА Структурная изомерия начинается с четвертого представителя – бутина С 4 H 6. Однако эти изомеры различаются только положением тройной связи, а не строением углеродного скелета. Структурная изомерия начинается с пятого члена ряда – пентина С 5 H 8. Эта особенность в строении, связана с тем, что ацетиленовая группировка имеет только две валентности. Это обусловливает меньшее число изомеров в ряду алкинов по сравнению с алкенами.
АЛКИНЫ Углеводороды, в цепи которых находится тройная связь называются ацетиленовыми или алкинами. Их общая формула Сn. H 2 n– 2. Родоначальник этого ряда – ацетилен. ИЗОМЕРИЯ. НОМЕНКЛАТУРА Структурная изомерия начинается с четвертого представителя – бутина С 4 H 6. Однако эти изомеры различаются только положением тройной связи, а не строением углеродного скелета. Структурная изомерия начинается с пятого члена ряда – пентина С 5 H 8. Эта особенность в строении, связана с тем, что ацетиленовая группировка имеет только две валентности. Это обусловливает меньшее число изомеров в ряду алкинов по сравнению с алкенами.
 АЛКИНЫ Алкины по систематической (ИЮПАК) номенклатуре называют по тем же правилам, что и алканы, но суффикс –ан заменяют на –ин. Главную цепь выбирают так, чтобы в ней находилась тройная связь. Эту цепь нумеруют с того конца, к которому ближе тройная связь. По рациональной номенклатуре алкины называют как алкилзамещенные ацетилена. Если в углеводородной цепи есть двойные и тройные связи, то нумерация атомов С начинается с того конца цепи, к которому ближе тройная связь. 3
АЛКИНЫ Алкины по систематической (ИЮПАК) номенклатуре называют по тем же правилам, что и алканы, но суффикс –ан заменяют на –ин. Главную цепь выбирают так, чтобы в ней находилась тройная связь. Эту цепь нумеруют с того конца, к которому ближе тройная связь. По рациональной номенклатуре алкины называют как алкилзамещенные ацетилена. Если в углеводородной цепи есть двойные и тройные связи, то нумерация атомов С начинается с того конца цепи, к которому ближе тройная связь. 3
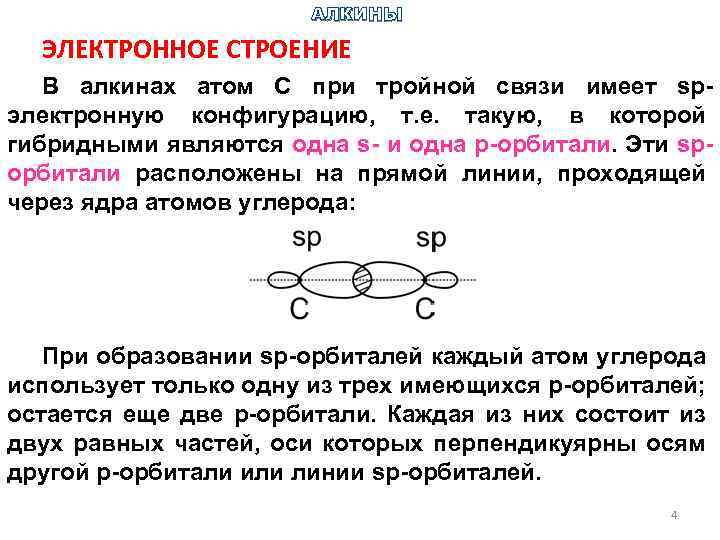 АЛКИНЫ ЭЛЕКТРОННОЕ СТРОЕНИЕ В алкинах атом С при тройной связи имеет spэлектронную конфигурацию, т. е. такую, в которой гибридными являются одна s- и одна р-орбитали. Эти spорбитали расположены на прямой линии, проходящей через ядра атомов углерода: При образовании sp-орбиталей каждый атом углерода использует только одну из трех имеющихся р-орбиталей; остается еще две р-орбитали. Каждая из них состоит из двух равных частей, оси которых перпендикуярны осям другой р-орбитали или линии sp-орбиталей. 4
АЛКИНЫ ЭЛЕКТРОННОЕ СТРОЕНИЕ В алкинах атом С при тройной связи имеет spэлектронную конфигурацию, т. е. такую, в которой гибридными являются одна s- и одна р-орбитали. Эти spорбитали расположены на прямой линии, проходящей через ядра атомов углерода: При образовании sp-орбиталей каждый атом углерода использует только одну из трех имеющихся р-орбиталей; остается еще две р-орбитали. Каждая из них состоит из двух равных частей, оси которых перпендикуярны осям другой р-орбитали или линии sp-орбиталей. 4
 АЛКИНЫ Схема строения молекулы ацетилена Каждая р-орбиталь занята одним электроном. Эта орбиталь может перекрываться с р-орбиталью другого атома С, так что происходит спаривание электронов и образуются две π-связи. Если одно облако π-связи изобразить над и под линией, соединяющей ядра атомов С, то другое облако связи будет находиться спереди и 5 сзади этой линии.
АЛКИНЫ Схема строения молекулы ацетилена Каждая р-орбиталь занята одним электроном. Эта орбиталь может перекрываться с р-орбиталью другого атома С, так что происходит спаривание электронов и образуются две π-связи. Если одно облако π-связи изобразить над и под линией, соединяющей ядра атомов С, то другое облако связи будет находиться спереди и 5 сзади этой линии.
 АЛКИНЫ Между облаками связей существует перекрывание, поэтому две связи сливаются, образуя одно цилиндрическое π-электронное облако вокруг линии, соединяющей ядра атомов С: Тройная связь имеет ось симметрии, поэтому изомерия алкинов бывает структурной и позиционной, связанной с расположением кратной связи. 6
АЛКИНЫ Между облаками связей существует перекрывание, поэтому две связи сливаются, образуя одно цилиндрическое π-электронное облако вокруг линии, соединяющей ядра атомов С: Тройная связь имеет ось симметрии, поэтому изомерия алкинов бывает структурной и позиционной, связанной с расположением кратной связи. 6
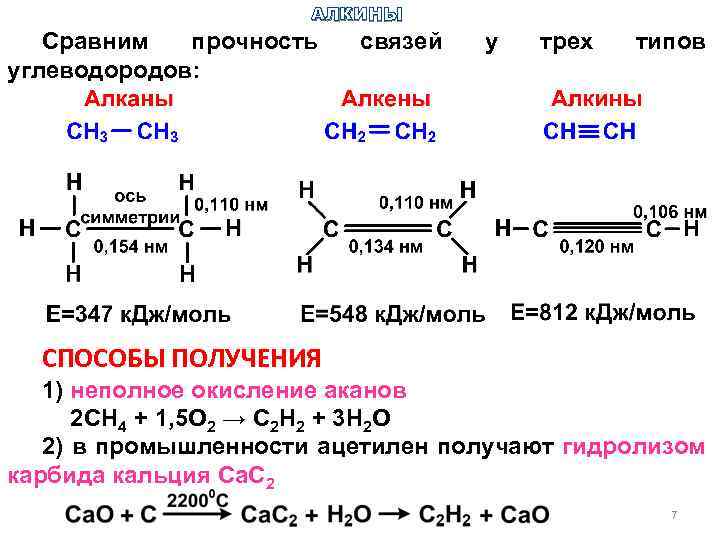 АЛКИНЫ Сравним прочность углеводородов: связей у трех типов СПОСОБЫ ПОЛУЧЕНИЯ 1) неполное окисление аканов 2 СН 4 + 1, 5 О 2 → С 2 Н 2 + 3 Н 2 О 2) в промышленности ацетилен получают гидролизом карбида кальция Ca. C 2 7
АЛКИНЫ Сравним прочность углеводородов: связей у трех типов СПОСОБЫ ПОЛУЧЕНИЯ 1) неполное окисление аканов 2 СН 4 + 1, 5 О 2 → С 2 Н 2 + 3 Н 2 О 2) в промышленности ацетилен получают гидролизом карбида кальция Ca. C 2 7
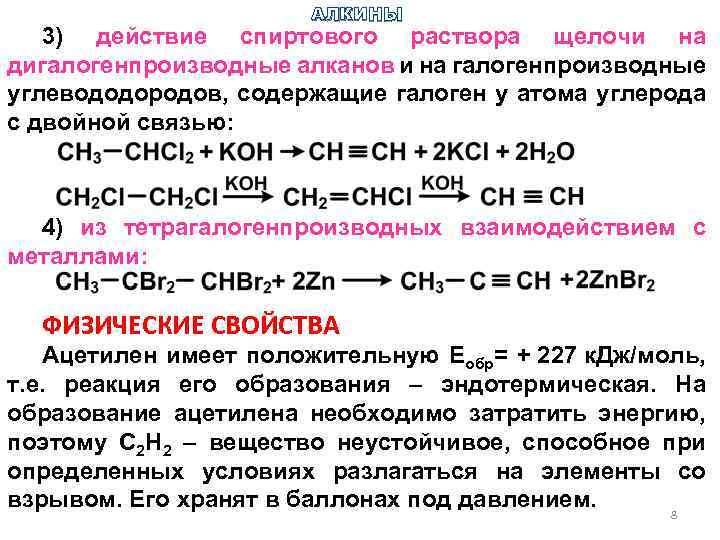 АЛКИНЫ 3) действие спиртового раствора щелочи на дигалогенпроизводные алканов и на галогенпроизводные углевододородов, содержащие галоген у атома углерода с двойной связью: 4) из тетрагалогенпроизводных взаимодействием с металлами: ФИЗИЧЕСКИЕ СВОЙСТВА Ацетилен имеет положительную Еобр= + 227 к. Дж/моль, т. е. реакция его образования – эндотермическая. На образование ацетилена необходимо затратить энергию, поэтому С 2 Н 2 – вещество неустойчивое, способное при определенных условиях разлагаться на элементы со взрывом. Его хранят в баллонах под давлением. 8
АЛКИНЫ 3) действие спиртового раствора щелочи на дигалогенпроизводные алканов и на галогенпроизводные углевододородов, содержащие галоген у атома углерода с двойной связью: 4) из тетрагалогенпроизводных взаимодействием с металлами: ФИЗИЧЕСКИЕ СВОЙСТВА Ацетилен имеет положительную Еобр= + 227 к. Дж/моль, т. е. реакция его образования – эндотермическая. На образование ацетилена необходимо затратить энергию, поэтому С 2 Н 2 – вещество неустойчивое, способное при определенных условиях разлагаться на элементы со взрывом. Его хранят в баллонах под давлением. 8
 АЛКИНЫ Ацетилен используют в органическом синтезе, а также при сварке и резке металлов. При горении (окислении) ацетилена выделяется большое количество тепла: С 2 Н 2 + 2, 5 О 2 = 2 СО 2 + Н 2 О, ΔН = -1300 к. Дж/моль Основные закономерности в изменении tкип и tпл в ряду алкинов сходны с алкенами. Положение тройной связи в углеродной цепи еще больше влияет на tкип. Например, 1 -бутин кипит при 8, 5 C, а 2 -бутин – при 27 C. Все бутены при обычных условиях – вещества газообразные. Необходимо отметить, что ацетилен при атмосферном давлении может находиться только в твердом или газообразном состояниях. Плавление его возможно только под давлением. 9
АЛКИНЫ Ацетилен используют в органическом синтезе, а также при сварке и резке металлов. При горении (окислении) ацетилена выделяется большое количество тепла: С 2 Н 2 + 2, 5 О 2 = 2 СО 2 + Н 2 О, ΔН = -1300 к. Дж/моль Основные закономерности в изменении tкип и tпл в ряду алкинов сходны с алкенами. Положение тройной связи в углеродной цепи еще больше влияет на tкип. Например, 1 -бутин кипит при 8, 5 C, а 2 -бутин – при 27 C. Все бутены при обычных условиях – вещества газообразные. Необходимо отметить, что ацетилен при атмосферном давлении может находиться только в твердом или газообразном состояниях. Плавление его возможно только под давлением. 9
 АЛКИНЫ ХИМИЧЕСКИЕ СВОЙСТВА Благодаря наличию π-облака алкины вступают во взаимодействие с электрофилами. π-облако тройной связи стянуто настолько сильно, что атомы С доступны для атаки нуклеофилами. Поэтому для алкинов характерны реакции присоединения электрофилов и нуклеофилов, замещения, полимеризации и изомеризации. Реакции присоединения электрофилов: 1. Гидрирование. Галогеноводороды присоединяются к алкинам непосредственно или в присутствии катализатора по правилу Марковникова: 10
АЛКИНЫ ХИМИЧЕСКИЕ СВОЙСТВА Благодаря наличию π-облака алкины вступают во взаимодействие с электрофилами. π-облако тройной связи стянуто настолько сильно, что атомы С доступны для атаки нуклеофилами. Поэтому для алкинов характерны реакции присоединения электрофилов и нуклеофилов, замещения, полимеризации и изомеризации. Реакции присоединения электрофилов: 1. Гидрирование. Галогеноводороды присоединяются к алкинам непосредственно или в присутствии катализатора по правилу Марковникова: 10
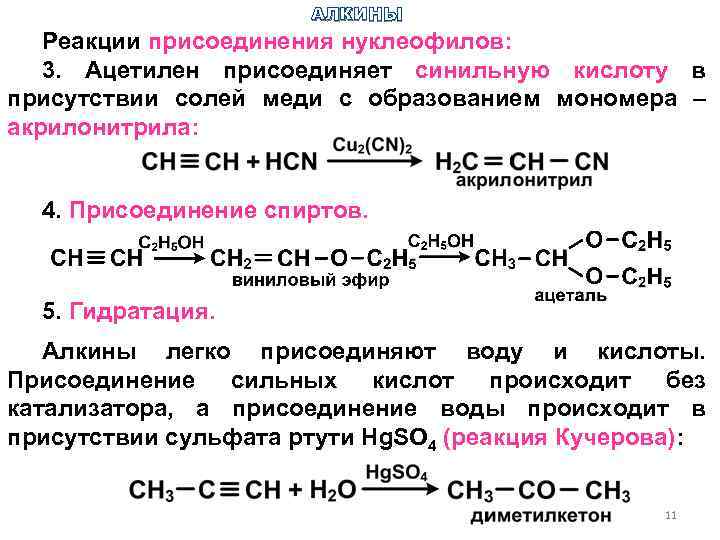 АЛКИНЫ Реакции присоединения нуклеофилов: 3. Ацетилен присоединяет синильную кислоту в присутствии солей меди с образованием мономера – акрилонитрила: 4. Присоединение спиртов. 5. Гидратация. Алкины легко присоединяют воду и кислоты. Присоединение сильных кислот происходит без катализатора, а присоединение воды происходит в присутствии сульфата ртути Hg. SO 4 (реакция Кучерова): 11
АЛКИНЫ Реакции присоединения нуклеофилов: 3. Ацетилен присоединяет синильную кислоту в присутствии солей меди с образованием мономера – акрилонитрила: 4. Присоединение спиртов. 5. Гидратация. Алкины легко присоединяют воду и кислоты. Присоединение сильных кислот происходит без катализатора, а присоединение воды происходит в присутствии сульфата ртути Hg. SO 4 (реакция Кучерова): 11
 АЛКИНЫ 6. Металлирование. Реакция Фаворского Водородные атомы ацетилена способны замещаться металлами с образованием ацетиленидов. При этом ацетилен реагирует как более сильная кислота: Это качественные реакции на катионы Ag+ и Cu+, используемые в аналитической химии. Ацетилениды вступают в реакции нуклеофильного замещения или присоединения, например с кетонами, с образованием кислородсодержащих соединений – спиртов. Для этого используется смешанный ацетиленид магния (комплекс Иоцича), образующийся при действии ацетилена на магнийорганические соединения с 12 предельными радикалами:
АЛКИНЫ 6. Металлирование. Реакция Фаворского Водородные атомы ацетилена способны замещаться металлами с образованием ацетиленидов. При этом ацетилен реагирует как более сильная кислота: Это качественные реакции на катионы Ag+ и Cu+, используемые в аналитической химии. Ацетилениды вступают в реакции нуклеофильного замещения или присоединения, например с кетонами, с образованием кислородсодержащих соединений – спиртов. Для этого используется смешанный ацетиленид магния (комплекс Иоцича), образующийся при действии ацетилена на магнийорганические соединения с 12 предельными радикалами:
 АЛКИНЫ Для увеличения выхода спирта синтез проводят в абсолютном эфире в присутствии сухого порошкообразного KOH. Это реакция Фаворского: 13
АЛКИНЫ Для увеличения выхода спирта синтез проводят в абсолютном эфире в присутствии сухого порошкообразного KOH. Это реакция Фаворского: 13
 АЛКИНЫ В промышленности используют метод Реппе – конденсация ацетилена с муравьиным альдегидом в присутствии ацетиленида меди: 8. Реакция замещения водорода галогенами Водородные атомы у ацетиленовой связи могут замещаться на атомы галогенов при действии гипогалогенитов (Na. Cl. O). При использовании ацетилена образуются самовоспламеняющиеся на воздухе вещества: 14
АЛКИНЫ В промышленности используют метод Реппе – конденсация ацетилена с муравьиным альдегидом в присутствии ацетиленида меди: 8. Реакция замещения водорода галогенами Водородные атомы у ацетиленовой связи могут замещаться на атомы галогенов при действии гипогалогенитов (Na. Cl. O). При использовании ацетилена образуются самовоспламеняющиеся на воздухе вещества: 14
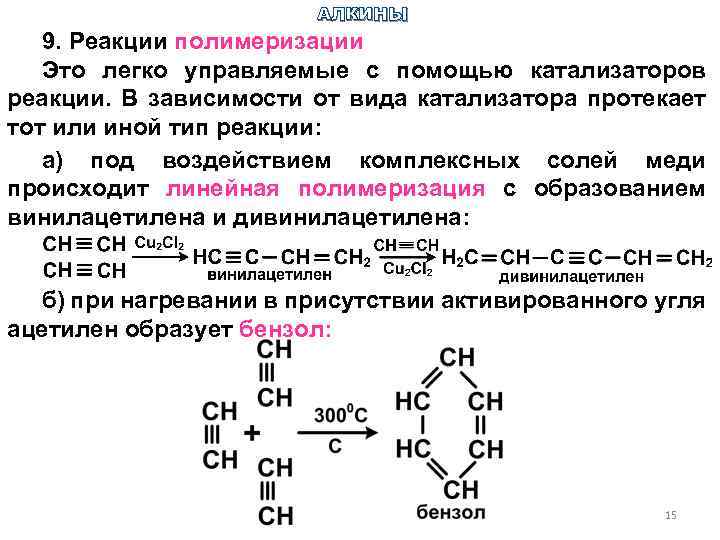 АЛКИНЫ 9. Реакции полимеризации Это легко управляемые с помощью катализаторов реакции. В зависимости от вида катализатора протекает тот или иной тип реакции: а) под воздействием комплексных солей меди происходит линейная полимеризация с образованием винилацетилена и дивинилацетилена: б) при нагревании в присутствии активированного угля ацетилен образует бензол: 15
АЛКИНЫ 9. Реакции полимеризации Это легко управляемые с помощью катализаторов реакции. В зависимости от вида катализатора протекает тот или иной тип реакции: а) под воздействием комплексных солей меди происходит линейная полимеризация с образованием винилацетилена и дивинилацетилена: б) при нагревании в присутствии активированного угля ацетилен образует бензол: 15
 АЛКИНЫ в) при действии на ацетилен комплексных соединений Ni образуются циклооктатетраен: 10. Изомеризация Это процесс, связанный с перемещением тройной связи или с превращением в диеновые угеводороды. Под действием щелочных металлов тройная связь переходит на конец молекулы, получаются ацетилениды. Действие спиртовых растворов щелочей способствует переходу ацетиленовой связи с конца молекулы в центр. Промежуточными продуктами в этих превращениях являются алленовые углеводороды: 16
АЛКИНЫ в) при действии на ацетилен комплексных соединений Ni образуются циклооктатетраен: 10. Изомеризация Это процесс, связанный с перемещением тройной связи или с превращением в диеновые угеводороды. Под действием щелочных металлов тройная связь переходит на конец молекулы, получаются ацетилениды. Действие спиртовых растворов щелочей способствует переходу ацетиленовой связи с конца молекулы в центр. Промежуточными продуктами в этих превращениях являются алленовые углеводороды: 16
 АЛКИНЫ В присутствии катализаторов алкины могут превращаться в сопряженные диеновые через стадию образования алленовых углеводородов: 17
АЛКИНЫ В присутствии катализаторов алкины могут превращаться в сопряженные диеновые через стадию образования алленовых углеводородов: 17


