3-ТВЕРДОЕ ТЕЛО.ppt
- Количество слайдов: 32
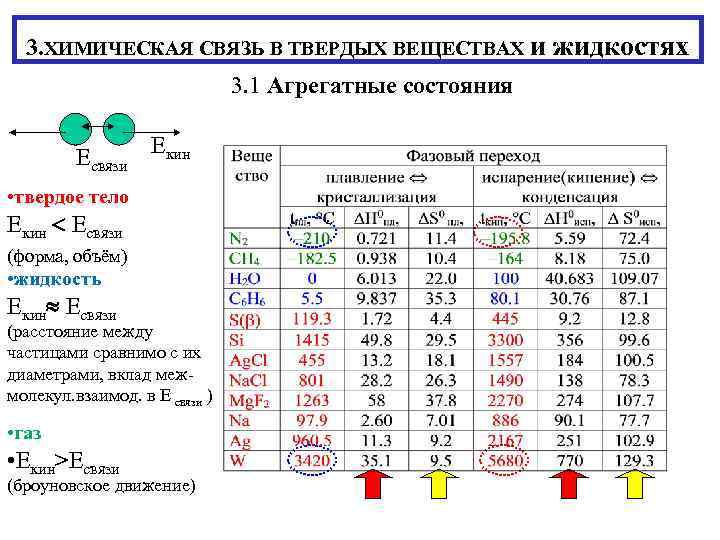 3. ХИМИЧЕСКАЯ СВЯЗЬ В ТВЕРДЫХ ВЕЩЕСТВАХ и жидкостях 3. 1 Агрегатные состояния Есвязи Екин • твердое тело Екин Есвязи (форма, объём) • жидкость Екин Есвязи (расстояние между частицами сравнимо с их диаметрами, вклад меж- молекул. взаимод. в Е связи ) • газ • Екин>Есвязи (броуновское движение)
3. ХИМИЧЕСКАЯ СВЯЗЬ В ТВЕРДЫХ ВЕЩЕСТВАХ и жидкостях 3. 1 Агрегатные состояния Есвязи Екин • твердое тело Екин Есвязи (форма, объём) • жидкость Екин Есвязи (расстояние между частицами сравнимо с их диаметрами, вклад меж- молекул. взаимод. в Е связи ) • газ • Екин>Есвязи (броуновское движение)
 Среднее расстояние (размеры пространства) между частицами 1 моль NA = 6. 02 1023 частиц Газ для одной частицы Кристалл(твёрдое в-во) V = 22. 4 л V = V / NA серебро a a d Жидкость - бром (Br 2) d Br 2 4. 5 А
Среднее расстояние (размеры пространства) между частицами 1 моль NA = 6. 02 1023 частиц Газ для одной частицы Кристалл(твёрдое в-во) V = 22. 4 л V = V / NA серебро a a d Жидкость - бром (Br 2) d Br 2 4. 5 А
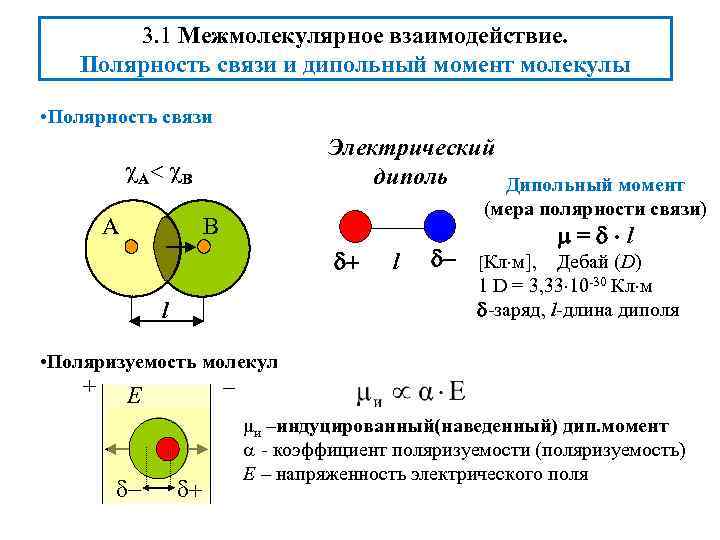 3. 1 Межмолекулярное взаимодействие. Полярность связи и дипольный момент молекулы • Полярность связи Электрический диполь Дипольный момент А В A (мера полярности связи) B l l = l [Кл м], Дебай (D) 1 D = 3, 33 10 -30 Кл м -заряд, l-длина диполя • Поляризуемость молекул + – Е μи –индуцированный(наведенный) дип. момент - коэффициент поляризуемости (поляризуемость) Е – напряженность электрического поля
3. 1 Межмолекулярное взаимодействие. Полярность связи и дипольный момент молекулы • Полярность связи Электрический диполь Дипольный момент А В A (мера полярности связи) B l l = l [Кл м], Дебай (D) 1 D = 3, 33 10 -30 Кл м -заряд, l-длина диполя • Поляризуемость молекул + – Е μи –индуцированный(наведенный) дип. момент - коэффициент поляризуемости (поляризуемость) Е – напряженность электрического поля
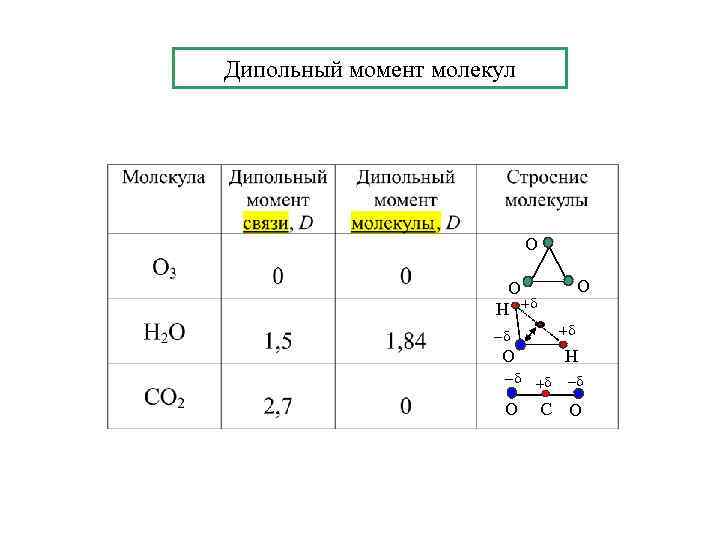 Дипольный момент молекул О О О Н + + О Н + O С O
Дипольный момент молекул О О О Н + + О Н + O С O
![Силы Ван-дер-Ваальса [без обмена электронами, межмолекулярное взаимодействие (притяжение) диполей] 1. Ориентационный эффект (Кьезома) (взаимодействие(электростатическое Силы Ван-дер-Ваальса [без обмена электронами, межмолекулярное взаимодействие (притяжение) диполей] 1. Ориентационный эффект (Кьезома) (взаимодействие(электростатическое](https://present5.com/presentation/122021610_416243412/image-5.jpg) Силы Ван-дер-Ваальса [без обмена электронами, межмолекулярное взаимодействие (притяжение) диполей] 1. Ориентационный эффект (Кьезома) (взаимодействие(электростатическое притяжение) пост. диполь – пост. диполь) + 1 + 2 + + 2. Индукционный эффект (Дебая ) (взаимодействие постоянный диполь – наведенный(индуцированный) диполь). + 3. Дисперсионный эффект (Лондона) (взаимодействие мгновенных диполей). 1 2
Силы Ван-дер-Ваальса [без обмена электронами, межмолекулярное взаимодействие (притяжение) диполей] 1. Ориентационный эффект (Кьезома) (взаимодействие(электростатическое притяжение) пост. диполь – пост. диполь) + 1 + 2 + + 2. Индукционный эффект (Дебая ) (взаимодействие постоянный диполь – наведенный(индуцированный) диполь). + 3. Дисперсионный эффект (Лондона) (взаимодействие мгновенных диполей). 1 2
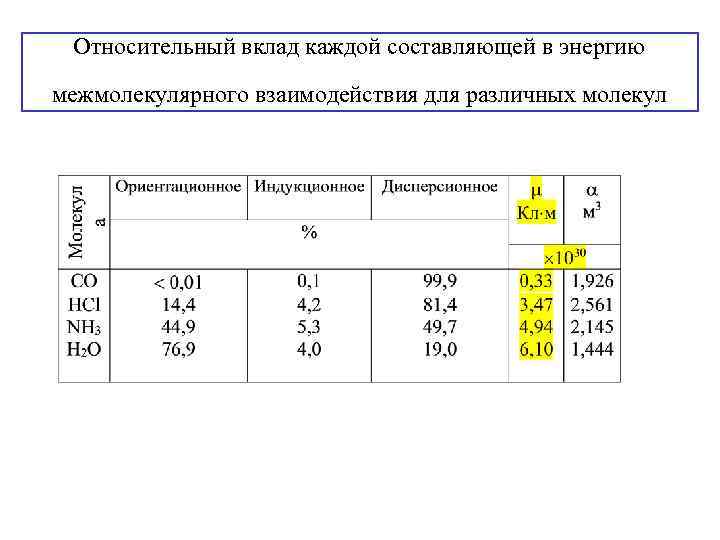 Относительный вклад каждой составляющей в энергию межмолекулярного взаимодействия для различных молекул
Относительный вклад каждой составляющей в энергию межмолекулярного взаимодействия для различных молекул
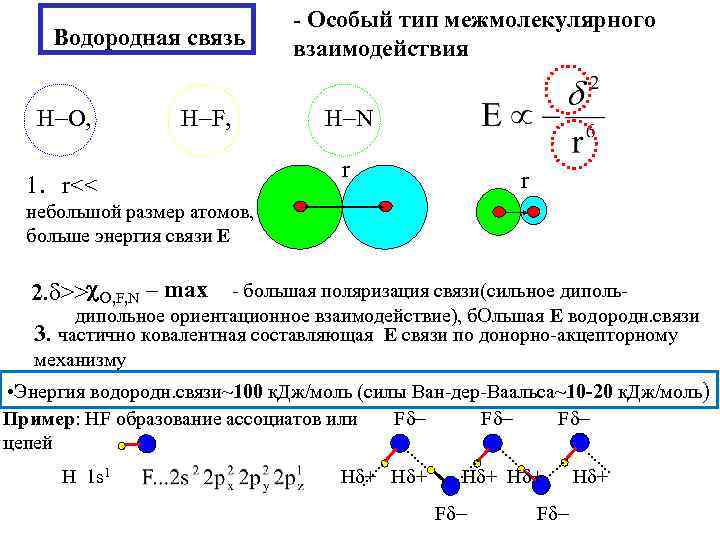 Водородная связь H O, H F, - Особый тип межмолекулярного взаимодействия H N r 1. r<< r небольшой размер атомов, больше энергия связи Е 2. >> O, F, N – max - большая поляризация связи(сильное диполь- дипольное ориентационное взаимодействие), б. Ольшая Е водородн. связи 3. частично ковалентная составляющая Е связи по донорно-акцепторному механизму • Энергия водородн. связи~100 к. Дж/моль (силы Ван-дер-Ваальса~10 -20 к. Дж/моль) F F Пример: HF образование ассоциатов или цепей H 1 s 1 H + H + F
Водородная связь H O, H F, - Особый тип межмолекулярного взаимодействия H N r 1. r<< r небольшой размер атомов, больше энергия связи Е 2. >> O, F, N – max - большая поляризация связи(сильное диполь- дипольное ориентационное взаимодействие), б. Ольшая Е водородн. связи 3. частично ковалентная составляющая Е связи по донорно-акцепторному механизму • Энергия водородн. связи~100 к. Дж/моль (силы Ван-дер-Ваальса~10 -20 к. Дж/моль) F F Пример: HF образование ассоциатов или цепей H 1 s 1 H + H + F
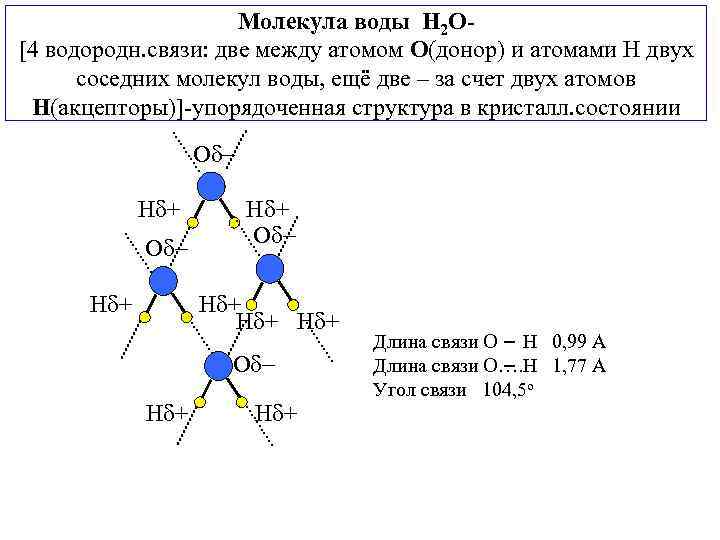 Молекула воды H 2 O[4 водородн. связи: две между атомом О(донор) и атомами Н двух соседних молекул воды, ещё две – за счет двух атомов Н(акцепторы)]-упорядоченная структура в кристалл. состоянии О Н + О О Н + Н + О Н + Длина связи О Н 0, 99 А Длина связи О…. Н 1, 77 А Угол связи 104, 5 о
Молекула воды H 2 O[4 водородн. связи: две между атомом О(донор) и атомами Н двух соседних молекул воды, ещё две – за счет двух атомов Н(акцепторы)]-упорядоченная структура в кристалл. состоянии О Н + О О Н + Н + О Н + Длина связи О Н 0, 99 А Длина связи О…. Н 1, 77 А Угол связи 104, 5 о
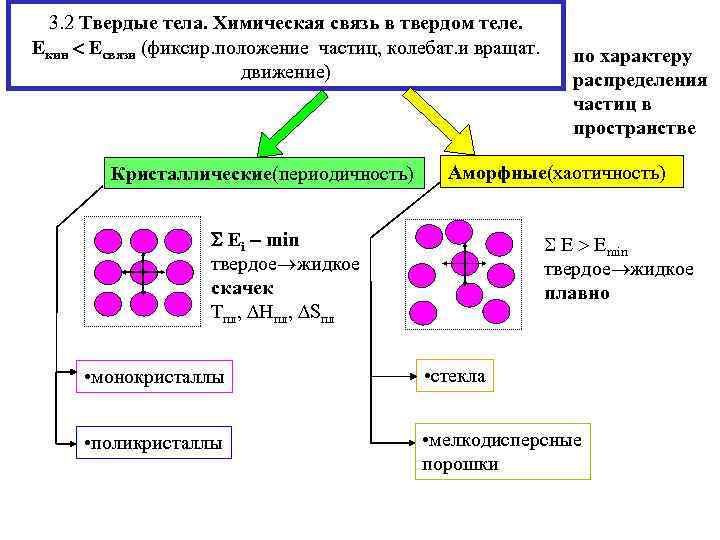 3. 2 Твердые тела. Химическая связь в твердом теле. Екин Есвязи (фиксир. положение частиц, колебат. и вращат. движение) Кристаллические(периодичность) по характеру распределения частиц в пространстве Аморфные(хаотичность) Еi min твердое жидкое скачек Тпл, Нпл, Sпл Е Еmin твердое жидкое плавно • монокристаллы • стекла • поликристаллы • мелкодисперсные порошки
3. 2 Твердые тела. Химическая связь в твердом теле. Екин Есвязи (фиксир. положение частиц, колебат. и вращат. движение) Кристаллические(периодичность) по характеру распределения частиц в пространстве Аморфные(хаотичность) Еi min твердое жидкое скачек Тпл, Нпл, Sпл Е Еmin твердое жидкое плавно • монокристаллы • стекла • поликристаллы • мелкодисперсные порошки
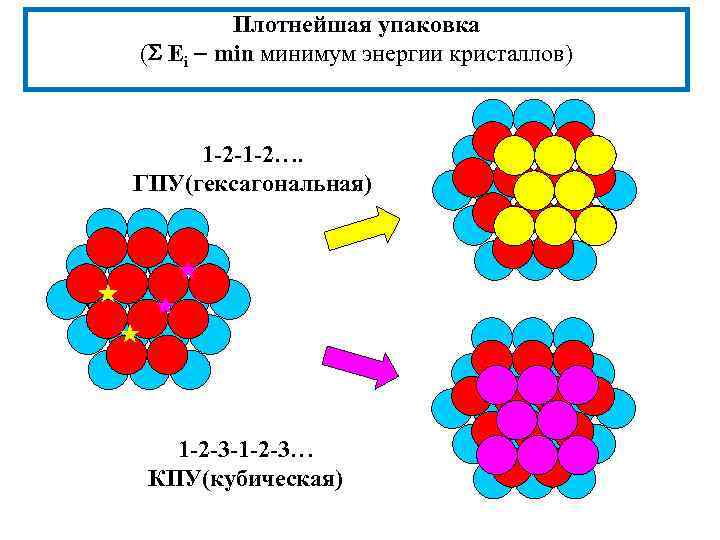 Плотнейшая упаковка ( Еi min минимум энергии кристаллов) 1 -2 -1 -2…. ГПУ(гексагональная) 1 -2 -3 -1 -2 -3… КПУ(кубическая)
Плотнейшая упаковка ( Еi min минимум энергии кристаллов) 1 -2 -1 -2…. ГПУ(гексагональная) 1 -2 -3 -1 -2 -3… КПУ(кубическая)
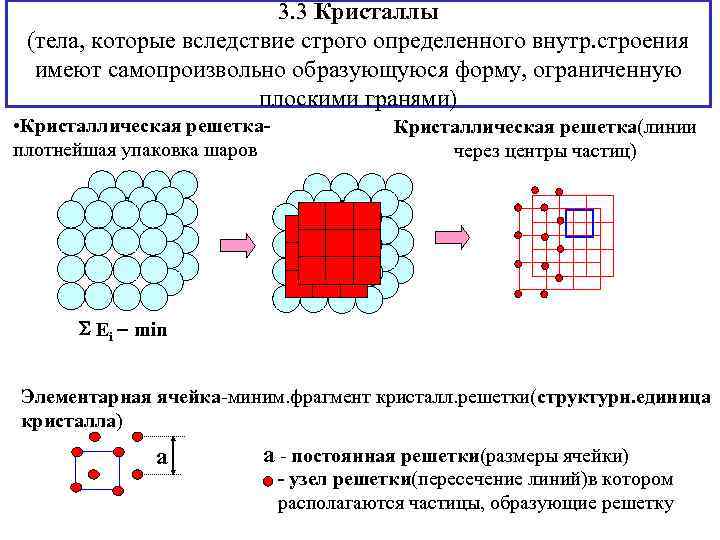 3. 3 Кристаллы (тела, которые вследствие строго определенного внутр. строения имеют самопроизвольно образующуюся форму, ограниченную плоскими гранями) • Кристаллическая решеткаплотнейшая упаковка шаров Кристаллическая решетка(линии через центры частиц) Еi min Элементарная ячейка-миним. фрагмент кристалл. решетки(структурн. единица кристалла) а а - постоянная решетки(размеры ячейки) - узел решетки(пересечение линий)в котором располагаются частицы, образующие решетку
3. 3 Кристаллы (тела, которые вследствие строго определенного внутр. строения имеют самопроизвольно образующуюся форму, ограниченную плоскими гранями) • Кристаллическая решеткаплотнейшая упаковка шаров Кристаллическая решетка(линии через центры частиц) Еi min Элементарная ячейка-миним. фрагмент кристалл. решетки(структурн. единица кристалла) а а - постоянная решетки(размеры ячейки) - узел решетки(пересечение линий)в котором располагаются частицы, образующие решетку
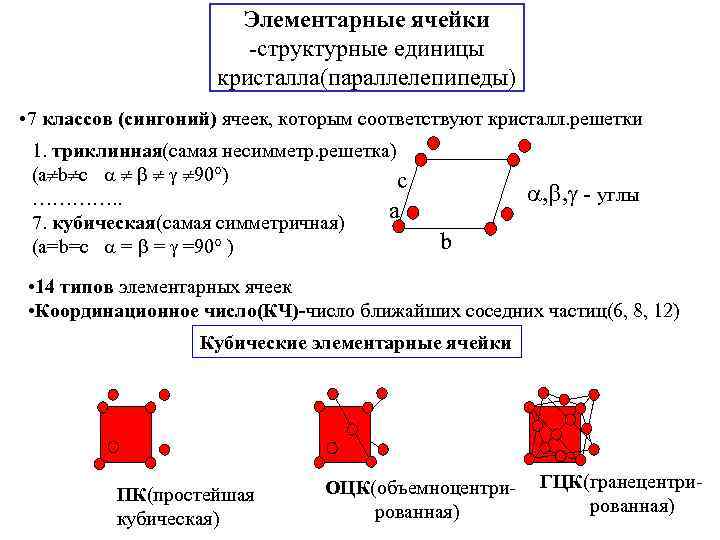 Элементарные ячейки -структурные единицы кристалла(параллелепипеды) • 7 классов (сингоний) ячеек, которым соответствуют кристалл. решетки 1. триклинная(самая несимметр. решетка) (a b c 90°) c …………. . а 7. кубическая(самая симметричная) (a=b=c = = =90° ) , , - углы b • 14 типов элементарных ячеек • Координационное число(КЧ)-число ближайших соседних частиц(6, 8, 12) Кубические элементарные ячейки ПК(простейшая кубическая) ОЦК(объемноцентри рованная) ГЦК(гранецентри рованная)
Элементарные ячейки -структурные единицы кристалла(параллелепипеды) • 7 классов (сингоний) ячеек, которым соответствуют кристалл. решетки 1. триклинная(самая несимметр. решетка) (a b c 90°) c …………. . а 7. кубическая(самая симметричная) (a=b=c = = =90° ) , , - углы b • 14 типов элементарных ячеек • Координационное число(КЧ)-число ближайших соседних частиц(6, 8, 12) Кубические элементарные ячейки ПК(простейшая кубическая) ОЦК(объемноцентри рованная) ГЦК(гранецентри рованная)
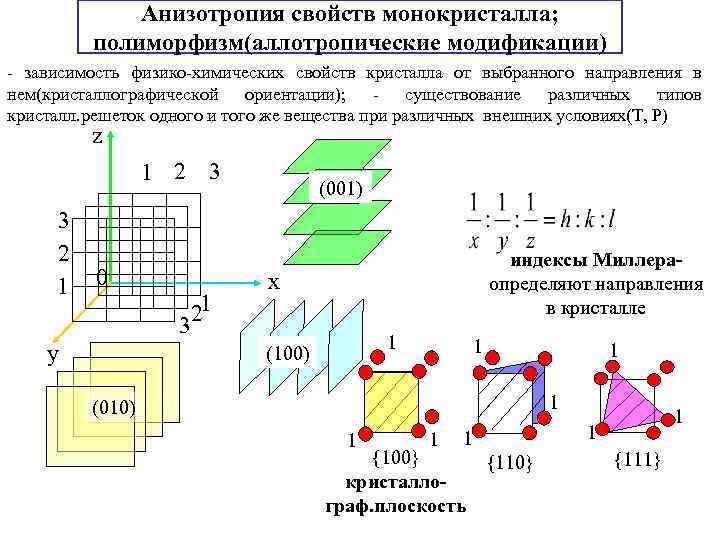 Анизотропия свойств монокристалла; полиморфизм(аллотропические модификации) - зависимость физико-химических свойств кристалла от выбранного направления в нем(кристаллографической ориентации); - существование различных типов кристалл. решеток одного и того же вещества при различных внешних условиях(Т, Р) z 1 2 3 3 2 1 0 y 1 2 3 (001) индексы Миллераопределяют направления в кристалле x 1 (100) (010) 1 0 1 1 {100} {110} кристаллограф. плоскость 1 1 0 {111} 1
Анизотропия свойств монокристалла; полиморфизм(аллотропические модификации) - зависимость физико-химических свойств кристалла от выбранного направления в нем(кристаллографической ориентации); - существование различных типов кристалл. решеток одного и того же вещества при различных внешних условиях(Т, Р) z 1 2 3 3 2 1 0 y 1 2 3 (001) индексы Миллераопределяют направления в кристалле x 1 (100) (010) 1 0 1 1 {100} {110} кристаллограф. плоскость 1 1 0 {111} 1
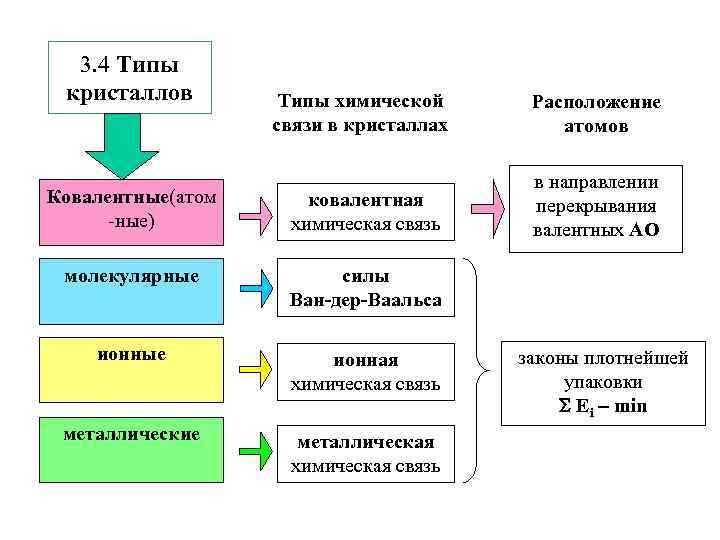 3. 4 Типы кристаллов Типы химической связи в кристаллах Расположение атомов Ковалентные(атом -ные) ковалентная химическая связь в направлении перекрывания валентных АО молекулярные силы Ван-дер-Ваальса ионные ионная химическая связь металлические металлическая химическая связь законы плотнейшей упаковки Еi min
3. 4 Типы кристаллов Типы химической связи в кристаллах Расположение атомов Ковалентные(атом -ные) ковалентная химическая связь в направлении перекрывания валентных АО молекулярные силы Ван-дер-Ваальса ионные ионная химическая связь металлические металлическая химическая связь законы плотнейшей упаковки Еi min
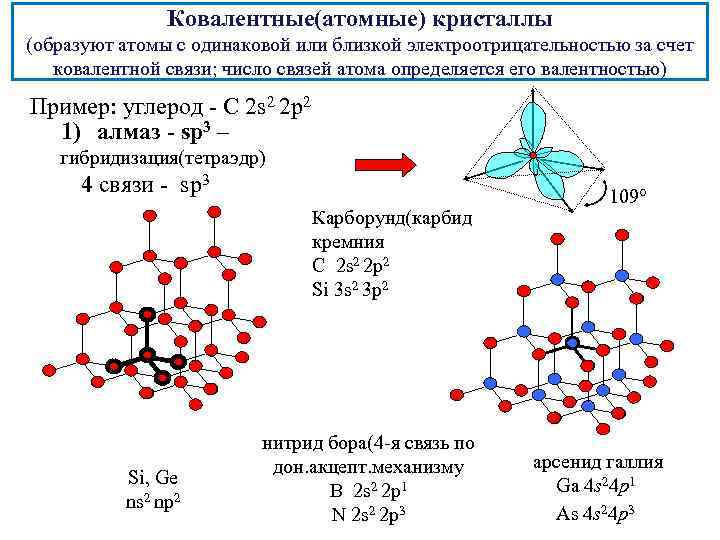 Ковалентные(атомные) кристаллы (образуют атомы с одинаковой или близкой электроотрицательностью за счет ковалентной связи; число связей атома определяется его валентностью) Пример: углерод - С 2 s 2 2 p 2 1) алмаз - sp 3 – гибридизация(тетраэдр) 4 связи - sp 3 Карборунд(карбид кремния С 2 s 2 2 p 2 Si 3 s 2 3 p 2 Si, Ge ns 2 np 2 нитрид бора(4 -я связь по дон. акцепт. механизму B 2 s 2 2 p 1 N 2 s 2 2 p 3 109 арсенид галлия Ga 4 s 24 p 1 As 4 s 24 p 3
Ковалентные(атомные) кристаллы (образуют атомы с одинаковой или близкой электроотрицательностью за счет ковалентной связи; число связей атома определяется его валентностью) Пример: углерод - С 2 s 2 2 p 2 1) алмаз - sp 3 – гибридизация(тетраэдр) 4 связи - sp 3 Карборунд(карбид кремния С 2 s 2 2 p 2 Si 3 s 2 3 p 2 Si, Ge ns 2 np 2 нитрид бора(4 -я связь по дон. акцепт. механизму B 2 s 2 2 p 1 N 2 s 2 2 p 3 109 арсенид галлия Ga 4 s 24 p 1 As 4 s 24 p 3
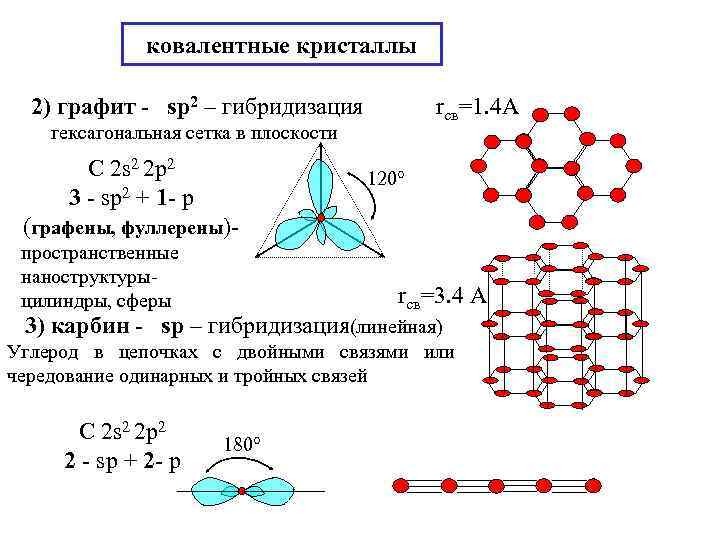 ковалентные кристаллы 2) графит - sp 2 – гибридизация rсв=1. 4 А гексагональная сетка в плоскости С 2 s 2 2 p 2 3 - sp 2 + 1 - р 120 (графены, фуллерены)пространственные наноструктурыцилиндры, сферы rсв=3. 4 А 3) карбин - sp – гибридизация(линейная) Углерод в цепочках с двойными связями или чередование одинарных и тройных связей С 2 s 2 2 p 2 2 - sp + 2 - р 180
ковалентные кристаллы 2) графит - sp 2 – гибридизация rсв=1. 4 А гексагональная сетка в плоскости С 2 s 2 2 p 2 3 - sp 2 + 1 - р 120 (графены, фуллерены)пространственные наноструктурыцилиндры, сферы rсв=3. 4 А 3) карбин - sp – гибридизация(линейная) Углерод в цепочках с двойными связями или чередование одинарных и тройных связей С 2 s 2 2 p 2 2 - sp + 2 - р 180
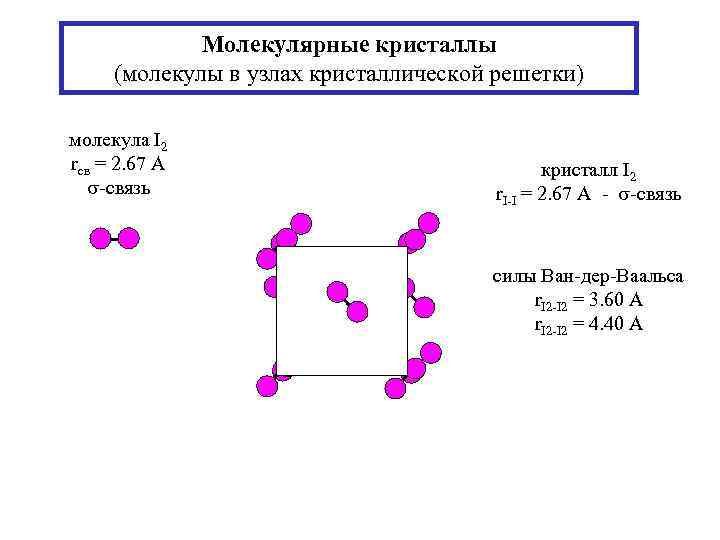 Молекулярные кристаллы (молекулы в узлах кристаллической решетки) молекула I 2 rсв = 2. 67 А -связь кристалл I 2 r. I-I = 2. 67 А - -связь силы Ван-дер-Ваальса r. I 2 -I 2 = 3. 60 А r. I 2 -I 2 = 4. 40 А
Молекулярные кристаллы (молекулы в узлах кристаллической решетки) молекула I 2 rсв = 2. 67 А -связь кристалл I 2 r. I-I = 2. 67 А - -связь силы Ван-дер-Ваальса r. I 2 -I 2 = 3. 60 А r. I 2 -I 2 = 4. 40 А
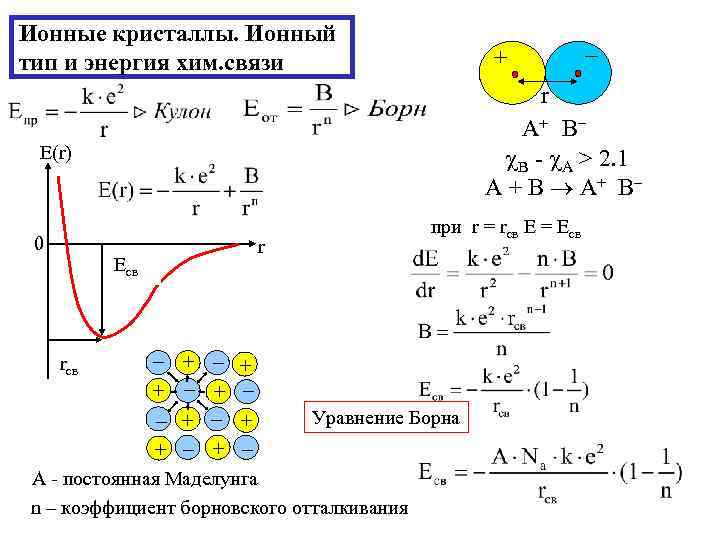 Ионные кристаллы. Ионный тип и энергия хим. связи + r АВ A+ B B - A > 2. 1 A + B A+ B E(r) 0 r Есв rсв + + + при r = rсв Е = Есв + Уравнение Борна + А - постоянная Маделунга n – коэффициент борновского отталкивания
Ионные кристаллы. Ионный тип и энергия хим. связи + r АВ A+ B B - A > 2. 1 A + B A+ B E(r) 0 r Есв rсв + + + при r = rсв Е = Есв + Уравнение Борна + А - постоянная Маделунга n – коэффициент борновского отталкивания
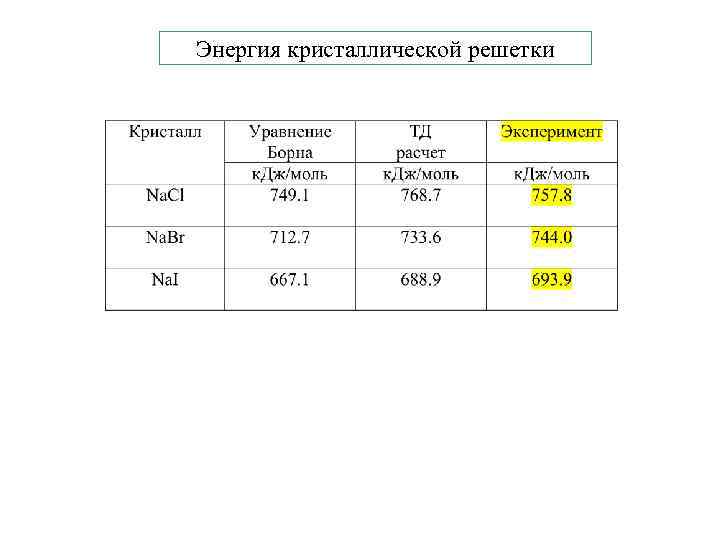 Энергия кристаллической решетки
Энергия кристаллической решетки
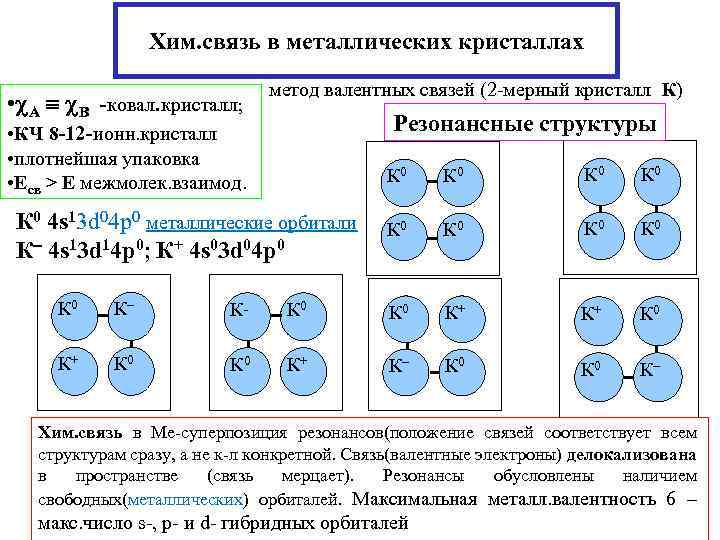 Хим. связь в металлических кристаллах • A B -ковал. кристалл; • КЧ 8 -12 -ионн. кристалл метод валентных связей (2 -мерный кристалл К) Резонансные структуры • плотнейшая упаковка • Есв > Е межмолек. взаимод. К 0 К 0 К 0 К+ К+ К 0 К+ К К 0 4 s 13 d 04 р0 металлические орбитали К 4 s 13 d 14 р0; К+ 4 s 03 d 04 р0 К К К+ К 0 Хим. связь в Ме-суперпозиция резонансов(положение связей соответствует всем структурам сразу, а не к-л конкретной. Связь(валентные электроны) делокализована в пространстве (связь мерцает). Резонансы обусловлены наличием свободных(металлических) орбиталей. Максимальная металл. валентность 6 – макс. число s-, p- и d- гибридных орбиталей
Хим. связь в металлических кристаллах • A B -ковал. кристалл; • КЧ 8 -12 -ионн. кристалл метод валентных связей (2 -мерный кристалл К) Резонансные структуры • плотнейшая упаковка • Есв > Е межмолек. взаимод. К 0 К 0 К 0 К+ К+ К 0 К+ К К 0 4 s 13 d 04 р0 металлические орбитали К 4 s 13 d 14 р0; К+ 4 s 03 d 04 р0 К К К+ К 0 Хим. связь в Ме-суперпозиция резонансов(положение связей соответствует всем структурам сразу, а не к-л конкретной. Связь(валентные электроны) делокализована в пространстве (связь мерцает). Резонансы обусловлены наличием свободных(металлических) орбиталей. Максимальная металл. валентность 6 – макс. число s-, p- и d- гибридных орбиталей
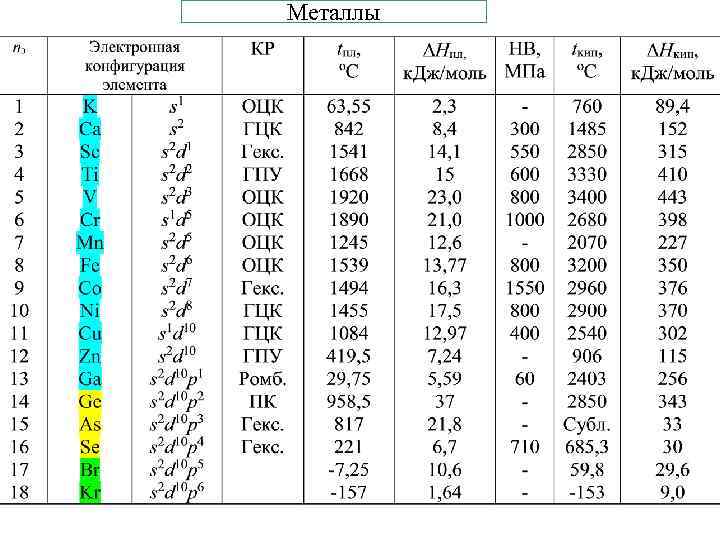 Металлы
Металлы
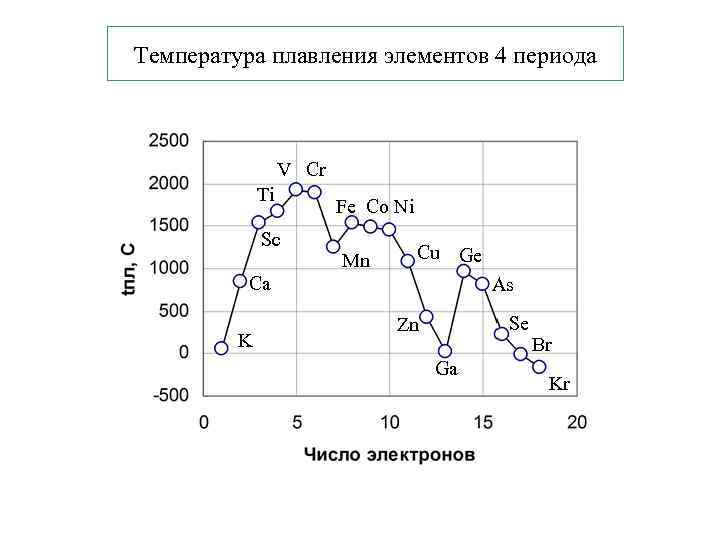 Температура плавления элементов 4 периода V Cr Ti Sc Fe Co Ni Cu Ge Mn Ca As K Se Zn Br Ga Kr
Температура плавления элементов 4 периода V Cr Ti Sc Fe Co Ni Cu Ge Mn Ca As K Se Zn Br Ga Kr
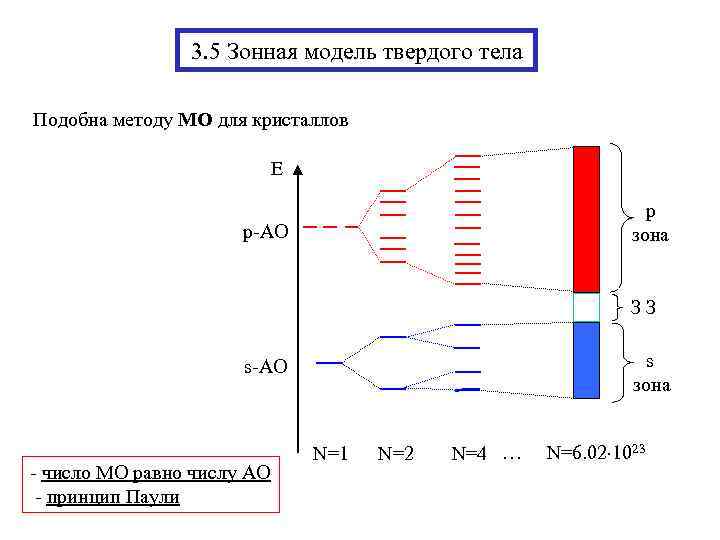 3. 5 Зонная модель твердого тела Подобна методу МО для кристаллов E p зона p-АО З З s зона s-АО - число МО равно числу АО - принцип Паули N=1 N=2 N=4 … N=6. 02 1023
3. 5 Зонная модель твердого тела Подобна методу МО для кристаллов E p зона p-АО З З s зона s-АО - число МО равно числу АО - принцип Паули N=1 N=2 N=4 … N=6. 02 1023
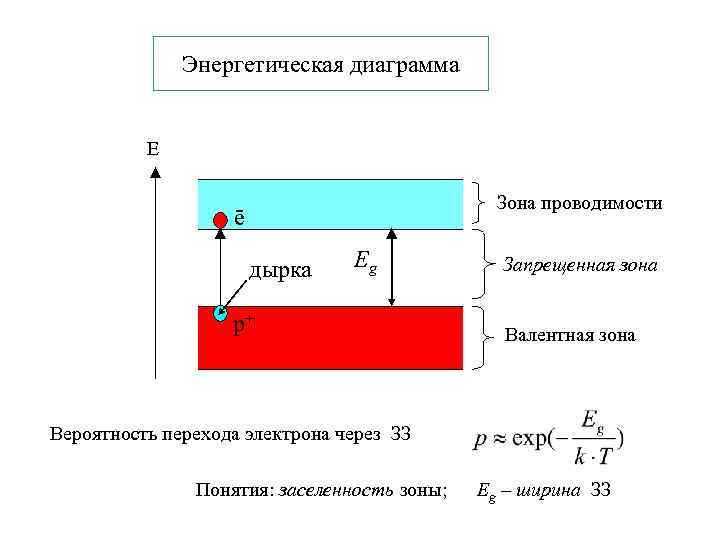 Энергетическая диаграмма Е Зона проводимости ē дырка Eg р+ Запрещенная зона Валентная зона Вероятность перехода электрона через ЗЗ Понятия: заселенность зоны; Eg – ширина ЗЗ
Энергетическая диаграмма Е Зона проводимости ē дырка Eg р+ Запрещенная зона Валентная зона Вероятность перехода электрона через ЗЗ Понятия: заселенность зоны; Eg – ширина ЗЗ
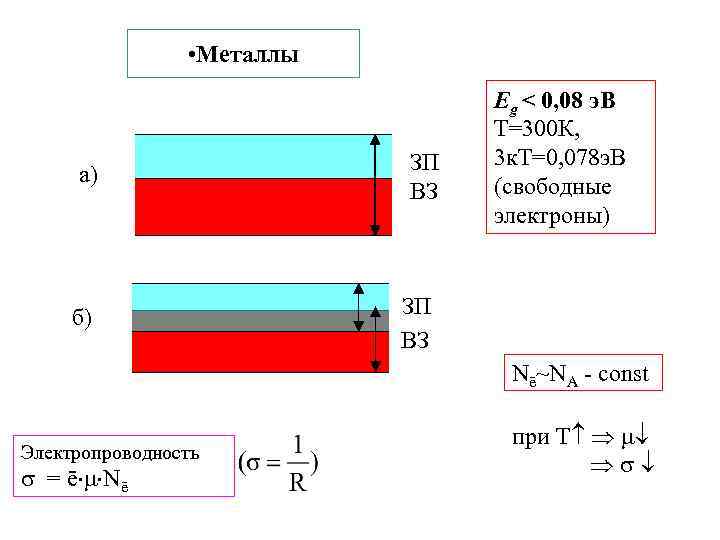 • Металлы а) б) ЗП ВЗ Eg < 0, 08 э. В Т=300 К, 3 к. Т=0, 078 э. В (свободные электроны) ЗП ВЗ Nē~NА - const Электропроводность = ē Nē при Т
• Металлы а) б) ЗП ВЗ Eg < 0, 08 э. В Т=300 К, 3 к. Т=0, 078 э. В (свободные электроны) ЗП ВЗ Nē~NА - const Электропроводность = ē Nē при Т
 • Диэлектрики Eg > > 3 э. В > > к. Т-энергии тепловых колебаний Eg Nē = 0
• Диэлектрики Eg > > 3 э. В > > к. Т-энергии тепловых колебаний Eg Nē = 0
 • Полупроводник 0, 08 э. В < Eg < 3 э. В ЗП ē ВЗ Eg р+ при T=0 K при T>>0 K Nē; Nр = 0 (T=0 K) = 0 Nē; Nр f(T) = ē ē Nē + ē р Nр
• Полупроводник 0, 08 э. В < Eg < 3 э. В ЗП ē ВЗ Eg р+ при T=0 K при T>>0 K Nē; Nр = 0 (T=0 K) = 0 Nē; Nр f(T) = ē ē Nē + ē р Nр
 3. 6 Кристаллические материалы • Дефекты кристаллической решетки Электронные(электронно-дырочная пара, несимм. разрыв хим. св. ) ē-р(А - А+); Экситоны(без разрыва хим. связи) ex 0 (А*) - 2 простейших точечных дефекта Точечные дефекты(нарушение регулярности): собственные: вакансии(отсутствие частицы в узле решетки; межузельные атомы или ионы A* AG V Ai A+ A- примесные (случайные или спец. вводятся) Линейные дефекты(дислокации)-линии вдоль которых нарушено правильное чередование атомных плоскостей(краевые, винтовые) Двумерные(поверхности, границы кристаллических зерен) Объемные(пузыри)
3. 6 Кристаллические материалы • Дефекты кристаллической решетки Электронные(электронно-дырочная пара, несимм. разрыв хим. св. ) ē-р(А - А+); Экситоны(без разрыва хим. связи) ex 0 (А*) - 2 простейших точечных дефекта Точечные дефекты(нарушение регулярности): собственные: вакансии(отсутствие частицы в узле решетки; межузельные атомы или ионы A* AG V Ai A+ A- примесные (случайные или спец. вводятся) Линейные дефекты(дислокации)-линии вдоль которых нарушено правильное чередование атомных плоскостей(краевые, винтовые) Двумерные(поверхности, границы кристаллических зерен) Объемные(пузыри)
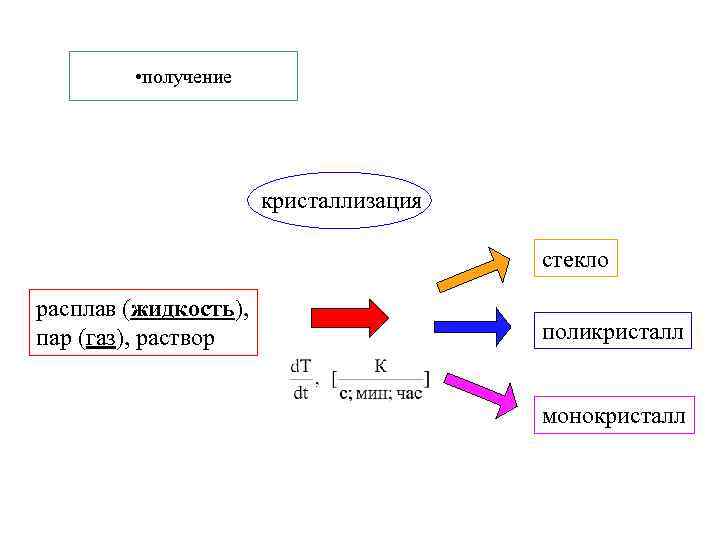 • получение кристаллизация стекло расплав (жидкость), пар (газ), раствор поликристалл монокристалл
• получение кристаллизация стекло расплав (жидкость), пар (газ), раствор поликристалл монокристалл
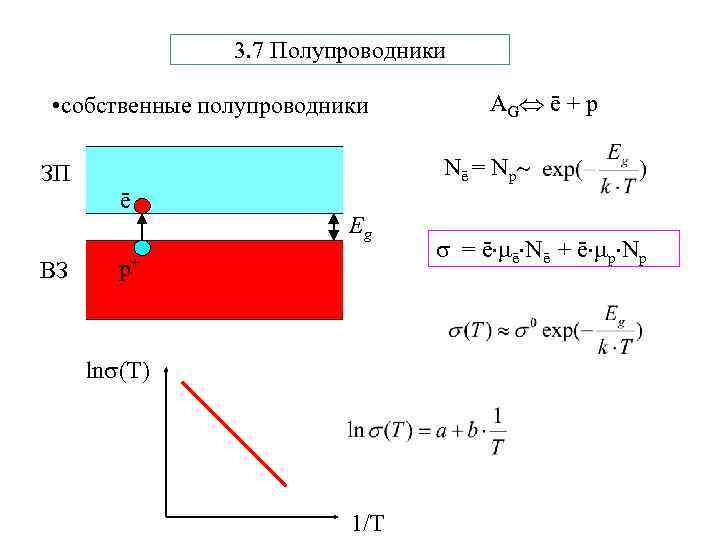 3. 7 Полупроводники • собственные полупроводники Nē = Nр ЗП ē ВЗ AG ē + p Eg р+ ln (T) 1/T = ē ē Nē + ē р Nр
3. 7 Полупроводники • собственные полупроводники Nē = Nр ЗП ē ВЗ AG ē + p Eg р+ ln (T) 1/T = ē ē Nē + ē р Nр
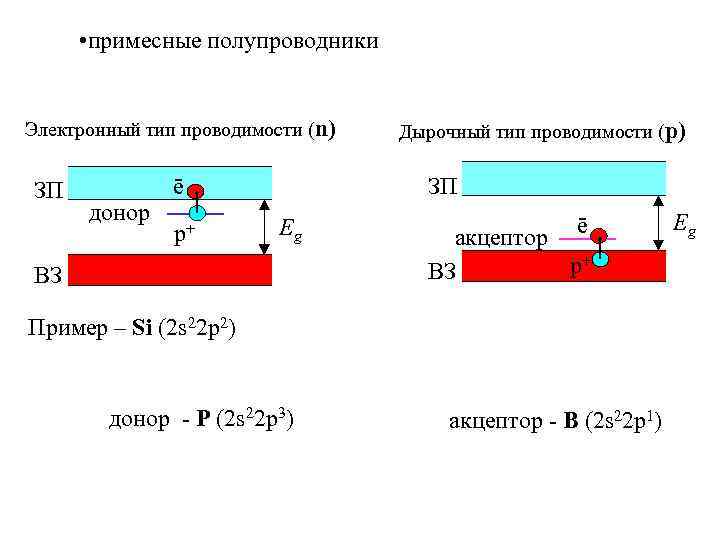 • примесные полупроводники Электронный тип проводимости (n) ЗП донор ē р+ Дырочный тип проводимости (р) ЗП Eg ВЗ ē акцептор р+ ВЗ Пример – Si (2 s 22 p 2) донор - P (2 s 22 p 3) акцептор - B (2 s 22 p 1) Eg
• примесные полупроводники Электронный тип проводимости (n) ЗП донор ē р+ Дырочный тип проводимости (р) ЗП Eg ВЗ ē акцептор р+ ВЗ Пример – Si (2 s 22 p 2) донор - P (2 s 22 p 3) акцептор - B (2 s 22 p 1) Eg
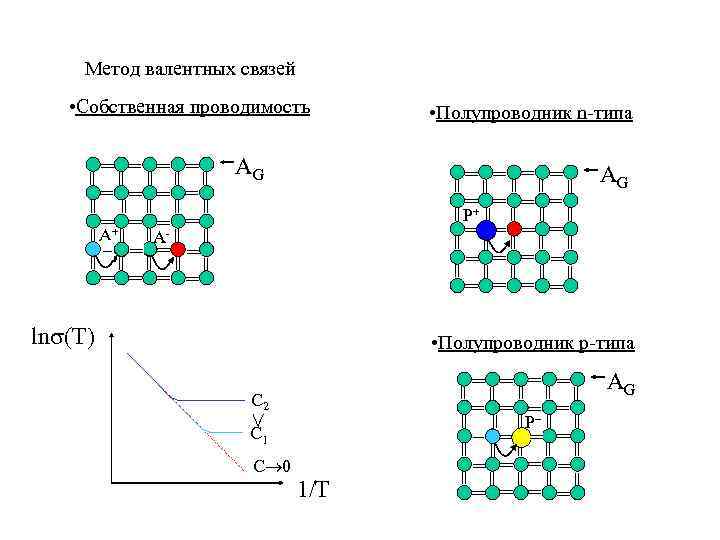 Метод валентных связей • Собственная проводимость = = = A= = = = AG = = Р+ = = = = = = = = ē = = = = = A+ ē = = • Полупроводник n-типа AG = = = = = = = = ln (T) • Полупроводник p-типа = = = = Р = = = = = < С 2 = = = С 1 1/T = = = С 0 = = = AG
Метод валентных связей • Собственная проводимость = = = A= = = = AG = = Р+ = = = = = = = = ē = = = = = A+ ē = = • Полупроводник n-типа AG = = = = = = = = ln (T) • Полупроводник p-типа = = = = Р = = = = = < С 2 = = = С 1 1/T = = = С 0 = = = AG


