TSM_4_Poverkhnost_2014.pptx
- Количество слайдов: 25
 3 ПОВЕРХНОСТЬ ТВЕРДОГО ТЕЛА Поверхность твердого тела есть обобщенное понятие. Все объемные, плоские тела имеют поверхность. В обычной жизни об этом на задумываются. А в машиностроении? Когда, где и как приходится обращать внимание на поверхность, учитывать ее характеристики.
3 ПОВЕРХНОСТЬ ТВЕРДОГО ТЕЛА Поверхность твердого тела есть обобщенное понятие. Все объемные, плоские тела имеют поверхность. В обычной жизни об этом на задумываются. А в машиностроении? Когда, где и как приходится обращать внимание на поверхность, учитывать ее характеристики.
 3 ПОВЕРХНОСТЬ ТВЕРДОГО ТЕЛА Поверхность твердого тела есть обобщенное понятие. Все объемные, плоские тела имеют поверхность. В обычной жизни об этом на задумываются. А в машиностроении? Когда, где и как приходится обращать внимание на поверхность, учитывать ее характеристики. Получение деталей с заданной шероховатостью. Очистка поверхности перед технологическими операциями. Поверхностная обработка деталей. Исследование микроструктуры материала. Вакуумные технологии в микроэлектронике. Влияние поверхности на механические свойства. Какие свойства материала и деталей определяются состоянием поверхности ? Какие характеристики поверхности определяют ее свойства?
3 ПОВЕРХНОСТЬ ТВЕРДОГО ТЕЛА Поверхность твердого тела есть обобщенное понятие. Все объемные, плоские тела имеют поверхность. В обычной жизни об этом на задумываются. А в машиностроении? Когда, где и как приходится обращать внимание на поверхность, учитывать ее характеристики. Получение деталей с заданной шероховатостью. Очистка поверхности перед технологическими операциями. Поверхностная обработка деталей. Исследование микроструктуры материала. Вакуумные технологии в микроэлектронике. Влияние поверхности на механические свойства. Какие свойства материала и деталей определяются состоянием поверхности ? Какие характеристики поверхности определяют ее свойства?
 3. 1 ОСОБЕННОСТИ СОСТОЯНИЯ ПОВЕРХНОСНОГО СЛОЯ Что такое поверхность? Обрыв объемного твердого тела. Граница твердая фаз – газ. Особенность структуры поверхности на атомном уровне можно показать на рисунке Из рисунка можно увидеть особенности энергетического состояния отдельного атома на поверхности и сравнить с состоянием в объеме.
3. 1 ОСОБЕННОСТИ СОСТОЯНИЯ ПОВЕРХНОСНОГО СЛОЯ Что такое поверхность? Обрыв объемного твердого тела. Граница твердая фаз – газ. Особенность структуры поверхности на атомном уровне можно показать на рисунке Из рисунка можно увидеть особенности энергетического состояния отдельного атома на поверхности и сравнить с состоянием в объеме.
 На практике под понятием ПОВЕРХНОСТЬ имеется ввиду поверхностный слой некоторой толщины. Особенности состояния поверхности: искажение кристаллической решетки, изменение взаимного (соседи), расположения изменение атомов химического состава (диффузия). Физические, химические (оксиды) неоднородности. На практике эти особенности проявляют себя в поверхностном слое толщиной до 5 – 20 межатомных расстояний. В общем случае необходимо рассматривать поверхностный слой и объемный материал как две разные системы, каждая из которых имеет свои особенности.
На практике под понятием ПОВЕРХНОСТЬ имеется ввиду поверхностный слой некоторой толщины. Особенности состояния поверхности: искажение кристаллической решетки, изменение взаимного (соседи), расположения изменение атомов химического состава (диффузия). Физические, химические (оксиды) неоднородности. На практике эти особенности проявляют себя в поверхностном слое толщиной до 5 – 20 межатомных расстояний. В общем случае необходимо рассматривать поверхностный слой и объемный материал как две разные системы, каждая из которых имеет свои особенности.
 3. 2 ПОВЕРХНОСТНАЯ ЭНЕРГИЯ Одной из главных характеристик поверхности является поверхностная энергия. С позиций термодинамики назовем ее свободная поверхностная энергия или удельная поверхностная энергия σ. F = E – TS и ∆F = ∆E - T∆S Здесь s – площадь поверхности. σ = ∆F/ s, Физический смысл σ : 1. Атомы на поверхности обладают большей энергией, чем атомы в объеме. Этот избыток на единичной площади и определяет величину поверхностной энергии σ. Или 2. Это энергия (работа), которая необходима для образования единицы новой площади поверхности. Из термодинамики известно, что всякая система стремиться к состоянию с минимальной энергией, т. е. при самопроизвольном процессе ∆F < 0 и наоборот, если в процессе ∆F > 0, то такой процесс является вынужденным. Данные условия проявляются при образовании и росте кристаллов и при формировании их поверхности.
3. 2 ПОВЕРХНОСТНАЯ ЭНЕРГИЯ Одной из главных характеристик поверхности является поверхностная энергия. С позиций термодинамики назовем ее свободная поверхностная энергия или удельная поверхностная энергия σ. F = E – TS и ∆F = ∆E - T∆S Здесь s – площадь поверхности. σ = ∆F/ s, Физический смысл σ : 1. Атомы на поверхности обладают большей энергией, чем атомы в объеме. Этот избыток на единичной площади и определяет величину поверхностной энергии σ. Или 2. Это энергия (работа), которая необходима для образования единицы новой площади поверхности. Из термодинамики известно, что всякая система стремиться к состоянию с минимальной энергией, т. е. при самопроизвольном процессе ∆F < 0 и наоборот, если в процессе ∆F > 0, то такой процесс является вынужденным. Данные условия проявляются при образовании и росте кристаллов и при формировании их поверхности.
 3. 3 МОДЕЛЬ ПОВЕРХНОСТИ Ученые Коссель и Сперанский предложили модель поверхности, на которой можно показать элементы структуры реального кристаллического тела (вакансии, дислокации), а также рассмотреть энергетическое состояние отдельных атомов (связь их поверхностью).
3. 3 МОДЕЛЬ ПОВЕРХНОСТИ Ученые Коссель и Сперанский предложили модель поверхности, на которой можно показать элементы структуры реального кристаллического тела (вакансии, дислокации), а также рассмотреть энергетическое состояние отдельных атомов (связь их поверхностью).

 Энергию связи атома с поверхностью можно определить по формуле Е = n(1) E 1 + n(2) E 2 где n(1) – число ближайших соседей, и энергия связи между ними - E 1 n(2) – число соседей 2 -го порядка и энергия связи между ними - E 2 Принято считать E 2 = 0. 1 E 1 Пример расчета энергии связи атома № 2 с поверхностью n(1) = 3, n(2) = 3 Е (2) = 3 E 1 + 3 E 2 = 3. 1 Е 1 атома № 4 с поверхностью. . . соседи 1 -го порядка соседи 2 -го порядка 1 2 3 4 5 6 7 8 9 10 11 12
Энергию связи атома с поверхностью можно определить по формуле Е = n(1) E 1 + n(2) E 2 где n(1) – число ближайших соседей, и энергия связи между ними - E 1 n(2) – число соседей 2 -го порядка и энергия связи между ними - E 2 Принято считать E 2 = 0. 1 E 1 Пример расчета энергии связи атома № 2 с поверхностью n(1) = 3, n(2) = 3 Е (2) = 3 E 1 + 3 E 2 = 3. 1 Е 1 атома № 4 с поверхностью. . . соседи 1 -го порядка соседи 2 -го порядка 1 2 3 4 5 6 7 8 9 10 11 12
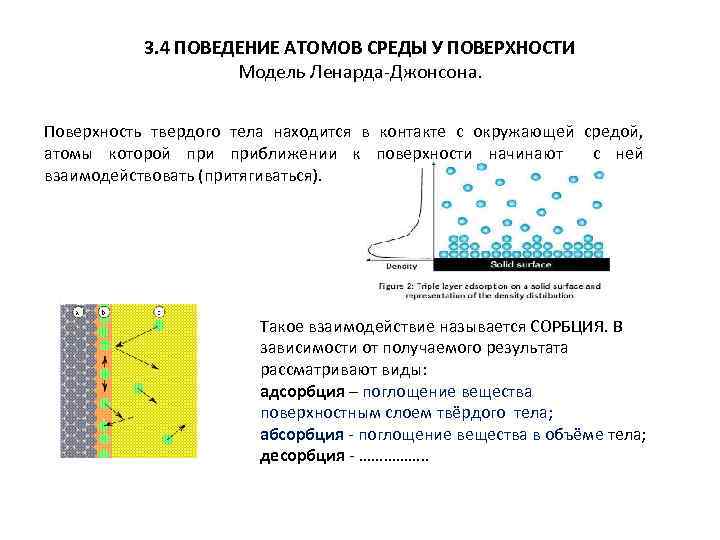 3. 4 ПОВЕДЕНИЕ АТОМОВ СРЕДЫ У ПОВЕРХНОСТИ Модель Ленарда-Джонсона. Поверхность твердого тела находится в контакте с окружающей средой, атомы которой приближении к поверхности начинают с ней взаимодействовать (притягиваться). Такое взаимодействие называется СОРБЦИЯ. В зависимости от получаемого результата рассматривают виды: адсорбция – поглощение вещества поверхностным слоем твёрдого тела; абсорбция - поглощение вещества в объёме тела; десорбция - ……………. .
3. 4 ПОВЕДЕНИЕ АТОМОВ СРЕДЫ У ПОВЕРХНОСТИ Модель Ленарда-Джонсона. Поверхность твердого тела находится в контакте с окружающей средой, атомы которой приближении к поверхности начинают с ней взаимодействовать (притягиваться). Такое взаимодействие называется СОРБЦИЯ. В зависимости от получаемого результата рассматривают виды: адсорбция – поглощение вещества поверхностным слоем твёрдого тела; абсорбция - поглощение вещества в объёме тела; десорбция - ……………. .
 адсорбция – поглощение вещества поверхностным слоем твёрдого тела; абсорбция - поглощение вещества в объёме тела;
адсорбция – поглощение вещества поверхностным слоем твёрдого тела; абсорбция - поглощение вещества в объёме тела;
 Сложный характер поведения атомов на поверхности
Сложный характер поведения атомов на поверхности
 Модель Ленарда-Джонсона. Потенциал Леннард-Джонса — простая модель парного взаимодействия молекул, описывающая зависимость энергии взаимодействия двух частиц от расстояния между ними. Эта модель достаточно реалистично передаёт свойства реального взаимодействия сферических молекул и поэтому широко используется в расчётах и при компьютерном моделировании. Джон Эдвард Леннард-Джонс (1894 -1954)
Модель Ленарда-Джонсона. Потенциал Леннард-Джонса — простая модель парного взаимодействия молекул, описывающая зависимость энергии взаимодействия двух частиц от расстояния между ними. Эта модель достаточно реалистично передаёт свойства реального взаимодействия сферических молекул и поэтому широко используется в расчётах и при компьютерном моделировании. Джон Эдвард Леннард-Джонс (1894 -1954)
 В зависимости от расстояния до которого сближается адсорбированный атом с поверхностью в модели Ленарда-Джонсона рассматривают два вида адсорбции, которые различаются энергетическими характеристиками (см. рис. ): физическая адсорбция и химическая адсорбция или хемосорбция.
В зависимости от расстояния до которого сближается адсорбированный атом с поверхностью в модели Ленарда-Джонсона рассматривают два вида адсорбции, которые различаются энергетическими характеристиками (см. рис. ): физическая адсорбция и химическая адсорбция или хемосорбция.
 В зависимости от расстояния до которого сближается адсорбированный атом с поверхностью в модели Ленарда-Джонсона рассматривают два вида адсорбции, которые различаются энергетическими характеристиками (см. рис. ): физическая адсорбция и химическая адсорбция или хемосорбция.
В зависимости от расстояния до которого сближается адсорбированный атом с поверхностью в модели Ленарда-Джонсона рассматривают два вида адсорбции, которые различаются энергетическими характеристиками (см. рис. ): физическая адсорбция и химическая адсорбция или хемосорбция.
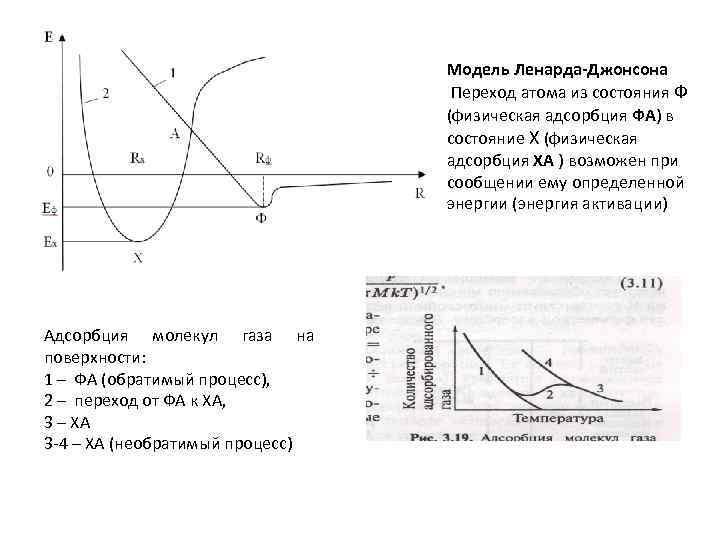 Модель Ленарда-Джонсона Переход атома из состояния Ф (физическая адсорбция ФА) в состояние Х (физическая адсорбция ХА ) возможен при сообщении ему определенной энергии (энергия активации) Адсорбция молекул газа на поверхности: 1 – ФА (обратимый процесс), 2 – переход от ФА к ХА, 3 – ХА 3 -4 – ХА (необратимый процесс)
Модель Ленарда-Джонсона Переход атома из состояния Ф (физическая адсорбция ФА) в состояние Х (физическая адсорбция ХА ) возможен при сообщении ему определенной энергии (энергия активации) Адсорбция молекул газа на поверхности: 1 – ФА (обратимый процесс), 2 – переход от ФА к ХА, 3 – ХА 3 -4 – ХА (необратимый процесс)
 Сравнительные характеристики физической и химической адсорбций Физическая адсорбция Хемосорбция Процесс обратимый: Процесс практически Концентрация адсорбента необратимый С ростом Т увеличивается С уменьшением Т возрастает Энергия активации Е = 10 – 40 к. Дж/моль Е сравнима с энергией конденсации Энергия активации Е = 50 – 400 к. Дж/моль Е сравнима с энергией химической реакции
Сравнительные характеристики физической и химической адсорбций Физическая адсорбция Хемосорбция Процесс обратимый: Процесс практически Концентрация адсорбента необратимый С ростом Т увеличивается С уменьшением Т возрастает Энергия активации Е = 10 – 40 к. Дж/моль Е сравнима с энергией конденсации Энергия активации Е = 50 – 400 к. Дж/моль Е сравнима с энергией химической реакции


 Весна 2015 Технология формирования покрытий Одной из самых главных характеристик покрытия любого назначения является адгезия, т. е. прочность сцепления покрытия с основой. Наиболее общим правилом получения высокой адгезии, т. е. прочного сцепления покрытия с основным материалом, являются два условия – физический контакт (ФК) между покрытием и подложкой и химическое взаимодействие (ХВ) на границе двух контактирующих фаз. От того как обеспечены эти два условия зависит величина адгезии σадг. В технологии вакуумного конденсационного напыления получения покрытий (ВКНП) за счет напыления частиц или осаждения пара покрытие формируется из потока частиц, находящихся в атомарном, молекулярном или их ионизированном состоянии. Physical Vapour Deposinion – физическое осаждение из паровой фазы.
Весна 2015 Технология формирования покрытий Одной из самых главных характеристик покрытия любого назначения является адгезия, т. е. прочность сцепления покрытия с основой. Наиболее общим правилом получения высокой адгезии, т. е. прочного сцепления покрытия с основным материалом, являются два условия – физический контакт (ФК) между покрытием и подложкой и химическое взаимодействие (ХВ) на границе двух контактирующих фаз. От того как обеспечены эти два условия зависит величина адгезии σадг. В технологии вакуумного конденсационного напыления получения покрытий (ВКНП) за счет напыления частиц или осаждения пара покрытие формируется из потока частиц, находящихся в атомарном, молекулярном или их ионизированном состоянии. Physical Vapour Deposinion – физическое осаждение из паровой фазы.
 Поведение атомов пара у поверхности В отличие от способов получения покрытий методом погружения в расплав и методом химического осаждения покрытий в технологии вакуумного конденсационного напыления (осаждении) главным механизмом формирования покрытия является взаимодействие отдельных атомов (молекул, ионов) с обрабатываемей поверхностью. Характер этого взаимодействия, т. е. условия процесса адсорбции отдельных атомов определяют величину адгезии получаемого покрытия. 20
Поведение атомов пара у поверхности В отличие от способов получения покрытий методом погружения в расплав и методом химического осаждения покрытий в технологии вакуумного конденсационного напыления (осаждении) главным механизмом формирования покрытия является взаимодействие отдельных атомов (молекул, ионов) с обрабатываемей поверхностью. Характер этого взаимодействия, т. е. условия процесса адсорбции отдельных атомов определяют величину адгезии получаемого покрытия. 20
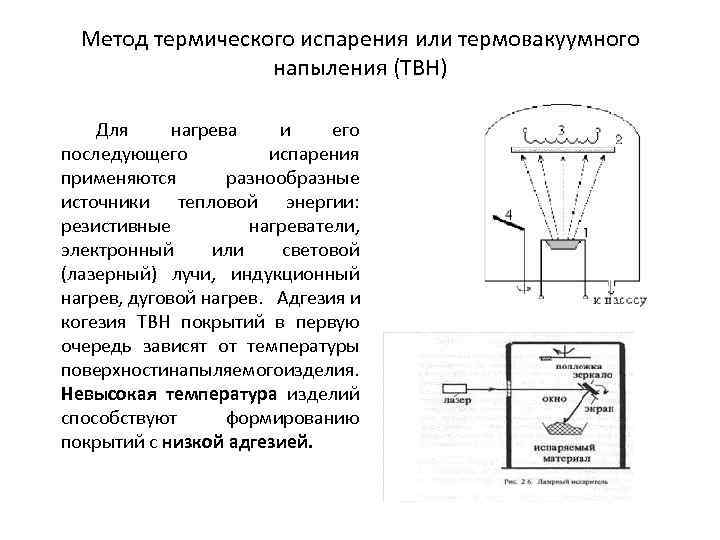 Метод термического испарения или термовакуумного напыления (ТВН) Для нагрева и его последующего испарения применяются разнообразные источники тепловой энергии: резистивные нагреватели, электронный или световой (лазерный) лучи, индукционный нагрев, дуговой нагрев. Адгезия и когезия ТВН покрытий в первую очередь зависят от температуры поверхности апыляемого зделия. н и Невысокая температура изделий способствуют формированию покрытий с низкой адгезией.
Метод термического испарения или термовакуумного напыления (ТВН) Для нагрева и его последующего испарения применяются разнообразные источники тепловой энергии: резистивные нагреватели, электронный или световой (лазерный) лучи, индукционный нагрев, дуговой нагрев. Адгезия и когезия ТВН покрытий в первую очередь зависят от температуры поверхности апыляемого зделия. н и Невысокая температура изделий способствуют формированию покрытий с низкой адгезией.
 3. 3 МОДЕЛЬ ПОВЕРХНОСТИ Ученые Коссель и Сперанский предложили модель поверхности, на которой можно показать элементы структуры реального кристаллического тела (вакансии, дислокации), а также рассмотреть энергетическое состояние отдельных атомов (связь их поверхностью).
3. 3 МОДЕЛЬ ПОВЕРХНОСТИ Ученые Коссель и Сперанский предложили модель поверхности, на которой можно показать элементы структуры реального кристаллического тела (вакансии, дислокации), а также рассмотреть энергетическое состояние отдельных атомов (связь их поверхностью).
 Задача Две одинаковые системы ( с равными массами М 1 = М 2) имеют разные формы: куб и шар. • Какая форма более устойчива с точки зрения термодинамики? • Как и во сколько раз отличаются свободные поверхностные энергии? Решение задачи их
Задача Две одинаковые системы ( с равными массами М 1 = М 2) имеют разные формы: куб и шар. • Какая форма более устойчива с точки зрения термодинамики? • Как и во сколько раз отличаются свободные поверхностные энергии? Решение задачи их
 Продолжение следует
Продолжение следует
 Контрольная работа (30 сентября) 1 Свойства материалов и структура 1. 1 Свойства материалов и как их можно изменять. 1. 2 Структура материалов. Масштабная иерархия и методы изучения. 1. 3 Структурные виды материалов (кристаллические, аморфные, смешанные структуры). 1. 4 Классификация кристаллических тел. 1. 5 Возможные структуры материала. Условия их образования. 2 Физико-химические основы материаловедения 2. 1 Реальные материалы, реальные процессы и их описание. 2. 2 Термодинамика поведения систем. 2. 3 Условия перехода системы из одного состояния в другое. 2. 4 Энергия системы и ее изменение. 1 -й закон термодинамики. 2. 5 Направление перехода системы из одного состояния в другое. 2. 5. 1 Энтропия и 2 -ой закон термодинамики. 2. 5. 2 Свободная энергия. 2. 8 Построение диаграмм состояний. 2. 8. 1 Эксперимент. 2. 8. 2 Теория. 3 Поверхность твердого тела 3. 1 Особенности состояния поверхностного слоя. 3. 2 Поверхностная энергия. 3. 3 Модель поверхности. 3. 4. Поведение атомов среды у поверхности. Модель Ленарда-Джонсона.
Контрольная работа (30 сентября) 1 Свойства материалов и структура 1. 1 Свойства материалов и как их можно изменять. 1. 2 Структура материалов. Масштабная иерархия и методы изучения. 1. 3 Структурные виды материалов (кристаллические, аморфные, смешанные структуры). 1. 4 Классификация кристаллических тел. 1. 5 Возможные структуры материала. Условия их образования. 2 Физико-химические основы материаловедения 2. 1 Реальные материалы, реальные процессы и их описание. 2. 2 Термодинамика поведения систем. 2. 3 Условия перехода системы из одного состояния в другое. 2. 4 Энергия системы и ее изменение. 1 -й закон термодинамики. 2. 5 Направление перехода системы из одного состояния в другое. 2. 5. 1 Энтропия и 2 -ой закон термодинамики. 2. 5. 2 Свободная энергия. 2. 8 Построение диаграмм состояний. 2. 8. 1 Эксперимент. 2. 8. 2 Теория. 3 Поверхность твердого тела 3. 1 Особенности состояния поверхностного слоя. 3. 2 Поверхностная энергия. 3. 3 Модель поверхности. 3. 4. Поведение атомов среды у поверхности. Модель Ленарда-Джонсона.


