Фазовые равновесия.pptx
- Количество слайдов: 40
 3 ФАЗОВЫЕ РАВНОВЕСИЯ
3 ФАЗОВЫЕ РАВНОВЕСИЯ
 3. 1 Основные понятия • • Фаза Фазовый переход или фазовое превращение Фазовое равновесие Составляющие вещества (b) Компонент (k) k=b–r Степень свободы системы или вариантность( f ) Диаграмма состояния (фазовая диаграмма) Фигуративная точка 3. 2 Правило фаз Гиббса (1876 г. ) • для равновесной термодинамической системы сумма чисел степеней свободы (f) и число фаз (φ) равна сумме чисел независимых компонентов (k) и внешних факторов, влияющих на систему (n). f +φ=k +n или f +φ = k +2
3. 1 Основные понятия • • Фаза Фазовый переход или фазовое превращение Фазовое равновесие Составляющие вещества (b) Компонент (k) k=b–r Степень свободы системы или вариантность( f ) Диаграмма состояния (фазовая диаграмма) Фигуративная точка 3. 2 Правило фаз Гиббса (1876 г. ) • для равновесной термодинамической системы сумма чисел степеней свободы (f) и число фаз (φ) равна сумме чисел независимых компонентов (k) и внешних факторов, влияющих на систему (n). f +φ=k +n или f +φ = k +2
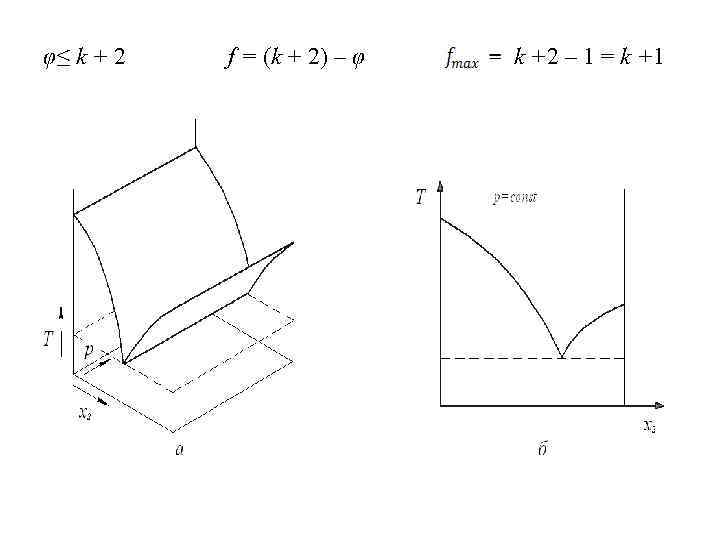 φ≤ k + 2 f = (k + 2) – φ k +2 – 1 = k +1
φ≤ k + 2 f = (k + 2) – φ k +2 – 1 = k +1
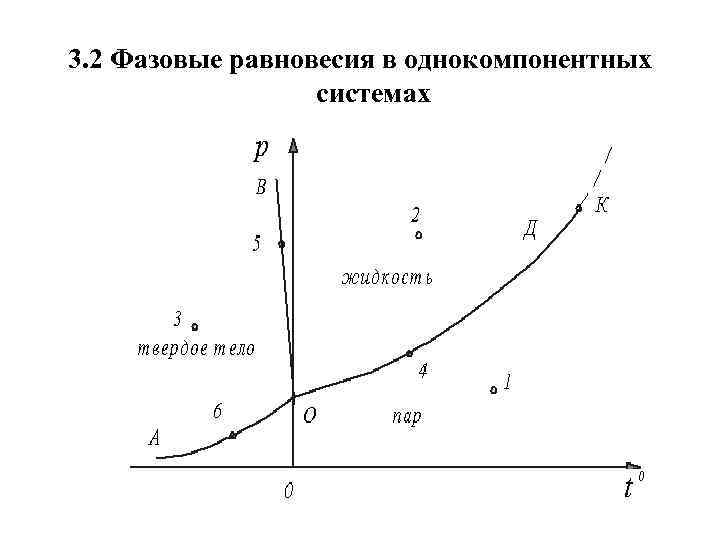 3. 2 Фазовые равновесия в однокомпонентных системах
3. 2 Фазовые равновесия в однокомпонентных системах
 3. 3. 2 Зависимость температуры сосуществования двух фаз от давления Уравнение Клапейрона-Клаузиуса: 1. Равновесие жидкость – пар. а) б)
3. 3. 2 Зависимость температуры сосуществования двух фаз от давления Уравнение Клапейрона-Клаузиуса: 1. Равновесие жидкость – пар. а) б)
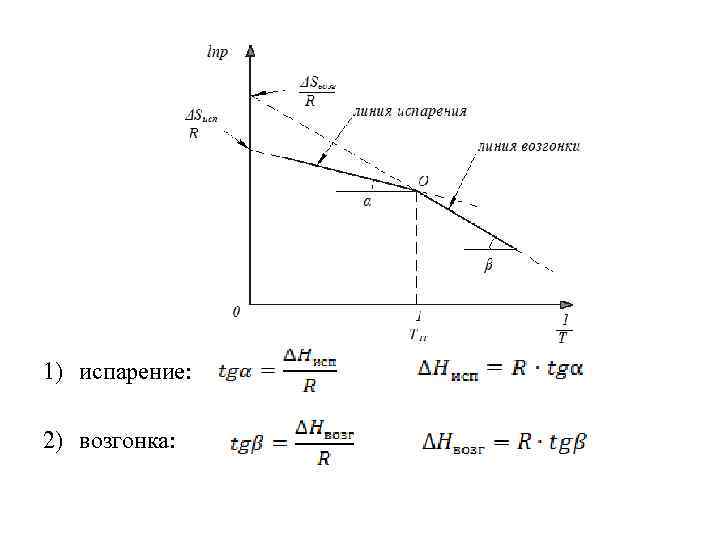 1) испарение: 2) возгонка:
1) испарение: 2) возгонка:
 Правила Трутона (Ф. Трутон): изменение упорядоченности при переходе из жидкого состояния в газообразное у большинства веществ примерно одинаково Уравнения Кистяковского: 2. Равновесие твердое тело – пар.
Правила Трутона (Ф. Трутон): изменение упорядоченности при переходе из жидкого состояния в газообразное у большинства веществ примерно одинаково Уравнения Кистяковского: 2. Равновесие твердое тело – пар.
 3. Равновесие твердое тело – жидкость 1) если , то ; 2) если , то 3. 4 ДВУХКОМПОНЕНТНЫЕ СИСТЕМЫ 3. 4. 1. Диаграммы состояния двухкомпонентных систем
3. Равновесие твердое тело – жидкость 1) если , то ; 2) если , то 3. 4 ДВУХКОМПОНЕНТНЫЕ СИСТЕМЫ 3. 4. 1. Диаграммы состояния двухкомпонентных систем
 • равновесие жидкость-пар в системе из неограниченно смешиваемых жидкостей; • равновесие жидкость-жидкость в системе из ограниченно смешиваемых жидкостей; • равновесие твердое тело-жидкость в системе, состоящей из твердого раствора; • равновесие твердое тело-жидкость, когда смешиваемые компоненты неограниченно растворимы в жидком состоянии, но нерастворимые в твердом состоянии.
• равновесие жидкость-пар в системе из неограниченно смешиваемых жидкостей; • равновесие жидкость-жидкость в системе из ограниченно смешиваемых жидкостей; • равновесие твердое тело-жидкость в системе, состоящей из твердого раствора; • равновесие твердое тело-жидкость, когда смешиваемые компоненты неограниченно растворимы в жидком состоянии, но нерастворимые в твердом состоянии.
 В 1. 2. 3. 4. 2 Равновесие жидкость-пар в системе из неограниченно смешиваемых жидкостей зависимости от соотношения сил межмолекулярного притяжения F 11 , F 22 , F 12 различают: Идеальные растворы, подчиняющиеся закону Рауля, для которых F 11 = F 22 = F 12 Реальные растворы с положительным или отрицательным отклонением от закона Рауля из-за различия межмолекулярных сил, но без максимума или минимума на фазовых диаграммах. Реальные растворы с максимумом или минимумом на фазовых диаграммах из-за значительного различия межмолекулярных сил.
В 1. 2. 3. 4. 2 Равновесие жидкость-пар в системе из неограниченно смешиваемых жидкостей зависимости от соотношения сил межмолекулярного притяжения F 11 , F 22 , F 12 различают: Идеальные растворы, подчиняющиеся закону Рауля, для которых F 11 = F 22 = F 12 Реальные растворы с положительным или отрицательным отклонением от закона Рауля из-за различия межмолекулярных сил, но без максимума или минимума на фазовых диаграммах. Реальные растворы с максимумом или минимумом на фазовых диаграммах из-за значительного различия межмолекулярных сил.
 1. Идеальные растворы Закон Рауля (Ф. Рауль, 1886 г. ): Закон Дальтона (Дж. Дальтон, 1801 г. ):
1. Идеальные растворы Закон Рауля (Ф. Рауль, 1886 г. ): Закон Дальтона (Дж. Дальтон, 1801 г. ):
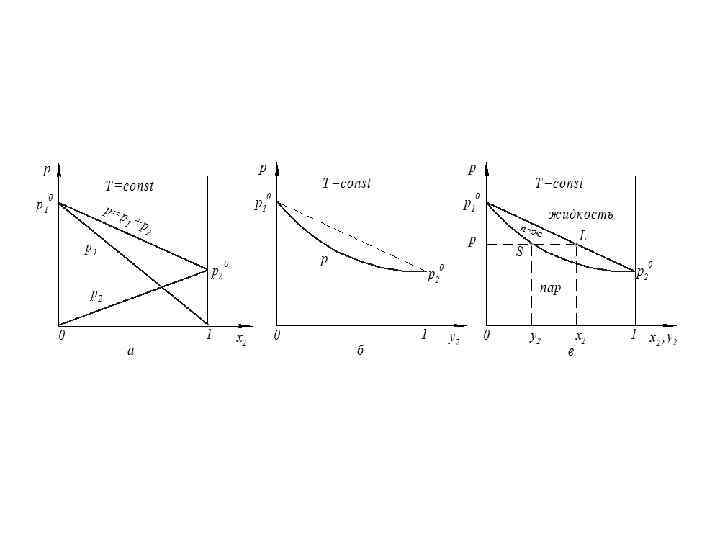
 1) если , то . Поэтому при условии получаем , то есть пар богат более летучим компонентом; 2) чем больше значение α, тем значительнее отличаются составы равновесного пара и жидкости где
1) если , то . Поэтому при условии получаем , то есть пар богат более летучим компонентом; 2) чем больше значение α, тем значительнее отличаются составы равновесного пара и жидкости где
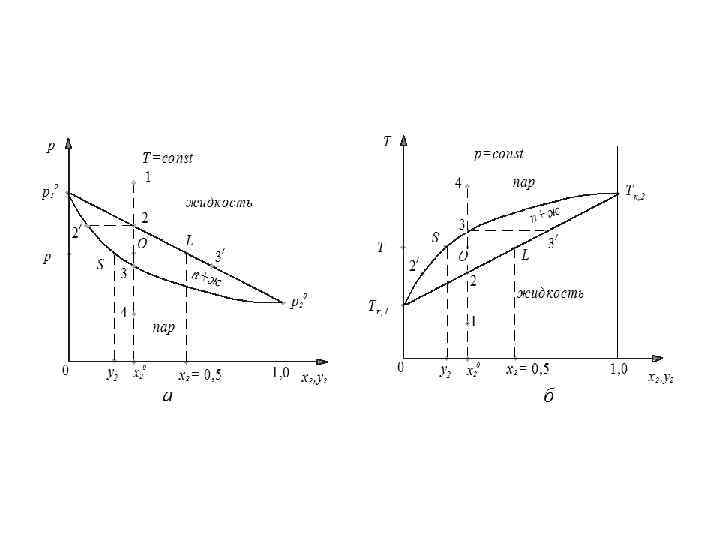
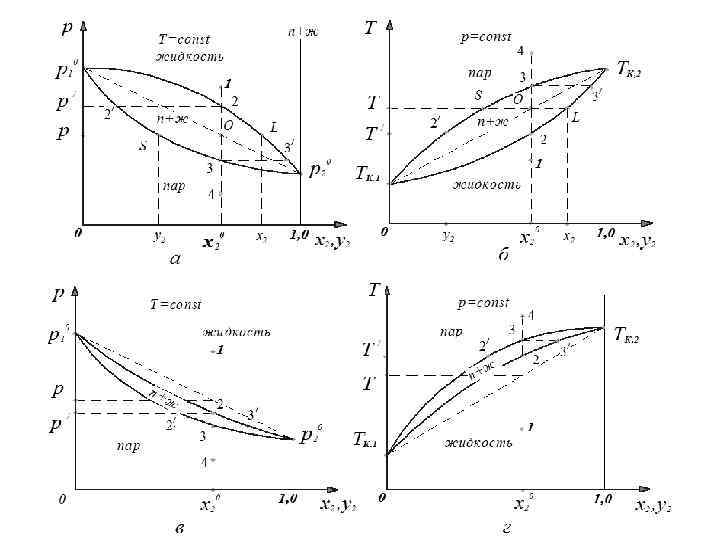
 Правило рычага: 2. Реальные растворы с отклонением от закона Рауля Различают положительное и отрицательное отклонения от закона Рауля : 1) положительное отклонение - F 11>F 12 и F 22>F 12 2) отрицательное отклонение - F 11
Правило рычага: 2. Реальные растворы с отклонением от закона Рауля Различают положительное и отрицательное отклонения от закона Рауля : 1) положительное отклонение - F 11>F 12 и F 22>F 12 2) отрицательное отклонение - F 11
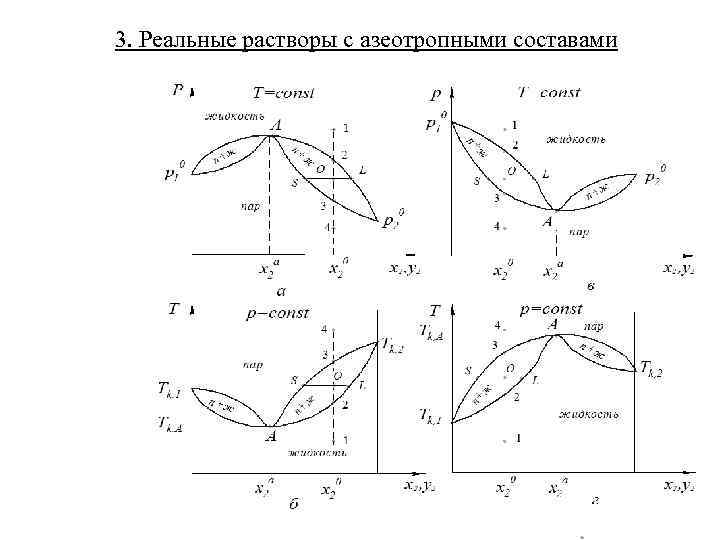 3. Реальные растворы с азеотропными составами
3. Реальные растворы с азеотропными составами
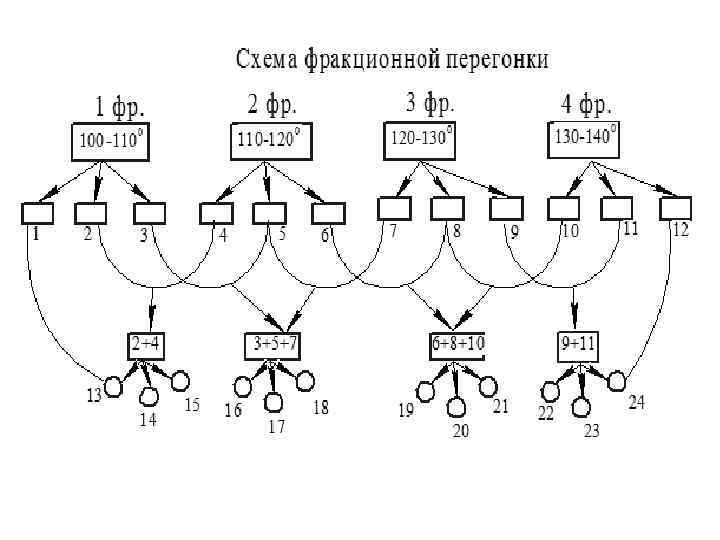
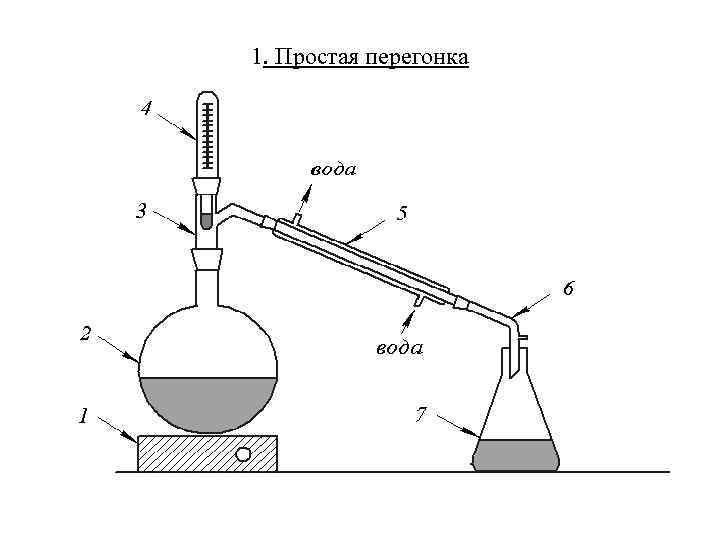 1. Простая перегонка
1. Простая перегонка
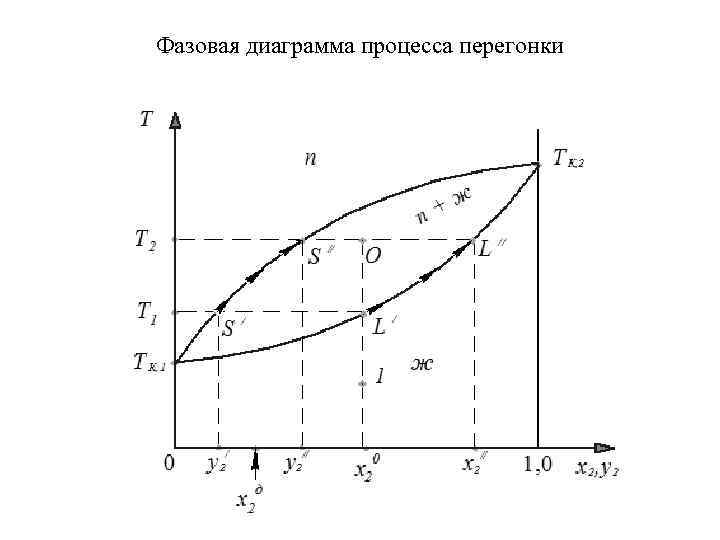 Фазовая диаграмма процесса перегонки
Фазовая диаграмма процесса перегонки
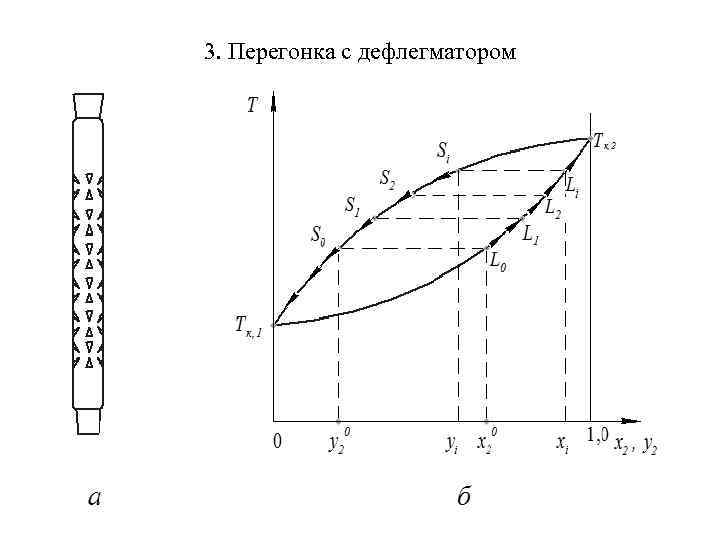 3. Перегонка с дефлегматором
3. Перегонка с дефлегматором
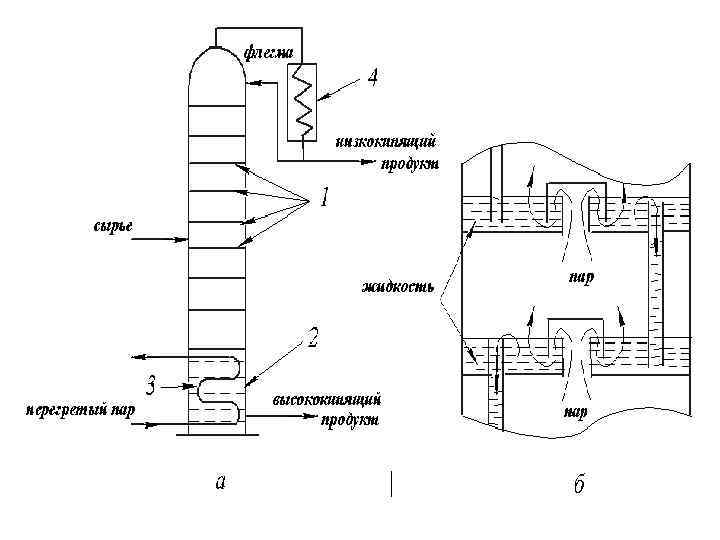
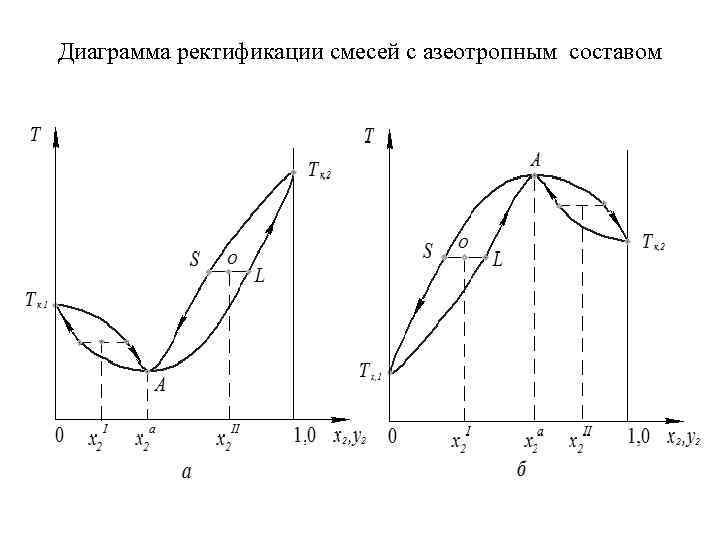 Диаграмма ректификации смесей с азеотропным составом
Диаграмма ректификации смесей с азеотропным составом
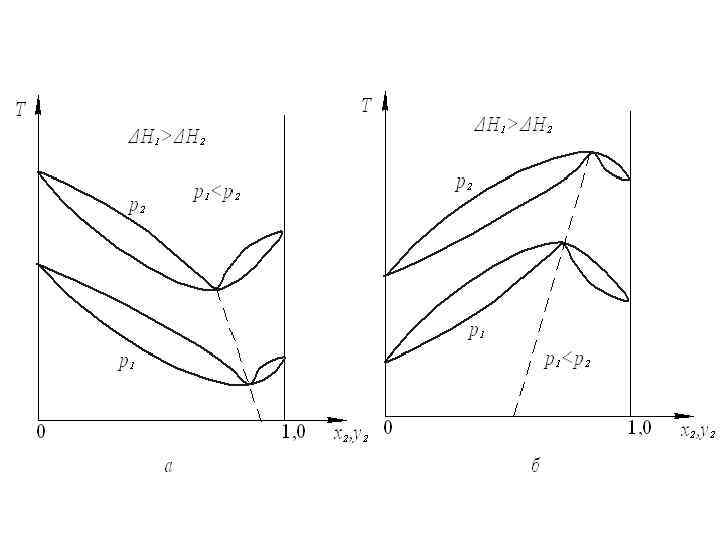
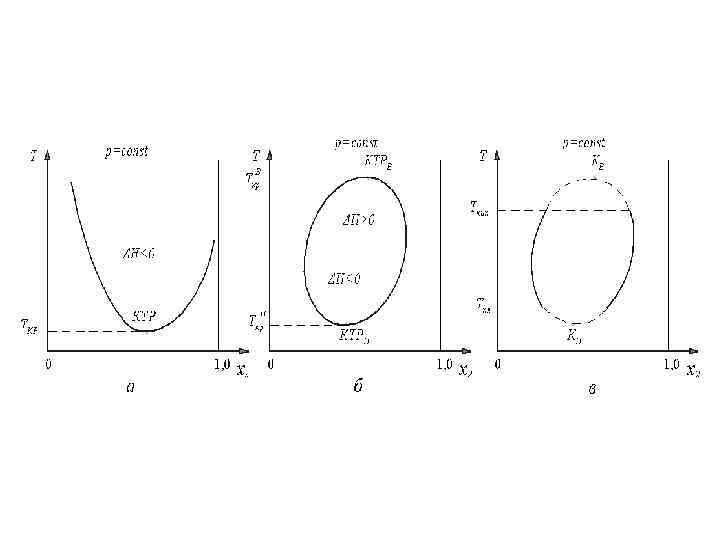
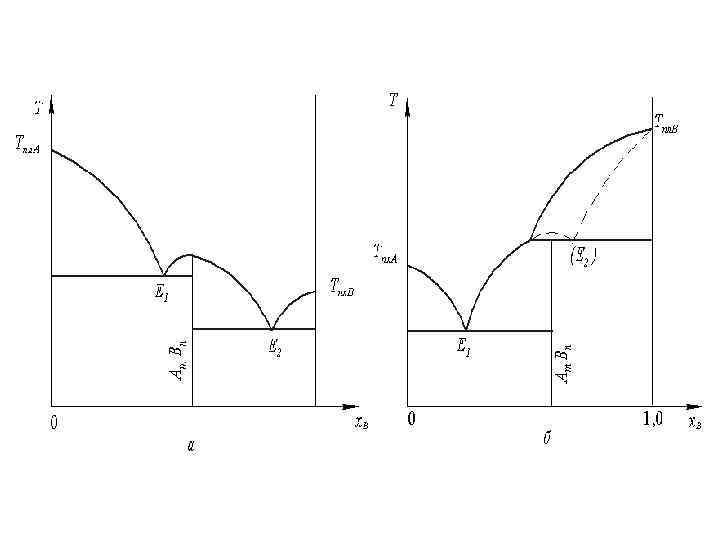
 Законы Вревского (1911 г. ): 1 -й закон: При повышении температуры раствора в равновесном паре повышается относительное содержание того компонента, парциальная молярная энтальпия испарения которого больше. 2 -закон: В азеотропной смеси с минимумом на изобаре (максимумом на изотерме, рис. а) при повышении давления (температуры) возрастает концентрация компонента с большей парциальной молярной теплотой испарения. В азеотропной смеси с максимумом на изобаре (минимумом на изотерме, рис. б) при повышении давления (температуры) возрастает концентрация компонента с меньшей парциальной молярной теплотой испарения
Законы Вревского (1911 г. ): 1 -й закон: При повышении температуры раствора в равновесном паре повышается относительное содержание того компонента, парциальная молярная энтальпия испарения которого больше. 2 -закон: В азеотропной смеси с минимумом на изобаре (максимумом на изотерме, рис. а) при повышении давления (температуры) возрастает концентрация компонента с большей парциальной молярной теплотой испарения. В азеотропной смеси с максимумом на изобаре (минимумом на изотерме, рис. б) при повышении давления (температуры) возрастает концентрация компонента с меньшей парциальной молярной теплотой испарения
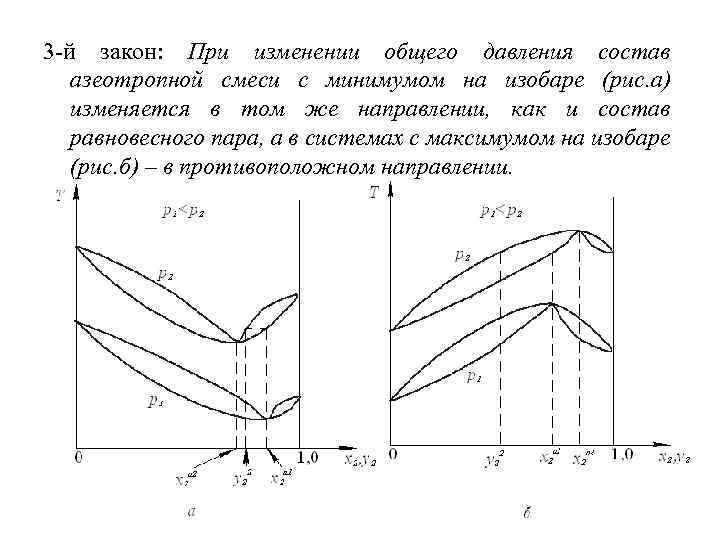 3 -й закон: При изменении общего давления состав азеотропной смеси с минимумом на изобаре (рис. а) изменяется в том же направлении, как и состав равновесного пара, а в системах с максимумом на изобаре (рис. б) – в противоположном направлении.
3 -й закон: При изменении общего давления состав азеотропной смеси с минимумом на изобаре (рис. а) изменяется в том же направлении, как и состав равновесного пара, а в системах с максимумом на изобаре (рис. б) – в противоположном направлении.
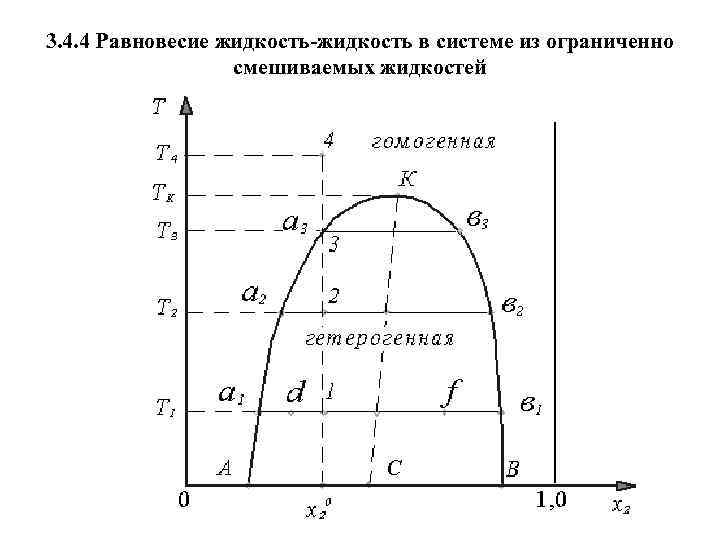 3. 4. 4 Равновесие жидкость-жидкость в системе из ограниченно смешиваемых жидкостей
3. 4. 4 Равновесие жидкость-жидкость в системе из ограниченно смешиваемых жидкостей
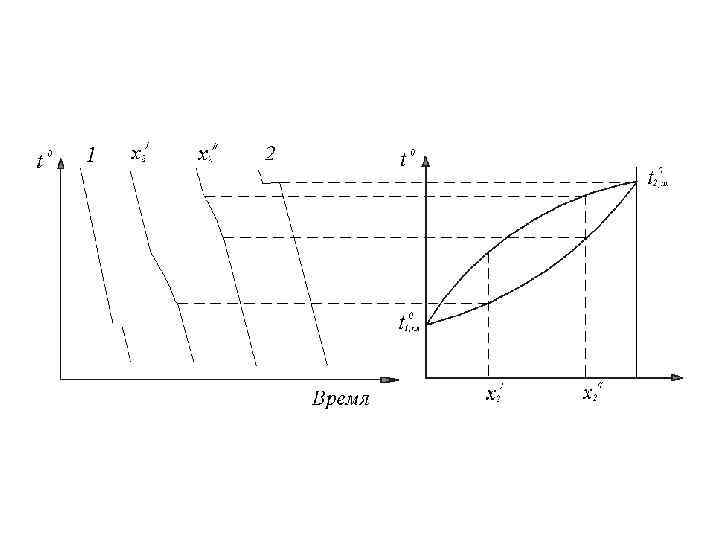
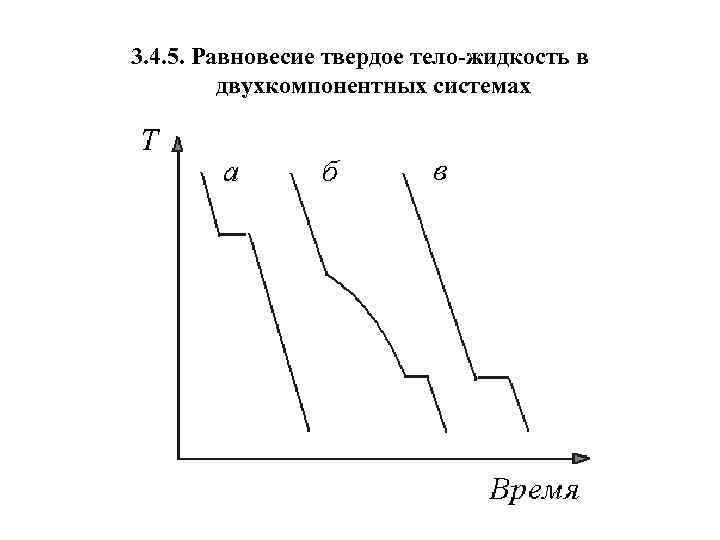 3. 4. 5. Равновесие твердое тело-жидкость в двухкомпонентных системах
3. 4. 5. Равновесие твердое тело-жидкость в двухкомпонентных системах
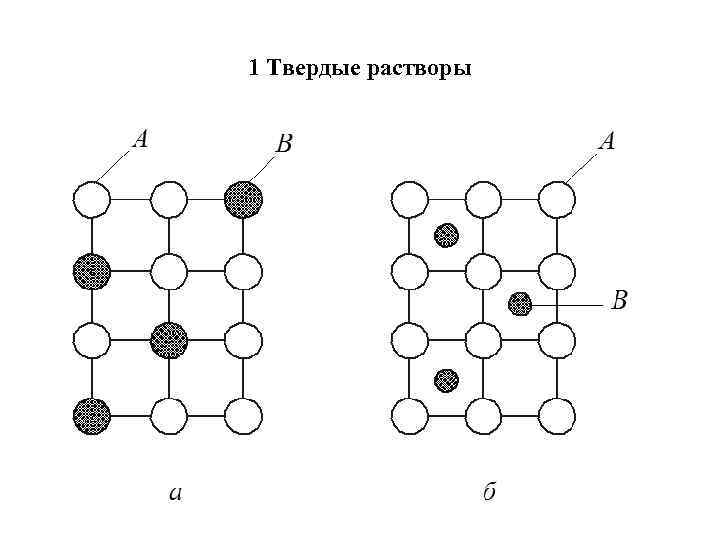 1 Твердые растворы
1 Твердые растворы
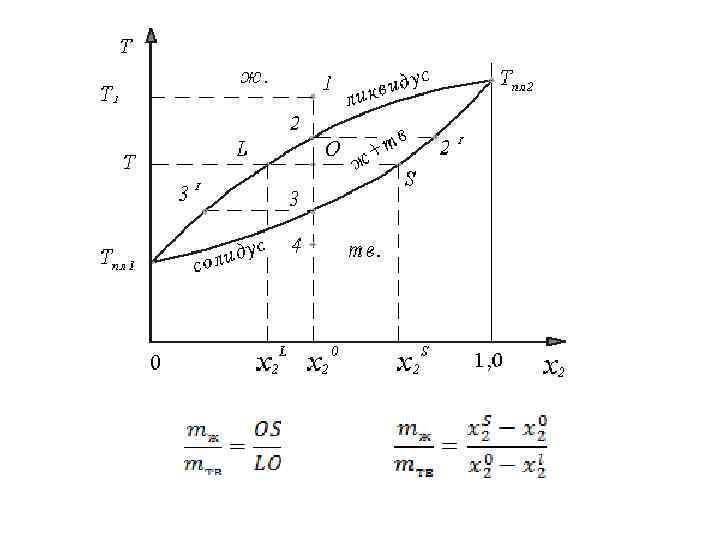
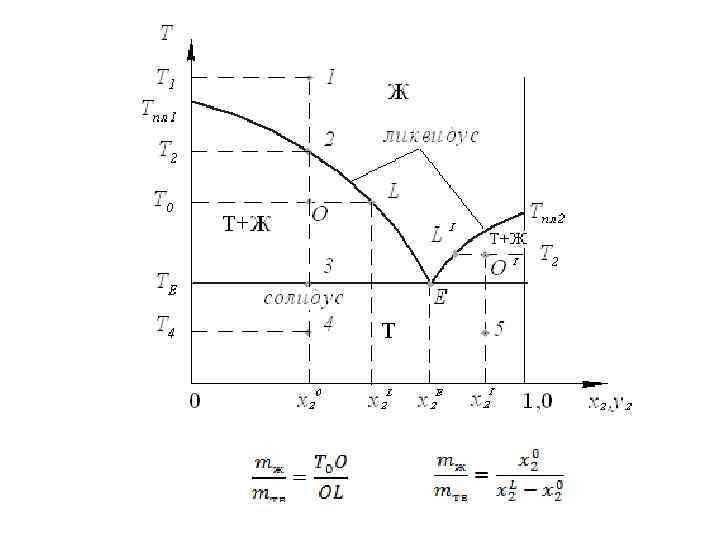
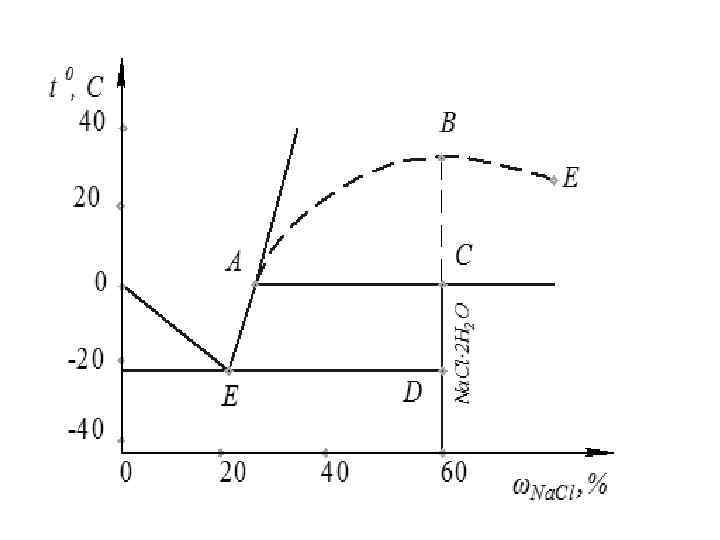
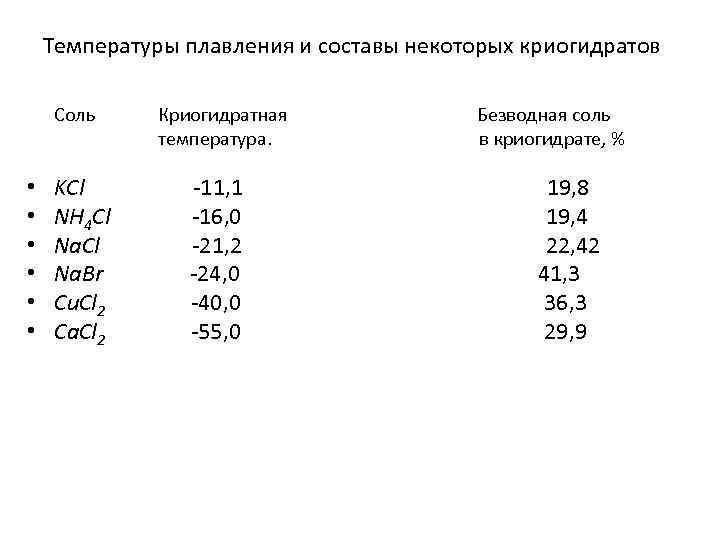 Температуры плавления и составы некоторых криогидратов Соль Криогидратная Безводная соль температура. в криогидрате, % • • • KCl -11, 1 19, 8 NH 4 Cl -16, 0 19, 4 Na. Cl -21, 2 22, 42 Na. Br -24, 0 41, 3 Cu. Cl 2 -40, 0 36, 3 Ca. Cl 2 -55, 0 29, 9
Температуры плавления и составы некоторых криогидратов Соль Криогидратная Безводная соль температура. в криогидрате, % • • • KCl -11, 1 19, 8 NH 4 Cl -16, 0 19, 4 Na. Cl -21, 2 22, 42 Na. Br -24, 0 41, 3 Cu. Cl 2 -40, 0 36, 3 Ca. Cl 2 -55, 0 29, 9
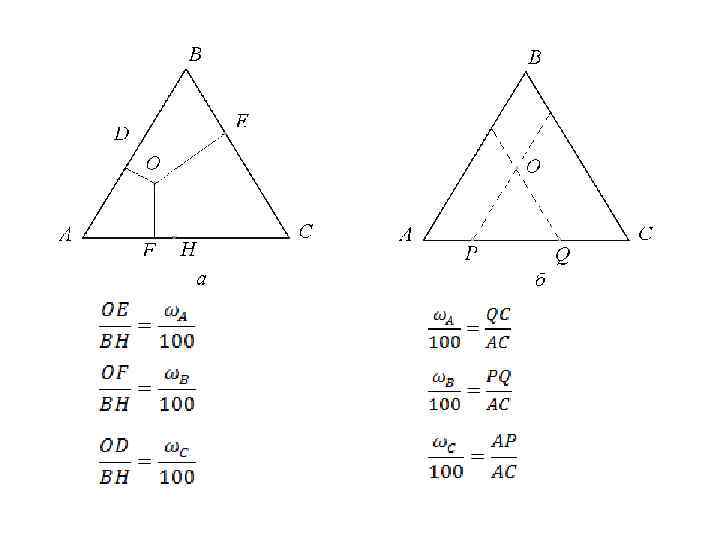
 3. 5 Диаграммы состояния трехкомпонентных систем 1. Неограниченная взаимная растворимость компонентов n=2 k=3 = k +1 = 3 + 1 = 4
3. 5 Диаграммы состояния трехкомпонентных систем 1. Неограниченная взаимная растворимость компонентов n=2 k=3 = k +1 = 3 + 1 = 4
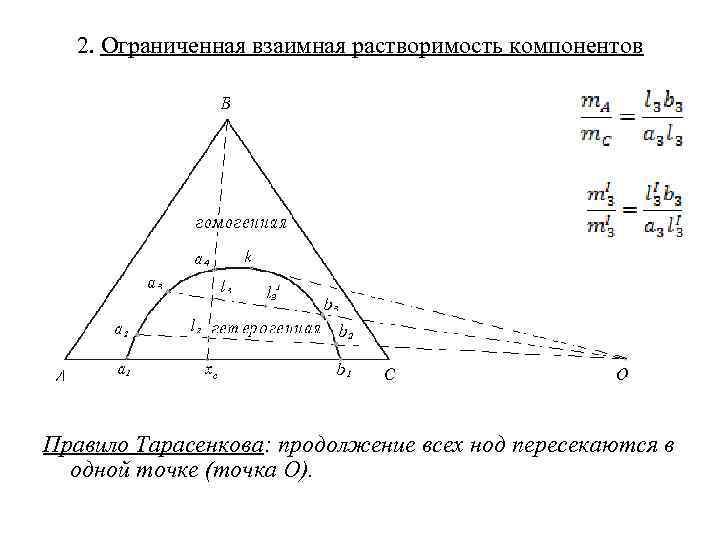 2. Ограниченная взаимная растворимость компонентов Правило Тарасенкова: продолжение всех нод пересекаются в одной точке (точка О).
2. Ограниченная взаимная растворимость компонентов Правило Тарасенкова: продолжение всех нод пересекаются в одной точке (точка О).
 Закон распределения: отношение концентрации третьего компонента в двух равновесных жидких фазах является величиной постоянной и не зависит от количества этого компонента
Закон распределения: отношение концентрации третьего компонента в двух равновесных жидких фазах является величиной постоянной и не зависит от количества этого компонента


