38f990aa496d728172f20d4b0c15989d.ppt
- Количество слайдов: 44

27 -29 сентября 2017 г. Программа повышения квалификации «Основы надлежащей практики фармаконадзора. Организация работы уполномоченного лица» УПРАВЛЕНИЕ СИГНАЛОМ Основные источники информации: 1. Правила надлежащей практики фармаконадзора Евразийского экономического союза (от 3 ноября 2016 г № 87). 2. Приказ Росздравнадзора № 1071 «Об утверждении порядка осуществления фармаконадзора» (от 15 февраля 2017 г) Журавлева Евгения Олеговна Начальник научно-аналитического отдела ЦЭБЛС

Основные термины и определения по теме управление сигналом • Сигнал – информация, поступающая от одного или нескольких источников, которая предполагает наличие новой потенциальной причинноследственной связи или нового аспекта известной взаимосвязи между воздействием лекарственного препарата (ЛП) и нежелательным явлением (НЯ) или совокупностью взаимосвязанных НЯ, оцениваемая как достаточная для дальнейших действий по верификации сигнала. Как правило, для генерирования сигнала требуется более 1 единичного сообщения в зависимости от серьезности нежелательного явления и качества информации;

Основные термины и определения по теме управление сигналом • • Сигнал, по которому выполняется работа – сигнал, который был выявлен до отчетного периода периодического отчета по безопасности и на дату окончания сбора данных находился в процессе оценки; Закрытый сигнал - сигнал, оценка которого была завершена в отчетный период составления периодического отчета по безопасности; Важная отсутствующая информация – значимые пробелы в имеющихся знаниях об определенных аспектах безопасности лекарственного препарата или группах пациентов, которым назначается лекарственный препарат; Новый идентифицированный сигнал – сигнал, впервые идентифицированный в течение отчетного периода периодического отчета по безопасности, с указаниями дальнейших действий для его оценки;

Основные термины и определения по теме управление сигналом • Валидированный сигнал – сигнал, для которого в процессе выполнения валидации и оценки подтверждающих данных установлено, что имеющаяся документация достаточна для предположения наличия новой потенциальной причинно-следственной связи или нового аспекта известной взаимосвязи между приемом подозреваемого ЛП и развитием неблагоприятного последствия и, следовательно, определена необходимость осуществления комплекса дальнейших действий по оценке сигнала.

Обязательные элементы сигнального менеджмента • 1. Структура и процессы 1. 1 Источники получения сигналов и их обработка 1. 2 Методология обработки 1. 3 Процесс обработки сигналов 1. 4 Требования к качеству • 2. Роли и обязанности 2. 1 Роль и обязанности уполномоченных органов государствчленов 2. 2 Функции и обязанности держателя регистрационного удостоверения 2. 3 Процессы последующего регулирования 2. 4 Открытость

1. Структура и процессы. 1. 1 Источники получения сигналов и их обработка Источники получения сигналов включают все данные, получаемые применении ЛП : доклинические, клинические данные, данные методов фармаконадзора и системы контроля качества. В них могут содержаться сведения, получаемые из систем спонтанного репортирования и активного мониторинга, а также информация полученная в ходе проведения неинтервенционных исследований и иных видов организованного сбора данных. Статьи из научной медицинской литературы (отечественная и зарубежная): - систематический обзор литературы широко используемых справочных баз данных (в том числе Medline, Excerpta Medica Embase); - опубликованные тезисы в материалах конференций или проекты монографий; Периодические отчеты по безопасности; Информационно-телекоммуникационная сеть «Интернет» , в качестве другого источника информации (веб-сайты, блоги, форумы ). Все возможные и доступные для пациентов системы, через которые потребитель может сообщить об опыте развития НР на лекарственный препарат;

1. Структура и процессы. 1. 2 Методология обработки • • • Процедура выявления сигналов должна придерживаться структурированной и методологии, которая может варьироваться в зависимости от вида лекарственного препарата, по которому выполняется процедура. С целью оценки доказательной основы, , подтверждающей поступивший сигнал, должны принимать во внимание клиническую значимость, степень достоверности взаимосвязи, согласованность данных, экспериментальные результаты, возможные сходные по характеру явления данные. При приоритизации сигналов учитывают различные факторы: новизну выявленной взаимосвязи или лекарственного препарата, факторы, имеющие отношение к значимости взаимосвязи, серьезности соответствующей реакции и факторы, имеющие отношение к документированию сообщения.

1. Структура и процессы. 1. 3 Процесс обработки сигналов Выявление сигнала; Валидация сигнала; Анализ и приоритизация сигнала; Оценка сигнала; Рекомендации по действиям уполномоченных органов государств - членов; • Обмен информацией; • • •

1. Структура и процессы. 1. 3 Процесс обработки сигналов Возможные нюансы при обработке сигналов: • В том случае, если обнаружение сигналов, в основном, базируется на обзоре индивидуальных сообщений о НР, процедура может включать верификацию и предварительную приоритизацию обнаруженного сигнала; • Если сигнал выявлен по объединенным результатам исследования, как правило, невозможно оценить каждое индивидуальное сообщение, и в результате валидации может потребоваться сбор дополнительных данных; Рекомендации по действиям (с последующим принятием решения согласно действующему законодательству) и обмен информацией являются компонентами, которые необходимо учитывать на каждой стадии процесса.

1. Структура и процессы. 1. 3 Процесс обработки сигналов Выявление сигнала • Метод выявления сигнала должен соответствовать объему данных; • Учитывать данные из всех доступных источников; • Результаты обзора кумулятивных данных должны своевременно и надлежащим образом оцениваться квалифицированным лицом; • При обнаружении угрозы общественному здоровью необходимо предпринимать незамедлительные и эффективные действия; • Процесс выявления сигналов должен быть надлежащим образом документирован;

1. Структура и процессы. 1. 3 Процесс обработки сигналов Выявление сигнала Обзор индивидуальных отчетов о безопасности: -спонтанные сообщения; -активные формы мониторинга; -клинические исследования; -литературный обзор; Информация, подлежащая оценке, должна включать: • • - количество сообщений (без дублированных сообщений и сообщений, оформленных ненадлежащим образом); - данные пациента (возраст и пол); -подозреваемый ЛП и информация о нем (например, введенная доза) ; -развившуюся НР ; -временную взаимосвязь; -клинический исход в связи с продолжением или прекращением приема лекарственного препарата; -наличие потенциальных альтернативных причин развития НЯ; -оценку отправителем сообщения причинно-следственной связи.

1. Структура и процессы. 1. 3 Процесс обработки сигналов Выявление сигнала Статистические анализы в больших базах данных Статистический анализ позволяет выявить комбинации ЛП-НР, встречающиеся чаще, чем можно ожидать, исходя из известных характеристик, а также более высокий уровень репортирования о данной комбинации, по сравнению с другими ЛП в базе данных; При использовании статистических методов идентификации сигналов следует учитывать: - объем данных; - полноту доступной информации; - серьезность НР; и выборе критериев

1. Структура и процессы. 1. 3 Процесс обработки сигналов Выявление сигнала Статистические отчеты могут быть предназначены для выявления подозреваемых НР, соответствующих предварительно определенным: • Критериям частоты; • Степени тяжести; • Клинической значимости; • Новизны; При использовании автоматического скрининга в процессе обнаружения сигналов соответствующие индивидуальные сообщения о НР, выбранные в качестве потенциальных сигналов, в последующем изучаются по отдельности и вне зависимости от используемого статистического метода, в дальнейшем подвергаются клинической оценке.

1. Структура и процессы. 1. 3 Процесс обработки сигналов Валидация сигнала При выполнении валидации сигнала необходимо учитывать следующее: • Клиническую значимость (установленная причинно-следственная связь, серьезность реакции и ее исход, новизна реакции, лекарственные взаимодействия, реакции у особых групп пациентов); • Предшествующую информацию (информация может быть уже включена в краткую характеристику ЛП, сигнал был оценен ранее и является основанием для регуляторной процедуры); • Наличие других соответствующих источников информации с бóльшим объемом данных по определенной НР (литературные данные, результаты экспериментов, обзор более крупных баз данных); Валидации подлежат также и ранее выявленные сигналы, в случае появления новых данных по частоте развития НР, степени тяжести или исхода.

1. Структура и процессы. 1. 3 Процесс обработки сигналов Валидация сигнала Держатели регистрационных удостоверений и регуляторные органы должны разработать системы отслеживания с целью учета результатов валидации сигналов, включая причины, по которым сигналы не были приняты как свидетельствующие о предположительно новой причинно-следственной связи или новом аспекте известной взаимосвязи. Результаты валидации определяют необходимость дальнейшей оценки сигнала.

1. Структура и процессы. 1. 3 Процесс обработки сигналов Анализ и приоритизация сигналов. Процесс приоритизации должен включать в себя: • Доказательность и согласованность информации; • Влияние на пациентов, в зависимости от степени тяжести, обратимости, потенциала предотвращения и клинического исхода НР, результаты прекращения лечения применительно к течению заболевания; • Повышенная частота или степень тяжести известного нежелательного действия; • Новизна подозреваемой НР;

1. Структура и процессы. 1. 3 Процесс обработки сигналов Анализ и приоритизация сигналов. Процесс приоритизации должен включать в себя: • • Особое внимание заслуживают сигналы на новые действующие вещества, заявление на получение регистрационного удостоверения которых еще находится на рассмотрении национальным регуляторным органом, а сигнал о безопасности поступил из третьей страны, в которой он уже зарегистрирован; Влияние на общественное здоровье, в зависимости от степени использования лекарственного препарата в общей группе пациентов и в популяционных группах риска, способ использования лекарственного препарата (например, неправильное использование или использование не по заявленным показаниям) Результаты процедуры приоритизации сигнала должны: - включать в себя рекомендации по временным рамкам оценки сигнала; - быть занесены в систему отслеживания с обоснованием присвоенного уровня приоритизации сигнала.

1. Структура и процессы. 1. 3 Процесс обработки сигналов Оценка сигнала. Оценка состоит из тщательного фармакологического, медицинского и эпидемиологического изучения всей имеющейся информации по соответствующему сигналу. Обзор должен включать в себя: • доступные доклинические и клинические данные; • данные досье ЛП при подаче заявления на регистрацию и последующие изменения; • литературные статьи; • спонтанные сообщения; • неопубликованную информацию от держателей регистрационных удостоверений и национальных регуляторных органов.

1. Структура и процессы. 1. 3 Процесс обработки сигналов Оценка сигнала. В некоторых случаях сигналы необходимо оценивать согласно терапевтическому уровню или классу системы органов, либо на уровне стандартизированного запроса (при использовании словаря медицинской терминологии Med. DRA. ) В случае, если на первой стадии оценки сигнала был сделан вывод о потенциальном риске развившейся тяжелой НР, могут быть приняты временные меры по ограничению применения ЛП.

1. Структура и процессы. 1. 3 Процесс обработки сигналов Рекомендации по действию регуляторных органов. Необходимость действий определяется в ходе всего процесса управления сигналом, целью которых является ранняя минимизация риска. Если уполномоченный орган государства-члена запрашивает у держателя регистрационного удостоверения проведение дополнительных действий, то в таком запросе указывается срок их выполнения, включая отчеты о достигнутых целях и промежуточных результатах пропорционально степени тяжести и влиянию проблемы по безопасности на общественное здоровье. В зависимости от полученных результатов в ходе оценки сигнала могут потребоваться временные меры по обеспечению безопасного и эффективного применения лекарственного препарата или устранению риска, включая возможность временного приостановления действия регистрационного удостоверения ЛП.

1. Структура и процессы. 1. 3 Процесс обработки сигналов Обмен информацией Цель - распространение информации о сигналах, сбор дополнительных данных, последующая оценка вопроса безопасности и принятие решений о защите здоровья пациентов. Валидированные сигналы, которые могут оказывать влияние на общественное здоровье и соотношение «польза-риск» ЛП и вся соответствующая информация о сигналах, должны быть незамедлительно переданы в уполномоченные органы государств - членов ЕАЭС с предложениями возможных действий. Регуляторные органы передают результаты оценки сигналов держателям регистрационного удостоверения.

1. Структура и процессы. 1. 4 Требования к качеству Прослеживаемость - Все ключевые процедуры процесса обработки сигнала должны надлежащим периодически отслеживаться. образом документироваться и Системы качества и документация - должна быть разработана система обеспечения и контроля качества в соответствии со стандартами системы качества, которая будет применяться ко всем процессам управления сигналами. Необходимо распределить функции и обязанности внутри компании относительно действий и ведения документации, контроля и изучения вопросов качества, а также принятия корректирующих и предупредительных мер. Сюда также относятся обязанности по аудиту обеспечения качества в системе управления сигналами, включая аудит субподрядчиков контрактных сторон, выполняющих какие-либо работы по данному направлению. Обучение. Персонал должен быть специально обучен выполнению действий по обработке сигналов согласно распределенным функциям и обязанностям. Обучение должно включать терминологию и доступные базы данных с источниками сигналов.

2. Роли и обязанности. 2. 1 Роль и обязанности уполномоченных органов государствчленов ЕАЭС Обеспечивают контроль данных на своей территории, включая информацию, полученную из иных источников, указанных в подразделе «Источники получения сигналов» ; Выполняют валидацию и иные этапы процедуры обработки сигналов, полученных из доступных источников; Передают сигналы, прошедшие через процедуры валидации и оценки, в соответствующие экспертные комитеты государств с целью определения целесообразности последующих действий по дальнейшему изучению или минимизации риска. Выполняют информирование других уполномоченных органов государств-членов ЕАЭС о выявленных сигналах, прошедших валидацию, и разработанных мерах.

2. Роли и обязанности. 2. 2 Функции и обязанности держателя регистрационного удостоверения. Держатель регистрационного удостоверения: Контролирует все имеющиеся данные и информацию по сигналам; Отслеживают новую информацию по безопасности, появляющуюся в базах данных и осуществляет международное обнаружение сигналов; выявленные сигналы подлежат валидации с учетом компонентов представляемой информации, изложенной в разделе «Валидация сигнала» ; Передает в уполномоченные органы государств-членов ЕАЭС информацию о валидированных сигналах;

2. Роли и обязанности. 2. 2 Роль и обязанности держателя регистрационного удостоверения. Держатель регистрационного удостоверения: Уведомляет уполномоченные органы государствчленов ЕАЭС в случае выявления экстренной проблемы по безопасности в результате осуществления деятельности по обнаружению сигналов; Сотрудничает с уполномоченными органами государств -членов ЕАЭС в выполнении процедур оценки сигналов путем представления дополнительной информации по запросу ; Обеспечивает аудиторский надзор по всем процедурам выявления сигнала.

2. Роли и обязанности. 2. 3 Процессы последующего регулирования. По результатам процедуры валидации сигнала могут быть приняты следующие решения: • Дополнительная оценка или действия не требуются; • Изменение регистрационного статуса : действие регистрационного удостоверения может быть приостановлено, отозвано или не продлено; • Необходимо выполнение внепланового инспектирования с целью подтверждения того, что держатель регистрационного удостоверения соблюдает требования к системе фармаконадзора, установленные актами органов Союза и законодательством государств-членов; • Необходимо включение подозреваемого лекарственного препарата в перечень продукции, которая подлежит дополнительному мониторингу;

2. Роли и обязанности. 2. 3 Процессы последующего регулирования. Со стороны держателя регистрационного удостоверения могут потребоваться следующие действия: • • • Провести дополнительную оценку данных и представить результаты такой оценки согласно установленным временным срокам; Предоставить ПООБ с учетом выявленного нового аспекта профиля безопасности; Представить план управления рисками или его обновленный вариант; Держатель регистрационного удостоверения должен профинансировать пострегистрационное исследование в соответствии с согласованным протоколом и предоставить заключительные результаты такого исследования; Держателем регистрационного удостоверения должны быть приняты меры, требуемые для обеспечения безопасного и эффективного применения лекарственного препарата;

2. Роли и обязанности. 2. 4 Открытость. Государствам –членам ЕАЭС необходимо осуществлять контроль своевременного доведения до общественности важной информации о проблемах по безопасности, выявленных системой фармаконадозора, путем публикаций на веб-портале и при помощи других доступных средств

Спасибо за внимание! Интересующие вас вопросы можно направить по Gyravleva@expmed. ru

Опыт внедрения процесса управления сигналами в российской фармацевтической компании Журавлев Р. И. , к. м. н. , старший специалист отдела безопасности лекарственных средств АО «Р-Фарм»

Детекция (выявление) сигнала • Проводится для всех зарегистрированных препаратов, для которых АО «Р-Фарм» является держателем РУ либо отвечает за выявление сигналов и управление ими в соответствии с контрактными обязательствами. • Проводится раз в две недели на основании обзора информации по определенному препарату из всех источников: • • • Спонтанные сообщения Сообщения из клинических исследований Сообщения от лицензионных партнеров Обзор медицинской литературы (Pub. Med, Google Scholar, вендор) Информации от регуляторов: Ø сайт НЦЭСМП (regmed. ru) Ø сайт Росздравнадзора Ø Рассылка FDA Medwatch Ø Рассылка MHRA Drug Safety Update
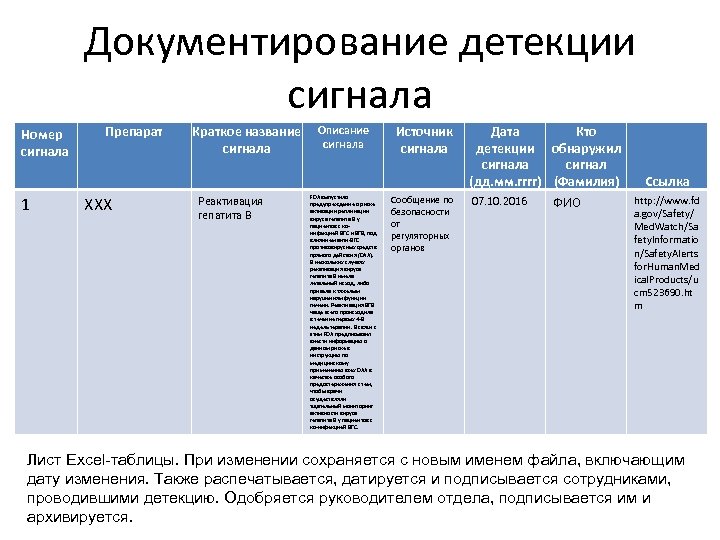
Документирование детекции сигнала Номер сигнала 1 Препарат XXX Краткое название сигнала Реактивация гепатита B Описание сигнала FDA выпустило предупреждение о риске активации репликации вируса гепатита В у пациентов с коинфекцией ВГС и ВГВ, под влиянием анти-ВГС противовирусных средств прямого действия (DAA). В нескольких случаях рекативация вируса гепатита В имела летальный исход, либо привела к тяжелым нарушениям функции печени. Реактивация ВГВ чаще всего происходила в течение первых 4 -8 недель терапии. В связи с этим FDA предписывает внести информацию о данном риске в инструкцию по медицинскому применению всех DAA в качестве особого предостережения с тем, чтобы врачи осуществляли тщательный мониторинг активности вируса гепатита В у пациентов с ко-инфекцией ВГС. Источник сигнала Сообщение по безопасности от регуляторных органов Дата Кто детекции обнаружил сигнала сигнал (дд. мм. гггг) (Фамилия) 07. 10. 2016 ФИО Ссылка http: //www. fd a. gov/Safety/ Med. Watch/Sa fety. Informatio n/Safety. Alerts for. Human. Med ical. Products/u cm 523690. ht m Лист Excel-таблицы. При изменении сохраняется с новым именем файла, включающим дату изменения. Также распечатывается, датируется и подписывается сотрудниками, проводившими детекцию. Одобряется руководителем отдела, подписывается им и архивируется.

Валидация сигнала • Каждый выявленный сигнал должен быть валидирован в течение 7 дней с момента детекции • При валидации сигнала принимаются во внимание следующие аспекты: 1) Клиническая значимость наблюдения (серьезность, тяжесть, новизна реакции, проявление в особых популяциях) 2) Предшествующая осведомленность – степень в которой информация описана в референсной документации по препарату (ИМП) 3) Доступность других релевантных источников информации (данные литературы о сходных случаях, данные экспериментальных исследований, данные о биологических механизмах развития реакций)
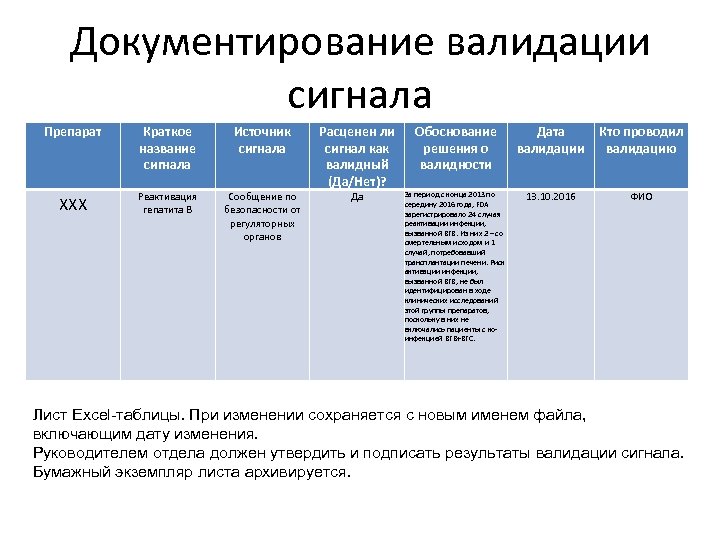
Документирование валидации сигнала Препарат Краткое название сигнала Источник сигнала XXX Реактивация гепатита B Сообщение по безопасности от регуляторных органов Расценен ли сигнал как валидный (Да/Нет)? Да Обоснование решения о валидности Дата валидации Кто проводил валидацию За период с конца 2013 по середину 2016 года, FDA зарегистрировало 24 случая реактивации инфекции, вызванной ВГВ. Из них 2 – со смертельным исходом и 1 случай, потребовавший трансплантации печени. Риск активации инфекции, вызванной ВГВ, не был идентифицирован в ходе клинических исследований этой группы препаратов, поскольку в них не включались пациенты с коинфекцией ВГВ+ВГС. 13. 10. 2016 ФИО Лист Excel-таблицы. При изменении сохраняется с новым именем файла, включающим дату изменения. Руководителем отдела должен утвердить и подписать результаты валидации сигнала. Бумажный экземпляр листа архивируется.

Приоритизация Установка приоритета в оценке – ответственность руководителя отдела Приоритет должен быть установлен не позднее 1 рабочего дня с момента валидации сигнала Высокоприоритетный сигнал – оценка в течение 7 календарных дней с момента валидации Низкоприоритетный сигнал – оценка в течение 30 календарных дней с момента валидации. При установке приоритета целесообразно учитывать: • Влияние на пациентов (тяжесть, обратимость, предотвратимость) • Степень использования и паттерны использования препарата в общей и особой популяциях • Большое число случаев, сообщенных в течение короткого периода времени • Сила и согласованность доказательств, подтверждающих причинноследственную связь • Высокий интерес масс-медиа к препарату или нежелательной реакции
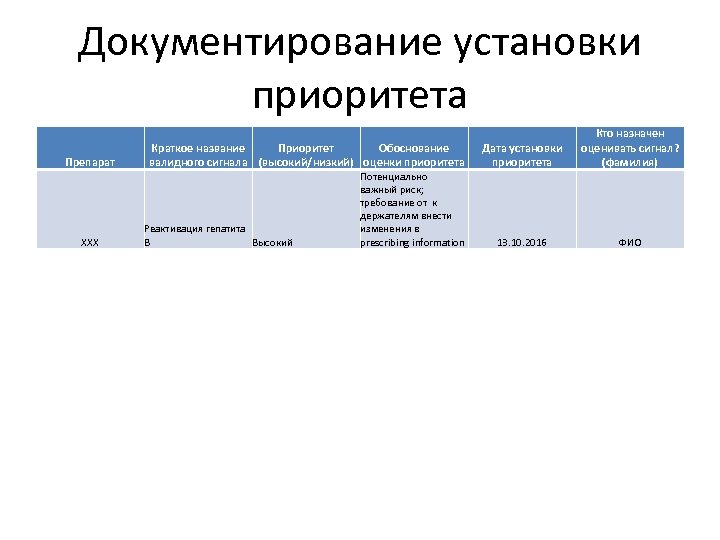
Документирование установки приоритета Препарат XXX Краткое название Приоритет Обоснование валидного сигнала (высокий/низкий) оценки приоритета Реактивация гепатита B Высокий Потенциально важный риск; требование от к держателям внести изменения в prescribing information Дата установки приоритета Кто назначен оценивать сигнал? (фамилия) 13. 10. 2016 ФИО

Оценка сигнала Оценка доступных фармакологических, доклинических и клинических данных и информации из других источников, например консультаций экспертов. Варианты оценки: 1. Оценка сигнала продолжается. В этом случае статус оценки сигнала должен быть вновь обновлен в следующие 7/30 дней для выско/низкоприоритетных сигналов 2. Сигнал опровергнут (рассматриваемое событие расценено как несвязанное с препаратом в процессе всесторонней оценки) 3. Сигнал расценен как риск, не являющийся важным (идентифицированный или потенциальный) 4. Сигнал расценен как важный риск (идентифицированный или потенциальный)
Идентифицированный риск Неблагоприятное событие, для которого существуют адекватные доказательства связи с препаратом. Примеры идентифицированного риска: Ø нежелательная реакция адекватно продемонстрирована в доклинических исследованиях и подтверждена клиническими данными; Ø нежелательная реакция наблюдалась в хорошо спланированных клинических или эпидемиологических исследованиях, и величина различия по соответствующему показателю между группой препарата и группой сравнения указывает на наличие причинной взаимосвязи (сравнение может проводиться с применением плацебо, активного препарата или отсутствием воздействия). Ø указания на нежелательную реакцию присутствуют в нескольких хорошо задокументированных спонтанных сообщениях, где причинная взаимосвязь четко подтверждается временной взаимосвязью и биологической правдоподобностью, например анафилактические реакции или реакции в месте введения. 38 Guideline on Good Pharmacovigilance Practices (GVP) Module V MA/838713/2011, adopted 25/06/2012

Потенциальный риск Неблагоприятное событие, в отношении которого существуют некоторые основания для подозрения связи с препаратом, но эта связь не подтверждена: Ø токсикологические находки в доклинических исследованиях, которые не наблюдались в клинических исследованиях; Ø нежелательные явления наблюдались в клинических или эпидемиологических исследованиях, и величина различий по соответствующему показателю между группой препарата и группой сравнения (плацебо, активный препарат или группа не подвергавшаяся воздействию) дает основание подозревать связь с приемом препарата, но не достаточно убедительна для указания на наличие такой связи; Ø сигнал, возникший при анализе системы спонтанных сообщений о нежелательных реакциях; Ø нежелательное явление, связанное с применением других препаратов того же класса или которого можно ожидать на основании известных свойств лекарственного препарата (класс-эффект) 39 Guideline on Good Pharmacovigilance Practices (GVP) Module V MA/838713/2011, adopted 25/06/2012

Важный риск • это идентифицированный или потенциальный риск, который может оказать влияние на баланс польза-риск для лекарственного препарата или имеет последствия для общественного здоровья. • Обычно любой риск который скорее всего будет включен в раздел «Противопоказания» или «С осторожностью» информации по препарату и/или Инструкции по медицинскому применению следует расценивать как важный.
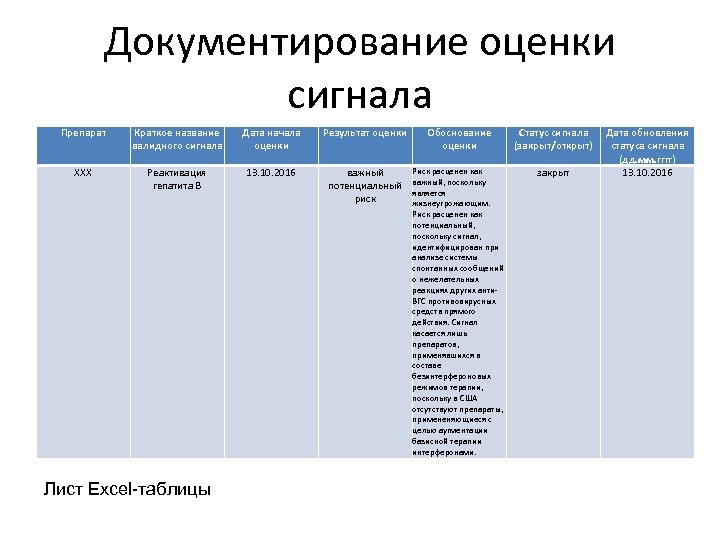
Документирование оценки сигнала Препарат Краткое название валидного сигнала Дата начала оценки Результат оценки Обоснование оценки Статус сигнала (закрыт/открыт) XXX Реактивация гепатита B 13. 10. 2016 важный потенциальный риск Риск расценен как важный, поскольку является жизнеугрожающим. Риск расценен как потенциальный, поскольку сигнал, идентифицирован при анализе системы спонтанных сообщений о нежелательных реакциях других анти. ВГС противовирусных средств прямого действия. Сигнал касается лишь препаратов, применявшихся в составе безинтерфероновых режимов терапии, поскольку в США отсутствуют препараты, примененяющиеся с целью аугментации базисной терапии интерферонами. закрыт Лист Excel-таблицы Дата обновления статуса сигнала (дд. мм. гггг) 13. 10. 2016

Рекомендация действия Оценка сигнала должна приводить к выработке рекомендации о том необходимо или нет в данный момент принятие дальнейших действий в связи с сигналом. Рекомендация действий может включать запрос на следующие действия: • неотложные меры, включая отзыв препарата с рынка • дополнительное изучение риска • действия по минимизации риска • периодическое мониторирование и обзор сигнала, например в рамках ПОБЛП • обновление информации о продукте посредством регуляторной процедуры • проведение пострегистрационного исследования безопасности Руководитель отдела безопасности лекарственных средств должен уведомить непосредственного руководителя о новом идентифицированном или потенциальном риске в течение одного рабочего дня с момента завершения оценки сигнала. Эта коммуникация должна включать предлагаемое действие в связи с сигналом. Непосредственный руководитель должен одобрить предложенное действие либо предложить альтернативное действие в течение 1 рабочего дня с момента получения информации от руководителя ОБЛС.
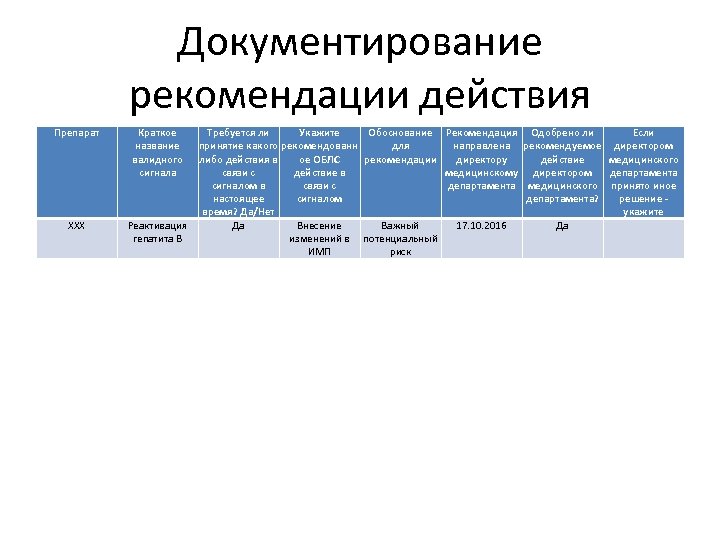
Документирование рекомендации действия Препарат XXX Краткое название валидного сигнала Требуется ли Укажите Обоснование Рекомендация Одобрено ли Если принятие какого рекомендованн для направлена рекомендуемое директором либо действия в ое ОБЛС рекомендации директору действие медицинского связи с действие в медицинскому директором департамента сигналом в связи с департамента медицинского принято иное настоящее сигналом департамента? решение время? Да/Нет укажите Реактивация Да Внесение Важный 17. 10. 2016 Да гепатита B изменений в потенциальный ИМП риск

Обмен информацией • Информация о валидированных сигналах, оцененных как представляющие новый важный идентифицированный или потенциальный риск, должна сообщаться в регуляторные органы в виде экспресс-отчетности. В коммуникации с регуляторным органом по данному вопросу должны быть описаны предлагаемые действия. • Информация обо всех других сигналах должна сообщаться в рамках периодической отчетности (ПОБЛП).
38f990aa496d728172f20d4b0c15989d.ppt