Диссоциация.ppt
- Количество слайдов: 4
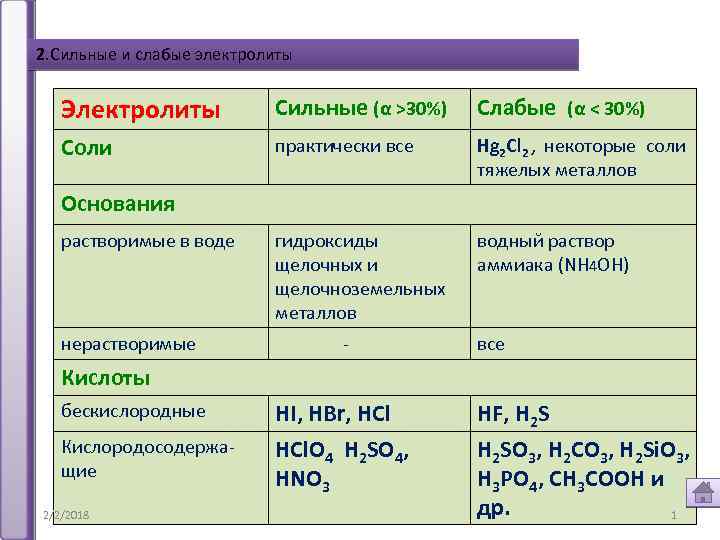
2. Сильные и слабые электролиты Электролиты Сильные (α >30%) Слабые (α < 30%) Соли практически все Hg 2 Cl 2 , некоторые cоли тяжелых металлов гидроксиды щелочных и щелочноземельных металлов водный раствор аммиака (NH 4 OH) Основания растворимые в воде нерастворимые - все Кислоты бескислородные Кислородосодержащие 2/2/2018 HI, HBr, HCl. O 4 H 2 SO 4, HNO 3 HF, H 2 SO 3, H 2 CO 3, H 2 Si. O 3, Н 3 РO 4, CH 3 COOH и др. 1

Диссоциация кислот 5. Диссоциация кислот, оснований, солей Кислоты - это электролиты, при диссоциации которых в водных растворах в качестве катионов образуются только ионы водорода. НCl → Н+ + Cl - + Н Н 2 SO 4 → Н 2 CO 3 2/2/2018 2

Диссоциация оснований Основания это электролиты, при - диссоциации которых в водных растворах в качестве анионов образуются только гидроксид-ионы. KOH K + + OН - ОН - Ca(OH)2 NH 4 OH 2/2/2018 3

Диссоциация средних солей Средние соли - это электролиты, которые в водных растворах диссоциируют на катионы металла и анионы кислотного остатка. Na+ + Na. Cl 2 K+ K 2 SO 4 Al(NO 3)3 Me 2/2/2018 n+ Сl+ SO 4 2 - 3+ Al + 3 NO 3 - (кислотный остаток) в 4
Диссоциация.ppt